Similar presentations:
Хроматографические методы анализа
1.
ХРОМАТОГРАФИЧЕСКИЕМЕТОДЫ АНАЛИЗА
2.
Хроматография –физико – химический метод
разделения
и анализа смеси
веществ, основанный на различном распределении компонентов между двумя несмешивающимися фазами.
3. Основные понятия
Сорбция – поглощение газов, паров ирастворенных веществ твердыми или
жидкими поглотителями (сорбентами);
Сорбтив – вещество, молекулы
которого способны сорбироваться;
Сорбат – вещество в адсорбированном состоянии;
4.
Элюирование – процесс перемещениявеществ вместе с подвижной фазой
через слой неподвижной фазы
Элюент – растворитель или газ,
проходящий через слой неподвижной
фазы – подвижная фаза;
Элюат – подвижная фаза, выходящая
из колонки и содержащая разделенные
компоненты
5.
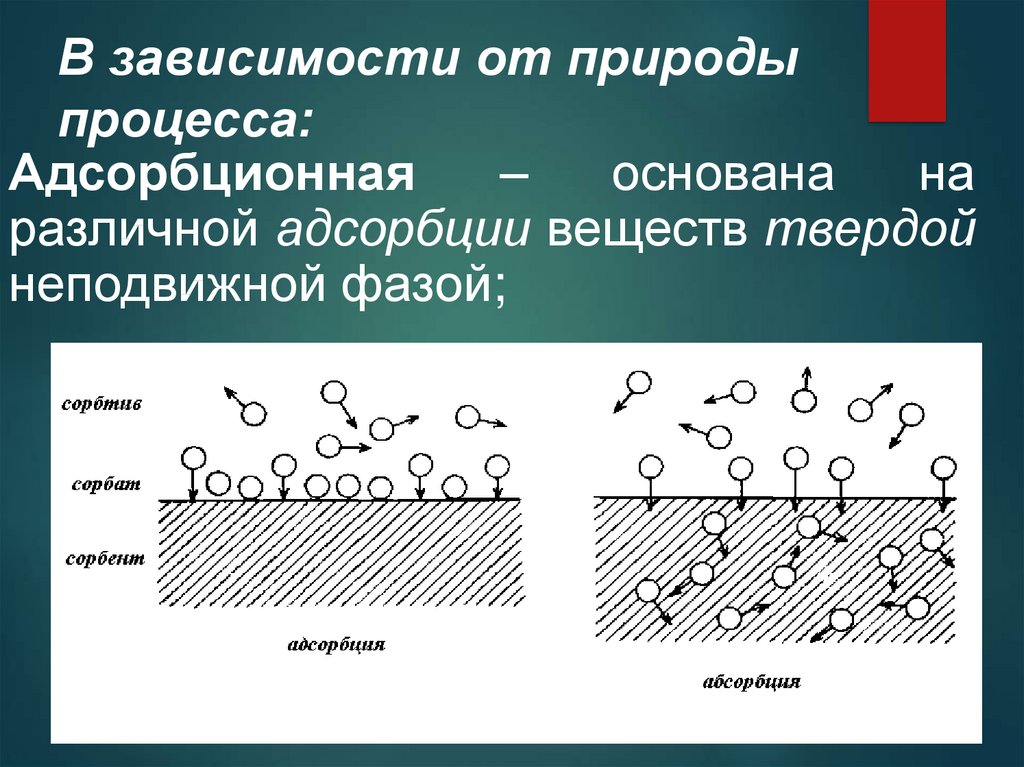
6. В зависимости от природы процесса:
Адсорбционная–
основана
на
различной адсорбции веществ твердой
неподвижной фазой;
7.
Распределительная – основана наразличной растворимости сорбатов в
жидкой неподвижной фазе;
Ионообменная
- основана на
различной способности к ионному
обмену
веществ
с
ионогенными
группами неподвижной фазы;
8.
Осадочная – основана на различнойрастворимости
осадков
,
получающихся
после
реакции
взаимодействия
с
осадителем,
содержащимся в неподвижной фазе;
Эксклюзионная
(молекулярно
–
ситовая или гелевая) – основана на
различии в размерах и формах молекул
разделяемых веществ;
9.
Аффинная–
основана
на
специфических
взаимодействиях
биологических объектов (ферментов, и
т.д.) с группами на поверхности твердой
фазы.
10. В зависимости от способа оформления процесса:
Колоночная – процесс разделенияпроводят в колонках, заполненных
неподвижной фазой;
Плоскостная – процесс разделения
проводят
на
хроматографической
бумаге (бумажная) или тонком слое
сорбента, нанесенном на подложку
(тонкослойная).
11. Теоретические основы хроматографии
12.
Основа процесса хроматографиинеравновесная адсорбция
–
Изотерма адсорбции Ленгмюра
max kC /(1 kC)
В области низких
давлений
(концентраций):
maxkC
уравнение Генри
13.
Эффективность разделения компонентов определяется числом теоретических тарелок (N).! Чем больше N и уже их высота (H),
тем эффективнее колонка
Высота, эквивалентная теоретической тарелке – ВЭТТ – (H) определяется:
14.
A – вихревая диффузия:где l – характеристика набивки колонки, dp – диаметр зерна сорбента
15.
B – продольная (осевая) диффузия –диффузия компонентов в подвижной
фазе:
где g – эмпирический коэффициент, DM
– коэффициент диффузии
16.
С – внутренняя диффузия – зависит отспособности
адсорбироваться
на
неподвижной фазе;
u – линейная скорость потока
L – длина колонки, tM – время удерживания несорбируемого компонента.
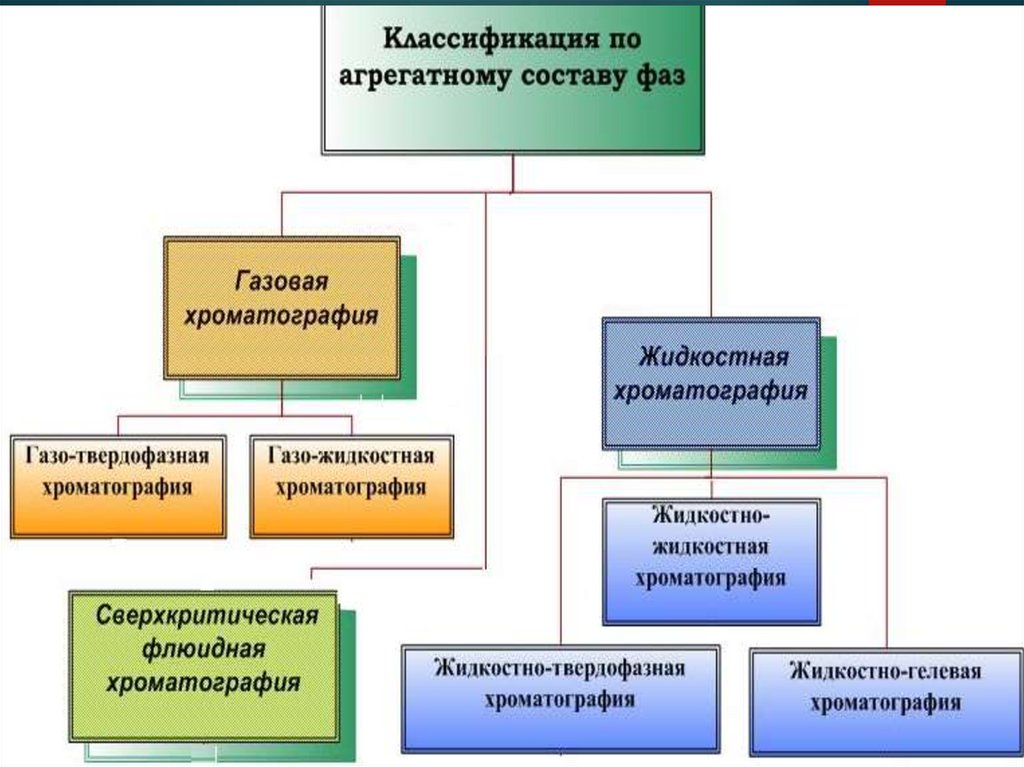
17. Газовая хроматография
18.
Газовая хроматография - это методразделения летучих
соединений,
основанный
на
распределении
веществ между подвижной фазой (ПФ)
- газом и неподвижной фазой (НФ) с
сорбентом с большой площадью
поверхности
19.
Подвижная фаза - инертный газ(азот,
гелий,
водород,
аргон,
углекислый газ), протекающий через
НФ;
! ПФ выполняет только транспортную функцию
! ПФ должна обеспечивать максимальную чувствительность детектора
20.
Неподвижная фазаВ газо-адсорбционной хроматографии - твердый сорбент с развитой
мелкопористой поверхностью; размер
зерен 0.1-0.5 мм
силикагель
активный уголь
21.
полимерныеадсорбенты
алюмосиликаты
В газо-жидкостной хроматографии пленка жидкости, нанесенная на
поверхность твердого носителя
22.
Типы жидкой НФ:Неполярные (насыщенные углеводороды);
Умеренно
полярные
эфиры, нитрилы);
Полярные
гликоли)
!
(многоатомные
(сложные
спирты,
Полярность НФ должна быть близка к полярности веществ
анализируемой пробы
23.
Требования к жидкой НФ :1) хорошо
растворять
компоненты
смеси;
2) прочно удерживаться на твердом
носителе;
3) быть термически устойчивой;
4) быть
нелетучей
при
данной
температуре;
5) обладать высокой селективностью;
6) быть химически инертной.
24. Жидкостная хроматография
25.
Подвижная фаза в жидкостнойхроматографии – чистый растворитель или смесь растворителей
Жидкостная хроматография в которой
используют колонки малого размера и
высокое давление ПФ (до 0.5 – 70
МПа) называют высокоэффективной жидкостной хроматографией
(ВЭЖХ)
26. Ионообменная хроматография
27. Неподвижная фаза
Ионитыприродного
синтетического происхождения:
или
цеолиты, глинистые материалы
(природные алюмосиликаты);
сульфированые активные угли;
синтетические
смолы
ионообменные
28. Неподвижная фаза
Катиониты–
обменивающиеся
с
катионами:
иониты,
раствором
Сильнокислотные - R-SO3H
Среднекислотные - R-PO3H2
Слабокислотные -
R-COOH
R-OH
29. Уравнение катионного обмена
R-SO3H + Na+ R-SO3Na + H+Н- форма
Na- форма
! Форма катионита определяется его
противоионом,
т.е.
катионом,
способным к обмену
30. Неподвижная фаза
Аниониты – иониты, обменивающиесяс раствором анионами:
Сильноосновные - R-[N(CH3)3]+OH-
Среднеосновные - R-[NH(CH3)2]+OHСлабоосновные - R-[NH3] +OH-
31. Уравнение анионного обмена
R-[NH3]+OH− + Cl− R-[NH3]+Cl − + OH−OН- форма
Cl- форма
Амфолиты – иониты, содержащие как
катионогенные, так и анионогенные
группы
32. Регенерация ионитов
!Ионный обмен обратимРегенерация
–
восстановление
свойств ионита
Регенерация катионита:
R-SO3Na + H+ R-SO3H + Na+
Регенерация анионита:
R-[NH3]+Cl − + OH− R-[NH3]+OH− + Cl−
33. Плоскостная хроматография
34. Неподвижная фаза
Неподвижная фаза – хроматографическаябумага
или
пластинки,
покрытые тонким слоем сорбента
Подвижная фаза – смесь растворителей.
































 chemistry
chemistry








