Similar presentations:
Виртуальный химический эксперимент
1. Виртуальный химический эксперимент
Основной государственныйэкзамен по химии
2.
Особенности виртуального химическогоэксперимента
1. Используя знания химических свойств веществ,
способов их получения и качественные реакции,
составить цепочку превращений
2. Для химических превращений указать условия
их протекания, признаки происходящих реакций
3. Написать уравнения реакций получения веществ,
указать химизм реакций
4. При выполнении опытов соблюдать правила
техники безопасности
5. Подготовить необходимое лабораторное
оборудование для проведения реального
эксперимента из предложенного
6. Задание выполняется только под наблюдением
эксперта-экзаменатора
3. Образец №1
Даны вещества: медь, оксид меди(II), растворы хлорида натрия, хлорида
бария, фосфорной и серной кислот
(разбав.).
1. Используя необходимые вещества
из этого списка, получите в результате
проведения двух последовательных реакций
раствор хлорида меди (II).
2. Составьте схему превращений, в
результате которых можно получить
указанное вещество.
3. Запишите уравнения двух
реакций. Для второй реакции составьте
сокращённое ионное уравнение.
4.
Алгоритм решения5.
Решение задачи №16.
Образец№2
Для проведения эксперимента
предложены следующие реактивы: железо,
медь, растворы хлорида железа (III),
гидроксида натрия и сульфата меди (II).
1. Требуется получить гидроксид
железа (II) в результате двух
последовательных реакций.
2. Составьте схему превращений, в
результате которых можно получить
указанное вещество.
3. Запишите уравнения двух реакций.
4. Для реакции ионного обмена
составьте сокращённое ионное уравнение.
Укажите условия и признаки
протекающих реакций.
7.
Алгоритм решения8.
Решение задачи №21. Fe + CuSO4 = FeSO4 + Cu↓
голубой р-р → зеленоватый р-р + красная медь
2. FeSO4 + 2NaOH = Na2SO4 + Fe(OH)2↓
Fe2+ + 2OH- = Fe(OH)2↓
белый осадок
Вывод: способ получения
нерастворимого основания – реакция
взаимодействия растворимой соли со
щёлочью
9.
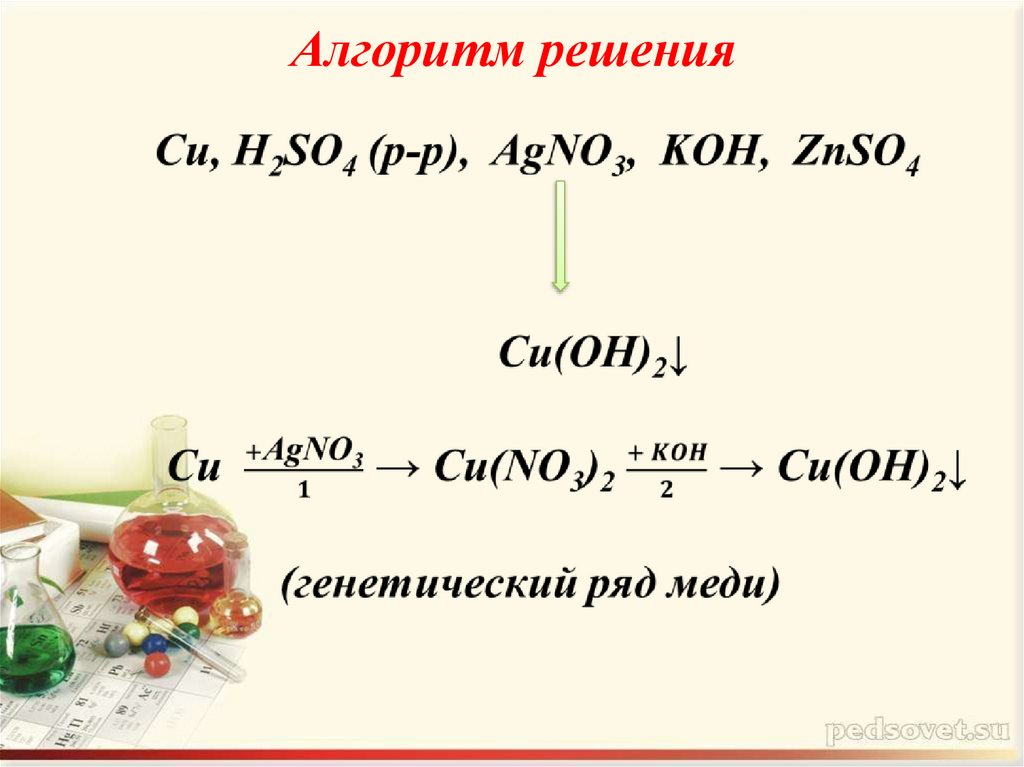
А теперь решите самостоятельноДаны вещества: медь, растворы серной
кислоты, нитрата серебра, гидроксида калия
и сульфата цинка.
1. Используя необходимые вещества
только из этого списка, получите в
результате проведения двух последовательных
реакций гидроксид меди (II).
2. Составьте схему превращений, в
результате которых можно получить
указанное вещество.
3. Запишите уравнения двух реакций.
Для второй реакции составьте сокращённое
ионное уравнение.
10.
Алгоритм решения11.
Решение задачи1. Cu + 2AgNO3 = Cu(NO3)2 + 2Ag↓
красный
→
голубоватый р-р + «зеркальный» налёт
2. Cu(NO3)2 + 2KOH = Cu(OH)2↓ + 2KNO3
синий осадок
Cu2+ + 2OH- = Cu(OH)2↓
Вывод: способ получения
нерастворимого основания – реакция
взаимодействия растворимой соли со
щёлочью
12. Благодарю за внимание
Мещерякова Светлана Николаевна, учитель химии и биологииМБОУ «Фруктовская СОШ»
г. Луховицы, МО
БЛАГОДАРЮ
ЗА ВНИМАНИЕ











 chemistry
chemistry








