Similar presentations:
Отчет по практической подготовке при проведении производственной практики «Технологическая практика» на базе ООО «СЭУ»
1.
МИНИСТЕРСТВО НАУКИ И ВЫСШЕГО ОБРАЗОВАНИЯ РОССИЙСКОЙФЕДЕРАЦИИ
ФЕДЕРАЛЬНОЕ ГОСУДАРСТВЕННОЕ БЮДЖЕТНОЕ
ОБРАЗОВАТЕЛЬНОЕ УЧРЕЖДЕНИЕ ВЫСШЕГО ОБРАЗОВАНИЯ
«ДОНСКОЙ ГОСУДАРСТВЕННЫЙ ТЕХНИЧЕСКИЙ УНИВЕРСИТЕТ»
(ДГТУ)
Факультет Биоинженерия и ветеринарная медицина
Подразделение, ответственное за реализацию образовательной программы
кафедра «Химия»
Заведующий
кафедрой
____________
«Химия»
« 29 »
2023 г.
июня
В.Э. Бурлакова
ОТЧЕТ
по практической подготовке при проведении производственной практики
«Технологическая практика»
на базе ООО «СЭУ»
Обучающийся_________________________
И.П. Крутиков
Обозначение отчета ПП.68.0000.000
Группа ЕИ21
Направление 28.03.02
Наноинженерия
Профиль Функциональные наноматериалы
Руководитель практической подготовки от предприятия
_____________ _____________
К.М. Лопатин
Руководитель практической подготовки от ДГТУ: __________________
М.А. Таутиева
М.П
Оценка ______________ __________________ ____________________________
Ростов-на-Дону
2023 г.
1
2.
МИНИСТЕРСТВО НАУКИ И ВЫСШЕГО ОБРАЗОВАНИЯ РОССИЙСКОЙФЕДЕРАЦИИ
ФЕДЕРАЛЬНОЕ ГОСУДАРСТВЕННОЕ БЮДЖЕТНОЕ ОБРАЗОВАТЕЛЬНОЕ
УЧРЕЖДЕНИЕ ВЫСШЕГО ОБРАЗОВАНИЯ
«ДОНСКОЙ ГОСУДАРСТВЕННЫЙ ТЕХНИЧЕСКИЙ УНИВЕРСИТЕТ»
(ДГТУ)
Факультет Биоинженерия и ветеринарная медицина
Подразделение, ответственное за реализацию
образовательной программы или ее компонентов
кафедра «Химия»
ЗАДАНИЕ
на практическую подготовку при проведении производственной практики
«Технологическая практика»
на базе ООО «СЭУ»
в период с «19» июня 2023 г. по «01» июля 2023 г.
Обучающийся Илья Петрович Крутиков
Обозначение отчета ПП.680000.000 Группа ЕИ21
Срок представления отчета на кафедру «29» июня 2023 г.
Содержание индивидуального задания
процесс осаждения цинк-фосфатного покрытия на металлические изделия и
количественное определение состава электролитов щелочного цинкования и
фосфатирования
Руководитель практической
подготовки от ДГТУ
______________________________М.А. Таутиева
Задание принял к исполнению
______________________________И.П. Крутиков
2
3.
МИНИСТЕРСТВО НАУКИ И ВЫСШЕГО ОБРАЗОВАНИЯ РОССИЙСКОЙФЕДЕРАЦИИ
ФЕДЕРАЛЬНОЕ ГОСУДАРСТВЕННОЕ БЮДЖЕТНОЕ
ОБРАЗОВАТЕЛЬНОЕ УЧРЕЖДЕНИЕ ВЫСШЕГО ОБРАЗОВАНИЯ
«ДОНСКОЙ ГОСУДАРСТВЕННЫЙ ТЕХНИЧЕСКИЙ
УНИВЕРСИТЕТ» (ДГТУ)
Факультет Биоинженерия и ветеринарная медицина
Подразделение, ответственное за
реализацию образовательной
программы или ее компонентов
кафедра «Химия»
Рабочий график (план) проведения практической подготовки
№
1
Мероприятие
Срок выполнения
3
Прохождение вводного и первичного инструктажа по охране
труда на рабочем месте, и инструктажа по пожарной
безопасности на объекте. Изучение правил охраны труда и
пожарной безопасности, правил внутреннего трудового
распорядка профильной организации
Знакомство с предприятием. Изучение предприятия. Анализ
использования ресурсов и материально-технического
обеспечения деятельности предприятия. Анализ
функционального пространства предприятия
Подведение итогов и написание отчета
4
Подготовка и предоставление отчета о прохождении практики 29.07.2023
2
19.06.2023
20.06.2023 – 26.06.2023
27.06.2023 – 28.06.2023
Руководитель практической
подготовки от предприятия ___________________________________
К.М. Лопатин
Руководитель практической
подготовки от ДГТУ
_______________________________________ М.А. Таутиева
Ростов-на-Дону
2023 г.
ДНЕВНИК ПРОХОЖДЕНИЯ ПРАКТИЧЕСКОЙ ПОДГОТОВКИ
3
4.
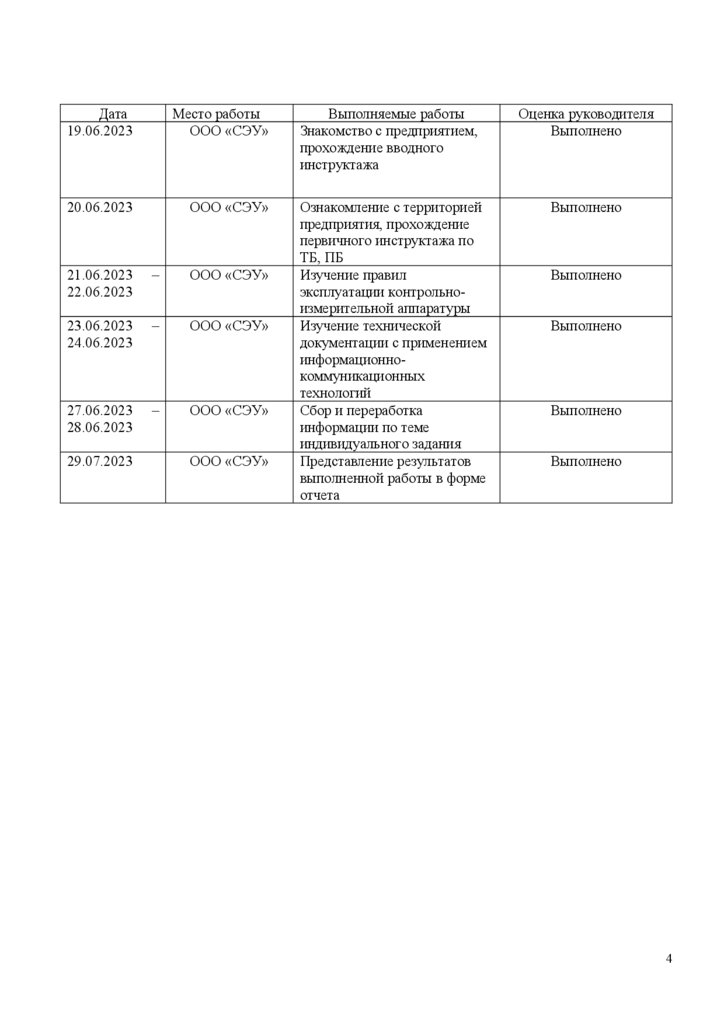
Дата19.06.2023
Место работы
ООО «СЭУ»
Выполняемые работы
Знакомство с предприятием,
прохождение вводного
инструктажа
Оценка руководителя
Выполнено
20.06.2023
ООО «СЭУ»
Ознакомление с территорией
предприятия, прохождение
первичного инструктажа по
ТБ, ПБ
Изучение правил
эксплуатации контрольноизмерительной аппаратуры
Изучение технической
документации с применением
информационнокоммуникационных
технологий
Сбор и переработка
информации по теме
индивидуального задания
Представление результатов
выполненной работы в форме
отчета
Выполнено
21.06.2023
22.06.2023
–
ООО «СЭУ»
23.06.2023
24.06.2023
–
ООО «СЭУ»
27.06.2023
28.06.2023
–
ООО «СЭУ»
29.07.2023
ООО «СЭУ»
Выполнено
Выполнено
Выполнено
Выполнено
4
5.
Кол-волистов
Форма
т
№ строки
Обозначения
Наименование
Примечание
Документация общая
1
А4
2
А4
ПП.680000.000
Изм Лист № Докум.
Крутиков
Разраб.
И.П.
Руков.п
Таутиева
р
М.А.
Дат
Подп. а
Задание на практику
1
Отчет по производственной
практике
18
ПП.680000.000
Отчет по практической
подготовке при проведении
производственной практики
(ведомость отчета)
Лит.
Лист
Листов
1
ДГТУ
Группа ЕИ21
5
6.
ОТЗЫВ - ХАРАКТЕРИСТИКАОбучающийся Илья Петрович Крутиков
2 курса группы ЕИ21 кафедра «Химия»
Вид практики производственная (технологическая)
Наименование места практики ООО «СЭУ»
Обучающийся выполнил задания программы практики
Процесс осаждения цинк-фосфатного покрытия на металлические изделия и
количественное определение состава электиролитов щелочного цинкования и
фосфатирования.
Дополнительно ознакомился/изучил
Инструкции по определению содержания ионов цинка в аммиачном растворе
и в цинктатном электролите; инструкцией по определению содержания
щелочи и карбонатов в цинктатном электролите. Методические материалы
по цинкованию, его технике и технологии
Заслуживает оценки____________
Руководитель практики
от предприятия
Лопатин К.М.
«29» июня 2023 г.
Оглавление
ВВЕДЕНИЕ................................................................................................................................................7
6
7.
1 Литературный обзор...............................................................................................................................81.1 Цинкатные электролиты.....................................................................................................................8
1.2 Технология процесса цинковго покрытия, осажденного из щелочного электролита с
фосфатированием....................................................................................................................................11
2 Методики количественного определения состава..............................................................................15
2.1 Определение содержание цинка в цинкатном электролите..........................................................15
2.2 Определение содержания щелочи и карбонатов в цинктатном электролите................................16
ЗАКЛЮЧЕНИЕ.......................................................................................................................................17
СПИСОК ЛИТЕРАТУРЫ.......................................................................................................................17
ВВЕДЕНИЕ
Примерно половина всего мирового потребления цинка приходится на долю
покрытий для защиты стальных изделий от коррозии. Цинк - металл серебристобелого цвета, при нанесении на сталь является анодом, поэтому защищает ее в том
числе и электрохимически.
7
8.
Электролитические цинковые покрытия, как правило, без финишной обработки неприменяются. Под финишной обработкой подразумевается создание на поверхности
цинка конверсионных пленок - хроматных, фосфатных и их разновидностей а также
пропитка конверсионных пленок уплотняющими составами и/или нанесение на
конверсионные пленки органических полимерных пленок.
Существенно более высокой коррозионной стойкостью по сравнению с чистым
цинком обладают покрытия сплавами цинка с никелем, кобальтом, железом с
последующей финишной обработкой.
Электролиты цинкования подразделяются на:
- кислые
- слабокислые
- нейтральные и слабощелочные
- щелочные
В первую группу входят простые кислые электролиты - сульфатные, хлоридные,
борфторидные, смешанные, например, сульфатно-хлоридные.
Во вторую входят хлоридные аммонийные, сульфатные аммонийные и хлоридные
безаммонийные.
В третью группу входят аммиакатные, амниокомплексные, пирофосфатные.
В последнюю - цианидные и цинкатные.
На сегодняшний день в промышленности распространены простые сульфатные и
цинкатные электролиты. Они отличаются друг от друга прежде всего зависимостью
выхода по току от плотности тока. Кислые электролиты не зависят от нее, а
цинкатные имеют сильную зависимость и, вследствие этого, ограниченную область
допустимых рабочих плотностей тока. Однако, рассеивающая способность в
цинкатном электролите выше, чем в щелочном и в нем можно обрабатывать
сложнопрофильные детали.
1 Литературный обзор
1.1 Цинкатные электролиты
8
9.
Особое место в ряду комплексных электролитов занимают щелочные цинкатныеэлектролиты. Они просты по составу и состоят из двух основных компонентов:
оксида цинка и щелочи.
Исторический этап в области электрохимического цинкования - разработка
цинкатных электролитов - был связан с работами Н. Т. Кудрявцева с сотрудниками,
проведенными в конце 1930 - начале 1940-х годов. В опубликованной в 1941 году
статье Н. Т. Кудрявцева и А. А. Никифоровой, было отмечено, что выполнен цикл
исследований в связи с возникновением настоятельной потребности в замене
вредных, нестойких, дорогих и дефицитных цианидных электролитов более
удобными в работе и дешевыми растворами.
В 1940-1941 годах исследователями была проведена всесторонняя проверка
цинкатных электролитов без добавок и на основании ее сделан вывод об их
непригодности к промышленному использованию, так как без добавок из цинкатного электролита цинк выделяется на катоде в виде губчатых осадков даже при
низкой плотности тока (ниже предельной плотности тока).
Было изучено влияние около 30 различных органических и неорганических веществ
на качество покрытий. В электролите с добавкой соли олова, показавшем
наилучшие результаты, были исследованы влияние концентрации цинка и свободной щелочи на качество покрытия, связь между концентрацией цинка и допустимым
верхним пределом плотности тока, выбраны оптимальный состав электролита и
режим работы.
Для
промышленного
применения
первоначально
предложенный
цинкатный
электролит имел состав:
Zn
8- 10 г/л (0,12-0,15 н)
КОН своб..
80 - 200 г/л (1,5-3,5 н)
или NаОН своб.
60 - 140 г/л (1,5-3,5 н)
Sn
0,15 -0,25 г/л
Электролит работал при температуре 50°С и катодной плотности тока 0,4-2,5 А/дм 2
с выходом потоку 98-100%, против 70-80% в цианидных растворах. Было
установлено, что катодная поляризация в цинкатных растворах носит преиму9
10.
щественноконцентрационный
характер
и
снижается
при
перемешивании.
Перемешивание электролита позволило увеличить верхний предел плотности тока в
2-3 раза и, соответственно, повысить производительность процесса.
Электролит был внедрен в промышленность, успешно применялся на ряде
предприятий в годы Великой Отечественной войны.
За рубежом процесс щелочного бесцианидного цинкования был разработан позднее
на основе запатентованного в 1942 году электролита Кутцельнига. Предложенный
электролит проявлял тенденцию к образованию тусклых, губчатых осадков и
поэтому первоначально не нашел практического применения. Лишь после
применения органических добавок, улучшающих качество осадков, электролит
начал использоваться.
Однако все предложенные электролиты не могли в полной мере соперничать с
цианидными электролитами в производительности и качестве покрытий. На
практике обнаружилась малая производительность цинкатных электролитов по
сравнению с высоко цианидными электролитами.
Позже
Н.
Т.
Кудрявцевым
с
сотрудниками
был
предложен
новый,
усовершенствованный вариант этого нециа- нидного электролита, содержащего
высокоэффективную блескообразующую добавку, который был внедрен на
автомобильном заводе им. Ленинского комсомола (АЗЛК) и проработал там
несколько лет.
Исследования
механизма
действия
добавок
легли
в
основу
современных
бесцианидных электролитов цинкования нового поколения. Сам электролит
цинкования по существу остается неизменным с момента его изобретения и состоит
из двух основных компонентов - цинка и щелочи:
Zn( мет)
KOH
8-15 г/л
60-150 г/л
Усилия исследователей были направлены на поиск новых органических и
неорганических веществ, добавление которых к электролиту позволило бы
улучшить технологические свойства цинкатного электролита, расширить диапазон
рабочих плотностей тока, повысить качество покрытий.
10
11.
1.2 Технология процесса цинковго покрытия, осажденного из щелочногоэлектролита с фосфатированием
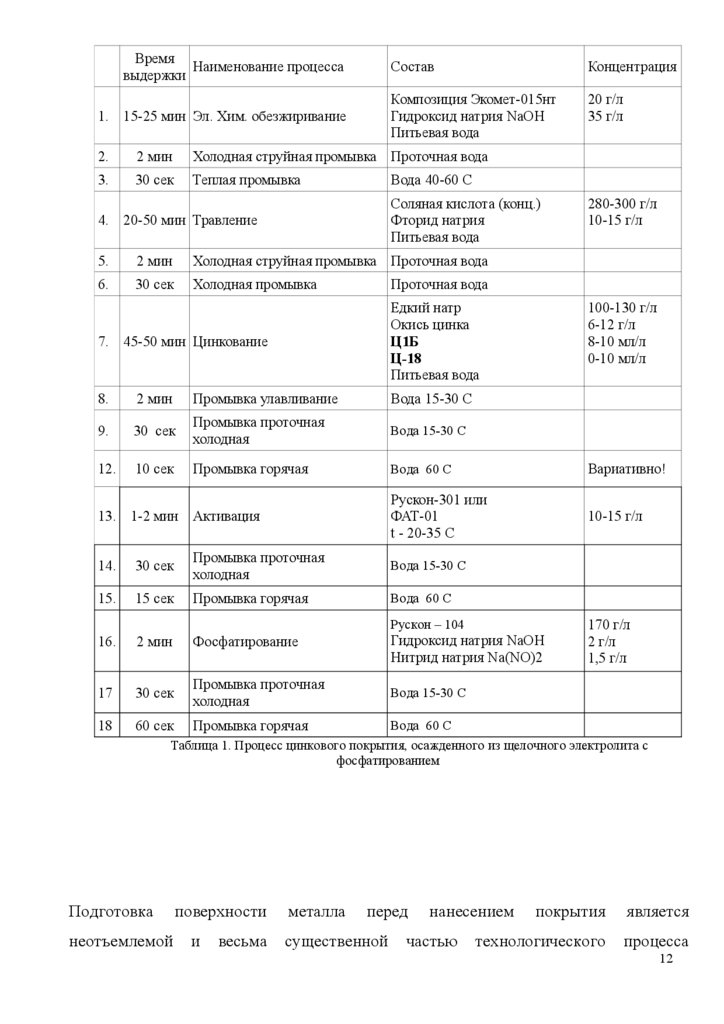
Процесс осаждения цинк-фосфатного покрытия на металлические изделия
происходит в несколько этапов (таблица 1).
Рабочий объем ванны фосфатирования = 910 литров.
11
12.
ВремяНаименование процесса
выдержки
1. 15-25 мин Эл. Хим. обезжиривание
Состав
Концентрация
Композиция Экомет-015нт
Гидроксид натрия NaOH
Питьевая вода
20 г/л
35 г/л
2.
2 мин
Холодная струйная промывка Проточная вода
3.
30 сек
Теплая промывка
Вода 40-60 С
Соляная кислота (конц.)
Фторид натрия
Питьевая вода
4. 20-50 мин Травление
5.
2 мин
Холодная струйная промывка Проточная вода
6.
30 сек
Холодная промывка
280-300 г/л
10-15 г/л
Проточная вода
7. 45-50 мин Цинкование
Едкий натр
Окись цинка
Ц1Б
Ц-18
Питьевая вода
8.
2 мин
Промывка улавливание
Вода 15-30 С
9.
30 сек
Промывка проточная
холодная
Вода 15-30 С
12.
10 сек
Промывка горячая
Вода 60 С
Вариативно!
Рускон-301 или
ФАТ-01
t - 20-35 С
10-15 г/л
13. 1-2 мин Активация
14.
30 сек
Промывка проточная
холодная
Вода 15-30 С
15.
15 сек
Промывка горячая
Вода 60 С
16.
2 мин
Фосфатирование
17
30 сек
Промывка проточная
холодная
18
60 сек
Промывка горячая
Рускон – 104
100-130 г/л
6-12 г/л
8-10 мл/л
0-10 мл/л
Гидроксид натрия NaOH
Нитрид натрия Na(NO)2
170 г/л
2 г/л
1,5 г/л
Вода 15-30 С
Вода 60 С
Таблица 1. Процесс цинкового покрытия, осажденного из щелочного электролита с
фосфатированием
Подготовка
неотъемлемой
поверхности
и
весьма
металла
перед
существенной
нанесением
частью
покрытия
является
технологического
процесса
12
13.
цинкования. Основная задача подготовительных операций заключается в удалении спокрываемой поверхности загрязнений и ее активирование для обеспечения
прочности сцепления покрытия с металлом основы.
На первом этапе происходит электрохимическое обезжиривание.
Очистка изделий при электрохимическом обезжиривании происходит в процессе
электролиза, когда сами изделия выполняют роль одного из электродов - катода или
анода. В первом случае обезжиривание называют катодным, во втором - анодным. В
качестве противоположного электрода при электрохимическом обезжиривании
применяют полосы из обычной малоуглеродистой или никелированной стали.
Недопустимо применение электродов из нержавеющей стали в качестве анода из-за
возможности
растворения
хрома,
входящего
в
состав
стали.
Скорость
обезжиривания определятся плотностью тока и другими параметрами процесса
температурой электролита и его химическим составом.
При катодном обезжиривании на поверхности обезжириваемых деталей бурно
выделяются водород, при анодном, соответственно, кислород. Выделяющиеся газы
в течение первых же секунд разрывают и удаляют пленку жировых и загрязнений и
выполняют роль эмульгаторов. Кроме того, выделяющиеся пузырьки газа создают
вдоль поверхности детали вертикальный поток электролита, который энергично
перемешивает электролит, улучшая обезжиривание. В этом случае ПАВэмульгаторы можно не применять или их концентрация должна быть понижена
чтобы не вызвать избыточное пенообразование.
Далее идет холодная струйная промывка, затем теплая промывка (вода 40-60
°C). После него наступает момент травления.
Травление – процесс удаления окалины, ржавчины, оксидов и других продуктов
коррозии с поверхности металлов в разбавленных, чаще всего неорганических
кислотах (соляная кислота).
В задачи травления входит максимальное ускорение удаления оксидов при
минимальном растворении металла детали. С этой целью в кислотные растворы
вводят ингибиторы коррозии, которые адсорбируясь на уже протравленной
поверхности стали, тормозят ее дальнейшее растворение, не препятствуя
13
14.
взаимодействию кислоты с оксидами.Далее идет холодная струйная промывка (2 минуты), затем холодная промывка (
30 секунд). На следующем этапе происходит цинкование.
Процесс цинкования длится 45-50 минут. Цинк наносят на углеродистые стали и
чугуны (иногда на алюминий и некоторые другие металлы), главным образом, с
целью антикоррозионной защиты. Поэтому доминирующим качеством цинковых
покрытий является их коррозионная стойкость в совокупности с физикомеханическими свойствами покрытий - внешним видом, прочностью сцепления с
основой, пластичностью и некоторыми другими.
Оценку внешнего вида цинковых покрытий проводят визуальным осмотром без
применения увеличительной техники.
После промывки наступает процесс активации.
Целью активации является удаление тонких оксидных и адсорбционных пленок
различных веществ, имеющихся на поверхности и ухудшающих сцепление
покрытия с основой. Активацию желательно выполнять в растворе, “родственном”
электролиту цинкования, следуя принципу: кислая активация перед кислыми
электролитами, щелочная – щелочными.
Активатор фосфатирования «Рускон-301» - предназначен для активации стальных и
оцинкованных изделий перед фосфатированием.
После промывки холодной и горячей водой, наступает процесс фосфатирование.
Фосфатирование - химическая обработка изделий, в результате которой на их
поверхности образуется солевое (фосфатное) покрытие. Фосфатирование может
проходить при температуре рабочего раствора 20-40оС или 40-70оС. Рускон – 104
используют
для
фосфатирования
стальных
изделий
перед
окраской,
промасливанием и холодной деформацией методом окунания, а также получения
противозадирного покрытия в промышленном производстве.
14
15.
2 Методики количественного определения состава2.1 Определение содержание цинка в цинкатном электролите
Метод основан на титровании ионов цинка (Zn 2+) Трилоном Б в присутствии
индикатора эриохрома черного Т (ЭХЧТ). В слабощелочной среде цинк образует
растворимый в воде комплекс. В эквивалентной точке в присутствии эриохрома
черного «Т» наблюдается изменение фиолетовой окраски раствора в синюю.
В коническую колбу на 250 мл внесем 1 мл электролита, предварительно
отфильтрованного электролита,
прилили 50 мл дистиллированной воды, 10 мл
аммиачного буферного раствора 0,1 грамм ( на кончике шпателя) сухой индикатор
смеси ЭХЧТ. Тировали 0,1 Н раствором Трилона Б до перехода фиолетовой окраски
в синюю (V1 , мл).
Содержание ионов цинка (Zn2+) в г/л рассчитали по формуле:
Zn
2 +¿=
V 1∗0,00327∗1000∗К
¿
V
, где
V1 - количество О,1Н раствора трилона Б, пошедшего на титрование, мл;
0,00327- теоретический титр О,1Н раствора трилона Б по цинку;
V - объем электролита, взятый для анализа, мл;
К- поправочный коэффициент к титру О,1 Н трилона Б
Также существует второй метод:
К 2 мл электролита добавили 50 мл дистиллированной воды, 10 мл аммиачного
буферного раствора 0,1 г (на кончике шпателя) сухой индикаторной смеси ЭХЧТ.
Титровать 0,1 Н раствором Трилона Б до перехода фиолетовой окраски в синюю (V1
, мл).
Zn
¿
2 +¿=6,538∗ K∗V ¿
15
16.
2.2 Определение содержания щелочи и карбонатов в цинктатномэлектролите.
Метод основан на реакции нейтрализации. Данным методом определяют щелочь
(NaOH) и карбонаты (Na2CO3). Пробу электролитов последовательно титруем
соляной кислотой в присутствии индикаторов фенолфталеина и метилового
оранжевого.
В присутствии фенолфталеина титруем свободный едкий натр и половину карбоната
натрия оставшийся карбонат натрия титруем в присутствии индикатора метилового
оранжевого. Цинк в растворе предварительно связываем в устойчивый комплекс с
Трилоном Б.
Предварительно необходимо провести определение ионов цинка в электролите по
инструкции «Определение содержания ионов цинка в цинкатном элетролите»
В коническую колбу на 250 мл внесем 1 мл (V) предварительно отфильтрованного
электролита, добавим О,1 Н раствор Трилон Б, в обьеме, пошедшем на титрование
ионов цинка ( Zn2+), прильём 50 мл дистиллированной воды и 1-2 капли индикатора
фенолфталеина.
Титруем О,1 Н раствором соляной кислоты до обесцвечивания (V1 , мл). В это же
раствор добавим несколько капель метилового оранжевого и продолжим титрование
соляной кислотой до изменения окраски из желтой в оранжевую (V2, мл).
Содержание щелочи в г/л рассчитываем по формуле:
NaOH=
( V 1 V 2 )∗0,004 , где
V
0,004-г/экв едкого натра, соответствующий 1 мл 0,1 Н раствора соляной кислоты
Содержание карбонатов в г/л рассчитываем по формуле:
N a2 CO3 =
V 1∗2∗0,0053
, где
V
0,0053- г/экв карбоната натрия, соответствующий 1 мл 0,1 Н раствора соляной
кислоты
16
17.
Второй метод:K 2,5 мл электролита добавили 50 мл дистиллированной воды, 10 мл хлорида бария,
0,1 M фенолфталеина титруем щавелевой кислотой 0,5 H до исчезновения
малиновой окраски.
Расчет:
NaOH=V ∗8,0 где V- объем щавелевой кислоты, пошедший на титрование, мл.
ЗАКЛЮЧЕНИЕ
В ходе практики был изучен процесс осаждения цинк-фосфатного покрытия на
металлические изделия и научился определять содержание цинка, щелочи и
карбонатов в цинктатном электролите.
СПИСОК ЛИТЕРАТУРЫ
1.
Окулов В. В. Цинкование. Техника и технология. – Глобус, 2008.
17
18.
2.Михайлова А. Г. Гальваническое цинкование //18.03. 01 Химическая
технология. – 2018.
3.
Xu, L. Phosphating treatment and corrosion properties of Mg–Mn–Zn alloy for
biomedical application / L. Xu, E. Zhang, K. Yang /Journal of Materials Science:
Materials in Medicine. – 2009. – Т. 20. – №. 4. – С. 859-867.
18

















 industry
industry








