Similar presentations:
Теория электролитической диссоциации
1.
Учитель химииЛицея № 387 им. Н.В.Белоусова
Кировского района Санкт-Петербурга
Воронцова Екатерина Михайловна
2.
Настоящий ученикучится открывать
неизвестное с
помощью
известного и тем
самым
приближается к
учителю.
Иоганн Вольфганг
Гёте
3.
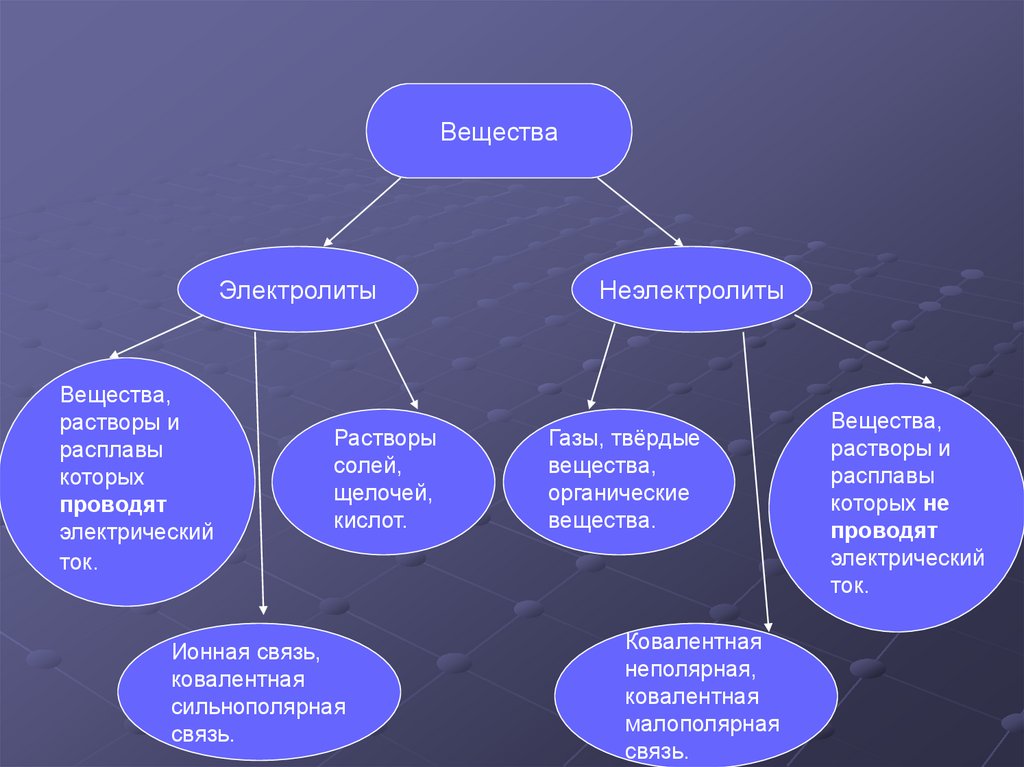
ВеществаЭлектролиты
Вещества,
растворы и
расплавы
которых
проводят
электрический
ток.
Растворы
солей,
щелочей,
кислот.
Ионная связь,
ковалентная
сильнополярная
связь.
Неэлектролиты
Газы, твёрдые
вещества,
органические
вещества.
Ковалентная
неполярная,
ковалентная
малополярная
связь.
Вещества,
растворы и
расплавы
которых не
проводят
электрический
ток.
4.
Теория электролитическойдиссоциации.
Сванте Аррениус (1887 г.).
1. При растворении в воде электролиты
распадаются на положительно и отрицательно
заряженные ионы.
Процесс распада электролита на ионы при
растворении его в воде или расплавлении
называется электролитической диссоциацией.
2. Под действием электрического напряжения
катионы двигаются к катоду, а анионы к аноду.
3. Диссоциация – обратимый процесс. Ассоциация – процесс соединения ионов.
5. Строение молекулы воды
O-
104,50
H
H
+
5
6. Механизм электролитической диссоциации хлорида натрия.
Ионный вид связи.Расположите в правильной
последовательности этапы механизма.
1. Диссоциация хлорида
натрия.
2. Гидратация – окружение
молекулами воды ионов
натрия и хлора. Образование
гидратированных ионов.
3. Ориентация полярных
молекул воды вокруг
кристалла хлорида натрия.
7. Механизм электролитической диссоциации хлорида натрия.
Ионный вид связи.Проверьте правильную
последовательность этапов
механизма.
1. Ориентация полярных
молекул воды вокруг
кристалла хлорида натрия.
2. Диссоциация хлорида
натрия.
3. Гидратация – окружение
молекулами воды ионов
натрия и хлора. Образование
гидратированных ионов.
8. Механизм электролитической диссоциации соляной кислоты.
Ковалентная полярная связь.Подумайте, сколько этапов в
данном механизме, что на них
происходит?
Проверяем!
1. Ориентация полярных
молекул воды вокруг
молекулы соляной
кислоты.
3. Диссоциация соляной кислоты.
2. Изменение вида связи с
ковалентной полярной
на ионную.
4. Гидратация. Образование гидратированных ионов.
9. Правила составления синквейна.
1. Тема (1 существительное).2. Описание темы (2 прилагательных).
3. Описание действия в рамках темы ( 3
глагола)
4. Фраза из 4 слов, показывающая
отношение к теме.
5. Суть темы ( 1 слово).
10. Домашнее задание.
Учить тему.Задачник № 2.1
Учебник с.22 №5 (творческое задание
по желанию)









 chemistry
chemistry








