Similar presentations:
Карбоновые кислоты: строение, классификация и номенклатура, физические свойства
1.
КАРБОНОВЫЕ КИСЛОТЫ:СТРОЕНИЕ, КЛАССИФИКАЦИЯ И
НОМЕНКЛАТУРА, ФИЗИЧЕСКИЕ
СВОЙСТВА
2.
Какиеклассы
кислородсодержащих
органических веществ вы знаете?
2. Какие из веществ данных классов способны
окисляться?
3. От чего зависят продукты окисления?
4. Как называются конечные продукты
окисления спиртов и альдегидов в кислой среде?
5. Какие карбоновые кислоты вы знаете?
Почему их называют карбоновыми кислотами?
1.
3.
Открытие кислот:Благодаря работам
известного шведского
химика Карла Вильгельма
Шееле к концу 18 века стало
известно около десяти
различных органических
кислот.
Он выделил и
описал щавелевую,
лимонную, молочную и
другие кислоты.
4.
5.
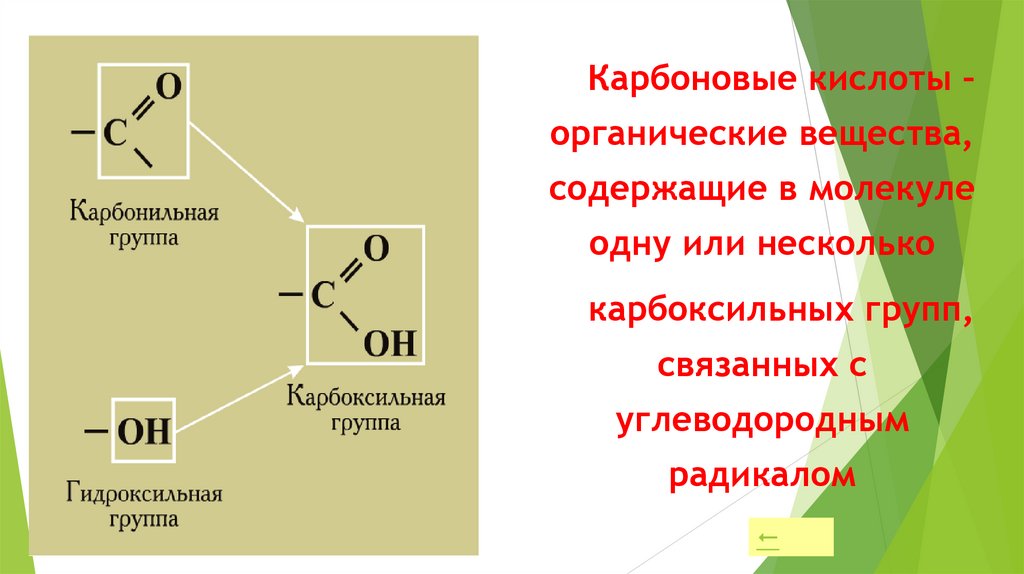
Карбоновые кислоты –органические вещества,
содержащие в молекуле
одну или несколько
карбоксильных групп,
связанных с
углеводородным
радикалом
6.
Классификациякарбоновых кислот
7.
Номенклатуракарбоновых кислот
8.
Функциональной группой карбоновых кислотявляется карбоксильная группа. Именно она
определяет характерные химические свойства
кислот.
9.
Строениекарбоксильной
группы
10.
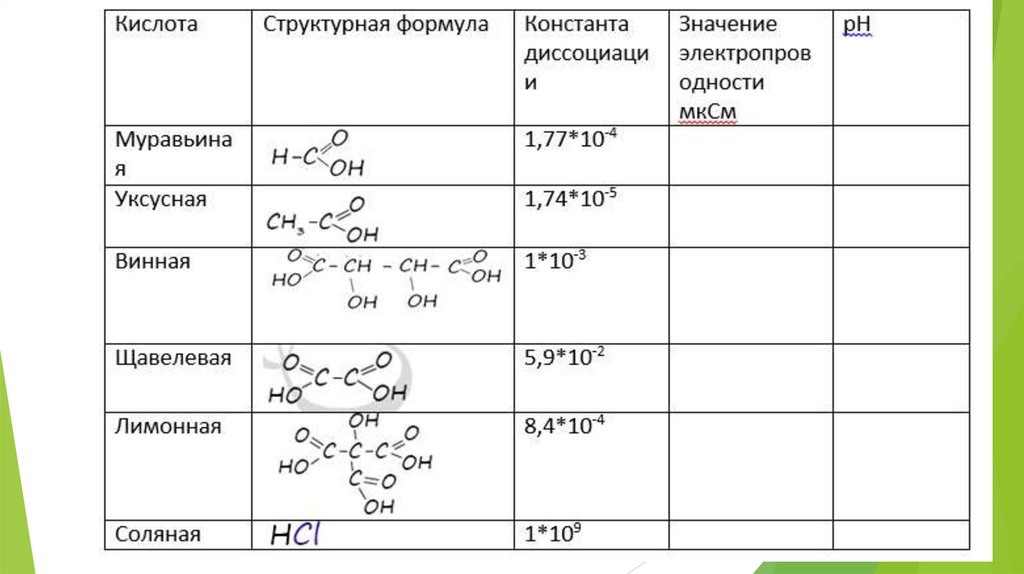
Определение силыкислот
11.
Определение силы кислот с помощьюспециальных датчиков: pH-метра и
электропроводности
Работа pH-метра основана на измерении электродвижущей
силы (ЭДС), которая создается электродами после
погружения в раствор.
Чем меньше значения рН, тем сильнее кислота
12.
Единицей электропроводности по системе СИявляется сименс (См) – электрическая проводимость
участка электрической цепи с сопротивлением 1 Ом.
Чем больше значения электропроводности, тем сильнее кислота.
Для сильных кислот эти значения примерно 20000мкСм,
для дистиллированной воды – примерно 15 -20 мкСм за счёт того, что
дистиллированная вода поглощает углекислый газ и образующаяся
угольная кислота незначительно диссоциирует на ионы.
13.
Выполнение лабораторной работыЦель работы: определить рН и электропроводность растворов
карбоновых кислот, выяснить их взаимосвязь; определить
факторы, влияющие на силу кислот, сравнить рН и
электропроводность карбоновых кислот с неорганическими
кислотами.
14.
15.
Вывод: карбоновые кислоты являются кислотами………. силы; сила кислот зависит от:
А) длины углеводородного радикала, т.к. увеличение числа
атомов углерода в радикале уменьшает полярность связи
О – Н, а значит, уменьшает силу кислот;
Б) количества карбоксильных групп; (по 1й ступени диссоциации
дикарбоновые
кислоты
сильнее
монокарбоновых),
т.к.
от
количества карбоксильных групп зависит число ионов водорода,
определяющих силу кислот;
16.
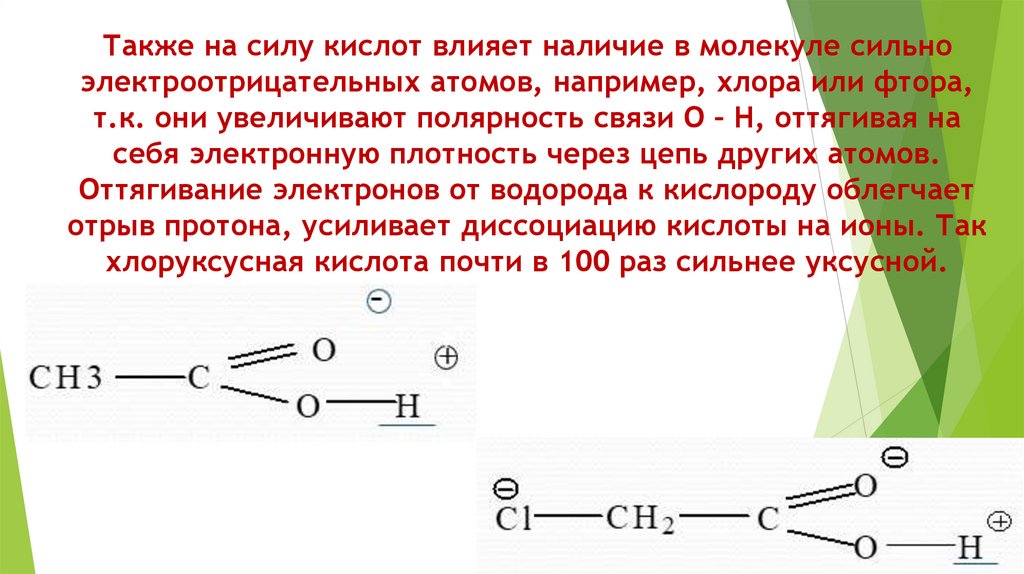
Также на силу кислот влияет наличие в молекуле сильноэлектроотрицательных атомов, например, хлора или фтора,
т.к. они увеличивают полярность связи О – Н, оттягивая на
себя электронную плотность через цепь других атомов.
Оттягивание электронов от водорода к кислороду облегчает
отрыв протона, усиливает диссоциацию кислоты на ионы. Так
хлоруксусная кислота почти в 100 раз сильнее уксусной.
17.
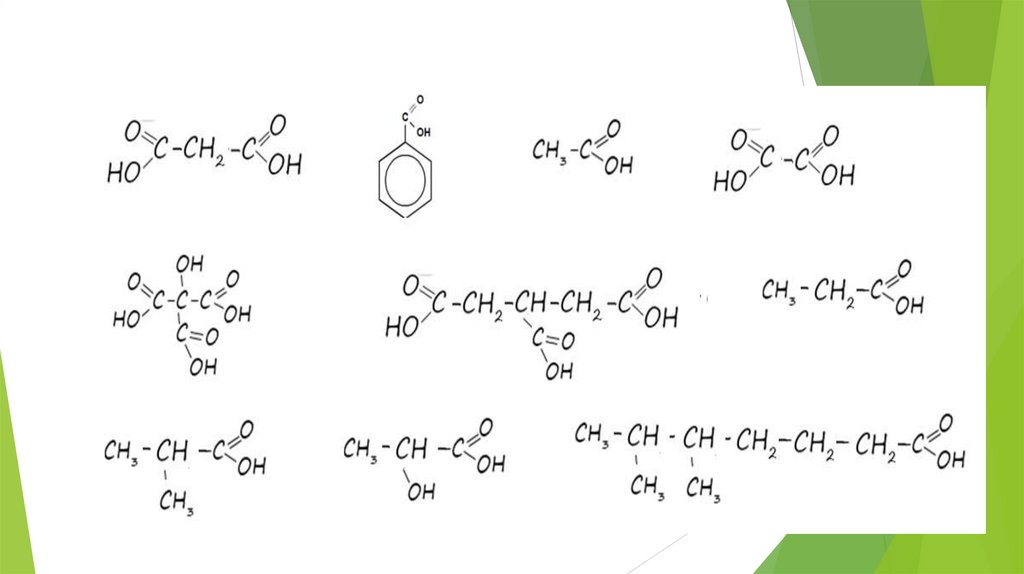
Объясните данный ряд кислот18.
Тестирование:1. Какие из названных кислот являются органическими?
а) муравьиная; б) азотная;
в) серная; г) лимонная.
2. Почему болезненны укусы муравьев?
а) обжигают муравьиной кислотой;
б) выделяют яд;
в) разъедают муравьиной щелочью;
г) вонзают острые зубчики.
3. Как называют соли уксусной кислоты?
а) ацетаты; б) бустилаты;
в) пропилаты; г) постулаты.
4. Какого названия кислоты не существует?
а) лимонная; б) щавелевая;
в) винная; г) виноградная.
5. Какие кислоты являются витаминами?
а) никотиновая; б) аскорбиновая;
в) ацетилсалициловая; г) янтарная.
А,Г
А
А
Г
А,Б
19.
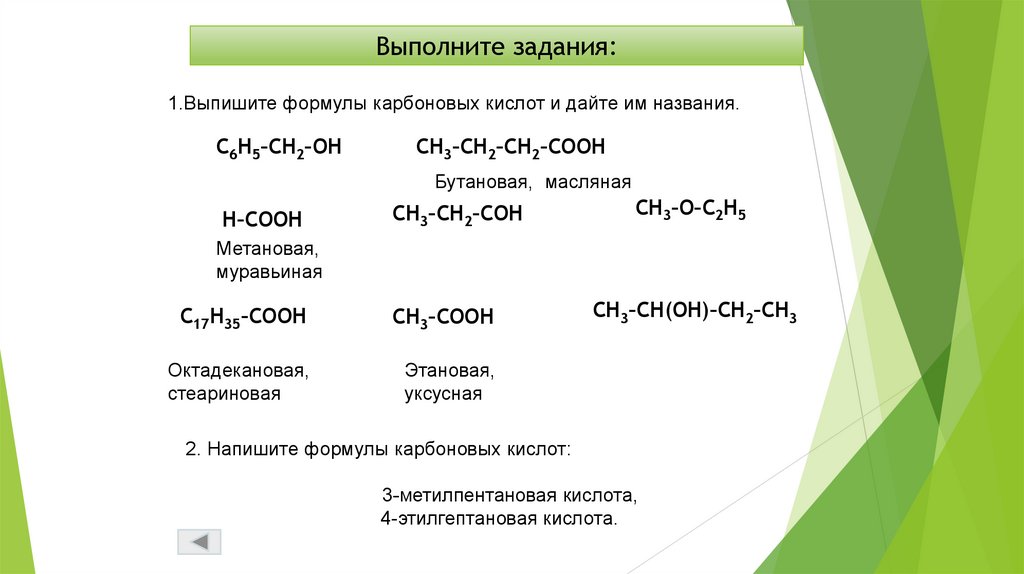
Выполните задания:1.Выпишите формулы карбоновых кислот и дайте им названия.
C6H5–CH2–OH
CH3–CH2–CH2–COOH
Бутановая, масляная
H–COOH
CH3–CH2–COH
CH3–O–C2H5
Метановая,
муравьиная
C17H35–COOH
CH3–COOH
Октадекановая,
стеариновая
Этановая,
уксусная
CH3–CH(OH)–CH2–CH3
2. Напишите формулы карбоновых кислот:
3-метилпентановая кислота,
4-этилгептановая кислота.
20.
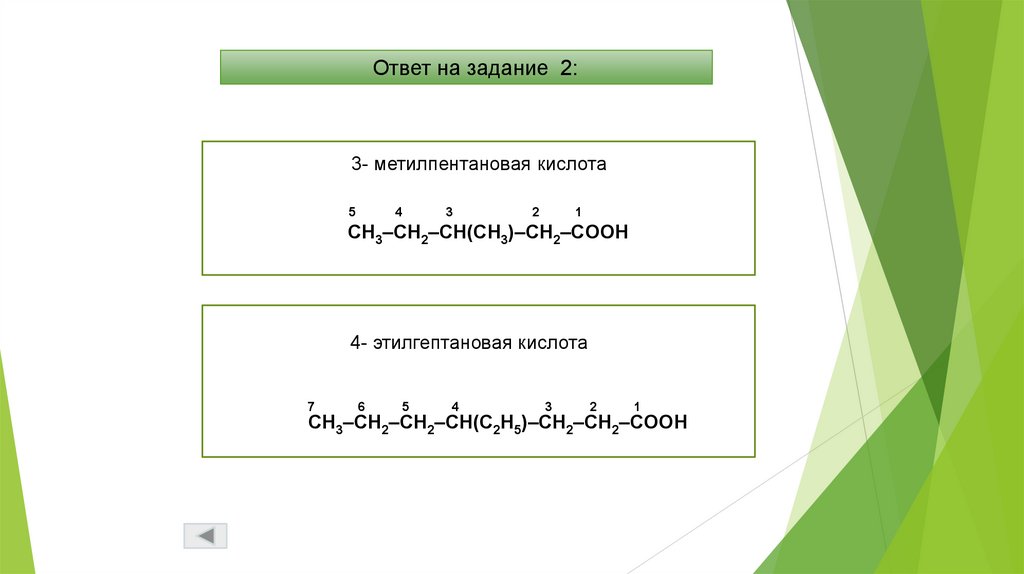
Ответ на задание 2:3- метилпентановая кислота
5
4
3
2
1
CH3–CH2–CH(CH3)–CH2–COOH
4- этилгептановая кислота
7
6
5
4
3
2
1
CH3–CH2–CH2–CH(C2H5)–CH2–CH2–COOH
21.
Домашнее задание1)
2)
3)
4)
Записать физические свойства кислот, показать зависимость
физических свойств карбоновых кислот от строения молекулы.
Почему среди кислот нет газов?
Какие типы изомерии характерны для карбоновых кислот?
Записать примеры.
Записать формулы всех изомеров и двух гомологов для
пентановой кислоты. Назвать их.
Выучить тривиальные названия кислот до С6 включительно.
1 вопрос – на оценку «3»
1 и 2 вопросы – на оценку «4»
1, 2, 3 вопросы – на оценку «5»















 chemistry
chemistry








