Similar presentations:
Карбоновые кислоты. Карбоновые кислоты в живых организмах
1.
Карбоновые кислоты2. Карбоновые кислоты в живых организмах
3. Карбоновые кислоты в живых организмах
В 1714 г. по указу Петра I в Петербурге был заложенаптекарский сад.
Там выращивали лекарственные
растения, снабжая ими аптеки или перерабатывая их
на лекарства. Так вот, листья одного из таких
растений, помещенные в молоко, предохраняют его от
скисания. Свежее мясо и рыба, переложенные этим
растением, дольше сохраняются. Из его корней можно
получить желтый краситель. Из волокон можно
изготовить сети, не гниющие в воде. Мы знаем это
растение по сказке Андерсена.
Личный опыт общения с этим растением способен
довести до слез. Наконец, это растение узнают даже
слепые. Это – …Назовите это растение!
4. Карбоновые кислоты в живых организмах
Щавелеваякислота. HOOC-COOH
Она широко распространена в природе: содержится в
щавеле,
смородине,
апельсинах,
малине.
Но её
не
используют
в
пищевой
промышленности.
Эта кислота сильнее уксусной в 200 раз и может
разъедать посуду.
Её соли могут
откладываться в организме человека, образуя камни.
5.
Эту кислоту называли «кислойвлажностью», «древесной кислотой»,
т.к. долгое время ее получали из
древесины.
В 1789 г. русский химик
Т.Е.Ловиц впервые получил
кристаллическую
(ледяную) уксусную
кислоту.
6. Карбоновые кислоты – это производные углеводородов, содержащие в молекуле одну или несколько карбоксильных групп.
карбонильная группаO
C
OH
гидроксильная
группа
карбоксильная
группа
7. Классификация карбоновых кислот
1. По числу карбоксильных групп:Одноосновные : CH3COOH уксусная
Двухосновные : HOOC – CH2 – COOH малоновая
Многоосновные: HOOC – CH2C(OH)(COOH)CH2 –
COOH лимонная
2. По характеру углеводородного радикала:
Предельные : CH3 – (CH2)10 – COOH лауриновая
Непредельные: CH2 = CH – COOH акриловая
Ароматические: C6H5 – COOH бензойная
8. Общая формула одноосновных карбоновых кислот
R – COOH или CnH2n+1COOHНоменклатура:
К названию соответствующего предельного УВ
прибавляется окончание - овая и слово кислота:
Метан – метановая кислота HCOOH
Этан – этановая кислота CH3 - COOH
Пропан – пропановая CH3 – CH2 - COOH
Бутан – бутановая кислота СН3 – СН2 – СН2 - СООН
9.
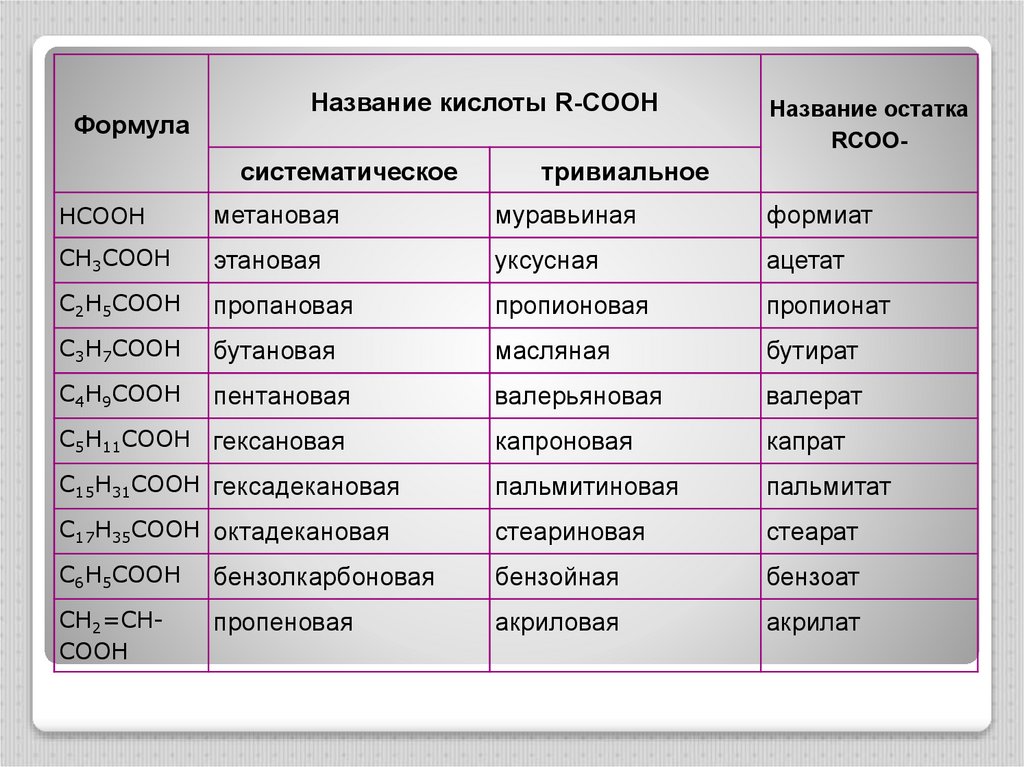
ФормулаНазвание кислоты R-COOH
систематическое
Название остатка
RCOO-
тривиальное
HCOOH
метановая
муравьиная
формиат
CH3COOH
этановая
уксусная
ацетат
C2H5COOH
пропановая
пропионовая
пропионат
C3H7COOH
бутановая
масляная
бутират
C4H9COOH
пентановая
валерьяновая
валерат
C5H11COOH
гексановая
капроновая
капрат
C15H31COOH гексадекановая
пальмитиновая
пальмитат
C17H35COOH октадекановая
стеариновая
стеарат
C6H5COOH
бензолкарбоновая
бензойная
бензоат
CH2=СHCOOH
пропеновая
акриловая
акрилат
10. Укажите формулы карбоновых кислот:
а) CH3 – CH3б) CH3 – CH2 – OH
в) CH3 – COOH
г) CH3 – O – CH3
д) CH3 – CH2 – COOH
11.
Выполните задания:1.Выпишите формулы карбоновых кислот и дайте им названия.
C6H5–CH2–OH
CH3–CH2–CH2–COOH
Бутановая, масляная
H–COOH
CH3–CH2–COH
CH3–O–C2H5
Метановая,
муравьиная
C17H35–COOH
CH3–COOH
Октадекановая,
стеариновая
Этановая,
уксусная
CH3–CH(OH)–CH2–CH3
2. Напишите формулы карбоновых кислот:
3-метилпентановая кислота,
4-этилгептановая кислота.
12. Физические свойства одноосновных карбоновых кислот
Низшие карбоновые кислоты – жидкости с острымзапахом, хорошо растворимые в воде.
С повышением относительной молекулярной массы
растворимость кислот в воде уменьшается, а
температура кипения повышается.
Высшие кислоты, начиная с пеларгоновой (нонановой)
CH3 – (CH2)7 – COOH, - твердые вещества, без запаха,
нерастворимые в воде.
13. Химические свойства кислот
Общие свойства карбоновых кислот аналогичнысоответствующим свойствам неорганических
кислот:
1.
2.
3.
4.
5.
Диссоциируют в водном растворе.
Реагируют с металлами.
Реагируют с основными и амфотерными
оксидами и гидроксидами.
Реагируют с солями более слабых летучих кислот.
Реагируют со спиртами
14. 1. Кислоты диссоциируют на ионы водорода и ионы кислотного остатка:
CH3COOHH+ + CH3COO-
2. Реагируют с металлами:
2CH3COOH + Zn
(CH3COO)2Zn + H2
ацетат цинка
Соли уксусной кислоты – ацетаты
15.
3. Реагируют с основными и амфотерными оксидами игидроксидами.
2HCOOH + MgO
(HCOO)2Mg + H2O
2CH3COOH + Zn(OH)2
(CH3COO)2Zn + H2O
4. Реагируют с солями более слабых летучих кислот.
2HCOOH + Na2SiO3
2HCOONa + H2SiO3
2CH3COOH + Na2CO3
2CH3COONa + H2O + CO2
5. Реагируют со спиртами.
O
O
R C
+ H OR*
R C
+ H2O
OH
O R*
кислота
спирт
сложный эфир
16. Получение карбоновых кислот
Окислением спиртовОкислением альдегидов
Окислением углеводородов
Существуют и другие способы получения карбоновых кислот
17.
Применение карбоновых кислотПрименение муравьиной кислоты
18. Уксусная кислота используется в химической промышленности
19.
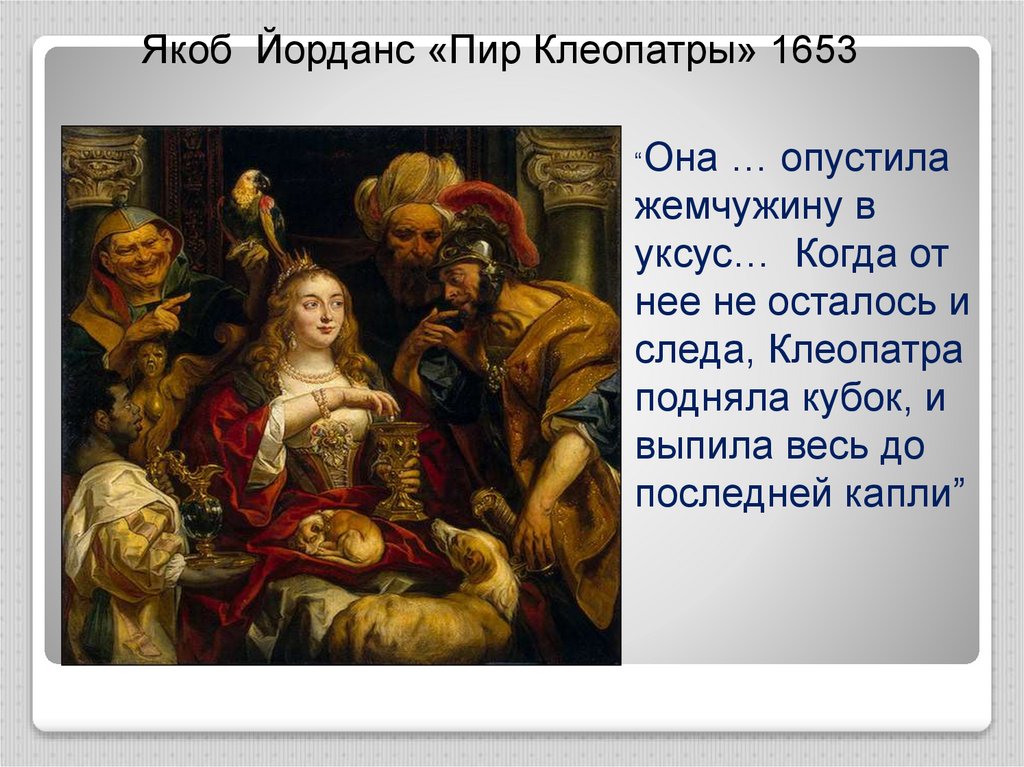
Якоб Йорданс «Пир Клеопатры» 1653“Она … опустила
жемчужину в
уксус… Когда от
нее не осталось и
следа, Клеопатра
подняла кубок, и
выпила весь до
последней капли”
20.
Картина написана на сюжет из «Естественной истории» Плиния Старшего (I в.). Египетскаяцарица Клеопатра (I в. до н. э.), славившаяся красотой и умом, отличалась также
экстравагантностью своего поведения.
Однажды на глазах своего возлюбленного, римского полководца Марка Антония, Клеопатра
растворила в бокале с уксусом крупную жемчужину, а затем выпила его содержимое. На
картине изображен момент, когда царица опускает в бокал серьгу, а Марк Антоний, его
спутник Энобард и негр-слуга застыли в немом изумлении, всем своим видом выражая
сожаление о погибшей ценности и одновременно — восхищение поступком Клеопатры. А
вот ухмылка и презрительный жест придворного шута яснее всяких слов говорят о
нелепости и глупости подобного расточительства.
Картина заставляет вспомнить нравоучительные аллегории Х. Босха и П. Брейгеля
Старшего.
Отрывок из произведения Г.Р.Хаггарда “Клеопатра”:
“… Она вынула из уха одну их тех жемчужин … и … опустила жемчужину в уксус. Наступило
молчание, потрясенные гости, замерев наблюдали, как несравненная жемчужина медленно
растворяется в крепком уксусе. Вот от ней осталось и следа, и тогда Клеопатра подняла
кубок, покрутила его, взбалтывая уксус, и выпила весь до последней капли…”
Римский историк Плиний-старший в своем труде «Естественная история» рассказывает об
эпизоде, когда Клеопатра побилась об заклад с Марком Антонием, что сумеет приготовить
самое драгоценное яство из когда-либо подававшихся. Клеопатра сняла одну из своих
жемчужных серег (как утверждал Плиний, ценой в баснословные 10 миллионов сестерциев)
и опустила ее в чашу кислого вина (уксуса). Жемчуг якобы растворился в уксусе, и
Клеопатра выпила чашу до дна, тем самым победив в этой затее.


















 chemistry
chemistry








