Similar presentations:
Производство азотных удобрений
1. Производство азотных удобрений
2. Азотные удобрения — неорганические и органические азотосодержащие вещества. Получают главным образом из синтетического аммиака.
Азотные удобрения представляютсобой белый или желтоватый
кристаллический порошок (кроме
цианамида калия и жидких
удобрений) , хорошо растворимы в
воде. Большинство из них обладает
высокой гигроскопичностью и требует
особой упаковки и хранение.
3. Азотные удобрения содержат азот в трех основных формах:
1) в форме аммиака, связанного с какой-нибудь минеральнойкислотой, — аммиачные удобрения;
2) в нитратной форме, т. е. в виде солей азотной кислоты,—
нитратные удобрения;
3) в амидной форме—амидные удобрения.
4.
• К аммиачным удобрениям относятся: сульфат аммония, хлористый аммоний,бикарбонат аммония, жидкие аммиачные удобрения.
• К аммиачно-нитратным удобрениям относятся: аммиачная селитра (нитрат
аммония, азотнокислый аммоний), известковая селитра (сульфонитрат аммония,
лейна-селитра, монтан-селитра, нитросульфат аммония).
• Нитратные удобрения — натриевая селитра (нитрат натрия, азотнокислый
натрий, чилийская селитра), кальциевая селитра (нитрат кальция, азотнокислый
кальций, известковая селитра, норвежская селитра), калийная селитра (нитрат
калия, азотнокислый калий). Калийная селитра, кроме азота, содержит калий и
является источником азотно-калийного питания растений.
• Амидные удобрения — мочевина (карбамид), цианамид кальция, мочевиноформальдегидные удобрения. Наиболее ценна мочевина.
5. Аммиачная селитра или нитрат аммония NH4NO3
АММИАЧНАЯ СЕЛИТРАИЛИ НИТРАТ АММОНИЯ NH4NO3
6. В основе процесса производства аммиачной селитры лежит гетерогенная реакция взаимодействия газообразного аммиака с раствором
В ОСНОВЕ ПРОЦЕССА ПРОИЗВОДСТВА АММИАЧНОЙ СЕЛИТРЫЛЕЖИТ ГЕТЕРОГЕННАЯ РЕАКЦИЯ ВЗАИМОДЕЙСТВИЯ
ГАЗООБРАЗНОГО АММИАКА С РАСТВОРОМ АЗОТНОЙ КИСЛОТЫ:
NH3+HNO3 = NH4NO3;
ΔН = —144.9КДЖ
ПРИНЦИПИАЛЬНАЯ СХЕМА ПРОИЗВОДСТВА:
7.
18.
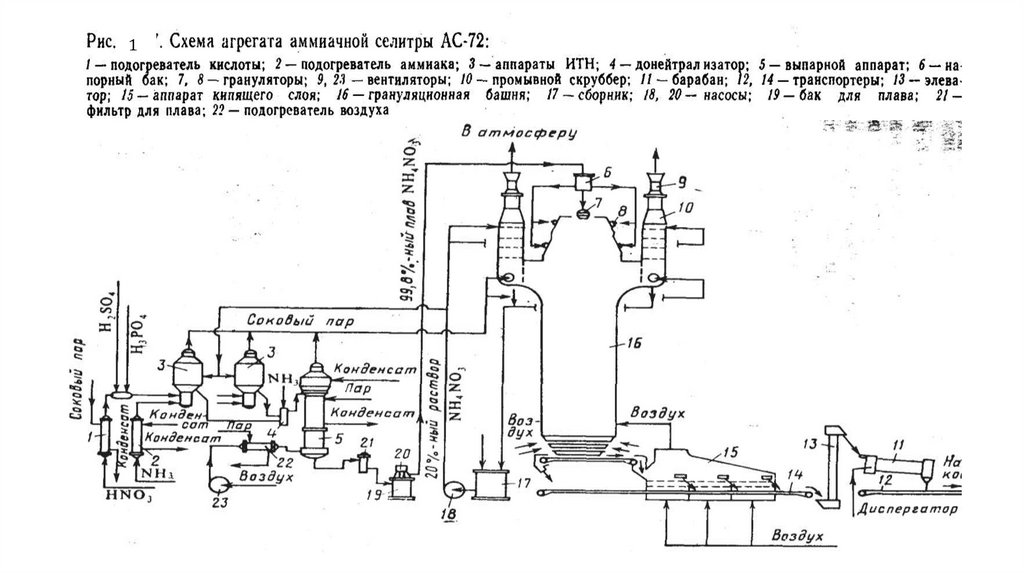
На рисунке 1 приведена схема современного крупнотоннажного агрегата по производствуаммиачной селитры АС-72 мощностью 1360 т/сут. Исходная 58—60 %-ная азотная кислота
подогревается в подогревателе до 70—80°С соковым паром из аппарата ИТН (специальные
аппараты непрерывного действия, в которых происходит реакция нейтрализации) 3 и подается на
нейтрализацию. Перед аппаратами 3 к азотной кислоте добавляют фосфорную и серную кислоты в
таких количествах, чтобы в готовом продукте содержалась 0,3—0,5% Р2О5 и 0,05—0,2% сульфата
аммония
В агрегате установлены два аппарата использования теплоты нейтрализации (ИТН),
работающие параллельно. Кроме азотной кислоты в них подают газообразный аммиак,
предварительно нагретый в подогревателе 2 паровым конденсатом до 120— 130°С. Количества
подаваемых азотной кислоты и аммиака регулируют таким образом, чтобы на выходе из аппарата
ИТН раствор имел небольшой избыток кислоты (2—5 г/л), обеспечивающий полноту поглощения
аммиака.
В нижней части аппарата происходит реакция нейтрализации при температуре 155—170°С;
при этом получается концентрированный раствор, содержащий 91—92% NH4NO3. В верхней части
аппарата водяные пары (так называемый соковый пар) отмываются от брызг аммиачной селитры и
паров азотной кислоты. Часть теплоты сокового пара используется на подогрев азотной кислоты.
Затем соковый пар направляют на очистку и выбрасывают в атмосферу.
9.
Кислый раствор аммиачной селитры направляют в донейтрализатор 4; куда поступает аммиак,необходимый для взаимодействия с оставшейся азотной кислотой. Затем раствор подают в
выпарной аппарат 5. Полученный плав, содержащий 99,7—99,8% селитры, при 175°С проходит
фильтр 21 и центробежным погружным насосом 20 подается в напорный бак 6, а затем в
прямоугольную металлическую грануляционную башню 16.
В верхней части башни расположены грануляторы 7 и 8, в нижнюю часть которых подают
воздух, охлаждающий падающие сверху капли селитры. Во время падения капель селитры с высоты
50—55 м при обтекании их потоком воздуха образуются гранулы удобрения. Температура гранул на
выходе из башни равна 90—110°С; горячие гранулы охлаждают в аппарате кипящего слоя 15. Это
прямоугольный аппарат, имеющий три секции и
снабженный решеткой с отверстиями.
Под решетку вентиляторами подают воздух; при этом создается псевдоожиженный слой
гранул селитры, поступающих по транспортеру из грануляционной башни. Воздух после охлаждения
попадает в грануляционную башню.
Гранулы аммиачной селитры транспортером 14 подают на обработку поверхностно-активными
веществами во вращающийся барабан. Затем готовое удобрение транспортером 12 направляют на
упаковку.
10. Карбамид или мочевина (NH2)2CO
КАРБАМИДИЛИ МОЧЕВИНА (NH2)2CO
Карбамид белое кристаллическое вещество,
содержащее 46,6% азота, среди азотных
удобрений занимает второе место по объему
производства после аммиачной селитры. Рост
производства карбамида обусловлен
широкой сферой его применения в сельском
хозяйстве. Он обладает большей
устойчивостью к выщелачиванию по
сравнению с другими азотными
удобрениями.
11.
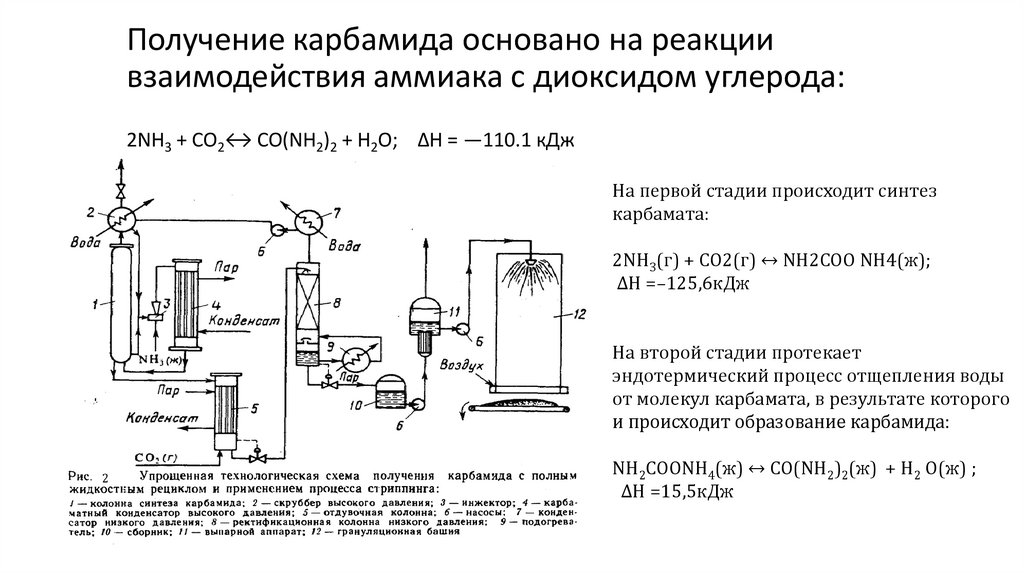
Получение карбамида основано на реакциивзаимодействия аммиака с диоксидом углерода:
2NH3 + CO2↔ CO(NH2)2 + H2O; ΔН = —110.1 кДж
На первой стадии происходит синтез
карбамата:
2NH3(г) + CO2(г) ↔ NH2СОО NH4(ж);
ΔН =–125,6кДж
На второй стадии протекает
эндотермический процесс отщепления воды
от молекул карбамата, в результате которого
и происходит образование карбамида:
2
NH2СООNH4(ж) ↔ CO(NH2)2(ж) + H2 O(ж) ;
ΔН =15,5кДж
12.
На рис. 2 приведена упрощенная схема крупнотоннажного агрегата синтеза карбамида сжидкостным рециклом и применением стриппингпроцесса. В ней можно выделить узел
высокого давления, узел низкого давления и систему грануляции. Водный раствор карбамата
аммония и углеаммонийных солей, а также аммиак и диоксид углерода поступают в нижнюю
часть колонны синтеза 1 из конденсатора высокого давления 4. В колонне синтеза при
температуре 170—190°С и давлении 13—15 МПа заканчивается образование карбамата и
протекает реакция синтеза карбамида. Расход реагентов подбирают таким образом, чтобы в
реакторе молярное отношение NH3:СО2 составляло 2,8—2,9. Жидкая реакционная смесь (плав)
из колонны синтеза карбамида поступает в отдувочную колонну 5, где стекает по трубкам вниз.
Противотоком к плаву подают сжатый в компрессоре до давления 13— 15 МПа диоксид
углерода, к которому для образования пассивирующей пленки и уменьшения коррозии
оборудования добавлен воздух в количестве, обеспечивающем в смеси концентрацию кислорода
0,5-0,8%. Отдувочная колонна обогревается водяным паром. Парогазовая смесь из колонны 5,
содержащая свежий диоксид углерода, поступает в конденсатор высокого давления 4. В него же
вводят жидкий аммиак. Он одновременно служит рабочим потоком в инжекторе 3, подающем в
конденсатор раствор углеаммонийных солей из скруббера 2 и при необходимости часть плава из
колонны синтеза. В конденсаторе образуется карбамат. Выделяющуюся при реакции теплоту
используют для получения водяного пара.
13.
Из верхней части колонны синтеза непрерывно выходят непрореагировавшие газы,поступающие в скруббер высокого давления 2, в котором большая часть их конденсируется за
счет водного охлаждения, образуя водный раствор карбамата и углеаммонийных солей.
Водный раствор карбамида, выходящий из отдувочной колонны 5, содержит 4-5%
карбамата. Для окончательного его разложения раствор дросселируют до давления 0,3-0,6
МПа и затем направляют в верхнюю часть ректификационной колонны 8. Жидкая фаза стекает
в колонне вниз по насадке противотоком к парогазовой смеси, поднимающейся снизу вверх;
из верхней части колонны выходят NH3, CO2 и водяные пары. Водяные пары конденсируются в
конденсаторе низкого давления 7, при этом растворяется основная часть аммиака и диоксида
углерода. Полученный раствор направляют в скруббер 2. Окончательная очистка газов,
выбрасываемых в атмосферу, производится абсорбционными методами (на схеме не
показана).
70%-ный водный раствор карбамида, выходящий из нижней части ректификационной
колонны 8, отделяют от парогазовой смеси и направляют после снижения давления до
атмосферного сначала на вы-парку, а затем на грануляцию. Перед распылением плава в
грануляционной башне 12 к нему добавляют кондиционирующие добавки, например
мочевиноформальдегидную смолу, чтобы получить неслеживающееся удобрение, не
портящееся при хранении.
14. Жидкие азотные удобрения
• растворы аммиачной селитры;• карбамида;
• кальциевой селитры;
• их смесей в жидком аммиаке или в концентрированной
аммиачной воде – так называемые аммиакаты.
15. Жидкие азотные удобрения
Плюсы• обеспечивает возможность
ускоренного строительства азотных
заводов по «короткой» схеме;
• дешевизна;
• жидкие удобрения не обладают такими
отрицательными свойствами твердых
удобрений, как гигроскопичность,
слеживаемость, согрегация и т.п
Минусы
• в случае большой их концентрации
происходит высаливание,
кристаллизация солей при понижении
температуры;
• требуется сооружение резервуаров
большой емкости для хранения
жидких удобрений;
• обладают повышенными
коррозионными свойствами по
отношению к черным металлам.













 chemistry
chemistry








