Similar presentations:
Организация проведения научных исследований в медицине
1.
АО “Медицинский Университет Астана”Кафедра менеджмента и экспериментальной деятельности в здравоохранении
СРС
На тему: “Организация проведения научных
исследований в медицине”
Выполнила: Ахметжанова Д.А.
Резидент УиА 155
Проверил: к.м.н. Айгужин Б. К.
г. Астана, 2017 г.
2. Научные исследования
• прикладные,фундаментальные,
стратегические научные исследования,
осуществляемые субъектами научной и
(или) научно-технической деятельности в
рамках научно-исследовательских, опытноконструкторских и технологических работ,
надлежащими научными методами и
средствами
в
целях
достижения
результатов научной и (или) научнотехнической деятельности.
3.
Компетенция государственных органов вобласти научной и (или) научно-технической
деятельности
Закон Республики Казахстан от 18 февраля
2011 года № 407-IV «О науке» (с
изменениями и дополнениями по состоянию
на 13.11.2015 г.)
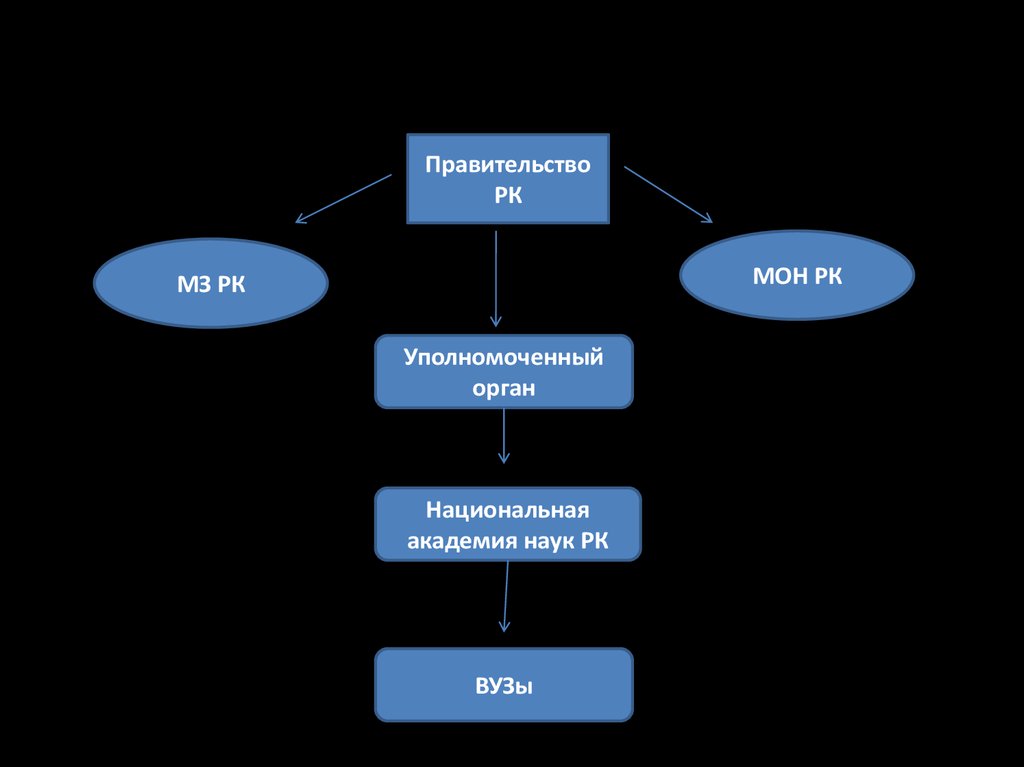
4.
ПравительствоРК
МОН РК
МЗ РК
Уполномоченный
орган
Национальная
академия наук РК
ВУЗы
5. Правительство Республики Казахстан:
1.2.
3.
4.
5.
разрабатывает основные направления государственной
политики в области науки и научно-технической деятельности
и организует ее осуществление;
определяет приоритетные направления научной, научнотехнической и инновационной деятельности в соответствии с
приоритетами социально-экономического развития, а также
приоритетные направления стратегических, фундаментальных
и прикладных научных исследований в Республике Казахстан;
вносит Президенту Республики Казахстан ежегодный
национальный доклад по науке;
утверждает правила аккредитации субъектов научной и (или)
научно-технической деятельности;
создает Высшую научно-техническую комиссию Республики
Казахстан при Правительстве Республики Казахстан и
утверждает ее положение и состав;
6. В компетенцию уполномоченного органа входят:
В компетенцию уполномоченногооргана входят:
1.
2.
3.
4.
5.
6.
координация научных, научно-технических проектов и программ
фундаментальных и прикладных научных исследований,
финансируемых из государственного бюджета;
разработка приоритетных направлений фундаментальных и
прикладных научных исследований в Республике Казахстан;
обеспечение
деятельности
Высшей
научно-технической
комиссии;
организация разработки научных, научно-технических проектов и
программ
фундаментальных
и
прикладных
научных
исследований, реализуемых за счет государственного бюджета, и
осуществления их реализации на стадиях формирования,
исполнения и завершения;
разработка правил организации и проведения государственной
научно-технической экспертизы;
разработка правил аккредитации субъектов научной и (или)
научно-технической деятельности, а также проведение их
аккредитации;
7. В компетенцию отраслевого уполномоченного органа входят:
В компетенцию отраслевогоуполномоченного органа входят:
1.
2.
3.
4.
участие в разработке предложений и реализации
государственной политики в области науки и научнотехнической деятельности, координация работы по
проведению научных исследований в соответствующей
отрасли;
участие в формировании приоритетных направлений
фундаментальных и прикладных научных исследований в
соответствующей отрасли;
организация разработки научных, научно-технических
проектов и программ, финансируемых из государственного
бюджета, и осуществления их реализации в соответствующей
отрасли;
утверждение отчетов по выполненным научным, научнотехническим проектам и программам в соответствующей
отрасли, финансируемым из государственного бюджета;
8. Финансовое обеспечение науки и научно-технической деятельности Закон РК о Науке статья 26
Финансовое обеспечение научной и научно-технической деятельности основывается на
различных источниках финансирования.
Для развития фундаментальных и приоритетных прикладных исследований, сохранения и
развития научного потенциала предусматривается выделение средств республиканского
бюджета.
Для целевого финансирования в виде грантов фундаментальных, инициативных и рисковых
исследований за счет средств республиканского бюджета и иных источников, не
запрещенных законодательством Республики Казахстан, Правительством Республики
Казахстан создается Фонд науки.
Положение о Фонде науки утверждается Правительством Республики Казахстан.
Научная и научно-техническая деятельность может осуществляться за счет собственных
финансовых ресурсов субъектов научной и научно-технической деятельности, привлеченных
финансовых средств спонсоров и пожертвований.
Научная и научно-техническая деятельность может осуществляться за счет грантов,
получаемых от национальных и иностранных спонсоров. В качестве спонсоров могут
выступать как физические, так и юридические лица.
Гранты, полученные по международному договору Республики Казахстан или от иностранных
спонсоров, расположенных на территории Казахстана, используются в соответствии с
условиями договора предоставления грантов без ущерба национальным интересам в области
научной и научно-технической деятельности.
Финансирование научных исследований осуществляется на основе программно-целевого
принципа.
9.
Государственный заказ на проведение приоритетных научных исследований может размещаться в
государственных и негосударственных научных учреждениях, прошедших соответственно аттестацию либо
аккредитацию, на конкурсной основе согласно программно-целевому принципу.
Программно-целевое финансирование осуществляется для:
фундаментальных научных исследований;
приоритетных прикладных научных исследований;
стратегических направлений исследований, отвечающих интересам национальной безопасности и
независимости республики;
государственных целевых научно-технических программ по приоритетным направлениям развития науки,
техники и технологии;
проведения исследований в рамках международных программ.
Государство осуществляет развитие государственной научной инфраструктуры и сохранение уникальных
научно-технических объектов и может субсидировать приобретение научного оборудования для научных
организаций в соответствии с законодательством Республики Казахстан.
Программно-целевое финансирование научных исследований и научно-технических программ
осуществляется на конкурсной основе с обязательным проведением государственной научной и научнотехнической экспертизы предлагаемых программ и результатов научных исследований.
Финансирование прикладных научных исследований может осуществляться за счет заемных средств.
10. Научные организации
• Научной организацией является юридическое лицо,основным видом деятельности которого являются
осуществление
научной,
научно-технической
и
инновационной деятельности, в том числе реализация
права на объекты интеллектуальной собственности, а
также проведение научно-исследовательских и опытноконструкторских работ.
• При
научной
организации
могут
создаваться консультативно-совещательные органы.
• Государственными научными организациями являются
научные организации, основанные на государственной
собственности.
11. Национальная академия наук Республики Казахстан
• национальные и отраслевые академии, действующие всфере
научной
и
(или)
научно-технической
деятельности, творческие союзы ученых, являющиеся
общественными объединениями, принимают участие в
формировании и реализации научной, научнотехнической и инновационной политики, разработке
приоритетных направлений развития науки, научнотехнической
экспертизе
фундаментальных
и
прикладных научных исследований, работ, выдвинутых
на соискание научных премий, в разработке проектов
нормативных, правовых актов в научно-технической
сфере, профессиональной консолидации ученых для
обеспечения
социально-экономического
развития
Республики Казахстан.
12. Научная деятельность высших учебных заведений
1.2.
3.
4.
Основным видом деятельности, осуществляемой высшим учебным заведением,
наряду с образовательной является: научная, научно-техническая и
инновационная, в том числе реализация права на объекты интеллектуальной
собственности, а также проведение научно-исследовательских и опытноконструкторских работ.
Высшие учебные заведения, а также их научные работники имеют равное право
на пользование услугами научных лабораторий коллективного пользования,
участие в конкурсах научных, научно-технических проектов и программ,
финансируемых из государственного бюджета и иных источников, не
запрещенных законодательством Республики Казахстан.
Высшие учебные заведения наряду с внедрением в учебный образовательный
процесс передовых достижений науки вправе привлекать к процессу обучения
ученых научных, научно-исследовательских организаций, в том числе
зарубежных.
Государственные высшие учебные заведения вправе создавать научные
лаборатории, научно-исследовательские институты, опытные производства,
специализированные субъекты инновационной инфраструктуры, проектноконструкторские организации, а также научно-образовательные консорциумы в
порядке, установленном законодательством Республики Казахстан.
13. Исследовательский университет
1.2.
3.
4.
Исследовательский университет является высшим учебным заведением,
реализующим утвержденную Правительством Республики Казахстан
программу развития университета и участвующим в организации и
проведении фундаментальных и прикладных научных исследований и
иных научно-технических, опытно-конструкторских работ.
Основной задачей исследовательского университета является
интеграция научной деятельности и образовательного процесса на всех
уровнях высшего и послевузовского образования.
Исследовательский университет самостоятельно разрабатывает и
реализует стандарты образовательных программ высшего и
послевузовского образования. Требования к условиям реализации и
результатам освоения образовательных программ не могут быть ниже
соответствующих программ высшего и послевузовского образования,
устанавливаемых государственными стандартами.
Исследовательский университет вправе устанавливать дополнительные
требования профильной направленности при приеме на обучение по
программам высшего и послевузовского образования.
14.
• Управление научной и (или) научнотехнической деятельностью• Закон Республики Казахстан от 18 февраля
2011 года № 407-IV «О науке» (с
изменениями
и
дополнениями
по
состоянию на 13.11.2015 г.)
15. Управление научной, научно-технической и инновационной деятельностью и ее принципы
• Вцелях
развития
и
функционирования
национальной научной системы в Республике
Казахстан
с
соблюдением
распределения
стратегических, экспертных и административных
функций управление научной и (или) научнотехнической деятельностью осуществляется:
1. Правительством Республики Казахстан;
2. Высшей научно-технической комиссией;
3. национальными научными советами;
4. уполномоченным органом;
5. отраслевыми уполномоченными органами.
16. Управление научной и (или) научно-технической деятельностью основывается на следующих принципах:
1.2.
3.
4.
5.
6.
7.
8.
9.
приоритетности научной и (или) научно-технической деятельности в
целях повышения конкурентоспособности национальной экономики;
прозрачности, объективности и равенства субъектов научной и (или)
научно-технической деятельности при получении государственной
поддержки;
экономической эффективности и результативности государственной
поддержки субъектов научной, научно-технической и инновационной
деятельности;
развития приоритетных направлений фундаментальных и прикладных
научных исследований;
объективности и независимости экспертизы научных, научнотехнических проектов и программ;
интеграции науки, образования и производства;
подготовки высококвалифицированных кадров по приоритетным
направлениям науки и научно-технической деятельности;
развития
международного
научного
и
научно-технического
сотрудничества;
стимулирования коммерциализации технологий в приоритетных
секторах экономики через предоставление преференций.
17. Высшая научно-техническая комиссия
1.2.
3.
Высшая научно-техническая комиссия является коллегиальным органом
при Правительстве Республики Казахстан, возглавляемым ПремьерМинистром Республики Казахстан.
Состав Высшей научно-технической комиссии формируется из числа
членов
Правительства
Республики
Казахстан,
руководителей
государственных органов, ведущих ученых, экспертов различных
отраслей знаний, представителей национальных управляющих
холдингов, национальных институтов развития, национальных
холдингов,
национальных
компаний,
субъектов
частного
предпринимательства и научных общественных объединений и
утверждается постановлением Правительства Республики Казахстан.
Основными задачами Высшей научно-технической комиссии являются
формирование стратегических задач и приоритетов, направленных на
развитие научной, научно-технической и инновационной деятельности,
определение
приоритетных
фундаментальных
и
прикладных
исследований по направлениям науки, рассмотрение предложений
национальных научных советов, разработка предложений по
финансированию из государственного бюджета научной и (или) научнотехнической деятельности.
18. Национальные научные советы
1.Национальные научные советы являются коллегиальными органами по
направлениям развития научной и (или) научно-технической деятельности.
2. Основными задачами национальных научных советов являются:
• 1) формирование специализированных научных направлений в соответствии
с приоритетами, определенными Высшей научно-технической комиссией;
• 2) определение форм и объемов финансирования, выделяемых для
проведения научных исследований;
• 3) оценка научной новизны, научно-технического уровня, перспективности,
степени разработанности предлагаемых научных, научно-технических
проектов и программ, экономической обоснованности запрашиваемого
объема финансирования;
• 4) оценка потребностей Республики Казахстан в новых научных направлениях;
• 5) осуществление конкурсного отбора научных, научно-технических проектов
и программ по фундаментальным и прикладным исследованиям,
предлагаемым на финансирование из государственного бюджета;
• 6) мониторинг хода реализации проводимых научных исследований, в том
числе с выездом на место.
19.
• Национальные научные советы принимают решения огрантовом и программно-целевом финансировании
(прекращении
финансирования)
за
счет
государственного бюджета:
• проектов и программ научно-исследовательских,
опытно-конструкторских и технологических работ;
• других программ в части научно-исследовательских,
опытно-конструкторских и технологических работ;
• проектов межгосударственных научно-технических
программ,
реализуемых
с
участием
научных
учреждений, организаций и предприятий Республики
Казахстан;
• инновационных проектов.
20. Порядок грантового финансирования научной и (или) научно-технической деятельности
• Грантовое финансирование выделяется на проведение научныхисследований, в целях повышения уровня научно-исследовательских
работ, научно-технического потенциала и конкурентоспособности научных
организаций и их коллективов, а также ученых.
• Грантовое
финансирование
предоставляется
безвозмездно
и
безвозвратно из средств государственного бюджета для реализации
фундаментальных и прикладных научных исследований.
• Отраслевые уполномоченные органы предложения о направлениях и
объемах грантового финансирования в соответствии с приоритетными
направлениями развития науки Республики Казахстан, утвержденными
Высшей научно-технической комиссией, направляют в уполномоченный
орган.
• Уполномоченный
орган
направляет
предложения
отраслевых
уполномоченных органов в Национальный центр государственной научнотехнической экспертизы в течение трех рабочих дней со дня окончания
срока представления предложений отраслевыми уполномоченными
органами.
21. Порядок программно-целевого финансирования научной и (или) научно-технической деятельности
• Программно-целевое финансирование направлено длярешения стратегически важных государственных задач и
осуществляется на конкурсной основе или по решению
Правительства Республики Казахстан вне конкурсных процедур.
• Высшей научно-технической комиссией на основании
представленных уполномоченным органом решений ННС
Национальным научным советам определяет приоритетные
направления программно-целевого финансирования, а также
целевые
научные,
научно-технические
программы,
подлежащие финансированию.
• Основанием программно-целевого финансирования научных
исследований являются стратегические планы социальноэкономического
развития,
программы
индустриальноинновационного развития страны и другие программы,
направленные на реализацию стратегически важных
государственных задач.
22. Национальный центр государственной научно-технической экспертизы
1.Национальный центр
государственной научнотехнической экспертизы
целях обеспечения единства администрирования, независимости,
В
прозрачности и публичности экспертизы научных, научно-технических и
инновационных проектов и программ Правительством Республики Казахстан
создается
Национальный
центр
государственной
научно-технической
экспертизы.
2. В компетенцию Национального центра государственной научно-технической
экспертизы входят:
• 1) организация работ по проведению государственной научно-технической
экспертизы научных, научно-технических проектов и программ, предлагаемых к
финансированию из государственного бюджета;
• 2) организация работы национальных научных советов;
• 3) направление результатов государственной научно-технической экспертизы в
Национальные научные советы;
• 4) оценка результатов выполненных научных, научно-технических и
инновационных проектов и программ (отчетов);
• 5) осуществление мониторинга результативности проводимых научных
исследований, научно-технических и инновационных проектов и программ;
• 6) обеспечение качественного подбора состава казахстанских и зарубежных
экспертов;
23.
• Концепция развития медицинской наукидо 2020 года (от 23 августа 2013 года №
485 )
24.
• Концепция развития медицинской науки до 2020 года разработана всоответствии со Стратегией развития Казахстана «Казахстан - 2050»,
Стратегией вхождения Казахстана в число 50-ти наиболее
конкурентоспособных стран мира, Стратегическим планом развития
Республики Казахстан до 2020 года, Государственной программой
развития здравоохранения Республики Казахстан «Саламатты
Қазақстан» на 2011-2015 годы, утвержденной Указом Президента
Республики Казахстан от 29 ноября 2010 года № 1113, в соответствии с
пунктом 1 статьи 179 Кодекса Республики Казахстан от 18 сентября
2009 года «О здоровье народа и системе здравоохранения»,
Концепцией инновационного развития Республики Казахстан до 2020
года, законами Республики Казахстан «О науке» и «О государственной
поддержке индустриально-инновационной деятельности» в целях
определения основных направлений дальнейшего развития науки и
инноваций в сфере здравоохранения Казахстана до 2020 года.
25.
• В настоящее время инфраструктура научно-исследовательскойдеятельности в области здравоохранения представлена 25
научно-исследовательскими организациями (18 научных
центров,
7
научно-исследовательских
институтов),
6
медицинскими ВУЗами и 2 организациями последипломного
образования. При этом в целях повышения самостоятельности
многие организации науки перешли на новые организационноправовые формы собственности: 9 из них являются
акционерными
обществами,
13
республиканскими
государственными предприятиями на праве хозяйственного
ведения, 11 - республиканскими государственными казенными
предприятиями. 15 организаций медицинской науки к
настоящему времени прошли сертификацию на соответствие
системы менеджмента качества.
26.
• За последние годы активно развивалисьмеханизмы обеспечения качества научных
исследований - деятельность комиссий по
вопросам этики, система научно-медицинской
экспертизы, внедрение в организациях
медицинской
науки
международных
стандартов научных исследований в условиях
доклинических (Good Laboratory Practice - GLP)
и клинических (Good Clinical Practice - GCP)
испытаний.
27.
• Из 40 отечественных научных журналов вобласти здравоохранения более 90%
выпускается медицинскими научными
организациями и ВУЗами, более 65%
являются узкоспециализированными. К
сожалению, ни один из казахстанских
журналов в области здравоохранения не
входит в международные базы данных
научных изданий.
28. +
• Сильными сторонами развития медицинской, фармацевтическойнауки и инновационной деятельности в здравоохранении являются
следующие факторы:
• наличие сети профильных организаций медицинской науки,
создание 4 современных научных центров в структуре
Национального
медицинского
холдинга
и
лабораторий
коллективного пользования на базе 2 медицинских университетов;
• повышение самостоятельности организаций медицинской науки;
• интенсивное развитие информационных технологий во всех
сферах, включая медицину и науку, доступ к полнотекстовым
научным журналам и базам данных;
• внедрение международных подходов в подготовке научных кадров
в системе здравоохранения - в магистратуре и PhD докторантуре;
• создание научных кластеров и инновационных консорциумов в
организациях медицинской науки;
• создание научных лабораторий коллективного пользования при
медицинских ВУЗах.
29. -
недостаточная материально-техническая база организаций медицинской
науки, кафедр и научных подразделений медицинских ВУЗов;
низкая конкурентоспособность и малая востребованность результатов
научных разработок отечественных ученых, низкий уровень публикуемости
отечественных
ученых в
зарубежных
рецензируемых журналах,
невостребованность казахстанских журналов за рубежом;
неэффективный менеджмент научных исследований;
низкое качество составления научных проектов и заявок;
недостаточный потенциал исследователей и отсутствие эффективных рычагов
повышения их мотивации к саморазвитию;
недостаточная интеграция медицинского образования, науки и практики;
низкий уровень привлечения высококвалифицированных специалистов
практического здравоохранения в научные исследования и разработки;
отсутствие механизмов привлечения молодых специалистов в научноисследовательский процесс;
недостаточно развитая и практически отсутствующая в системе
здравоохранения
инфраструктура
поддержки,
продвижения
и
коммерциализации результатов научных исследований и разработок.
30. Возможности:
• наличие Стратегии развития страны, отрасли, Государственнойпрограммы развития здравоохранения, обеспеченных финансовыми
ресурсами;
• реализация совместно с Всемирным банком инвестиционного
проекта «Передача технологий и проведение институциональной
реформы в секторе здравоохранения Республики Казахстан»;
• внедрение Единой информационной системы здравоохранения;
• создание Национального центра государственной научно-технической
экспертизы;
• введение новых форм финансирования национальной науки:
базовое, грантовое и программно-целевое;
• доступ к международным базам данных полнотекстовых научных
электронных изданий (Web of Knowledge, Springer, Elsevier).
31. Цель, задачи и принципы развития медицинской и фармацевтической науки и инноваций в здравоохранении
• Цель: Достижение конкурентоспособности и востребованностиразработок в сфере отечественной медицинской и фармацевтической
науки и внедрение на их основе передовых медицинских технологий
и инноваций, обеспечивающих сохранение и улучшение здоровья
населения Республики Казахстан.
• Задачи:
• 1) совершенствование менеджмента на всех уровнях научноинновационного процесса;
• 2) развитие научной и инновационной инфраструктуры системы
здравоохранения;
• 3) повышение качества подготовки научных кадров, развитие
научного и инновационного потенциала работников организаций
здравоохранения;
• 4) формирование эффективной системы продвижения научных
разработок и инноваций в практическое здравоохранение и мировое
исследовательское пространство.
32. Клинические исследования проводятся в следующих случаях:
1. по решению уполномоченного органа принеобходимости получения дополнительных
сведений о безопасности и эффективности
испытуемых образцов;
2. разработки новых оригинальных лекарственных
средств отечественными производителями;
3. исследования новых показаний к применению,
изменения лекарственной формы, дозирования
и способа применения;
4. исследования в рамках международных
многоцентровых клинических исследований (3 и
4 фазы исследований).
33. Заказчик во время проведения клинических исследований
1. обеспечивает своевременную поставку исследуемогообразца исследователю;
2. документально оформляет процедуры доставки,
приемки, выдачи, возврата и уничтожения
исследуемого образца;
3. отрабатывает процедуру изъятия исследуемого
образца и оформления соответствующих актов (при
отзыве бракованных партий, возвращении образца
после окончания исследований или по истечении
срока годности);
4. принимает меры, обеспечивающие стабильность
исследуемого образца на протяжении всего
исследования.
34. Испытуемый может быть включен в исследование только при получении информации:
• 1) об образце для клинического исследования исути клинического исследования;
• 2) о безопасности и эффективности образца для
клинического исследования, а также степени
риска для его здоровья;
• 3) о действиях в случае непредвиденных
эффектов влияния образца для клинического
исследования на состояние его здоровья;
• 4) об условиях страхования его здоровья.
35. В информационном согласии и других предоставляемых материалах, при разъяснительной беседе с испытуемым, должны быть освещены следующие в
В информационном согласии и других предоставляемых материалах, приразъяснительной беседе с испытуемым, должны быть освещены
следующие вопросы:
1) исследовательский характер испытания;
2) задачи испытания;
3) лечение исследуемым препаратом и вероятность случайного попадания в одну
из групп испытания;
4) процедуры испытания, включая инвазивные методы;
5) обязанности испытуемого;
6) процедуры испытания, носящие экспериментальный характер;
7) неудобства для испытуемого, а также объективно предсказуемый риск;
8) объективно ожидаемая польза. В случае, если испытание не имеет
терапевтических целей, необходимо сообщить об этом испытуемому;
9) другие виды медикаментозного или немедикаментозного лечения, которые
могут быть назначены испытуемому, а также их потенциальные польза и риск;
10) компенсация и/или лечение, на которые испытуемый может рассчитывать в
случае нанесения вреда его здоровью в ходе испытания;
11) размер выплат испытуемому, если таковые предусмотрены;
12) расходы испытуемого, если таковые ожидаются, связанные с его участием в
испытании;
13) участие в испытании является добровольным, и испытуемый может отказаться
в письменной форме от участия в испытании или выбыть из него в любой момент
без каких либо санкций или ущемления своих прав на другие виды лечения;
36. В информационном согласии и других предоставляемых материалах, при разъяснительной беседе с испытуемым, должны быть освещены следующие в
В информационном согласии и других предоставляемых материалах, приразъяснительной беседе с испытуемым, должны быть освещены
следующие вопросы:
14) мониторы, аудиторы, государственный орган, экспертная организация,
Комиссия по вопросам этики получат непосредственный доступ к записям в
первичной медицинской документации испытуемого не нарушая при этом
анонимности испытуемого. Подписывая письменное информированное согласие,
испытуемый или его законный представитель дают разрешение на доступ к этой
документации;
15) сведения, идентифицирующие личность испытуемого, будут сохраняться в
тайне и могут быть раскрыты только в пределах, установленных
законодательством Республики Казахстан. При публикации результатов испытания
анонимность испытуемого будет сохранена;
16) испытуемый будет своевременно ознакомлен с новыми сведениями, которые
могут повлиять на желание испытуемого продолжить участие в испытании;
17) список лиц, к которым можно обратиться для получения дополнительной
информации об испытании и правах испытуемого, а также специалистов, с
которыми испытуемый может связаться в случае нанесения вреда его здоровью в
ходе испытания;
18) возможные обстоятельства и/или причины, по которым участие испытуемого в
испытании может быть прекращено;
19) предполагаемая длительность участия испытуемого в испытании;
20) приблизительное число испытуемых, участвующих в испытании.
37. Порядок определения медицинских организаций для проведения клинических исследований
Медицинская организация должна отвечать необходимым требованиям, по проведению
клинических исследований и (или) испытаний фармакологических и лекарственных средств,
изделий медицинского назначения и медицинской техники.
Перечень медицинских организаций для проведения клинических исследований
утверждается уполномоченным органом в виде приказа в соответствии с Положением о
клинической базе по проведению клинических исследований и (или) испытаний после
предварительной экспертизы.
Экспертизу медицинской организации на соответствие установленным требованиям по
проведению клинических исследований проводит экспертная организация.
При медицинской организации создается комиссия по вопросам этики, которая проводит
оценку этических и нравственно-правовых аспектов проведения клинического испытания.
Деятельность комиссии регламентируется законодательством Республики Казахстан,
международными правилами и межгосударственными соглашениями (Хельсинская
декларация Всемирной ассоциации врачей) в области здравоохранения.
Перечень клинических баз может пересматриваться по мере необходимости по решению
уполномоченного органа.
38. Этическая регуляция проведения биомедицинских исследований
- Уважение к человеку:Относиться к человеку как к автономной
личности, обладающей правом принимать
собственные решения.
Обеспечить дополнительную защиту для
людей с ограниченной способностью принимать
решения.
Получить информированное согласие от
людей, которые способны делать выбор
действий в их отношении.
39. Процесс получения добровольного информированного согласия у потенциального участника исследования включает следующие элементы:
раскрытие информации;понимание раскрытой информации;
добровольность участия (отсутствие
принуждения и чрезмерного стимула);
для людей с ограниченной способностью
принимать решения – создание на местах
дополнительных гарантий об их
дополнительной защите.
40. Принцип благодеяния требует:
ненанесения вреда;минимизации вреда;
максимизации пользы;
проведения анализа риска и пользы для
человека-субъекта исследования и
стремления к благоприятному их
соотношению.
41. Принцип справедливости понимается как “справедливость в распределении” и требует, чтобы:
исследование разрабатывали так, чтобыего тяготы и польза были распределены
справедливо для разных слоев населения;
соблюдалась справедливость в подборе
участников исследования (нельзя набирать
участников, исходя из их легкой доступности);
42. Исследовательский этический комитет (ИЭК) или этическая комиссия – это мультидисциплинарный, независимый орган, занимающийся экспе
Исследовательский этический комитет (ИЭК) или этическаякомиссия – это мультидисциплинарный, независимый орган,
занимающийся экспертизой научных исследований c целью
обеспечения:
• – условий для защиты человека-субъекта
исследования;
• – гарантий, что исследование служит
интересам человека, групп и/или общества в
целом;
• – проверки исследования на предмет их
этической разумности (управления рисками,
соблюдения конфиденциальности, получения
добровольного информированного согласия).
43. Мультидисциплинарность ИЭК обеспечивается представительством разных профессий.
- научные медицинские работники и врачи,- представители смежных с медициной
профессий и немедицинских
специальностей (юристы, социальные
работники и др.).
- представители немедицинских
специальностей, защищающих интересы
широких общественных масс.
44. По виду рассматриваемых исследований ИЭК подразделяются на:
• ИЭК, рассматривающие биомедицинские исследования (доклинические
исследования, клинические испытания и медико-биологические
эксперименты);
• ИЭК, рассматривающие немедицинские исследования (исследования в
биологии, психологии, этнографии, социологии, антропологии);
• универсальные ИЭК, рассматривающие как биомедицинские, так и
немедицинские исследования.
• По уровню экспертизы ИЭК бывают:
• национальными;
• региональными;
• институциональными или локальными, которые подразделяются на ИЭК при
НИИ и университетские ИЭК (общие и факультетские).
Впервые ИЭК были созданы на основании “Рекомендаций для врачей,
занимающихся биомедицинскими научными исследованиями с привлечением
людей”, принятых на 18-й Генеральной Ассамблее Всемирной Медцинской
Ассоциации (Хельсинки, 1964)
45.
В сфере здравоохранения Казахстана «система этической экспертизы научных исследований»
двухступенчатая: Центральная комиссия по вопросам этики при МЗ РК и локальные комиссии
по вопросам этики при научно- исследовательских институтах, центрах и учебных заведениях
высшего медицинского образования. Процедуру обязательной этической экспертизы
проходят клинические испытания по приказу министра здравоохранения РК No 53 «Об
утверждении Инструкции по проведению клинических исследований и (или) испытаний
фармакологических и лекарственных средств в Республике Казахстан» от 14 февраля 2005 г.
Согласно приказу право на проведение клинических испытаний имеют только
аккредитованные учреждения ведомства. Обязательным условием аккредитации
учреждения было создание комиссий по вопросам этики клинических исследований.
Cоздание локальных комиссий по вопросам этики на базе научных организаций
здравоохранения и клинических баз высших
медицинских учебных заведений
предписано Приказом министра
здравоохранения РК No442 "Об утверждении правил проведения доклинических
исследований, медико-биологических экспериментов и клинических испытаний в Республике
Казахстан» от 25.07.2007 г. Приказ министра МЗ РК No 425 от 30.07.2008 г. учредил создание
Центральной комиссии по вопросам этики при МЗ РК, с целью проведения этической
экспертизы международных и республиканских исследований 4 .
46.
Без одобрения комиссий по этике документы клинического испытания не
могут быть утверждены уполномоченным органом (МЗ РК), а само
исследование не может быть начато.
Нормативно-правовое регулирование и этическая экспертиза исследований в
биологии и медицине в Казахстане осуществляется на основе следующих
базовых документов: «Кодекс о здоровье народа и системе
здравоохранения” (2009) 5 ; Государственный стандарт Республики
Казахстан. Надлежащая клиническая практика. Основные положения СТ РК
1616-2006. 6 ; Государственный стандарт Республики Казахстан.
Надлежащая лабораторная практика. Основные положения СТ РК 1613-2006
7 ; Правила проведения доклинических исследований, медикобиологических экспериментов и клинических испытаний в РК (No422 от
25.05.2007г) 8 ; Правила проведения клинических исследований и (или)
испытаний фармакологических и лекарственных средств, изделий
медицинского назначения и медицинской техники. Приказ министра
здравоохранения Республики Казахстан от 19 ноября 2009 года No 744;
47.
НАУЧНОЕ ИССЛЕДОВАНИЕ ВКЛЮЧАЕТ В СЕБЯНЕСКОЛЬКО БЛОКОВ ИНТЕГРИРОВАННЫХ
ЭТАПОВ.
48.
НАУЧНОЕ ИССЛЕДОВАНИЕ ВКЛЮЧАЕТ В СЕБЯНЕСКОЛЬКО БЛОКОВ ИНТЕГРИРОВАННЫХ
ЭТАПОВ.
• Первый — предплановые исследования,
составление и утверждение плана НИР.
49.
НАУЧНОЕ ИССЛЕДОВАНИЕ ВКЛЮЧАЕТ В СЕБЯНЕСКОЛЬКО БЛОКОВ ИНТЕГРИРОВАННЫХ
ЭТАПОВ.
• Первый — предплановые исследования,
составление и утверждение плана НИР.
• Второй включает собственно процесс
исследования (сбор материалов,
характеризующих изучаемую проблему,
накопление фактических данных о ней, их
систематизация, выработка определенных
представлений о проблеме).
50.
НАУЧНОЕ ИССЛЕДОВАНИЕ ВКЛЮЧАЕТ В СЕБЯНЕСКОЛЬКО БЛОКОВ ИНТЕГРИРОВАННЫХ
ЭТАПОВ.
• Первый — предплановые исследования,
составление и утверждение плана НИР.
• Второй включает собственно процесс
исследования (сбор материалов,
характеризующих изучаемую проблему,
накопление фактических данных о ней, их
систематизация, выработка определенных
представлений о проблеме).
• Третья часть исследования — оформление
результатов научного поиска (интерпретация,
отчет, публикация
51.
Первой и, возможно, важнейшей составнойчастью научно-исследовательской работы
является предплановое исследование, которое
включает выбор темы, выдвижение рабочей
гипотезы, патентно-информационную
проработку планируемой НИР, составление
рабочего плана НИР, освоение методик.
52.
• Выбор темы исследования — крайне сложный творческийпроцесс, во многом обеспечивающий успех научной деятельности.
Тема исследования должна быть актуальной, отличаться новизной,
иметь научно-практическое значение. Поскольку выполнение
научных исследований требует больших материально-технических
и временных затрат, творческих усилий, выбор научной темы
представляется важнейшим этапом НИР.
• Выбор темы исследования целесообразно начинать с изучения
опыта предшествующих поколений ученых. С этой целью
необходимо изучить исследуемую проблему не только по
источникам литературы, но и овладеть современной методической
базой, знать, какие исследования проводятся в ведущих научных
школах мира. Таким образом, на первом этапе планирования
главное — исключить возможность дублирования и обеспечить
достаточно высокий уровень собственных знаний по определенной
проблеме. На втором этапе планирования следует найти
оригинальный подход в постановке задачи исследования, а затем и
в ее решении, используя новые методические подходы, области их
использования и т.д.
53.
В качестве приемов, позволяющих осуществлять поиск новыхрешений в научных исследованиях, можно использовать:
1. Ознакомление р текущей и ретроспективной информацией,
преимущественно обзорно-аналитического характера.
2. Ознакомление с новейшими достижениями науки и
техники в смежных областях знания и перенос в них
методов и методических приемов из своей области знания
или, наоборот, заимствование их из смежных областей.
3. Разработку новых, более совершенных методов
исследования, технологий, приборов или композиционных
материалов, открывающих широкие перспективы их
использования в научных исследованиях.
4. Методы системного анализа, наукометрические методы и т.
д.
54.
Тема НИР должна отличаться:55.
Тема НИР должна отличаться:1) новизной исследуемого вопроса и
получаемых результатов;
56.
Тема НИР должна отличаться:1) новизной исследуемого вопроса и
получаемых результатов;
2) актуальностью;
57.
Тема НИР должна отличаться:1) новизной исследуемого вопроса и
получаемых результатов;
2) актуальностью;
3) научно-практической значимостью;
58.
Тема НИР должна отличаться:1) новизной исследуемого вопроса и
получаемых результатов;
2) актуальностью;
3) научно-практической значимостью;
4) доказательностью выдвигаемых
исследователем положений,
вытекающих из полученных
результатов.
59.
Научно-исследовательские работы подразделяютна инициативные и заказные,
индивидуальные и коллективные
(комплексные).
60.
• Инициативные исследования чаще всего носятпоисковый характер и, как правило,
финансируются за счет внутренних средств
научного учреждения, полученного гранта и т. д.
Заказная тематика входит в состав различных
государственных программ или выполняется по
договору с другими НИИ (ведомством) и
соответственно финансируется Минздравом,
научными фондами и другими заказчиками.
Индивидуальные НИР, как правило, являются
фрагментами кандидатских или докторских
диссертаций, разделом комплексного
исследования или хоздоговора.
61.
• Комплексные (коллективные) исследованияформируются в рамках программно-целевого
планирования для решения крупных научных
проблем и призваны ликвидировать
мелкотемье, более рационально использовать
имеющиеся ресурсы. Каждая научноисследовательская работа подлежит
обязательной государственной регистрации как
при планировании, так и при ее завершении для
исключения дублирования и параллелизма в
работе.
62.
• План НИР (может быть оформлен в видедоговора между заказчиком и исполнителем)
включает в себя обоснование, календарный
план, калькуляцию стоимости, штатное
расписание, отчет о проведенном патентноинформационном исследовании с заключением
об исключении дублирования и
целесообразности планирования НИР.
63.
• Тема НИР, как правило, планируется на научнуюгруппу или лабораторию. Это и определяет
численность исследователей и фонд заработной
платы. Соотношение численности научного и
вспомогательного состава зависит от характера
планируемой работы и может колебаться от 1:1
до 1:4.
• Тема НИР должна широко обсуждаться
коллективом лаборатории, Ученого совета,
экспертных Советов на всех этапах
планирования, выполнения и завершения темы.
64.
• Патентно-информационные исследования являютсяодним из основных разделов предплановых
исследований. Они проводятся с целью определения
научно-технического уровня и тенденций развития в
планируемой области знания, патентоспособности
предлагаемой к планированию НИР и исключения
дублирования. Патентно-информационные
исследования осуществляются на основе анализа
патенгной, научно-технической, коммерческой и других
видов информации в соответствии с Законом Республики
Казахстан "О патентах на изобретения».
• По завершении темы НИР патентно-информационное
исследование проводится в более углубленном виде:
определяются новизна, технический уровень, патентная
чистота разработанного объекта, целесообразность его
правовой защиты за рубежом и продажи лицензий.
65.
• Результаты НИР во многом определяются правильностьювыбранных методов исследования. Наиболее широко
применяемым в медицине эмпирическим методом
является натурное наблюдение в естественных,
клинических или лабораторных условиях. Объектами
этого наблюдения могут быть здоровые или больные
люди, продукты выделения и ткани живого организма,
трупный материал, микроорганизмы и продукты их
жизнедеятельности и т. д. Натурное наблюдение включает
всевозможные методики исследования —
гистологические, психофизиологические и т. д.
Отличительной особенностью методов натурного
наблюдения является то, что они осуществляются только в
отношении самого объекта научного изучения и только в
обычных, естественных условиях его существования.
Никакие модели, замещающие объект изучения,
изменения условий его обитания не допускаются.
66.
• В отличие от натурного наблюденияэкспериментальное исследование ставит
перед собой задачу изучения явления в строго
контролируемых и воспроизводимых условиях
при активном воздействии экспериментатора
на объект изучения.
• Среди экспериментальных методов
исследования следует выделить лабораторные
опыты, психофизиологические исследования
на людях, эксперименты на животных,
клинические испытания, натурные испытания
опытных образцов или объектов,
математическое моделирование.
67.
• При экспериментах на животных важную роль играетправильный выбор объекта исследования, поскольку
различные виды животных имеют различную реактивность
на определенные внешние раздражители и по-разному
моделируют патологические процессы, протекающие в
человеческом организме. Так, например, собака наиболее
часто используется при изучении различных
патофизиологических процессов, токсикологические
исследования чаще всего проводят на кошках,
микробиологические — на белых мышах, крысах, морских
свинках, кроликах. Самые ответственные исследования
проводят на обезьянах, видовая специфичность которых
наиболее близка к человеческому организму. Во всех
случаях необходимо, чтобы подопытные животные были
здоровыми, однородными (инбредные линии),
однополыми, примерно одинаковой массы и возраста.
Исключительно важное значение для достоверности
полученных данных имеют условия содержания
подопытных животных и уход за ними.
68.
• Клинические исследования — завершающий этапНИР по разработке новых лекарственных
препаратов, методов диагностики и профилактики.
Поскольку их проводят на больных и
добровольцах, а также учитывая их особую
важность, клинические испытания разрешаются в
директивном порядке специально
уполномоченными государственными органами.
При организации клинических испытаний особое
внимание должно уделяться подбору пациентов и
аналогичной по составу и количеству контрольной
группы. При клинических испытаниях новых
методов лечения в качестве контроля должны
использоваться больные, получающие
общепринятое лечение, а не только плацебо.
69.
Для оценки эффективности новых методовдиагностики, профилактики и лечения,
исключения ошибок и правильной
интерпретации результатов клинических
исследований их необходимо проводить в
рамках рандомизированных контролируемых
исследований, считающихся "золотым
стандартом" для клинических сопоставлений.
70.
• Контролируемое клиническое исследование — это проспективноеисследование, в котором сопоставляемые группы получают различные
виды лечения: больные контрольной группы — стандартное (обычно
лучшее по современным представлениям), а больные опытной группы
— новое лечение. Важнейшее условие, обеспечивающее надежность
контролируемого исследования, — однородность группы больных по
всем признакам, которые влияют на исход заболевания (пол, возраст,
наличие сопутствующих заболеваний, тяжесть и стадия основного
заболевания и т. д.). Учитывая наличие множества взаимосвязанных
факторов, определяющих прогноз, а также "скрытых" прогностических
факторов, достичь сопоставимости групп наблюдения в наиболее
полном объеме можно только при использовании метода случайного
распределения пациентов на группы, т. е. рандомизации (random —
случайный). Истинная рандомизация предполагает обязательное
соблюдение непредсказуемого характера распределения больных на
группы (исследователь не может предугадать, в какую группу попадает
следующий больной, — "слепой отбор"). Для повышения
эффективности рандомизации проводится предварительная
стратификация — распределение вариантов лечения осуществляется в
однородных группах больных, сформированных по ведущим
прогностическим признакам (стратификационная рандомизация).
71.
Однако следует учитывать, что несопоставимость групп наблюдения может возникнуть
и после рандомизации (в результате отказа больных от лечения, серьезных
осложнений и т. д.). Считается, что если более 80% включенных в исследование
больных наблюдались до его окончания, результаты могут быть достаточно
надежными. Выбывание из исследования более 20% больных дает основание
сомневаться в полученных результатах.
Для снижения вероятности случайных или систематических ошибок опытная и
контрольная группы должны включать достаточное число наблюдений. Достаточность
определяется предполагаемыми различиями в эффекте лечения между опытной и
контрольной группами (чем больше эффект, тем меньшими могут быть группы), видом
статистического показателя эффекта терапии (при использовании средних величин
исследования группы могут быть меньше), соотношением между числом больных в
опытной и контрольной группах (при условии равенства по численности группы могут
быть более малочисленными).
Определение оптимального числа случаев наблюдения составляет важный этап
планирования эксперимента. Так, в случаях, когда результаты исследования будут
выражаться качественно, требуется гораздо большее число наблюдений, чем при
использовании количественных оценок, выраженных среднеарифметическими
величинами. Кроме этого, следует помнить, что малое число исследований уменьшает
их точность и достоверность, однако при большом числе исследований вместе с
достоверностью возрастают и стоимость эксперимента, и сроки его проведения. Для
увеличения точности исследования в 2 раза необходимо увеличить число наблюдений
в 4 раза. При этом число наблюдаемых случаев в контрольной и опытных группах не
обязательно должно быть одинаковым. Число случаев, необходимых для проведения
эксперимента, определяется при планировании НИР в каждом конкретном случае
индивидуально по специальным формулам, описанным в ряде справочников по
медицинской статистике.
72.
• В связи с тем что в одном учреждении нередко невозможно осуществитьрассчитанное количество наблюдений, проводят кооперированные
исследования — систему научных, научно-организационных и практических
мероприятий, проводимых по единой программе и методике одновременно в
нескольких учреждениях.
• При планировании клинического исследования необходимо четко определить
следующие положения: рационально ли определена "норма" — отсутствие
болезни и обоснована ли "точка разделения" здоровых и больных; оценены
ли воспроизводимость, чувствительность и специфичность используемых
методов и т. д.
• При клинической оценке новых методов диагностики необходимо прежде
всего сопоставить предлагаемый метод с референсным, т. е. с самым
надежным из соответствующих методов. При правильной организации
исследования оценка результатов нового метода должна производится
"вслепую" — так, чтобы специалист не знал результатов других анализов у
этого пациента и прежде всего результатов референсного метода. В
противном случае неизбежны систематические ошибки типа "приближения к
предполагаемому диагнозу", поскольку специалист, зная предполагаемый
диагноз, непреднамеренно склонен к предвзятости при оценке результатов,
особенно в случаях, когда возможно двоякое их толкование. Чтобы избежать
таких ошибок, можно использовать двухэтапную оценку. На первом этапе
специалист рассматривает материалы (ЭКГ, лабораторные препараты и т. д.)
под номером исследования и лишь по необходимости проводит оценку с
учетом дополнительных данных.
73.
Методы исследования должны быть предварительно апробированы в ходе
предплановых исследований. При этом следует убедиться в их чувствительности,
специфичности, воспроизводимости, наличии реактивов на весь объем
исследования, соответствии метода уровню мировых стандартов. Этим же
требованиям должна отвечать и аппаратура. При отсутствии у исследователя
дорогостоящей техники не обязательно ее закупать: можно ее арендовать или
использовать в ходе кооперированных исследований.
Каждая тема НИОКР, прошедшая утверждение у заказчика и получившая
финансирование, должна быть зарегистрирована в государственном регистре (в
России — во Всероссийском НТИ Центре, в Беларуси — в Центре Государственной
регистрации РБ).
При планировании НИР следует учитывать и заключительный этап научного
исследования — анализ и интерпретацию полученных результатов с целью
выявления имеющихся закономерностей. Анализ статистических данных производят
путем соответствующей математической обработки полученных результатов,
приемы и способы которой подробно описаны в специальных руководствах по
медицинской статистике. В последние годы статистическую обработку данных стали
проводить на ПЭВМ с использованием специальных пакетов программ (например,
Statgraph и др.), позволяющих быстро рассчитать средние величины и
относительные коэффициенты, выявить характер и силу связи, степень
достоверности, построить аналитические таблицы, диаграммы и графики.
В целом на процессы предплановых исследований, анализа и обобщения
полученных результатов и их публикацию следует выделять не менее 10%
планируемых ресурсов (временных, финансовых, кадровых), а на внедрение
научных результатов в практику — не менее 25%. В то же время для многих НИР
стадия внедрения планируется как самостоятельное исследование, а оформление
научных результатов в виде публикаций, изобретений и т. д. осуществляется
учеными уже после завершения НИР в процессе выполнения последующих
исследований, нередко вытекающих из предыдущих результатов.








































































 medicine
medicine








