Similar presentations:
Введение. Основные понятия и законы химии. Тема 1
1.
КГТУХимия.
Булычёв Александр
Григорьевич
к.х.н., доц.
2.
Основная учебная литература1. . Князев, Д.А. Неорганическая химия: учебник для вузов / Д.А.Князев,
С.Н. Смарыгин. - Москва: Дрофа, 2005. - 591 с.
2. Гуров, А.А. Химия / А.А. Гуров, Ф.З. Бадаев, Л.П. Овчаренко - Москва: Изд-во
МГТУ им. Н.Э. Баумана, 2007. - 784 с.
Дополнительная учебная литература
1. Угай, Я.А. Общая и неорганическая химия: учебник / Я.А. Угай. - Москва: Высшая
школа, 2004. – 527с.
2. Коровин, Н.В. Общая химия / Н.В. Коровин. - Москва: Высшая школа, 2002.- 558с.
3. Глинка, Н.Л. Общая химия: учеб. пособие для вузов / Н.Л. Глинка; под ред.
А.И. Ермакова.- изд. 29-е.- Москва: Интеграл-Пресс, 2001. - 728 с.
4. Глинка, Н.Л. Задачи и упражнения по общей химии: учеб. пособие для вузов / Н.Л.
Глинка; под ред. В.А. Рабиновича, Х.М. Рубиной. - Москва: Интеграл-Пресс, 2001. - 240 с.
5. Рабинович, В.А. Краткий химический справочник / В.А. Рабинович,
З.Я. Хавин. - Ленинград: Химия, 1978. - 392 с.
3.
Лекция №1Часть 1
Основные понятия и законы химии
4.
Тема 1. Введение. Основные понятия и законыхимии
1. Понятие о материи и о веществе.
2. Предмет и задачи химии.
3. Закон сохранения массы и энергии. Закон постоянства
состава: дальтониды и бертоллиды.
4. Количество вещества. Моль.
5.
6.
7.
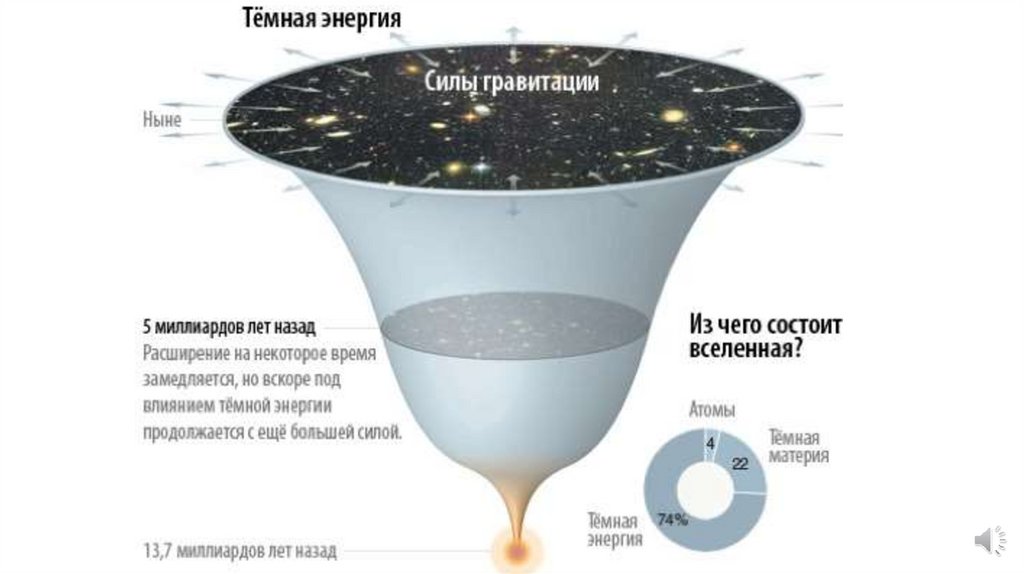
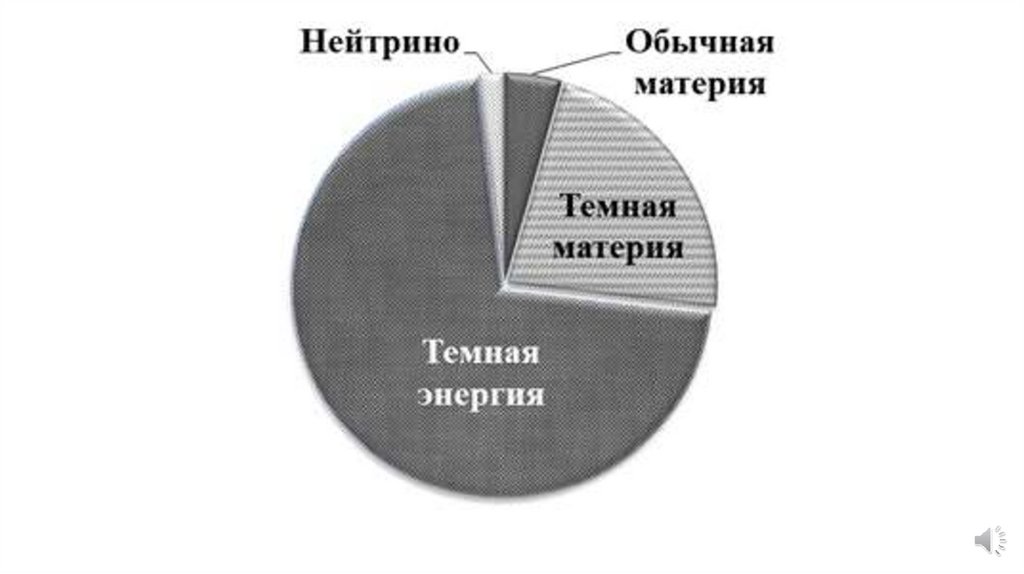
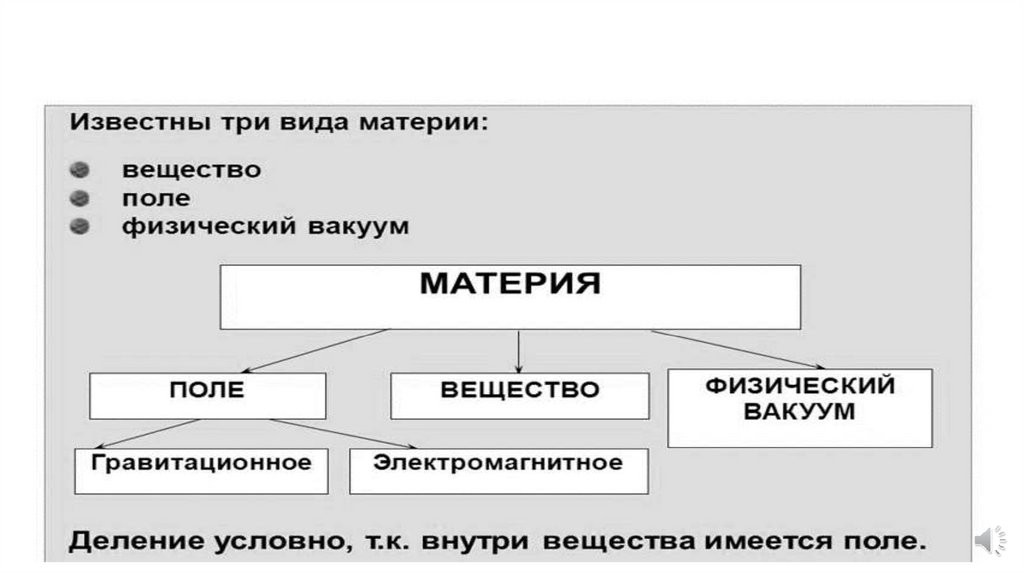
Материя8.
Материя9.
ПРЕДМЕТ ХИМИИ• Химия – естественная наука, изучающая вещества, их
строение, свойства и превращения.
• Вещество – это любой вид материи, обладающий
собственной массой (массой покоя).
10.
ПРЕДМЕТ ХИМИИМерой движения и взаимодействия различных видов материи
служит энергия
Мерой инерции материи является масса
Энергия и масса – важнейшие взаимосвязанные свойства материи
Е = m•с2,
где с - скорость света в вакууме (с = 3•108 м/с)
11.
ПРЕДМЕТ ХИМИИПревращения веществ,
сопровождающиеся изменением
состава, называются
химическими реакциями.
12.
ОСНОВНЫЕ ЗАКОНЫ ХИМИИЗакон сохранения материи и энергии
Если в одном месте что-то убудет, то в другом
обязательно прибудет. Энергия и масса не
исчезают, они просто трансформируются из
одного состояния в другое
Закон сохранения массы – частный случай
закона сохранения материи и энергии
Масса веществ, вступающих в химическую
реакцию, равна массе веществ,
образующихся в результате реакции
17.07.2023
12
13.
Атом• Демокрит: атом – наименьшая и неделимая частица
материи (греч. – неделимый).
• Атом – это наименьшая частица химического элемента,
способная к самостоятельному существованию и
являющаяся носителем его свойств.
• Атом – электронейтральная микросистема, состоящая из
положительно заряженного ядра и соответствующего числа
электронов
14.
Химический элементХимический элемент – вид атомов с
одинаковым зарядом ядра.
15.
Молекула• Молекула – это наименьшая частица вещества,
определяющая его свойства и способная к
самостоятельному существованию.
• Молекула состоит из атомов одного или различных
химических элементов и существует как единая
динамическая система атомных ядер и электронов.
16.
Закон постоянства состав(Пруст 1801-1808):• Каждое химическое соединение имеет вполне
определенный и постоянный состав.
дальтониды – да.
О2, СН3СООН
бертоллиды – нет!
V0,9-1,3О, Na2S1-5
17.
18.
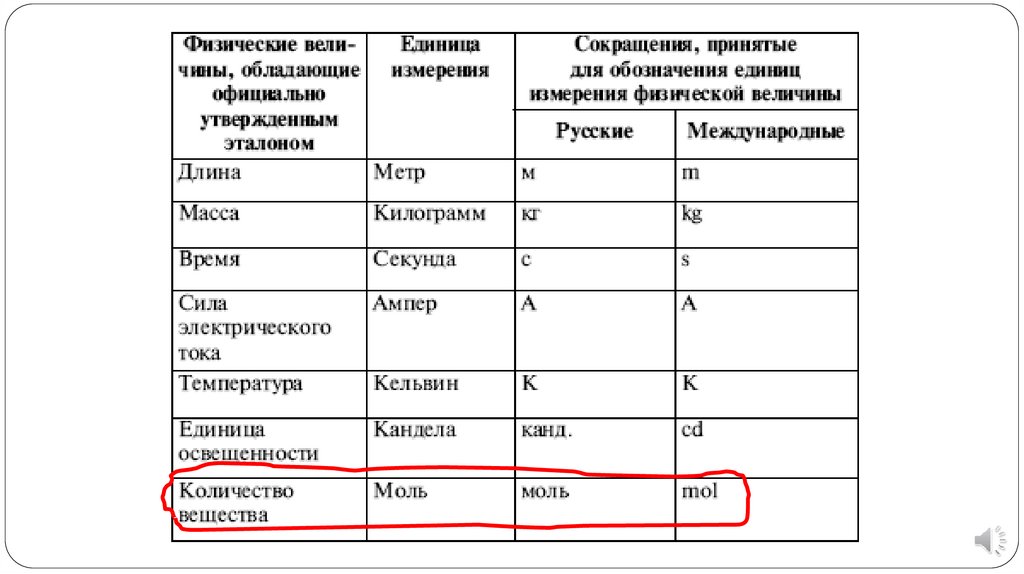
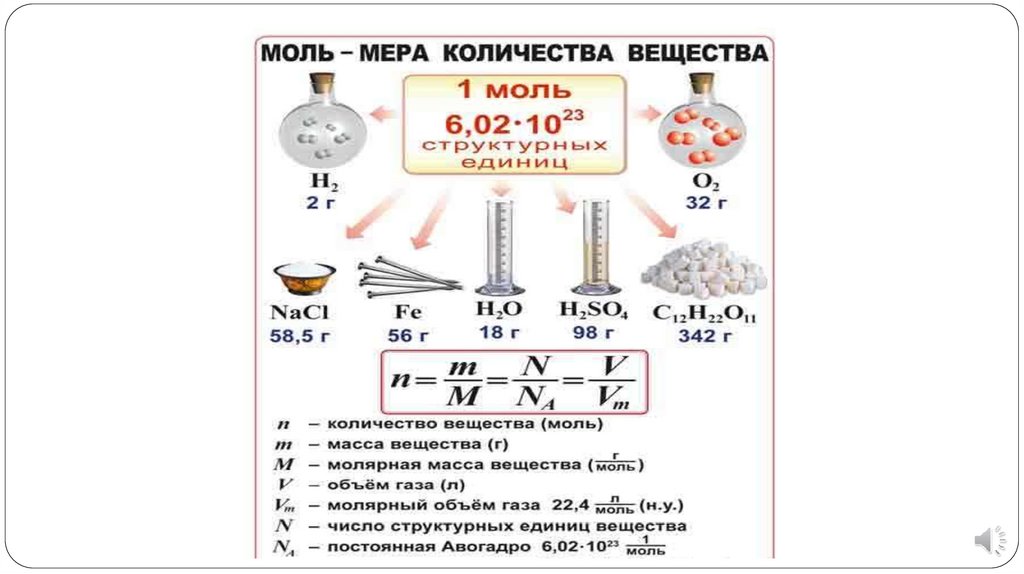
Количество веществаКоличество вещества — физическая
величина,
характеризующая количество однотипных
структурных единиц, содержащихся в
веществе. Под структурными единицами
понимаются любые частицы, из которых
состоит вещество (атомы, молекулы,
ионы, электроны или любые другие
частицы).
19.
Моль - количество веществасистемы, которое содержит столько
структурных единиц(атомов,
молекул, ионов, электронов и т.п.),
сколько атомов содержится в 0,012
кг углерода-12, т.е.
6,02 х
23
10
атомов, молекул, ионов, электронов и т.п
19
20.
21.
Массу одного моля вещества называютмолярной массой (М)
Отношение массы вещества (m) к его
количеству (n) представляет собой молярную
массу вещества:
m
M г / моль
n
22.
23.
в-вав-ва
в-ва
















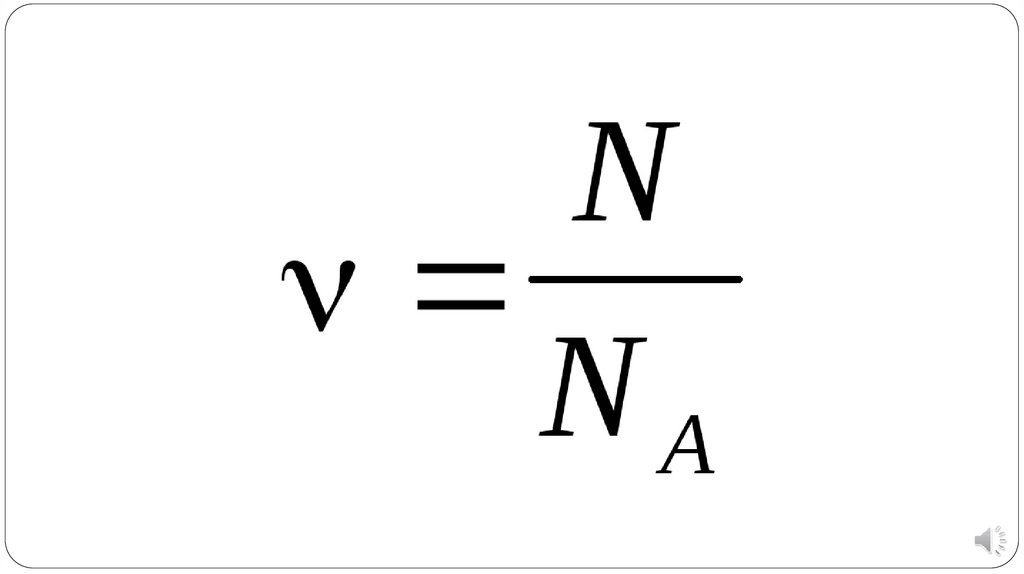
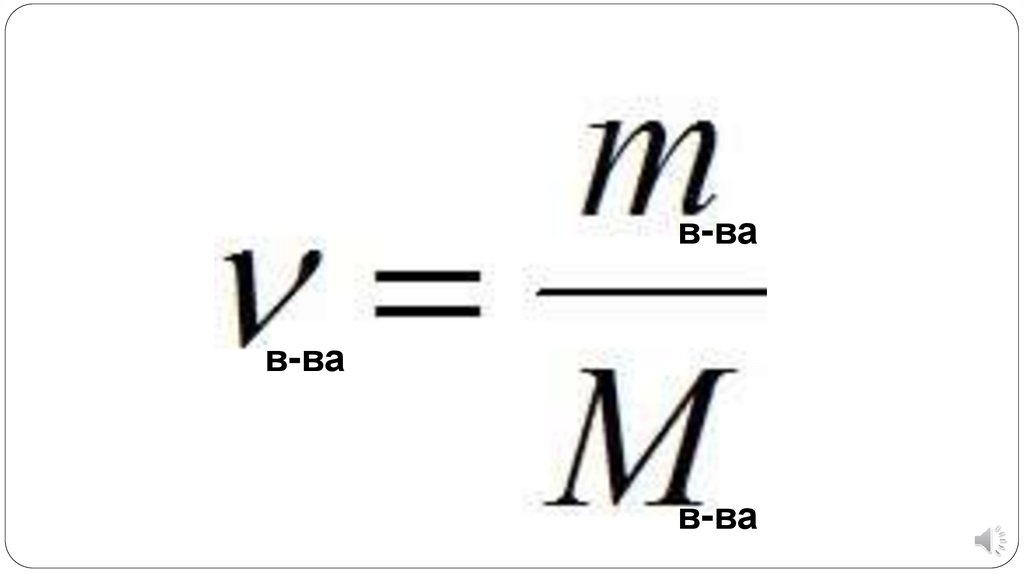
 chemistry
chemistry








