Similar presentations:
Определение лекарственных веществ и их метаболитов в биологических жидкостях
1.
Определение лекарственныхвеществ и их метаболитов в
биологических жидкостях
Лекция по учебной дисциплине «Фармацевтическая химия» для
студентов 3 курса ф/ф ДФПО и МФИУ по специальности «Фармация» с
русским языком обучения
2.
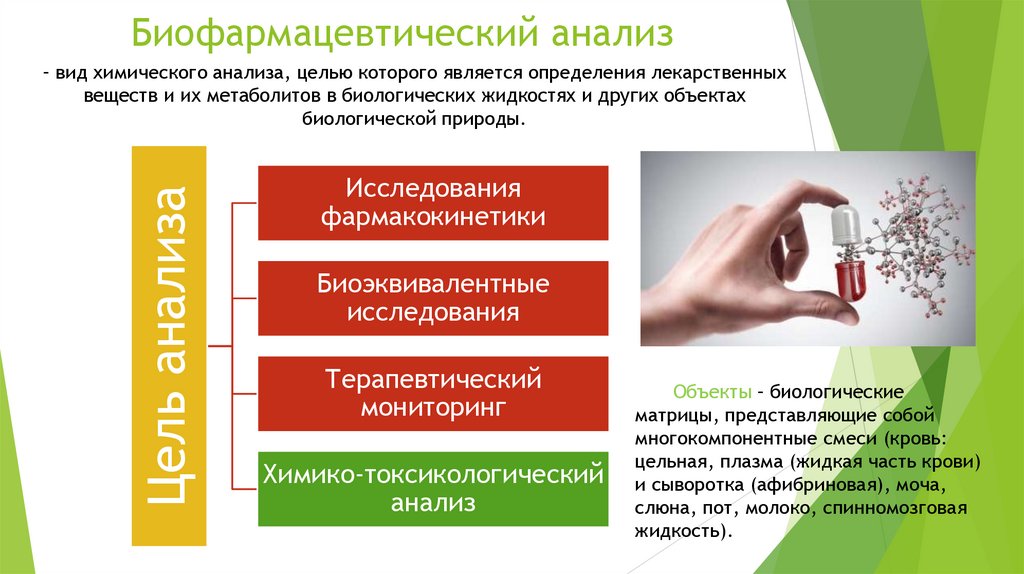
Биофармацевтический анализЦель анализа
– вид химического анализа, целью которого является определения лекарственных
веществ и их метаболитов в биологических жидкостях и других объектах
биологической природы.
Исследования
фармакокинетики
Биоэквивалентные
исследования
Терапевтический
мониторинг
Химико-токсикологический
анализ
Объекты – биологические
матрицы, представляющие собой
многокомпонентные смеси (кровь:
цельная, плазма (жидкая часть крови)
и сыворотка (афибриновая), моча,
слюна, пот, молоко, спинномозговая
жидкость).
3.
Особенности биофармацевтическогоанализа:
Объекты – биологические жидкости – многокомпонентные
смеси веществ.
Условия пробоподготовки зависят от вида биологической
жидкости, свойств лекарственного вещества и метода
анализа.
Концентрации определяемых веществ могут быть очень
малыми (нмоль, нг).
Определяемые вещества могут находиться в образце как в
свободном, так и в связанном виде; как в исходном виде,
так и в виде метаболитов (фармакологически активных и
неактивных).
4.
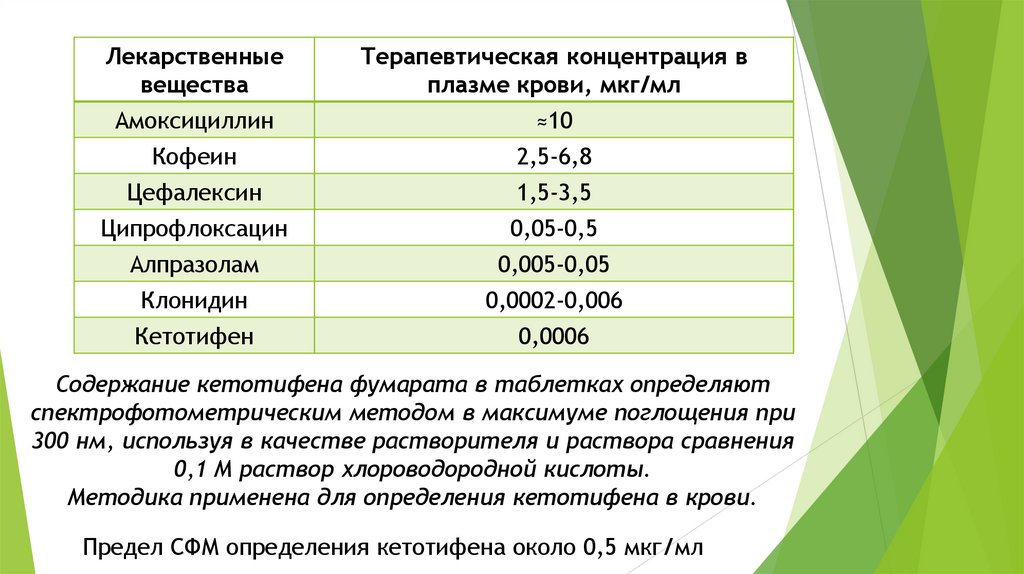
Лекарственныевещества
Терапевтическая концентрация в
плазме крови, мкг/мл
Амоксициллин
≈10
Кофеин
2,5-6,8
Цефалексин
1,5-3,5
Ципрофлоксацин
0,05-0,5
Алпразолам
0,005-0,05
Клонидин
0,0002-0,006
Кетотифен
0,0006
Содержание кетотифена фумарата в таблетках определяют
спектрофотометрическим методом в максимуме поглощения при
300 нм, используя в качестве растворителя и раствора сравнения
0,1 М раствор хлороводородной кислоты.
Методика применена для определения кетотифена в крови.
Предел СФМ определения кетотифена около 0,5 мкг/мл
5.
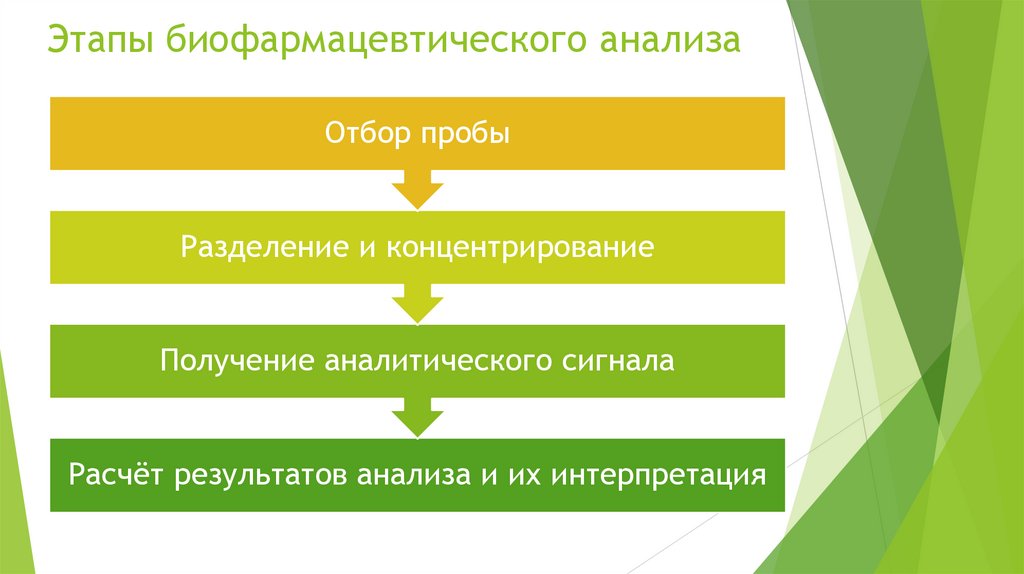
Этапы биофармацевтического анализаОтбор пробы
Разделение и концентрирование
Получение аналитического сигнала
Расчёт результатов анализа и их интерпретация
6.
Методы разделения и концентрированияРазделение – любой процесс или операция, в результате
которых компоненты, составляющие исходную смесь,
отделяются один от другого.
Процесс, при котором нужные компоненты выделяют в
самостоятельную фазу или часть фазы, называется
выделением.
Концентрирование – процесс или операция повышения
содержания определяемого вещества по отношению к матрице
или матричным компонентам.
7.
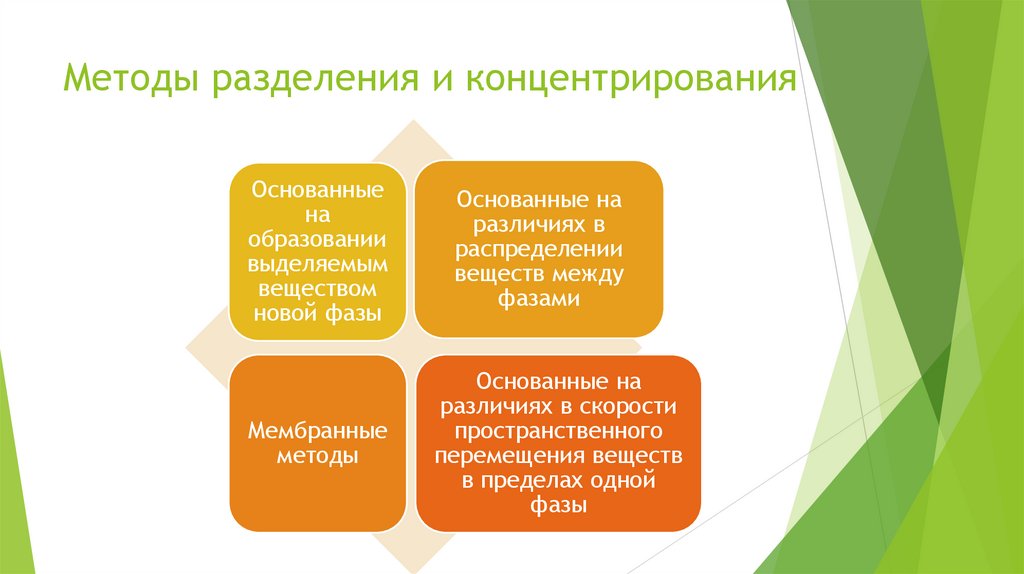
Методы разделения и концентрированияОснованные
на
образовании
выделяемым
веществом
новой фазы
Мембранные
методы
Основанные на
различиях в
распределении
веществ между
фазами
Основанные на
различиях в скорости
пространственного
перемещения веществ
в пределах одной
фазы
8.
Наиболее часто используемые методы:Осаждение (как метод очистки).
Жидкость-жидкостная экстракция.
Твёрдофазная экстракция (сорбция).
Мембранные методы (диализ, осмос).
Методы, основанные на различной скорости
пространственного перемещения веществ в
пределах одной фазы (центрифугирование,
электрофорез).
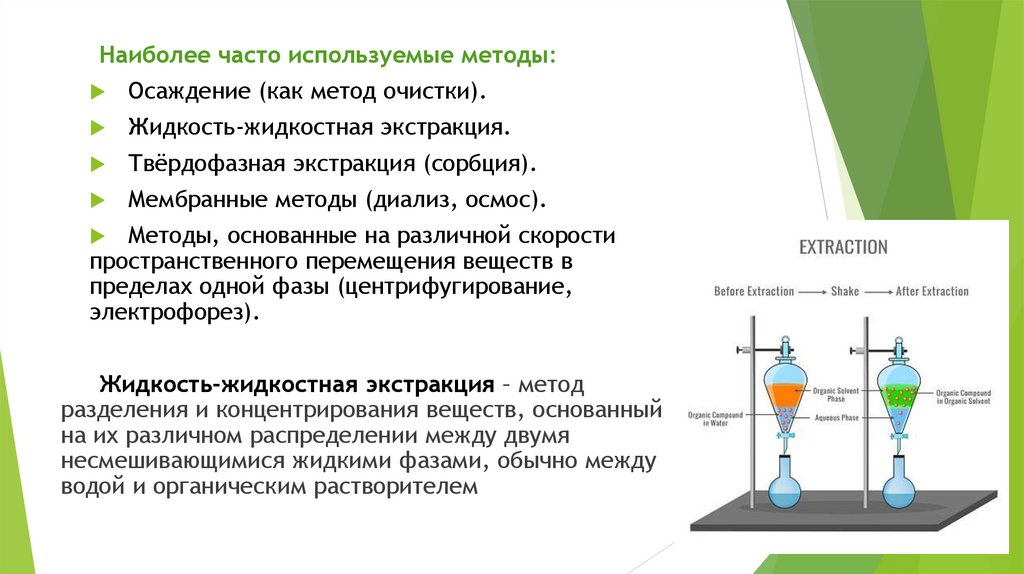
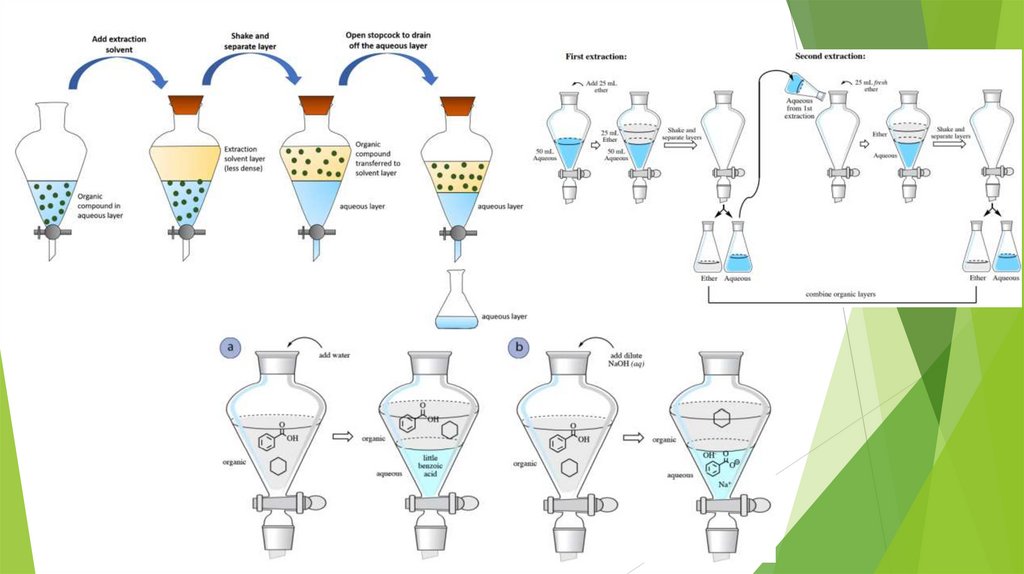
Жидкость-жидкостная экстракция – метод
разделения и концентрирования веществ, основанный
на их различном распределении между двумя
несмешивающимися жидкими фазами, обычно между
водой и органическим растворителем
9.
10.
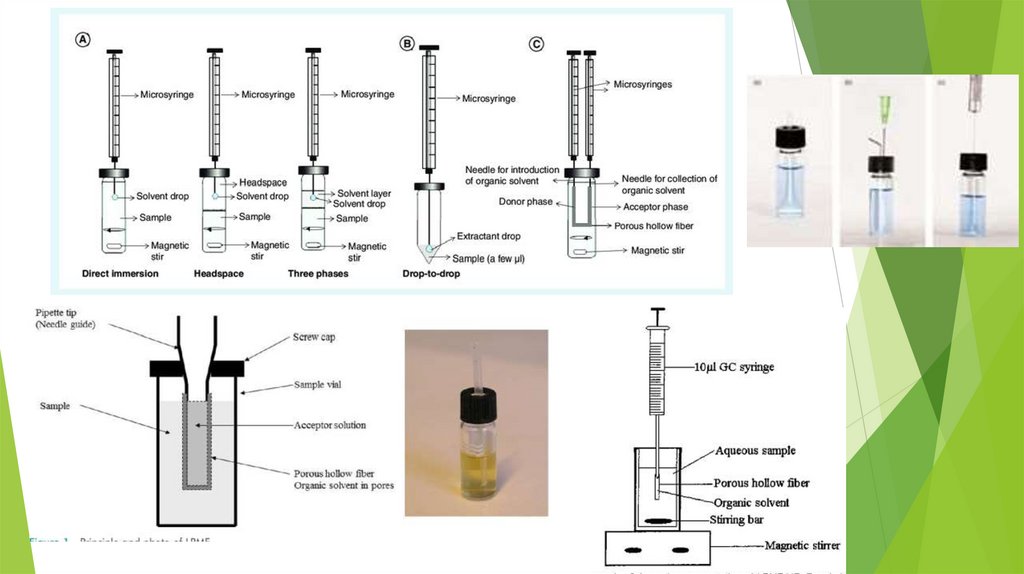
Жидкостная микроэкстракция (liquid-phasemicroextraction, LPME)
1 – кончик пипетки;
2 – стеклянный флакон с
завинчивающейся крышкой;
3 – органический
растворитель;
4 – пористое полое волокно;
5 – исследуемый образец;
Органический растворитель (экстрагент) находится в полости
пористого волокна, которое удерживается на крышке
стеклянного флакона. Внутрь флакона помещается исследуемый
образец (при необходимости создаётся определённое значение
pH). Время экстракции составляет 15-45 минут.
11.
12.
Сорбционное разделение иконцентрирование
– совокупность процессов, сопровождающихся
поглощением разделяемых веществ твёрдыми сорбентами
либо тонкими слоями жидкостей, находящихся на инертных
носителях.
Неорганические сорбенты (С, Al2O3 и др.).
Силикагели и химически модифицированные силикагели.
Органические полимеры.
По типу взаимодействий:
гидрофобные
(модифицированные
силикагели);
водородная связь
(гидратированные
силикагели);
ионный обмен
(сульфокислоты
полимеров)
13.
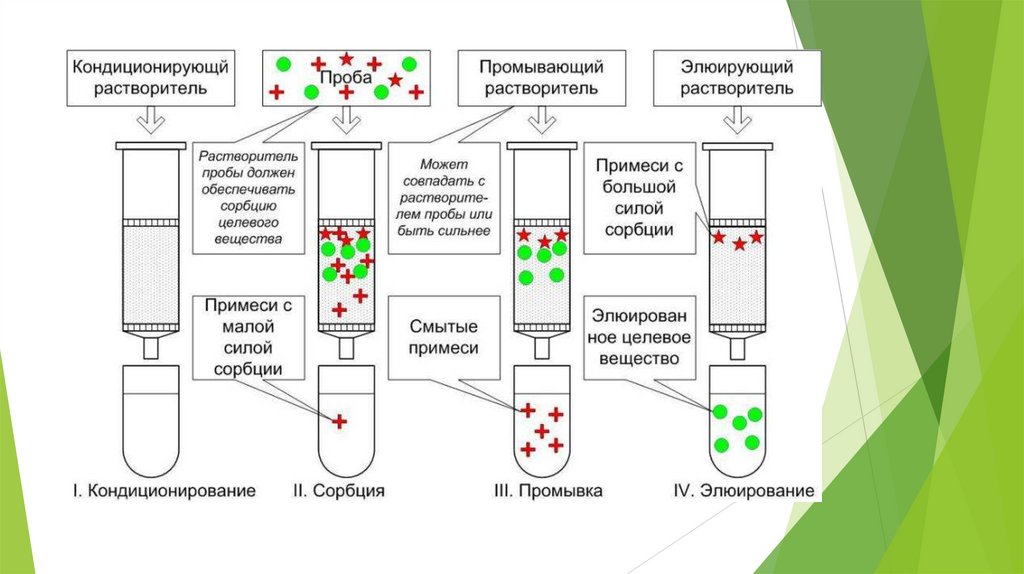
Твёрдофазная экстракция (solid-phaseextraction, SPE)
– метод разделения и концентрирования веществ,
основанный на сорбции на твёрдых сорбентах и
последующем элюировании (вымывании, экстракции) с
сорбента с помощью определённых растворителей.
Одностадийная (сорбируются только примеси).
Двухстадийная (сорбируются примеси и аналит, элюируют
аналит).
Трёхстадийная (сорбируются примеси и аналит, элюируют
вначале примеси, затем аналит).
14.
15.
16.
Методы определенияХроматографические, в том числе ЖХ-МС;
Белоксвязывающие (иммунохимические);
Капиллярный электрофорез;
Спектрометрические;
Электрохимические;
Другие.
17.
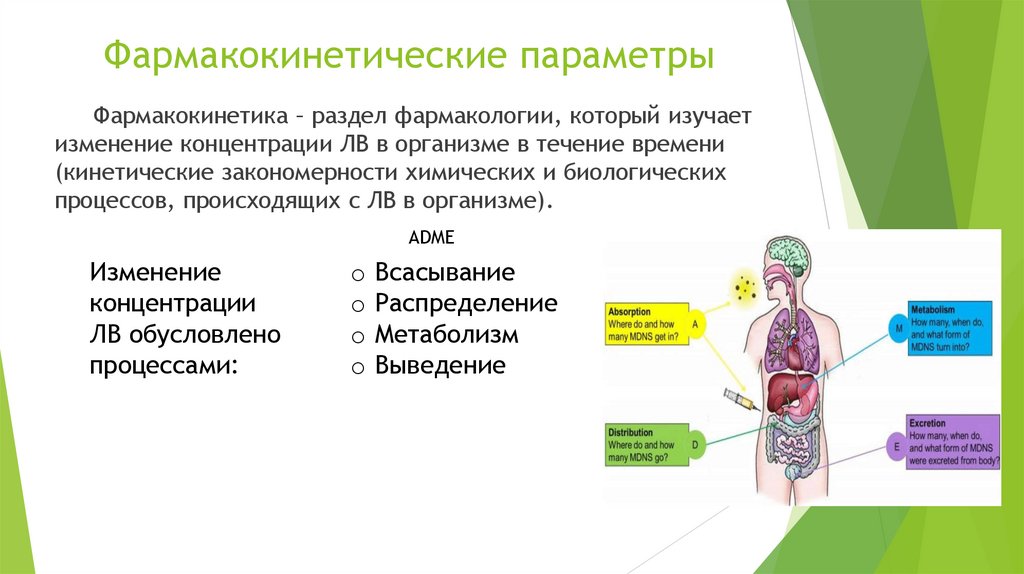
Фармакокинетические параметрыФармакокинетика – раздел фармакологии, который изучает
изменение концентрации ЛВ в организме в течение времени
(кинетические закономерности химических и биологических
процессов, происходящих с ЛВ в организме).
ADME
Изменение
концентрации
ЛВ обусловлено
процессами:
o Всасывание
o Распределение
o Метаболизм
o Выведение
18.
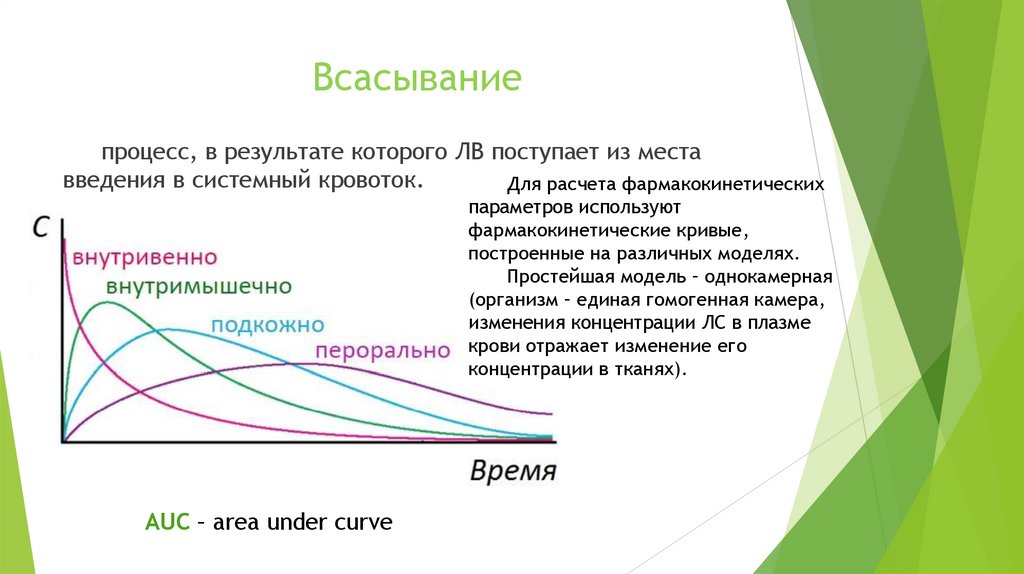
Всасываниепроцесс, в результате которого ЛВ поступает из места
введения в системный кровоток.
Для расчета фармакокинетических
параметров используют
фармакокинетические кривые,
построенные на различных моделях.
Простейшая модель – однокамерная
(организм – единая гомогенная камера,
изменения концентрации ЛС в плазме
крови отражает изменение его
концентрации в тканях).
AUC – area under curve
19.
20.
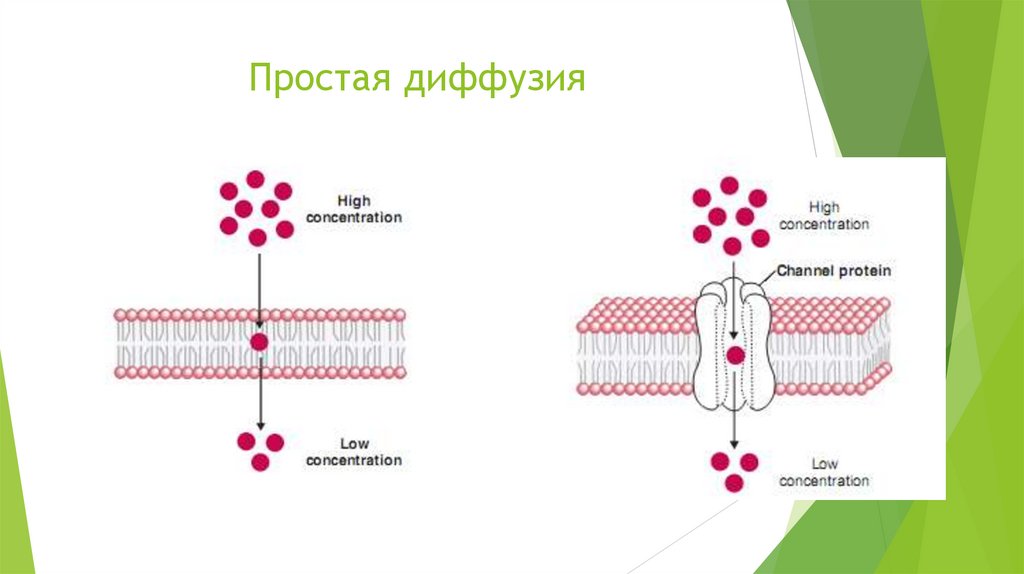
Простая диффузия21.
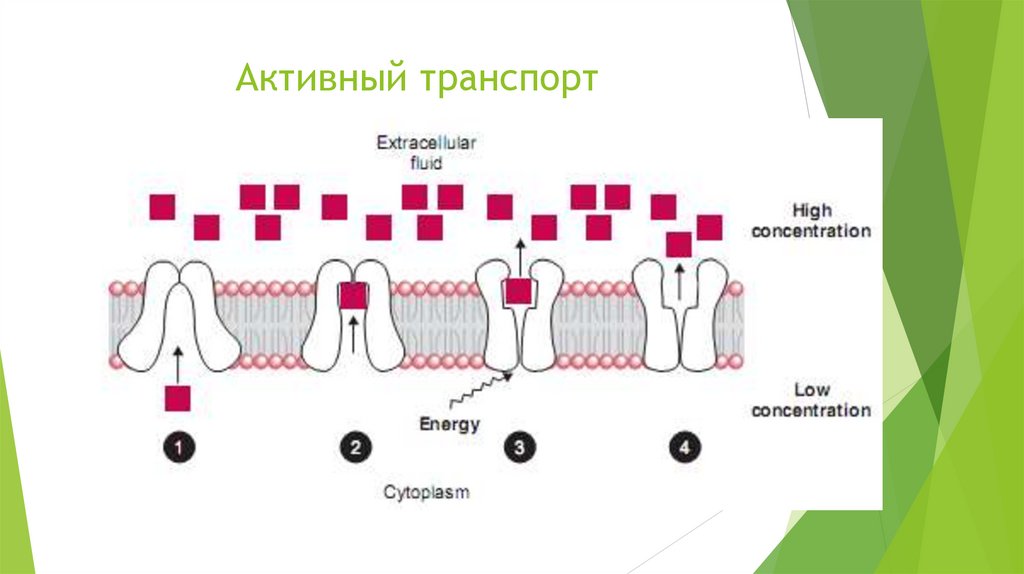
Активный транспорт22.
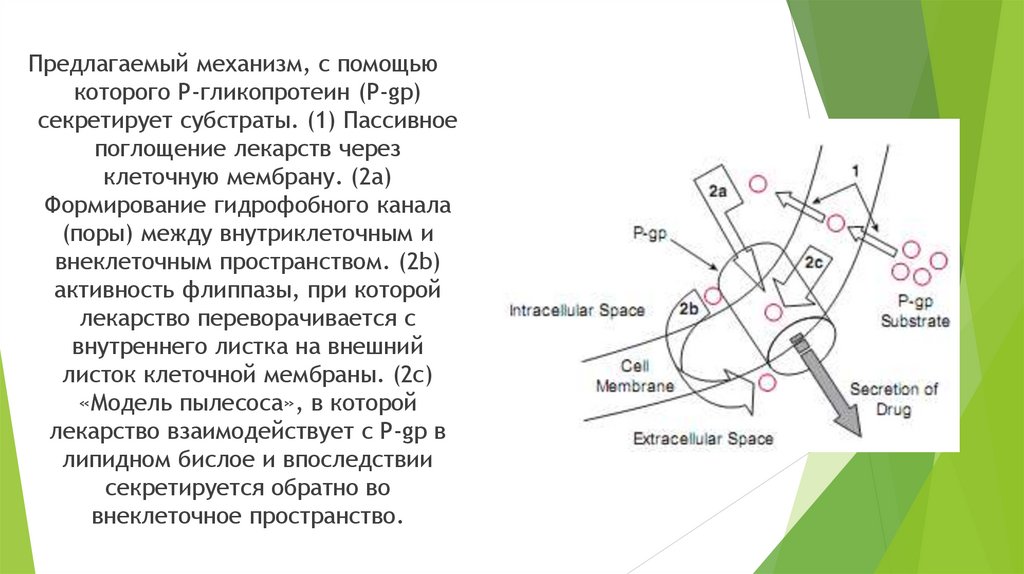
Предлагаемый механизм, с помощьюкоторого P-гликопротеин (P-gp)
секретирует субстраты. (1) Пассивное
поглощение лекарств через
клеточную мембрану. (2а)
Формирование гидрофобного канала
(поры) между внутриклеточным и
внеклеточным пространством. (2b)
активность флиппазы, при которой
лекарство переворачивается с
внутреннего листка на внешний
листок клеточной мембраны. (2c)
«Модель пылесоса», в которой
лекарство взаимодействует с P-gp в
липидном бислое и впоследствии
секретируется обратно во
внеклеточное пространство.
23.
Доля лекарственного средства,существующего в неионизированной форме в
растворе, зависит как от константы
диссоциации лекарственного средства, так и от
рН раствора в месте абсорбции.
Для слабых кислот:
Для слабых кислот:
24.
Биодоступностьпараметр, который показывает, какая часть от введённой
дозы ЛВ поступила в системный кровоток, а также скорость, с
которой это происходит.
При в/в введении
биодоступность равна
100%, при других
способах введения она
меньше.
ЛВ
БД (per os), %
Ловастатин
5
Ацикловир
20
Амитриптилин
30-60
Ципрофлоксацин
70
Линезолид
100
25.
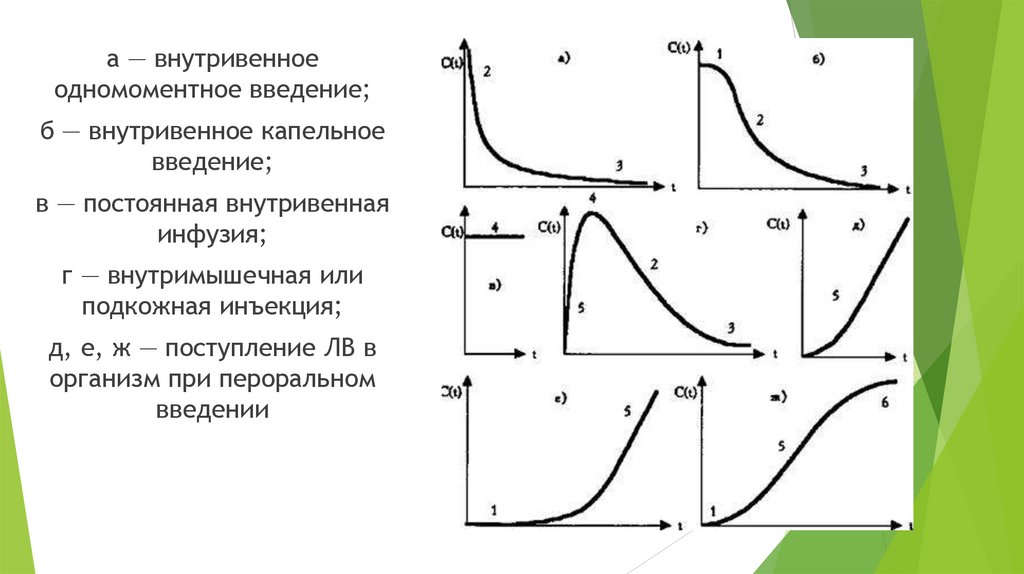
а — внутривенноеодномоментное введение;
б — внутривенное капельное
введение;
в — постоянная внутривенная
инфузия;
г — внутримышечная или
подкожная инъекция;
д, е, ж — поступление ЛВ в
организм при пероральном
введении
26.
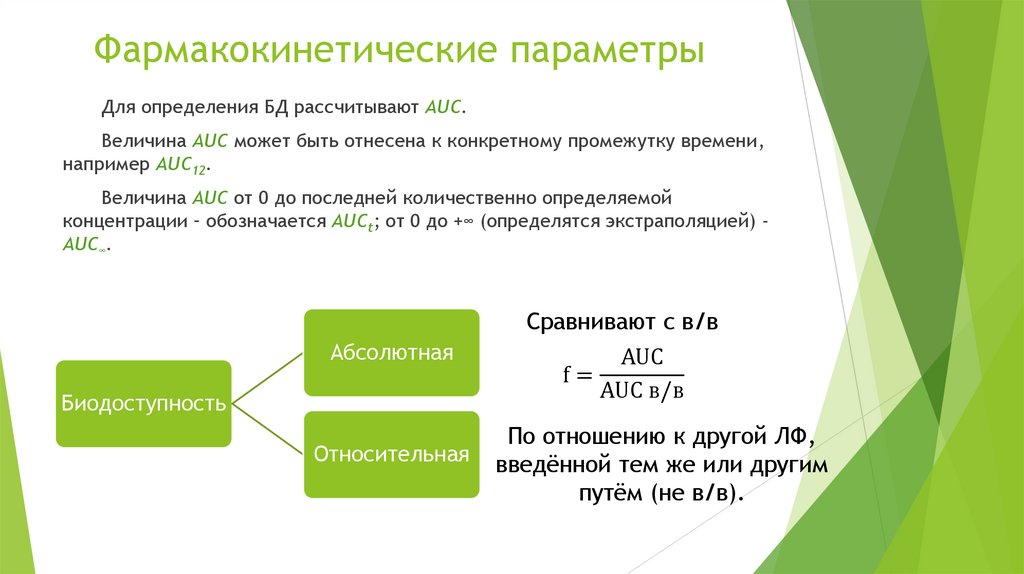
Фармакокинетические параметрыДля определения БД рассчитывают AUC.
Величина AUC может быть отнесена к конкретному промежутку времени,
например AUC12.
Величина AUC от 0 до поcледней количественно определяемой
концентрации – обозначается AUCt; от 0 до +∞ (определятся экстраполяцией) AUC∞.
Абсолютная
Биодоступность
Относительная
Сравнивают с в/в
AUC
f=
AUC в/в
По отношению к другой ЛФ,
введённой тем же или другим
путём (не в/в).
27.
РАСПРЕДЕЛЕНИЕ - процесс распространения ЛВ по органами тканям после того, как оно поступило в системный кровоток.
Кажущийся объём распределения (Vd, apparent volume of
distribution) – гипотетический объём жидкости, в котором
необходимо растворить введённую дозу ЛВ, чтобы его
концентрация стала ровной концентрации в плазме крови.
D
Vd =
C0
28.
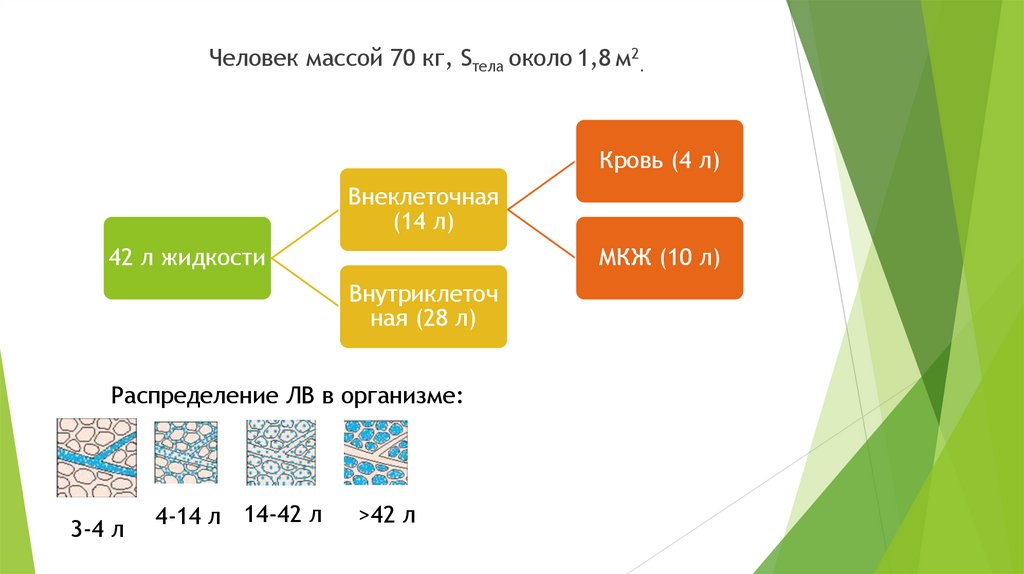
Человек массой 70 кг, Sтела около 1,8 м2.Кровь (4 л)
Внеклеточная
(14 л)
42 л жидкости
МКЖ (10 л)
Внутриклеточ
ная (28 л)
Распределение ЛВ в организме:
3-4 л
4-14 л 14-42 л
>42 л
29.
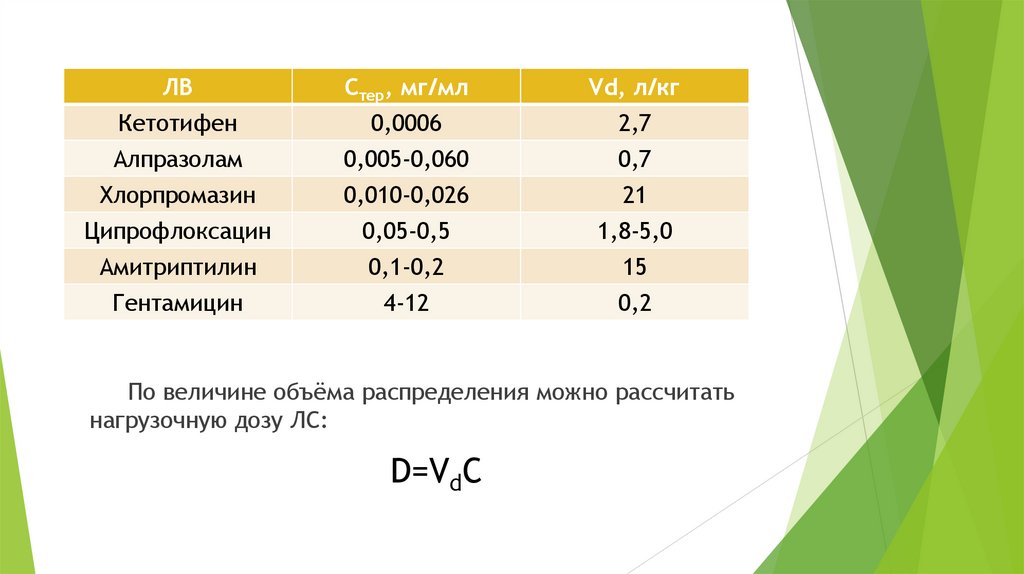
ЛВСтер, мг/мл
Vd, л/кг
Кетотифен
0,0006
2,7
Алпразолам
0,005-0,060
0,7
Хлорпромазин
0,010-0,026
21
Ципрофлоксацин
0,05-0,5
1,8-5,0
Амитриптилин
0,1-0,2
15
Гентамицин
4-12
0,2
По величине объёма распределения можно рассчитать
нагрузочную дозу ЛС:
D=VdC
30.
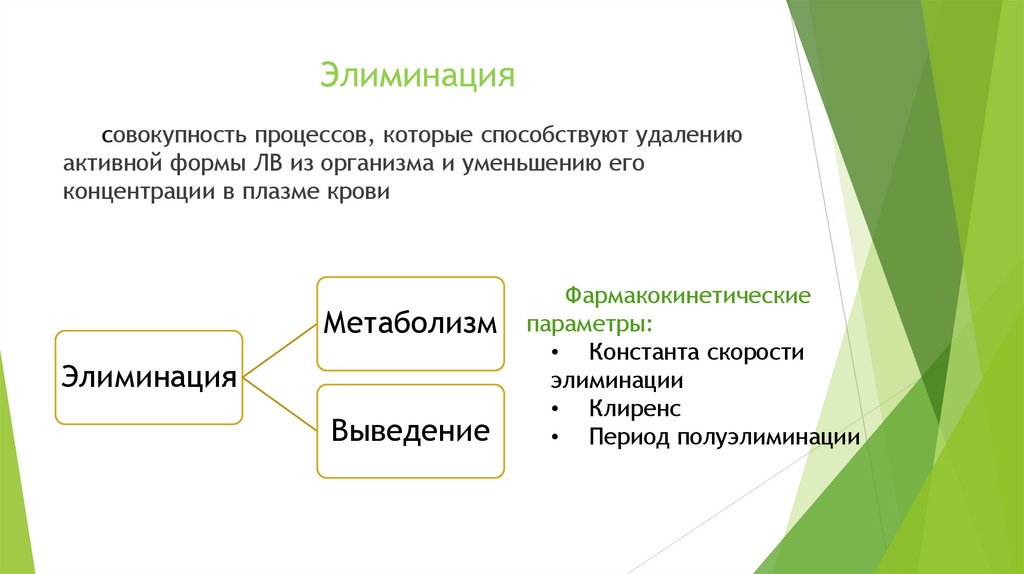
Элиминациясовокупность процессов, которые способствуют удалению
активной формы ЛВ из организма и уменьшению его
концентрации в плазме крови
Метаболизм
Элиминация
Выведение
Фармакокинетические
параметры:
• Константа скорости
элиминации
• Клиренс
• Период полуэлиминации
31.
Фармакокинетические параметрыДля большинства ЛВ процесс элиминации описывается
кинетическим уравнением первого порядка:
dC
=-kelC
dt
C=C0e-kelT
Константа скорости элиминации первого порядка (kel,
мин-1) – параметр, показывающий какая часть ЛВ
элиминируется из организма в единицу времени.
Для некоторых веществ процесс элиминации описывается
кинетическим уравнением нулевого порядка – не зависит от
начальной концентрации (этанол – 10 г/час).
32.
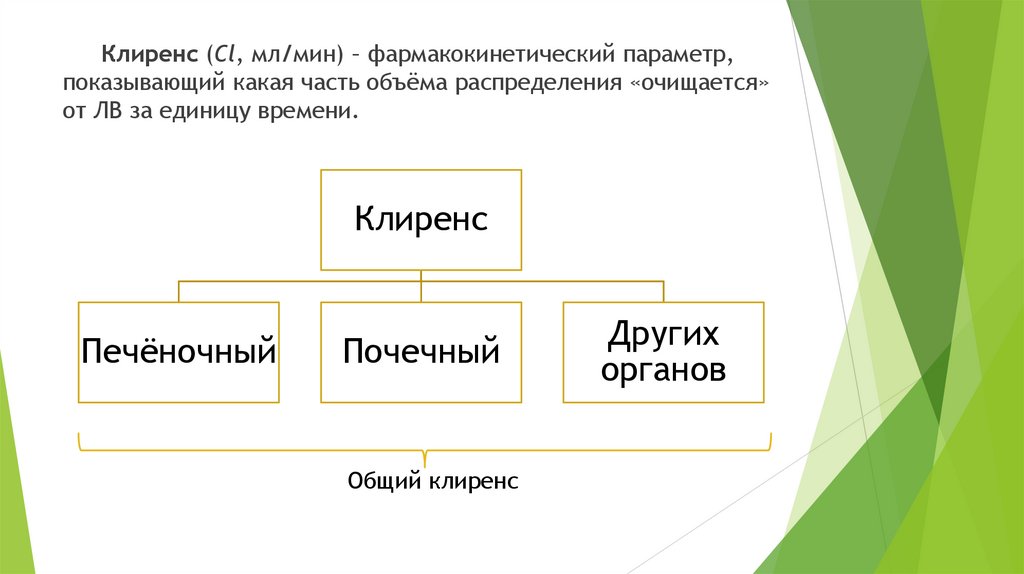
Клиренс (Cl, мл/мин) – фармакокинетический параметр,показывающий какая часть объёма распределения «очищается»
от ЛВ за единицу времени.
Клиренс
Печёночный
Почечный
Общий клиренс
Других
органов
33.
ЛВCl, мл/(мин*кг)
Фенобарбитал
0,06
Алпразолам
0,7
Гентамицин
1
Хлорпромазин
8,6
Амитриптилин
11,5
Клиренс служит для
подбора
поддерживающей
дозы, позволяющей
достичь равновесной
концентрации ЛВ в
плазме крови:
Скорость введения = Cl*Cтер
Связь с другими
параметрами:
D
Cl =
AUC
Cl = kelVd
34.
Период полуэлиминации (t1/2, мин) – время, необходимоедля уменьшения концентрации ЛВ в плазме крови (любым
путём) в 2 раза.
ЛВ
t1/2, часы
Гентамицин
2-4
Алпразолам
11-15
Хлорпромазин
15-30
Фенобрабитал
90-100
Амиодарон
14-107 суток
Величина t1/2 используется для
определения промежутка
времени, необходимого для
достижения равновесной
концентрации ЛВ в плазме
крови.
ln2Vd
t1/2 =
Cl
35.
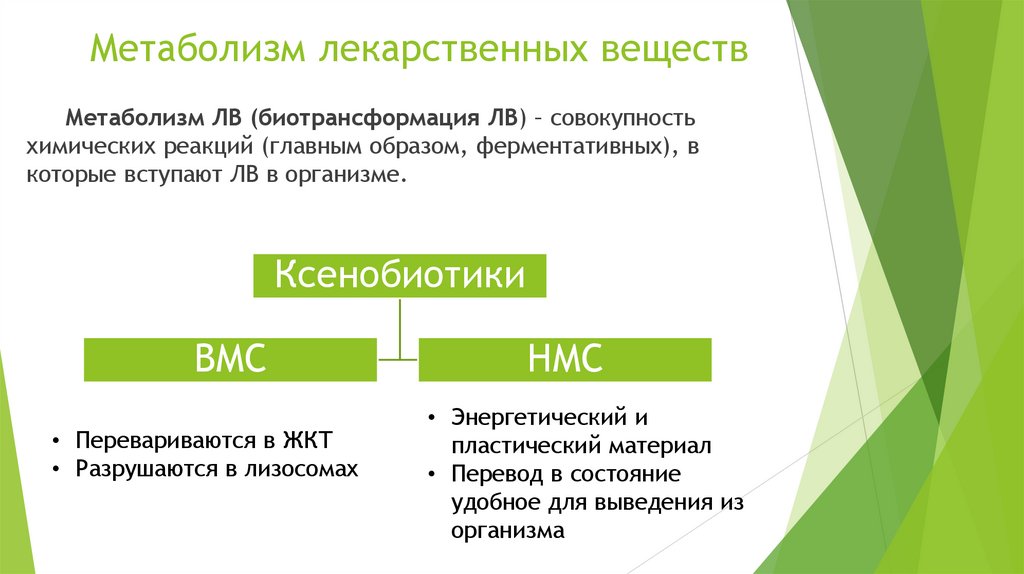
Метаболизм лекарственных веществМетаболизм ЛВ (биотрансформация ЛВ) – совокупность
химических реакций (главным образом, ферментативных), в
которые вступают ЛВ в организме.
Ксенобиотики
ВМС
• Перевариваются в ЖКТ
• Разрушаются в лизосомах
НМС
• Энергетический и
пластический материал
• Перевод в состояние
удобное для выведения из
организма
36.
В процессе метаболизма ксенобиотик (ЛВ) становитсяменее липофильным и быстрее выводится из организма;
Липофильные ЛВ метаболизируются
чем гидрофильные.
в большей степени,
37.
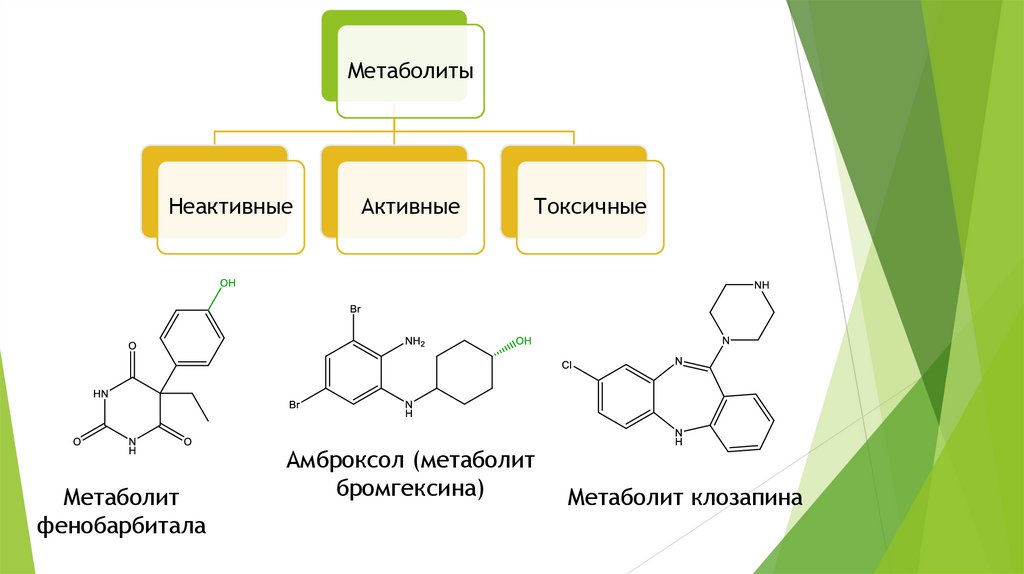
МетаболитыНеактивные
Метаболит
фенобарбитала
Активные
Токсичные
Амброксол (метаболит
бромгексина)
Метаболит клозапина
38.
39.
40.
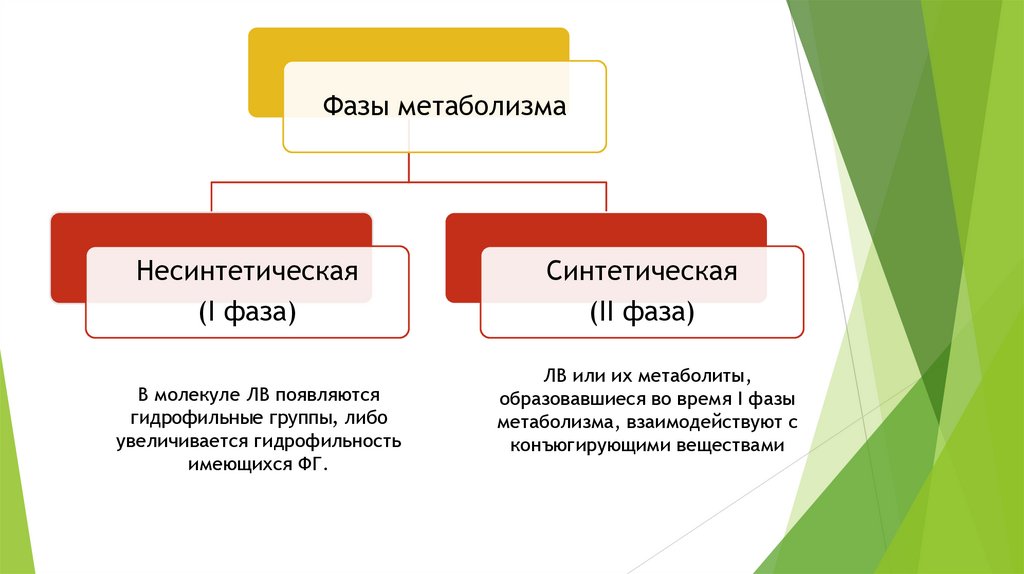
Фазы метаболизмаНесинтетическая
(I фаза)
В молекуле ЛВ появляются
гидрофильные группы, либо
увеличивается гидрофильность
имеющихся ФГ.
Синтетическая
(II фаза)
ЛВ или их метаболиты,
образовавшиеся во время I фазы
метаболизма, взаимодействуют с
конъюгирующими веществами
41.
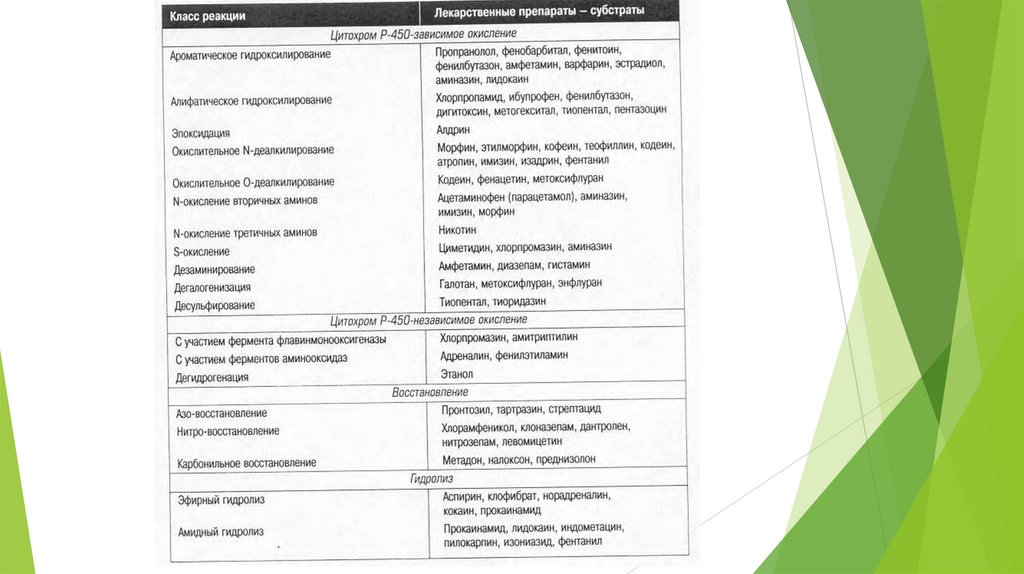
Реакции I фазы метаболизмаI фаза
метаболизма
Окисление
Восстановление
Гидролиз
ОВР происходят в гепатоцитах («микросомальное окисление»).
Их катализируют ферменты, входящие в состав суперсемейства
цитохромов Р450 (более 300 изоформ для 60 типов ОВР)
42.
43.
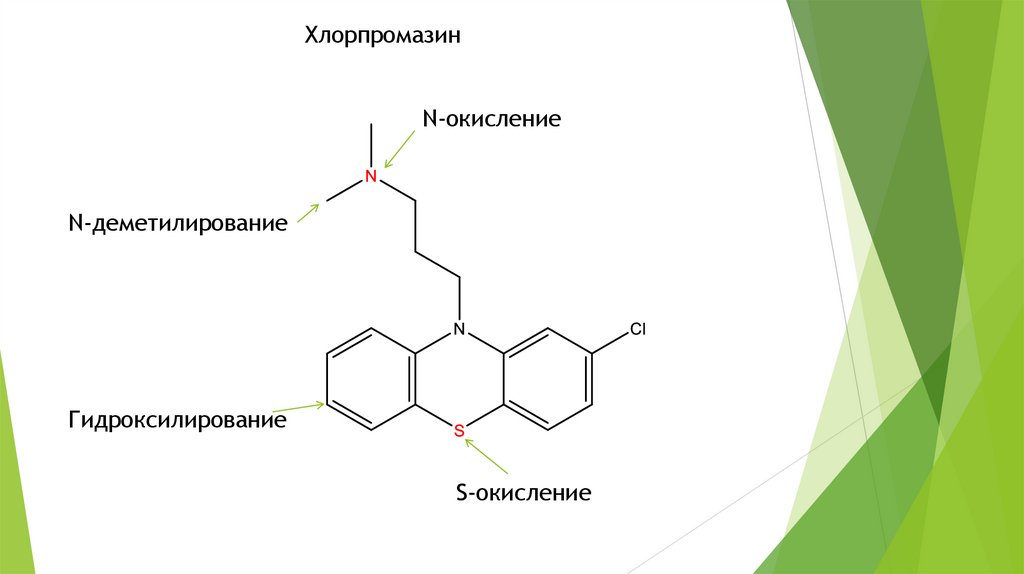
ХлорпромазинN-окисление
N-деметилирование
Гидроксилирование
S-окисление
44.
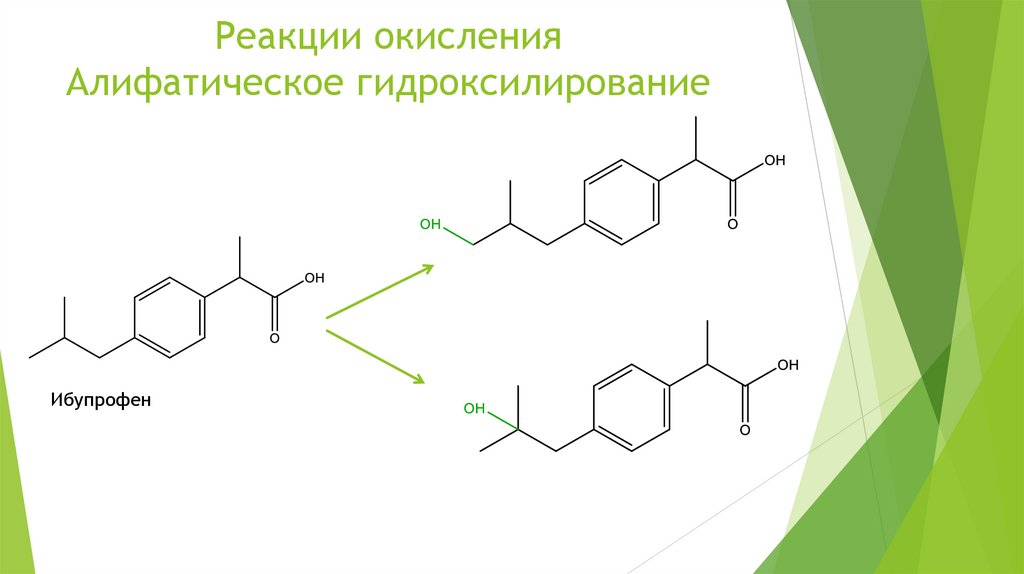
Реакции окисленияАлифатическое гидроксилирование
Ибупрофен
45.
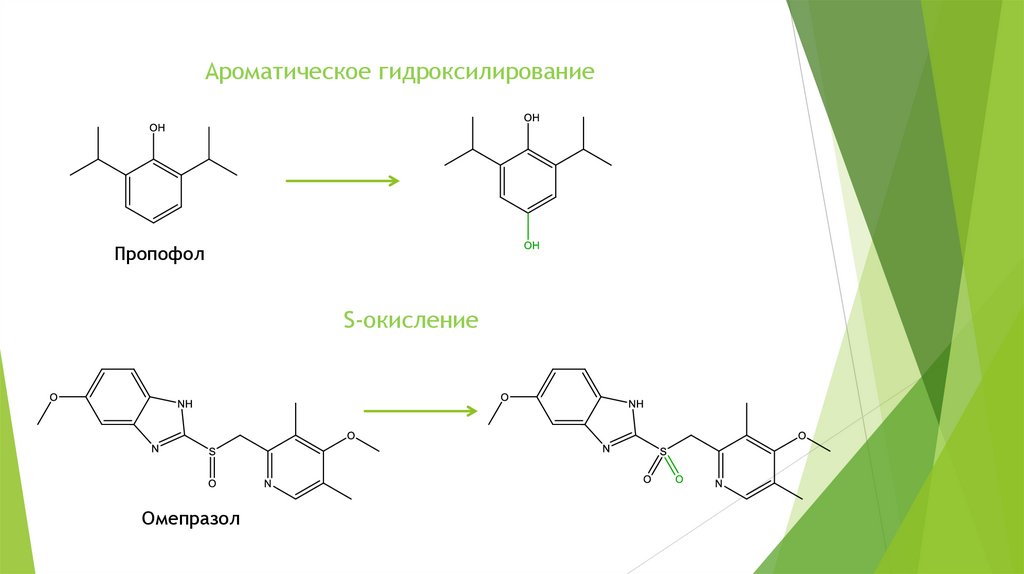
Ароматическое гидроксилированиеПропофол
S-окисление
Омепразол
46.
N-окислениеПефлоксацин
47.
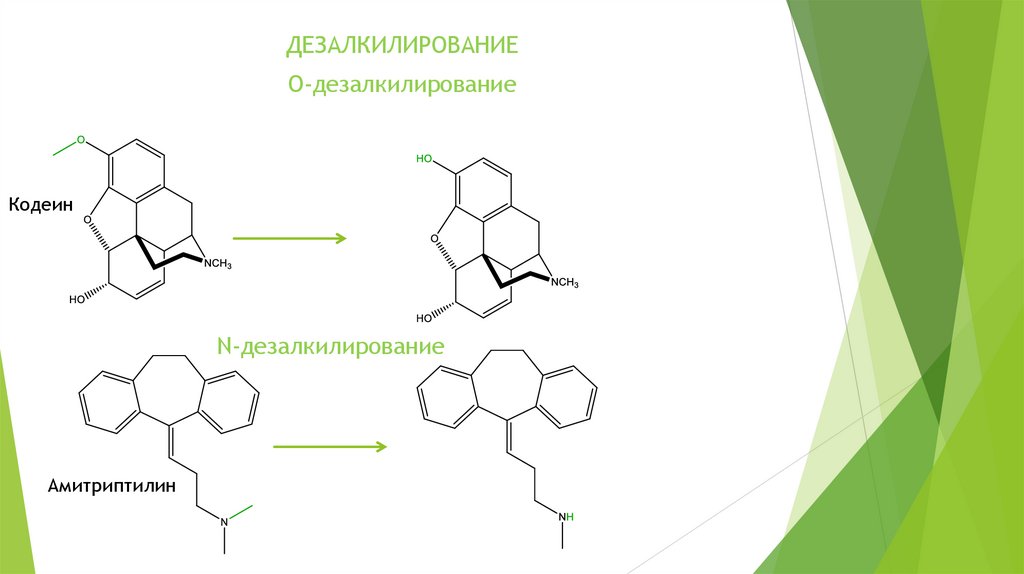
ДЕЗАЛКИЛИРОВАНИЕO-дезалкилирование
Кодеин
N-дезалкилирование
Амитриптилин
48.
S-дезалкилированиеТиоридазин
49.
ДезаминированиеЭфедрин
Десульфирование
Тиопентал
50.
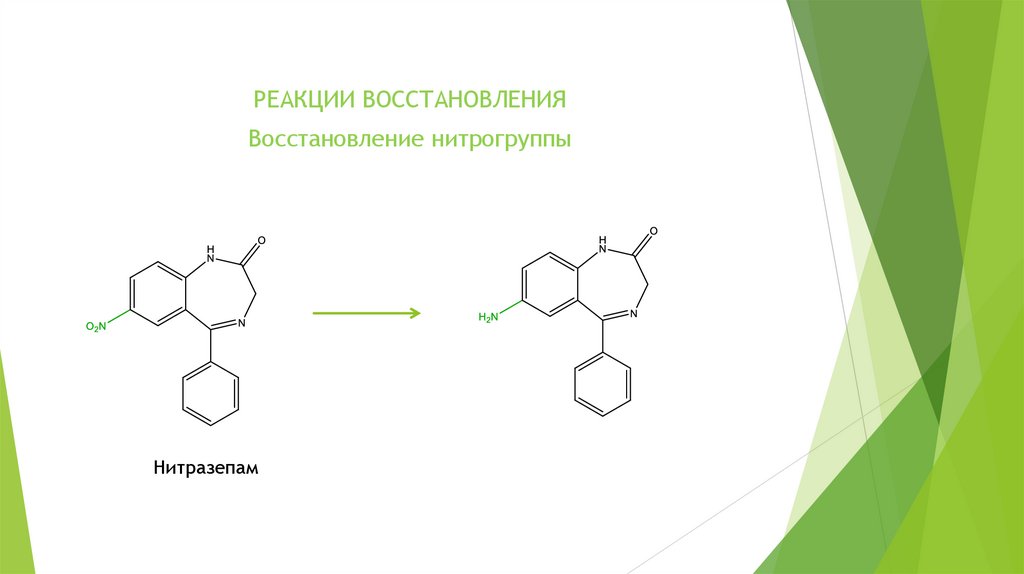
РЕАКЦИИ ВОССТАНОВЛЕНИЯВосстановление нитрогруппы
Нитразепам
51.
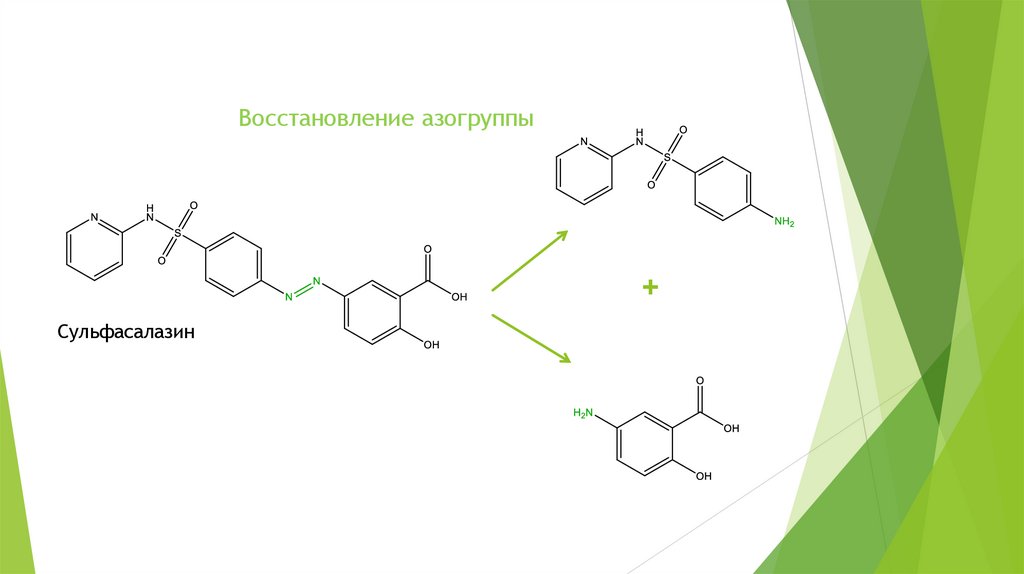
Восстановление азогруппы+
Сульфасалазин
52.
Восстановление оксогруппыХлоралгидрат
Варфарин
53.
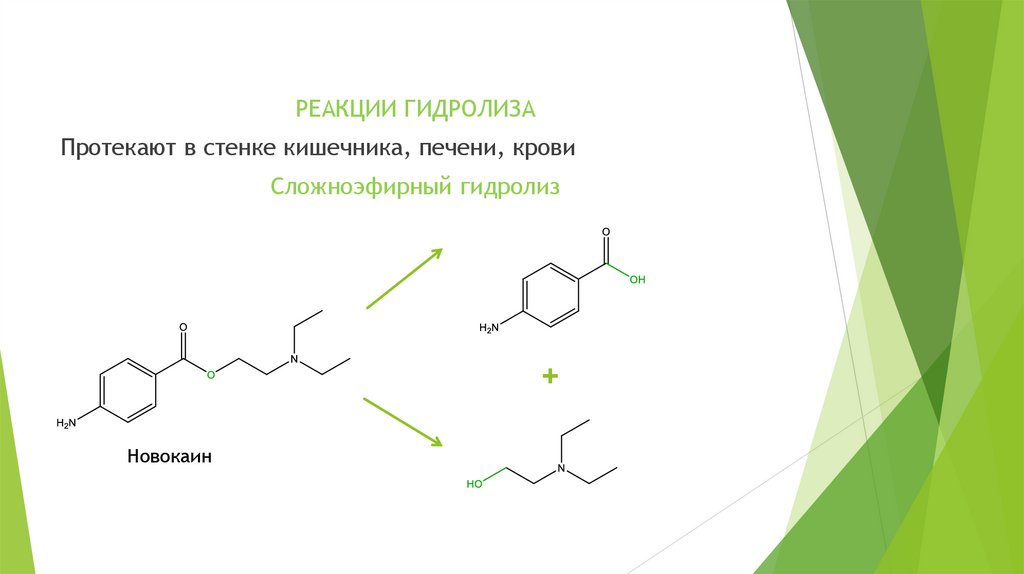
РЕАКЦИИ ГИДРОЛИЗАПротекают в стенке кишечника, печени, крови
Сложноэфирный гидролиз
+
Новокаин
54.
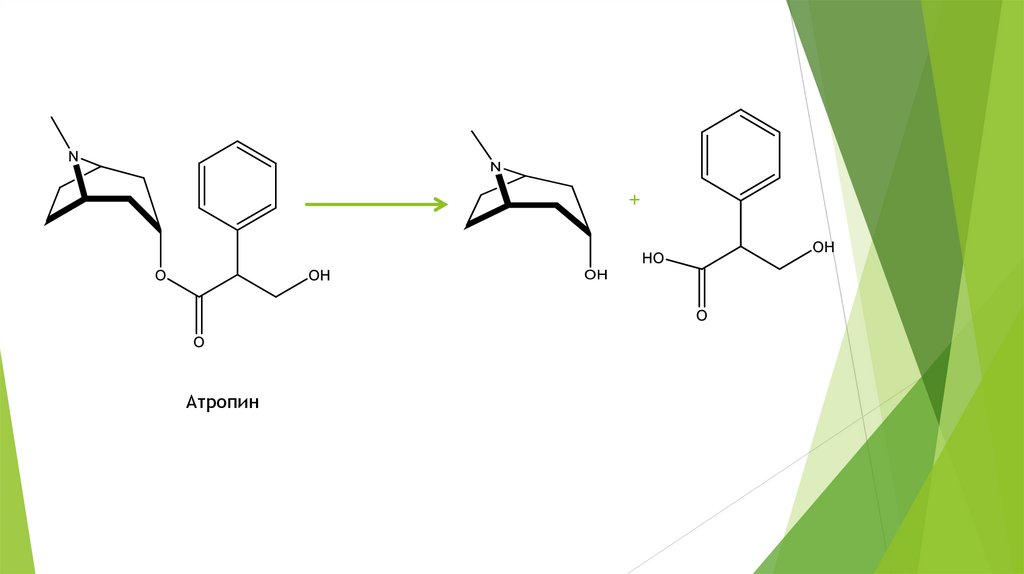
+Атропин
55.
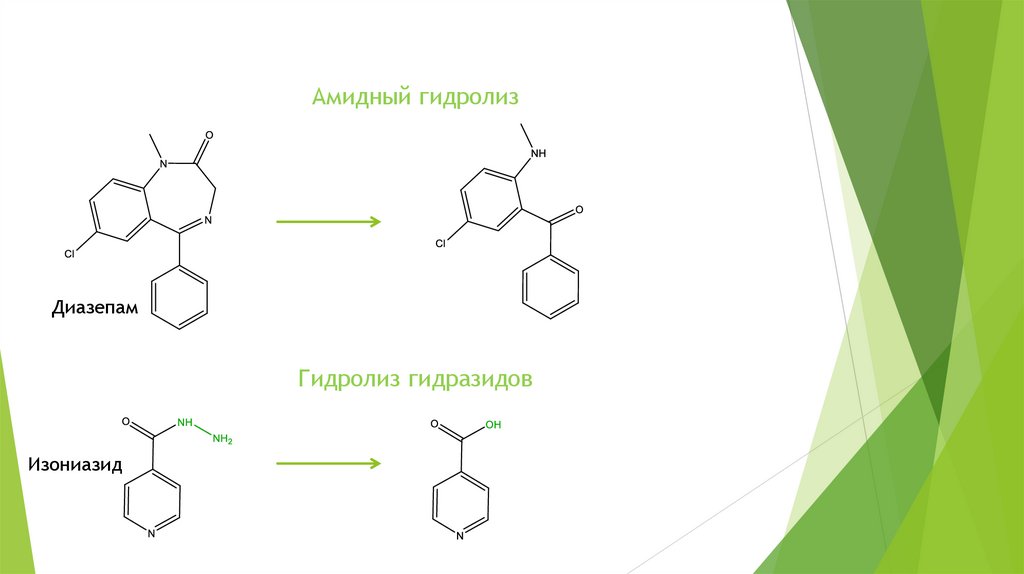
Амидный гидролизДиазепам
Гидролиз гидразидов
Изониазид
56.
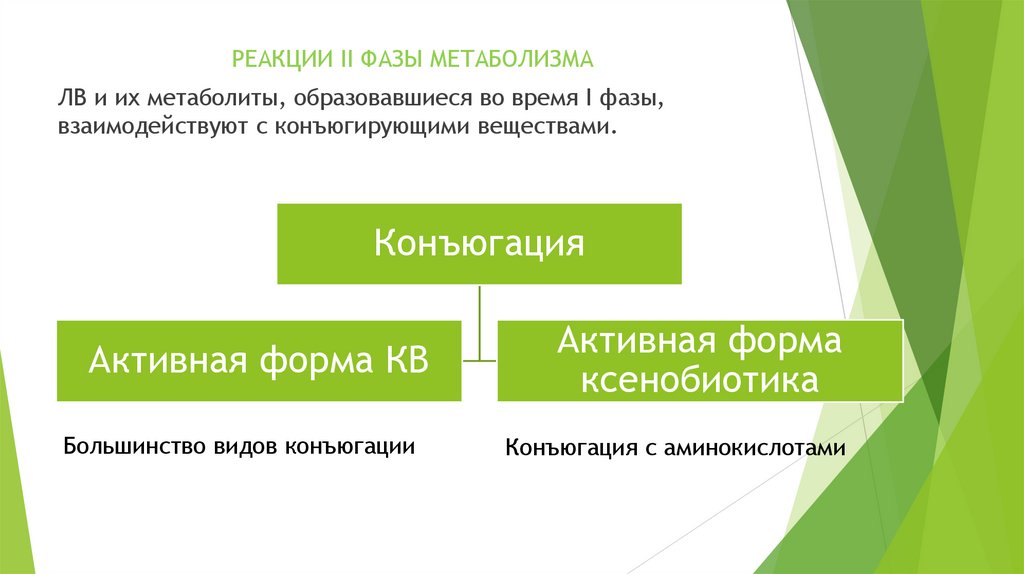
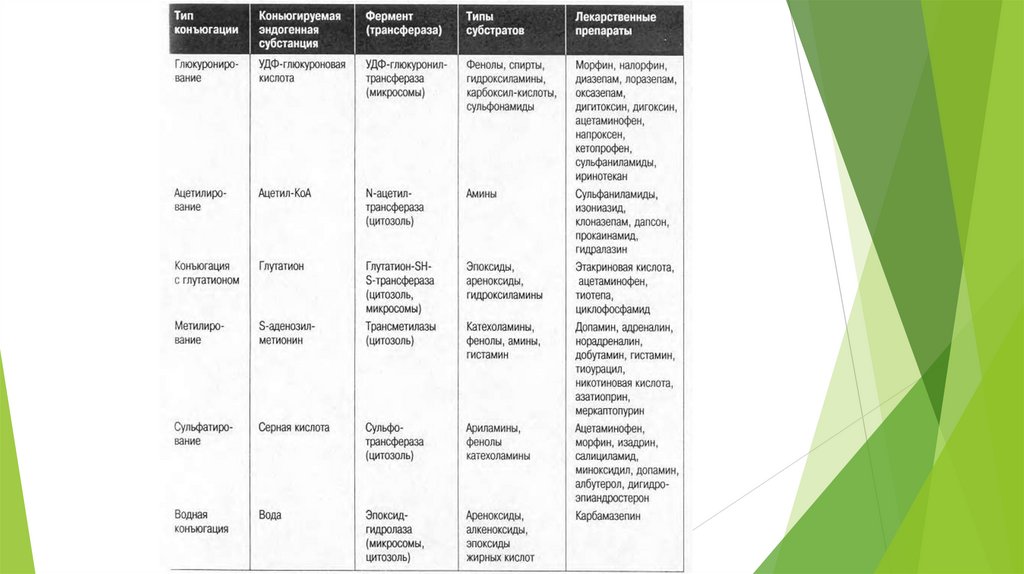
РЕАКЦИИ II ФАЗЫ МЕТАБОЛИЗМАЛВ и их метаболиты, образовавшиеся во время I фазы,
взаимодействуют с конъюгирующими веществами.
Конъюгация
Активная форма КВ
Активная форма
ксенобиотика
Большинство видов конъюгации
Конъюгация с аминокислотами
57.
58.
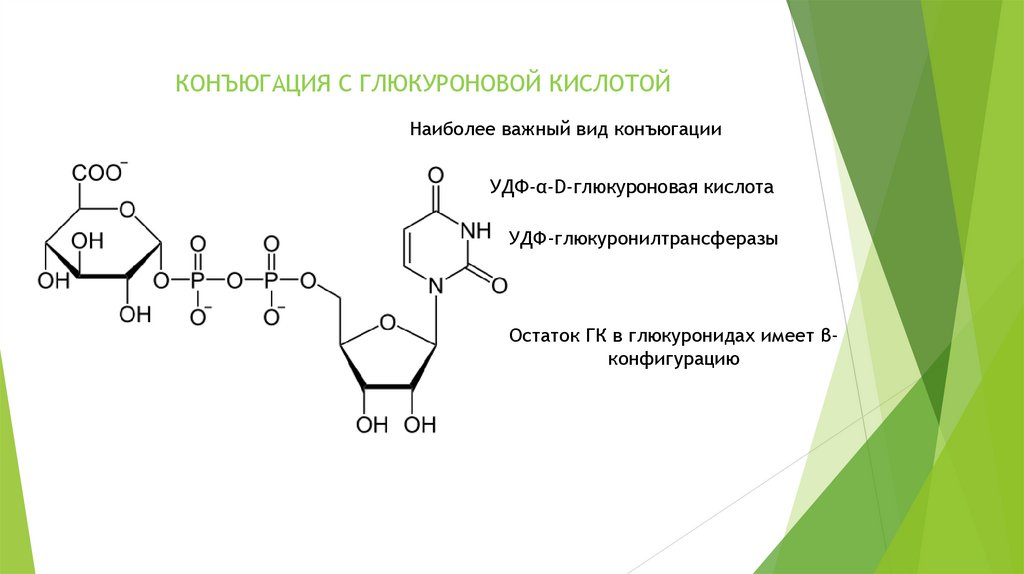
КОНЪЮГАЦИЯ С ГЛЮКУРОНОВОЙ КИСЛОТОЙНаиболее важный вид конъюгации
УДФ-α-D-глюкуроновая кислота
УДФ-глюкуронилтрансферазы
Остаток ГК в глюкуронидах имеет βконфигурацию
59.
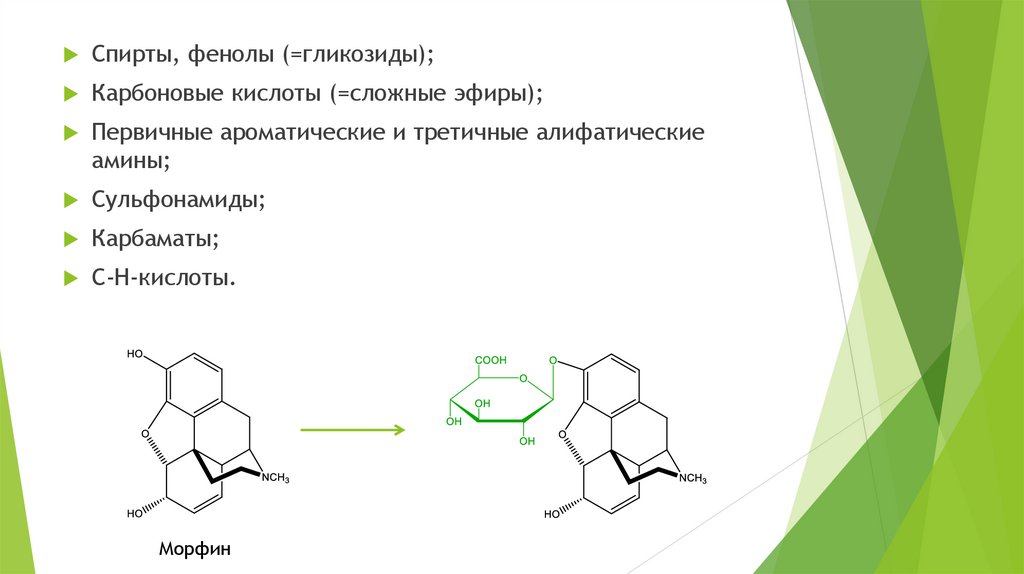
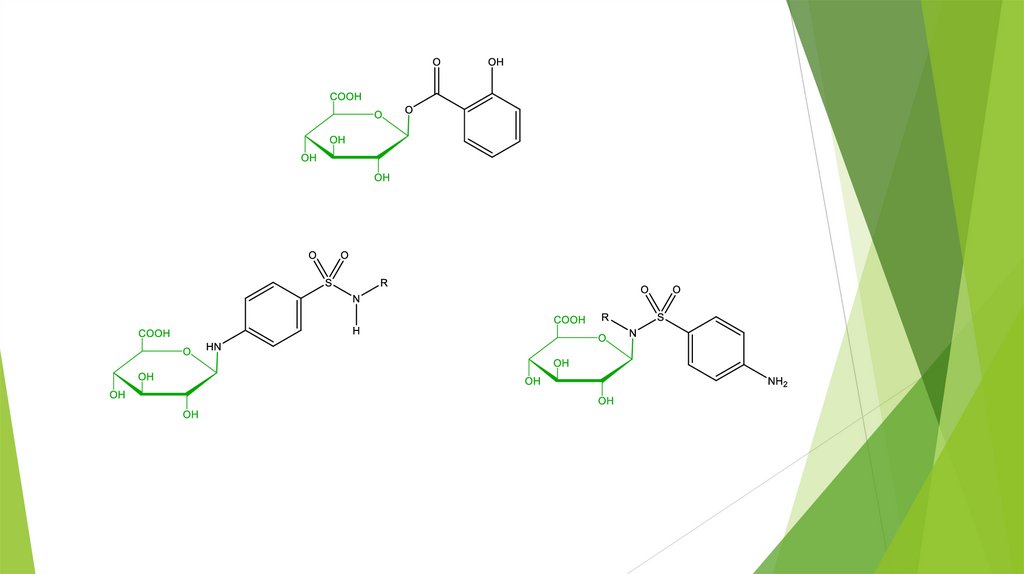
Спирты, фенолы (=гликозиды);Карбоновые кислоты (=сложные эфиры);
Первичные ароматические и третичные алифатические
амины;
Сульфонамиды;
Карбаматы;
C-H-кислоты.
Морфин
60.
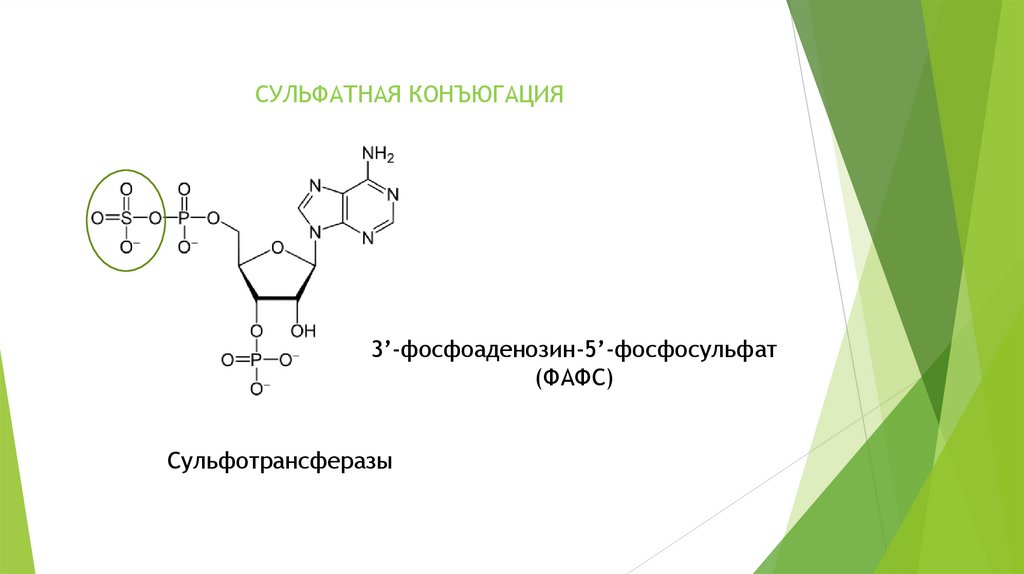
61.
СУЛЬФАТНАЯ КОНЪЮГАЦИЯ3’-фосфоаденозин-5’-фосфосульфат
(ФАФС)
Сульфотрансферазы
62.
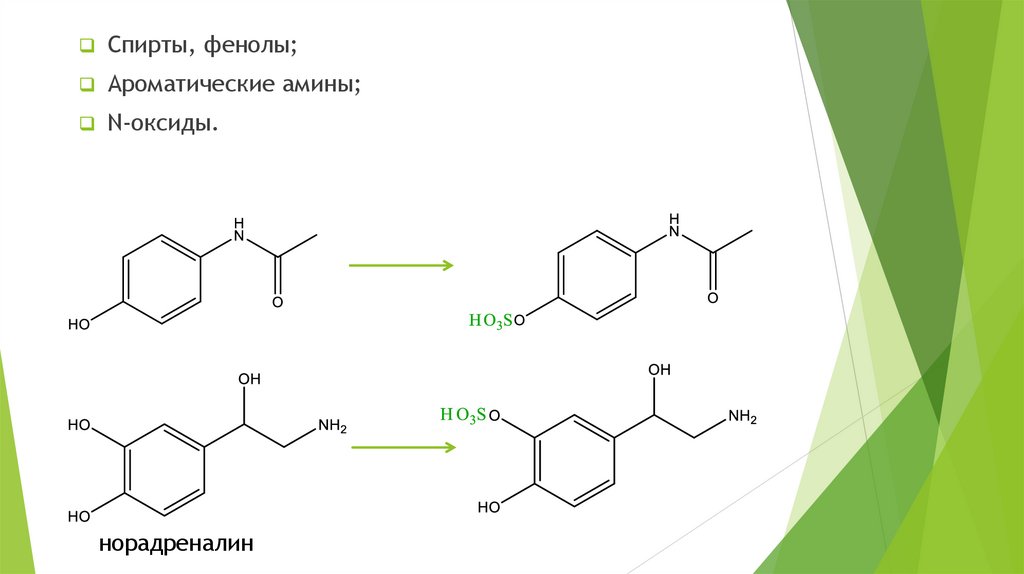
Спирты, фенолы;Ароматические амины;
N-оксиды.
норадреналин
63.
МЕТИЛИРОВАНИЕS-аденозилметионин
Метилтрансферазы
64.
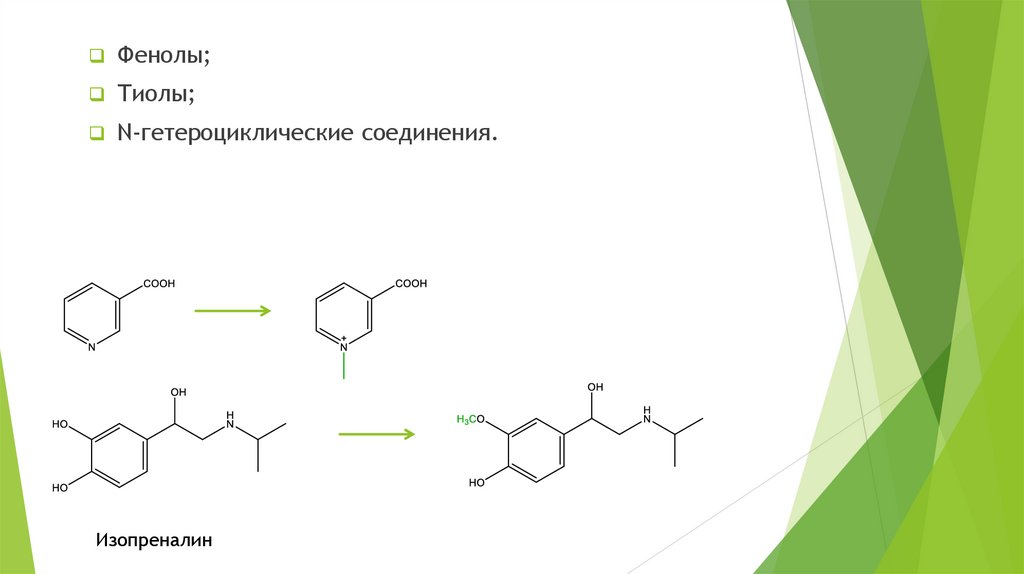
Фенолы;Тиолы;
N-гетероциклические соединения.
Изопреналин
65.
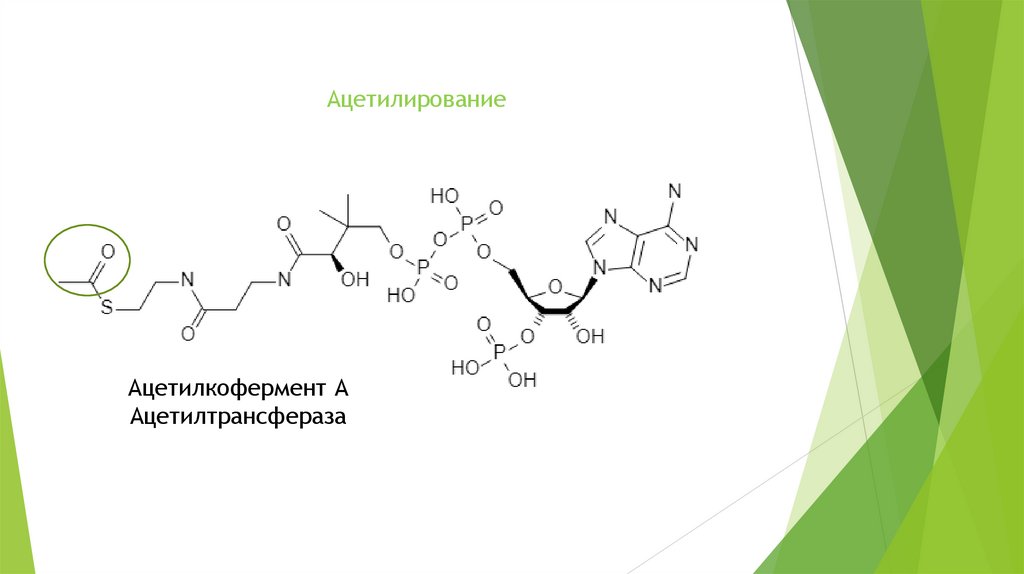
АцетилированиеАцетилкофермент А
Ацетилтрансфераза
66.
Первичные амины;Вторичные амины;
Замещённые гидразины.
Прокаинамид
67.
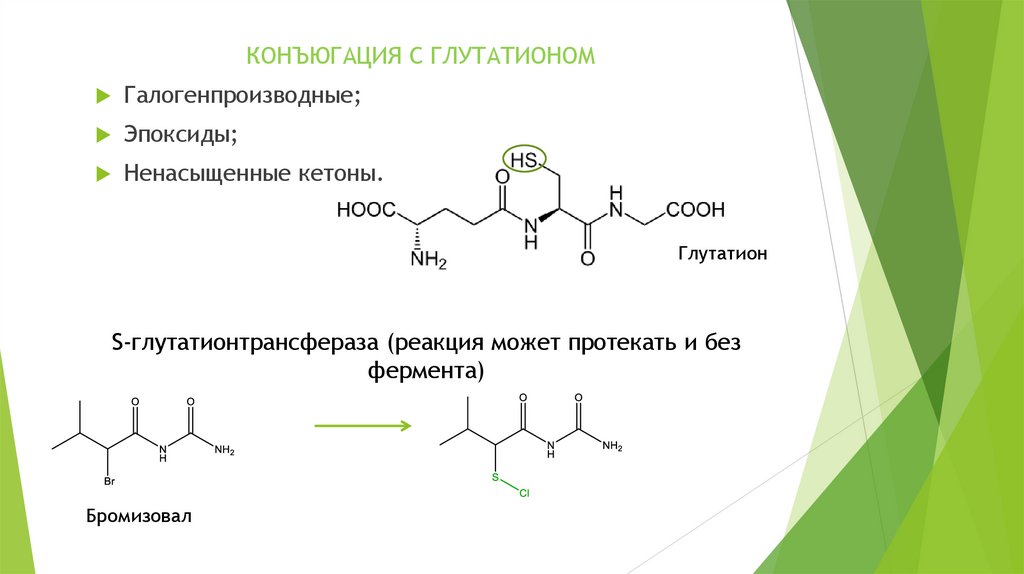
КОНЪЮГАЦИЯ С ГЛУТАТИОНОМГалогенпроизводные;
Эпоксиды;
Ненасыщенные кетоны.
Глутатион
S-глутатионтрансфераза (реакция может протекать и без
фермента)
Бромизовал
68.
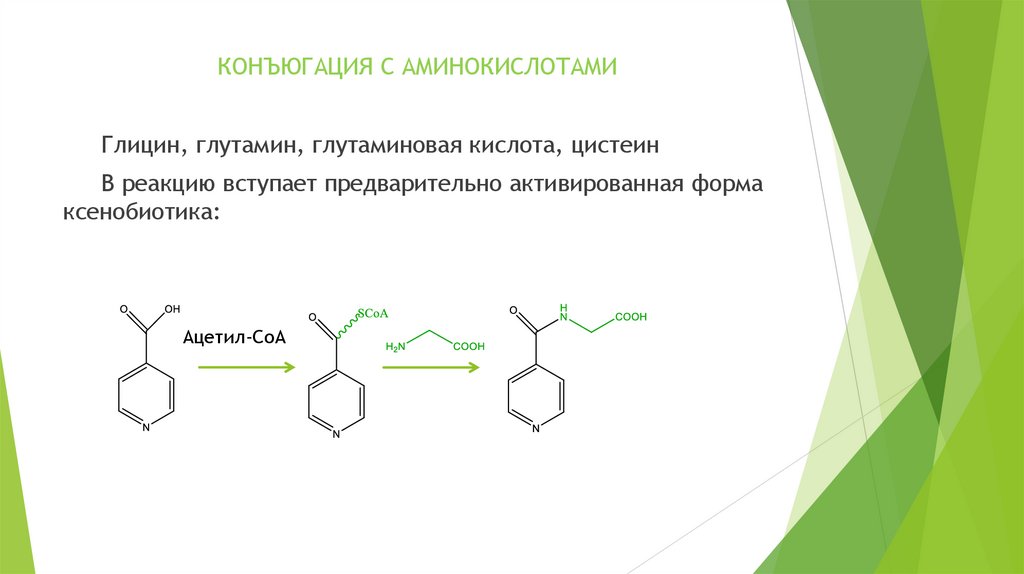
КОНЪЮГАЦИЯ С АМИНОКИСЛОТАМИГлицин, глутамин, глутаминовая кислота, цистеин
В реакцию вступает предварительно активированная форма
ксенобиотика:
Ацетил-CoA
69.
Эффект первого прохождения черезпечень
ЛС с высоким печеночным клиренсом имеют высокую
степень извлечения (экстракции) из крови из-за высокой
емкости (активности) метаболизирующих ферментов. Они
быстро и легко метаболизируются, поэтому их печеночный
клиренс определяется величиной и скростью кровотока.
ЛС с низким печеночным клиренсом – их метаболизм не
зависит от печеночного кровотока, а зависит от активности
ферментов и степени связывания с белками плазмы крови.
Т.е. ЛС, значительно связанные с БПК, будут иметь ниже
клиренс по сравнению с теми, которые связаны слабее.
70.
ЛП с высоким печеночным клиренсом всасываются в тонкойкишке и попадают в систему воротной вены, откуда поступают
в печень, где метаболизируются на 50-80% до поступления в
системный кровоток. Это и называется «ЭФФЕКТОМ ПЕРВОГО
ПРОХОЖДЕНИЯ ЧЕРЕЗ ПЕЧЕНЬ».
Для таких ЛП БД при всасывании в кишечнике может
составлять 100%, а итоговая БД будет низкой.
Например, аминазин, аспирин, верапамил, изопреналин,
кортизол, метоклопрамид, лидокаин, органические нитраты,
пропранолол, метопролол, имипрамин, морфин,
метилтестостерон и др.
71.
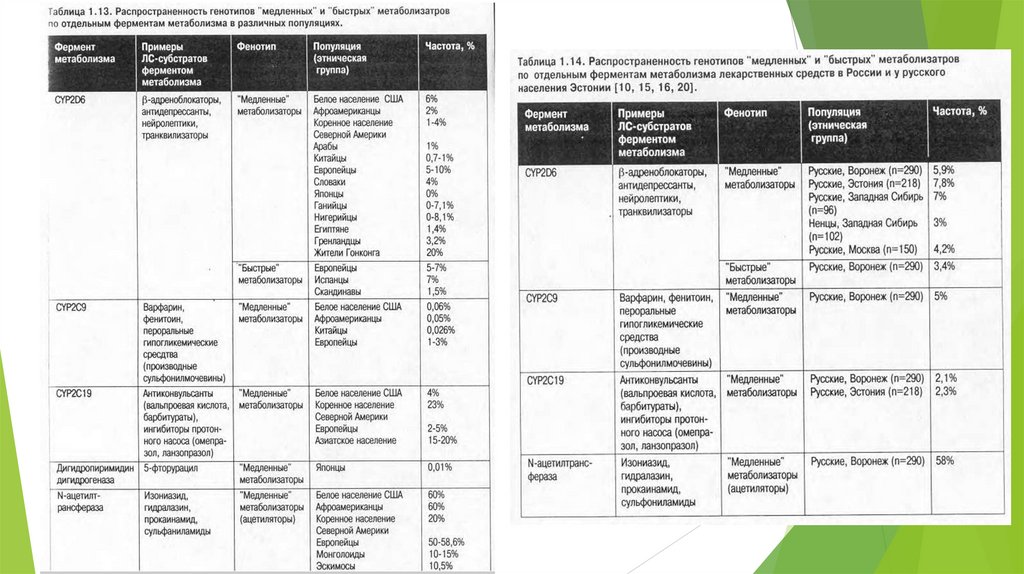
Методы изучения метаболизма«ГЕНОТИПИРОВАНИЕ» - косвенный метод определения активности
того или иного фермента метаболизма на основаниии изучения его гена
методом полимеразной цепной реакции.
«ФЕНОТИПИРОВАНИЕ» - прямой метод определения активности того
или иного фермента по фармакокинетике его специфического субстрата
(«маркерного» субстрата) и его метаболитов.
«ЭКСТЕНСИВНЫЕ МЕТАБОЛИЗЕРЫ» - лица с нормальной скоростью
метаболических реакций. Большинство населения.
«МЕДЕЛННЫЕ» МЕТАБОЛИЗЕРЫ» - лица со сниженной скоростью
метаболизма определенных ЛС. Синтезируется «дефектный» фермент или
отсуствует. Лс накапливается в высоких концентрациях в организме, что
приводит к развитию нежелательных эффектов.
«СВЕРХАКТИВНЫЕ» ИЛИ БЫСТРЫЕ МЕТАБОЛИЗЕРЫ» - лица с
повышенной скоростью метаболизма определенных ЛС. Для таких лиц доза
должна быть выше.
72.
73.
Цитохром Р450 (CYP450)— большая группа ферментов, отвечающая за метаболизм
ксенобиотиков и лекарственных препаратов.
Ферменты семейства цитохрома Р450 осуществляют
окислительную биотрансформацию лекарственных препаратов и,
таким образом, выполняют дезинтоксикационную функцию.
С участием цитохромов происходит метаболизм многих
классов лекарственных средств, таких как ингибиторы
протонной помпы, антигистаминные препараты, ингибиторы
ретровирусной протеазы, бензодиазепины, блокаторы
кальциевых каналов и другие.
74.
Цитохром Р450 представляет комплекс белка с ковалентносвязанным гемом (металлопротеином), обеспечивающим
присоединение кислорода. Гем, в свою очередь, является
комплексом протопорфирина IX и двувалентного атома железа.
Цитохром Р450-зависимые
монооксигеназы катализируют расщепление различных
веществ посредством гидроксилирования с участием донора
электрона НАДФН и молекулярного кислорода. В этой реакции
один атом кислорода присоединяется к субстрату, а второй
восстанавливается до воды.
Существует в виде множества изоформ.
75.
Индукция фермента метаболизмаУвеличение количества и активности фермента из-за
воздействия химических агентов (в т.ч. ЛП). Индукторы
цитохрома Р 450. Ускорение метаболизма вдет к снижению
фармакологической активности.
Механизмы индукции:
«Фенобарбиталовый» тип – непосредственное действие
молекулы индуктора на регуляторную область гена, что
приводит к индукции фермента метаболизма ЛС.
76.
«Рифампицин-дексаметазоновый» - индукция опосредованавзаимодействием молекулы-индуктора со специфическими
рецепторами, которые относятся як белкам регуляторам
транскрипции. Индукторы связваясь с этими рецепторам, в
виде комплекса проникают в ядро клетки, где воздействуют на
регуляторную область гена.
«Этаноловый» тип – стабилизация молекуля фермента
метаболизма ЛС вследствие образования комплекса с
некоторыми ксенобиотиками (этанол, ацетон). Активируется
система фосфорилирования в гепатоцитах через цАМФ.
77.
Экстрагепатический метаболизмКишечник (морфин, этинилэстрадиол);
Легкие;
Почки (морфин, парацетамол, фуросемид,
хлорамфеникол)
78.
Ингибирование ферментовметаболизма
Снижение активности ферментов, которое может сопровождаться
усилением активности ферментов, связанная с удлинением циркуляции
ЛС в организме.
Механизмы:
Связывание с регуляторной областью гена метаболизма ЛС.
Циметидин, омепразол, флуоксетин, фторхинолоны, макролиды, СА.
Конкурентное метаболическое взаимодействие. Некоторые ЛС с
высокой афиноостью к изоформам ферментов ингибируют
метаболизм ЛП с низким аффинитетом. Верапамил, нифедипин,
хинидин.
Прямая инактивация ферментов (гастоден). Фумарокумарины
сока грейпфрута и лайма.
































 medicine
medicine








