Similar presentations:
Коррозия металлов
1.
Коррозия металловХИМИЯ – 11
2.
Ежегодно в мире «теряется»до ¼ произведённого железа…
Коррозия – рыжая крыса,
Грызёт металлический лом.
В. Шефнер
Результат:
прямые потери массы металла;
косвенные потери - утрата важнейших
свойств.
3.
Общее понятиеМеталлы и сплавы подвержены коррозии под воздействием окружающей среды. Причина
этого разрушения лежит в химических свойствах металлов – в их способности вступать в
окислительно-восстановительные реакции с веществами окружающей среды и
окисляться.
Коррозия (от латинского «corrodere» разъедать) – самопроизвольный
окислительно-восстановительный процесс разрушения металлов и
сплавов вследствие взаимодействия с окружающей средой.
Общеизвестным примером коррозии является ржавление железа.
Существуют разные виды коррозии металлов и их сплавов. Наиболее распространены
два вида: химическая и электрохимическая.
3
4.
А. По площади и характеру поражения: сплошная, точечная,язвенная, межкристаллическая.
Б. По природе агрессивных сред: воздушная, почвенная, морская,
биологическая (вызванная водорослями, моллюсками, плесенью),
коррозия в смазке, газовая.
В. По механизму возникновения: химическая, электрохимическая,
электрическая (под действием блуждающих токов).
5.
Химическая коррозияКоррозию металлов и сплавов (их окисление) вызывают такие компоненты
окружающей среды, как вода, кислород, оксиды углерода и серы, содержащиеся в
воздухе, водные растворы солей (морская вода, грунтовые воды). Эти компоненты
непосредственно окисляют металл – происходит химическая коррозия.
Химическая коррозия – это коррозия,
обусловленная взаимодействием металлов
и сплавов с веществами, содержащимися в
окружающей среде, при этом происходит
окислительно-восстановительное
разрушение металла без возникновения
электрического тока в системе.
К химической коррозии относятся:
- газовая коррозия;
- коррозия в жидкостях-неэлектролитах.
5
6.
При химической коррозии идет окисление металла без возникновения цепиэлектрического тока:
3Fe + 2O2 = Fe3O4 (FeO•Fe2O3),
4Al + 3O2 = 2Al2O3.
Для поверхности алюминия этот процесс благоприятен, т.к. оксидная пленка плотно
прилегает к поверхности металла и нет дальнейшего допуска кислорода к металлу.
Почему не рекомендуют варить овощи в алюминиевой посуде?
7.
Газовая коррозияГазовая коррозия – это вид коррозии, обусловленный непосредственным
взаимодействием металла или сплава с сухими газами, жидкостями, не являющимися
электролитами, твёрдыми веществами.
Суть её заключена в окислении металла в процессе непосредственного химического
взаимодействия с веществами окружающей среды (газовая, жидкостная коррозия).
Примером газовой коррозии может служить окисление железа в атмосфере хлора:
2Fe + 3Cl2 = 2FeCl3
Окисление кислородом воздуха:
2Fe + O2 = 2FeO
4Fe + 3O2 = 2Fe2O3
3Fe + 3O2 = FeO·Fe2O3 (смешанный оксид железа (II, III) )
4Fe + 3O2 + 6H2O = 4Fe(OH)3 (на воздухе в присутствии влаги)
3Fe + 4H2O(пар) = Fe3O4 + 4H2
Химически чистое железо почти не корродирует. Вместе с тем техническое железо,
которое содержит различные примеси, например в чугунах и сталях, ржавеет, так как
одной из причин возникновения коррозии является наличие примесей в металле, его
неоднородность.
7
8.
Химическая коррозия в жидкостях-неэлектролитахЖидкости-неэлектролиты - это жидкие среды, которые не являются
проводниками электричества.
К ним относятся:
- органические (бензол, фенол, хлороформ, спирты, керосин, нефть,
бензин);
- неорганического происхождения (жидкий бром, расплавленная сера и т.д.).
Чистые неэлектролиты не реагируют с металлами, но с добавлением даже
незначительного количества примесей процесс взаимодействия резко
ускоряется.
Для защиты конструкций от химической коррозии в жидкостяхнеэлектролитах на ее поверхность наносят покрытия, устойчивые в данной
среде.
8
9.
Электрохимическая коррозияЭто наиболее распространённый вид коррозии, приносящий наибольший вред
металлам и изделиям из них.
Электрохимическая коррозия – это вид коррозии, связанный с протеканием
электрохимических реакций на поверхности металла или его сплава при их
контакте с раствором электролита.
В этом случае образуется гальванический элемент, электродами которого и являются
металлы, находящиеся в растворе электролита (вода, в которой растворён
углекислый газ, кислоты и др.). Возникает электрохимический процесс, т.е. наряду с
химическими процессами связанными с отдачей электронов и окислением металла,
протекают и электрические (перенос электрона от одного участка металла к другому).
Fe → Fe2+
9
10.
Защита от коррозииИзоляция металла от среды
Изменение состава металла (сплава)
Изменение среды
11.
Способы защиты от коррозии1. Поверхностные защитные
покрытия металлов:
Металлические:
анодное – покрытие более активным
металлом Zn, Cr;
катодное – покрытие менее активным
металлом Ni, Sn, Ag, Au.
Белая жесть (лужёное железо) – не
защищает от разрушения в случае
нарушения покрытия.
Неметаллические покрытия:
органические (лаки, краски,
пластмассы, резина - гумирование,
битум);
неорганические (эмали).
11
12.
Способы защиты от коррозии2. Создание сплавов,
стойких к коррозии.
Достигается введением в
состав стали хрома,
марганца, никеля
(нержавеющая сталь).
«Нержавейка», из которой
изготавливают столовые приборы,
содержит до 12% хрома и до 10%
никеля.
Изготавливают
антикоррозийные сплавы,
содержащие до 12% Cr, а
также сплавы с добавками
никеля, кобальта, меди и
других металлов.
12
13.
Способы защиты от коррозии3. Протекторная защита.
Сущность протекторной защиты заключается в том, что металлическую
конструкцию (подземный трубопровод, корпус судна и т. д.), находящуюся в
растворе электролита (подземные и почвенные воды, морская вода и т. д.),
соединяют с протектором – более активным металлом, чем металл защищаемой
конструкции.
В процессе коррозии протектор служит анодом и разрушается, предохраняя от
разрушения конструкцию.
В качестве протектора
для стальных
конструкций обычно
используют
алюминий, цинк,
магний и их сплавы.
Разрушение
цинковых
накладок на
корпусе корабля.
ПРОТЕКТОРЫ
13
14.
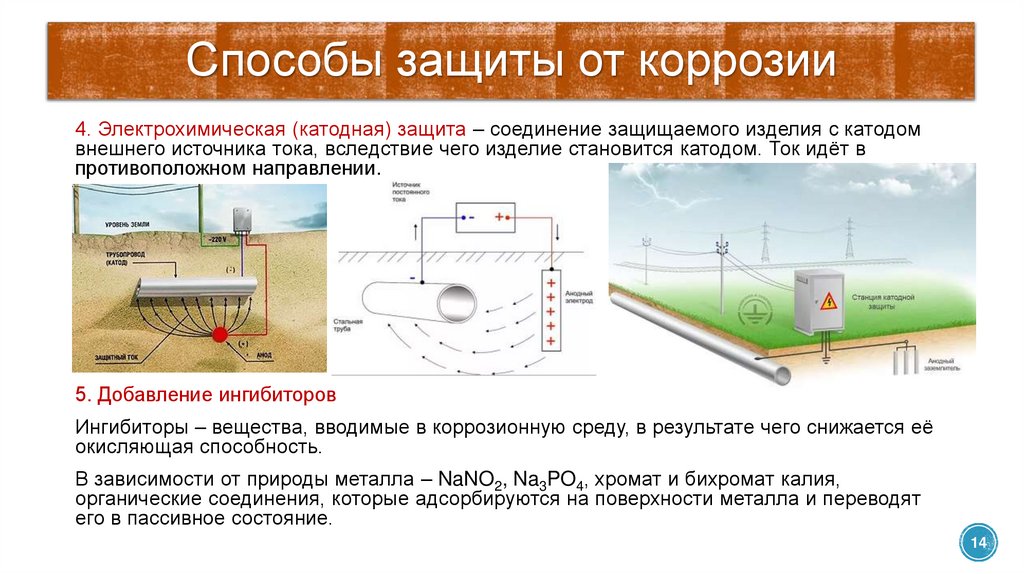
Способы защиты от коррозии4. Электрохимическая (катодная) защита – соединение защищаемого изделия с катодом
внешнего источника тока, вследствие чего изделие становится катодом. Ток идёт в
противоположном направлении.
5. Добавление ингибиторов
Ингибиторы – вещества, вводимые в коррозионную среду, в результате чего снижается её
окисляющая способность.
В зависимости от природы металла – NaNO2, Na3PO4, хромат и бихромат калия,
органические соединения, которые адсорбируются на поверхности металла и переводят
его в пассивное состояние.
14
15.
Задания:1. Стоматологи не рекомендуют рядом
со стальной коронкой (Fе) ставить
золотую (Аu). Объясните их позицию с
точки зрения протекающих процессов.
2. Как будет протекать процесс коррозии в том
случае, если железную водосточную трубу прибить к
дому алюминиевыми гвоздями?
15














 chemistry
chemistry








