Similar presentations:
Газовые законы
1. Тема. Газовые законы
23.12.2022Тема. Газовые законы
2. Изопроцессы в газах
Процессы, протекающие при неизменном значенииодного из параметров, называют изопроцессами.
Рассмотрим следующие изопроцессы:
Название
процесса
Изотермический
процесс
Изобарный
процесс
Изохорный
процесс
Постоянная
величина
T = const
p = const
V = const
3. (Название процесса)
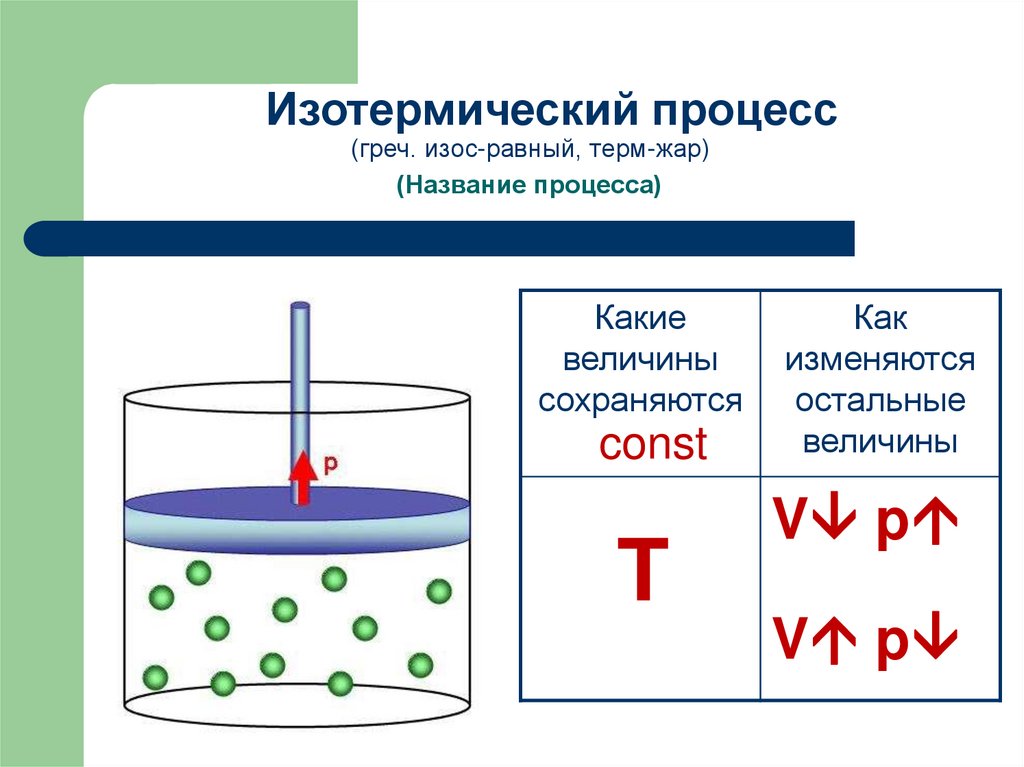
Изотермический процесс(греч. изос-равный, терм-жар)
(Название процесса)
Какие
величины
сохраняются
const
T
Как
изменяются
остальные
величины
V p
V p
4. Изотермический процесс -
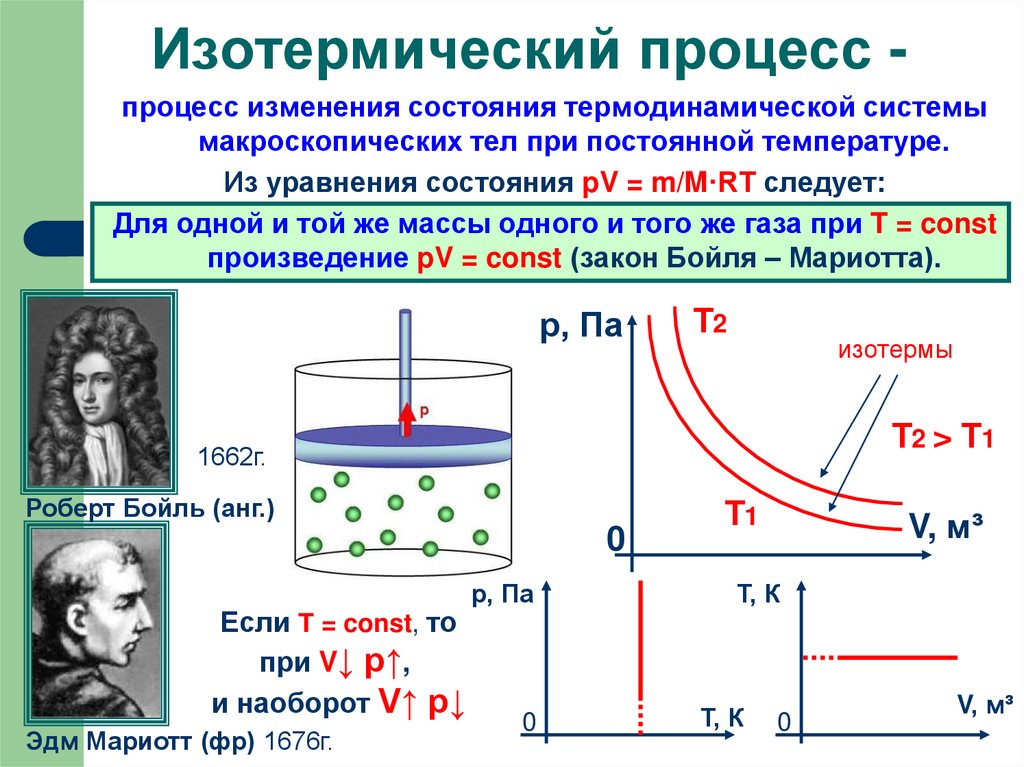
Изотермический процесс процесс изменения состояния термодинамической системымакроскопических тел при постоянной температуре.
Из уравнения состояния pV = m/M·RT следует:
Для одной и той же массы одного и того же газа при T = const
произведение pV = const (закон Бойля – Мариотта).
р, Па
Т2
изотермы
Т2 > Т1
1662г.
Роберт Бойль (анг.)
0
Если T = const, то
при V↓ p↑,
и наоборот V↑ p↓
Эдм Мариотт (фр) 1676г.
р, Па
0
Т1
V, м³
Т, К
Т, К
0
V, м³
5. (Название процесса)
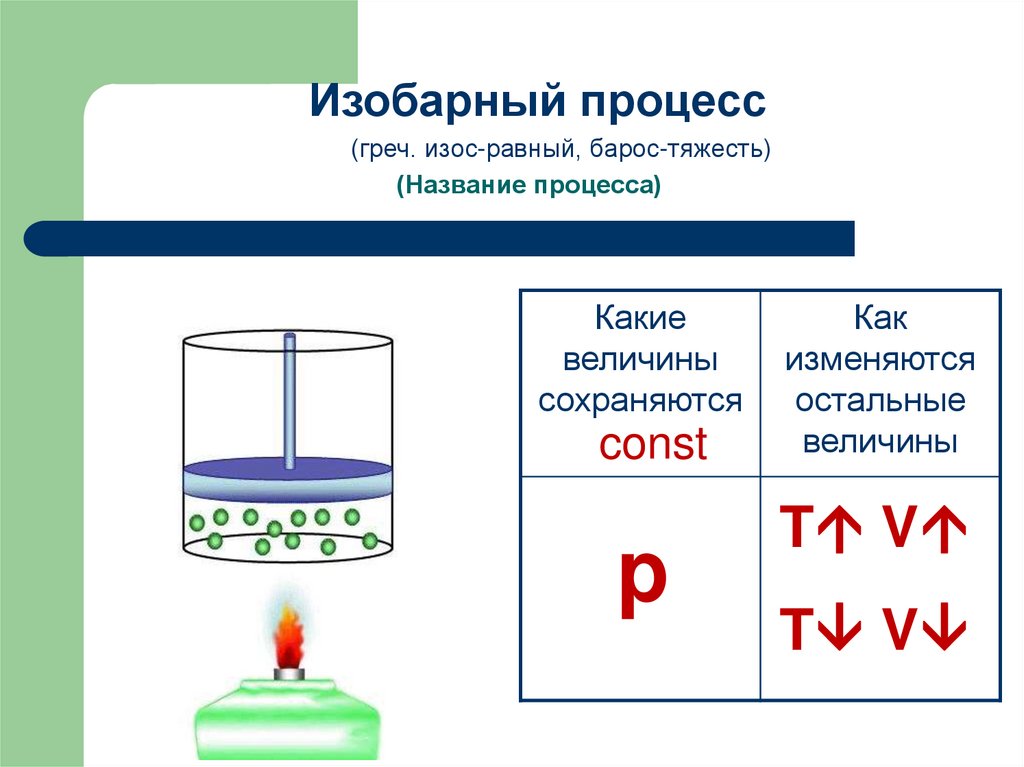
Изобарный процесс(греч. изос-равный, барос-тяжесть)
(Название процесса)
Какие
величины
сохраняются
const
p
Как
изменяются
остальные
величины
T V
T V
6. Изобарный процесс -
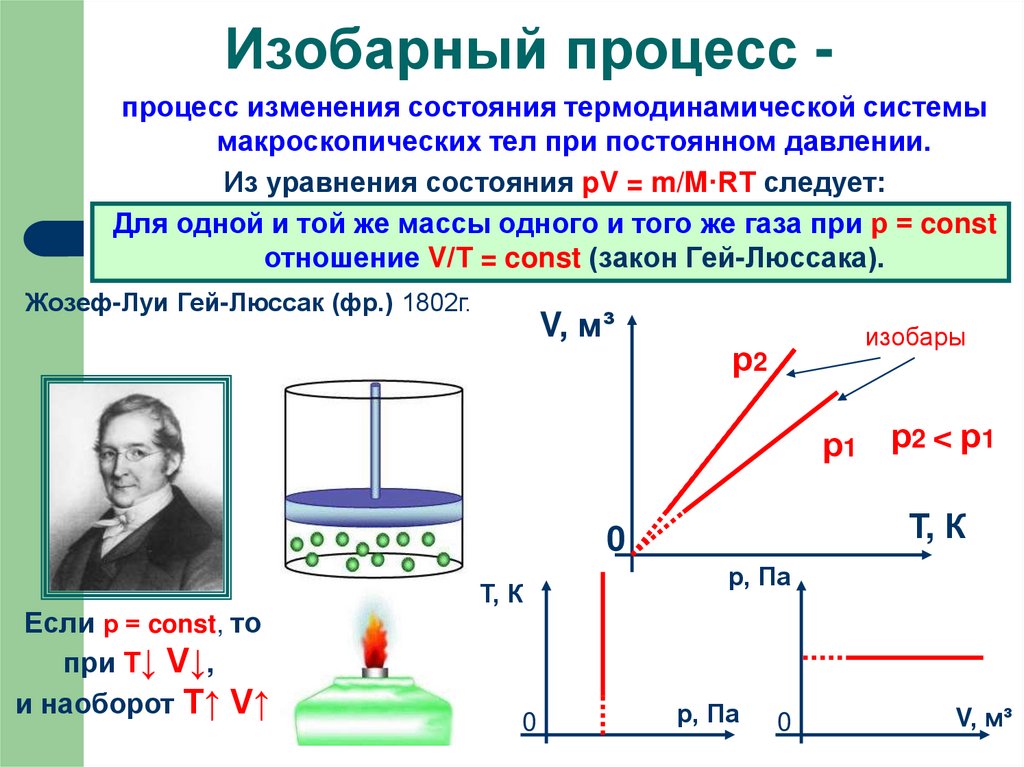
Изобарный процесс процесс изменения состояния термодинамической системымакроскопических тел при постоянном давлении.
Из уравнения состояния pV = m/M·RT следует:
Для одной и той же массы одного и того же газа при р = const
отношение V/Т = const (закон Гей-Люссака).
Жозеф-Луи Гей-Люссак (фр.) 1802г.
V, м³
изобары
р2
р1 р2 < р1
Т, К
0
Если р = const, то
при Т↓ V↓,
и наоборот T↑ V↑
Т, К
0
р, Па
р, Па
0
V, м³
7. (Название процесса)
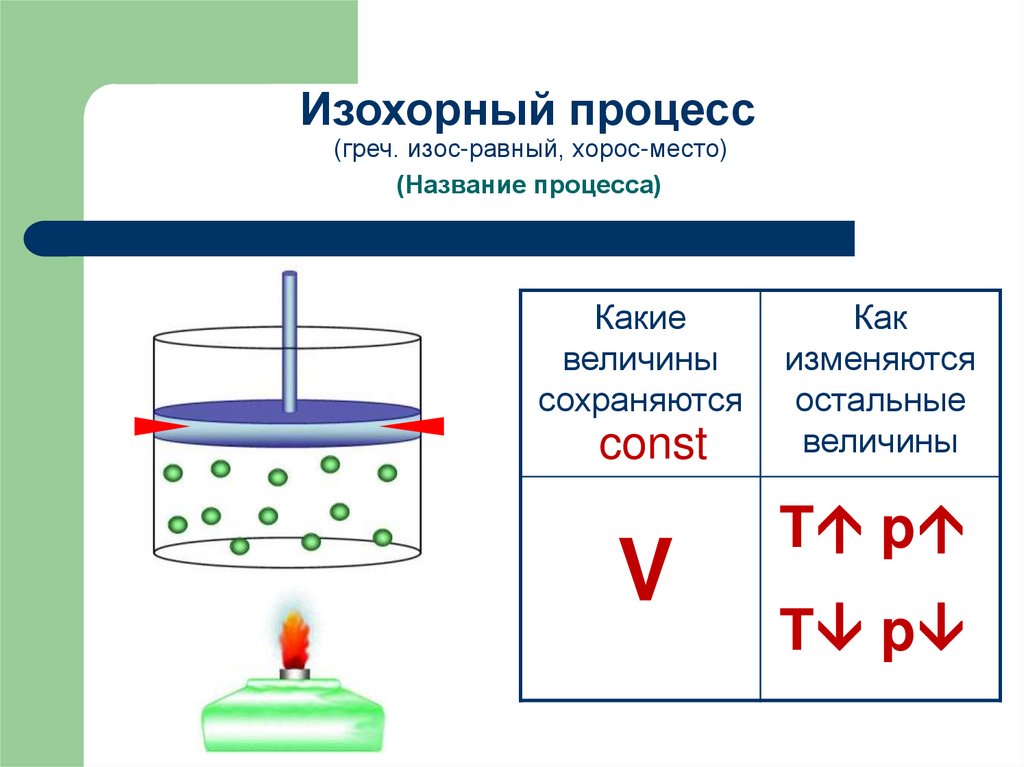
Изохорный процесс(греч. изос-равный, хорос-место)
(Название процесса)
Какие
величины
сохраняются
const
V
Как
изменяются
остальные
величины
T p
T p
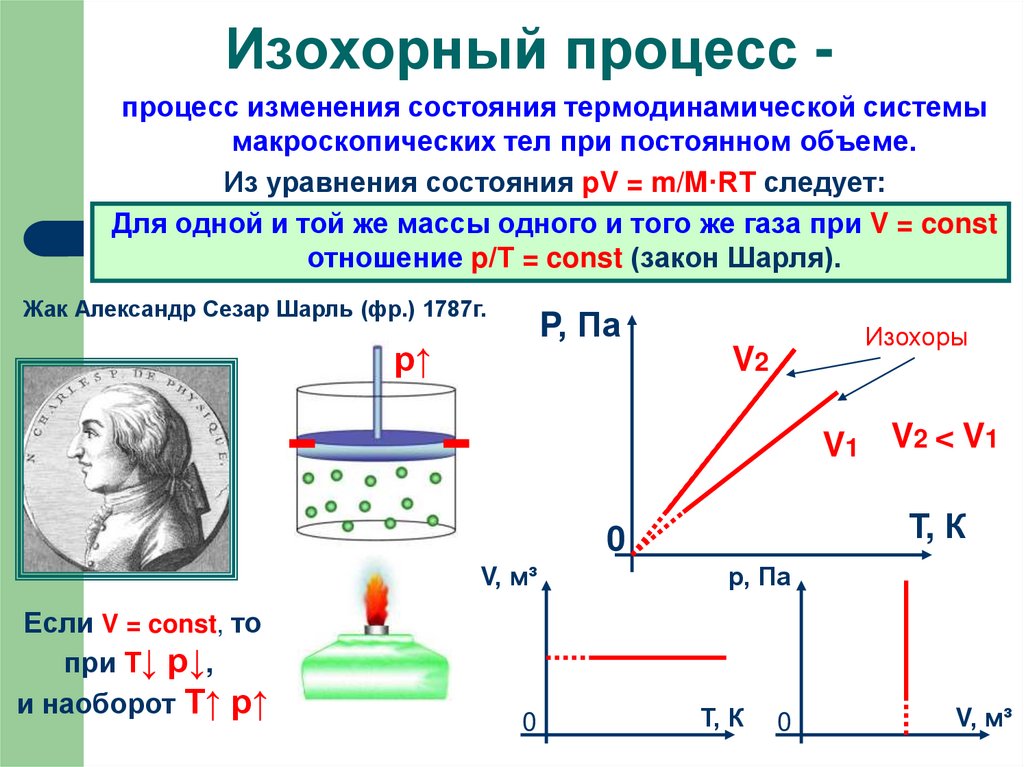
8. Изохорный процесс -
Изохорный процесс процесс изменения состояния термодинамической системымакроскопических тел при постоянном объеме.
Из уравнения состояния pV = m/M·RT следует:
Для одной и той же массы одного и того же газа при V = const
отношение p/Т = const (закон Шарля).
Жак Александр Сезар Шарль (фр.) 1787г.
P, Па
р↑
Изохоры
V2
V1 V2 < V1
Т, К
0
V, м³
Если V = const, то
при Т↓ p↓,
и наоборот T↑ p↑
0
р, Па
Т, К
0
V, м³
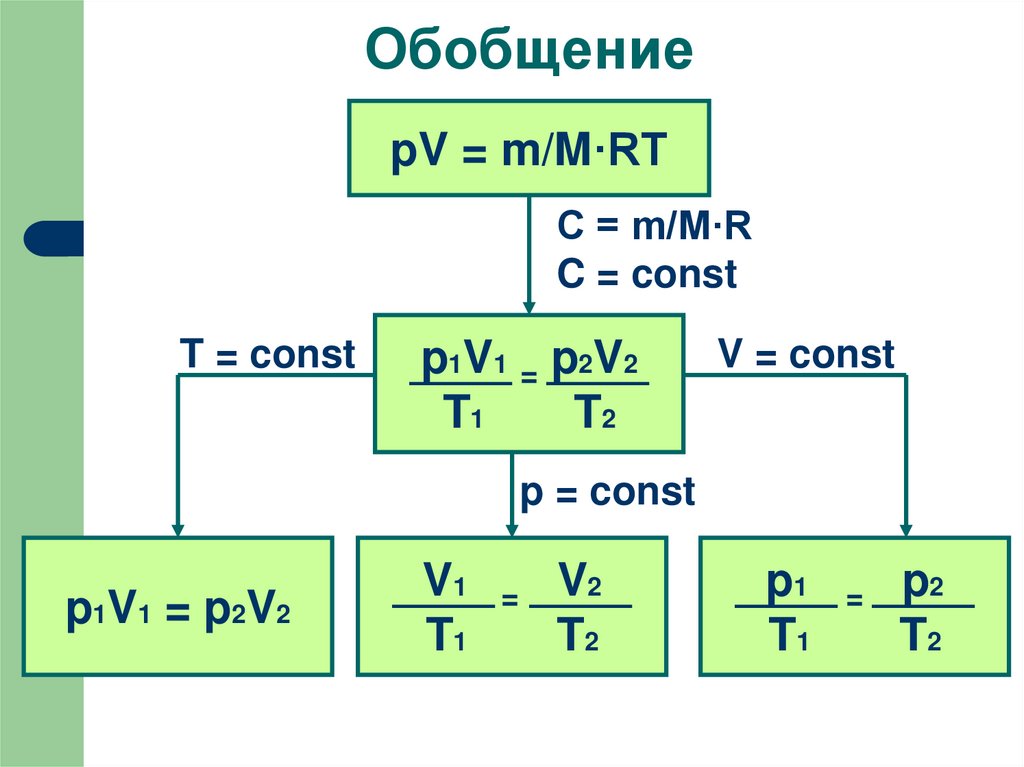
9. Обобщение
pV = m/M·RTC = m/M·R
C = const
T = const
p1V1 = p2V2
T1
T2
V = const
p = const
p1V1 = p2V2
V1
T1
=
V2
T2
p1
T1
=
p2
T2
10. Повторение
1.2.
3.
4.
5.
6.
7.
8.
9.
10.
11.
12.
13.
Перечислите основные положения МКТ.
Дайте определение относительной молекулярной
массы.
Что такое количество вещества?
Что такое молярная масса?
Какое движение называют броуновским?
Какой газ называют идеальным в МКТ?
Дайте определение и приведите примеры
макроскопических параметров.
Дайте определение и приведите примеры
микроскопических параметров.
Запишите основное уравнение МКТ. Чем оно
замечательно?
Что такое температура? В каких единицах она
измеряется?
Какое состояние системы называют тепловым
равновесием?
Запишите уравнение состояния идеального газа. Чьи
имена носит это уравнение и почему?
Какие макроскопические параметры используются в
уравнении Менделеева – Клапейрона?
11.
ДЕМО_2016_91
12.
9_СГ_060215В14
13.
9_СГ_060215В22
14.
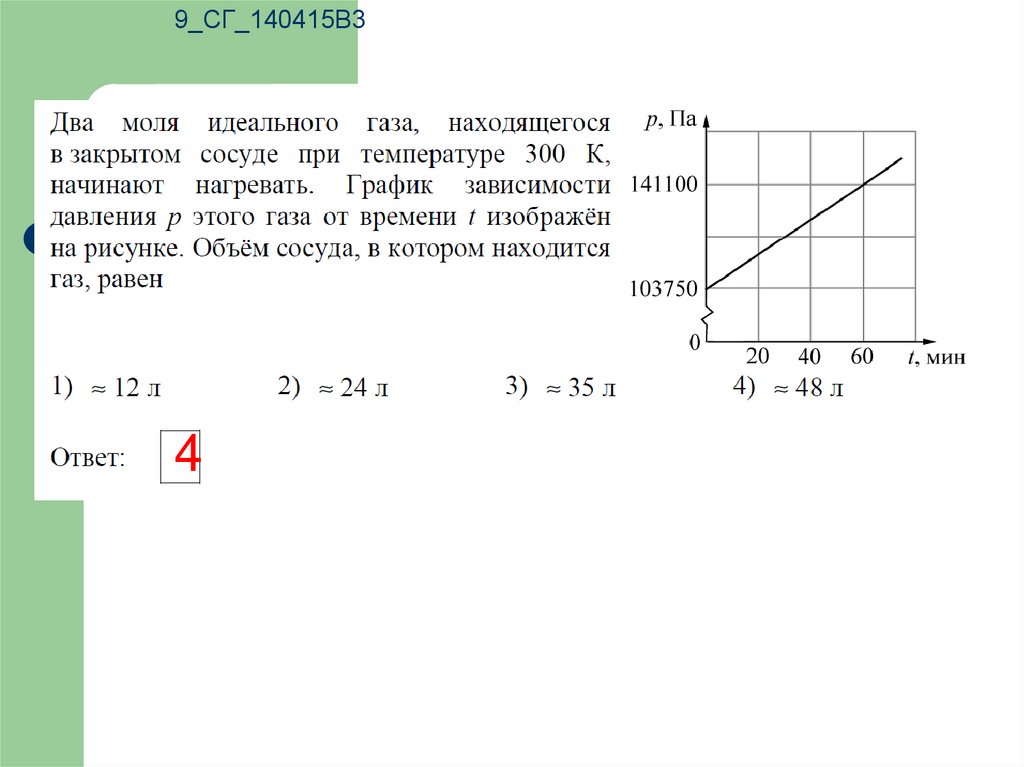
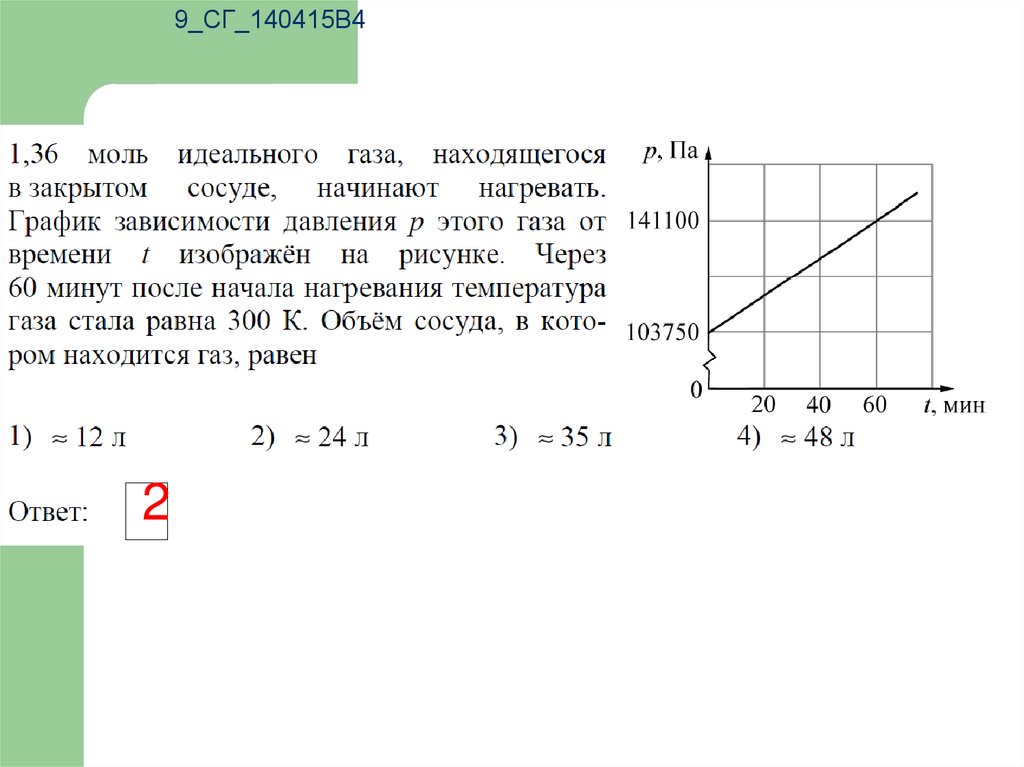
9_СГ_140415В34
15.
9_СГ_140415В42
16.
12_СГ_120515В113
17.
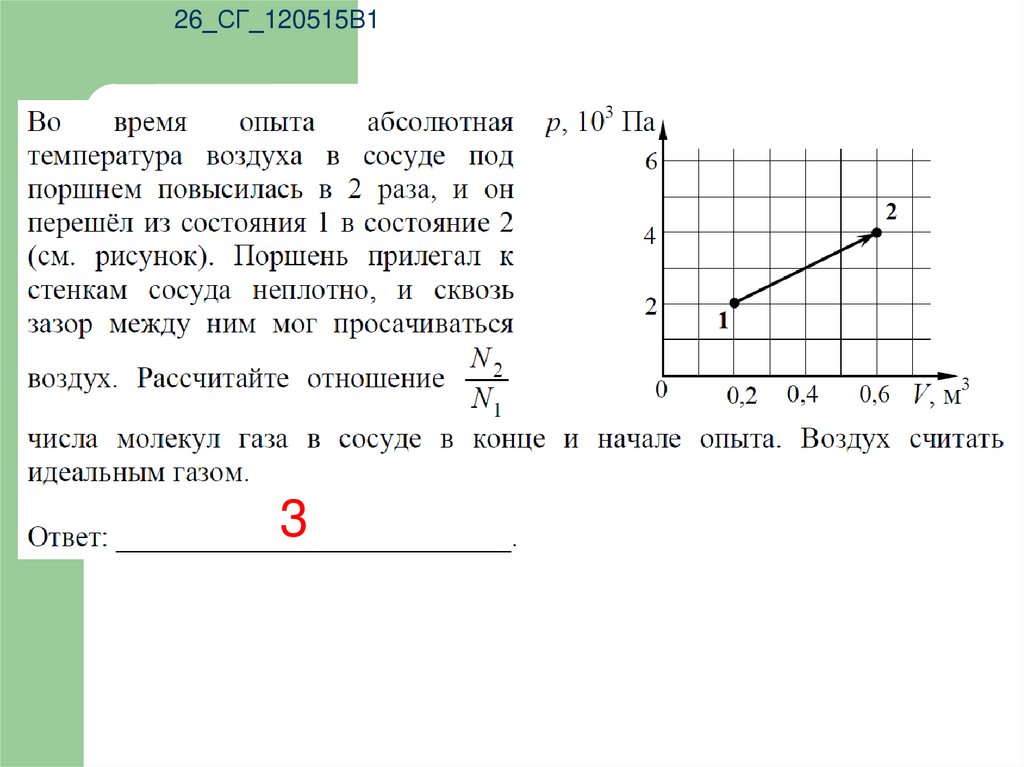
26_СГ_120515В13
18.
9_СГ_120515В21
19.
11_СГ_211215В323
20.
11_СГ_211215В433
21.
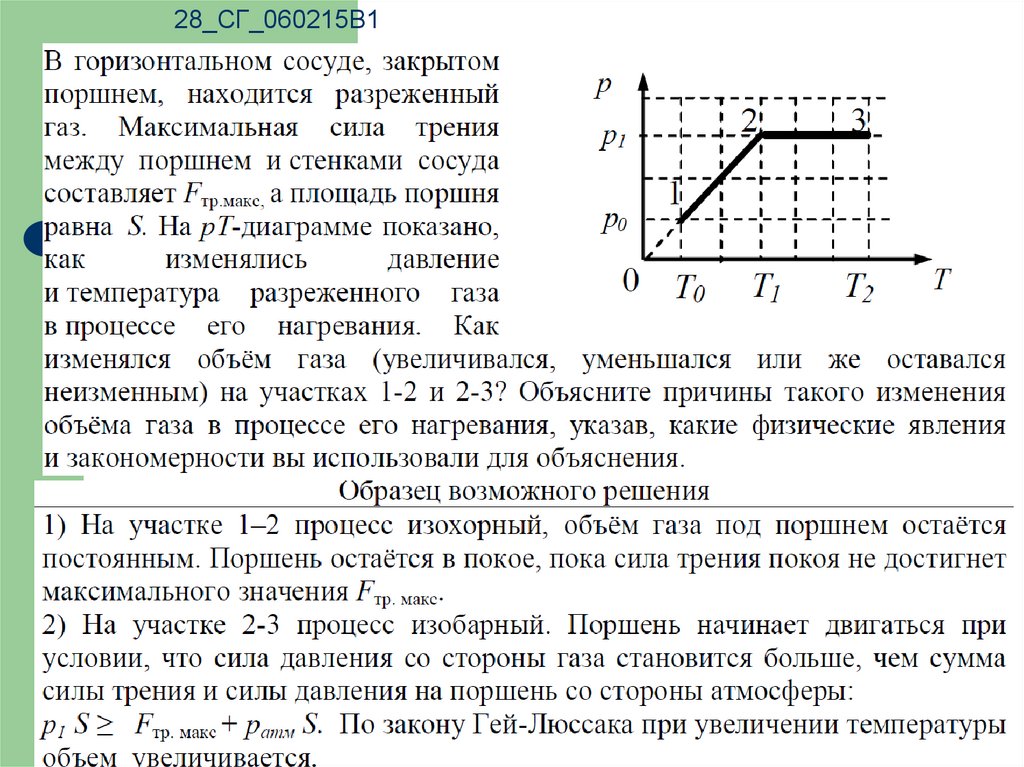
28_СГ_060215В122.
30_СГ_211215В330_СГ_211215В4













 physics
physics








