Similar presentations:
Дикарбоновые кислоты
1.
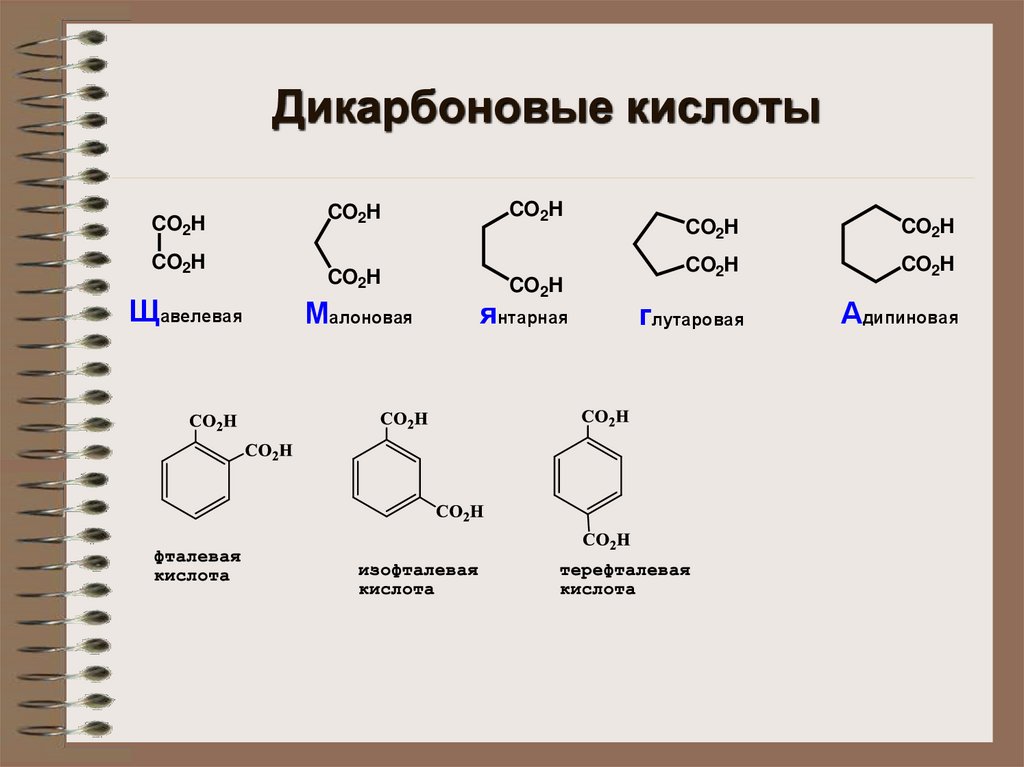
Дикарбоновые кислотыCO2H
CO2H
Щавелевая
CO2H
CO2H
Малоновая
CO2H
CO2H
янтарная
CO2H
CO2H
CO2H
CO2H
глутаровая
Адипиновая
2.
3.
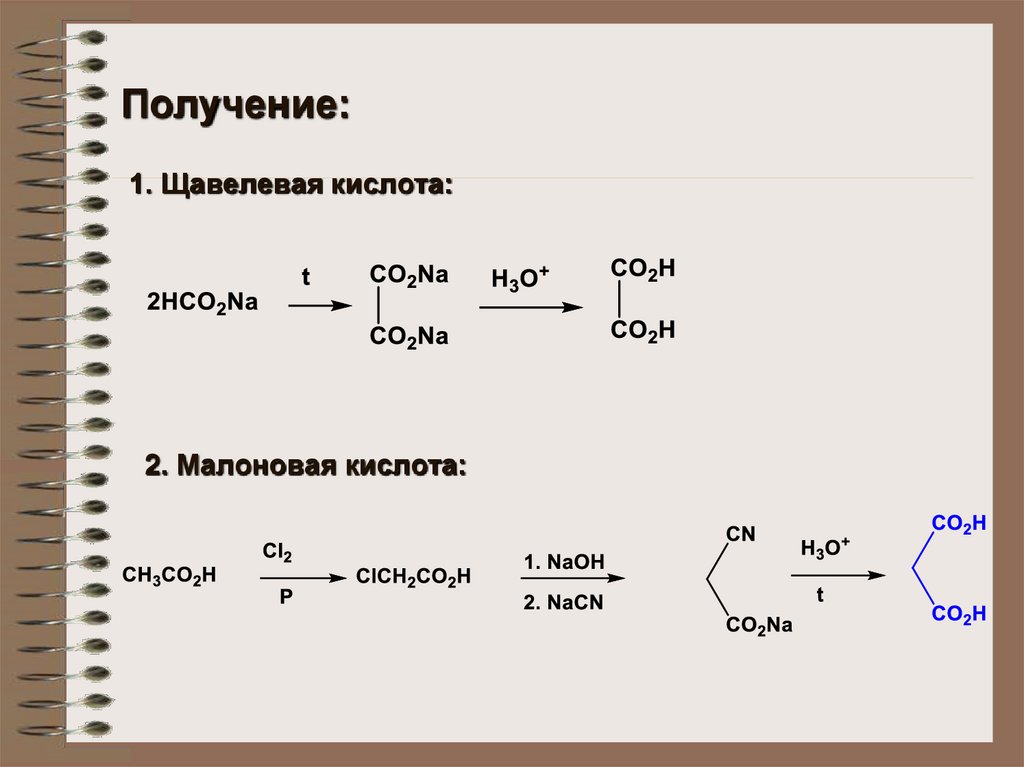
Получение:1. Щавелевая кислота:
2. Малоновая кислота:
4.
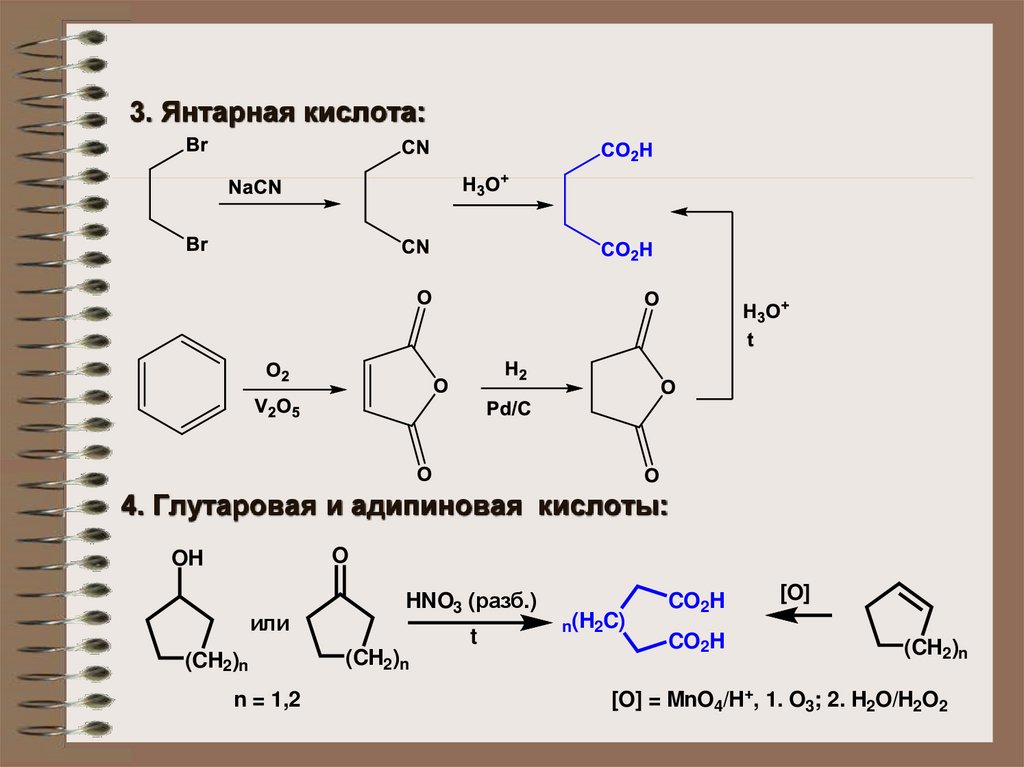
3. Янтарная кислота:4. Глутаровая и адипиновая кислоты:
O
OH
или
(CH2 )n
n = 1,2
HNO3 (разб.)
t
(CH2 )n
n(H2C)
CO2H
CO2H
[O]
(CH2 )n
[O] = MnO4/H+, 1. O3; 2. H2O/H2O2
5.
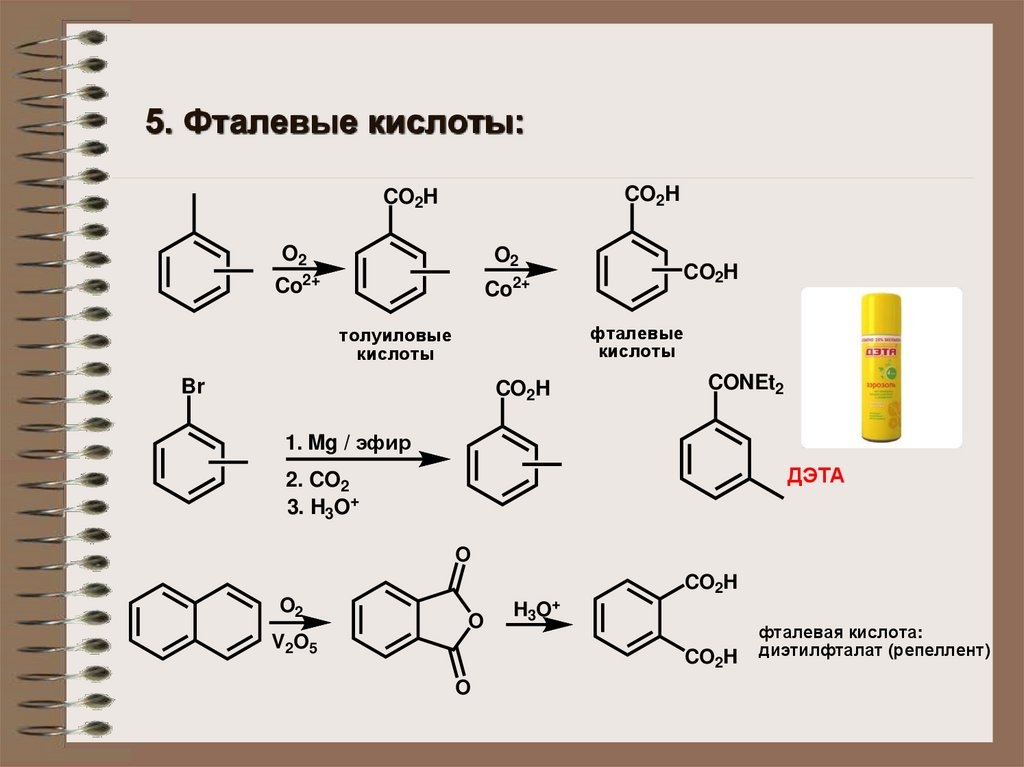
5. Фталевые кислоты:CO2H
CO2H
O2
O2
Co2+
Co2+
CO2H
фталевые
кислоты
толуиловые
кислоты
Br
CO2H
CONEt2
1. Mg / эфир
ДЭТА
2. CO2
3. H3O+
O
CO2H
O2
O
V2O5
H3O+
CO2H
O
фталевая кислота:
диэтилфталат (репеллент)
6.
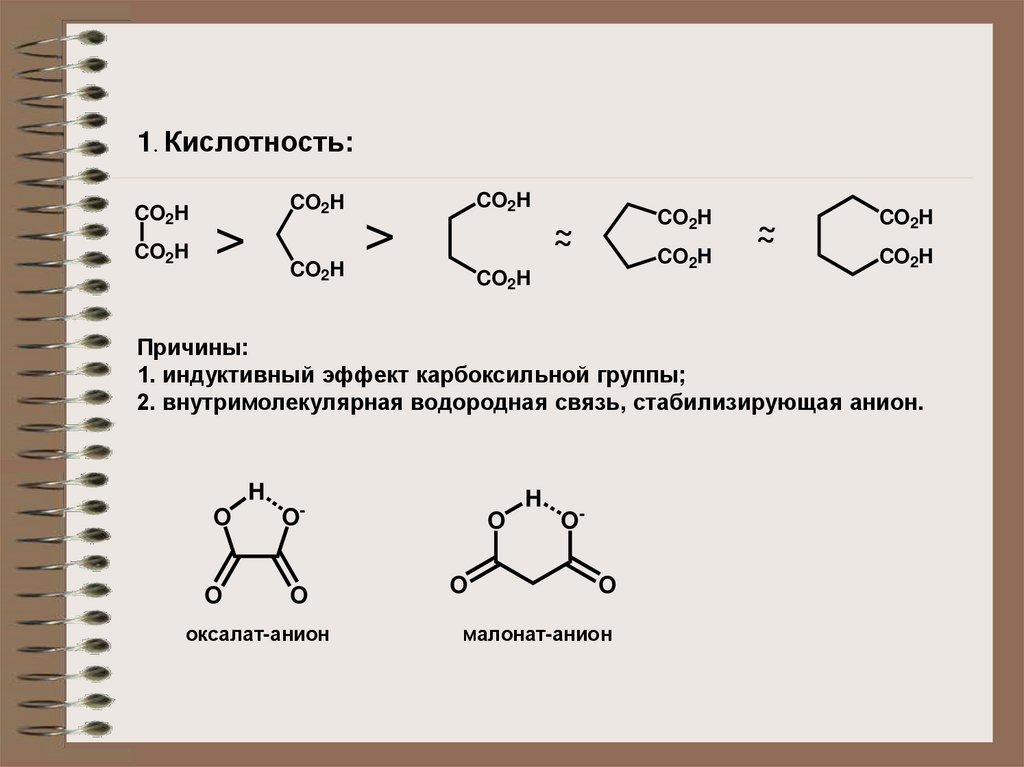
1. Кислотность:CO2H
CO2H
CO2H
>
CO2H
>
CO2H
~
~
CO2H
CO2H
CO2H
~
~
CO2H
CO2H
Причины:
1. индуктивный эффект карбоксильной группы;
2. внутримолекулярная водородная связь, стабилизирующая анион.
H
O
O-
O
O
оксалат-анион
H
O
O
OO
малонат-анион
7.
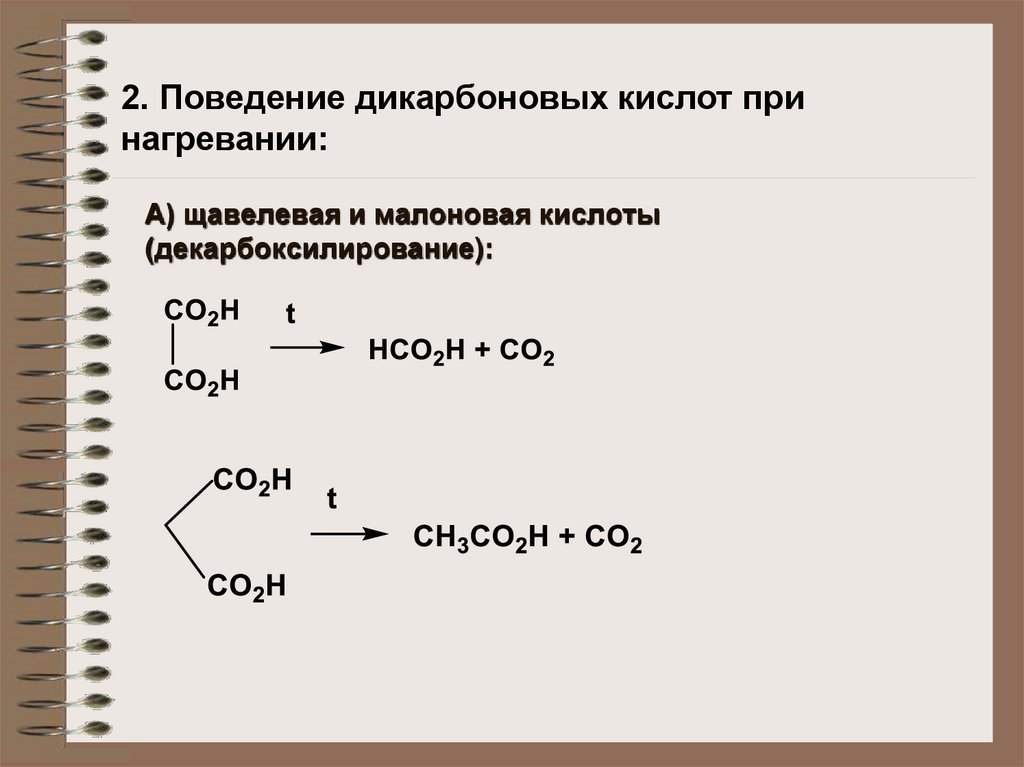
2. Поведение дикарбоновых кислот принагревании:
А) щавелевая и малоновая кислоты
(декарбоксилирование):
8.
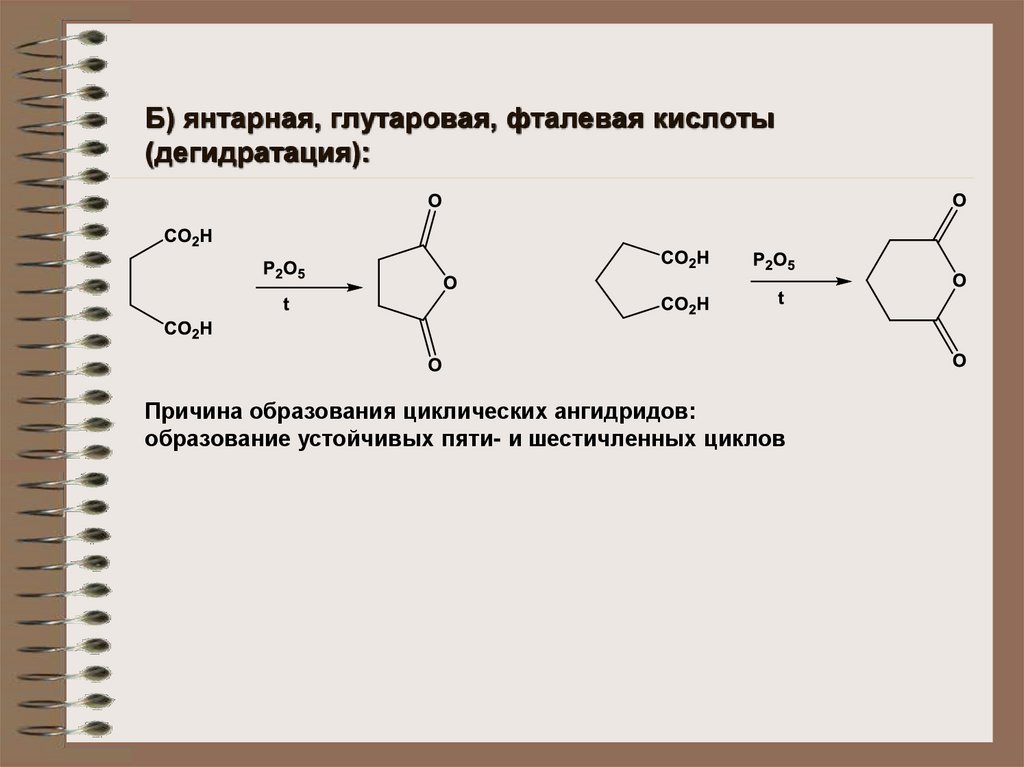
Б) янтарная, глутаровая, фталевая кислоты(дегидратация):
Причина образования циклических ангидридов:
образование устойчивых пяти- и шестичленных циклов
9.
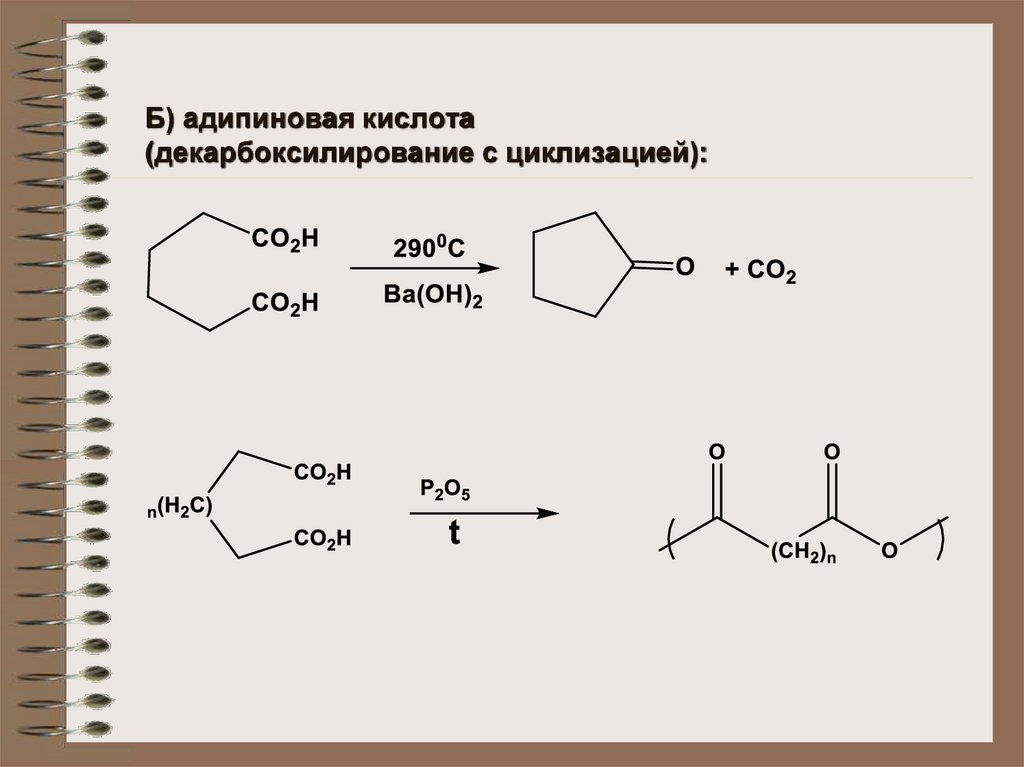
Б) адипиновая кислота(декарбоксилирование с циклизацией):
10.
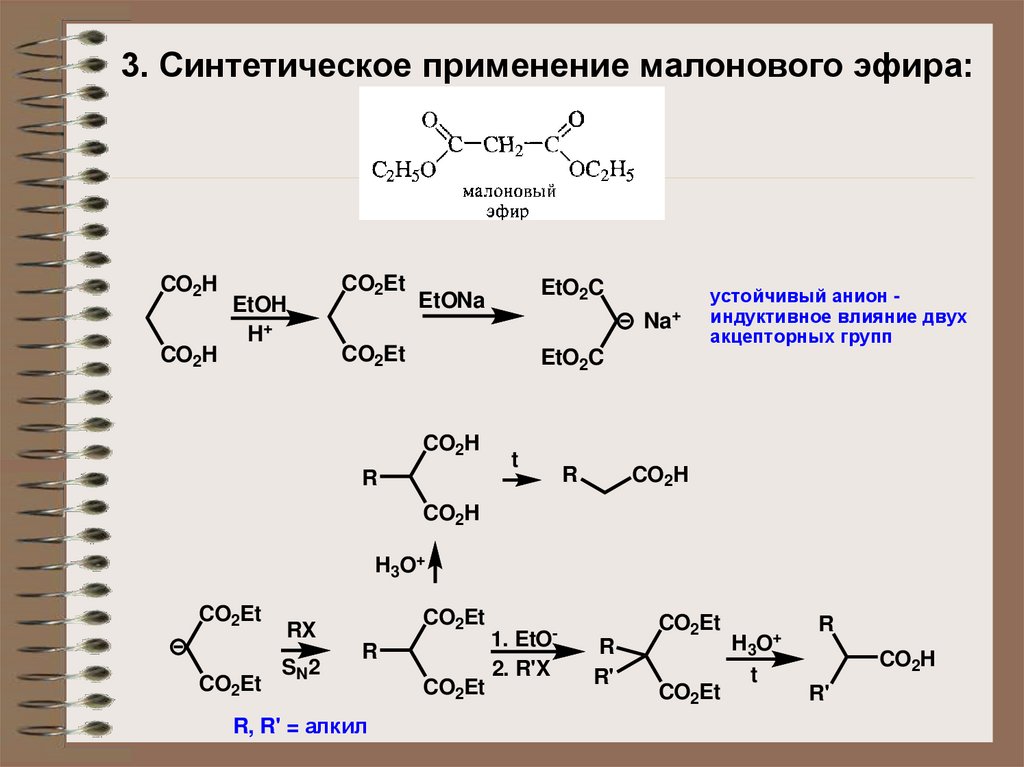
3. Синтетическое применение малонового эфира:CO2H
CO2Et
EtOH
H+
EtO2C
EtONa
+
Na
CO2Et
CO2H
устойчивый анион индуктивное влияние двух
акцепторных групп
EtO2C
CO2H
R
t
R
CO2H
CO2H
H3O+
CO2Et
CO2Et
CO2Et
RX
SN2
R
R, R' = алкил
CO2Et
1. EtO2. R'X
CO2Et
R
R'
CO2Et
H3O+
t
R
CO2H
R'
11.
CO2EtCO2Et
ClCH2CO2Et
EtO2C
CO2Et
CO2Et
H3O+
t
CO2H
CO2H
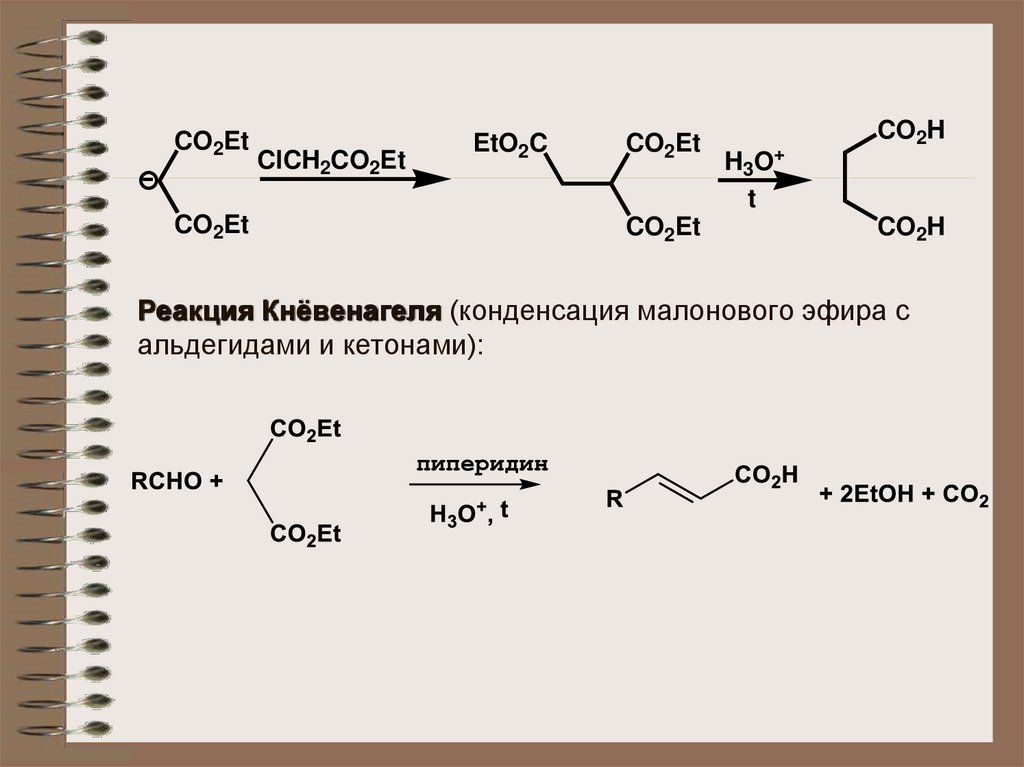
Реакция Кнёвенагеля (конденсация малонового эфира с
альдегидами и кетонами):
12.
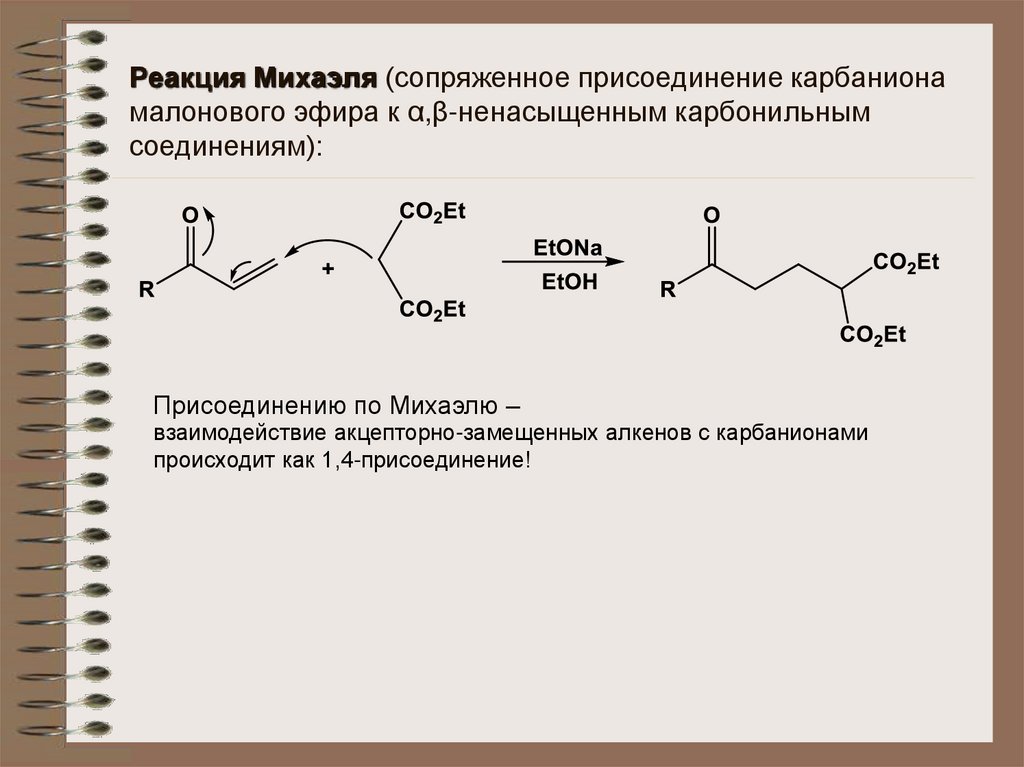
Реакция Михаэля (сопряженное присоединение карбанионамалонового эфира к α,β-ненасыщенным карбонильным
соединениям):
Присоединению по Михаэлю –
взаимодействие акцепторно-замещенных алкенов с карбанионами
происходит как 1,4-присоединение!
13.
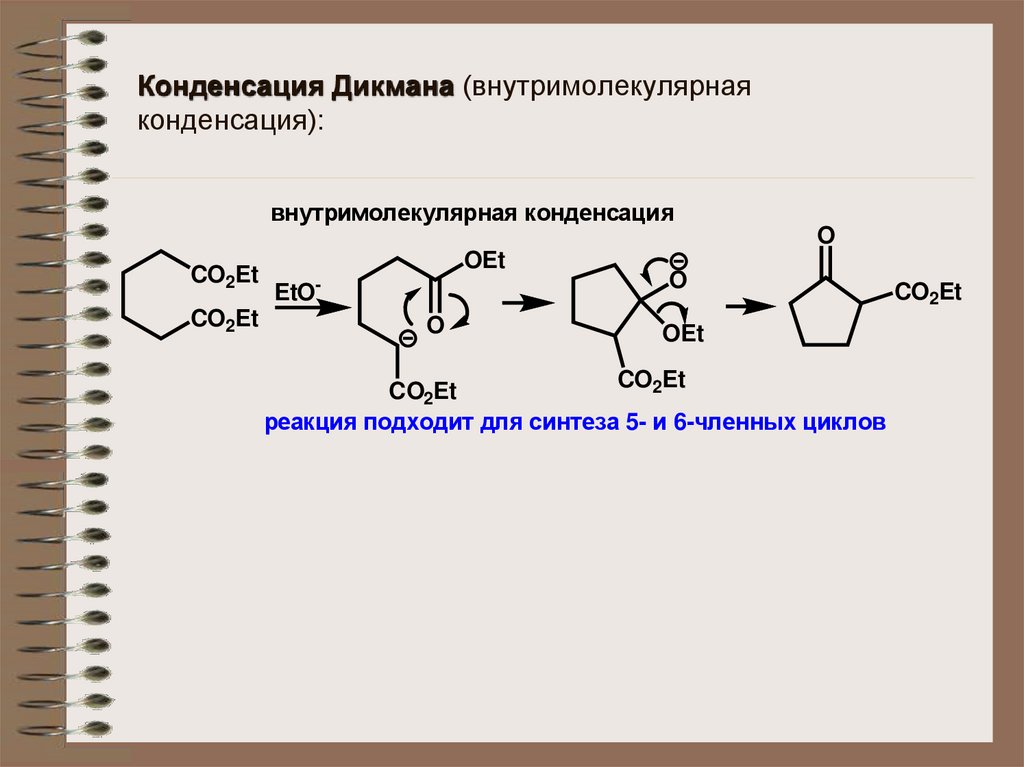
Конденсация Дикмана (внутримолекулярнаяконденсация):
внутримолекулярная конденсация
O
CO2Et
CO2Et
OEt
EtOO
O
OEt
CO2Et
CO2Et
реакция подходит для синтеза 5- и 6-членных циклов
CO2Et
14.
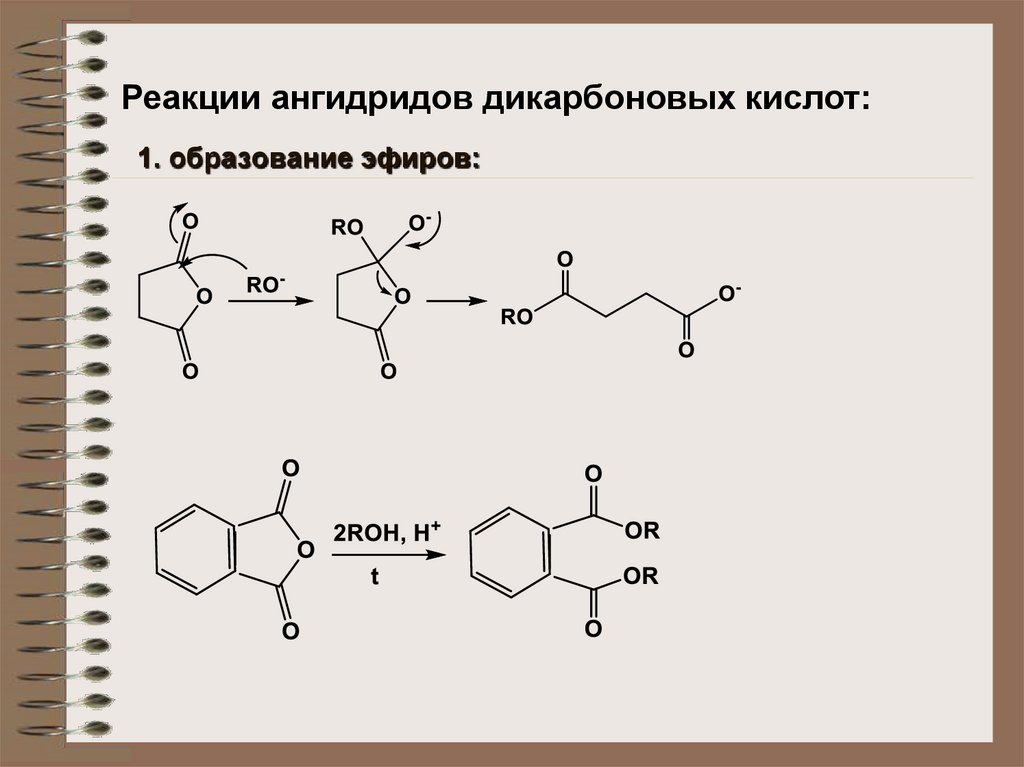
Реакции ангидридов дикарбоновых кислот:1. образование эфиров:
15.
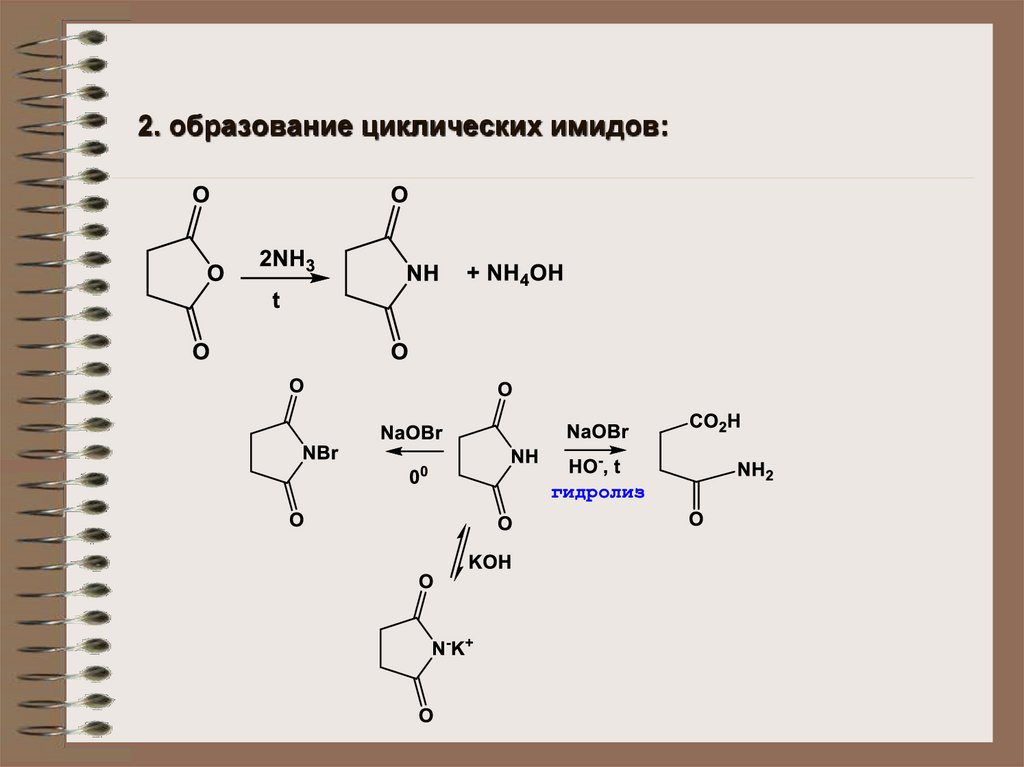
2. образование циклических имидов:16.
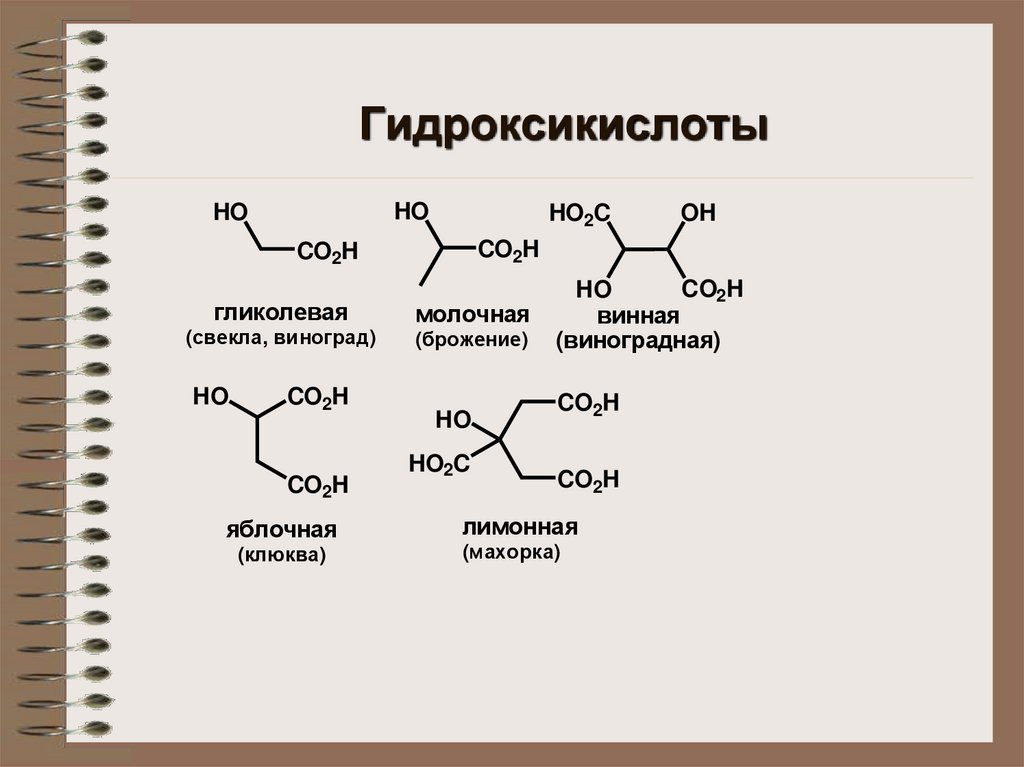
ГидроксикислотыHO
HO
HO2C
CO2H
CO2H
гликолевая
(свекла, виноград)
HO
CO2H
CO2H
OH
молочная
(брожение)
HO
HO2C
CO2H
HO
винная
(виноградная)
CO2H
CO2H
яблочная
лимонная
(клюква)
(махорка)
17.
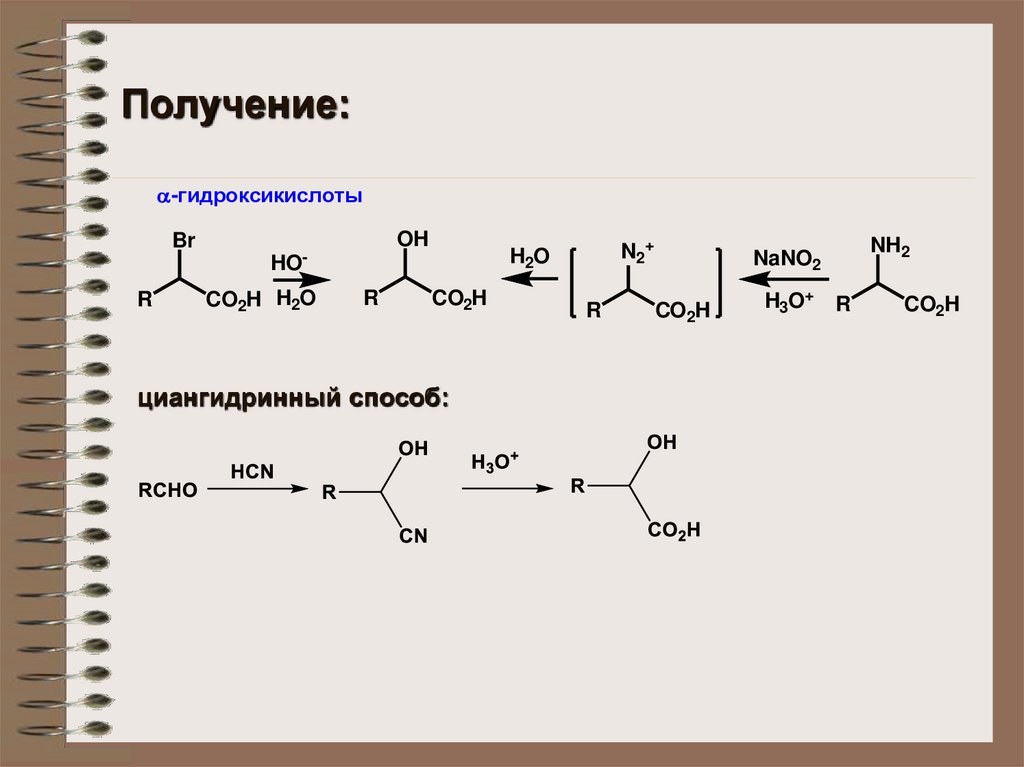
Получение:-гидроксикислоты
Br
R
OH
CO2H H2O
R
N2+
H2O
HOCO2H
циангидринный способ:
R
NH2
NaNO2
CO2H
H3O+
R
CO2H
18.
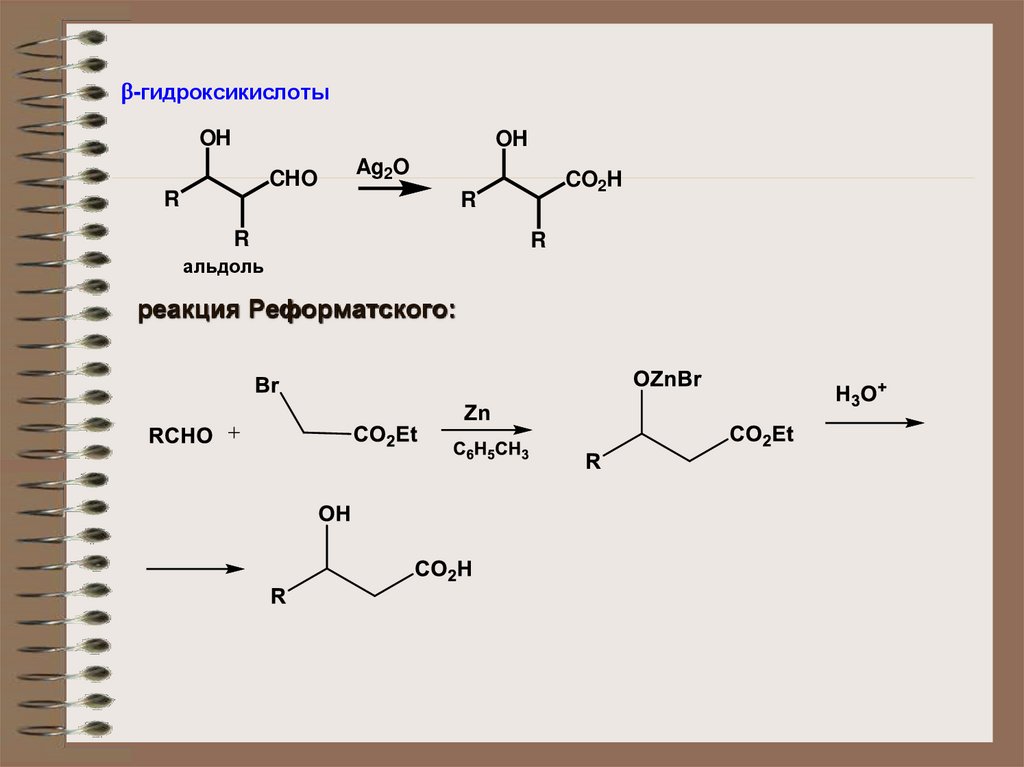
-гидроксикислотыOH
OH
CHO
Ag2O
R
CO2H
R
R
альдоль
реакция Реформатского:
R
19.
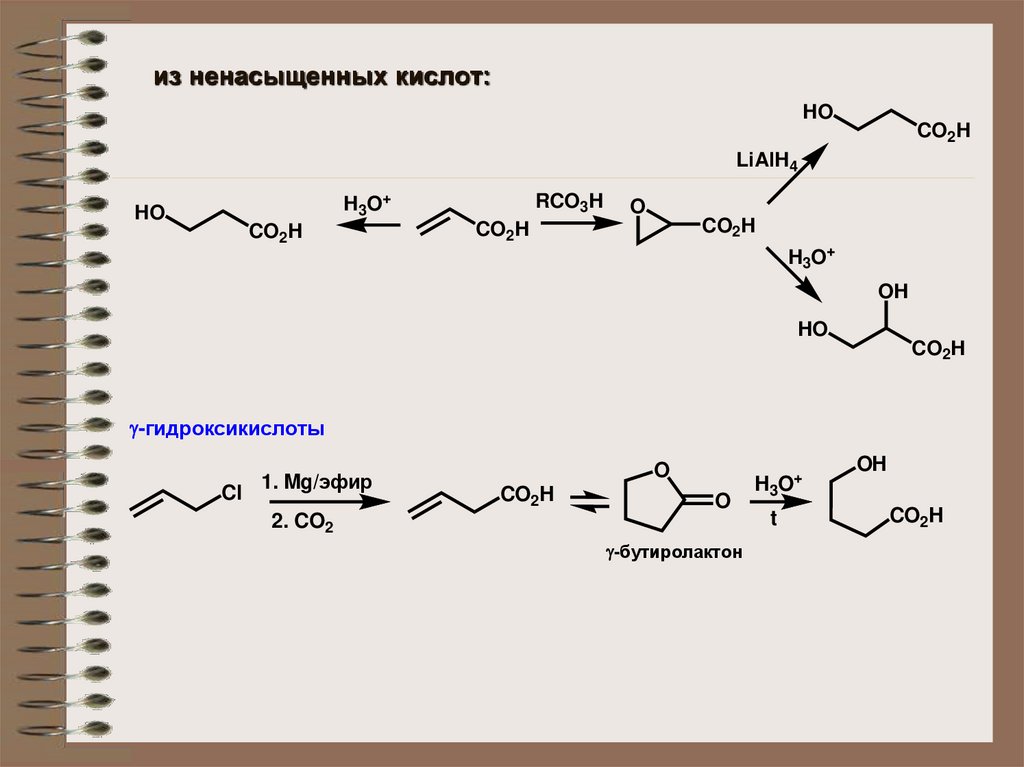
из ненасыщенных кислот:HO
CO2H
LiAlH4
H3O+
HO
CO2H
RCO3H
O
CO2H
CO2H
H3O+
OH
HO
CO2H
-гидроксикислоты
Cl
1. Mg/эфир
O
CO2H
+
O
2. CO2
-бутиролактон
OH
H3O
t
CO2H
20.
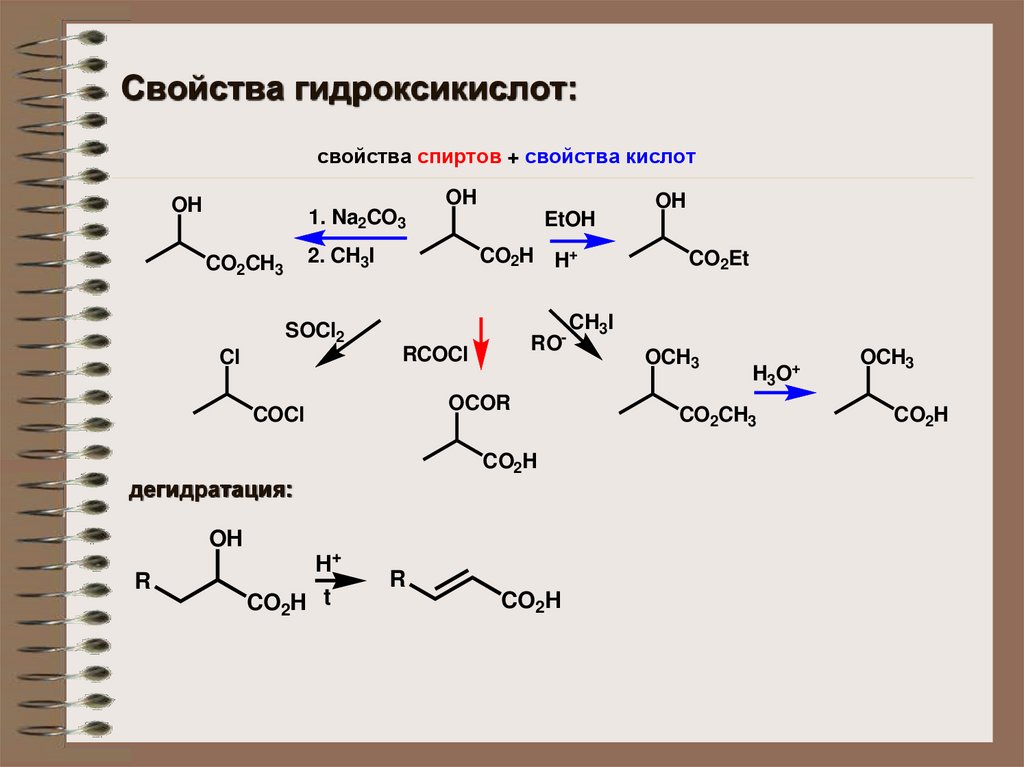
Свойства гидроксикислот:свойства спиртов + свойства кислот
OH
OH
1. Na2CO3
EtOH
2. CH3I
CO2CH3
CO2H H+
SOCl2
-
RO
RCOCl
Cl
OCOR
COCl
CO2H
дегидратация:
OH
R
H+
CO2H t
R
CO2H
OH
CO2Et
CH3I
OCH3
H3O+
CO2CH3
OCH3
CO2H
21.
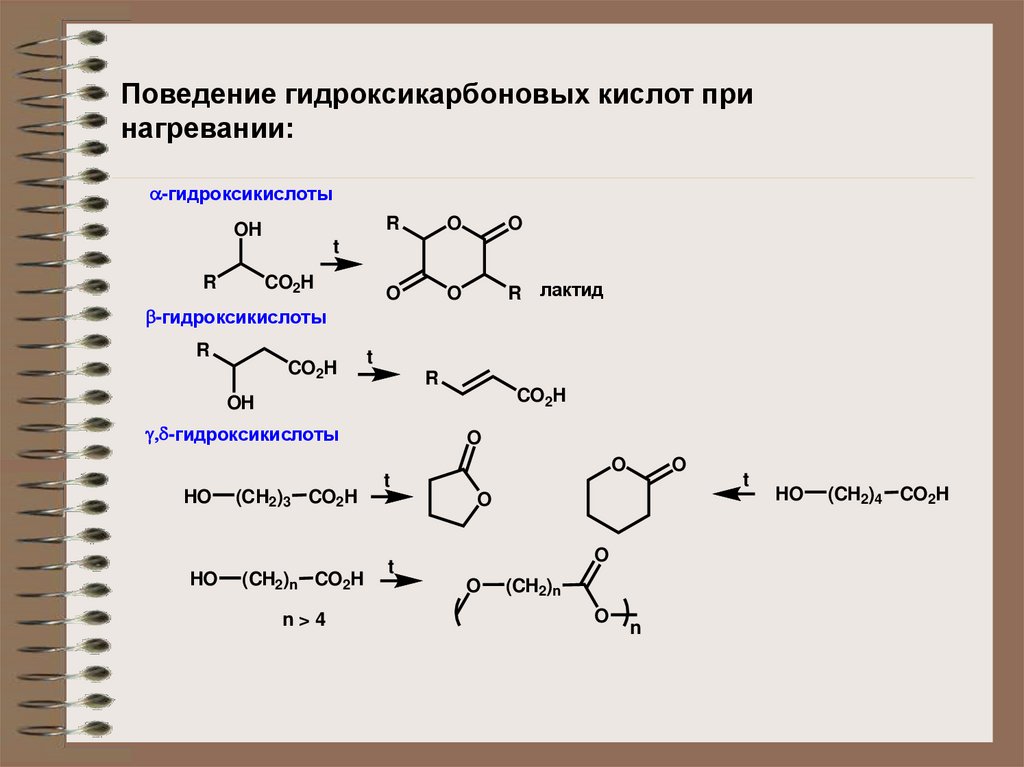
Поведение гидроксикарбоновых кислот принагревании:
-гидроксикислоты
OH
R
R
O
O
O
O
R лактид
t
CO2H
-гидроксикислоты
R
CO2H
t
R
CO2H
OH
-гидроксикислоты
HO
HO
(CH2)3 CO2H
(CH2)n CO2H
n>4
O
O
t
O
O
O
t
O
(CH2)n
O
n
t
HO
(CH2)4 CO2H

 chemistry
chemistry








