Similar presentations:
Химические свойства металлов
1.
Металлы — группа элементов, в виде простыхвеществ, обладающих характерными
металлическими свойствами.
2.
95 из1183.
Металлический блеск4.
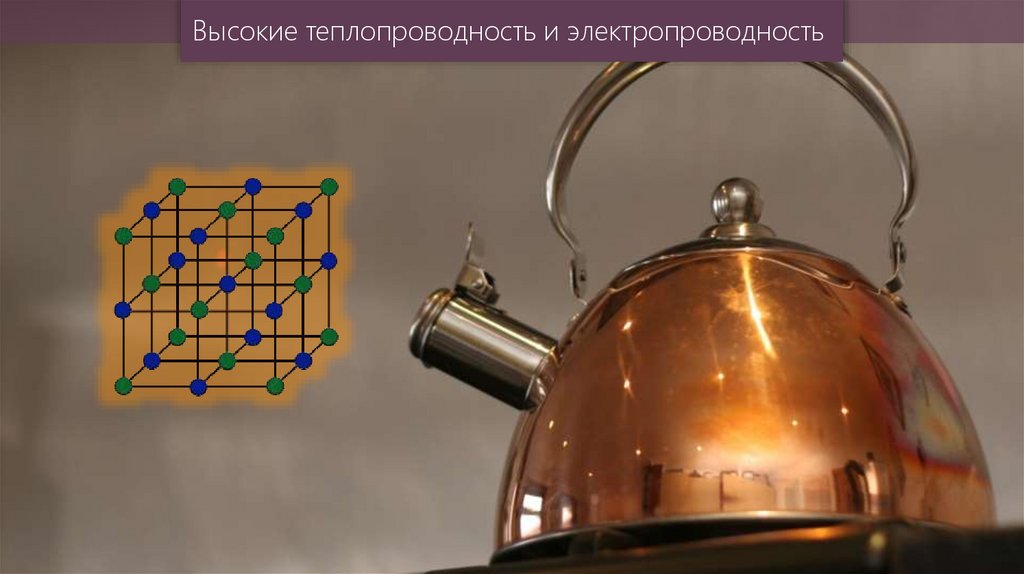
Высокие теплопроводность и электропроводность5.
Плотность и ковкость6.
Температура плавления38,9°С
температура
плавления ртути
Wilco Oelen
Ртуть (Hg)
7.
Температура плавления29°C
29,8°C
Dnn87
Цезий (Cs)
Aiyizo
Галлий (Ga)
8.
Температура плавления3410°С
температура плавления
вольфрама
Вольфрам (W)
9.
ТвёрдостьAlchemist-hp
Хром (Cr)
10.
ТвёрдостьDnn87
Калий (K)
Dnn87
Dnn87
Рубидий (Rb)
Цезий (Cs)
11.
Физические свойстваметаллов заключаются
в том, что они ковкие,
пластичные, тягучие
вещества, которые
способны проводить
тепло и электрический
ток.
12.
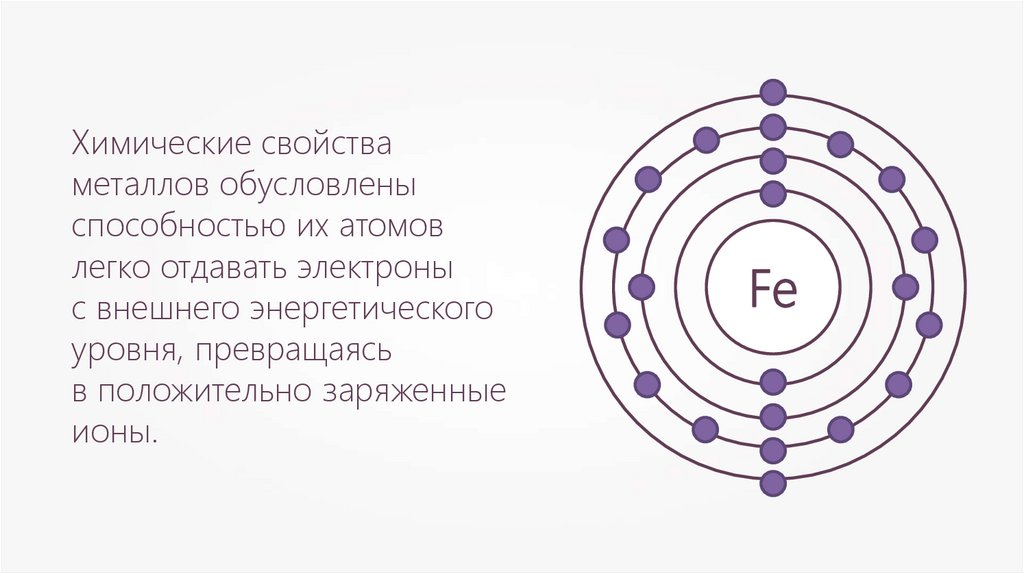
Химические свойстваметаллов обусловлены
способностью их атомов
легко отдавать электроны
с внешнего энергетического
уровня, превращаясь
в положительно заряженные
ионы.
Fe
13.
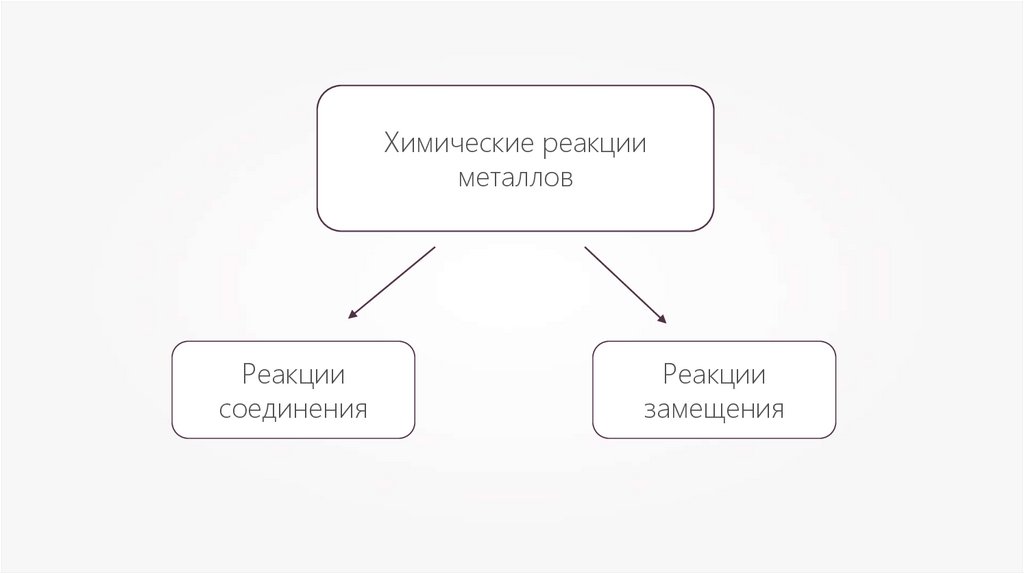
Химические реакцииметаллов
Реакции
соединения
Реакции
замещения
14.
A+BC=AC+BА
В
С
Реакции замещения — это такие реакции,
в результате которых атомы простого вещества
замещают атомы одного из химических
элементов в сложном веществе.
15.
A+B=ABА
В
Реакции соединения — это такие реакции,
в результате которых из одного или нескольких
веществ образуется одно сложное вещество.
16.
0n+
Me - ne → Me
—
В химических реакциях металлы способны
отдавать электроны, т.е. быть восстановителями,
проявлять в образовавшихся соединениях
только положительную степень окисления.
17.
Взаимодействие металлов с неметаллами0
0
t
+2
-2
2Mg + О2 = 2MgО
18.
19.
20.
Взаимодействие металлов с неметалламис образованием солей
0
0
+3 -1
2Al + 3Br2 = 2AlBr3
21.
Опыт взаимодействия алюминия с серойСера
(S)
Алюминиевая
пудра
(Al)
22.
Опыт взаимодействия алюминия с серойСульфид алюминия
(Al2S3)
23.
Взаимодействие алюминия с серой0
0
+3 -2
2Al + 3S = Al2S3
Окислитель
24.
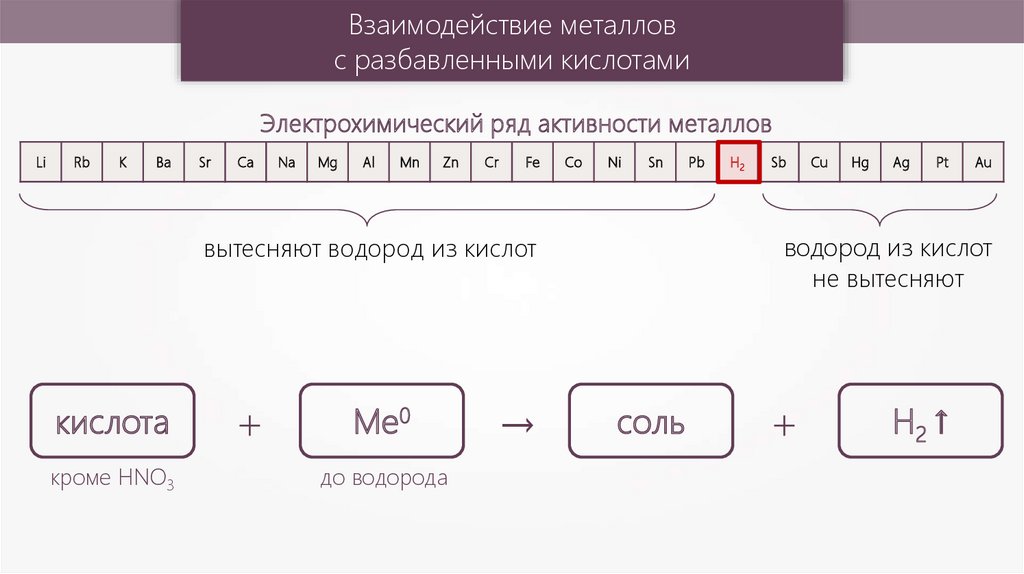
Взаимодействие металловс разбавленными кислотами
Электрохимический ряд активности металлов
Li
Rb
K
Ba
Sr
Ca
Na
Mg
Al
Mn
Zn
Cr
Fe
Co
Ni
Sn
кроме HNO3
+
Ме0
до водорода
→
H2
Sb
Cu
Hg
Ag
Pt
Au
водород из кислот
не вытесняют
вытесняют водород из кислот
кислота
Pb
соль
+
H2 ↑
25.
Взаимодействие цинка с соляной кислотой0
+1
+2
0
Zn + 2HCl = ZnCl2 + H2↑
Соляная
кислота
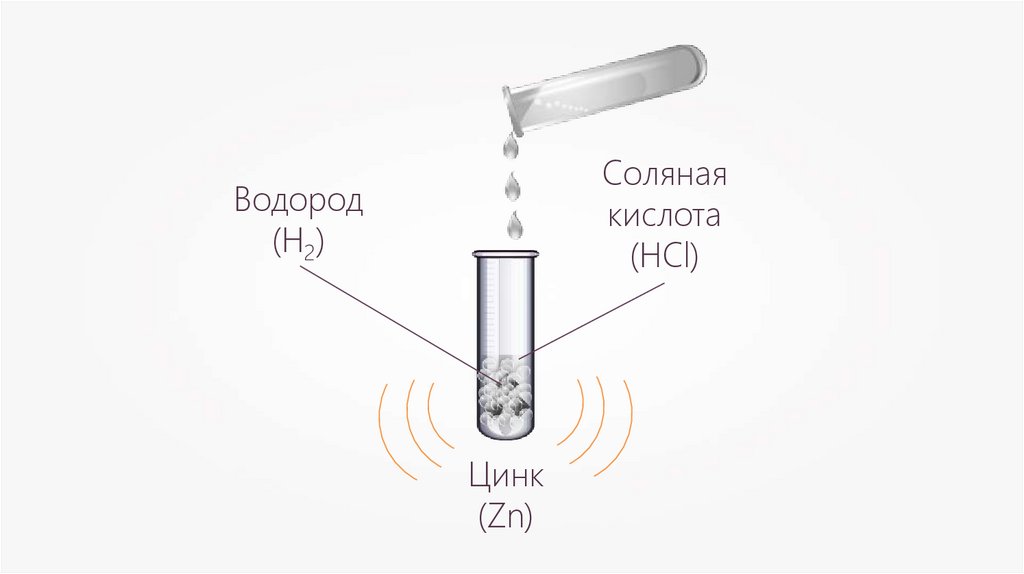
26.
Солянаякислота
(HCl)
Водород
(H2)
Цинк
(Zn)
27.
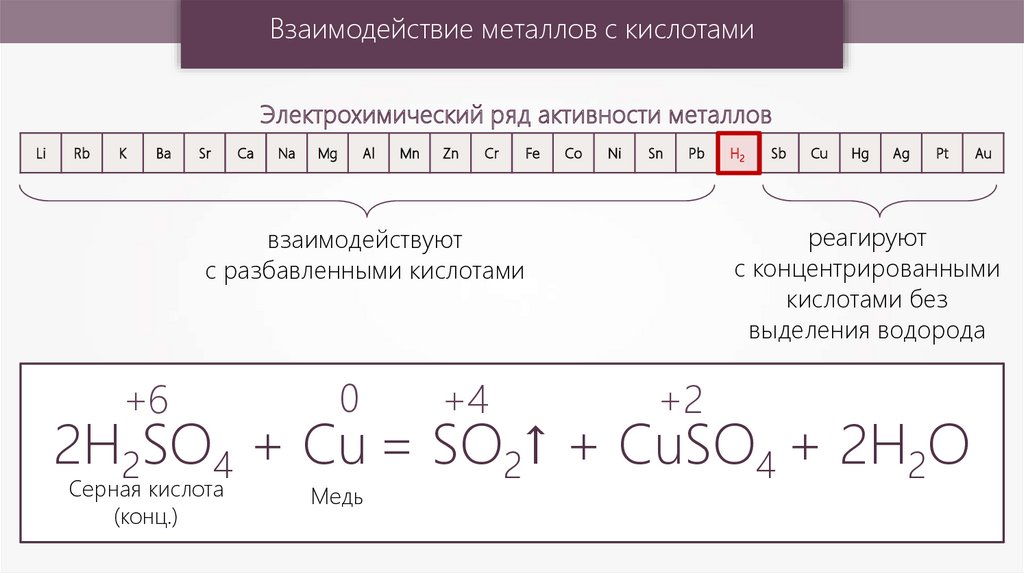
Взаимодействие металлов с кислотамиЭлектрохимический ряд активности металлов
Li
Rb
K
Ba
Sr
Ca
Na
Mg
Al
Mn
Zn
Cr
Fe
Co
Ni
Sn
Pb
0
+4
Sb
Cu
Hg
Ag
Pt
+2
2H2SO4 + Cu = SO2↑ + CuSO4 + 2H2O
Серная кислота
(конц.)
Медь
Au
реагируют
с концентрированными
кислотами без
выделения водорода
взаимодействуют
с разбавленными кислотами
+6
H2
28.
Взаимодействие металла с водойЭлектрохимический ряд активности металлов
Li
Rb
K
Ba
Sr
Ca
Na
Mg
Al
Mn
Zn
Cr
Fe
Co
Ni
Sn
активные металлы
0
Pb
H2
Sb
Cu
Hg
Ag
Pt
не вытесняют
водород
+1
+1
0
2Na + 2H2O → 2NaOH + H2↑
Восстановитель
Окислитель
Au
29.
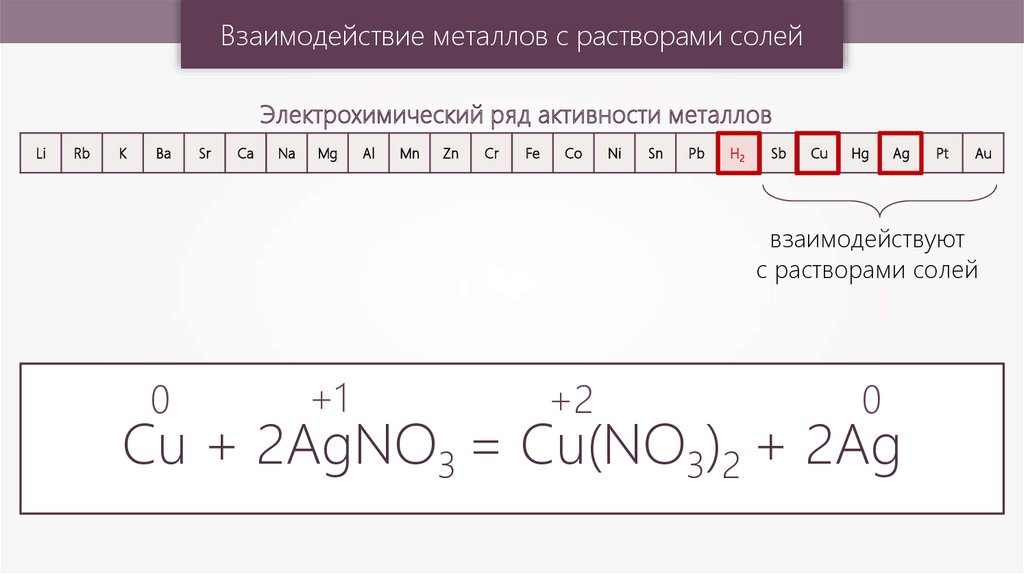
Взаимодействие металлов с растворами солейЭлектрохимический ряд активности металлов
Li
Rb
K
Ba
Sr
Ca
Na
Mg
Al
Mn
Zn
Cr
Fe
Co
Ni
Sn
Pb
H2
Sb
Cu
Hg
Ag
Pt
Au
взаимодействуют
с растворами солей
0
+1
+2
0
Cu + 2AgNO3 = Cu(NO3)2 + 2Ag
30.
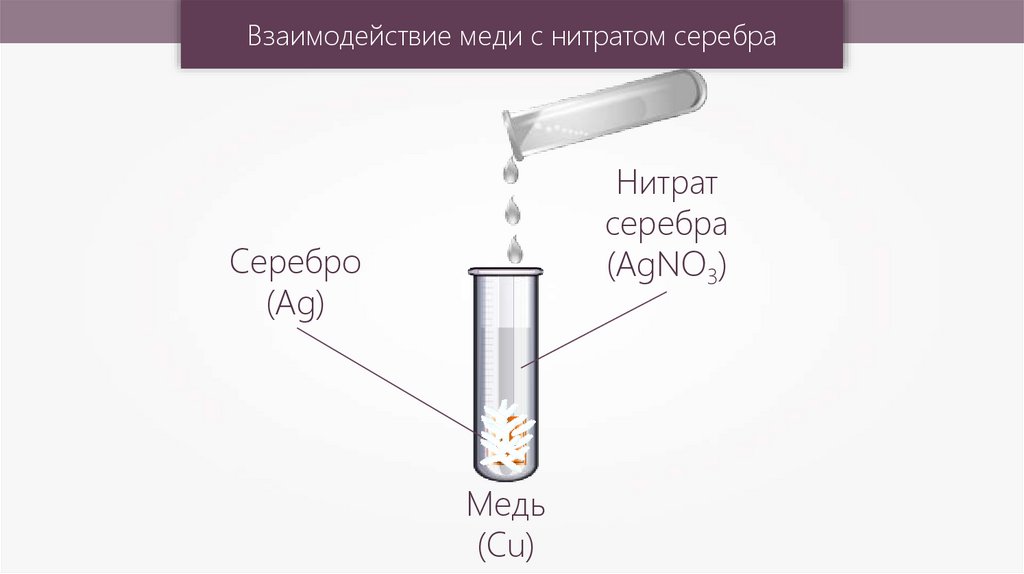
Взаимодействие меди с нитратом серебраНитрат
серебра
(AgNO3)
Серебро
(Ag)
Медь
(Cu)
31.
Взаимодействие меди с нитратом серебраCu + 2AgNO3 = Cu(NO3)2 + 2Ag
Восстановитель
Окислитель
32.
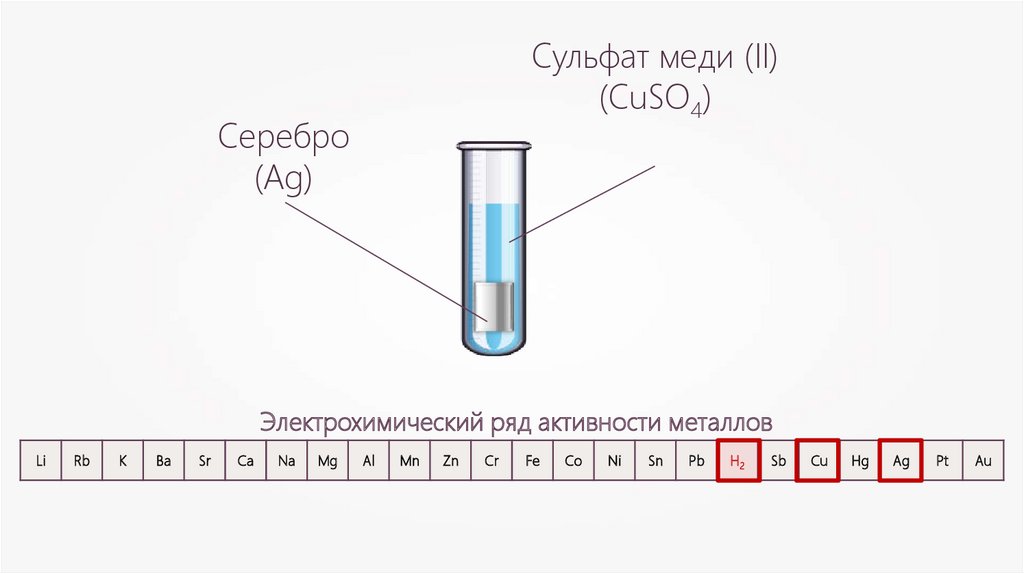
Сульфат меди (II)(CuSO4)
Серебро
(Ag)
Электрохимический ряд активности металлов
Li
Rb
K
Ba
Sr
Ca
Na
Mg
Al
Mn
Zn
Cr
Fe
Co
Ni
Sn
Pb
H2
Sb
Cu
Hg
Ag
Pt
Au
33.
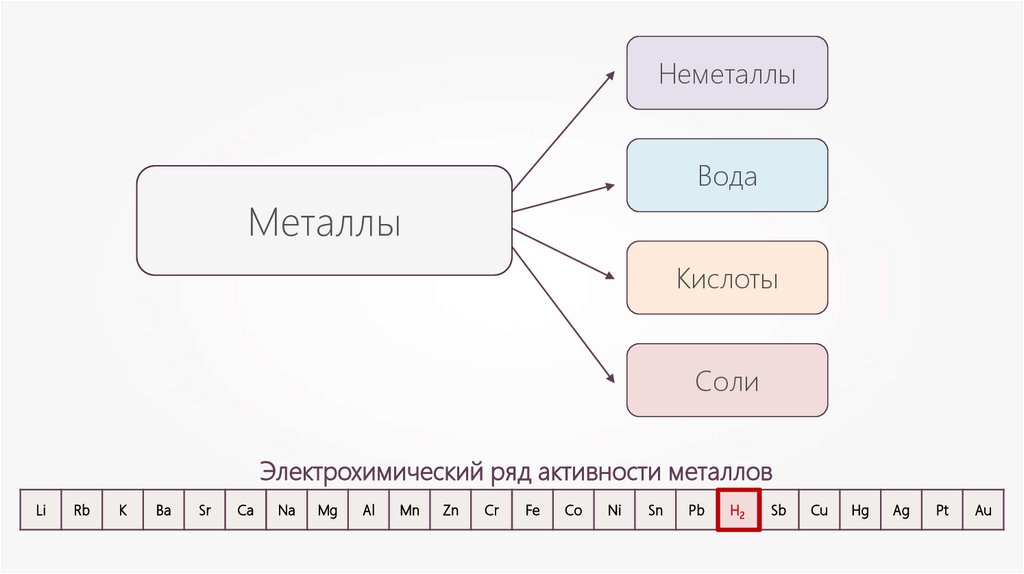
НеметаллыВода
Металлы
Кислоты
Соли
Электрохимический ряд активности металлов
Li
Rb
K
Ba
Sr
Ca
Na
Mg
Al
Mn
Zn
Cr
Fe
Co
Ni
Sn
Pb
H2
Sb
Cu
Hg
Ag
Pt
Au























 chemistry
chemistry








