Similar presentations:
Біотехнічні основи технології харчових продуктів
1.
БІОТЕХНІЧНІ ОСНОВИ ТЕХНОЛОГІЇ ХАРЧОВИХ ПРОДУКТІВ)План
1. Ферменти як біологічні каталізатори.
2. Гідролази. Механізм їх дії та значення для харчових
технологій.
3. Оксидоредуктазы. Механізм їх дії та роль в харчових
технологіях.
2.
Ферменти поділені на 6 основних класів:
1. оксидоредуктази
2. трансферази
3. гідролази
4. ліази
5. ізомерази
6. лігази (синтетази).
3.
• Для харчової науки ферменти являють інтересв трьох аспектах:
• 1) при переробці харчової сировини важливо знати і
контролювати дію внутрішньоклітинних ферментів, які
можуть викликати бажані або небажані зміни;
• 2) цілеспрямоване застосування ферментних
препаратів;
• 3) чисті ферментні препарати застосовують як
аналітичний засіб в хімії та технології харчових
продуктів – без виділення визначають кількість
речовини в системі.
4.
Гідролази (3 клас) каталізують розщеплення складних сполук
на більш прості з приєднанням води.
Діляться вони на 11 підкласів.
ГІДРОЛАЗИ (3-й клас, 11 підкласів)
Естерази
Ліпази
Фосфатаза
Пектинестераза
Карбогідрази
Глікозидази
Гліконаз
и
Протеази
Протеінази
Пептидази
5.
• Підклас 3.1. Естерази. Розщеплюютьскладноефірний зв'язок.
• R1 - CO - O - R2 + H2O R1 - COОН + R2ОН
• Можуть каталізувати реакції розщеплення і
синтезу. З ферментів цього класу велике
значення мають ліпази, пектинестерази,
фосфатази.
• Пектинестераза каталізує реакцію відщеплення
метанолу від пектину:
• Пектин + nH2O = nСН3ОН + пектат
• Фосфатази гідролізують складні ефіри
фосфорної кислоти (нуклеотиди, фосфатиди).
6.
• Підклас 3.2. Карбогідрази• Каталізують гідроліз вуглеводів по рівнянню:
• R1 - O - R2 + Н2О = R1OН + R2ОН
7.
Розрізняють глікозидази, що каталізують розщепленняолігосахаридів (до 10 мономерн. од.) і глікозидів,
і гліконази, що діють на субстрати
з великим ступенем полімеризації.
Фермент
Глікозидази
Субстрат
-глюкозидаза
мальтоза, сахароза
-глюкозидаза
целобіоза
-галактозидаза
лактоза
-фруктофуранозидаза
Гліконази
сахароза, рафіноза
-амілаза
крохмаль, декстрини
-амілаза
крохмаль, декстрини
глюкоамілаза
крохмаль,
мальтоза
полігалактуроназа
пектин,
полігалактуронова
кислота
клітковина, геміцелюлози
целюлаза
комплекс
ферментів: -1-4, -1-3, -1-6
-глюконазы
Примітка
в пророслому зерні
декстрини, ( -амілаза), відщеплює по 1
молекулі глюкози
8.
здійснюють гідролітичне розщеплення білків і пептидів.Вони гідролізують білки і поліпептиди по рівнянню:
R1-CO-NH-R2 + HOH = R1COOH + R2NH2
У зв'язку з тим, що ці ферменти каталізують
розщеплення пептидного зв'язку, їх називають пептидгідролазами
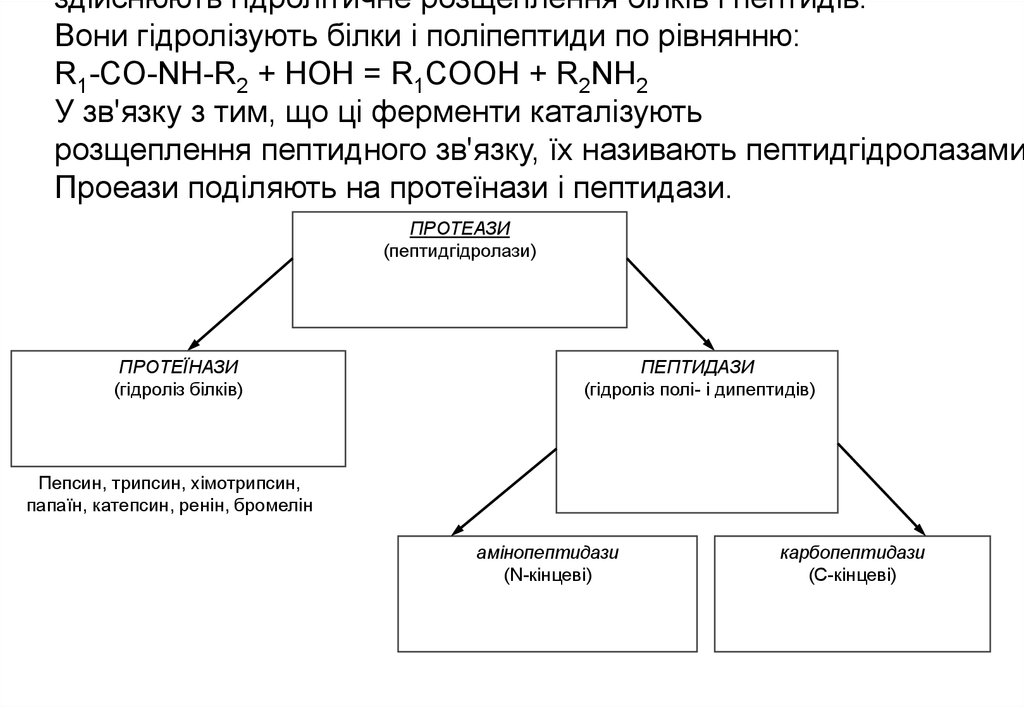
Проеази поділяють на протеїнази і пептидази.
ПРОТЕАЗИ
(пептидгідролази)
ПРОТЕЇНАЗИ
(гідроліз білків)
ПЕПТИДАЗИ
(гідроліз полі- і дипептидів)
Пепсин, трипсин, хімотрипсин,
папаїн, катепсин, ренін, бромелін
амінопептидази
(N-кінцеві)
карбопептидази
(С-кінцеві)
9.
3. Оксидоредуктази. Каталізують окислювально-відновні реакції.Окислювальний субстрат розглядається як донор водню
або електронів.
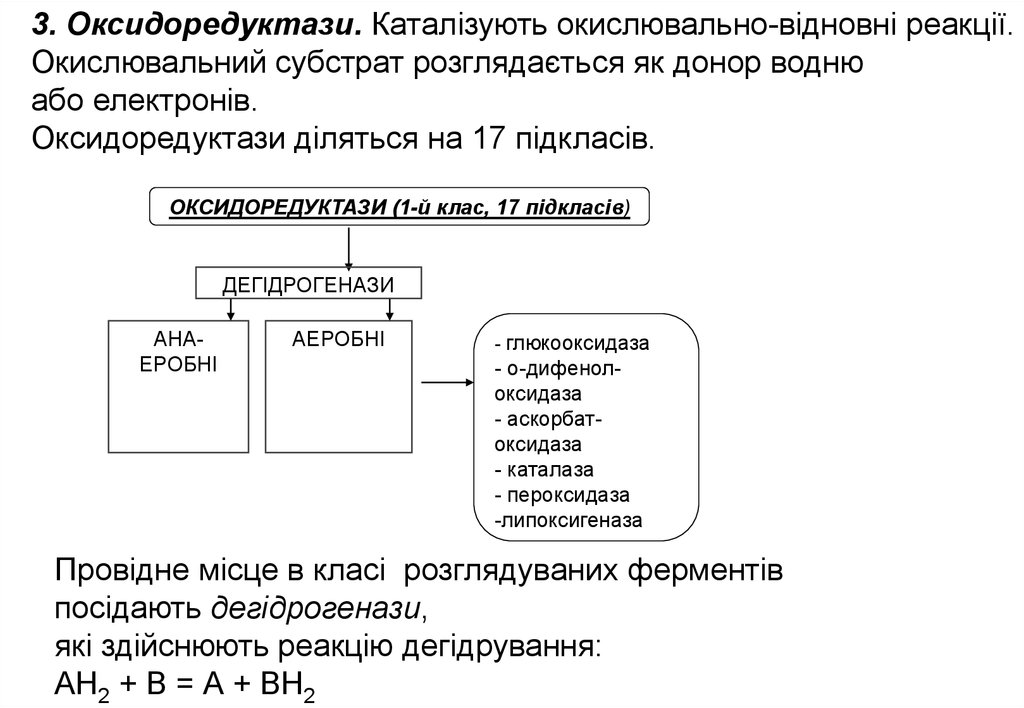
Оксидоредуктази діляться на 17 підкласів.
ОКСИДОРЕДУКТАЗИ (1-й клас, 17 підкласів)
ДЕГІДРОГЕНАЗИ
АНАЕРОБНІ
АЕРОБНІ
- глюкооксидаза
- о-дифенолоксидаза
- аскорбатоксидаза
- каталаза
- пероксидаза
-липоксигеназа
Провідне місце в класі розглядуваних ферментів
посідають дегідрогенази,
які здійснюють реакцію дегідрування:
АН2 + В = А + ВН2
10.
За механізмом переносу водню на акцептордегідрогенази поділяють на аеробні та анаеробні.
Аеробні дегідрогенази здатні передавати водень
субстрату кисню повітря ( з утворенням води і перекису
водню):
Серед представників аеробних дегідрогеназ:
Глюкозооксидаза, переносить Н2 від глюкози на О2 з утворенням Н2О2.
о-Дифенолоксидаза – (тривіальні назви тирозиназа, катехолаза,
фенолаза, поліфенолоксидаза), фермент каталізує окислення моно-, ди - і
трифенолів.
Аскорбатоксидаза каталізує окислення аскорбінової кислоти.
Каталаза дегідрує молекулу пероксиду водню:
Н2О2 + Н2О2 О2 + 2Н2О
Пероксидаза каталізує реакцію:
АН2 + Н2О2 А + 2Н2О
Ліпоксигеназа каталізує реакцію:
ненасичена жирна кислота + О2 = перекис ненасиченої жирної кислоти
R - СН2 - СН = R1 + О2 R - СН = СН-R1 ООН








 chemistry
chemistry