Similar presentations:
Простые вещества - неметаллы
1.
2.
Периодическая система химических элементов Д.И. МенделееваГруппы элементов
Пери –
оды
I
1
Н
2
Li
3
Na
6.939
3
Литий
Калий
29
Сu
Cs
85,47
196,967
Ag
48
112,40
55 Ва
Аu
[223]
Бор
Скандий
Иттрий
Сd In
114,82
Барий
80
200,59
Rа
Индий
*
138,81
Hg ТI
[226]
49
Кремний
VIII
VII
204,37
91,22
81
Радий
R2О
RO
Zr
Sn
118,69
Таллий
Гафний
41
92,906
Свинец
Rf
Nb
Ниобий
Кислород
73
180,948
Та
Тантал
[262]
Сера
51,996
Хром
Db
Фтор
34 Br
Селен
42
95,94
Мо
183.85
[263]
Технеций
52 I
W
58,9332
Со
Кобальт
75
186,2
Re
Рений
44
101,07
Ru
Рутений
45
102,905
Rh
Родий
[262]
Борий
RO2
R2O5
RO3
R2O7
RH4
RH3
RH2
RH
58,71
Ni
Никель
36
83,80
46
106,4
Pd
Палладий
76
190,2
Оs
54
131,30
Ксенон
77
192,2
Ir
Иридий
78
195,09
Рt
Платина
Rn
85
Bh
28
Xe
Астат
107
Аргон
39,948
Криптон
Осмий
210
18
Кr
53
84 At
Сиборгий
27
126,9044
[210]
Sg
Fe
Железо
Йод
Полоний
106
Тс
[99]
55,847
35
Бром
43
26
79,904
78,96
Теллур
74
Хлор
10
Ar
17
4.0026
20,183
Неон
35,453
Марганец
78,96
Nе
9
18,9984
Cr 25
Мn
44,956
24
83 Ро
Висмут
105
32,064
Вольфрам
208,980
F
17 Cl
51 Тe
121,75
Актиний Резерфордий Дубний
R2O3
8
15,9994
Молибден
Сурьма
82 Вi
207,19
О
33 Se
74,9216
Мышьяк
50 Sb
Олово
** Ас 104
88 89
138,81
[261]
Франций
32 As
72,59
Цирконий
Pb
Фосфор
2
Гелий
15 S
30,9738
Ванадий
Германий
40
Азот
7
14,0067
Ti 23
V
50,942
La 72
Hf
178.49
Лантан
Ртуть
87
Y
88,905
N
14 P
28,086
31 Ge
26,9815
38 39
56 57
Углерод
Титан
Галлий
137.34
6
12,01115
Sc 22
47,90
44,956
Zn Ga
87,62
С
13 Si
26,9815
Алюминий
Кадмий
132,905
5
10,811
20 21
Стронций
Золото
Fr
65,37
37 Sr
Цезий
79
40,08
Кальций
30
В
12 Al
24,312
Цинк
Рубидий
47
4
9,0122
Магний
19 Сa
Серебро
ЛВС
Ве
11 Мg
22,9898
39,102
107,868
Высшие
оксиды
VI
Не
Бериллий
Натрий
Rb
7
V
Водород
Медь
6
IV
1
63,546
5
III
1,00797
К
4
II
108
[265]
Hs
Хассий
109
[266]
Мt
Мейтнерий
RO4
Радон
86
[222]
3. Неметаллы – химические элементы, которые образуют в свободном виде простые вещества, не обладающие физическими свойствами
металлов.К неметаллам относятся инертные газы.
Каждая молекула инертного газа состоит
из одного атома.
Покажите как распределяются электроны
в атомах гелия и неона
4.
НеметаллыГазообразные
Жидкие
Твёрдые
5.
Периодическая система химических элементов Д.И. МенделееваГруппы элементов
Пери –
оды
I
1
Н
2
Li
3
Na
6.939
3
Литий
Калий
29
Сu
Cs
85,47
196,967
Ag
48
112,40
55 Ва
Аu
[223]
Бор
Скандий
Иттрий
Сd In
114,82
Барий
80
200,59
Rа
Индий
*
138,81
Hg ТI
[226]
49
Кремний
204,37
91,22
81
Sn
VII
Радий
R2О
RO
118,69
Таллий
Гафний
41
92,906
Свинец
Rf
Nb
Ниобий
73
180,948
Та
Тантал
[262]
Сера
VIII
Не
2
51,996
Хром
Db
Фтор
34 Br
Селен
42
95,94
Мо
183.85
[263]
[99]
Технеций
52 I
55,847
W
58,9332
Со
Кобальт
75
186,2
Re
Рений
44
101,07
Ru
Рутений
45
102,905
Rh
Родий
[262]
Борий
RO2
R2O5
RO3
R2O7
RH4
RH3
RH2
RH
Никель
36
83,80
46
106,4
Pd
Палладий
54
131,30
Ксенон
76
190,2
Оs
77
192,2
Ir
Иридий
78
195,09
Рt
Платина
Rn
85
Bh
Ni
Xe
Радон
Астат
107
58,71
39,948
Криптон
Осмий
210
28
Кr
53
84 At
Сиборгий
27
126,9044
[210]
Sg
Fe
Железо
Йод
Полоний
106
Тс
43
26
35
Бром
18
Аргон
79,904
78,96
Теллур
74
Хлор
10
Ar
17
4.0026
20,183
Неон
35,453
Марганец
78,96
Nе
9
18,9984
Cr 25
Мn
44,956
24
83 Ро
Висмут
105
32,064
Вольфрам
208,980
F
17 Cl
51 Тe
121,75
Актиний Резерфордий Дубний
R2O3
Кислород
Молибден
Сурьма
82 Вi
207,19
8
15,9994
33 Se
74,9216
Мышьяк
50 Sb
Олово
** Ас 104
88 89
138,81
[261]
Франций
Zr
Цирконий
Pb
Фосфор
32 As
72,59
О
15 S
30,9738
Ванадий
Германий
40
Азот
7
14,0067
Ti 23
V
50,942
La 72
Hf
178.49
Лантан
Ртуть
87
Y
88,905
N
14 P
28,086
31 Ge
26,9815
38 39
56 57
Углерод
Титан
Галлий
137.34
6
12,01115
Sc 22
47,90
44,956
Zn Ga
87,62
С
13 Si
26,9815
Алюминий
Кадмий
132,905
5
10,811
20 21
Стронций
Золото
Fr
65,37
37 Sr
Цезий
79
40,08
Кальций
30
В
12 Al
24,312
Цинк
Рубидий
47
4
9,0122
Магний
19 Сa
Серебро
ЛВС
Ве
11 Мg
22,9898
39,102
107,868
Высшие
оксиды
VI
Гелий
Бериллий
Натрий
Rb
7
V
Водород
Медь
6
IV
1
63,546
5
III
1,00797
К
4
II
108
[265]
Hs
Хассий
109
[266]
Мt
Мейтнерий
RO4
86
[222]
6. Строение внешнего электронного слоя атомов гелия и неона
He )2
Ne ) )
2
8
7. Применение гелия
8. Применение неона
9. Применение аргона
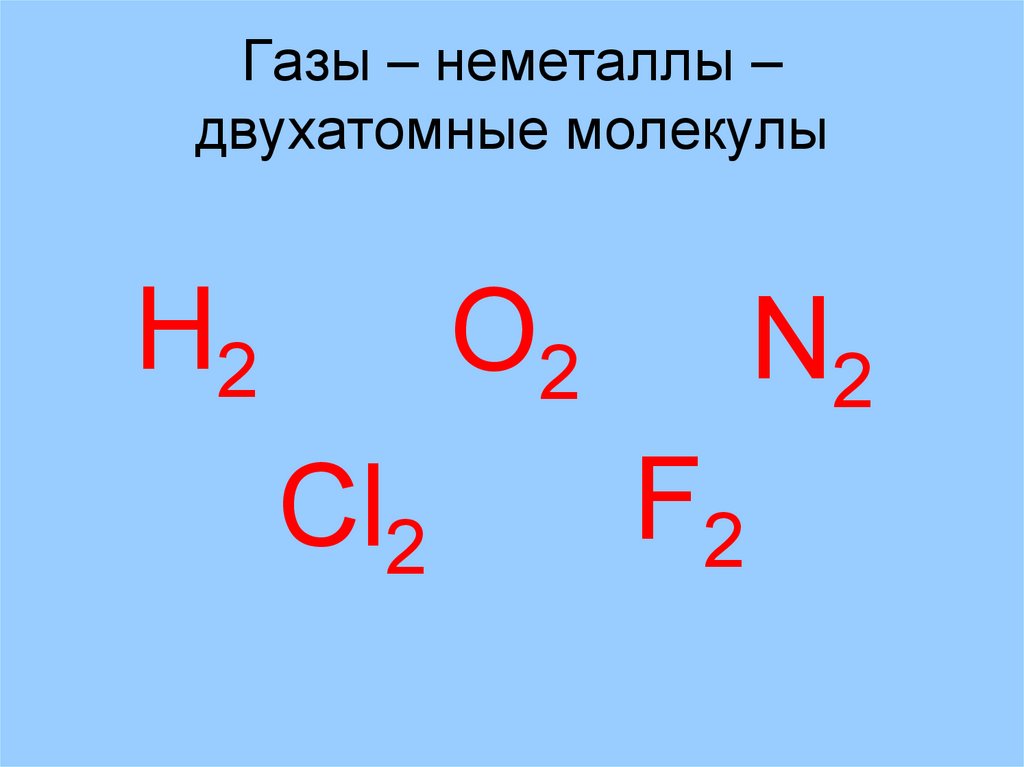
В начало10. Газы – неметаллы – двухатомные молекулы
Н2О2
Cl2
N2
F2
11.
N2Cl2
F2
В начало
12. Способность атомов одного химического элемента образовывать несколько простых веществ называют аллотропией, а эти простые
вещества – аллотропнымивидоизменениями или
модификациями
13. Жидкие вещества - неметаллы
В началоЖидкие вещества - неметаллы
14. Твёрдое вещество – неметалл - йод
Твёрдое вещество – неметалл йодДалее
15. Аллотропия углерода. Алмаз
16. Аллотропия углерода. Графит
17. Аллотропия фосфора. Красный и белый фосфор
Р418. Аллотропия серы. Кристаллическая, пластическая и моноклинная
19. Аллотропия кислорода. Кислород и озон
20. Аллотропия олова
Серое олово ( «оловянная чума)»Белое олово
21.
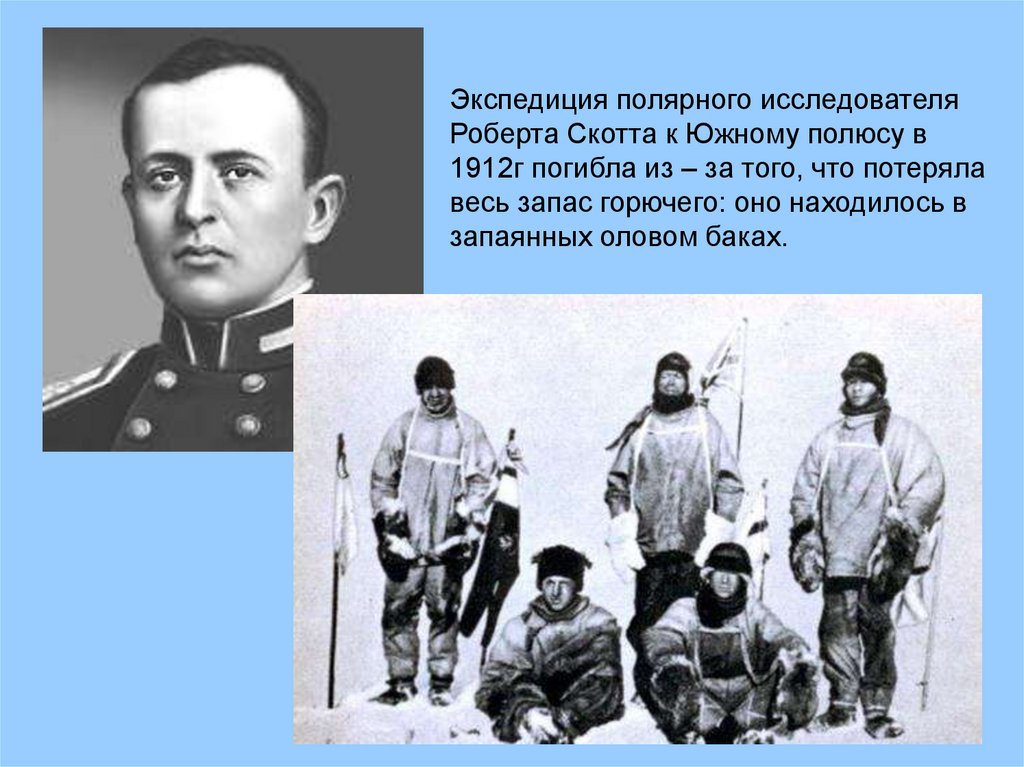
Экспедиция полярного исследователяРоберта Скотта к Южному полюсу в
1912г погибла из – за того, что потеряла
весь запас горючего: оно находилось в
запаянных оловом баках.

















 chemistry
chemistry








