Similar presentations:
Карбоновые кислоты
1.
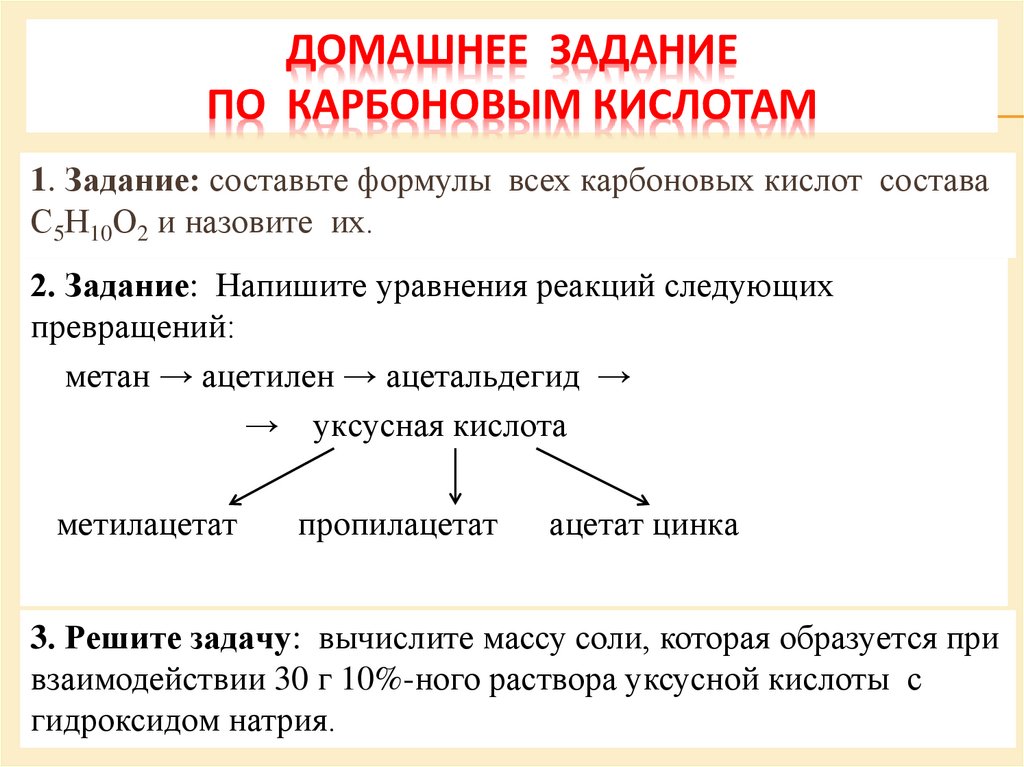
ДОМАШНЕЕ ЗАДАНИЕПО КАРБОНОВЫМ КИСЛОТАМ
1. Задание: составьте формулы всех карбоновых кислот состава
С5Н10О2 и назовите их.
2. Задание: Напишите уравнения реакций следующих
превращений:
метан → ацетилен → ацетальдегид →
→ уксусная кислота
метилацетат
пропилацетат
ацетат цинка
3. Решите задачу: вычислите массу соли, которая образуется при
взаимодействии 30 г 10%-ного раствора уксусной кислоты с
гидроксидом натрия.
2.
Сложные эфиры3.
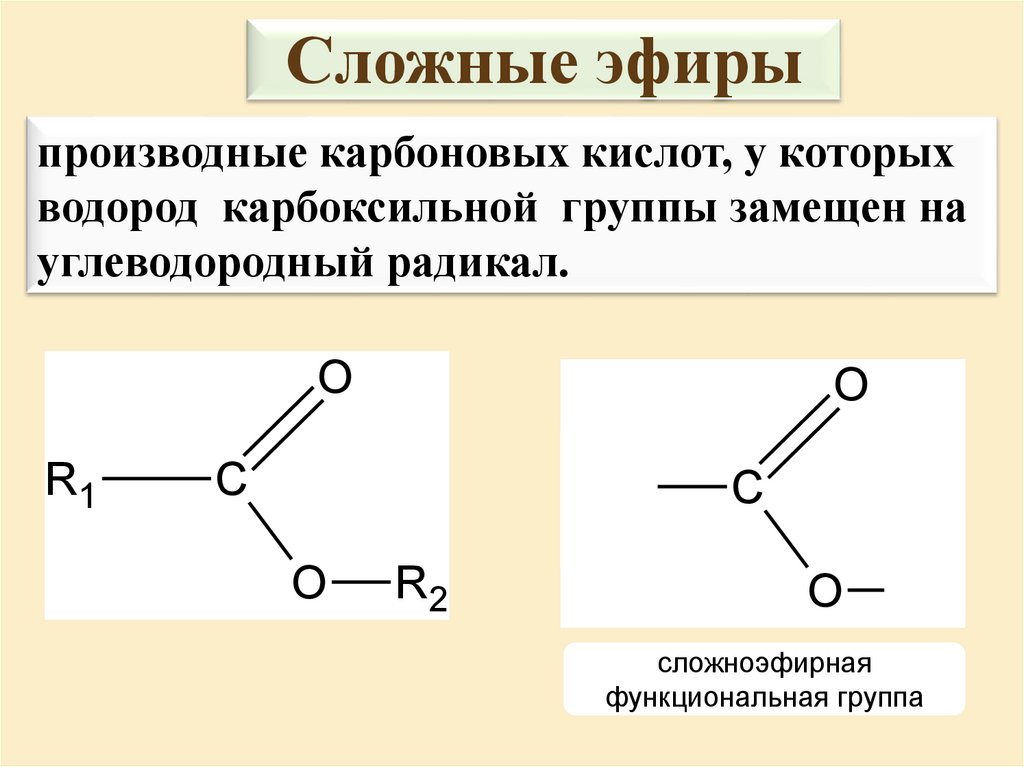
Сложные эфирыпроизводные карбоновых кислот, у которых
водород карбоксильной группы замещен на
углеводородный радикал.
O
R1
O
С
R1
O
R2
С
O
R2
сложноэфирная
функциональная группа
4.
Общая формула гомологического рядапредельных сложных эфиров
С n H 2 n O2
Сложноэфирная
функциональная группа
O
O
R1
R1
С
С
O
O
R2
где R1 и R2 – любые углеводородные
радикалы предельного строения
R2
5.
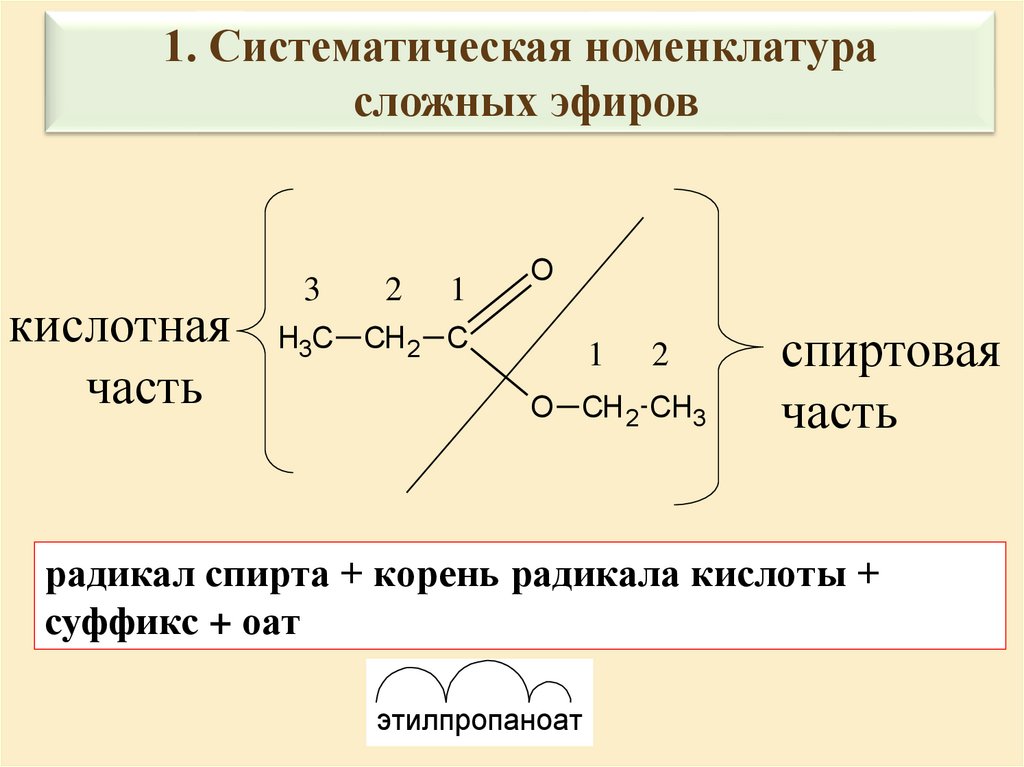
1. Систематическая номенклатурасложных эфиров
кислотная
часть
3
2
1
O
H3C СН 2 С
1
2
O СН 2 CH3
спиртовая
часть
радикал спирта + корень радикала кислоты +
суффикс + оат
этилпропаноат
6.
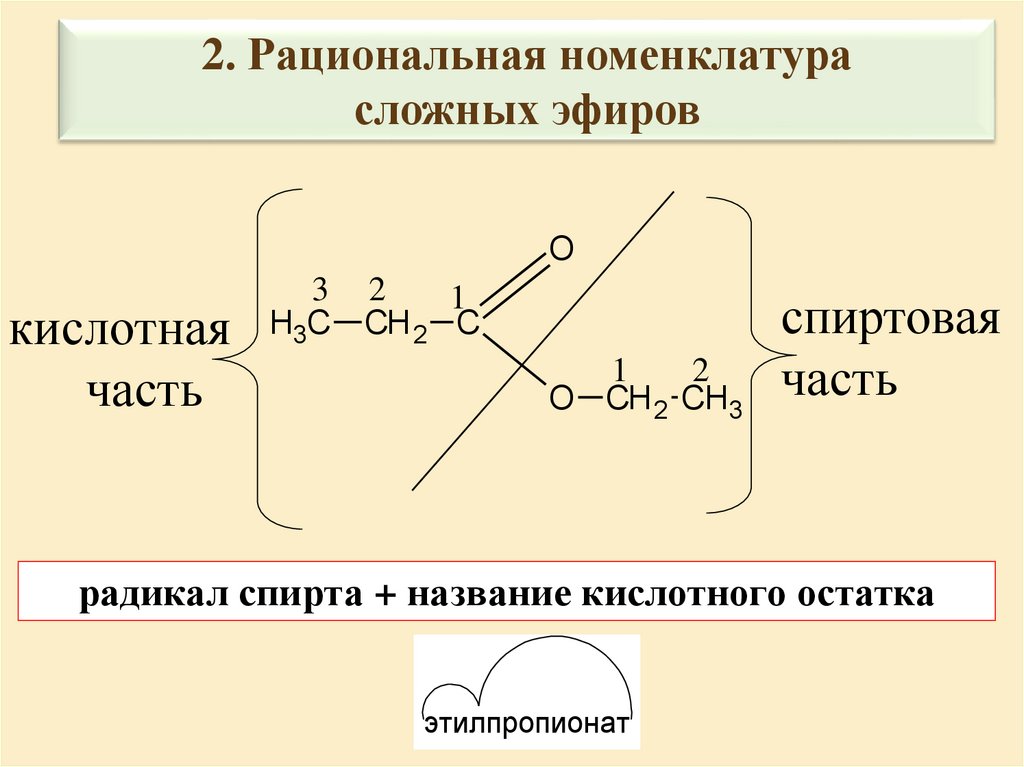
2. Рациональная номенклатурасложных эфиров
O
кислотная
часть
3 2
1
H3C СН 2 С
1
2
O СН 2 CH3
спиртовая
часть
радикал спирта + название кислотного остатка
этилпропионат
7.
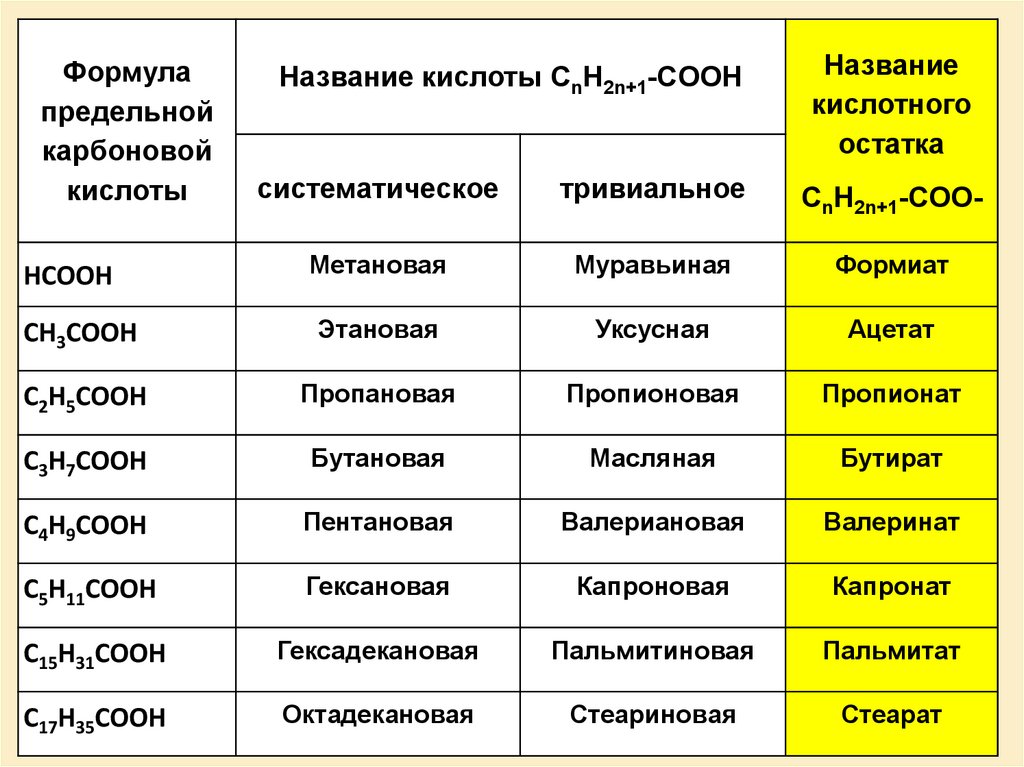
Формулапредельной
карбоновой
кислоты
Название кислоты СnH2n+1-COOH
Название
кислотного
остатка
систематическое
тривиальное
СnH2n+1-COO-
Метановая
Муравьиная
Формиат
CH3COOH
Этановая
Уксусная
Ацетат
C2H5COOH
Пропановая
Пропионовая
Пропионат
C3H7COOH
Бутановая
Масляная
Бутират
C4H9COOH
Пентановая
Валериановая
Валеринат
C5H11COOH
Гексановая
Капроновая
Капронат
C15H31COOH
Гексадекановая
Пальмитиновая
Пальмитат
C17H35COOH
Октадекановая
Стеариновая
Стеарат
HCOOH
8.
3. Тривиальные названия сложных эфировO
кислотная
часть
3 2
1
H3C СН 2 С
1
2
O СН 2 CH3
спиртовая
часть
название спирта + эфир + название кислоты в Р.п.
этиловый эфир пропановой кислоты
9.
OH
С
O
СН 2
CH3
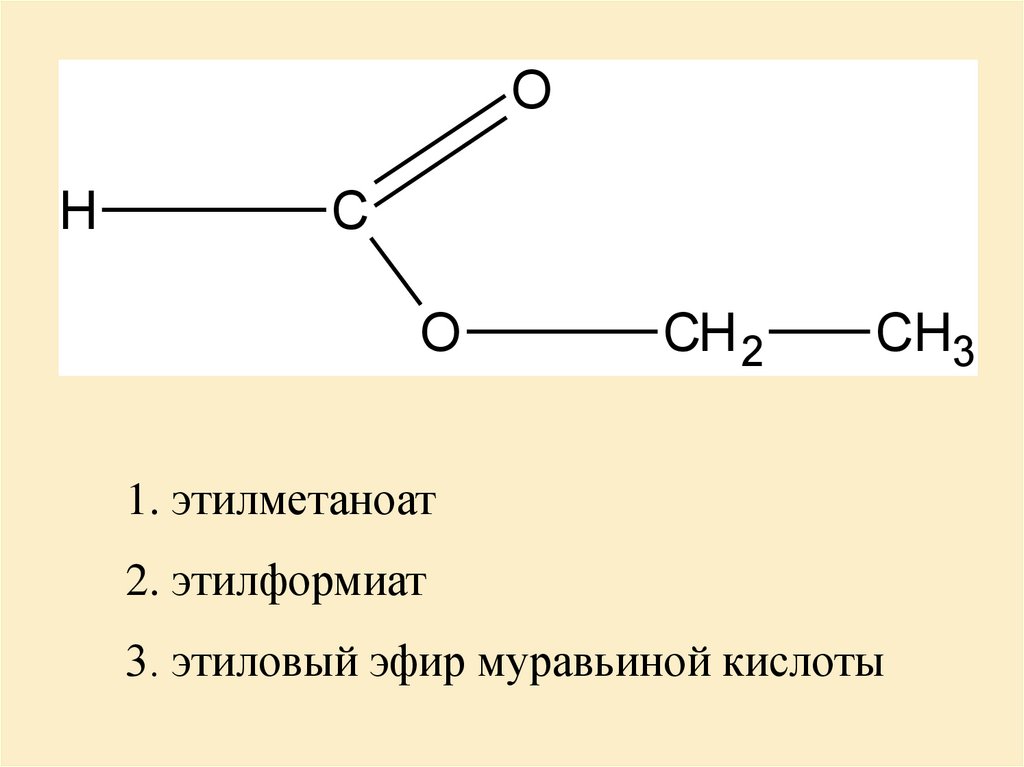
1. этилметаноат
2. этилформиат
3. этиловый эфир муравьиной кислоты
10.
OH3C
С
O
1. метилэтаноат
2. метилацетат
3. метиловый эфир уксусной кислоты
CH3
11.
OH3C
С
O
СН 2
СН 2
1. пропилэтаноат
2. пропилацетат
3. пропиловый эфир уксусной кислоты
CH3
12.
OH3C
С
O
СН 2
СН 2
СН 2
1. бутилэтаноат
2. бутилацетат
3. бутиловый эфир уксусной кислоты
CH3
13.
OH3C
СН2
СН2
С
O
1. метилбутаноат
2. метилбутират
3. метиловый эфир масляной кислоты
CH3
14.
Изомерия сложных эфировположения
функциональной
группы
межклассовая
Структурная изомерия
углеродного
скелета
15.
Изомерия сложных эфиров1. Углеродного скелета
O
H3C
С
O
СН 2
СН 2
CH3
пропилэтанат
O
H3C
С
CH3
O
СН
изопропилэтанат
CH3
16.
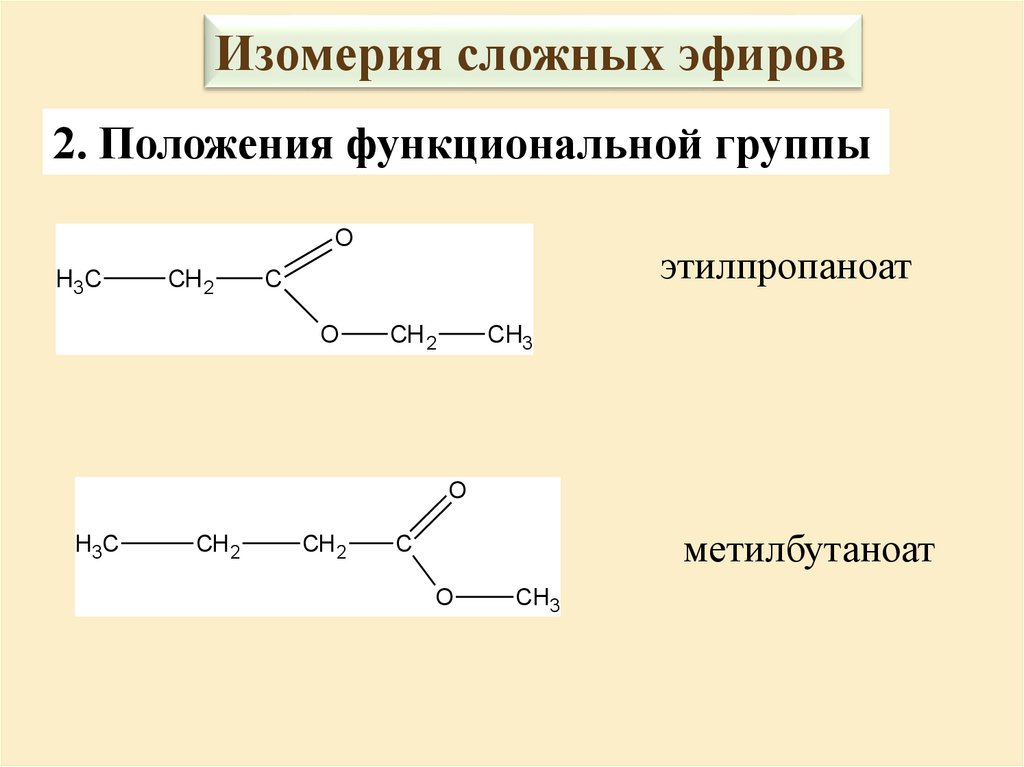
Изомерия сложных эфиров2. Положения функциональной группы
O
H3C
СН 2
этилпропаноат
С
O
СН 2
CH3
O
H3C
СН 2
СН 2
метилбутаноат
С
O
CH3
17.
Изомерия сложных эфиров3. Межклассовая изомерия с карбоновыми
кислотами
С3Н6О2
O
O
H3C
СН 2
С
H3C
OH
пропановая кислота
С
O
метилэтаноат
CH3
18.
Физические свойства сложных эфировЛетучие жидкости, мало растворимы в воде хорошо растворимы
в спиртах и других эфирах, легче воды, хорошие растворители,
обладают приятным запахом, отвечающими за запахи цветов,
ягод и фруктов
ЭФИР
этиловый эфир муравьиной кислоты
этиловый эфир масляной кислоты
ЗАПАХ
РОМА
АНАНАСА
бутиловый эфир уксусной кислоты
ГРУШИ
пентиловый эфир муравьиной кислоты
ВИШНИ
изобутиловый эфир уксусной кислоты
БАНАНОВ
бутиловый эфир масляной кислоты
АБРИКОСОВ
метиловый эфир масляной кислоты
ЯБЛОК
19.
20.
НАХОЖДЕНИЕ В ПРИРОДЕСложные эфиры входят в состав различных плодов,
ягод, фруктов.
Запах может определять
только один сложный
эфир (ананас, вишня,
слива, яблоки и др.) или
сложное сочетание
разных сложных эфиров
«букет» (в землянике
аромат 40 разных сложных
эфиров).
21.
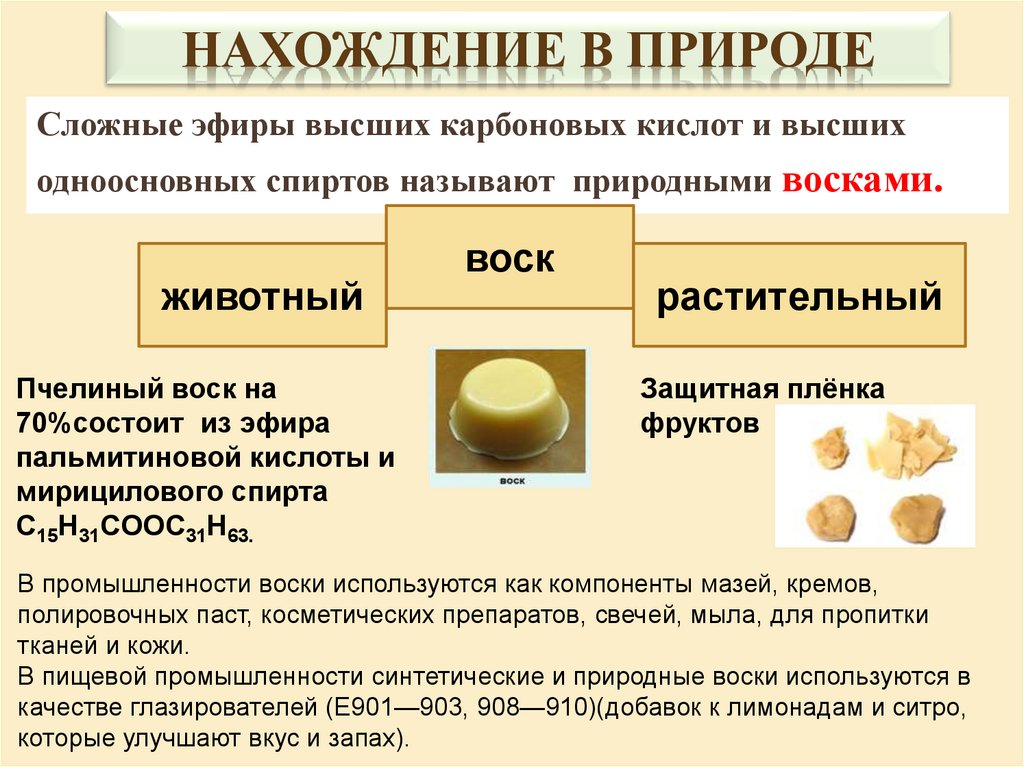
НАХОЖДЕНИЕ В ПРИРОДЕСложные эфиры высших карбоновых кислот и высших
одноосновных спиртов называют природными восками.
животный
Пчелиный воск на
70%состоит из эфира
пальмитиновой кислоты и
мирицилового спирта
C15H31COOC31H63.
воск
растительный
Защитная плёнка
фруктов
В промышленности воски используются как компоненты мазей, кремов,
полировочных паст, косметических препаратов, свечей, мыла, для пропитки
тканей и кожи.
В пищевой промышленности синтетические и природные воски используются в
качестве глазирователей (Е901—903, 908—910)(добавок к лимонадам и ситро,
которые улучшают вкус и запах).
22.
ПОЛУЧЕНИЕРеакция этерификации - реакции между спиртами и
кислотами, в результате которых образуются сложные
эфиры и выделяется вода (от лат. ether - эфир).
O
R
H
С
O
O
+
H
+
H
O
R
R1
Особенности реакции этерификации:
1. Обратима
2. Протекает в присутствии ионов Н+
3. От кислоты отщепляется группа ОН-
+
С
O
R1
H2O
23.
ПОЛУЧЕНИЕуксусная кислота этиловый спирт
пентановая (валерьяновая)
кислота
этиловый эфир
уксусной кислоты
бутиловый спирт
бутиловый эфир валерьяновой кислоты
24.
Химические свойства1. Гидролиз сложных эфиров (водный) процесс взаимодействия сложных эфиров с водой, который
является обратным реакции этерификации. Протекает с
образованием карбоновой кислоты и спирта.
O
R1
H2O/H+
C
O
R2
этиловый эфир уксусной кислоты
O
+
R1
R2
OH
уксусная кислота
этиловый спирт
OH
25.
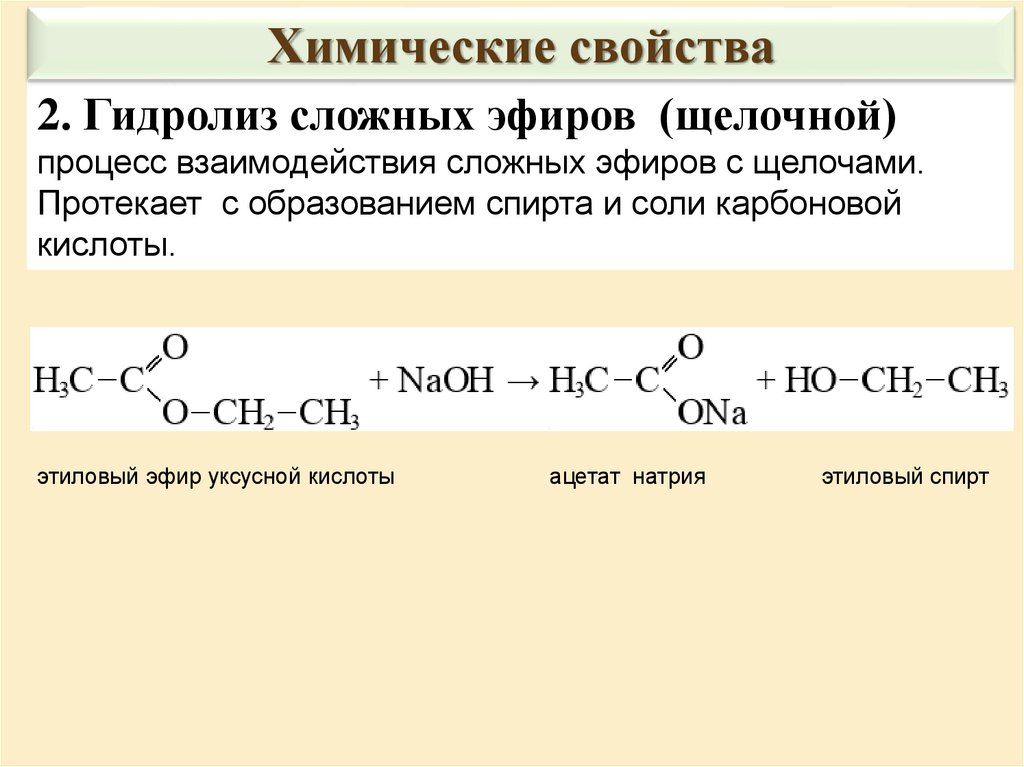
Химические свойства2. Гидролиз сложных эфиров (щелочной)
процесс взаимодействия сложных эфиров с щелочами.
Протекает с образованием спирта и соли карбоновой
кислоты.
этиловый эфир уксусной кислоты
ацетат натрия
этиловый спирт
26.
Применение сложных эфировВ косметической
промышленности
В производстве мыла и СМС
В пищевой промышленности
В производстве
свечей
27.
Применение сложных эфировМедицина и ароматерапия.
О целебных свойствах душистых веществ
известно с незапамятных времён. Сложилась
целая наука о лечении запахами —
ароматерапия.
Ароматерапия — это полностью натуральный
метод успокоения или устранения многих
недугов. Все формы процедур — массаж,
ванны, ингаляции — основаны на введении в
организм человека высококачественных,
чистых, не содержащих химических носителей
или добавок эфирных масел. Замечено, что
запахи мирта, лимона, мяты оказывают
тонизирующее действие на нервную систему,
а ароматы розы, жасмина, лаванды —
успокаивающее. Ароматические вещества
способны снимать усталость, головную боль,
нормализовать сон, улучшать деятельность
головного мозга.
28.
СЛОЖНЫЕ ЭФИРЫСложные эфиры широко используются в качестве
растворителей, пластификаторов, ароматизаторов.
Эфиры МУРАВЬИНОЙ КИСЛОТЫ
HCOOCH3 — метилформиат,
метилформиат tкип = 32 °C; растворитель жиров, минеральных
и растительных масел, целлюлозы, жирных кислот; ацилирующий агент;
используют в производстве некоторых уретанов, формамида.
HCOOC2H5 — этилформиат,
этилформиат tкип = 53 °C; растворитель нитрата и ацетата
целлюлозы; ацилирующий агент; отдушка для мыла, его добавляют
к некоторым сортам рома, чтобы придать ему характерный аромат; применяют
в производстве витаминов B1, A, E.
HCOOCH2CH(CH3)2 — изобутилформиат несколько
напоминает запах ягод малины.
HCOOCH2CH2CH(CH3)2 — изоамилформиат (изопентилформиат)
растворитель смол и нитроцеллюлозы.
HCOOCH2C6H5 — бензилформиат,
бензилформиат tкип = 202 °C; имеет запах жасмина;;
жасмина
используется как растворитель лаков и красителей.
HCOOCH2CH2C6H5 — 2 - фенилформиат имеет запах хризантем.
хризантем
29.
Эфиры УКСУСНОЙ КИСЛОТЫCH3COOCH3 — метилацетат,
метилацетат tкип = 58 °C; по растворяющей способности
аналогичен ацетону и применяется в ряде случаев как его заменитель, однако
он обладает большей токсичностью, чем ацетон.
CH3COOC2H5 — этилацетат,
этилацетат tкип = 78 °C; подобно ацетону растворяет
большинство полимеров. По сравнению с ацетоном его преимущество в
более высокой температуре кипения (меньшей летучести).
CH3COOC3H7 — н-пропилацетат,
пропилацетат tкип = 102 °C; по растворяющей
способности подобен этилацетату.
CH3COOCH(CH3)2 — изопропилацетат,
изопропилацетат tкип = 88 °C; по растворяющим
свойствам занимает промежуточное положение между этил- и пропилацетатом.
CH3COOC5H11 — н-амилацетат (н-пентилацетат), tкип = 148 °C; напоминает
по запаху грушу, применяется как растворитель для лаков, поскольку он
испаряется медленнее, чем этилацетат.
CH3COOCH2CH2CH(CH3)2 — изоамилацетат (изопентилацетат)
напоминает по запаху бананы.
CH3COOC8H17 — н-октилацетат имеет запах апельсинов.
30.
Эфиры МАСЛЯНОЙКИСЛОТЫ
C3H7COOCH3 — метилбутират,
метилбутират tкип = 102,5 °C; по запаху напоминает ранет.
C3H7COOC2H5 — этилбутират,
этилбутират tкип = 121,5 °C; имеет характерный запах
ананасов.
C3H7COOC4H9 — бутилбутират,
бутилбутират tкип = 166,4 °C;
C3H7COOC5H11 — н-амилбутират (н-пентилбутират) и
C3H7COOCH2CH2CH(CH3)2 — изоамилбутират (изопентилбутират)
имеют запах груш, а также служат растворителями в лаках для ногтей.
Эфиры ИЗОВАЛЕРИАНОВОЙ
КИСЛОТЫ
(CH3)2CHCH2COOCH2CH2CH(CH3)2 — изоамилизовалерат
(изопентилизовалерат) имеет запах яблока.
31.
ДОМАШНЕЕ ЗАДАНИЕНа листе формата А4 приготовить проект про один
любой сложный эфир по плану:
1. Структурная формула и все названия
2. Структурная формула одного изомера и все его
названия.
3. Физические свойства выбранного эфира
4. Уравнение реакция этерификации - получения эфира
5. Уравнения реакций водного и щелочного гидролиза
6. Применение.






















 chemistry
chemistry








