Similar presentations:
Пороки сердца
1.
ПОРОКИ СЕРДЦАВыполнила: Зуева Анастасия Юрьевна
2.
Врожденные пороки сердца представляют собой аномалии структуры и (или) функции сердечнососудистой системы, возникающие в результате нарушения ее эмбрионального развития.I. Пороки с неизмененным (или мало измененным) легочным кровотоком: аномалии расположения
сердца, аномалии дуги аорты, ее коарктация, стеноз аорты; недостаточность клапанов сердца.
II.
Пороки
с
гиперволемией
малого
круга
кровообращения:
1) Не сопровождающиеся ранним цианозом – не происходит сброс крови из правых отделов в левые;
2) Сопровождающиеся цианозом – так или иначе кровь, идущая в большой круг кровообращения
смешивается
с
венозной
кровью
из
правых
отделов
сердца.
III.
Пороки
с
гиповолемией
малого
круга
кровообращения:
1)
не
сопровождающиеся
цианозом
изолированный
стеноз
легочного
ствола;
2) сопровождающиеся цианозом - триада, тетрада и пентада Фалло, трикуспидальная атрезия с сужением
легочного ствола или малым дефектом межжелудочковой перегородки, аномалия Эбштейна (смещение
створок трикуспидального клапана в правый желудочек), гипоплазия правого желудочка.
IV. Комбинированные пороки с нарушением взаимоотношений между различными отделами сердца
и крупными сосудами: транспозиция аорты и легочного ствола (полная и корригированная), их
отхождение от одного из желудочков и др.
3.
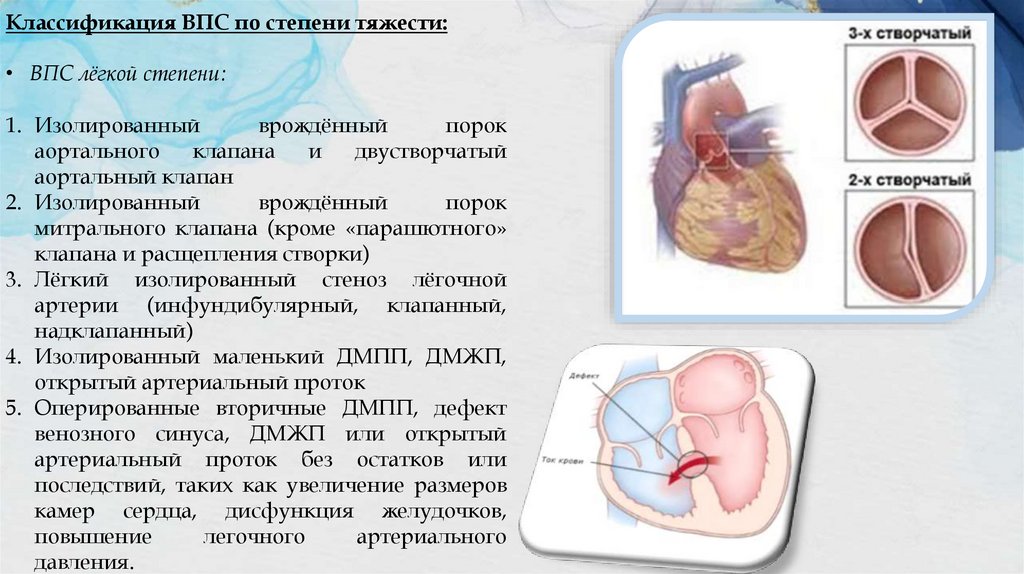
Классификация ВПС по степени тяжести:• ВПС лёгкой степени:
1. Изолированный
врождённый
порок
аортального
клапана
и
двустворчатый
аортальный клапан
2. Изолированный
врождённый
порок
митрального клапана (кроме «парашютного»
клапана и расщепления створки)
3. Лёгкий изолированный стеноз лёгочной
артерии (инфундибулярный, клапанный,
надклапанный)
4. Изолированный маленький ДМПП, ДМЖП,
открытый артериальный проток
5. Оперированные вторичные ДМПП, дефект
венозного синуса, ДМЖП или открытый
артериальный проток без остатков или
последствий, таких как увеличение размеров
камер сердца, дисфункция желудочков,
повышение
легочного
артериального
давления.
4.
• ВПС умеренной степени (в этом случае не возникаетжизнеугрожающих гемодинамических нарушений):
1. Частичный или тотальный аномальный дренаж
лёгочных вен
2. Аномальная коронарная артерия, исходящая из
лёгочной артерии
3. Аномальная коронарная артерия, исходящая из
противоположного синуса
4. Аортальный стеноз – подклапанный или
надклапанный
5. Вторичный ДМПП, умеренный или большой
невосстановленный (за исключением сосудистых
заболеваний лёгких)
6. Коарктация аорты
7. Двухкамерный правый желудочек
8. Аномалия Эбштейна
5.
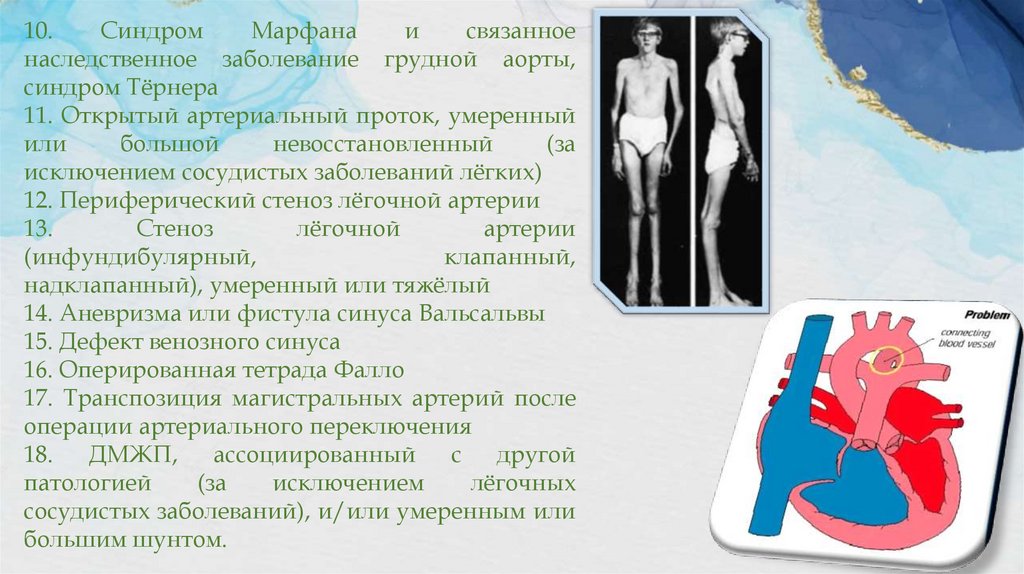
10.Синдром
Марфана
и
связанное
наследственное заболевание грудной аорты,
синдром Тёрнера
11. Открытый артериальный проток, умеренный
или
большой
невосстановленный
(за
исключением сосудистых заболеваний лёгких)
12. Периферический стеноз лёгочной артерии
13.
Стеноз
лёгочной
артерии
(инфундибулярный,
клапанный,
надклапанный), умеренный или тяжёлый
14. Аневризма или фистула синуса Вальсальвы
15. Дефект венозного синуса
16. Оперированная тетрада Фалло
17. Транспозиция магистральных артерий после
операции артериального переключения
18.
ДМЖП,
ассоциированный
с
другой
патологией
(за
исключением
лёгочных
сосудистых заболеваний), и/или умеренным или
большим шунтом.
6.
• ВПСтяжелой
степени
(оперированные и неоперированные,
если нет уточнения):
1. Любой
ВПС
(оперированный
и
неоперированный),
ассоциированный
с
сосудистым заболеванием лёгких
2. Любой синий ВПС (неоперированный или
паллиативная операция)
3. Двойное отхождение магистральных сосудов от
правого желудочка
4. Операция Фонтена в анамнезе
5. Прерванная дуга аорты
6. Атрезия лёгочной артерии (все формы)
7. Транспозиция магистральных артерий (кроме
пациентов
после
операции
артериального
переключения).
7.
Классификация приобретённых пороков сердца:Приобретенные пороки сердца классифицируются по следующим признакам:
Этиология:
ревматический,
вследствие
инфекционного
эндокардита,
атеросклеротический, сифилитический и т.д.
Локализация пораженных клапанов и их количество: изолированный или локальный
(при поражении 1 клапана), комбинированный (при поражении 2-х и более
клапанов); пороки аортального, митрального, трикуспидального клапанов, клапана
ствола легочной артерии.
Морфологическое и функциональное поражение клапанного аппарата: стеноз
атриовентрикулярного отверстия, недостаточность клапана и их сочетание.
Степень выраженности порока и степень нарушения гемодинамики сердца: не
оказывающий существенного влияния на внутрисердечное кровообращение,
умеренно или резко выраженный.
Состояние общей гемодинамики: компенсированные пороки сердца (без
недостаточности
кровообращения),
субкомпенсированные
(с
преходящей
декомпенсацией,
вызываемой
физическими
перегрузками,
лихорадкой,
беременностью и т. д.) и декомпенсированные (с развившейся недостаточностью
кровообращения).
8.
Механизм образования тонов сердца:I тон образуется из нескольких компонентов:
1. мышечного, обусловленного колебаниями миокарда предсердий (предсердный компонент) и
желудочков;
2. клапанного, обусловленного закрытием атриовентрикулярных клапанов и открытием
полулунных клапанов аорты и легочного ствола;
3. сосудистого, связанного с колебаниями начальных отрезков аорты и легочного ствола при
растяжении их кровью в период изгнания.
II тон образуется во время диастолы после короткой паузы. Он выслушивается лучше у
основания сердца, поскольку возникает при захлопывании полулунных створок клапанов аорты
и легочного ствола. В отличии от I тона он менее продолжительный (0,07сек ) и более высокий.
II тон имеет клапанный и сосудистый компоненты. Клапанный компонент II тона обусловлен
захлопыванием полулунных клапанов аорты и легочного ствола, а сосудистый компонент –
колебанием стенок этих сосудов.
9.
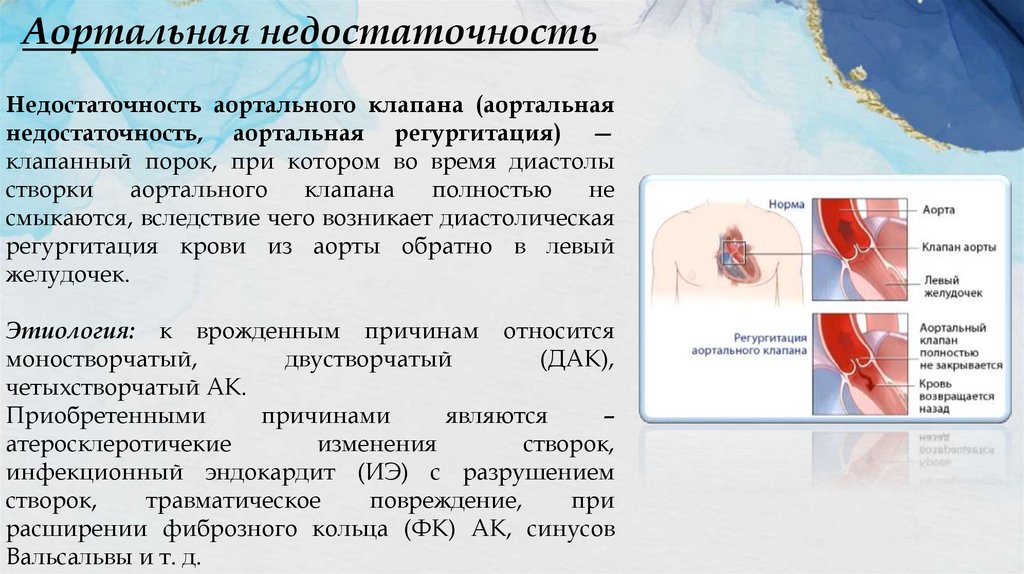
Аортальная недостаточностьНедостаточность аортального клапана (аортальная
недостаточность, аортальная регургитация) —
клапанный порок, при котором во время диастолы
створки
аортального
клапана
полностью
не
смыкаются, вследствие чего возникает диастолическая
регургитация крови из аорты обратно в левый
желудочек.
Этиология: к врожденным причинам относится
моностворчатый,
двустворчатый
(ДАК),
четыхстворчатый АК.
Приобретенными
причинами
являются
–
атеросклеротичекие
изменения
створок,
инфекционный эндокардит (ИЭ) с разрушением
створок,
травматическое
повреждение,
при
расширении фиброзного кольца (ФК) АК, синусов
Вальсальвы и т. д.
10.
Патогенез: при острой тяжелой АН в левый желудочек нормального размеравозвращается большой объем крови, и ЛЖ не имеет времени адаптироваться к
перегрузке объёмом.
Неспособность желудочка к быстрой компенсаторной дилатации →
уменьшение ударного объёма → тахикардия (как компенсаторный механизм
для поддержания СВ, но недостаточно) → снижается миокардиальная перфузия
субэндокарда (тк конечное диастолическое давление ЛЖ приближается к
дастолическому давлению в аорте и коронарных артериях) → дилатация ЛЖ и
истончение его стенки (из-за увеличения постнагрузки) в сочетании с
тахикардией → увеличение потребности миокарда в кислороде → ишемия →
осложнения → внезапная смерть.
При хронической АН в ЛЖ формируется ряд компенсаторных механизмов, в
том числе увеличение конечно-диастолического объёма и податливости камеры
ЛЖ → увеличение объёма без повышения давления наполнения ЛЖ и
комбинации концентрической и эксцентрической гипертрофии (т.о., АН
создаёт условия для комбинации перегрузки объёмом и перегрузки давлением).
11.
12.
Клиническая картина: большинство пациентов с хронической АН остаютсябессимптомными на протяжении фазы компенсации, которая может длиться десятилетиями.
При декомпенсации порока появляются прогрессирующая одышка, ортопноэ, приступы
сердечной астмы, утомляемость. Могут отмечаться типичные ангинозные боли даже при
отсутствии поражения коронарных артерий.
При тяжёлой АН высок риск развития отёка лёгких или кардиогенного шока!
Диагностика: - сбор жалоб и анамнеза у всех пациентов с подозрением на АН для
верификаци диагноза.
- физикальное обследование: обратить внимание на пульсацию артерий шеи и нижних
конечностей, измерить АД. Патономотичные признаки тяжёлой АН – видимая пульсация
общих сонных артерий, иногда височных и подключичных вен («пляска каротид»), «высокий
пульс», усиленный и смещенный влево и вниз верхушечный толчок, псевдокапиллярный
пульс (признак Квинке), покачивание головы (симптом Мюссе), пульсация в правом
подреберье.
- аускультативные феномены: диастолический шум во II межреберье справа от грудины и в
III – IV у левого края грудины и проводится на верхушку сердца, по характеру
высокочастотный, чаще убывающий, связан с быстрым снижением объёма или степени
регургитации в течение диастолы; ослабление I тона на верхушке сердца, ослабление II тона
над аортой.
13.
- проведение лабораторных исследований не требуется для установления диагноза АН- проведение 12-канальной ЭКГ: изменения неспецифичны, представляют собой признаки
гипертрофии ЛЖ, отклонение оси влево, расширение левого предсердия. В случае острой АН →
неспецифические изменения сегмента ST и синусовая тахикардия, обусловленная повышенной
активацией симпатической НС.
14.
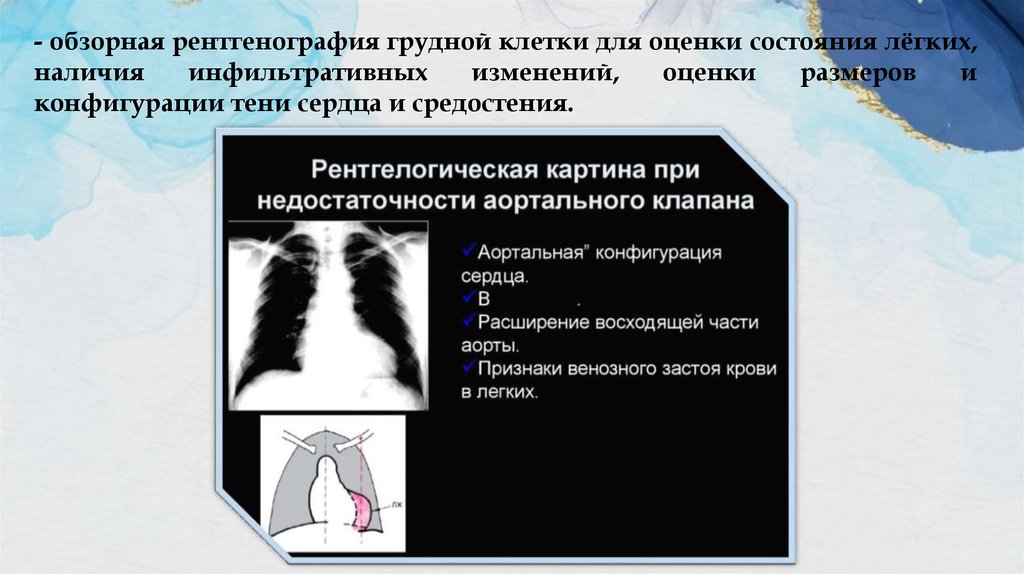
- обзорная рентгенография грудной клетки для оценки состояния лёгких,наличия
инфильтративных
изменений,
оценки
размеров
и
конфигурации тени сердца и средостения.
15.
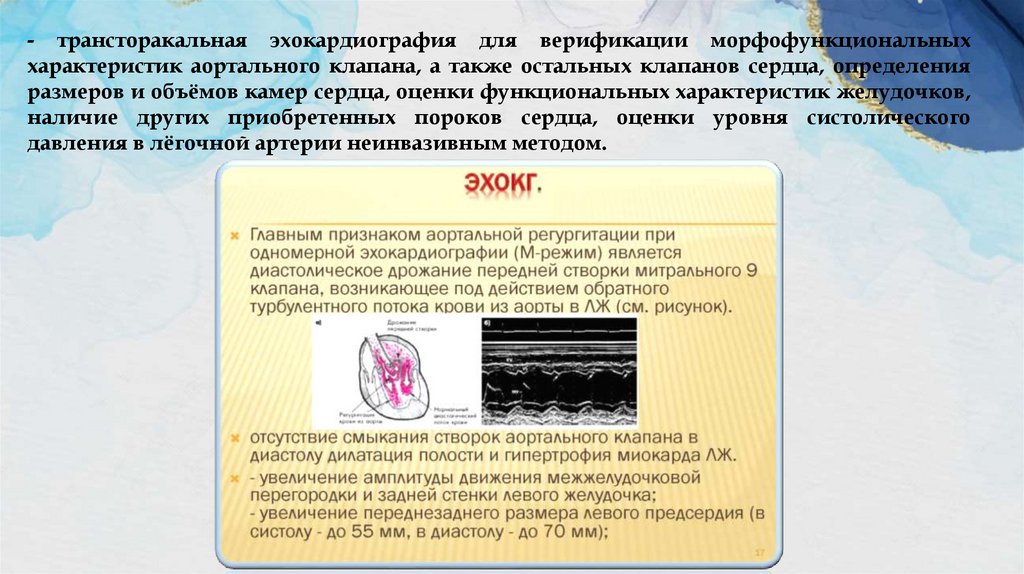
- трансторакальная эхокардиография для верификации морфофункциональныххарактеристик аортального клапана, а также остальных клапанов сердца, определения
размеров и объёмов камер сердца, оценки функциональных характеристик желудочков,
наличие других приобретенных пороков сердца, оценки уровня систолического
давления в лёгочной артерии неинвазивным методом.
16.
Консервативное лечение: пациентам с тяжелой АН, расширением ЛЖ и/илидисфункцией ЛЖ, но с ожидаемым риском неблагоприятного исхода хирургического
вмешательства выше риска при медикаментозном лечении, рекомендуется:
- иАПФ
- антагонисты рецепторов ангиотензина II
- антагонисты кальция дигидроперидинового ряда
- бета-адреноблокаторы
- диуретики
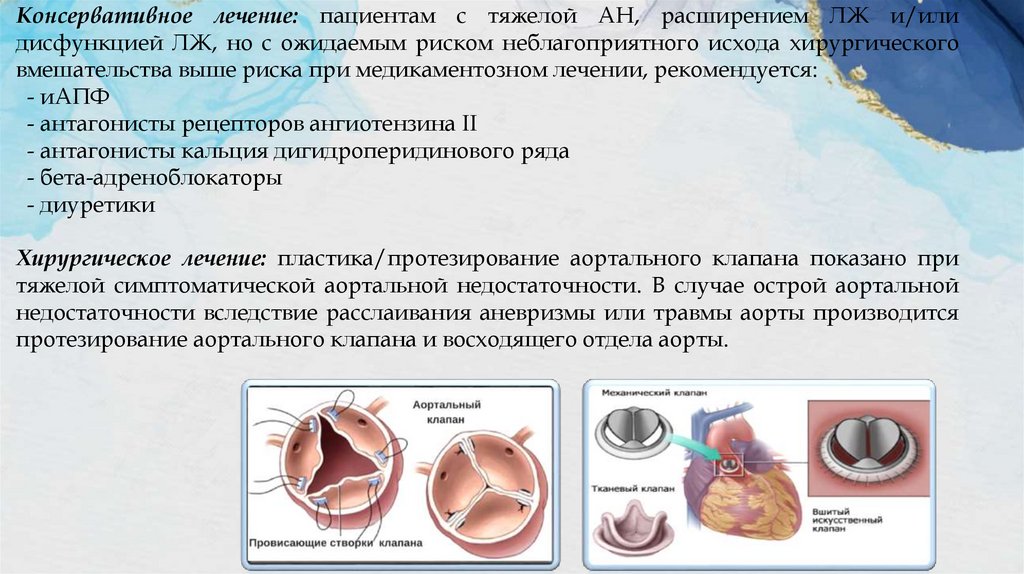
Хирургическое лечение: пластика/протезирование аортального клапана показано при
тяжелой симптоматической аортальной недостаточности. В случае острой аортальной
недостаточности вследствие расслаивания аневризмы или травмы аорты производится
протезирование аортального клапана и восходящего отдела аорты.
17.
Врождённая митральная недостаточностьВрожденная митральная недостаточность (ВМН) – это врожденный порок сердца
(ВПС), характеризующийся поражением клапанных, подклапанных структур митрального
клапана (МК) с возникновением обратного тока крови из левого желудочка (ЛЖ) в левое
предсердие (ЛП) во время систолы.
Этиология и патогенез:
Формирование
атриовентрикулярного
клапана
завершается
на
ранних
стадиях
эмбриологического развития. Любой из компонентов МК (фиброзное кольцо, створки,
сухожильные хорды и папиллярные мышцы) оказывается нефункциональным вследствие
дефектов эмбриональных закладок эндокарда, нарушений структуры соединительной ткани,
формирующей клапан, генетически обусловленной миксоматозной дегенерацией.
ВМН характеризуется постоянным обратным током крови в систолу из ЛЖ в ЛП. Изменения
гемодинамики зависят от выраженности регургитации. Перегрузка объемом приводит к
гипертрофии и дилатации левых камер сердца с развитием атриомегалии и, в последующем,
дилатации ЛЖ. Расширение левых камер сердца приводит к дополнительной дилатации
фиброзного кольца и дисфункции папиллярных мышц, что увеличивает объем регургитации. По
мере прогрессирования МР объем ЛЖ увеличивается, а сократительная функция снижается
(механизм Франк-Старлинга), что приводит к снижению фракции выброса с уменьшением
ударного объема и сердечного выброса.
18.
Причины приобретённой митральной недостаточности:Острая митральная недостаточность может развиваться вследствие
разрывов сосочковых мышц, сухожильных хорд, отрыва створок
митрального клапана при остром инфаркте миокарда, тупой травме
сердца, инфекционном эндокардите. Разрыв сосочковых мышц вследствие
инфаркта миокарда сопровождается летальным исходом в 80–90% случаев.
Развитие хронической митральной недостаточности может быть
обусловлено поражением клапана при системных заболеваниях:
ревматизме, склеродермии, системной красной волчанке, эозинофильном
эндокардите Леффлера. Ревматическая болезнь сердца обусловливает
около 14% всех случаев изолированной митральной недостаточности.
Ишемическая дисфункция митрального комплекса наблюдается у 10%
пациентов с постинфарктным кардиосклерозом. К митральной
недостаточности может приводить пролапс митрального клапана, надрыв,
укорочение или удлинение сухожильных хорд и папиллярных мышц. В
ряде случаев митральная недостаточность является следствием системных
дефектов соединительной ткани при синдромах Марфана и ЭлерсаДанлоса.
Относительная митральная недостаточность развивается в отсутствие
повреждения клапанного аппарата при дилатации полости левого
желудочка и расширении фиброзного кольца. Такие изменения
встречаются при дилатационной кардиомиопатии, прогрессирующем
течении артериальной гипертензии и ИБС, миокардитах, аортальных
пороках сердца.
19.
В клиническом течении митральной недостаточностивыделяют 3 стадии:
I (компенсированная стадия) - незначительная недостаточность митрального
клапана; митральная регургитация составляет 20-25% от систолического объема
крови. Митральная недостаточность компенсируется за счет гиперфункции
левых отделов сердца.
II (субкомпенсированная стадия) - митральная регургитация составляет 25-50%
от систолического объема крови. Развивается застой крови в легких и медленное
нарастание бивентрикулярной перегрузки.
III (декомпенсированная стадия) - резко выраженная недостаточность
митрального клапана. Возврат крови в левое предсердие в систолу составляет 5090%
от
систолического
объема.
Развивается
тотальная
сердечная
недостаточность.
20.
Клиническаякартина:
Врожденная
митральная
недостаточность не имеет специфических симптомов и
клиническая картина обусловлена, преимущественно,
признаками прогрессирующей СН, развивающейся по мере
увеличения объема митральной регургитации и ухудшения
систолической функции ЛЖ Если в стадию компенсации у
пациента могут отсутствовать жалобы, то по мере увеличения
объема МР и ухудшения систолической функции ЛЖ
появляются жалобы на одышку, быструю утомляемость и
сердцебиение при физической нагрузке, а далее и в покое,
кашель. По мере вовлечения правых камер сердца на фоне
повышения систолического давления в ЛА и снижения
сократительной способности ПЖ возможно появление
отеков,
гидроторакса.
Развитие
правожелудочковой
недостаточности
также
сопровождается
появлением
акроцианоза, увеличением печени, набуханием шейных вен,
асцитом. При компрессии возвратного гортанного нерва
расширенным левым предсердием или легочным стволом
возникает осиплость голоса или афония (синдром Ортнера).
У пациентов с бессимптомной тяжелой митральной
регургитацией обычно выслушивается шум в сердце в ходе
плановой диспансеризации или, либо развиваются аритмии
(чаще всего фибрилляции предсердий). В стадию
декомпенсации МН может манифестировать признаками
застойной сердечной недостаточности (одышка в покое,
отеки конечностей, отек легких).
21.
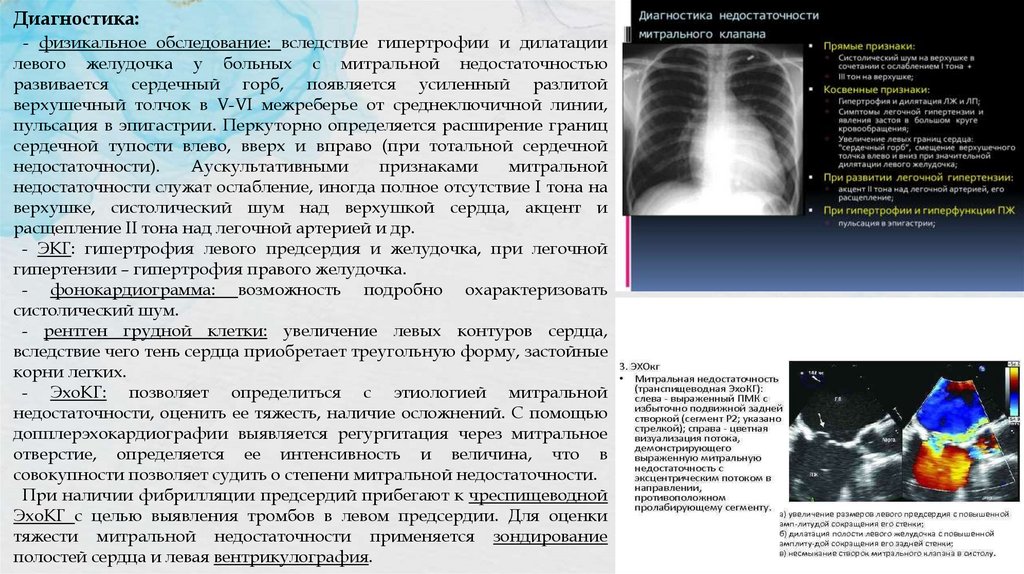
Диагностика:- физикальное обследование: вследствие гипертрофии и дилатации
левого желудочка у больных с митральной недостаточностью
развивается сердечный горб, появляется усиленный разлитой
верхушечный толчок в V-VI межреберье от среднеключичной линии,
пульсация в эпигастрии. Перкуторно определяется расширение границ
сердечной тупости влево, вверх и вправо (при тотальной сердечной
недостаточности).
Аускультативными
признаками
митральной
недостаточности служат ослабление, иногда полное отсутствие I тона на
верхушке, систолический шум над верхушкой сердца, акцент и
расщепление II тона над легочной артерией и др.
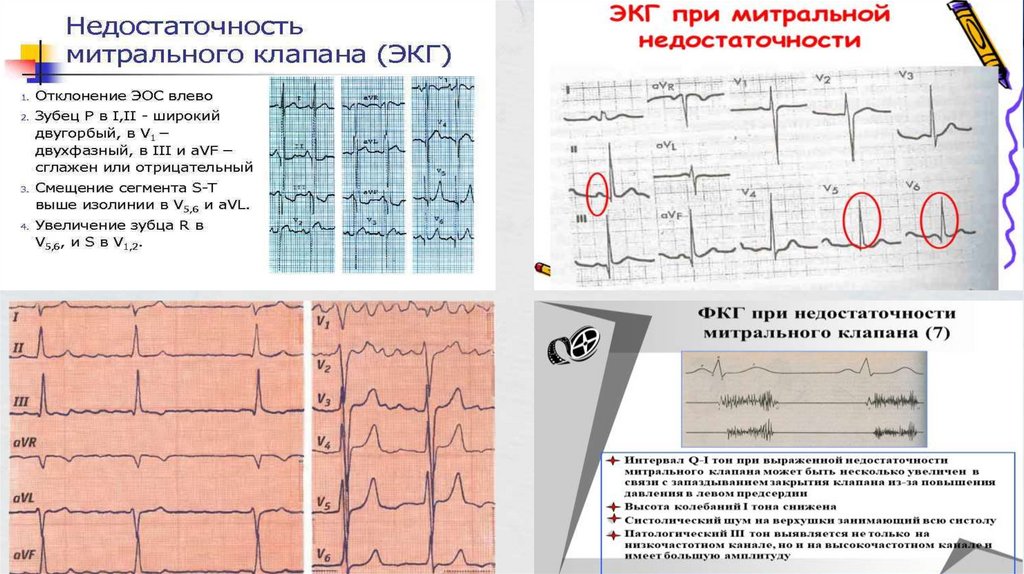
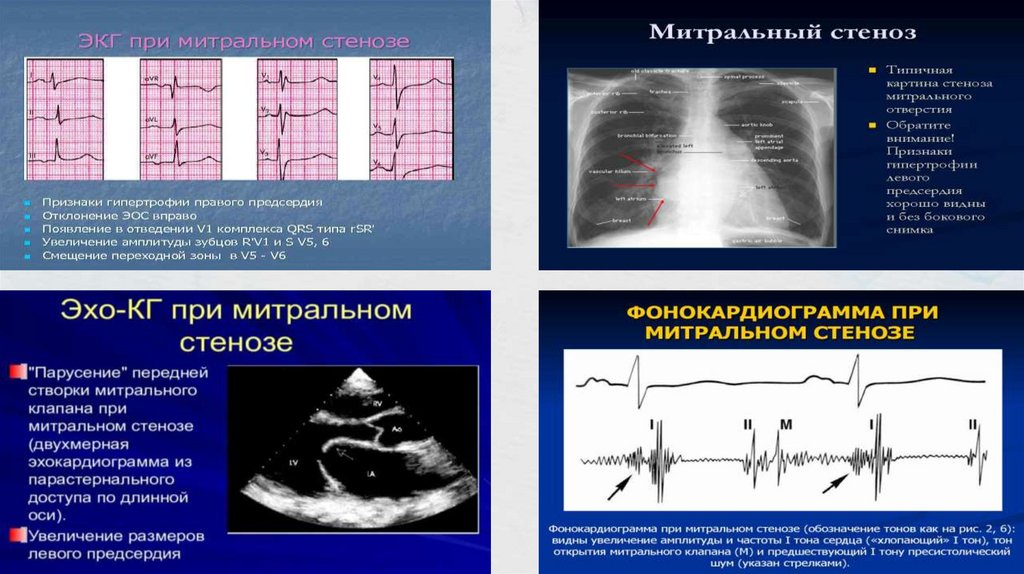
- ЭКГ: гипертрофия левого предсердия и желудочка, при легочной
гипертензии – гипертрофия правого желудочка.
- фонокардиограмма: возможность подробно охарактеризовать
систолический шум.
- рентген грудной клетки: увеличение левых контуров сердца,
вследствие чего тень сердца приобретает треугольную форму, застойные
корни легких.
- ЭхоКГ: позволяет определиться с этиологией митральной
недостаточности, оценить ее тяжесть, наличие осложнений. С помощью
допплерэхокардиографии выявляется регургитация через митральное
отверстие, определяется ее интенсивность и величина, что в
совокупности позволяет судить о степени митральной недостаточности.
При наличии фибрилляции предсердий прибегают к чреспищеводной
ЭхоКГ с целью выявления тромбов в левом предсердии. Для оценки
тяжести митральной недостаточности применяется зондирование
полостей сердца и левая вентрикулография.
22.
23.
Лечение:Острая МН – диуретики и периферические вазодилататоры.
Субкомпенсированная стадия - ингибиторы АПФ, бета-адреноблокаторы, вазодилататоры, сердечные
гликозиды, мочегонные препараты.
При развитии ФП – непрямые антикоагулянты.
Отсутствие кальциноза створок и сохранная подвижность клапанного аппарата - пластика
митрального клапана, аннулопластика, укорачивающей пластика хорд и др.
При наличии кальцификации клапана, выраженного утолщения хорд - протезирование митрального
клапана биологическим или механическим протезом.
24.
Аномалия ЭбштейнаАномалия Эбштейна (АЭ) - сложный врожденный порок сердца (ВПС), обусловленный смещением
септальной и задней створок трехстворчатого клапана (ТК) и характеризующийся необычайной
вариабельностью анатомических вариантов порока. Она включает широкий спектр анатомических и
функциональных аномалий трехстворчатого клапана и правого желудочка.
Этиология: На сегодняшний день доказано, что в определенной мере высокая частота порока во
внутриутробном периоде связана с приемом матерью препаратов лития. У женщин, принимавших в
течение первых триместров беременности препараты, содержащие карбонат лития, вероятность
появления детей с аномалией Эбштейна значительно увеличивается. Известно то, что у плодов, у
которых аномалия определяется внутриутробно, встречаются самые неблагоприятные анатомические
варианты порока, определяющие высокую смертность внутриутробно или сразу после рождения.
В литературе имеются сообщения о нормальных родах у неоперированных пациентках. Иными словами,
пациенты с незначительной недостаточностью ТК могут быть асимптомными достаточно долго, и такие
пациенты в хирургическом лечении не нуждаются.
Взрослые с аномалией Эбштейна должны наблюдаться в специализированных центрах, имеющих опыт
лечения ВПС у взрослых, в частности аномалии Эбштейна.
25.
Особенности гемодинамики:Анатомическую основу аномалии Эбштейна составляет неправильное расположение трехстворчатого клапана, при котором его
створки (обычно задняя и перегородочная) оказываются деформированы и смещены в полость правого желудочка. В этом случае
створки клапана крепятся ниже фиброзного кольца, иногда на уровне выходного отдела правого желудочка. Смещение клапана
сопровождается атриализацией правого желудочка, т. е. состоянием, при котором часть правого желудочка составляет
продолжение и единую полостью с правым предсердием.
Таким образом, смещение створок обусловливает деление правого желудочка на 2 функциональные части: надклапанную
атриализованную, образующую общую полость с правым предсердием, и подклапанную – меньшую по размерам,
функционирующую как правый желудочек. При этом правое предсердие и атриализованная часть правого желудочка
значительно расширены, а полость правого желудочка – уменьшена.
Гемодинамические нарушения, сопутствующие аномалии Эбштейна, зависит от степени трикуспидальной недостаточности,
размеров функционирующего правого желудочка и величины сброса крови справа налево через межпредсердные
коммуникации.
Электрические процессы в правом предсердии, состоящем из двух частей, не синхронизированы: сокращение собственно
правого предсердия происходит в систолу предсердий, а атриализованной части правого желудочка - в систолу желудочков.
Вследствие трикуспидальной недостаточности происходит регургитация венозной крови обратно в правое предсердие; ударный
объем правого желудочка снижается, что сопровождается уменьшением легочного кровотока. Правое предсердие дилатируется
и гипертрофируется, давление в нем прогрессирующе повышается, вызывая возникновение венозно-артериального шунта через
дефект в межпредсердной перегородке.
Право-левый сброс крови играет двоякую роль: с одной стороны он позволяет избежать перегрузки правого предсердия и
компенсирует порок; с другой стороны - способствует развитию артериальной гипоксемии.
26.
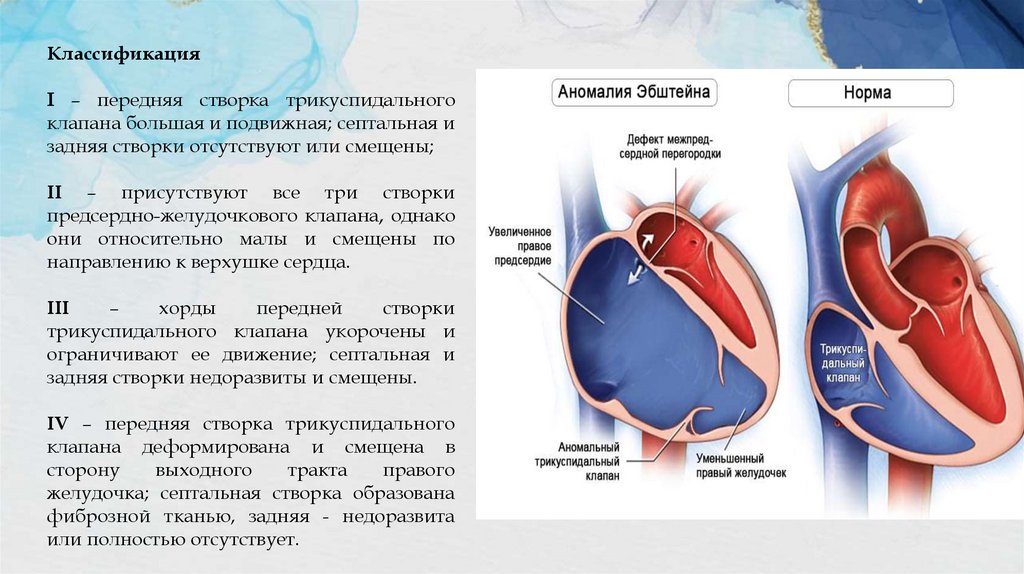
КлассификацияI – передняя створка трикуспидального
клапана большая и подвижная; септальная и
задняя створки отсутствуют или смещены;
II – присутствуют все три створки
предсердно-желудочкового клапана, однако
они относительно малы и смещены по
направлению к верхушке сердца.
III
–
хорды
передней
створки
трикуспидального клапана укорочены и
ограничивают ее движение; септальная и
задняя створки недоразвиты и смещены.
IV – передняя створка трикуспидального
клапана деформирована и смещена в
сторону
выходного
тракта
правого
желудочка; септальная створка образована
фиброзной тканью, задняя - недоразвита
или полностью отсутствует.
27.
Клиническая картинаКлинические проявления аномалии Эбштейна зависят от величины и степени смещения створок
трехстворчатого клапана, размеров атриализованной части правого желудочка и размеры межпредсердного
сообщения. Клиническая картина аномалии Эбштейна у ряда пациентов бессимптомна, и они ведут обычный
образ жизни. В ряде случаев они могут выполнять даже тяжелую физическую работу. У этой категории
пациентов признаки нарушения кровообращения появляются только с течением времени. У других пациентов,
при раннем появлении цианоза, заболевание манифестирует в раннем детстве и резко прогрессирует.
Постоянной жалобой пациентов с аномалией Эбштейна является одышка. У подавляющего большинства
пациентов одышка возникает только при физической нагрузке. Около 90% пациентов страдают от быстрой
утомляемости. Патогномоничным признаком для аномалии Эбштейна, по нашему мнению, являются приступы
сердцебиения (80-90% пациентов). Аномалия Эбштейна часто сопровождается цианозом.
Диагностика
- физикальное обследование: при осмотре отмечается выраженный цианоз лица, одышка и усиленная
пульсация яремных вен и сердцебиение.
Аускультативно выслушивается:
o Широкое расщепление первого тона (за счет более позднего закрытия удлиненной передней створки
трехстворчатого клапана).
o Систолический шум трикуспидальной недостаточности по классификации Levin 2-3/6, максимальный в точке
проекции трехстворчатого клапана – у основания мечевидного отростка, и чуть левее по направлению к
верхушке сердца (проекция смещенного клапана).
o Ранний диастолический шум образуется при колебательных движениях удлиненной передней створки.
o У большинства пациентов определялся систолический шум дующего характера.
28.
- ЭхоКГ: смещение книзу створок трикуспидального клапана,увеличение размеров правого предсердия, замедленное
смыкание трехстворчатого клапана, смещение створок, наличие
атриализированного правого желудочка, шунтирующий проток
крови справа налево через ДМПП (по данным допплерэхокардиографии).
Фетальная
ЭхоКГ,
выполненная
в
пренатальном периоде, позволяет диагностировать аномалию
Эбштейна в 60% случаев.
- ЭКГ: отклонение ЭОС вправо, признаки гипертрофии и
дилатации
правого
предсердия,
пароксизмальную
желудочковую экстрасистолию и предсердную тахикардию
(синдром WPW), трепетание предсердий, мерцательную
аритмию, полную (неполную) блокаду правой ножки пучка Гиса.
фонокардиограмма:
характеризуется
наличием
систолического шума в проекции правого желудочка;
запаздыванием I тона; раздвоенным II тоном; III, IV тонами
большой амплитуды.
- рентген грудной клетки: резкое увеличение правых отделов
сердца, шаровидной формой тени сердца, повышенной
прозрачностью легочных полей.
Для уточнения формы и степени тяжести аномалии Эбштейна
проводится
МРТ,
зондирование
полостей
сердца,
вентрикулография.
29.
30.
Консервативное лечение:1. Сердечные гликозиды (Дигоксин 0,05-0,08 мг/кг/сут). Данная группа
показана при развитии сердечной недостаточности. Применение дигоксина противопоказано детям до 3 лет.
2. Диуретики (Фуросемид - начальная разовая доза у детей определяется из расчета 1-2 мг/кг массы тела/сут
с возможным увеличением дозы до максимальной 6 мг/кг/сут);
3. Антиаритмики. Пропафенон (Дозы и схема лечения взрослым подбираются индивидуально. В период
подбора дозы и для поддерживающей терапии суточная доза составляет 450–600 мг; максимальная суточная
доза — 900 мг в 3 приема). Показана данная группа препаратов при нарушениях ритма сердца, при
развитии синдрома Вольфа-Паркинсона-Уайта. У детей возможно применение вне зарегистрированных
показаний только по решению врачебной комиссии.
Хирургическое лечение: Показаниями к хирургической коррекции аномалии Эбштейна служат наличие
жалоб, недостаточности кровообращения и нарушений ритма сердца. Оптимальным для операции является
возраст 15-17 лет, при тяжелой форме порока вмешательство проводится в более ранние сроки.
Радикальная корригирующая операция при аномалии Эбштейна включает пластику или протезирование
трикуспидального клапана, пластику ДМПП, ликвидацию атриализованного правого желудочка. В
некоторых случаях целесообразным является выполнение операции Фонтена. Иногда на первом этапе для
увеличения легочного кровотока и уменьшения гипоксемии прибегают к наложению анастомоза по
Блэлоку-Тауссигу, наложению двунаправленного кава-пульмонального анастомоза.
Добавочные пути проведения импульса при WPW синдроме подвергаются радиочастотной абляции. Для
лечения аритмий применяется имплантация кардиостимуляторов или кардиовертер-дефибрилляторов.
31.
Митральный стенозМитральный стеноз (МС) - обструкция пути притока ЛЖ на уровне МК в результате структурной деформации
аппарата МК, препятствующая необходимому открытию МК во время диастолического наполнения левого желудочка.
Этиология: Самая частая причина МС ревматический кардит. Изолированный МС определяется у 40% пациентов с
ревматическими пороками сердца, а ревматический анамнез присутствует приблизительно у 60% пациентов с чистым
МС. Соотношение женщин и мужчин с изолированным МС составляет 2:1. Врожденный порок МК встречается редко и
наблюдается главным образом у детей. Причиной приобретенной обструкции МК выступает ревматизм, реже –
миксома левого предсердия, шаровидный тромб, затрудняющий функционирование клапана, мукополисахаридоз и
резкий кальциноз фиброзного кольца. Ревматический процесс приводит к утолщению и кальцификации створок,
сращению комиссур и хорд или их комбинации. Результат –воронкообразный митральный аппарат со значительным
уменьшением площади отверстия.
Патогенез: В норме площадь митрального отверстия составляет 4-6 кв. см, а его сужение до 2 кв. см и менее
сопровождается появлением нарушений внутрисердечной гемодинамики. Стенозирование атриовентрикулярного
отверстия препятствует изгнанию крови из левого предсердия в желудочек → включаются компенсаторные механизмы:
давление в полости предсердия повышается с 5 до 20-25 мм рт. ст., происходит удлинение систолы левого предсердия →
гипертрофия миокарда левого предсердия → дальнейшее прогрессирование порока и рост трансмитрального
гардиента давления сопровождается ретроградным повышением давления в системе легочных сосудов → развитие
легочной гипертензии → увеличивается нагрузка на правый желудочек и затрудняется опорожнение правого
предсердия →
гипертрофия правых отделов сердца → в силу необходимости преодоления значительного
сопротивления в легочной артерии и развития склеротических и дистрофических изменений миокарда снижается
сократительная функция правого желудочка и происходит его дилатация → возрастает нагрузка на правое предсердие,
что в конечном итоге приводит в декомпенсации кровообращения по большому кругу.
32.
КлассификацияПо площади сужения левого атриовентрикулярного отверстия
выделяют 4 степени митрального стеноза:
I степень – незначительный стеноз (площадь отверстия > 3 кв. см)
II степень - умеренный стеноз (площадь отверстия 2,3-2,9 кв. см)
III степень - выраженный стеноз (площадь отверстия 1,7–2,2 кв. см)
IV степень - критический стеноз (площадь отверстия 1,0–1,6 кв. см)
В
соответствии
с
прогрессированием
гемодинамических
расстройств течение митрального стеноза проходит 5 стадий:
I – стадия полной компенсации митрального стеноза левым
предсердием. Субъективные жалобы отсутствуют, однако
аускультативно выявляются прямые признаки стеноза.
II - стадия нарушений кровообращения в малом круге.
Субъективные симптомы возникают только при физической
нагрузке.
III – стадия выраженных признаков застоя в малом круге и
начальных признаков нарушения кровообращения в большом
круге.
IV - стадия выраженных признаков застоя в малом и большом
круге кровообращения. У больных развивается мерцательная
аритмия.
V – дистрофическая стадия, соответствует III стадии сердечной
недостаточности
33.
Клиническая картина:Клинические
признаки
митрального
стеноза,
как
правило,
возникают
при
площади
атриовентрикулярного отверстия менее 2 кв. см. Отмечается повышенная утомляемость, одышка при
физическом усилии, а затем и в покое, кашель с выделением прожилок крови в мокроте, тахикардия,
нарушение ритма сердца по типу экстрасистолии и мерцательной аритмии. При выраженном стенозе
возникает ортопноэ, ночные приступы сердечной астмы, в более тяжелых случаях - отек легких.
В случае значительной гипертрофии левого предсердия может происходить сдавление возвратного
нерва с развитием дисфонии. Около 10% пациентов со стенозом митрального отверстия предъявляют
жалобы на боли в сердце, не связанные с физической нагрузкой. При сопутствующем коронарном
атеросклерозе, субэндокардиальной ишемии возможны приступы стенокардии. Пациенты часто
страдают повторными бронхитами, бронхопневмонией, крупозной пневмонией. При сочетании стеноза
с митральной недостаточностью часто присоединяется бактериальный эндокардит.
Внешний вид больных с митральным стенозом характеризуется цианозом губ, кончика носа и ногтей,
наличием ограниченной багрово-синюшной окраски щек («митральный румянец» или «румянец
куклы»). Гипертрофия и дилатация правого желудочка нередко обусловливают развитие сердечного
горба.
По мере развития правожелудочковой недостаточности появляется тяжесть в животе, гептомегалия,
периферические отеки, набухание шейных вен, водянка полостей (правосторонний гидроторакс, асцит).
Основной причиной летального исхода при митральном пороке служит тромбоэмболия легочной
артерии.
34.
Диагностика:- анамнез: ревматический анамнез удается проследить у 50–60% пациентов с митральным стенозом.
- физикальное обследование: пальпация надсердечной области выявляет так называемое «кошачье
мурлыканье» - пресистолическое дрожанье, перкуторно границы сердца смещены вверх и вправо.
Аускультативная картина характеризуется хлопающим I тоном и тоном открытия митрального клапана
(«митральный щелчок»), наличием диастолического шума.
- фонокардиография: позволяет соотнести выслушиваемый шум с той или иной фазой сердечного цикла.
- ЭКГ: выявляет гипертрофию левого предсердия и правого желудочка, нарушения сердечного ритма
(мерцательную аритмию, экстрасистолию, пароксизмальную тахикардию, трепетание предсердий),
блокаду правой ножки пучка Гиса.
- ЭхоКГ: удается обнаружить уменьшение площади митрального отверстия, уплотнение стенок
митрального клапана и фиброзного кольца, увеличение левого предсердия. Чреспищеводная ЭхоКГ при
митральном стенозе необходима для исключения вегетаций и кальциноза клапана, наличия тромбов в
левом предсердии.
- рентген: (рентгенографии грудной клетки, рентгенографии сердца с контрастированием пищевода)
характеризуются выбуханием дуги легочной артерии, левого предсердия и правого желудочка,
митральной конфигурацией сердца, расширением теней полых вен, усилением легочного рисунка и
другими косвенными признаками митрального стеноза.
- инвазивная диагностика: при зондировании полостей сердца обнаруживается повышенное давление в
левом предсердии и правых отделах сердца, увеличение трансмитрального градиента давления. Левые
вентрикулография и атриография, а также коронарная ангиография показаны всем претендентам на
протезирование митрального клапана.
35.
36.
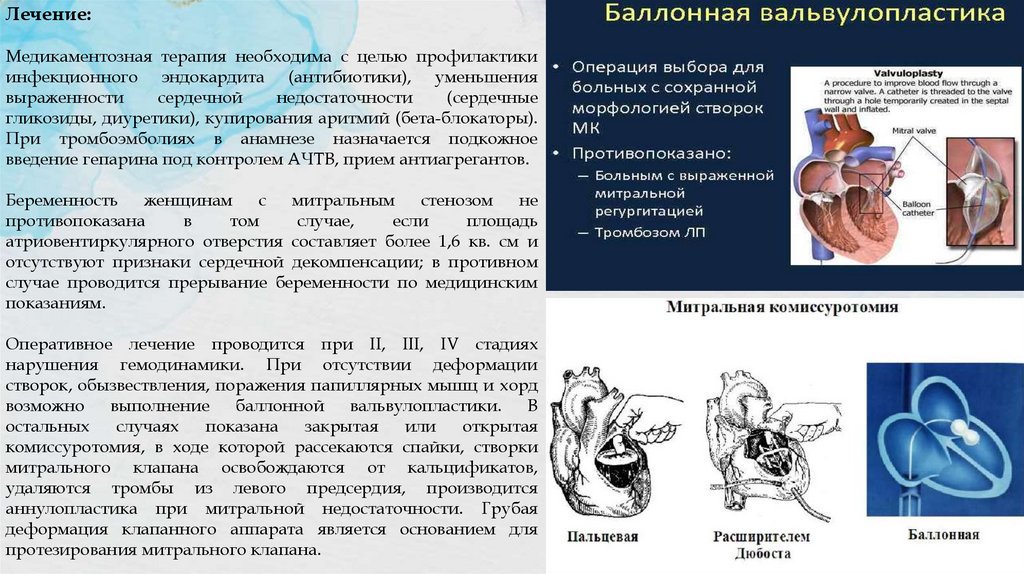
Лечение:Медикаментозная терапия необходима с целью профилактики
инфекционного эндокардита (антибиотики), уменьшения
выраженности
сердечной
недостаточности
(сердечные
гликозиды, диуретики), купирования аритмий (бета-блокаторы).
При тромбоэмболиях в анамнезе назначается подкожное
введение гепарина под контролем АЧТВ, прием антиагрегантов.
Беременность
женщинам
с
митральным
стенозом
не
противопоказана
в
том
случае,
если
площадь
атриовентиркулярного отверстия составляет более 1,6 кв. см и
отсутствуют признаки сердечной декомпенсации; в противном
случае проводится прерывание беременности по медицинским
показаниям.
Оперативное лечение проводится при II, III, IV стадиях
нарушения гемодинамики. При отсутствии деформации
створок, обызвествления, поражения папиллярных мышц и хорд
возможно
выполнение
баллонной
вальвулопластики.
В
остальных
случаях
показана
закрытая
или
открытая
комиссуротомия, в ходе которой рассекаются спайки, створки
митрального клапана освобождаются от кальцификатов,
удаляются тромбы из левого предсердия, производится
аннулопластика при митральной недостаточности. Грубая
деформация клапанного аппарата является основанием для
протезирования митрального клапана.
37.
Аортальный стенозАортальный
стеноз
(АС)
порок
сердца,
сопровождающийся деформацией створок и /или
сужением клапанного отверстия.
Этиология: Самая частая причина АС у взрослых –
кальцификация cтворок нормального трехстворчатого
клапана или врожденного двустворчатого клапана.
Кальциноз распространяется от основания створок к
их
свободному
краю,
вызывая
ограничение
подвижности створок и уменьшение площади
отверстия аорты без сращения по комиссурам.
Кальцинированный АС – активный патологический
процесс, характеризующийся отложением липидов,
воспалением и кальцификацией, во многом подобен
атеросклерозу.
АС
ревматической
этиологии,
обусловлен сращением по комиссурам с последующим
разрушением и в итоге кальцификацией краев
створок, встречается реже и нередко сопровождается
поражением МК.
Врожденный порок АК может также привести к
стенозу и является более частой причиной в молодом
возрасте.
38.
Патогенез: При аортальном стенозе развиваются грубыенарушения внутрисердечной, а затем и общей гемодинамики.
Это связано с затрудненным опорожнением полости левого
желудочка → увеличение градиента систолического давления
между левым желудочком и аортой, который может достигать
от 20 до 100 и более мм рт. ст. → повышенная нагрузка →
гипертрофия → сдавление гипертрофированным миокардом
субэндокардиальных сосудов и повышение конечного
диастолического давления в ЛЖ → нарушение коронарной
перфузии → коронарная недостаточность → снижение
сократительной способности гипертрофированного ЛЖ →
уменьшается величина ударного объема и фракции выброса →
миогенная левожелудочковая дилатация → повышение
конечного
диастолического
давления
→
развитие
систолической дисфункции левого желудочка → повышается
давление в левом предсердии и малом круге кровообращения,
т. е. развивается артериальная легочная гипертензия.
При этом клиническая картина аортального стеноза может
усугубляться относительной недостаточностью митрального
клапана («митрализацией» аортального порока). Высокое
давление в системе легочной артерии закономерно приводит к
компенсаторной гипертрофии правого желудочка, а затем и к
тотальной сердечной недостаточности.
39.
КлассификацияВ зависимости от степени гемодинамических нарушений аортальный стеноз
может
протекать
по
компенсированному
или
декомпенсированному
(критическому) клиническому варианту, в связи с чем выделяется 5 стадий.
I стадия (полная компенсация). Аортальный стеноз может быть выявлен только
аускультативно, степень сужения устья аорты незначительна. Больным
необходимо динамическое наблюдение кардиолога; хирургическое лечение не
показано.
II стадия (скрытая сердечная недостаточность). Предъявляются жалобы на
быструю утомляемость, одышку при умеренной физической нагрузке,
головокружение. Признаки аортального стеноза определяются по данным ЭКГ и
рентгенографии, градиент давления в диапазоне 36–65 мм рт. ст., что служит
показанием к хирургической коррекции порока.
III стадия (относительная коронарная недостаточность). Типично усиление
одышки, возникновение стенокардии, обмороков. Градиент систолического
давления превышает 65 мм рт. ст. Хирургическое лечение аортального стеноза на
данной стадии возможно и необходимо.
IV стадия (выраженная сердечная недостаточность). Беспокоит одышка в покое,
ночные приступы сердечной астмы. Хирургическая коррекция порока в
большинстве случаев уже исключена; у некоторых больных кардиохирургическое
лечение потенциально возможно, но с меньшим эффектом.
V стадия (терминальная). Неуклонно прогрессирует сердечная недостаточность,
выражены одышка и отечный синдром. Медикаментозное лечение позволяет
добиться лишь кратковременного улучшения; хирургическая коррекция
аортального стеноза противопоказана.
40.
Диагностика:-
-
-
физикальное обследование: внешний вид больного с аортальным стенозом
характеризуется бледностью кожных покровов («аортальной бледностью»),
обусловленной склонностью к периферическим вазоконстрикторным
реакциям;
в
поздних
стадиях
может
отмечаться
акроцианоз.
Периферические отеки выявляются при аортальном стенозе тяжелой
степени. При перкуссии определяется расширение границ сердца влево и
вниз;
пальпаторно
ощущается
смещение
верхушечного
толчка,
систолическое дрожание в яремной ямке. Аускультативными признаками
аортального стеноза служит грубый систолический шум над аортой и над
митральным клапаном, приглушение I и II тонов на аорте.
фонокардиограмма: изменение тона и патологические шумы.
ЭКГ: признаки гипертрофии левого желудочка, аритмии, иногда – блокады.
рентген: в период декомпенсации на рентгенограммах выявляется
расширение тени левого желудочка в виде удлинения дуги левого контура
сердца, характерная аортальная конфигурация сердца, постстенотическая
дилатация аорты, признаки легочной гипертензии. Вентрикулография
необходима для выявления сопутствующей митральной недостаточности.
Аортография и коронарография применяются для дифференциальной
диагностики аортального стеноза с аневризмой восходящего отдела аорты и
ИБС.
ЭхоКГ: утолщение заслонок аортального клапана, ограничение амплитуды
движения створок клапана в систолу, гипертрофия стенок левого
желудочка.
зондирование полостей сердца: позволяет косвенно судить о степени
аортального стеноза.
41.
42.
Консервативноелечение:
Медикаментозная
терапия при аортальном стенозе направлена на
устранение
аритмий,
профилактику
ИБС,
нормализацию АД, замедление прогрессирования
сердечной недостаточности.
Хирургическое
лечение:
Радикальная
хирургическая коррекция аортального стеноза
показана при первых клинических проявлениях
порока – появлении одышки, ангинозных болей,
синкопальных состояний.
- эндоваскулярная
балонная
дилатация
аортального стеноза
- пластика
аортального
клапана
(вальвулопластика)
- в детской кардиохирургии нередко выполняется
операция Росса, предполагающая пересадку
клапана легочной артерии в аортальную
позицию.
- пластика надклапанного или подклапанного
аортального стеноза
- протезирование
аортального
клапана
(пациентам с искусственным клапаном требуется
пожизненный прием антикоагулянтов)
43.
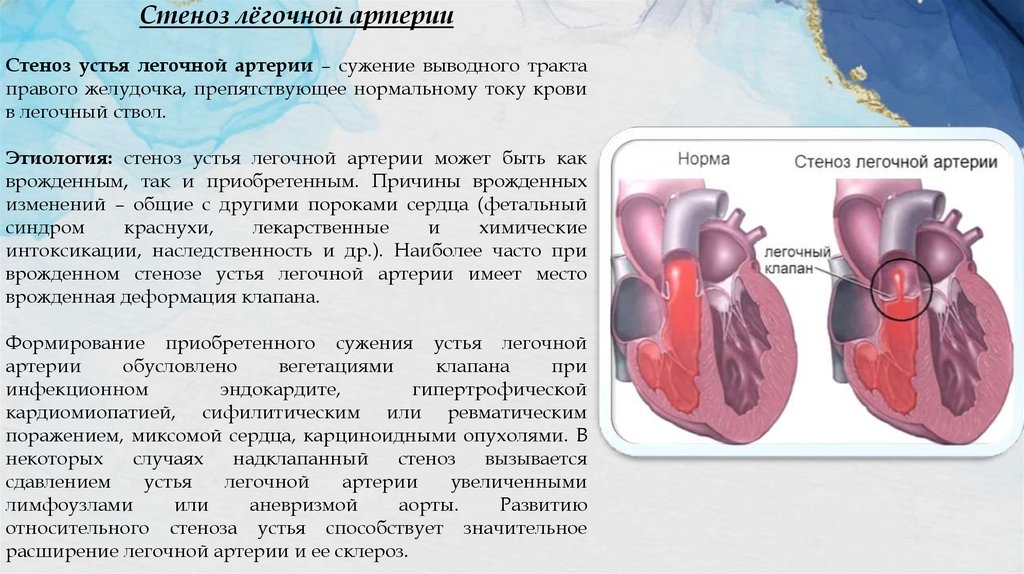
Стеноз лёгочной артерииСтеноз устья легочной артерии – сужение выводного тракта
правого желудочка, препятствующее нормальному току крови
в легочный ствол.
Этиология: стеноз устья легочной артерии может быть как
врожденным, так и приобретенным. Причины врожденных
изменений – общие с другими пороками сердца (фетальный
синдром
краснухи,
лекарственные
и
химические
интоксикации, наследственность и др.). Наиболее часто при
врожденном стенозе устья легочной артерии имеет место
врожденная деформация клапана.
Формирование приобретенного сужения устья легочной
артерии
обусловлено
вегетациями
клапана
при
инфекционном
эндокардите,
гипертрофической
кардиомиопатией, сифилитическим или ревматическим
поражением, миксомой сердца, карциноидными опухолями. В
некоторых
случаях
надклапанный
стеноз
вызывается
сдавлением
устья
легочной
артерии
увеличенными
лимфоузлами
или
аневризмой
аорты.
Развитию
относительного стеноза устья способствует значительное
расширение легочной артерии и ее склероз.
44.
Гемодинамика: Препятствие выходу из правого желудочка → значительное повышение в нем давления.Градиент давления на клапане отражает усиленную работу желудочка по обеспечению достаточного
сердечного выброса. При умеренном стенозе легочный кровоток остается адекватным определенный период
времени. Однако при тяжелой форме порока быстро развивается декомпенсация правого желудочка и
возрастает конечное диастолическое давление в нем → повышается давление в правом предсердии → может
возникнуть право-левый сброс крови через межпредсердное сообщение → снижение насыщения кислородом
артериальной крови → уменьшаются антеградный кровоток из правого желудочка, легочный кровоток и
возврат крови к левым отделам → снижение системного выброса. Последний может сохраняться на
удовлетворительном уровне в случаях адекватного перехода крови в левые отделы через открытое овальное
окно.
Классификация
В практических целях используется классификация, основанная на определении уровня систолического АД в
правом желудочке и градиента давления между правым желудочком и легочной артерией:
I стадия (умеренный стеноз устья легочной артерии) — систолическое давление в правом желудочке менее
60 мм рт. ст.; градиент давления 20-30 мм рт. ст.
II стадия (выраженный стеноз устья легочной артерии) — систолическое давление в правом желудочке от
60 до 100 мм рт. ст.; градиент давления 30-80 мм рт. ст.
III стадия (резко выраженный стеноз устья легочной артерии) — систолическое давление в правом
желудочке более 100 мм рт. ст.; градиент давления выше 80 мм рт. ст.
IV стадия (декомпенсация) – развивается дистрофия миокарда, тяжелое нарушение кровообращения.
Систолическое АД в правом желудочке снижается в связи с развитием его сократительной недостаточности.
45.
Клиническая картина: и время ее появления зависят от степени стеноза. При небольшойобструкции у ребенка отсутствуют жалобы, развитие его не страдает, цианоза не возникает.
Нередко патология сердца проявляется лишь шумом, который обнаруживают случайно. В то же
время
критический
легочный
стеноз
характеризуется
ранней
правожелудочковой
недостаточностью (увеличенная плотная печень, отечность), одышкой, центральным цианозом,
синдромом низкого сердечного выброса (угнетение ЦНС, холодные цианотичные конечности,
метаболический ацидоз).
Диагностика:
- физикальное обследование: Перкуторно границы сердца смещены вправо, при пальпации
определяется систолическая пульсация правого желудочка. Данные аускультации и
фонокардиографии характеризуются наличием грубого систолического шума, ослаблением II тона
над легочной артерией и его расщеплением.
- рентген: расширение границ сердца, постстенотическое расширение ствола легочной артерии,
обеднение легочного рисунка.
- ЭКГ: признаки перегрузки правого желудочка, отклонение ЭОС вправо.
- ЭхоКГ: дилатация правого желудочка, постстенотическое расширение легочной артерии.
- допплерография: позволяет выявить и определить разницу давления между правым желудочком
и легочным стволом.
- зондирование правых отделов сердца: величина давления в правом желудочке и градиент
давления между ним и легочной артерией.
- вентрикулография: увеличением полости правого желудочка, характерным замедлением
исчезновения контраста из правого желудочка.
46.
ЭКГ ребёнка, 1,5 года, состенозом
устья
лёгочной
артерии
47.
Лечение: Единственным эффективным методомлечения
порока
служит
хирургическое
устранение стеноза устья легочной артерии.
Операция показана при II и III стадии стеноза.
При клапанном стенозе выполняется открытая
вальвулопластика
(рассечение
сросшихся
комиссур) или эндоваскулярная баллонная
вальвулопластика.
Пластика надклапанного стеноза легочной
артерии предполагает реконструкцию зоны
сужения
с
использованием
ксеноперикардиального протеза или заплаты.
При
подклапанном
стенозе
производится
инфундибулэктомия
иссечение
гипертрофированной
мышечной
ткани
в
области выходного тракта правого желудочка.
Осложнениями хирургического лечения стеноза
может
явиться
недостаточность
клапана
легочной артерии различной степени.
48.
Триада, тетрада, пентада ФаллоТриада Фалло – сложная врожденная патология сердца, морфологическую
основу которой составляют три компонента: дефект межпредсердной
перегородки, стеноз (чаще клапанный) легочной артерии и гипертрофия
правого желудочка.
Тетрада Фалло – сочетанная врожденная аномалия сердца, характеризующаяся
стенозом выводного тракта правого желудочка, дефектом межжелудочковой
перегородки, декстропозицией аорты и гипертрофией миокарда правого
желудочка.
Пентада Фалло – редкий врождённый порок сердца, характеризующийся
стенозом легочной артерии, дефектом межжелудочковой перегородки,
смещением устья аорты вправо, гипертрофией миокарда преимущественно
правого желудочка и дефектом межпредсердной перегородки.
Этиология: морфологическая закладка сердца плода происходит в первый
триместр эмбрионального развития. В этот период под влиянием различных
неблагоприятных причин нормальное формирование сердца ребенка может
нарушаться. Негативными факторами могут выступать вирусные заболевания
беременной (краснуха, грипп, корь), эндокринные расстройства (сахарный
диабет), употребление алкоголя, прием лекарственных средств, авитаминозы,
хроническая гипоксия плода, облучение гамма-лучами и др. В формировании
данных пороков не отрицается роль наследственного фактора и хромосомных
мутаций.
49.
Особенности гемодинамики:Триада Фалло: умеренный стеноз → компенсация за счет повышения систолического давления в ПЖ →
адекватный уровень легочного кровотока → давление в правом предсердии нормальное → через
межпредсердный дефект происходит незначительный артериовенозный сброс из левого предсердия в правое
→ цианоз отсутствует, минутный объем легочного круга может быть несколько увеличен по сравнению с
нормой.
В случае более выраженного стеноза или длительного существования триады Фалло препятствие на пути
выхода крови из правого желудочка приводит к его повышенной работе → возрастает объемная перегрузка
правого желудочка → значительное повышение в нем как систолического, так и диастолического давления →
давление в правом предсердии увеличивается → смена направления шунта – венозная кровь начинает
сбрасываться из правого предсердия в левое → гипоксемия, уменьшение минутного объема малого круга и
возрастание минутного объема большого круга кровообращения, развитие относительной трикуспидальной
недостаточности.
Тетрада Фалло: Выраженность гемодинамических нарушений определяются степенью стеноза легочной
артерии и дефектом МЖП.
Направление и сброс крови определяется градиентом сопротивления участка стеноза ЛА и сосудов
большого круга кровообращения. Сброс крови справа налево → уменьшается МОК в малом круге
кровообращения → артериальная гипоксемия, компенсаторная полицитемия, гемоконцентрация (эритроциты
8–10 млн/мл, Ht – 70 – 80 %) → увеличение кислородной емкости крови.
Пентада Фалло: имеется дефект межпредсердной перегородки с дополнительным сбросом крови через него.
При сбросе крови справа налево → артериальная гипоксемия; при обратном сбросе из левого предсердия в
правое → некоторая компенсация ее, но увеличивается нагрузка правого желудочка.
50.
Клиническая картина и диагностика:ЭКГ:
1) гипертрофия и перегрузка правого желудочка;
Триада Фалло:
Жалобы: одышка, резко усиливающаяся при нагрузке, 2) гипертрофия правого предсердия.
вплоть до потери сознания.
ФКГ:
Осмотр, пальпация, перкуссия:
1) ромбовидный систолический шум во II м/р слева от
1) цианоз, вначале при нагрузке, а в более поздних
грудины;
стадиях и в покое;
2) снижение амплитуды II тона на легочной артерии
2) пальцы в виде барабанных палочек;
вплоть до полного исчезновения.
3) сердечный горб;
4) расширение перкуторных границ сердца вправо.
Рентгенодиагностика:
Аускультация:
1) митральная форма сердца;
2) увеличение правого предсердия;
1) грубый систолический шум с эпицентром во II м/р 3) увеличение правого желудочка;
слева от грудины;
4) удлинение и выбухание ствола легочной артерии;
2) ослабление или отсутствие II тона над легочной
5) обеднение легочного рисунка.
артерией.
ЭхоКГ: возможна визуализация всех структурных
компонентов триады Фалло.
51.
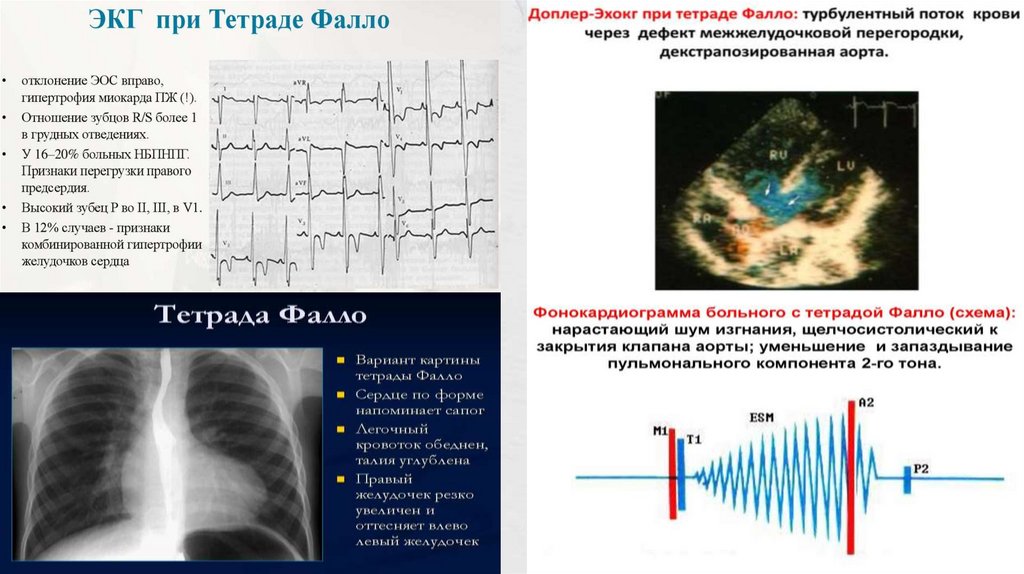
Тетрада и пентада Фалло:ЭКГ:
Жалобы: одышка, усиливающаяся при малейшей
нагрузке. Часто одышечно-цианотичные приступы
(гипоксические приступы).
1) гипертрофия и перегрузка правого желудочка;
2) гипертрофия правого предсердия.
Осмотр, пальпация, перкуссия:
1) отставание в физическом развитии;
2) диффузный цианоз;
3) пальцы в виде барабанных палочек;
4) сердечный горб;
5) расширение перкуторных границ сердца вправо.
Аускультация:
ФКГ:
1) ромбо- или лентовидный систолический шум с
эпицентром в III— IV м/р слева от грудины;
2) увеличение амплитуды I тона на верхушке;
3) снижение амплитуды II тона на легочной артерии.
Рентгенодиагностика:
1) аортальная форма сердца;
2) резкое увеличение правого желудочка;
3) обеднение легочного рисунка.
1) грубый систолический шум в III—IV м/р слева от
грудины;
2) систолический шум во II—III м/р слева от грудины; ЭхоКГ: возможна визуализация всех структурных
3) усиление I тона на верхушке;
компонентов порока.
4) ослабление II тона на легочной артерии.
52.
53.
Лечение:Триада Фалло: при возникновении гипоксемических кризов проводится кислородотерапия, вводятся
седативные препараты, бета-адреноблокаторы, сердечные гликозиды.
Хирургическое лечение: паллиативные операции не проводятся, т.к. вызываеют еще большую перегрузку
правых отделов сердца. Выполняют одномоментное или поэтапное устранение стеноза легочной артерии
путем вальвулотомии по Броку и закрытие дефекта межпредсердной перегородки. (Оперативное
вмешательство не проводят при триадах Фалло, осложненных необратимой легочной гипертензией)
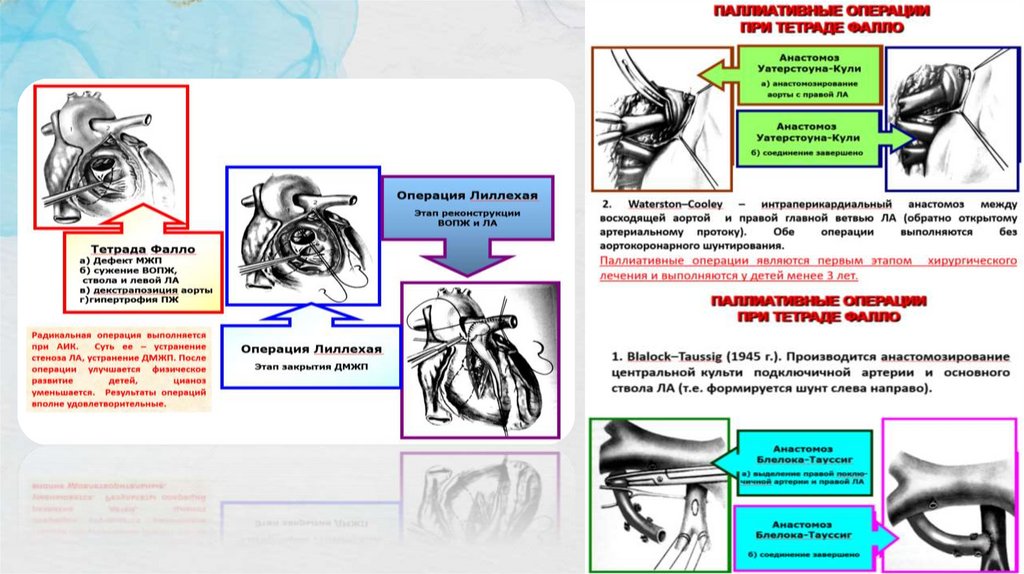
Тетрада и пентада Фалло: Медикаментозная терапия показана при развитии одышечно-цианотических
приступов: ингаляции увлажненного кислорода, внутривенное введение реополиглюкина, натрия
гидрокарбоната, глюкозы, эуфиллина. В случае неэффективности лекарственной терапии необходимо
незамедлительное наложение аортолегочного анастомоза. Паллиативные операции – цель: дать
возможность ребенку пережить опасный для ребенка интервал времени. Суть их в создании
межартериальных анастомозов. Направлены они на увеличение легочного кровотока и снижение
артериальной гипоксемии. К ним относятся: наложение подключично-легочного анастомоза БлелокаТауссиг, внутриперикардиальное анастомозирование восходящей аорты и правой легочной артерии,
наложение центрального аорто-легочного анастомоза с помощью синтетического или биологического
протеза, наложение анастомоза между нисходящей аортой и левой легочной артерией и др. Для
уменьшения гипоксемии применяются операции открытой инфундибулопластики и баллонной
вальвулопластики.
Радикальная коррекция тетрады Фалло предусматривает проведение пластики ДМЖП и устранения
обструкции выходного отдела правого желудочка. Обычно она проводится в возрасте от полугода до 3-х лет.
54.
55.
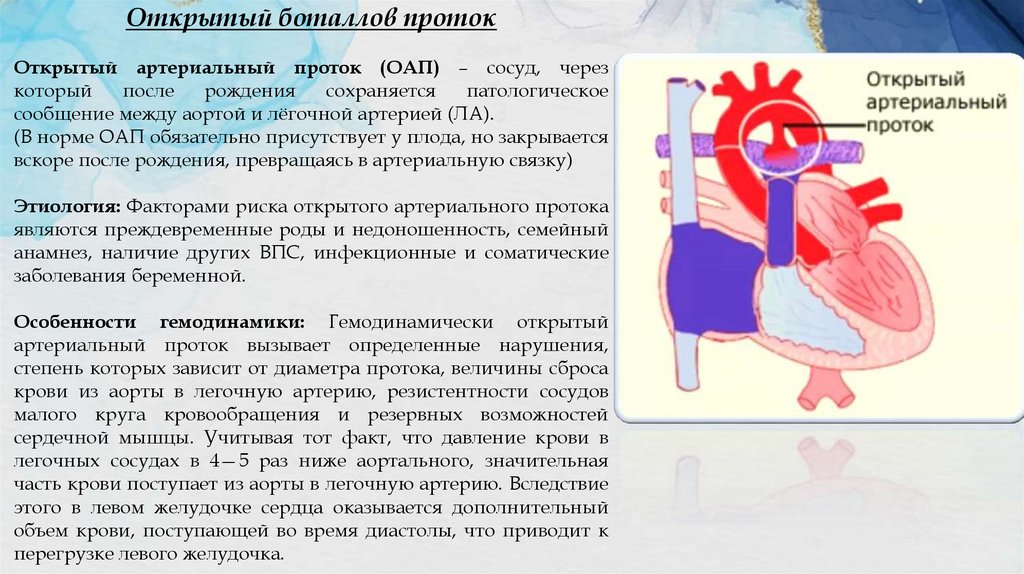
Открытый боталлов протокОткрытый артериальный проток (ОАП) – сосуд, через
который
после
рождения
сохраняется
патологическое
сообщение между аортой и лёгочной артерией (ЛА).
(В норме ОАП обязательно присутствует у плода, но закрывается
вскоре после рождения, превращаясь в артериальную связку)
Этиология: Факторами риска открытого артериального протока
являются преждевременные роды и недоношенность, семейный
анамнез, наличие других ВПС, инфекционные и соматические
заболевания беременной.
Особенности гемодинамики: Гемодинамически открытый
артериальный проток вызывает определенные нарушения,
степень которых зависит от диаметра протока, величины сброса
крови из аорты в легочную артерию, резистентности сосудов
малого круга кровообращения и резервных возможностей
сердечной мышцы. Учитывая тот факт, что давление крови в
легочных сосудах в 4—5 раз ниже аортального, значительная
часть крови поступает из аорты в легочную артерию. Вследствие
этого в левом желудочке сердца оказывается дополнительный
объем крови, поступающей во время диастолы, что приводит к
перегрузке левого желудочка.
56.
Классификация:В естественном течении открытого артериального протока
прослеживаются 3 стадии:
I - стадия первичной адаптации (первые 2-3 года жизни
ребенка). Характеризуется клинической манифестацией
открытого
артериального
протока;
нередко
сопровождается
развитием
критических
состояний,
которые в 20% случаев заканчиваются летальным исходом
без своевременной кардиохирургической помощи.
II - стадия относительной компенсации (от 2-3 лет до 20
лет).
Характеризуется
развитием
и
длительным
существованием
гиперволемии
малого
круга,
относительного стеноза левого атрио-вентрикулярного
отверстия, систолической перегрузки правого желудочка.
III - стадия склеротических изменений легочных
сосудов. Дальнейшее естественное течение открытого
артериального протока сопровождается перестройкой
легочных капилляров и артериол с развитием в них
необратимых склеротических изменений. На этой стадии
клинические
проявления
открытого
артериального
протока постепенно вытесняются симптомами легочной
гипертензии.
57.
Клиническая картина: типичная и атипичная• В случаях с типичным пороком новорожденные бледные, отстают в весе и росте. При обследовании
определяются систолическое дрожание при пальпации передней грудной стенки слева от грудины,
небольшое расширение границ сердца, а также притупление перкуторного звука во втором
межреберье слева спереди — так называемая зона Гергардта. При аускультации во втором межреберье
слева от грудины выслушивается грубый жужжащий, «машинообразный» шум, захватывающий обе
фазы сердечных сокращений. Такой шум не выслушивается, если разница давления крови в аорте и
легочной артерии несущественна.
• При атипичном течении порока у новорожденного также определяются снижение массы тела,
бледность кожных покровов, слабость, резкое увеличение границ сердца, которые появляются очень
рано и быстро ведут к ухудшению общего состояния больных. Над сердцем выслушивается
систолический шум, который объясняется уравниванием давления крови в аорте и легочной артерии
во время диастолы. Иногда шум может совсем отсутствовать. Наиболее тяжелым проявлением этого
порока является цианоз нижней половины туловища вследствие перемены шунта.
58.
Диагностика:- физикальное обследование: При осмотре пациента с
открытым артериальным протоком нередко выявляется
деформация грудной клетки (сердечный горб),
усиленная пульсация в проекции верхушки сердца.
Основным аускультативным признаком открытого
артериального протока служит грубый систолодиастолический шум с «машинным» компонентом во II
межреберье слева.
- рентген: кардиомегалия за счет увеличения размеров
левого желудочка, выбухание дуги легочной артерии,
усиление легочного рисунка, пульсация корней легких.
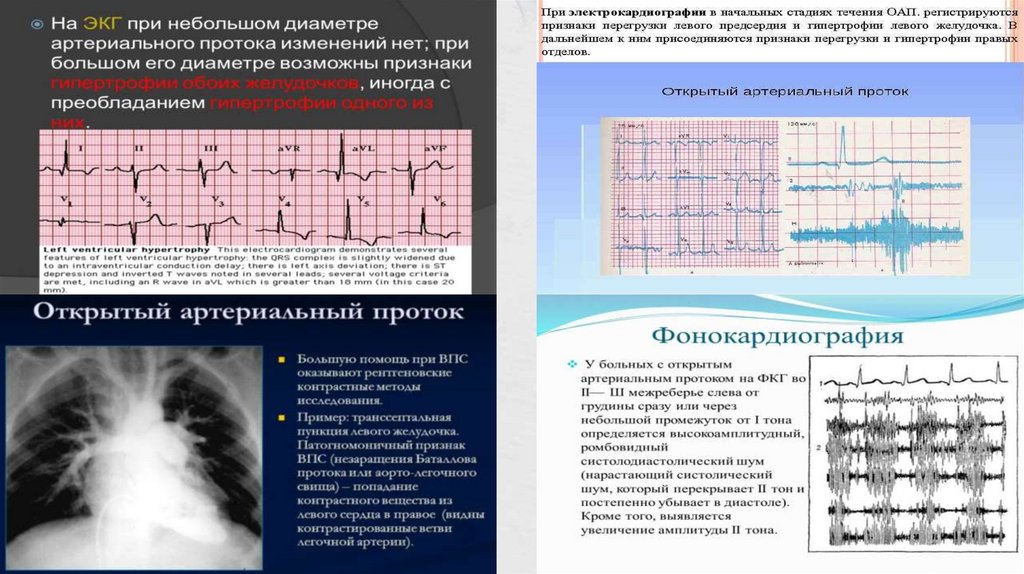
- ЭКГ: гипертрофию и перегрузку левого желудочка;
при легочной гипертензии – на гипертрофию и
перегрузку правого желудочка.
- ЭхоКГ: косвенные признаки порока, производится
непосредственная
визуализация
открытого
артериального протока, измеряются его размеры.
К проведению аортографии, зондирования правых
отделов сердца, МСКТ и МРТ сердца прибегают при
высокой легочной гипертензии и сочетании открытого
артериального порока с другими аномалиями сердца.
59.
60.
Лечение:У недоношенных детей применяется консервативное
ведение открытого артериального протока. Оно
предполагает
введение
ингибиторов
синтеза
простагландина (индометацина) с целью стимуляции
самостоятельной
облитерации
протока.
При
отсутствии эффекта от 3-кратного повторения
медикаментозного курса у детей старше 3-х недель
показано хирургическое закрытие протока.
Оперативное вмешательство:
- перевязка открытого артериального протока в
сочетании с наложением непрерывного шва со
стороны аорты и ЛА.
- Клипирование протока
- Транскатетерная эмболизация
оптимальный возраст для операции 2-5 лет
результаты хирургического лечения открытого
артериального
протока
показывают,
что
своевременная операция позволяет добиться полного
выздоровления
61.
Атрезия трёхстворчатого клапанаАтрезия трехстворчатого клапана (АТК) – врожденный
порок сердца (ВПС), при котором правое предсердие
(ПП) не открывается в желудочек через правый
атриовентрикулярный (АВ) клапан.
Этиология: В этиологии атрезии трехстворчатого
клапана
ведущая
роль
отводится
нарушению
формирования сердца на ранних сроках эмбриогенеза (28 недели). Тератогенными факторами в этот период
гестации могут являться вирусные инфекции (краснуха,
грипп),
хронический
алкоголизм
матери,
производственные
вредности,
прием
некоторых
лекарственных
средств
(сульфаниламидов,
антибиотиков, аспирина и др.).
Причинами, предрасполагающими к формированию
врожденных пороков сердца, служат возраст матери
старше 35 лет, токсикоз I триместра беременности, угроза
прерывания беременности, случаи мертворождения в
анамнезе, эндокринные заболевания (сахарный диабет).
Также следует иметь в виду наследственный фактор:
наличие в семье других детей или родственников с
врожденными пороками развития сердца.
62.
Особенности гемодинамики: Анатомической основой атрезии трехстворчатого клапана являетсяоблитерация правого предсердно-желудочкового отверстия. Вследствие этого неразвитым оказывается
и приточный конус правого желудочка, т. е имеет место гипоплазия правого желудочка →
шунтирование крови из правого предсердия в левое через дефект в межпредсердной перегородке →
через митральный клапан кровь поступает в левый желудочек, откуда может устремляться в двух
направлениях: либо в аорту, либо, через дефект в межжелудочковой перегородке, в нормально
развитый конус правого желудочка и оттуда - в легочную артерию. При отсутствии дефекта в
межжелудочковой перегородке сообщение между большим и малым кругом кровообращения
происходит через открытый артериальный проток или через системные коллатеральные артерии.
Т. о, при атрезии трехстворчатого клапана в левом желудочке происходит смешивание венозной
крови из полых вен и артериальной крови из легочных вен. В большинстве случаев больший объем
крови в дальнейшем попадает в аорту, меньшая часть – в легкие. Недостаточная степень
насыщенности крови кислородом обусловливает развитие цианоза. Ввиду недоразвития правого
желудочка, левый желудочек испытывает повышенную нагрузку, фактически полностью обеспечивая
насосную функцию сердца, что в конечном итоге приводит к развитию сердечной недостаточности.
Классификация:
Выделяют 2 основных клинико-морфологических типа АТК:
• С нормальным отхождением магистральных артерий (конкордантное вентрикулоартериальное
соединение; 60-70% наблюдений), который обычно ассоциирован с обедненным легочным
кровотоком;
• С транспозиционным отхождением магистральных артерий (дискордантное вентрикулоартериальное соединение; 30-40% случаев), при котором чаще имеет место чрезмерный легочный
кровоток.
63.
Клиническа картина: Выраженность клинических проявлений при атрезии трехстворчатого клапанаопределяется размером межпредсердного и межжелудочкового сообщения и величиной легочного
кровотока. Поэтому симптомы атрезии трехстворчатого клапана встречаются у пациентов в различной
степени и сочетаниях. Дети с атрезией трехстворчатого клапана отстают в физическом развитии от своих
здоровых сверстников. Типичны одышка в покое и ее увеличение при незначительной нагрузке
(активности, сосании, плаче и т. д.), симптом «барабанных палочек» и «часовых стекол», общий цианоз.
Нередко возникают гипоксемичесике кризы – приступы пароксизмальной одышки с выраженным
цианозом, обусловленные внезапным уменьшением легочного кровотока, увеличением сброса
неоксигенированной крови в левые отделы сердца и гипоксемией в большом круге кровообращения.
Одышечно-цианотические приступы при атрезии трехстворчатого клапана могут провоцироваться
психоэмоциональным напряжением, физической активностью, интеркуррентными заболеваниями,
протекающими с лихорадкой, диареей и др. факторами. Гипоксемический криз развивается внезапно,
ребенок при этом становится беспокойным, усиливаются одышка и цианоз, возникает тахикардия. В
тяжелых случаях такие приступы могут привести к судорогам, потере сознания, коме и летальному
исходу.
При атрезии трехстворчатого клапана быстро развивается недостаточность кровообращения по
большому кругу с характерными отеками, гепатомегалией, гидротораксом, асцитом. При отсутствии
хирургической коррекции порока большинство детей с атрезией трехстворчатого клапана погибает в
течение первого года жизни. При достаточно больших размерах шунта и нормальном легочном
кровотоке пациенты с некорригированной атрезией трехстворчатого клапана могут дожить до 15-30 и
даже более лет.
64.
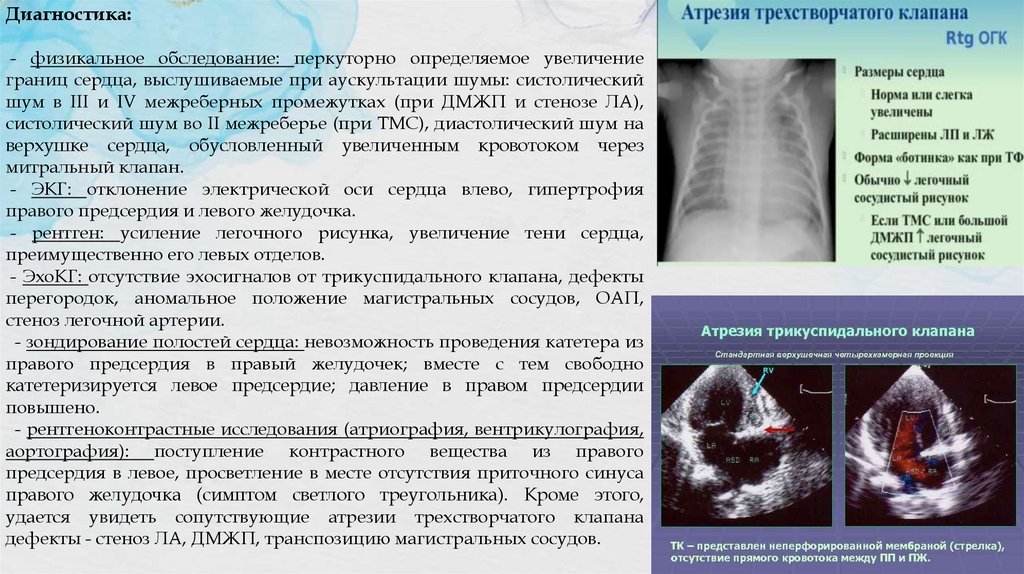
Диагностика:- физикальное обследование: перкуторно определяемое увеличение
границ сердца, выслушиваемые при аускультации шумы: систолический
шум в III и IV межреберных промежутках (при ДМЖП и стенозе ЛА),
систолический шум во II межреберье (при ТМС), диастолический шум на
верхушке сердца, обусловленный увеличенным кровотоком через
митральный клапан.
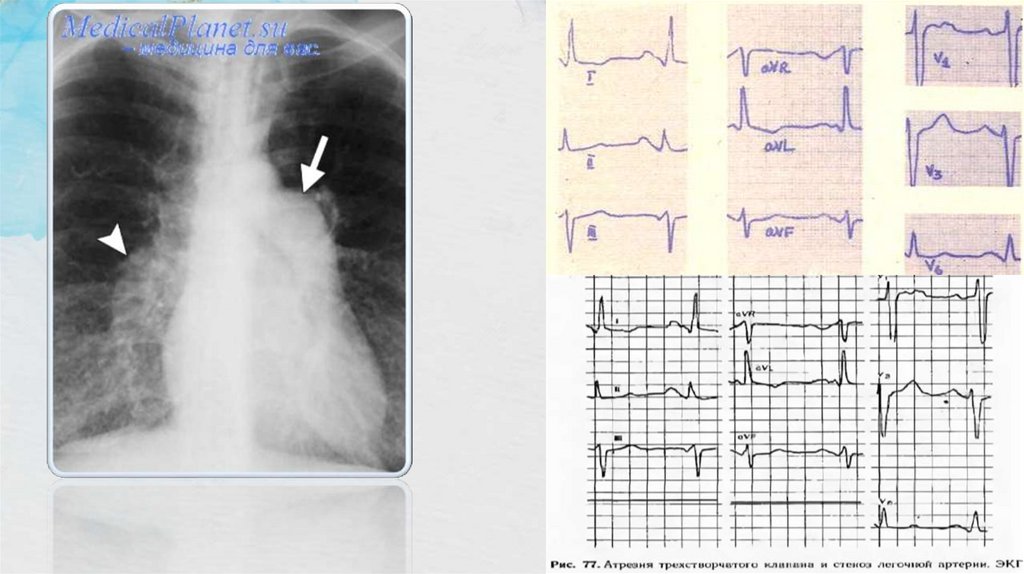
- ЭКГ: отклонение электрической оси сердца влево, гипертрофия
правого предсердия и левого желудочка.
- рентген: усиление легочного рисунка, увеличение тени сердца,
преимущественно его левых отделов.
- ЭхоКГ: отсутствие эхосигналов от трикуспидального клапана, дефекты
перегородок, аномальное положение магистральных сосудов, ОАП,
стеноз легочной артерии.
- зондирование полостей сердца: невозможность проведения катетера из
правого предсердия в правый желудочек; вместе с тем свободно
катетеризируется левое предсердие; давление в правом предсердии
повышено.
- рентгеноконтрастные исследования (атриография, вентрикулография,
аортография): поступление контрастного вещества из правого
предсердия в левое, просветление в месте отсутствия приточного синуса
правого желудочка (симптом светлого треугольника). Кроме этого,
удается увидеть сопутствующие атрезии трехстворчатого клапана
дефекты - стеноз ЛА, ДМЖП, транспозицию магистральных сосудов.
65.
66.
Лечение: Медикаментозная терапияпри атрезии трехстворчатого клапана
показана для купирования одышечноцианотических приступов и коррекции
недостаточности кровообращения.
Операции:
- выполняют атриосептостомию или
эндоваскулярную
баллонную
атриосептостомию,
позволяющую
расширить дефект межпредсердной
перегородки и снизить градиент
давления между предсердиями.
наложение
двухстороннего
двунаправленного
кавапульмонального
анастомоза
или
операция
Гленна-Фонтена,
предполагающие различные варианты
анастомозирования ВПВ и легочной
артерии.
- проведение операции Фонтена,
благодаря
которой
достигается
разобщение малого и большого круга
кровообращения и ликвидируются
нарушения гемодинамики.
67.
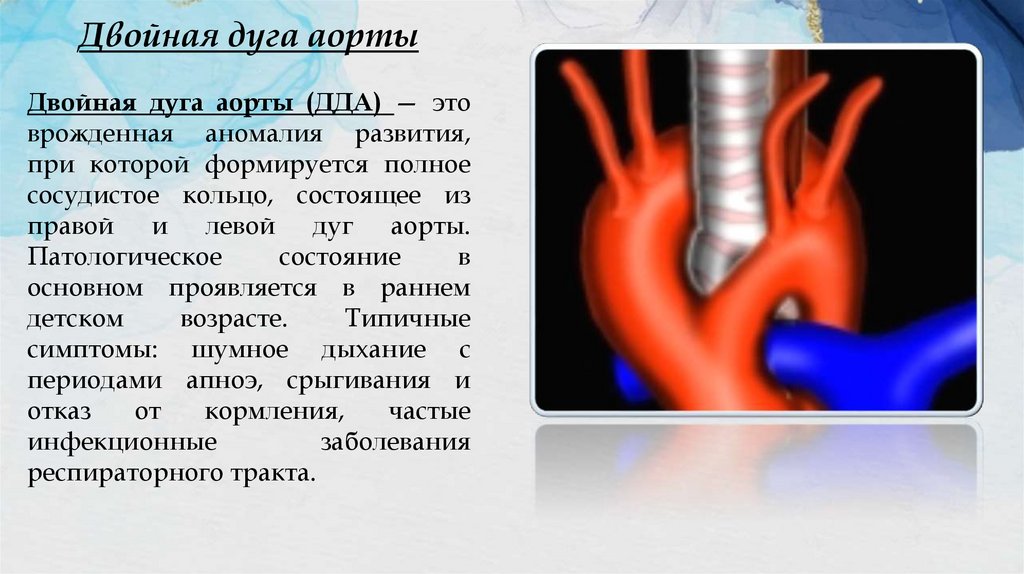
Двойная дуга аортыДвойная дуга аорты (ДДА) — это
врожденная аномалия развития,
при которой формируется полное
сосудистое кольцо, состоящее из
правой и левой дуг аорты.
Патологическое
состояние
в
основном проявляется в раннем
детском
возрасте.
Типичные
симптомы: шумное дыхание с
периодами апноэ, срыгивания и
отказ
от
кормления,
частые
инфекционные
заболевания
респираторного тракта.
68.
Клинические проявления двойной дуги обусловлены нарушениемвентиляции воздуха через трахею и нарушением прохождения пищи
по пищеводу. В большинстве случает первые симптомы аномалии
проявляются сразу после рождения ребенка либо в раннем детстве.
Начальные признаки наличия двойной дуги аорты — шумное
учащенное дыхание, эпизоды рефлекторного апноэ. Патологическое
сосудистое кольцо нарушает гемодинамику в крупных артериях и венах.
Происходит утолщение аортальной стенки, повышается ее
ригидность, что создает благоприятные условия для раннего начала
артериальной гипертензии. В области незрелых стенок двойной
сосудистой дуги зачастую формируются аневризмы, которые могут
спонтанно разрываться. Иногда наступает внезапная смерть от
острых кардиологических или пульмональных осложнений.
69.
Диагностика и лечение двойной дуги аортыДля ДДА характерно сходство клинических симптомов с бронхопульмональными и
эзофагеальными заболеваниями, что требует от врача проведения дифференциальной
диагностики. При физикальном исследовании выслушивается жесткое дыхание, хрипы в
легких, патологические сердечные шумы.
Для постановки диагноза проводятся инструментальные диагностические методы:
- МСКТ-ангиография,
- ЭХО-кардиография, - Бронхоскопия, ЭКГ (редко, по показаниям)
Медикаментозное лечение ДДА показано для коррекции витальных функций на этапе
предоперационной подготовки. Оно может включать антибиотики, глюкокортикоиды,
бронходилататоры при осложненном течении болезни.
Оперативное вмешательство — единственный способ радикального лечения двойной дуги
аорты. Операцию планируют в максимально ранние сроки после выявления ДДА, пока не
наступили необратимые изменения в трахее или пищеводе. Кардиохирургическая тактика
предполагает резекцию одной дуги аорты (чаще левой) с последующей пластикой ее стенки.
70.
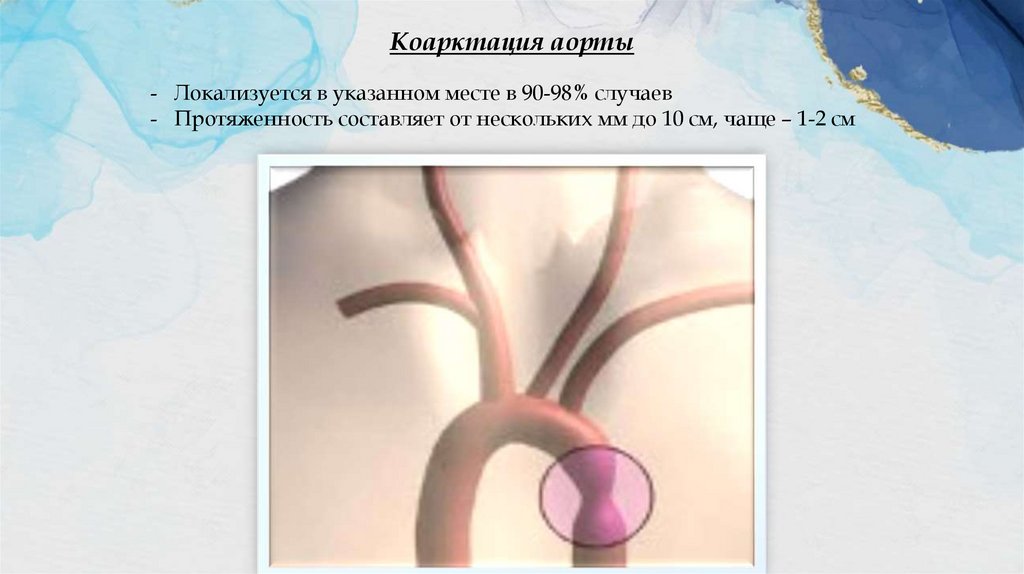
Коарктация аорты- Локализуется в указанном месте в 90-98% случаев
- Протяженность составляет от нескольких мм до 10 см, чаще – 1-2 см
71.
Симптомы при КА и их причины:• !!! Стенотическое изменение аорты в месте перехода ее дуги в нисходящую часть обусловливает
развитие двух режимов кровообращения в большом круге: проксимальнее места препятствия
кровотоку имеется артериальная гипертензия, дистальнее – гипотензия. В связи с этим
наблюдается наличие атлетического типа телосложения (преимущественное развитие плечевого
пояса при худых нижних конечностях); усиление пульсации сонных и межреберных артерий,
ослабление или отсутствие пульсации на бедренных артериях.
• У детей раннего возраста с коарктацией аорты могут отмечаться задержка роста и увеличения
массы тела. Преобладают симптомы левожелудочковой недостаточности: ортопноэ, одышка,
сердечная астма, отек легких.
• В более старшем возрасте, в связи с развитием легочной гипертензии, характерны жалобы на
головокружение, головную боль, сердцебиение, шум в ушах, снижение остроты зрения. При
коарктации аорты нередки носовые кровотечения, обмороки, кровохарканье, чувство онемения и
зябкости, перемежающаяся хромота, судороги в нижних конечностях, абдоминальные боли,
обусловленные ишемией кишечника.
72.
Диагностика:- ЭКГ: перегрузку и гипертрофию левых и/или
правых отделов сердца, ишемические изменения
миокарда.
ЭхоКГ:
позволяет
непосредственно
визуализировать
коарктацию
аорты
и
определить степень стеноза.
- рентген: кардиомегалия, выбухание дуги
легочной артерии, изменение конфигурации
тени дуги аорты, узурация ребер.
- аортография
- левая вентрикулография
Лечение:
медикаментозная
профилактика
инфекционного
эндокардита,
коррекция
артериальной
гипертензии
и
сердечной
недостаточности.
Операции:
- транслюминальная баллонная дилатация
- истмопластика
- резекция коарктации аорты
- шунтирование






















































 medicine
medicine








