Similar presentations:
Взаимодействие с водой
1.
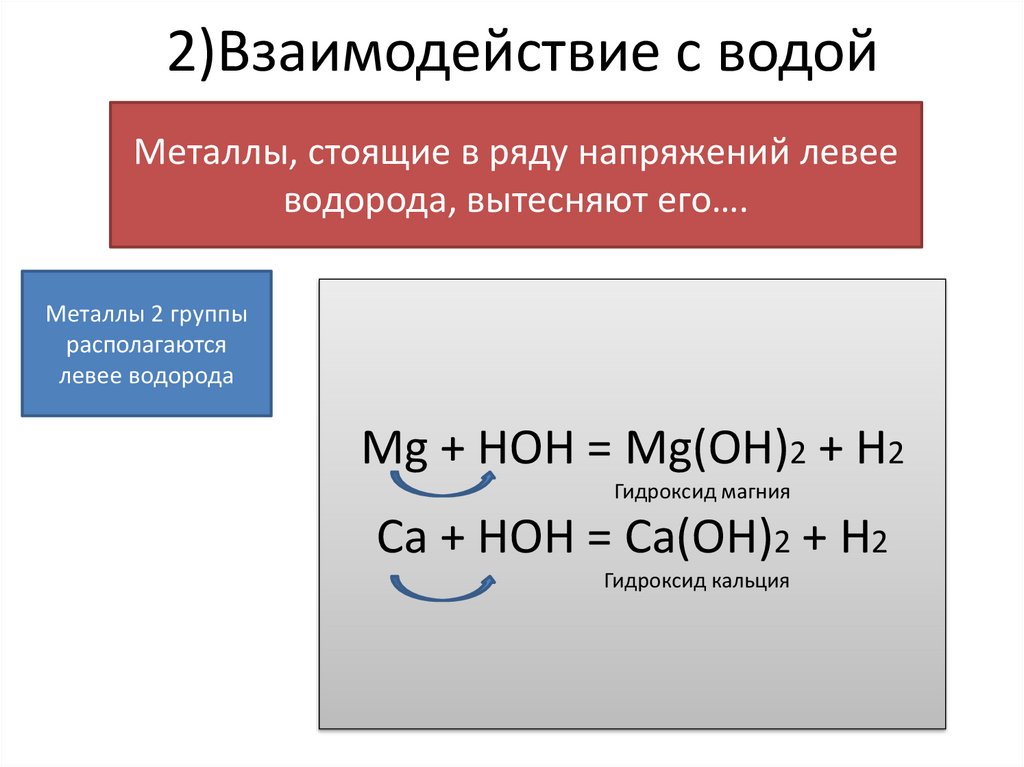
2)Взаимодействие с водойМеталлы, стоящие в ряду напряжений левее
водорода, вытесняют его….
Металлы 2 группы
располагаются
левее водорода
Mg + HOH = Mg(OH)2 + H2
Гидроксид магния
Ca + HOH = Ca(OH)2 + H2
Гидроксид кальция
2.
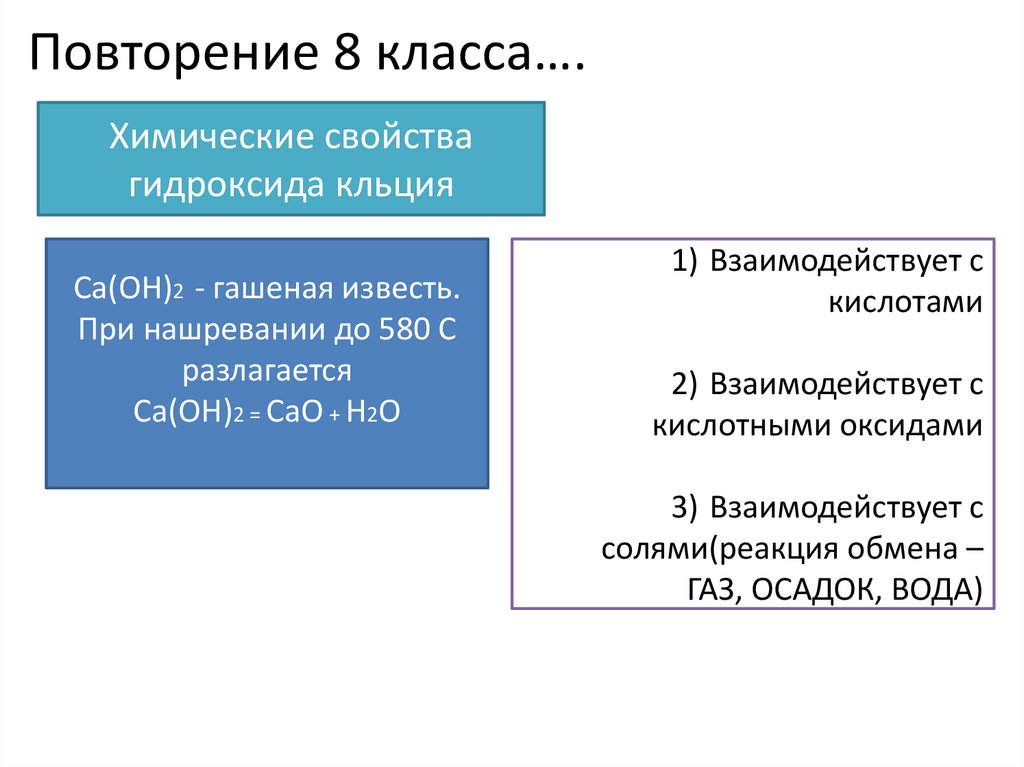
Повторение 8 класса….Химические свойства
гидроксида кльция
Ca(OH)2 - гашеная известь.
При нашревании до 580 С
разлагается
Ca(OH)2 = CaO + H2O
1) Взаимодействует с
кислотами
2) Взаимодействует с
кислотными оксидами
3) Взаимодействует с
солями(реакция обмена –
ГАЗ, ОСАДОК, ВОДА)
3.
Взаимодействует с кислотамиCa(OH)2 + HCl = CaCl2 + H2O
2+
+
- 2+
Ca + 2OH + H + Cl= Ca + 2 Cl + H2O
+
2OH + H = H2O
Ba(OH)2 + HNO3 =
(ДОПИСАТЬ РЕАКЦИЮ И СДЕЛАТЬ ПОЛНОЕ И СОКРАЩЕННОЕ ИОННОЕ УРАВНЕНИЕ)
НЕ ЗАБЫВАЕМ ЗАРЯДЫ!!!!
4.
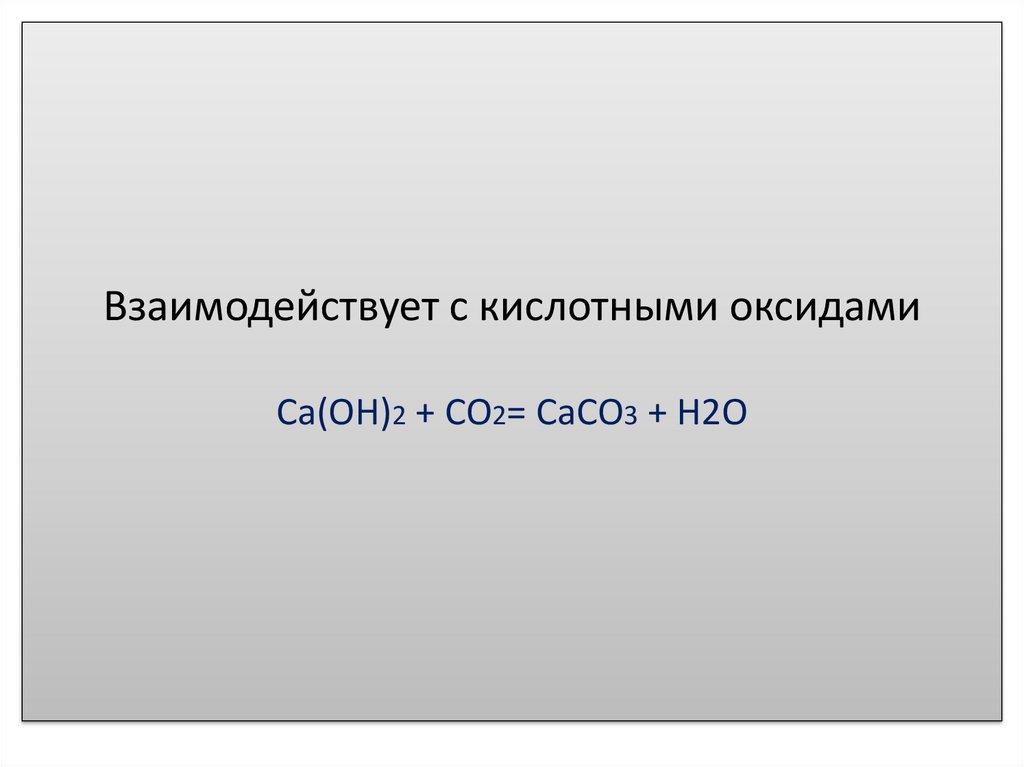
Взаимодействует с кислотными оксидамиCa(OH)2 + СО2= СаСО3 + Н2О
5.
Взаимодействует с солями(реакция обмена – ГАЗ, ОСАДОК, ВОДА)Ca(OH)2 + NH4Cl = CaCl2 + NH4OH ( NH3 ГАЗ H2O)
гидроксид аммония
2+
+ - 2+ Ca + 2OH + NH4 + Cl = Ca + 2Cl + NH3 + H2O
+
2OH + NH4 = NH3 + H2O
Ca(OH)2 + FeCl3=
(ДОПИСАТЬ РЕАКЦИЮ И СДЕЛАТЬ ПОЛНОЕ И
СОКРАЩЕННОЕ ИОННОЕ УРАВНЕНИЕ)
НЕ ЗАБЫВАЕМ ЗАРЯДЫ!!!!
6.
3)Взаимодействие с неметалламиОВР
0 0 +2 Ca + Cl2 = CaCl2
хлорид кальция
Для всех
0 0 +2 -2
Ca + S = CaS
сульфид кальция
0 0 +2 -3
Ca +N2 = Ca3N2
нитрид кальция
7.
4) Способны восстанавливатьредкие металлы – ниобий, тантал,
молибден, титан и др.
ОВР
Для всех
0 +4-2 +2-2 0
Mg + TiO2 = MgO + Ti
0
+5 -2 +2-2 0
Ca + V2O5 = CaO + V
8.
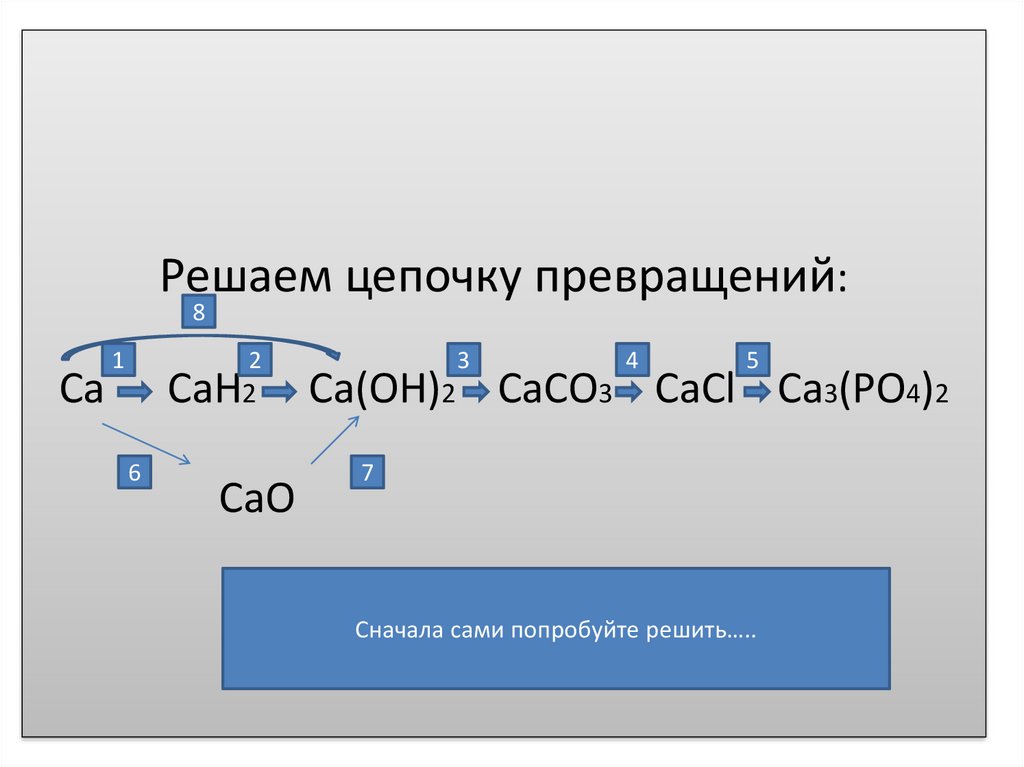
Решаем цепочку превращений:8
Са
1
2
СаН2
6
CaO
3
4
5
Са(ОН)2 СаСО3 СаСl Са3(PO4)2
7
Сначала сами попробуйте решить…..
9.
ОВР1) Ca + H2 = CaH2
2) CaH2 + H2O= Ca(OH)2
3) Ca(OH)2 + HCl = CaCO3 + H2O Ионное
4) CaCO3 + HCl = CaCl2 + CO2 + H2O Ионное
5) CaCl2 + H3PO4 = Ca3(PO4)2 + HCl Ионное
ОВР
6) Ca + O2 = CaO
7) CaO + H2O = Ca(OH)2
8) Ca + H2O = Ca(OH)2
Подписываем название реакции и название
вещества.
10.
Д/ЗMg
MgO
Mg(OH)2
MgCl2






 chemistry
chemistry








