Similar presentations:
Иммунная система органов дыхания. Иммунологические аспекты заболеваний сердца
1. Иммунная система органов дыхания. Иммунологические аспекты заболеваний сердца
Лекциядоц. Кордон Т.И.
2.
Органы дыхания находятся внепосредственном тесном контакте
с огромным количеством антигенов,
поэтому обладают иммунной
системой слизистых оболочек
(ИССО) и бронхо-ассоциированной
лимфоидной тканью (БАЛТ)
3.
Главная роль принадлежит факторамместного иммунитета - клеткам лимфоидного
ряда, макрофагам, нейтрофилам,
эозинофилам, тучным клеткам, и др.,
находящихся на слизистых оболочках.
Слизистые оболочки действуют как единая
система - по ней распространяются
активированные в одном ее участке
лимфоциты, имеющие функциональную
связь с системным иммунитетом.
4.
В иммунной системе слизистых оболочеквыделяют два участка:
- индуктивный (лимфоидная ткань) - в нем
протекают процессы иммунологического
распознавания, презентации антигена и
формируется популяция
антигенспецифических лимфоидных клеток.
- эффекторный (непосредственно слизистая
оболочка). В нем накапливаются Т-лимфоциты,
обеспечивающие клеточно-опосредованные
формы защиты слизистых оболочек.
5.
Дыхательный тракт (как ипищеварительный) является
входными воротами для огромного
потока антигенов, поэтому
содержит огромное количество
лимфатических фолликулов и их
скоплений, которые составляют
лимфоидную ткань,
ассоциированную со слизистыми
оболочками.
6. Лимфоидные элементы дыхательного тракта
миндалины – небные,глоточные,
лимфатическое
глоточное кольцо.
специализированные
2 — небная миндалина;
эпителиальные
М3 — глоточная
миндалина;
клетки, которые
5 — лимфатические
адсорбируют антиген и
фолликулы,
рассеянные в слизистой
представляют
оболочке задней стенки
глотки.
лимфоцитам.
7. Защиту органов дыхания обеспечивают:
слой эпителиальных клеток (постоянновозобновляется и покрыт слизью)
макрофаги, гранулоциты, дендритные
клетки и другие клетки, участвующие в
развитии воспаления
иммуноглобулины (в секрете носа
содержатся Ig всех классов
сапрофитные микробы, блокируя
рецепторы эпителия (20% случаев стрептококки группы А)
8. Механизмы защиты:
Антигены поступают через крипты эпителиялимфоидной ткани миндалин активируют
М-клетки презентуют его лимфоцитам.
В презентации антигена участвуют
дендритные клетки. До встречи с антигеном
они находятся в незрелом состоянии.
Захватывая и перерабатывая антиген,
клетки созревают и мигрируют в
лимфатические узлы и селезенку, где
выполняют АП-функцию.
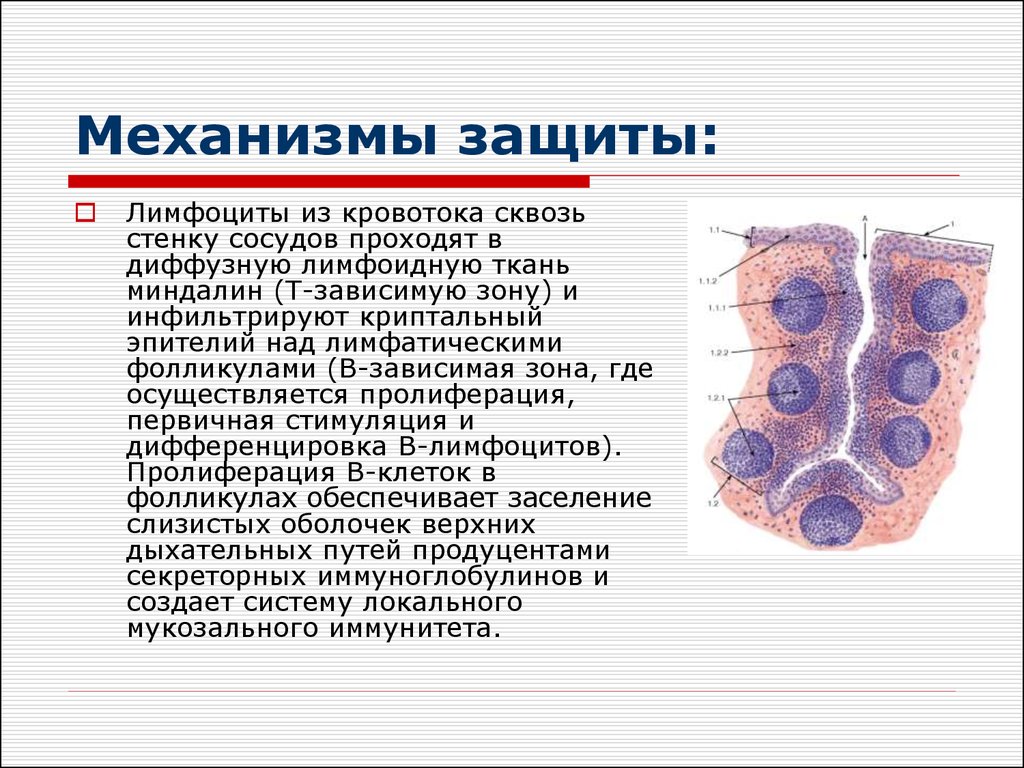
9. Механизмы защиты:
Лимфоциты из кровотока сквозьстенку сосудов проходят в
диффузную лимфоидную ткань
миндалин (Т-зависимую зону) и
инфильтрируют криптальный
эпителий над лимфатическими
фолликулами (В-зависимая зона, где
осуществляется пролиферация,
первичная стимуляция и
дифференцировка В-лимфоцитов).
Пролиферация В-клеток в
фолликулах обеспечивает заселение
слизистых оболочек верхних
дыхательных путей продуцентами
секреторных иммуноглобулинов и
создает систему локального
мукозального иммунитета.
10. Функции миндалин
защитная (синтез Ig основныхклассов и разрушение патогенных
микроорганизмов,
активированными лимфоцитами)
информационная (антигенная
стимуляция из полости глотки)
поддержание состава микрофлоры
верхних дыхательных путей
11.
В лимфоидных структурах верхних отделовреспираторного тракта образуются защитные
IgE (от паразитарных и инфекционных
возбудителей), но стимулирующие
слизеобразование и бронхоспазм.
IgЕ-продуцирующие плазматические клетки
локализуются в слизистой оболочке
дыхательных путей, поэтому синтез IgE
происходит в тканях, контактирующих с
внешней средой.
12. Заболевания органов дыхания имеют различную этиологию, и характеризуются острым или хроническим течением
--
Причины их развития:
инфекции бактериальной и вирусной природы (бронхит,
пневмония, плеврит, туберкулез, как осложнения длительно
прогрессирующего заболевания – дыхательная
недостаточность)
аллергические реакции (обструктивный бронхит, бронхиальная
астма)
особенности условий труда (вдыхание угольной пыли – антракоз,
пыли некоторых металлов – металлокониозы, силикоз кремний)
перерождение тканей (фиброз, склероз тканей, малигнизация)
анатомические нарушения нормального строения (врожденные
или приобретенные - расширения и деформация бронхов,
расширение альвеол)
переохлаждение, переутомление, стрессы, лекарственные
препараты и другие факторы.
13. При хронических неспецифических заболеваниях легких (ХНЗЛ) отмечают нарушения иммунного статуса с характерными признаками аутоиммунного
процесса.Традиционное лечение
(антибиотики, сульфаниламидные,
их комбинации с антигистаминными
препаратами, кортикостероиды)
иммунологическая недостаточность
аутоинфекция
вялотекущий
процесс в легких
новые
антибактериальные препараты
подавление иммунной
реактивности.
14.
У больных с хроническими заболеваниями легкихчасто наблюдается выраженное расстройство
местного иммунитета, характер которого зависит от
вида заболевания.
При БА существенно увеличивается IgE в слизи из
носа и бронхов по сравнению с их содержанием в
крови, уровень секреторного IgА – снижается.
У больных с ХБ, вызванного пиогенными
бактериями, - увеличено количество нейтрофилов
в бронхоальвеолярном секрете,но бактерицидные
функции этих клеток существенно снижены, а
также снижено количество лимфоцитов.
15. При пневмониях:
в остром периоде заболевания отмечается- угнетение РБТЛ периферической крови на ФГА;
- снижение общего количества лимфоцитов, Тхелперной и Т-супрессорной популяций
- содержание В-лимфоцитов меняется
разнонаправлено.
- концентрация иммуноглобулинов зависит от типа
заболевания, его стадии, тяжести течения и
возраста больного.
- подавление или стимуляция факторов
неспецифической антиинфекционной
резистентности - лизоцим, белки системы
комплемента, фагоцитарная активность
нейтрофилов.
16. При бронхите
снижается ответ лимфоцитов на ФГА вРБТЛ
снижается количество общих
лимфоцитов, Т-супрессоров, NK—клеток
количество В-лимфоцитов и отдельных
классов иммуноглобулинов может как
снижаться, так и повышаться
увеличивается содержание ЦИК
снижается уровень ИЛ-1 и ИЛ-2.
17. При бронхиальной астме
иммунные нарушения гетерогенные, зависят отмеханизмов развития (атопический, инфекционноаллергический).
всегда снижается количество Т-лимфоцитов
соответственно тяжести патологического процесса
снижается количество и функциональная
активность Т-супрессорных клеток.
Динамика содержания В-лимфоцитов и IgG и IgA
вариабельна, уровень IgE и ЦИК однозначно
повышен,
В связи с угнетением супрессорного звена
создаются условия для формирования
аутоиммунных реакций.
18. Иммунные реакции при туберкулезе
У большинства впервые инфицированныхпациентов период ранней туберкулезной инфекции
не сопровождается клиническими проявлениями
туберкулеза, а ограничивается иммунной
перестройкой организма.
Заражение человека туберкулезом происходит в
большинстве случаев (в 90–95%) через
дыхательные пути (аэрогенный путь), реже – через
желудочно-кишечный тракт (алиментарный путь),
очень редко через поврежденную кожу и слизистые
оболочки (контактный путь), возможно и
внутриутробное заражение плода у больной
туберкулезом матери.
19. Первичное инфицирование МБТ
МБТ, проникшие в ДП вместе с мокротой, слизью, могутвыводиться из бронхов, что препятствует их контакту с
альвеолярными макрофагами.
При первичном инфицировании полимофноядерные лейкоциты
пытаются поглотить и разрушить МБТ. Однако имеет место
незаврешенный фагоцитоз (бактерицидный потенциал
недостаточный). После начинается взаимодействие МБТ с
макрофагами. Лизосомальные ферменты не всегда могут
расщеплять и разрушать поглощенные МБТ. Переваривающая
активность макрофагов зависит от состояния макроорганизма,
возраста, пола, наследственности и от вирулентности
микобактерий.
Дисфункции лизосом связанны с повреждающим воздействием
на лизосомальные мембраны сульфатидов и корд-фактора МБТ
(макрофаг - резервуар МБТ). Исход первичного инфицирования
зависит от способности организма активировать макрофаги и
создавать условия для завершенного фагоцитоза.
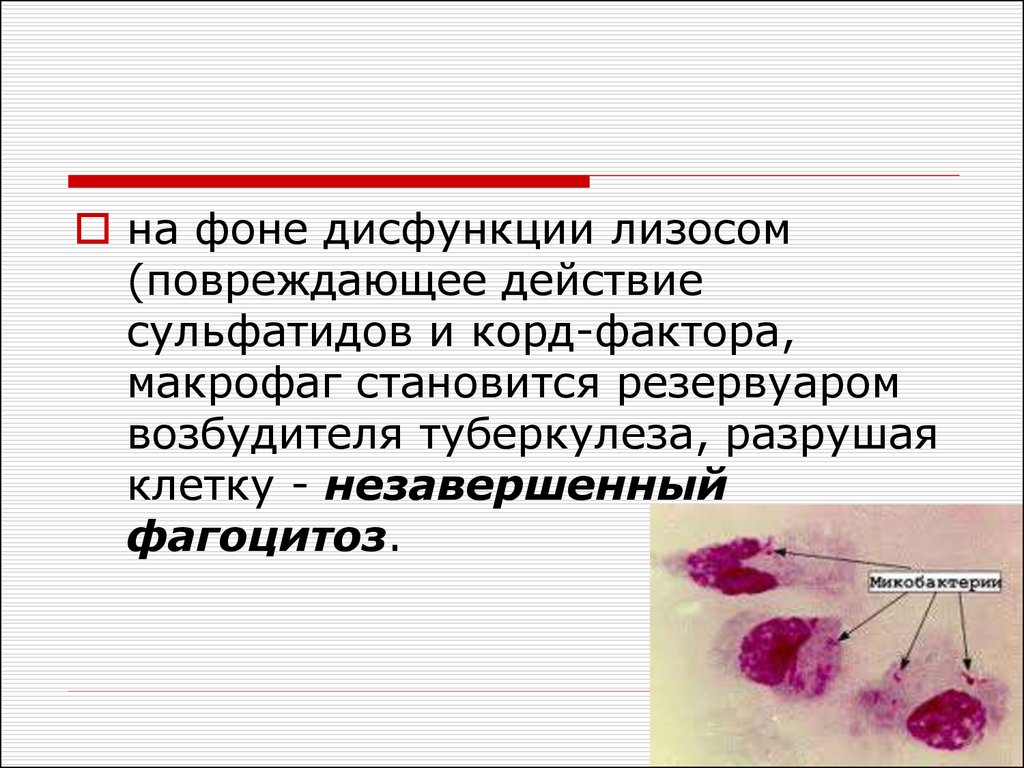
20.
на фоне дисфункции лизосом(повреждающее действие
сульфатидов и корд-фактора,
макрофаг становится резервуаром
возбудителя туберкулеза, разрушая
клетку - незавершенный
фагоцитоз.
21.
Ведущая роль в резистентности организма ктуберкулезу принадлежит вторичному клеточному
иммунитету (АПК и Т-лимфоциты).
Макрофаги экспрессируют на своей поверхности
антигены МБТ и выделяют медиаторы (ИЛ-1),
активирующие Т-лимфоциты. Т-лимфоциты
выделяют (ИЛ-2) - активируют миграцию и
ферментативную активность макрофагов в
отношении МБТ
Выделяемые макрофагами медиаторы активируют и
В-лимфоциты, но их эффективность
иммуноглобулинов незначительна.
22.
При повышении ферментативной активностимакрофагов выделяются провоспалительные
цитокины, способствующие повышению сосудистой
проницаемости, появлению ГЗТ.
ГЗТ – один из основных феноменов клеточного
противотуберкулезного иммунитета
(положительная кожная туберкулиновая реакция –
реакция Манту).
Реакции ГЗТ выявляются через 2–3 нед. после
инфицирования или вакцинации, а достаточно
выраженный иммунитет формируется через 8 нед.
23.
Развитие ГЗТ обеспечивают часть Ткиллеров совместно с макрофагами. КГЗТ относят все реакции взаимодействия
клеток с антигенами микобактерий.
В защите от туберкулеза определенное
значение имеют гуморальные факторы
естественной резистентности
(комплемент, лизоцим, пропердин,
интерферон и др.), особенно у
новорожденных детей, имеющих
физиологическую недостаточность
иммунной системы.
24.
В иммунизированном вакциной БЦЖорганизме макрофаги быстрее
мигрируют к месту внедрения МБТ,
обладают большей
переваривающей способностью, чем
в неиммунизированном.
25.
При интенсивном размножении МБТ увеличивается количествоТ-супрессоров, уменьшается иммунологическая активность Тхелперов, угнетается ГЗТ, что ведет к прогрессированию
туберкулезного процесса, формированию некротических
гранулем.
При небольшом количестве микобактерий после развития ГЗТ
макрофаги под действием медиаторов Т-лимфоцитов мигрируют
в место действия антигена и создают условия для образования
экссудативно-продуктивной гранулемы.
Макрофаги под влиянием фосфатидов и фагоцитированных в
них микобактерий трансформируются в эпителиоидные клетки
и гигантские многоядерные клетки Пирогова-Лангханса,
которые ограничивают очаг воспаления.
Формирование гранулемы следует рассматривать как
иммунологическую реакцию организма на туберкулезную
инфекцию.
26.
Для вторичного туберкулеза характерно наличиеприобретенного при первичном инфицировании
иммунитета. Его выраженность определяет
развитие и течение туберкулеза. Иммунное
состояние организма поддерживает сохраняющаяся
после первичного заражения инфекция, которая в
виде типичных или L-форм находится в очагах,
оставшихся после первичного инфицирования МБТ
или излеченного первичного туберкулеза.
Вторичный туберкулез преимущественно органный,
возникает в результате поступления МБТ из
заживших очагов первичного туберкулеза
(эндогенная реактивация) или повторного
аэрогенного или алиментарного заражения
(экзогенная суперинфекция).
27. Диагностика туберкулеза
Для выявления ГЗТ при туберкулезеприменяют реакции
бласттрансформации лимфоцитов,
торможения миграции лейкоцитов и
др.
В широкой практике для выявления
ГЗТ используют туберкулиновые
пробы.
28.
При острых инфекционных деструкциях легких впериферической крови уменьшается содержание
общих Т-лимфоцитов, Т-хелперов, угнетена их
функциональная активность в РБТЛ, снижено число
нулевых лимфоцитов. В-звено истощено вследствие
длительной полифункциональной активации
вследствие тяжелого воспалительного процесса,
сопровождающего деструкцию легких (увеличение
уровня В-лимфоцитов, дисбаланс продукции
иммуноглобулинов основных классов).
Одновременно возникают аутоиммунные
осложнения, связанные с накоплением ЦИК.
29. У больных с заболеваниями легких отмечается:
выраженный дефицит количества Тклеток, их основных субпопуляций;дисбаланс В-звена иммунитета;
снижение функциональной активности
фагоцитирующих клеток;
возрастание сенсибилизации организма
антигенами легочной ткани и антигенами
причинных возбудителей;
формированием аутоиммунных реакций.
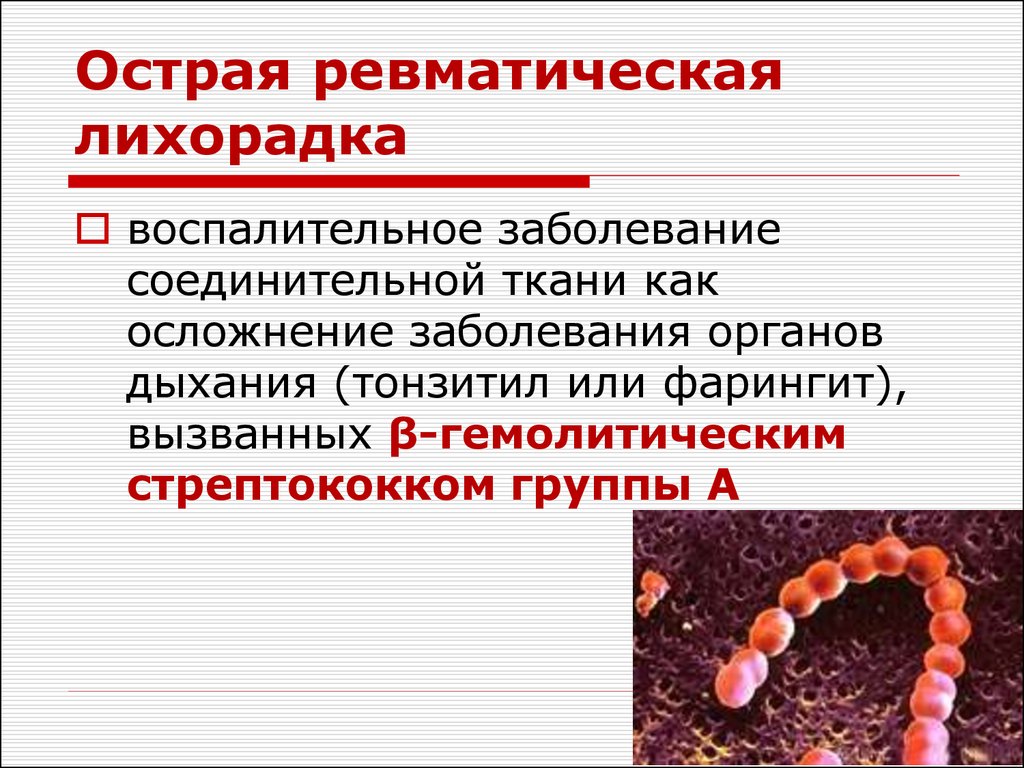
30. Острая ревматическая лихорадка
воспалительное заболеваниесоединительной ткани как
осложнение заболевания органов
дыхания (тонзитил или фарингит),
вызванных β-гемолитическим
стрептококком группы А
31.
Ревматическая болезнь сердца –заболевание, характеризующееся
поражением сердечных клапанов
или порока сердца
(недостаточность и/или стеноз),
сформировавшихся после
перенесенной ОРЛ.
32. Факторы риска ОРЛ:
возраст 7-20 лет;женский пол (женщины болеют в 2,6 раза чаще, чем
мужчины);
наследственность;
недоношенность;
врожденные аномалии соединительной ткани,
несостоятельность коллагеновых волокон;
перенесенная острая стрептококковая инфекция и
частые носоглоточные инфекции;
неблагоприятные условия труда или проживание в
помещении с повышенной влажностью, низкой
температурой воздуха.
33. Существует предрасположенность к ОРЛ
Среди больных ОРЛ чащевстречаются лица с группами крови
А(ІІ), В(ІІІ)
У больных ОРЛ повышена частота
носительства антигенов НLА-А11,
В35, DR5 и DR7
34.
В развитии ревматизма большую рольиграет повышение иммунологической
реактивности. Если в развитии острого
ревматизма главную роль играет
стрептококковая инфекция, то при
хронизации ревматизма главный фактор
–усиление антителообразования
относительно оболочек сердца (миокарда
и эндокарда), что приводит не только к
повреждению сердца, но и является
причиной развития осложнений.
35. Свойства β-гемолитических стрептококков группы А, вызывающие ОРЛ
•тропность к ткани носоглотки;• наличие большой гиалуроновой капсулы;
• способность индуцировать синтез
типоспецифических антител;
• высокая контагиозность;
• наличие крупных молекул М-протеина на
поверхности штаммов;
•наличие в молекулах М-протеина эпитопов,
перекрестно реагирующих с различными тканями
макроорганизма хозяина: миозином, мозгом и др.
36. Патогенез ОРЛ определяется:
иммунным ответом на антигены βгемолитического стрептококка группы А,приводящим к синтезу
противострептококковых антител –
антистрептолизина-О (АСЛ-О),
антистрептогиалуронидазы (АСГ),
антистрептокиназы (АСК),
антидезоксирибонуклеазы В, перекрестно
реагирующих с антигенами поражаемых
тканей человека («феномен молекулярной
мимикрии»).
37. ОРЛ протекает в три этапа:
I – тонзиллит (ангина) или фарингит, симптомыкоторого быстро проходят (обычно в течение
недели);
II – светлый промежуток (мнимое
благополучие), когда продолжаются
аутоиммунные процессы в тканях без внешних
проявлений (2 нед);
III – развитие типичной ревматической атаки
(повышение температуры тела, острое
воспаление мягких тканей суставов, поражение
сердца, серозных оболочек, сосудов, нервной
системы и др.).
38.
При ревматизме расстройства иммуннойсистемы характеризуются уменьшением
количества лейкоцитов, общих
лимфоцитов, Т-хелперов, Т-супрессоров
при одновременном повышении нулевых
клеток, снижением функциональной
активности в реакции РБТЛ на ФГА, но
ответ клеток на стрептококковый антиген
и антиген сердечной мышцы
интенсивный. Содержание В-лимфоцитов
может варьировать.
39.
Снижение супрессорной функции Т-лимфоцитов способствуетусилению аутоантителообразования.
При ревматизме значительно повышаются показатели
гуморального иммунитета на воздействие стрептококков и
их токсинов – повышение титра антистрептолизина-О (АСЛО),
антигиалуронидазы, антистрептокиназы, антител против Мпротеина, А-полисахарида.
Значительную роль играют аутоантитела против антигенов
миокарда.
Возрастание уровня ЦИК коррелирует в увеличением
содержания иммуноглобулинов, титром АСЛО и тяжестью
болезни. Комплексы, содержащие антитела против
стрептолизина-О способны фиксировать комплемент,
одновременно увеличивается выраженность кожный проб на
стрептококковый аллерген.
Таким образом, ревматизм сопровождается вторичным
иммунодефицитом Т-лимфоцитов и их субпопуляций с
развитием аутоиммунных и аллергических реакций.
40. Лечение ревматизма
антибиотики пенициллиновогоряда, макролиды, нестероидные
противовоспалительные средства,
иммуномодуляторы,глюкокортикостероиды,
иммунодепрессанты,
иммунокорректоры, плазмаферез.
41. Миокардиты
могут быть обусловлены различными этиологическимифакторами: бактериальные (дифтерия, менингит),
вирусные инфекции (пневмонии, ОРВИ), применение
лекарственных препаратов, сывороток, холангит, сепсис,
голодание, тепловой удар и т.п.
У больных миокардитом отмечается усиление РБТЛ на
стимуляцию антигеном миокарда, синтез аутоантител
против миокарда, угнетение функциональной активности
Т-лимфоцитов, Т-лимфопения, снижение уровня Тсупрессоров, повышение иммуноглобулинов основных
классов.
Для лечения, кроме специфических
противоинфекционных препаратов, применяют
противовоспалительные, десенсибилизирующие и
антигистаминные препараты.
42. Иммунологические аспекты инфаркта миокарда
Иммунные нарушения с однойстороны играют роль в
возникновении атеросклероза, с
другой – обуславливают
аллергическое аутоиммунное
поражение артерий. Возникновение
зоны инфаркта приводит к
образованию аутоантител и
развитию вторичной патологии.
43. Первичный инфаркт миокарда в острой фазе характеризуется:
снижением количества общих Тлимфоцитов, Т-супрессоров, снижениемфункций Т-лимфоцитов в РБТЛ на
митогены, увеличением В-лимфоцитов.
На 10 сутки болезни отмечается еще
большее снижение Т-лимфоцитов,
особенно Т-хелперов.
Через 3 недели количество клеток
начинает повышаться, как и
концентрация IgM.
44. При повторном инфаркте
характер иммунных нарушенийостается тем же, только
выраженность еще существенно
возрастает – дефицит количества Тлимфоцитов, особенно Тсупрессоров и существенное
увеличение образования
аутоантител против миокарда.
45.
Для лечения ИМ применяютиммунокоррегирующие препараты,
особенно те, которые обладают
способностью стимулировать
нуклеиновый обмен в мышце
сердца.










































 medicine
medicine








