Similar presentations:
Кислоты. Строение, классификации и свойства неорганических кислот
1.
“Ум заключается не тольков знании, но и в умении
прилагать знание на деле”.
(Аристотель).
2.
Вспомни…Какие соединения называют оксидами?
СаО, SО2, ВаО , Nа2О, Сl2О7, Al2O3
Какие соединения относят к основаниям?
КОН, Аl(ОН)3, Ва(ОН)2, Сu(ОН)2
Отчего зависит число гидроксильных
групп в основании?
3.
Работа с карточкамиИз предложенного списка веществ
выпишите оксиды и щёлочи:
CaO, CI2O7, NaOH, HCI, CO2, Cu(OH)2 ,
H2SO4 , LiOH , AL2O3, K2O, N2O5, H2CO3 ,
AI(OH)3 , SO3, Ca(OH)2, КОН
Оксиды:
Щёлочи:
4.
Правильные ответы:Оксиды:
CaO, CI2O7, CO2 , AL2O3, K2O,
N2O5, SO3
Щёлочи:
NaOH, LiOH, КОН
5.
Тема урока:«КИСЛОТЫ»
Цель урока: изучение строения,
классификации и свойств
неорганических кислот
6.
Задачи урока:изучить строение и свойства кислот;
познакомиться с классификацией кислот;
узнать формулы некоторых неорганических кислот;
познакомиться с правилами техники безопасности
при работе с кислотами;
научиться распознавать кислоты среди других
соединений;
научиться определять заряды ионов кислотных
остатков.
7.
Кислоты в природеЛимонная кислота
Аскорбиновая кислота
Муравьиная кислота
8.
Кислоты в жизни человекаВ организме
В кулинарии и продуктах питания
В медицине
В народном хозяйстве
Молочная кислота
образуется в
мышцах при
нагрузке
Соляная кислота в желудке способствует
перевариванию пищи
9.
Кислотные дожди – одна изэкологических проблем
Н2О
Н2SО3 Н2О
Н2О
НNО2
SО2 НNОН
2S
3
NО2
10.
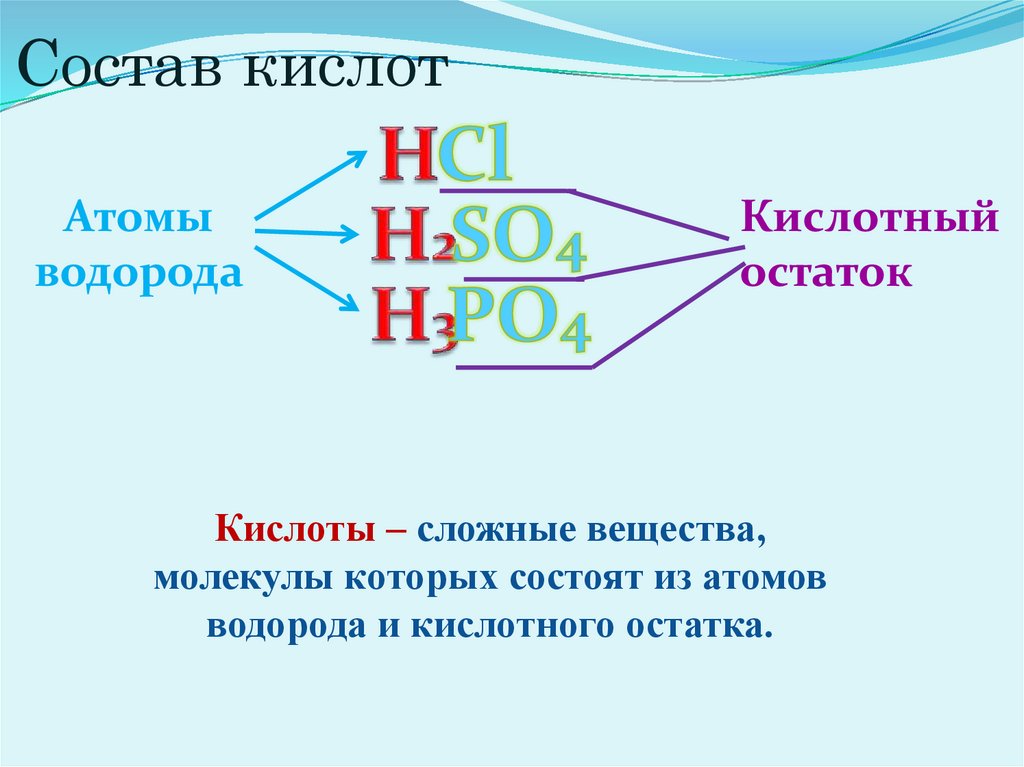
Состав кислотАтомы
водорода
Кислотный
остаток
Кислоты – сложные вещества,
молекулы которых состоят из атомов
водорода и кислотного остатка.
11.
Независимо от вида кислоты,индикаторы изменяют свой цвет
одинаково, а это означает, что
все кислоты обладают сходными
свойствами.
12.
13.
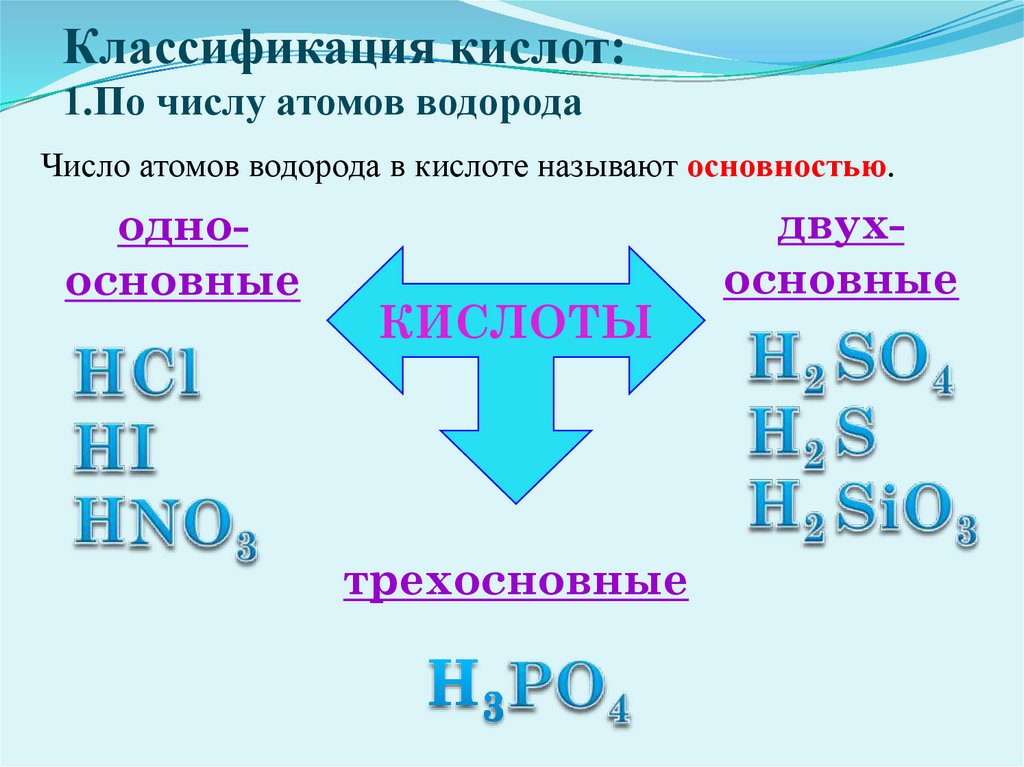
Классификация кислот:1.По числу атомов водорода
Число атомов водорода в кислоте называют основностью.
одноосновные
КИСЛОТЫ
трехосновные
двухосновные
14.
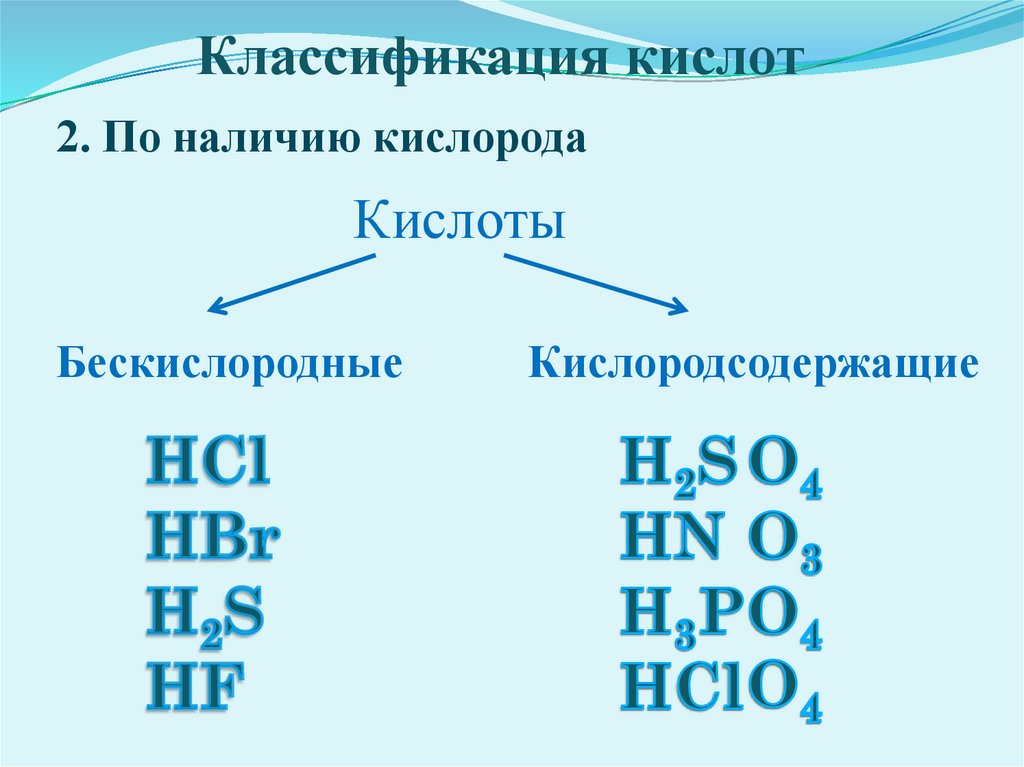
Классификация кислот2. По наличию кислорода
Кислоты
Бескислородные
Кислородсодержащие
15.
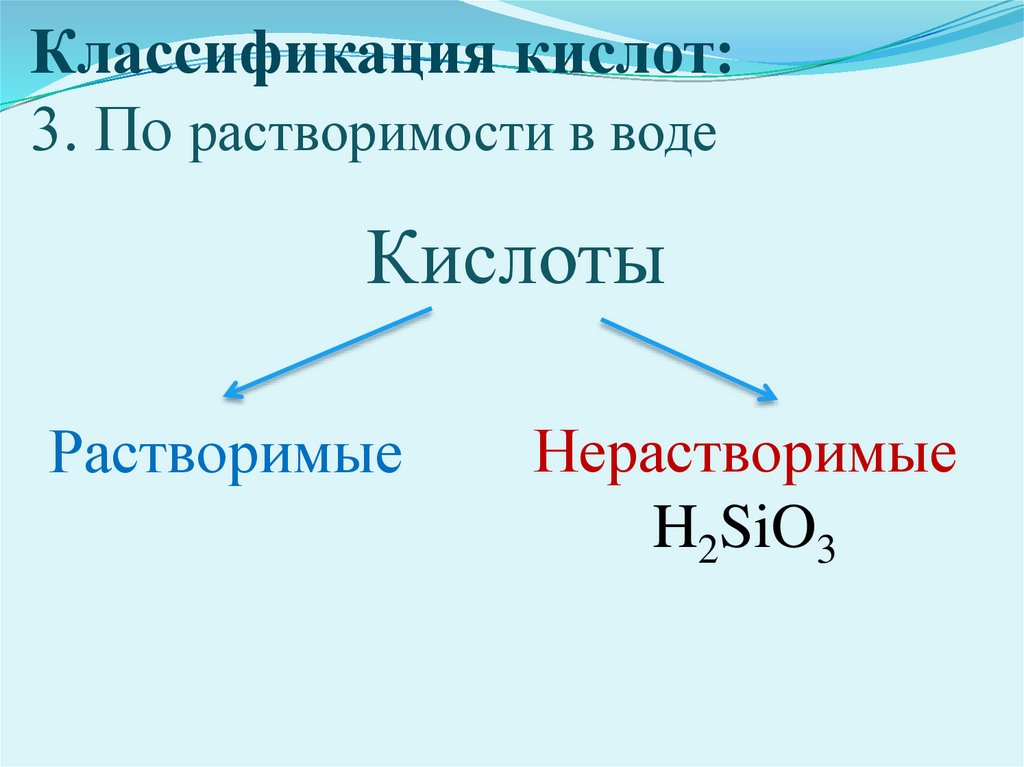
Классификация кислот:3. По растворимости в воде
Кислоты
Растворимые
Нерастворимые
H2SiO3
16.
Серная кислота - H2SO417.
ФизкультминуткаОчень химию мы любим!
Шеей влево, вправо крутим.
Воздух – это атмосфера.
Если правда - хлопай смело!
В атмосфере есть азот,
Делай вправо поворот!
Так же есть и кислород,
Делай влево поворот.
Воздух обладает массой.
Мы потопаем по классу!
К учителю повернемся
И дружно улыбнемся!
18.
Степень окисления –это условный заряд атомов
химического элемента в соединении,
вычисленный из предположения, что все
связи имеют ионный тип
19.
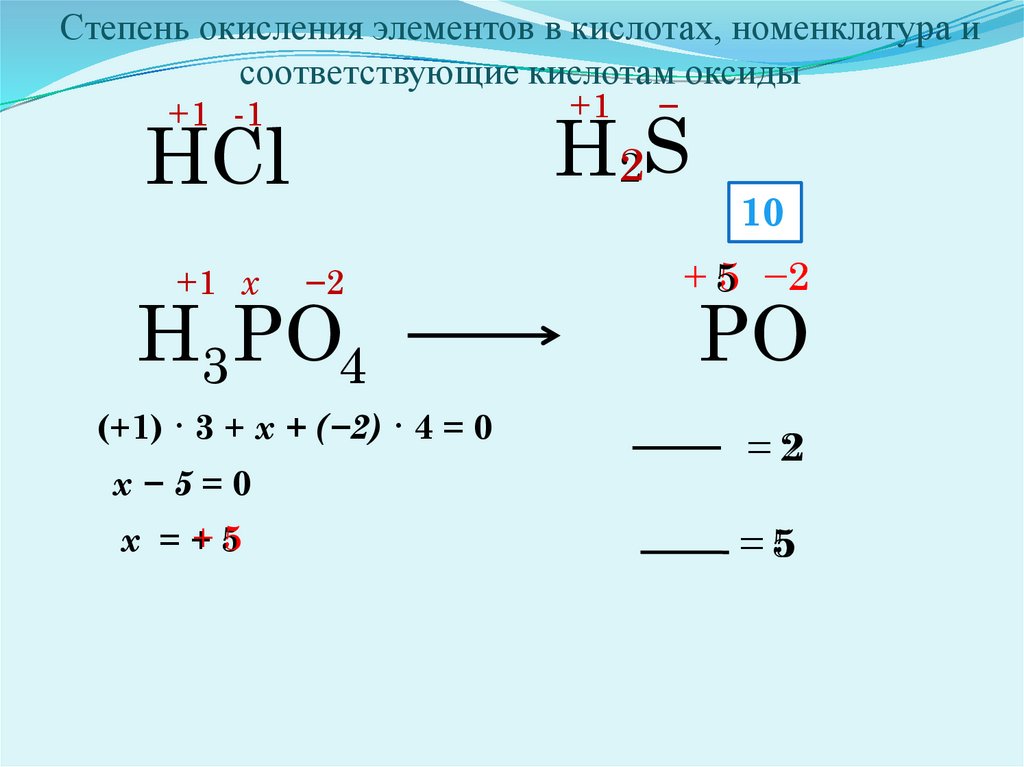
Степень окисления элементов в кислотах, номенклатура исоответствующие кислотам оксиды
+1
+1 -1
Н2S
НСl
+1 х
−2
Н3 РО4
(+1) · 3 + х + (−2) · 4 = 0
х−5=0
х =+5
−
10
+ 5 −2
2
РО
=2
=5
20.
Дайте характеристику кислотампо алгоритму:
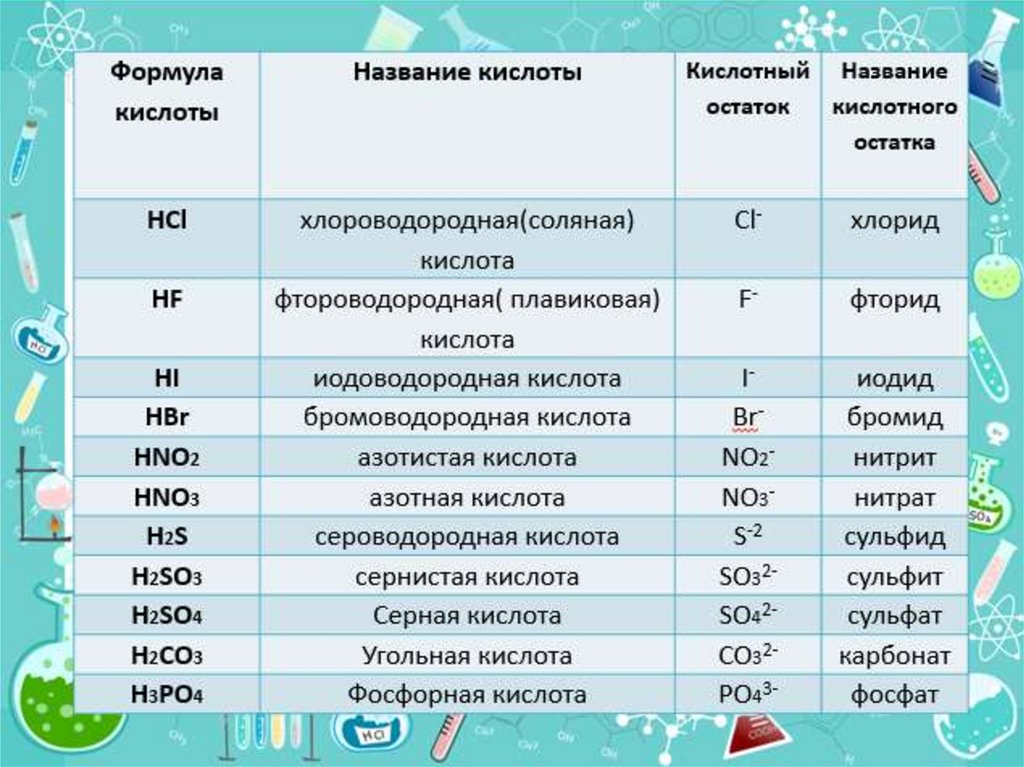
1.
Название кислоты
2.
Наличие кислорода
3.
Основность
4.
Растворимость
5.
Степень окисления элементов, образующих кислоту
6.
Заряд иона, образуемого кислотным остатком
7.
Соответствующий оксид
21.
Кислотные оксидыCI2 O7 →
CO2 →
N2 O5 →
S O3 →
22.
СамопроверкаCI2 +7O7 → Н CI +7O4
C+4O2 → Н2С+4О3
N2 +5O5, → Н N +5O3
S +6O3 → Н2 S +6O4
23.
Домашнее задание:1. Выучить формулы и названия кислот
2. § 21;
3. Дать характеристику кремниевой кислоте по
алгоритму ;
4. стр.126 упр. 3, 4 (а).
24.
ЗнаемХотим
узнать
Узнали
25.
«День прожит не зря,если ты узнал что-то новое»




















 chemistry
chemistry








