Similar presentations:
COVID-19 инфекция: вопросы и ответы
1.
COVID-19 инфекция:вопросы и ответы
Доцент кафедры инфекционных
болезней БГМУ Н.В.Соловей
13.02.2021
2.
Как показатели лабораторных исследованиймогут повлиять на выбор терапии
коронавирусной инфекции?
3.
Зачем нам данные лабораторныхисследований при лечении COVID-19?
1. Прогнозирование тяжелого течения COVID-19 на
момент обращения пациента за медицинской
помощью (= особая клиническая настороженность в
отношении пациентов с «неблагоприятным»
прогнозом)
2. Подтверждение развития гипервоспалительной фазы
инфекции (= кардинальное изменение тактики ведения
пациента)
3. Ранняя диагностика осложнений COVID-19 (органные
поражения, вторичные бактериальные и грибковые
инфекции, в том числе C.difficile-ассоциированная и
т.д.) (= добавление ЛС, направленных на купирование
возникших осложнений)
4.
Временная шкала COVID-19У пациентов c COVID-19
следует ориентироваться не на
сутки госпитализации, а на
сутки от появления симптомов
Начальная фаза
Легочная
фаза
Гипервоспалительная
фаза
Важно «поймать» ухудшающегося пациента для своевременных терапевтических
вмешательств!
«Критические дни» (переход в
8-12
гипервоспалительную фазу)
от момента
появления первых симптомов заболевания
Фиксируем дату
первых симптомов на
чек-листе или
медицинской карте!!!
Berlin D. et al. NEJM 2020
5.
Какие лабораторные показатели говорят огипервоспалительной фазе COVID-19?
прогрессирующее снижение PаO2/FiO2 в КЩС артериальной
крови (КЩС венозной крови бесполезна!!!)
прогрессирующее увеличение КФК, ЛДГ в БАК (маркеры
повреждения легких)
появление маркеров вовлечения в воспалительный процесс
иных органов, помимо легких
АЛТ и АСТ
мочевина и креатинина
амилазы и липазы
тропонина, КФК-МВ, миоглобина, proBNP и т.д.
прогрессирующая лимфопения, рост соотношения нейтрофилов
к лимфоцитам (NLR) в периферической крови (палочкоядерный
сдвиг – отражение тяжести COVID-19, а не присоединения
бактериальной инфекции!)
прогрессирующее увеличение ферритина, СРБ в БАК,
повышение / нарастание в динамике ИЛ-6
6.
Предлагаемая схема лабораторного мониторингагоспитализированного пациента с COVID-19 для ранней
диагностики гипервоспалительной фазы инфекции
ОАК: лейкоциты, нейтрофилы, лимфоциты, соотношение нейтрофилы /
лимфоциты, гемоглобин, гематокрит, тромбоциты
БАК: ЛДГ, КФК, альбумин, общий билирубин, АЛТ, АСТ, мочевина, креатинин,
электролиты, ферритин, СРБ, глюкоза
коагулограмма (с фибриногеном, Д-димерами)
уровень ИЛ-6 крови
+ при необходимости исключить бактериальную инфекцию, требующую неотложного назначения
антибиотиков, – прокальцитонин
+ при подозрении на кардиальное повреждение – КФК-MB, миоглобин, высокочувствительный
тропонин
Стартовая точка
лабораторных показателей
Госпитализация
Отслеживание динамики лабораторных показателей
Каждые 5-7 дней
(стабильное
состояние)
Начало
прогрессирования – в
любые сроки!
(усугубление дыхательной
недостаточности, появление
внелегочных осложнений)
Наиболее важен не единичный результат, а динамика ключевых
лабораторных маркеров тяжелой COVID-19 инфекции
7.
Сценарии динамической оценки ключевых лабораторныхпоказателей при COVID-19
Появление / отрицательная динамика маркеров
гипервоспалительной фазы COVID-19
Прогрессирующее
снижение сатурации
Блокаторы рецепторов
ИЛ-6 или аналогичные
средства ВНЕ
ЗАВИСИМОСТИ от
проводимой терапии ГКС
Отрицательная динамика
Стабильная сатурация
Есть факторы риска осложненного /
тяжелого течения COVID-19?
Да
Нет
Тщательные мониторинг
состояния и лабораторных данных
8.
Факторы риска тяжелого / осложненноготечения COVID-19
Лица с избыточным
весом (индекс массы
тела 30 и более!)
Лица старше 55-60 лет
Пациенты с
хроническими
Особое внимание к состоянию данных пациентов,
заболеваниями (особенно,
инфицированных SARS-CoV-2!
с сахарным диабетом 2
Коронавирусная инфекция также может приводить
типа и метаболическим
к обострению уже имеющихся хронических
синдромом!)
заболеваний, в том числе сосудистым катастрофам!
9.
Молодые пациенты с избыточнымвесом – группа риска по тяжелому
течению COVID-19!
Госпитализируем пожилых пациентов
с высоким ИМТ – даже при вначале не
тяжелом течении инфекции!!!
Brodin P. Nature Medicine 2021; 27:28
10.
При подозрении на присоединение бактериальной инфекции иее прогрессию может быть полезным прокальцитонин!
• остается неясным, повышается ли прокальцитонин только в результате
наслоения бактериальной инфекции или также вследствие повреждения
собственных органов и тканей у пациентов с COVID-19
• мета-анализ 14 исследований, 3492 пациента:
– повышенный уровень прокальцитонина ассоциирован с тяжелым течением
заболевания (ОР 5,92, 95% ДИ 3,20-10,94), неблагоприятными исходами (ОР 13,1,
95% ДИ 7,37-23,1)
– частота вторичных бактериальных инфекций варьировала от 4,8% до 19,5%
– 89,7% вторичных бактериальных инфекций развивались у ТЯЖЕЛЫХ пациентов
с COVID-19, ассоциировались с осложненным течением заболевания,
неблагоприятным прогнозом и высокими уровнями прокальцитонина
Повышенный уровень прокальцитонина не всегда свидетельствует о наличии
бактериальной инфекции у пациентов с тяжелой COVID-19 инфекцией
Нормальные значения прокальцитонина предполагают очень низкую вероятность
наличия бактериальной инфекции, требующей безотлагательного назначения
системной антибактериальной терапии
Vazana N. et al. Acta Clinica Belgica 2020
11.
Всем ли пациентам надо КТ ОГК, чтобы имописали пневмонит («матовые стекла»)?
12.
Рентгенологическая динамика у пациентов с COVID-19в зависимости от длительности заболевания
На ранних стадиях COVID-19 патологические отклонения
на обзорной Р-графии ОГК могут отсутствовать!
Отсутствие явных изменений на Р-графии ОГК при
наличии клиники пневмонита не говорит, что у
пациента «всех хорошо» и он не нуждается в
госпитализации! Первична клиника, параклинические
исследования – вторичны!!!
Stogiannos N. et al. Radiography 2020
13.
Затемнения по типу «матового стекла» у пациентов спневмонией, вызванной SARS-CoV-2
Три последовательных аксиальных среза КТ ОГК,
демонстрирующих мультифокальные затемнения по типу
«матового стекла» без признаков консолидации (слева) и
трехмерная объемная реконструкция, демонстрирующая
распределение затемнений по типу «матового стекла»
Зоны «матового стекла» – зоны гипоперфузии легочной ткани
Liu P. & Tan X.-Z. Radiology 2020
14.
Инструментальные данные на КТ ОГК при COVID-19на момент госпитализации пациентов
• Отклонения на КТ ОГК у всех пациентов,
у 98% (40/41) – двустороннее поражение
• Типичные отклонения у реанимационных
пациентов – билатеральные
мультилобальные и субсегментарные
зоны консолидации легочной ткани (А)
• Типичные отклонения у не
реанимационных пациентов – изменения
легочной ткани по типу матового стекла и
субсегментарные зоны консолидации (В)
• Впоследствии КТ ОГК демонстрировало
сохранение Р-картины матового стекла с
разрешением зон консолидации (С)
15.
Клинические характеристики COVID-19• Мета-анализ 10 исследований, общее число пациентов 50.446
• Распределение симптомов:
– лихорадка 89,1% (95% ДИ 81,8%-94,5%)
– кашель 72,2% (95% ДИ 65,7%-78,2%)
– миалгии или слабость 42,5% (95% ДИ 21,3%-65,2%)
• Отклонения по результатам КТ ОГК – у 96,6% (95% ДИ 92,1% - 99,3%)
ВИРУСНЫЙ ПНЕВМОНИТ ЕСТЬ ПРАКТИЧЕСКИ У ВСЕХ!
• Тяжелые случаи COVID-19 – у 18,1% (95% ДИ 12,7% - 24,3%)
• РДСВ развился у 14,8% (95% ДИ 4,6%-29,6%)
• Летальность 4,3% (95% ДИ 2,7% - 6,1%
Нет смысла выполнять КТ ОГК всем пациентам с COVID-19 – мы и так знаем,
что пневмонит будет даже у многих амбулаторных пациентов с нетяжелым
течением инфекции.
Чрезмерный акцент на КТ (врач лечит не КТ ОГК, а пациента!), указание
«объема поражения», «отрицательной динамики по КТ» может негативно
сказываться на психоэмоциональном состоянии пациентов, затрудняя их
выздоровление!
Sun P. et al. J Med Virol 2020; doi: 10.1002/jmv.25735
16.
Клинико-лабораторные критерииустановления диагноза COVID-19
1.
2.
3.
Однократный положительный тест ПЦР или
однократный положительный тест на
антиген SARS-CoV-2 в назофарингеальных
мазках
Типичная рентгенологическая симптоматика
(по данным КТ), клиническая картина, с
последующим положительным тестом
лабораторной диагностики.
Один положительный тест серологической
диагностики (в том числе ИХИ) в сочетании
с клинической картиной инфекции COVID19 (или один положительный тест серологической
диагностики (в том числе ИХИ) при отсутствии
клиники (бессимптомная форма) у контактов 1-ого
уровня)
Для установления диагноза достаточно наличия у пациента
ОДНОГО из клинико-лабораторных критериев
КТ ОГК может быть необходимым для верификации
диагноза COVID-19, если, несмотря на клинические
проявления, результаты молекулярно-генетических и
серологических обследований отрицательны
СРЕДНЯЯ и ВЫСОКАЯ вероятность
наличия вирусной пневмонии,
обусловленной COVID-19 по КТ паттернам
(приложение 5 приказа МЗ РБ 1195)
В заключении КТ должна отражаться
специалистом!
Характерный КТ паттерн расцениваем как
COVID-19, госпитализируем вместе с
пациентами с COVID-19, обследуем и лечим
согласно протоколу (приказу МЗ) 1195
Сроки ПОСЛЕДУЮЩЕГО
ПОЛОЖИТЕЛЬНОГО теста не
регламентированы (через неделю? через
месяц?)
IgM часто неспецифичны! (риск
ложноположительных результатов)
Клиника не регламентирована приказом
1195
На практике: IgM к SARS-CoV-2 + либо
характерный КТ паттерн либо
двухсторонняя интерстициальная пневмония
на Р-грамме ОГК либо симптоматика ОРЗ с
аносмией / дисгевзией
Приказ МЗ РБ от 11.11.2020 № 1195
17.
Зависит ли вероятность инфицирования и тяжестьтечения COVID-19 от возраста, пола,
национальности, группы крови?
18.
COVID-19 и возраст пациента• Анализ рисков инфицирования и неблагоприятного
исхода заболевания среди 5319 пациентов с
лабораторно доказанной COVID-19 инфекцией в
КНР
Риск инфицирования COVID-19 в
зависимости от возраста и пола
Риск летального исхода вследствие
COVID-19 в зависимости от
возраста пациентов
Hogndou L. et al. Frontiers in Medicine 2020; 7:article 190
19.
Систематическийобзор и мета-анализ
27 исследований из
34 географических
регионов
Экспоненциальная зависимость летальности от
возраста пациентов
Экспоненциальное
увеличение
летальности от
COVID-19 в
зависимости от
медианы возраста
пациентов:
10 лет -0,002%
25 лет – 0,01%
55 лет – 0,4%
65 лет – 1,4%
75 лет – 4,6%
85 лет – 15%
Levin A. et al. European Journal of Epidemiology 2020; 35:1123
20.
COVID-19: кто на самом деле «слабый пол»?• не продемонстрировано убедительных данных, что мужской
или женский пол предрасполагает к более частому
инфицированию COVID-19
• в то же время мужской пол ассоциирован с более частым
развитием тяжелого течения заболевания, необходимостью
госпитализации в реанимационное отделение, повышенной
частотой осложнений и неблагоприятных исходов
коронавирусной инфекции
Данные нескольких Европейский стран
Инфицирование COVID-19 наблюдалось с частотой 1:1 у
мужчин и женщин
У мужчин гораздо чаще отмечались необходимость в
госпитализации, поступление в ОРИТ, неблагоприятные
исходы болезни
Gebhard C. et al. Biol Sex Differ 2020; 11:29
21.
COVID-19 и расовая принадлежность• ряд исследований демонстрируют, что определенные расы (в
частности, афроамериканцы, латиноамериканцы и азиаты)
предрасположены к более частому инфицированию COVID19, а также большему риску ее тяжелого течения и
неблагоприятного исхода
Sze S. et al. EClinicalMedicine 2020; 29-30:100630
Rentsch C. et al. PLOS Medicine 2020; doi: 10.1371/journal.pmed.1003379
Jones J. et al. J Med Internet Res 2020; 22:e20001
• существуют определенные различия по распространенности
инфицирования COVID-19 в зависимости от географического
региона, что частично может быть ассоциировано с
распределением уровней витамина Д в популяции
22.
Влияет ли уровеньвитамина Д на риск
инфицирования
COVID-19
А – распространенность
недостаточности витамина
Д в популяции по миру
В – распространенность
инфицирования СOVID-19
в различных регионах
Наиболее уязвимые
популяции и страны к
COVID-19 имеют
наибольшую
распространенность
дефицита витамина Д
Verdoia M. & De Luca G. QJM: An
International Journal of Medicine 2020
23.
Каково влияние групп крови на COVID-19?• по результатам
систематического обзора
и мета-анализа 4
исследований группа
крови А (II)
ассоциирована с
предрасположенностью
к COVID-19, в то время
как пациенты с О (I)
группой наименее
чувствительны к
инфицированию новым
коронавирусом
24.
Внелегочные проявления Сovid-19(неврологические, поражения кожи,
гастроинтестинальные)
25.
Поражения кожи при COVID-19Эритематозно-фиолетовые
или пурпурные макулы на
пальцах рук, локтях, пальцах
ног и латеральной части
стоп с или без
сопутствующих отеков и
зуда. Разрешение через 2-8
недель. Возможно, в случае
явного дискомфорта
эффективны ГКС
• систематический обзор (публикации до
06.05.2020)
• 1593 пациента с предполагаемой COVID-19,
мужчины: женщины = 1:9, средний возраст 37,8
лет (от 0 до 91 года), 5,3% - дети до 18 лет
• перниоподобные (обморожение подобные)
поражения дистальных участков конечностей
(акроваскулиты, «ковидные пальцы») – 46%
всех сообщаемых кожных поражений при
COVID-19
• у ¾ пациентов с COVID-19 кожные проявления
отмечались ДО ДРУГИХ типичных
клинических проявлений коронавирусной
инфекции
• при гистологическом исследовании васкулиты
и/или тромбозы выявлены практических у 70%
пациентов с кожными проявлениями COVID-19
Perna A. et al. International Journal of Dermatology 2021
26.
Классификация поражений кожи при COVID-19• обзор англоязычных публикаций до 20 мая 2020 г. включительно с
кожными поражениями при COVID-19
• обобщение всех паттернов поражений кожи в 4 группы
Паттерн
Субтип
Локализация
Начало
Возраст
Симптомы
Экзантема
Варицелло
подобная
папулловезикулярная
Туловище ±
конечности
Раннее
Преимуществен
но взрослые
Зуд
Кореподобная
Туловище ±
конечности
Раннее
Взрослые
Зуд
Перниоподобные
поражения
Пальцы
Позднее
Преимуществен
но дети
Зуд
Пурпура /
петехиальная
сыпь
Туловище,
ягодицы,
конечности
Позднее
Взрослые
Жжение
Ливедоидные
поражения
Конечности
Позднее
Взрослые
Отсутствуют
Крапивница
Волдыри
Лицо, верхняя
часть туловища
Раннее
Взрослые
Зуд, лихорадка
Акропапуллезный
Эритематозные
папулы
Конечности
Позднее
Взрослые
Зуд
Сосудистый
Gisondi P. et al. JEADV 2020; 34:2499
27.
Примеры кожных поражений при COVID-19COVID-19-ассоциированная
пурпура на нижних конечностях
Ливедоидные /
пурпурные бляшки на
нижних конечностях
Диффузный острый
генерализованный
экзантематозный пустуллез
как побочная реакция на
гидроксихлорохин
Gisondi P. et al. JEADV 2020; 34:2499
28.
Гастроинтестинальные поражения при COVID-19Cha M. et al. World J Gastroenterol 2020; 26:2323
29.
Диарея – наиболее часто встречающееся поражениеЖКТ при COVID-19 после анорексии (1)
Abbasinia M. et al. Gastroenterology Nursing 2021; 44:E1
30.
Диарея – наиболее часто встречающееся поражениеЖКТ при COVID-19 после анорексии (2)
Abbasinia M. et al. Gastroenterology Nursing 2021; 44:E1
31.
Гастроинтестинальные поражения при COVID-19• 318 пациентов, госпитализированных с COVID-19
– 61% (195/318) – по меньшей мере 1 симптом со стороны
ЖКТ
• 35% - анорексия
• 34% - диарея
• 26% - тошнота
Redd W. et al. Gastroenterology 2020; 159:765
• 204 пациента, госпитализированных с COVID-19
– 50,5% (103/204) – по меньшей мере 1 симптом со стороны
ЖКТ
78,6% - анорексия
34% - диарея
4,9% - рвота
1,9% - абдоминальные боли
Pan L. et al. Am J Gastroenterol 2020; 115:766
Наличие эпизода диареи – у 1/3 пациентов с COVID-19!
Особое внимание при поступлении пациентов с клиникой «острой кишечной
инфекции» в период пандемии COVID-19!!!
32.
Лекарственно-индуцированные и COVID-19ассоциированные поражения печени
Anirvan P. et al. World J Hepatol 2020; 12:1182
33.
COVID-19 и поджелудочная железа• До 10% всех случаев острого панкреатита могут иметь
вирусный генез (наиболее часто вирус эпидемического
паротита, энтеровирусы, цитомегаловирус и т.д.)
• Острый панкреатит на фоне вирусной инфекции может быть
обусловлен:
– непосредственным цитопатическим поражением поджелудочной
железы вирусом
– дизрегуляторным воспалительным ответом, индуцированным
возбудителем (иммуноопосредованный механизм)
– лекарственными средствами, используемыми для лечения
вирусной инфекции
• Среди пациентов с тяжелой COVID-19 инфекцией:
– до 17% имеют признаки повреждения поджелудочной железы в
виде повышенной амилазы и липазы крови
– до 7% - визуализационные признаки, сопоставимые с
Liu F. et al. Clinical Gastroenterology and Hepatology 2020;18:2128
панкреатитом
Wang F. et al. Gastroenterology 2020
34.
Количество АПФ-2 (основного рецептора для SARSCoV-2) в поджелудочной железе больше, чем в легких• экспрессия информационной РНК АПФ-2 в клетках и тканях различных
органов
• АПФ-2 экспрессируется как на клетках экзокринных желез, так и на
клетках островков поджелудочной железы (острое развитие сахарного
диабета при COVID-19?)
Liu F. et al. Clinical Gastroenterology and Hepatology 2020;18:2128
35.
Как часто наблюдается вовлечение поджелудочнойжелезы при COVID-19 инфекции?
1.
2.
3.
Повышение
амилазы и липазы
наблюдалось
преимущественно у
тяжелых пациентов
При визуализации
видимых
изменений
поджелудочной
железы у
большинства
пациентов (8/13) не
было
Ни у одного
пациента не
развился
панкреонекроз
Liu F. et al. Clinical Gastroenterology and Hepatology 2020;18:2128
36.
Повышение липазы крови у пациентов сCOVID-19
• когортное исследование, 1003 последовательных пациента с
COVID-19
• у 83/1003 определялась липаза сыворотки крови (все
госпитализированы в стационар)
• у 16,8% (14/83) – повышение значений липазы выше 3 норм
от верхней границы
• по сравнению с пациентами с более низкими значениями
липазы, пациенты с более высокими значениями чаще
госпитализировались в ОРИТ (92,9% vs 32,8%, р<0,001) и
чаще нуждались в ИВЛ (78,6% vs 23,5%, р=0,002)
• выраженное повышение липазы являлось независимым
предиктором неблагоприятного течения COVID-19
Barlass U. et al. Clinical and Translational Gastroenterology 2020; 11:e00215
37.
Вариабельность поражения поджелудочнойжелезы при COVID-19 инфекции
изолированное повышение ферментов (амилазы,
липазы) без клинических и радиологических
признаков острого панкреатита
субклиническое течение с лабораторными и
радиологическими признаками острого панкреатита
клиническая симптоматика, напоминающая
панкреатит при отсутствии убедительных
лабораторных и/или радиологических признаков
заболевания
явный эпизод острого панкреатита
Gupta V. et al. Indian Journal of Surgery 2020
38.
Разнообразие неврологических поражений при COVID19 инфекции39.
Неврологические поражения при COVID-19• неврологические проявления развиваются примерно у ½
госпитализированных пациентов с COVID-19:
– наиболее частые: головная боль и энцефалопатия / делирий
– менее частые: говокружение, дизосмия / дисгевзия
– редкие: острые нарушения мозгового кровообращения, двигательные
расстройства, сенсорные и/или моторные полиневропатии, атаксии,
судороги, миелиты, менингиты и энцефалиты, генерализованный
миоклонус
• как во время активной инфекции, так и вскоре после нее возможны
неврологические иммуноопосредованные осложнения:
– острая воспалительная демиелинизирующая полинейропатия (синдром
Гийена-Барре)
– острый диссеминированный энцефаломиелит
– дебют рассеянного склероза и других иммуновоспалительных
поражений нервной системы
https://www.uptodate.com/contents/coronavirus-disease-2019-covid-19-neurologic-complications-and-management-of-neurologicconditions?search=covid%20neurologic&source=search_result&selectedTitle=1~150&usage_type=default&display_rank=1#H4153922458
40.
Потенциальные механизмы развитияОНМК у пациентов с COVID-19
1. Индукция выброса
SARS-CoV-2 каскада
провоспалительных
цитокинов
эндотелиальная
дисфункция, тяжелая
гиперкоагуляция, микро- и
макротромбозы
2. Нарушение функции
РААС в головном мозге,
обеспечивающей
антигипертензивный,
антитромботический,
антиатеросклеротический,
ангиогенный,
нейропротективный и
антиоксидантный
эффекты
3. Сопутствующее
поражение других органов
и систем (инфаркт
миокарда, аритмии,
кардиоэмболические
события и т.д.)
Kolikonda M. et al. Neuroepidemiology 2020;54:370
Fan H. et al. Neuropsychiatric Disease and Treatment 2020; 16:1359
41.
Как часто инсульт встречается среди всехневрологических поражений при COVID-19?
• систематический обзор случаев ишемического инсульта у пациентов с
COVID-19 с 1 декабря 2019 г. по 29 мая 2020 г.
• 39 работ, 135 пациентов
• распространенность ишемического инсульта - 1,2% (54/4466), варьировала
от 0,9% до 2,7% (обсервационные исследования)
• средний возраст 63,4±13,1 лет
• среднее время дебюта ОНМК от первых симптомов COVID-19 – 10±8
дней
• средний балл по шкале NIHSS - 19±8
• повышены средние уровни Д-димеров (9,2 ± 14,8 мг/л) и фибриногена (5,8
± 2,0 г/л); у значительного числа пациентов обнаружены
антифосфолипидные антитела
• нейровизуализация: большинство пациентов имело тромбоз крупных
церебральных артерий , эмболии или стеноз (62,1%); у 26,2%
регистрировался мультифокальный инсульт
• летальность – 38,0% (49/129)
42.
Как часто встречаются внутримозговыекровоизлияния (ВМК) у пациентов с COVID-19?
• ретроспективное когортное исследование
• 416 пациентов с подтвержденной COVID-19, которым
выполнялась нейровизуализация
– 7,9% (33/416) – внутримозговое кровоизлияние
– средний возраст 69,3±16,2 года
– мужчины – 64,2%
– получали антикоагулянты в лечебной дозе – 34,9%
• в регрессионном анализе антикоагулянтная терапия в
лечебной дозе ассоциировалось с повышенным риском
развития ВМК (OR 5,26, 95% ДИ 2,33-12,24, p<0,001)
• наличие ВМК увеличивало риск неблагоприятного исхода
(OR 2,6, 95% ДИ 1,2-5,9)
Melmed K. et al. Journal of Thrombosis and Thrombolysis 2020
43.
COVID-19 ассоциированный церебральныйвенозный тромбоз: систематический обзор
• 9 исследований, 14 пациентов с COVID-19 ассоциированным
церебральным венозным тромбозом (ЦВТ)
• медиана возраста 43 года (квартили – 36-58 лет)
• отягощенный медицинский анамнез – 60%
• медиана времени от начала симптомов COVID-19 до ЦВТ – 7
дней (квартили 6-14 дней)
• наиболее частая локализация ЦВТ - поперечный (75,0%) и
сигмовидный (50,0%) синусы; у 33,3% - вовлечение глубоких
церебральных вен
• у 75% пациентов – повышение Д-димеров, у 50,0% - СРБ
• большинство пациентов получили антикоагулянтную
терапию (91,7%)
• летальность – 45,5%
Tu T. et al. Journal of Stroke and Cerebrovascular Diseases 2020; 29:105379
44.
ОНМК и COVID-19Риск развития ОНМК при COVID-19 гораздо выше, чем при
гриппе и других острых респираторных заболеваниях
Превалируют ишемические инсульты в бассейне средней
мозговой артерии, в меньшей степени регистрируются
внутримозговые кровоизлияния и тромбозы вен головного
мозга
COVID-19 ассоциированные ОНМК могут развиваться у лиц
молодого возраста без каких-либо иных предрасполагающих
факторов риска
COVID-19 ассоциированные ОНМК могут развиваться у лиц
БЕЗ КЛИНИЧЕСКОЙ СИМПТОМАТИКИ коронавирусной
инфекции
Летальность при COVID-19 ассоциированных ОНМК
существенно выше, чем при ОНМК у пациентов без COVID-19
45.
Почему проблема делирия значима дляпациентов с COVID-19?
пожилые пациенты – особая группа риска развития делирия,
как и тяжелого течения COVID-19
делирий может быть одним из первых симптомов
коронавирусной инфекции
развитие гиперактивного делирия у пациентов с COVID-19 частая причина неэффективности неинвазивных методов
респираторной поддержки и перевода пациентов на ИВЛ
гипоактивный делирий часто не диагностируется, являясь
значимым предиктором неблагоприятного исхода заболевания
стандартные меры профилактики делирия трудно реализуемы в
условиях работы с COVID-19
для купирования делирия более часто используются
психоактивные лекарственные средства
46.
•. 2020 Nov;68(11):2440-Как часто делирий встречается у пациентов с
COVID-19?
• мультицентровое когортное исследование, 7
стационаров США, 817 пациентов, 47% мужчины,
средний возраст 77,7 лет
• оценка распространенности делирия среди пожилых
пациентов с COVID-19, обращающихся в отделения
неотложной терапии
• на момент первичного обращения делирий
диагностирован у 28% (226/817)
• развитие делирия ассоциировалось с
необходимостью госпитализации в ОРИТ (кОШ 1,67,
95% ДИ 1,30-2,15) и летальным исходом (кОШ 1,24,
95% ДИ 1,00-1,55)
Kennedy M. et al. JAMA Network Open 2020; 3:e2029540
47.
•. 2020 Nov;68(11):2440-Как часто делирий встречается у пациентов с
COVID-19 в реанимационных отделениях?
• мультицентровое когортное исследование, 69 ОРИТ из 14 стран
• 2088 пациентов ≥ 18 лет, госпитализированные в ОРИТ с COVID-19,
с 20.01.2020 до 28.04.2020
• медиана возраста 64 года (IQR 54-71)
• 66,9% на ИВЛ на день поступления в ОРИТ, 87,5% - в какие-либо во
время госпитализации в ОРИТ
– 64% пациентов получали седацию бензодиазепинами, медиана
продолжительности 7 дней
– 70,9% - седацию пропофолом, медиана продолжительности 7 дней
• 81,6% находились в коме с медианой длительности 10 дней (IQR 615)
• у 54,9% развился делирий с медианой длительности 5 дней (IQR 014 дней)
• 28-дневная летальность – 28,8%
48.
У реанимационных пациентов с COVID-19 делирийвстречается чаще, чем у реанимационных пациентов с
другими нозологиями!
•. 2020 Nov;68(11):2440-
Arnold C. Nature 2020; 588:22
49.
Серия случаев дебюта COVID-19 с делирияИзменения
ментального
статуса
относительно
базового
уровня
Возбуждение
Респиратор
-ная
симптоматика
Миоклонус
Ригидность
М., 76
лет
+
+
-
+
+
+
+
+
+
М., 70
лет
+
+
-
+
+
+
+
+
+
М., 68
лет
+
+
-
-
-
+
+
+
-
Ж., 87
лет
+
+
+
+
-
-
-
+
-
3 из 4 пациента –
мужчины, все
пациенты – старше
65 лет, все – с
предшествующими
когнитивными
нарушениями
(уязвимая группа?)
У всех нарушение
ментального
статуса – первый
признак COVID-19
и причина
обращения за
медицинской
помощью
Только у 1 из 4
пациентов имелась
явная респираторная
симптоматика, только у
2 из 4 – невыраженная
транзиторная
лихорадка и только у 2
из 4 – изменения на КТ
ОГК
Абулия
Алогия
Повышенный СРБ
Сыпь
У 3 из 4 пациентов –
мультифокальный миоклонус, у 2 из 4
– с гипертонусом
(гиперчувствительность базальных
ганглиев к вирусу и индуцируемому
им аутоиммунному воспалительному
ответу?)
Beach S. et al. General Hospital Psychiatry 2020; 65:47
50.
Медикаментозное лечение делирия при COVID-19:рекомендации Королевского колледжа психиатров (Великобритания) (3)
Лекарственное
средство
Путь введения
Диапазон
дозы (мг)
Кратность дозирования
в течение суток
Рекомендуемая
максимальная суточная
доза
Лоразепам
Перорально / внутримышечно /
внутривенно
0,5-1
От 1 до 4 раз в день
2 мг
Галоперидол
Перорально / внутримышечно /
подкожно (доступна жидкая
форма)
0,5-2
От 1 раза в день до
6-12 раз (каждые 24 часа)
5 мг
Рисперидон
Перорально (доступна жидкая
форма)
0,25-0,5
От 1 до 2 раз в день
2 мг
Оланзапин
Перорально / внутримышечно
(доступна жидкая форма)
2,5-5,0
От 1 до 2 раз в день
10 мг
Кветиапин
Перорально (доступна жидкая
форма)
12,5-50
От 1 до 2 раз в день
100 мг
Если нет улучшения состояния пациента в течение 4 дней – следует:
1) пересмотреть первоначальный диагноз делирия (исключаем другие органические
поражения нервной системы!!!)
2) продолжаем лечить сопутствующие делирию заболевания, интеркуррентные
инфекции
3) контролируем факторы, способствующие поддержанию делирия (дегидратация,
констипация, болевой синдром, побочные эффекты лекарственных средств и т.д.)
Delirium management advice for patients with confirmed or suspected COVID-19 in the acute trust setting
Available at: https://www.rcpsych.ac.uk/docs/default-source/members/faculties/old-age/covid-19-delirium-management-guidance.pdf?sfvrsn=2d5c6e63_4
51.
Энцефалопатия /делирий при COVID19
4 пациента старше 60
лет с COVID-19
впервые возникшие
когнитивные
нарушения, очаговые
неврологические знаки
или судороги
ни у одного не было
признаков энцефалита
на МРТ или
существенных
изменений ЦСЖ
все пациенты
улучшились после
иммунотерапии
(внутривенный
нормальный
иммуноглобулин
человека или пульстерапия
метилпреднизолоном)
Delorme C. et al. European Journal of Neurology 2020; 27:2651
52.
у всех 4 пациентов –одни и те же
патологические
изменения на ФДГПЭТ/КТ:
гипометаболизм в
лобных долях и
мозжечковый
гиперметаболизм
Delorme C. et al. European Journal of Neurology 2020; 27:2651
53.
COVID-19 индуцированная энцефалопатия• 5 пациентов (средний возраст 66,8 лет) развили
энцефалопатию после в среднем 12,6 дней от первых
симптомов COVID-19
• нарушение сознания, возбуждение, делирий, пирамидные
и экстрапирамидные знаки
• у всех МРТ ГМ – без специфических патологических
отклонений, отсутствие плеоцитоза и повышения уровня
белка в ЦСЖ, отрицательный результат ПЦР на РНК
SARS-CoV-2 в ЦСЖ
• ВНИГ 0,4 г/кг/сут в течение 5 дней, средние сроки
назначения ВНИГ – 29,8 дней от начала энцефалопатии
(диапазон 19-55 дней)
• улучшение нейропсихиатрической симптоматики – уже в
среднем через 3,4 дня (диапазон от 1 до 10 дней)
Muccioli L. et al. Journal of Neurology 2020
54.
Клинический случай COVID-19ассоциированного делирия (энцефалопатии) (1)
• пациент М., 56 лет
• поступил в УЗ «Городская клиническая
инфекционная больница» 27.11.2020 г. с диагнозом:
COVID-19 (ПЦР РНК SARS-CoV-2+ от 25.11.2020):
двусторонняя полисегментарная первично-вирусная
пневмония, ДН 0-1 ст.
• получал лечение: парацетамол, фрагмин,
дексаметазон, пантопразол, урсодеоксихолевая
кислота, гипотензивные
• на 13-ый день заболевания (10.12.2020) лечащим
врачом и родственниками отмечено «изменение
поведения» пациента
М.Т.Хитрун, Н.В.Соловей (в процессе публикации)
55.
Клинический случай COVID-19ассоциированного делирия (энцефалопатии) (2)
• консультация невролога 10.12.2020:
– самостоятельных жалоб на самочувствие пациент не предъявлял
– пациент дезориентирован во времени, частично ориентирован в месте
и собственной личности, восприятие не нарушено, значительно
нарушен устный счет и кратковременная память; концептуализация – 0
баллов. Пациент не смог назвать возраст своих детей, не смог описать
суть своей профессиональной деятельности
– при объективном неврологическом осмотре из отклонений – только
повышение тонуса в правой верхней конечности по
экстрапирамидному типу
• выполнена ЛП:
-
общеклиническое исследование ЦСЖ – без отклонений
интратекальные антитела к SARS-CoV-2 и ПЦР ЦСЖ на РНК SARSCoV-2 – отрицательные
ПЦР ЦСЖ на ДНК ВПГ-1,2, ВЗВ – отрицательная
• МРТ головного мозга с контрастированием: без патологии
М.Т.Хитрун, Н.В.Соловей (в процессе публикации)
56.
Клинический случай COVID-19ассоциированного делирия (энцефалопатии) (3)
• выставлен диагноз: COVID-19-ассоциированная
энцефалопатия (делирий)
• назначен внутривенный нормальный иммуноглобулин
человека в дозе 0,4 мг/кг/сут внутривенно капельно в течение
5 дней
• на 5-ый день лечения:
– частично ориентирован во времени (называет месяц и год),
ориентирован в месте и собственной личности, восприятие
не нарушено. Положительная динамика по устному счету
(считает до 3 действия), сохранялись нарушения
кратковременной памяти; концептуализация – 0 баллов.
– в объективном неврологическом статусе сохраняется
повышение тонуса в правой верхней конечности по
экстрапирамидному типу
М.Т.Хитрун, Н.В.Соловей (в процессе публикации)
57.
Клинический случай COVID-19ассоциированного делирия (энцефалопатии) (4)
• на 7-ой день лечения:
– пациент всесторонне ориентирован, восприятие не
нарушено, устный счет выполняет, кратковременная
память не нарушена; концептуализация – 3 балла
– в объективном неврологическом статусе сохраняется
повышение тонуса в правой верхней конечности по
экстрапирамидному типу
Выписан из стационара с выздоровлением
М.Т.Хитрун, Н.В.Соловей (в процессе публикации)
58.
Тест рисования часов (задание: «без десятидва») у пациента М. в динамике:
59.
COVID-19 у онкологических пациентов: есть лиособенности?
60.
Взаимосвязь между злокачественными новообразованиями,коморбидной патологией и COVID-19
61.
Терапия злокачественных новообразований сопровождается развитиемкоморбидных состояний, аггравирующих течение COVID-19
62.
COVID-19 и рак: особенности клинического течения• COVID-19 характеризуется более тяжелым течением, более
частыми осложнениями и неблагоприятными исходами у
пациентов со злокачественными новообразованиями:
– мета-анализ 32 исследований, 46.499 пациентов, 1776 со
злокачественными новообразованиями
• общая летальность выше у пациентов с раком (ОР 1,66, 95% ДИ 1,33-2,07)
• в подгрупповом анализе пациентов старше 65 лет общая летальность была
сопоставимой у пациентов с и без рака (ОР 1,06, 95% ДИ 0,79-1,14)
• необходимость в госпитализации в ОРИТ выше у пациентов с раком (ОР
1,56, 95% ДИ 1,31-1,87)
Giannakoulis V. et al. JCO Glob Oncol 2020; 6:799
– ретроспективный анализ из Великобритании, 17 млн
индивидуумов, 10.000 случаев смерти от COVID-19,
мультивариантный анализ
• пациенты с негематологическими опухолями, диагностированными в
течение предшествующего года, - риск смерти выше в 1,8 раз
• пациенты с гемобластозами – риск смерти выше в 4 раза
Williamson E. et al. Nature 2020; 584:430
63.
COVID-19 и рак: что известно сегодня• большинство исследований предполагает большую частоту
встречаемости COVID-19 у пациентов со злокачественными
новообразованиями, особенно с гемобластозами и раком
легких
• в большинстве случаев активное лечение рака должно быть
отсрочено / отменено до излечения активной COVID-19
инфекции (исключение – ингибиторы тирозинкиназы
Брутона – по некоторым исследованиям могут обуславливать
менее тяжелое течение COVID-19)
• часть глубоко иммунокомпрометированных пациентов с
раком могут длительно выделять жизнеспособный вирус
(вплоть до 60 дней от даты первых симптомов)
https://www.uptodate.com/contents/coronavirus-disease-2019-covid-19-risks-for-infection-clinical-presentation-testing-and-approach-to-infectedpatients-with-cancer?search=covid%20cancer&source=search_result&selectedTitle=1~150&usage_type=default&display_rank=1#H2969848688
64.
Пациенты с лимфопролиферативными заболеваниями, получившие терапиюритуксимабом, часто не могут самостоятельно элиминировать SARS-CoV-2
пациент С., 44 года
основной диагноз: Фолликулярная неходжкинская лимфома с поражением
подмышечных, паховых, забрюшинных л/у, л/у брюшной полости, стадия 3.
Состояние после 8 курсов ПХТ 2016-2017 гг. Состояние после лечения
неходжкинской лимфомы 2018 г ритуксимабом 2017-2019 гг.
Динамика заболевания:
–
–
–
–
–
–
–
–
–
–
–
конец мая 2020 г. – аносмия, слабость
начало июня – лихорадка до 38,0 С, ПЦР SARS-CoV-2+
июнь-июль – стационарное лечение, антибиотики, гидроксихлорохин, антикоагулянты, дексаметазон.
Разрешение температуры
через 3 недели после выписки из стационара – сухой кашель, лихорадка
август – госпитализация, внутривенный нормальный иммуноглобулин человека, разрешение
лихорадки
через 2 недели после выписки из стационара (середина августа – сентябрь) – лихорадка до 37,5 С 7
дней, затем до 38 С, принимал НПВС без особого эффекта
повторная госпитализация через 1 месяц (октябрь 2020), самостоятельное разрешение лихорадки в
течение недели
в конце октября родственники заболели с симптомами ОРВИ, после чего с начала ноября аналогичные
симптомы появились у пациента (лихорадка, насморк, кашель)
по данным многочисленных КТ – рецидивирующее течение COVID-19 инфекции, исключение
рецидива лимфомы
ПЦР на РНК SARS-CoV-2 из носоглотки: положительно от 05.06.20, отрицательно от 13.10.20,
19.10.2020 и 16.12.2020, SARS-CoV-2 IgG при повторных исследованиях отсутствовали
22.12.20 госпитализация в УЗ ГКИБ
65.
Пациенты с лимфопролиферативными заболеваниями, получившие терапиюритуксимабом, часто не могут самостоятельно элиминировать SARS-CoV-2
• несмотря на отсутствие положительных результатов ПЦР
респираторных смывов на SARS-CoV-2, учитывая наличие
ритуксимаб-индуцированного В-клеточного иммунодефицита,
рецидивирующее течение заболевания, результаты КТ ОГК принято
решение об использовании антиковидной плазмы реконвалесцентов
• 4 трансфузии в течении недели
• нормализация температуры через день после 1-ой трансфузии
антиковидной плазмы, клиническое выздоровление в течение недели
Введение первой дозы антиковидной плазмы
66.
Необходимы ли глюкокортикостероиды прилечении COVID-19 амбулаторным пациентам?
67.
ГКС при COVID-19 инфекции: польза и рискиПотенциальная польза
Купирование чрезмерного
воспалительного
иммунного ответа и
прогрессии заболевания,
уменьшение повреждения
легких и внелегочных
осложнений
Уменьшение вероятности
фиброза легких
Потенциальные риски
Замедление элиминации
вируса (при раннем
назначении!!!)
Предрасположенность к
вторичным
бактериальным
инфекциям
Побочные эффекты
(гипергликемия и
декомпенсация СД,
гипокалиемия, асептический
некроз головки бедренной
кости)
68.
Роль дексаметазона у пациентов с COVID-19,нуждающихся в респираторной поддержке: данные
исследования RECOVERY
• исследование RECOVERY (Randomised Evaluation of COVid-19
thERapY), Великобритания
• 2104 пациента, получавшие дексаметазон 6 мг 1 раз в день
перорально или внутривенно 10 дней, 4321 пациент в группе
стандартной терапии
• назначение дексаметазона на 1/3 уменьшало риск 28-дневного
летального исхода у пациентов на ИВЛ (ОР 0,65, 95% ДИ 0,480,88, р = 0,0003) и на 1/5 у пациентов, нуждавшихся только в
поддержке кислородом (ОР 0,80, 95% 0,67-0,96, р = 0,0021)
• дексаметазон не влиял на выживаемость пациентов, не
требовавших респираторной поддержки (!!!)
Основываясь на данных результатах, 1 смерть может
быть предотвратима при лечении дексаметазоном 8
пациентов на ИВЛ и 25 пациентов, требующих только
дополнительной поддержки кислородом
69.
Кому показаны ГКС при COVID-19 инфекции внереанимационных отделений?
• пациенты с подтвержденной COVID-инфекцией и
двухсторонним поражением легких (по результатам
КТ грудной клетки или рентгенографии грудной
клетки), нуждающиеся в подаче кислорода через
носовые канюли не менее 5 л/мин в прон-позиции и
сохранении SpO2 не выше 92%
• рекомендуемые дозы – приказ МЗ РБ от 21.11.2020 №
1195
• В УЗ «Городская клиническая инфекционная
больница»: дексаметазон 6-8 мг в сутки парентерально
до 10 дней
Приказ МЗ РБ от 21.11.2020 № 1195
70.
Раннее назначение малых доз ГКС может быть полезнымдля предотвращения прогрессии COVID-19?
• ретроспективное исследование, США
• 213 пациентов со среднетяжелыми (необходимость в
неинвазивной респираторной поддержке) и тяжелыми
(необходимость в ИВЛ) формами COVID-19 (38% - группа
стандартного лечения, 62% - ГКС)
• раннее назначение метилпреднизолона 0,5-1,0 мг/кг/сут в 2
введения внутривенно
• длительность лечения - 3 дня для среднетяжелых и 7 дней для
тяжелых пациентов
• комбинированный первичный исход (необходимость перевода в
ОРИТ, в ИВЛ, смерть) фиксировался у 34,9% против 54,3%
(р=0,005) в группе ГКС и без, соответственно
• мультивариантный анализ: применение ГКС – независимый
предиктор снижения вероятности комбинированного первичного
исхода (кОШ 0,41, 95% ДИ 0,22-0,77)
Fadel R. et al. Clinical Infectious Diseases 2020
71.
Раннее назначение ГКС ассоциировано с лучшими клиническимиисходами у реанимационных пациентов с COVID-19
• проспективное мультицентровое обсервационное когортное
исследование пациентов в критическом состоянии с COVID19, Испания
• раннее (до или в первые 48 ч госпитализации в ОРИТ) vs
позднее (после 48 ч госпитализации в ОРИТ) vs отсутствие
назначения ГКС
• пациенты, рано получившие ГКС, имели меньшую летальность
в ОРИТ (30,3% vs 36,6% vs 44,2% для получивших, не
получивших, отсрочено получивших ГКС, соответственно) и
меньшую 7-дневную летальность (7,2% vs 15,2% для
получивших ГКС рано и получивших ГКС отсрочено или не
получивших вовсе)
• раннее назначение ГКС ассоциировано с меньшей
длительностью ИВЛ, пребывания в ОРИТ, меньшим числом
вторичных инфекций
Monedero P. et al. Crit Care 2021; 25:2
72.
Раннее назначение ГКС может пролонгировать выделениеSARS-CoV-2 у не реанимационных пациентов?
• проспективное мультицентровое рандомизированное клиническое
исследование, не реанимационные отделения, КНР
• 86 пациентов, госпитализированных с COVID-19
• метилпреднизолон 1 мг/кг/сут внутривенно vs плацебо, 7 дней
• разница в клиническом ухудшении в двух группах отсутствовала
(4,8% vs 4,8%, р=1,00)
• медиана длительности ПЦР детекции SARS-CoV-2 в респираторных
смывах была выше: 11 дней (квартили 6-16 дней) в группе ГКС vs 8
дней (квартили 2-12 дней) в группе плацебо (р=0,030)
• уровни CD3+ T-клеток, CD8+ Т-клеток, NK клеток в группе ГКС
были статистически значимо меньше (р< 0,05)
• раннее назначение ГКС может способствовать супрессии иммунной
системы человека и более длительному выделению SARS-CoV-2 из
дыхательных путей
Tang X. et al. Respiration 2020; doi 10.1159/000512063
73.
Раннее назначение ГКС не сопровождаетсяулучшением клинических исходов COVID-19!
обсервационное исследование, 1461 госпитализированный пациент с COVID-19, Италия
пациенты, получившие первую дозу ГКС после 72 ч госпитализации имели меньший риск
смерти, чем пациенты, получившие ГКС в первые 72 ч госпитализации (HR 0,67, 95% ДИ 0,670,90, p = 0,01)
у пациентов, получавших ГКС и требовавших вспомогательной респираторной поддержки
кислородом, риск неблагоприятного исхода был меньше в группе ИВЛ (HR 0,38, 95% ДИ 0,240,60), но не в группах пациентов на высокопоточном кислороде (HR 0,46, 95% ДИ 0,20-1,07) или
другой оксигенотерапии (HR 0,84, 95% ДИ 0,35-2,00)
Bahl A. et al. Internal and Emergency Medicine 2021
74.
Прогнозирование ответа на ГКС• 12.862 пациента с COVID-19,
получавших и не получавших ГКС,
ретроспективный анализ, КНР
• оценка соотношения нейтрофилов
к лимфоцитам на момент
госпитализации в стационар
• NLR > 6,11 ассоциировался с более
низкой летальностью в случае
назначения пациентам ГКС
• при NLR ≤ 6,11 или наличие СД 2
типа назначение ГКС не
сопровождалось снижением
летальности, однако приводило к
риску гипергликемии и развитию
инфекционных осложнений
(альтернативные стратегии
иммуномодуляции?)
Cai J. et al. Cell Metabolism 2021; 33:258
75.
Выводыамбулаторные пациенты, а также госпитализированные пациенты, не
требующие вспомогательной респираторной поддержки и имеющие
длительность заболевания до 7 дней, НЕ ДОЛЖНЫ получать ГКС
амбулаторные пациенты со снижением SpO2 < 94% нуждаются в
респираторной поддержке и должны быть госпитализированы
только при невозможности госпитализации, несмотря на развитие дыхательной
недостаточности, возможно использование дексаметазона амбулаторно под
тщательным контролем состояния пациента
при раннем назначении ГКС, в том числе у амбулаторных пациентов с
COVID-19, наблюдается отсутствие влияние или ухудшение клинических
исходов коронавирусной инфекции
согласно проведенным исследованиям у не реанимационных пациентов
рекомендуется использовать минимально эффективные дозы ГКС
исследование RECOVERY – дексаметазон 6 мг/сут
оценка прогноза назначения ГКС по соотношению нейтрофилы к
лимфоцитам (NLR)
отрицательная динамика состояния пациента с COVID-19 на фоне терапии
ГКС требует в большинстве случаев не увеличения дозы ГКС, а эскалации
патогенетической (иммуномодулирующей) терапии
76.
Какова роль антибиотиков при лечении COVID19?77.
Как часто встречается бактериальная коинфекция у пациентов с COVID-19?30 исследований, 3834
пациента
бактериальная ко-инфекция –
у 7% (95% ДИ 3-12%)
госпитализированных
пациентов:
–
–
14% в ОРИТ
4% в отделениях иных типов
встречаемость
бактериальной ко-инфекции
при COVID-19 меньше, чем
при пандемическом гриппе
– рутинное назначение АБ в
случае подтвержденной
COVID-19 инфекции не
показано!
78.
Какие патогены чаще встречались при бактериальной коинфекции у пациентов с COVID-19?Патогены, традиционно
вызывающие внебольничную
пневмонию!
79.
Внебольничные бактериальные ко-инфекции упациентов с COVID-19 (1)
• случайная выборка 1705 пациентов с COVID-19,
госпитализированных в 38 стационаров Мичигана с
13.03.2020 по 18.06.2020
• оценивалось назначение ранней (в первые 2 дня
госпитализации) эмпирической антибактериальной терапии и
внебольничной бактериальной ко-инфекции (позитивная
культура или тест в первые 3 дня госпитализации)
• только у 3,5% пациентов (59/1705) подтверждена
внебольничная бактериальная ко-инфекция
– 56,6% пациентов получали раннюю эмпирическую антибактериальную
терапию
– частота назначения ранней эмпирической антибактериальной терапии
между стационарами варьировала от 27% до 84%
Vaughn V. et al. Clinical Infectious Diseases 2020
80.
Внебольничные бактериальные ко-инфекции упациентов с COVID-19 (2)
• ретроспективная серия случаев
836 госпитализированных
пациентов с COVID-19,
Великобритания
• у 3,2% (27/836) подтверждена
ранняя бактериальная коинфекция (в первые 5 дней
госпитализации)
• частый внебольничный
возбудитель бактериальной коинфекции – S.aureus
Hughes S. et al. Clinical Microbiology and Infection 2020; 26:1395
81.
Внебольничные бактериальные ко-инфекции упациентов с COVID-19 (3)
• обсервационное когортное исследование 989 последовательно
госпитализированных в клинику Барселоны пациентов с
COVID-19
• внебольничная бактериальная ко-инфекция обнаружена у
3,1% (31/989) пациентов, преимущественно вызванная
S.pneumoniae и S.aureus
Hughes S. et al. Clinical Microbiology and Infection 2020; 26:1395
82.
Принципы использования антибиотиков приCOVID-19 инфекции
1. Эмпирическое назначение антибиотиков амбулаторным пациентам с
внебольничной пневмонией ТОЛЬКО при невозможности исключить ее
бактериальную этиологию (до получения результатов лабораторного
обследования на COVID-19)
2. Более 95% пациентов с подтвержденной COVID-19 пневмонией не
нуждаются в антибиотикам!!!
3. Прокальцитонин полезен в ограничении чрезмерного назначения
антибиотиков у пациентов с COVID-19-ассоциированной пневмонией
(НОРМАЛЬНЫЙ ПРОКАЛЬЦИТОНИН – НЕТ АНТИБИОТИКАМ! В
ОТДЕЛЕНИЯХ! И ДАЖЕ В РЕАНИМАЦИОННЫХ!)
4. Вероятно, что этиологически значимые бактериальные возбудители у
пациентов с COVID-19 и наслоением бактериальной пневмонии такие же,
как у пациентов с внебольничной бактериальной пневмонией без COVID-19
(= схожие принципы выбора антибиотиков)
5. Микробиологическое исследование крови и мокроты необходимо
выполнять у длительно госпитализированных пациентов с подозрением на
ИСМП, вызванные полирезистентными возбудителями
83.
•. 2020 Dec 21;8(1):ofaa578.•. 2020 Dec 21;8(1):ofaa578.
Большинству амбулаторных
пациентов с COVID-19
антибиотики НЕ показаны! И
особенно в первые дни болезни!
• сопутствующая бактериальная инфекция встречается только у
1,2-4% пациентов с COVID-19
Lansbury L. et al. Journal of Infection 2020; 81:266
Vaughn V. et al. Clinical Infectious Diseases 2020; doi: 10.1093/cid/ciaa1239
Hughes S. et al. Clinical Microbiology and Infection 2020; 26:1395
Karaba S. et al. Open Forum Infectious Diseases 2020; 8:ofaa578
• крайне редко присоединение бактериальной инфекции у
нетяжелых пациентов с COVID-19 приводит к быстрому
существенному ухудшению их состояния (= у врача есть
время оценить пациента в динамике, дообследовать и решить,
надо ли назначать антибиотик!)
84.
Варианты поствирусных бактериальныхпневмоний
Макроорганизм
SARS-CoV-2
Бактерия
Сочетанная вируснобактериальная пневмония
Тяжесть обусловлена комплексным
взаимодействие между вирусом,
бактериями и факторами
макроорганизма
Макроорганизм
SARS-CoV-2
Бактерия
Поствирусная бактериальная
пневмония
Тяжесть обусловлена вирусиндуцированными изменениями в
иммунной системе
макроорганизма, влияющими на
течение бактериальной инфекции
85.
Клинические отличия между разными формамибактериальных пневмоний на фоне COVID-19
• Сочетанная вирусно-бактериальная пневмония:
– неотличима клинически от первично-вирусных пневмоний;
– для уточнения этиологии важны системные маркеры
воспаления, специфичные для бактериальной инфекции
(прокальцитонин), микробиологические и молекулярногенетические методы
• Поствирусная бактериальная пневмония:
– может развиваться в фазу выздоровления после перенесенного
COVID-19
– часто двухволновое течение (первая волна – симптоматика
COVID-19, период афебриллитета и нормализации состояния,
вторая волна – классическая симптоматика бактериальной
пневмонии)
86.
Эмпирическая терапия бактериальных пневмоний упациентов с COVID-19 в амбулаторных условиях
Ключевые возбудители: S.pneumoniae, S.aureus, H.influenzae,
M.pneumoniae, C.pneumoniae
Бета-лактам:
амоксициллин/клавуланат
±
макролид (кларитромицин, азитромицин)
Альтернативные ЛС:
цефуроксим аксетил
левофлоксацин
Раздел 10.5, приказ МЗ РБ от 11.11.2020 № 1195
87.
Эмпирическая терапия бактериальной пневмонии угоспитализированных пациентов с COVID-19
Бета-лактам:
- ингибитор-защищенный бета-лактам:
пиперациллин / тазобактам (более высокая активность в
отношении энтеробактерий по сравнению с амоксициллин/ клавуланатом,
средство выбора при ТЯЖЕЛОЙ ПНЕВМОНИИ)
амоксициллин/клавуланат
- ЦС III-IV поколения
- эртапенем
+ кларитромицин / азитромицин
ИЛИ
+ левофлоксацин / моксифлоксацин
Ключевые возбудители: S.pneumoniae, S.aureus,
Enterobacteriaceae, атипичные возбудители
88.
В случае наличия односторонней пневмонии поданным Р-графии ОГК до получения результата
лабораторного обследования на COVID, надо ли
назначать антибиотик (при наличии клинических
симптомов респираторной инфекции)
89.
Принципы дифференциального диагноза между вирусной ибактериальной пневмонией в пандемию COVID-19
Вирусная пневмония
Бактериальная пневмония
Типичные симптомы COVID-19 в течение
примерно недели до развития пневмонии,
Отсутствие характерных симптомов для
COVID-19 до появления симптоматики
пневмонии
Постепенное (подострое) развитие симптомов Быстрое развитие симптомов пневмонии в
пневмонии
первые несколько дней заболевания
Выраженные мышечные боли (миалгии)
Быстрое развитие дыхательной
недостаточности уже в первые дни болезни
Потеря обоняния (аносмия)
Наличие гнойной мокроты
Наличие одышки без плевритических болей
Плевритические боли
В анамнезе – контакт с пациентом с
подтвержденным или предполагаемым
случаем COVID-19
Аускультативно отклонения с обеих сторон;
диссонанс между скудными физикальными
данными и тяжестью состояния
Односторонняя аускультативная
симптоматика
https://www.cebm.net/covid-19/differentiating-viral-from-bacterial-pneumonia/
90.
Согласно существующим практическим рекомендациямпо лечению пациентов с внебольничной пневмонией
при невозможности исключить ее бактериальный генез
показано назначение антибиотиков
При лабораторной верификации COVID-19, стабильном
состоянии пациента системная антибактериальная
терапия может быть прекращена (риск бактериальной
ко-инфекции не превышает 3-5%)
В случае сохраняющихся сомнений об отсутствии /
наличии бактериальной ко-инфекции может быть
полезным определение прокальцитонина сыворотки
крови
91.
Роль витамина Д в лечении пациентов с COVID1992.
Почему для пациентов с COVID-19 важеннормальный уровень витамина Д?
• витамин Д увеличивает уровень Treg лимфоцитов,
ограничивающих чрезмерное неспецифическое воспаление
при COVID-19
Fisher S. et al. PloS One 2019;14:e0222313
Prietl B. et al. Eur J Nutrition 2014;53:751
• витамин Д уменьшает продукцию провоспалительных
цитокинов (ИЛ-6, ФНОа) и увеличивает продукцию
противовоспалительных
Alhassan Mohammed H. et al. Scand J Immunol 2017;85:386
• показана ассоциация между сниженным уровнем витамина Д
и повышенным риском тромботических осложнений (часто
встречаются при COVID-19)
Mohammad S. et al. Biomolecules 2019;9:649
• дефицит витамина Д часто встречается при сахарном диабете
и ожирении – известных факторах риска тяжелого и
осложненного течения COVID-19
Weir K. et al. Clin Med (Lond) 2020; 20:e107
93.
Уровень витамина Д часто снижен у пациентовреанимационных отделений
Amrein K. et al. Endocrine Connections 2018; 7: R304
94.
Витамин Д какиммуномодулятор
• Витамин Д обладает
двойным действием на
иммунный ответ и
воспаление
• Путем модуляции
экспрессии различных
генов усиливается
врожденный и
снижается
приобретенный
иммунный ответ, что
позволяет избежать
чрезмерного воспаления
при COVID-19
Perez E. et al. J Allergy Clin Immunol 2017; 139:S1
95.
Механизмы реализации иммуномодулирующейфункции витамина Д на врожденный и
приобретенный иммунитет
Xu Y. et al. J Transl Med 2020; 18:322
96.
Витамин Д используется для лечения целого рядазаболеваний человека
Низкий уровень витамина Д влияет на патогенез ряда заболеваний: аутоиммунных
(типа СКВ), синдрома высвобождения цитокинов, соматосенсорного дефицита,
остеопороза, инфекций (грипп, лихорадка Денге и т.д.).
Витамин Д необходим для поддержания оптимального баланса в иммунной системе и
профилактики аутоиммунных заболеваний.
Xu Y. et al. J Transl Med 2020; 18:322
97.
Влияет ли уровень витамина Д в сыворотке крови натяжесть COVID-19?
• исследование случай-контроль, КНР
• оценка уровня 25-гидроксивитамина Д (25(ОН)D) у 80 здоровых
лиц и 62 пациентов, диагностированных с COVID-19
• уровень 25(ОH)D был значительно ниже в группе пациентов с
COVID-19 по сравнению с группой здоровых лиц
• уровень 25(ОH)D был наименьшим в группе тяжелых и
реанимационных пациентов с COVID-19 по сравнению с с
пациентами с нетяжелым течением COVID-19
• дефицит витамина Д обнаружен у 41,9% пациентов с COVID-19
и только у 11,1% здоровых лиц
• дефицит витамина Д у тяжелых и реанимационных пациентов
достигал 80% по сравнению со 36% у пациентов с нетяжелым
течением инфекции
• уровень 25(OH)D 41,19 нмоль/л выявлен как протективный в
Ye K. et al. Journal of the American College of Nutrition 2020
отношении COVID-19
98.
Влияет ли уровень витамина Д в сыворотке крови натяжесть COVID-19?
Уровень витамина Д статистически значимо различался между
группой здорового контроля и случаями инфицирования COVID19, а также в группах легкой / среднетяжелой и тяжелой /
критической форм COVID-19
Ye K. et al. Journal of the American College of Nutrition 2020
99.
Сниженный уровень витамина Д может влиятьна тяжесть течения COVID-19, в том числе у
молодых пациентов
• ретроспективное когортное исследование, Испания
• 80 последовательных госпитализированных пациентов с
подтвержденной COVID-19
• оценка влияния дефицита витамина Д (< 20 нг/мл) на
риск неблагоприятных исходов инфекции
• показана тенденция связи между дефицитом витамина Д
и повышенным риском развития тяжелой формы
COVID-19 (OR 3,2, 95% ДИ 0,9-11,4, р=0,07)
• мужской пол был ассоциирован с дефицитом витамина
Д и тяжелым течением COVID-19 в молодом возрасте
Macaya F. et al. Nutr Hosp 2020; 37:1039
100.
Молодые мужчины с дефицитом витамина Дразвивали тяжелую форму COVID-19
Macaya F. et al. Nutr Hosp 2020; 37:1039
101.
Дефицит витамина Д утяжеляет COVID-19• систематический обзор и мета-анализ 27 исследований
• критерий включения: обсервационные исследования, в
которых измерялся уровень витамина Д у взрослых пациентов
с COVID-19
• дефицит витамина Д не ассоциировался с более высоким
шансом инфицирования COVID-19 (ОШ 1,35, 95% ДИ 0,80–
1,88)
• тяжелые случаи COVID-19 на 64% чаще встречались у
пациентов с дефицитом витамина Д (ОШ 1,64, 95% ДИ 1,30–
2,09) по сравнению со среднетяжелыми случаями
• недостаточность витамина Д увеличивало шанс
госпитализации (ОШ 1,81, 95% ДИ 1,41–2,21) и
неблагоприятного исхода от COVID-19 (ОШ 1,82, 95% ДИ
1,06-2,58)
102.
Рекомендуемые режимы дозирования витамина Ду пациентов с COVID-19: протокол EVMS
• Профилактика инфицирования COVID-19:
– витамин Д3 1000-3000 МЕ/сут (RDA - Recommended Daily
Allowance - 800-1000 МЕ/сут, безопасная верхняя граница
ежедневно - < 4000 МЕ/сут)
• Амбулаторные пациенты с симптомами COVID-19:
– витамин D3 2000-4000 МЕ/сут
• Стационарные пациенты с COVID-19 вне ОРИТ
(среднетяжелая форма инфекции) и в ОРИТ (тяжелая
форма инфекции, пациенты в критическом состоянии):
– витамин D3 20.000-60.000 МЕ вся доза однократно перорально.
Впоследствии повторять прием 20.000 МЕ каждые 7 дней до
выписки из стационара
103.
Какова роль пробиотиков при ведении пациентовс коронавирусной инфекцией?
104.
Пробиотики - живые микроорганизмы, которыепри введении в необходимом количестве,
оказывают положительный эффект на здоровье
хозяина
Консенсусное определение Международной Научной
Ассоциации Пробиотиков и Пребиотиков, 2014
Bifidobacterium spp.
B.bifidum
B. infantum
B. longum
B. thermophilum
B. lactis
Грамотрицательные бациллы
Escherichia coli Nissle (1917)
Грамположительные бациллы
Bacillus clausii
Дрожжеподобные грибки
Saccharomyces boulardii
Lactobacillus spp.
L. rhamnosus
L. casei
L. reuteri
L. acidophilus
L. plantarum
......
Грамположительные кокки
Streptococcus thermophilus
Enterococcus faecium
Streptococcus intermedieus
.........
105.
Нарушение микробиоты (дисбиоз) может влиятьна течение COVID-19 инфекции
• Изучение изменений кишечной микробиоты у госпитализированных
пациентов с COVID-19, оценка потенциальной ассоциации между составом
кишечной микробиоты и тяжестью течения заболевания, длительностью
выделения SARS-CoV-2 из ЖКТ
• Секвенирование образцов фекалий, полученных от 15 пациентов с COVID19, в течение госпитализации
• Пациенты с COVID-19 имели существенные изменения микробиоты с
уменьшением количества полезных комменсалов и увеличением числа
оппортунистических патогенов
• Дисбиоз сохранялся даже после полной элиминации SARS-CoV-2 и
клинического выздоровления пациентов
• Показана ассоциация между наличием определенных микроорганизмов в
составе кишечной микробиоты и тяжестью течения COVID-19, а также
длительностью выделения SARS-CoV-2 из ЖКТ
Zuo T. et al. Gastroenterology 2020; 159:944
106.
Превалирование определенных микроорганизмов кишечноймикробиоты у пациентов с COVID-19, по сравнению с группой
контроля (здоровые лица)
Gu S. et al. Clinical Infectious Disease 2020
107.
Что происходит с микробиотой ЖКТ при назначенииантибиотиков и других неблагоприятных воздействиях?
Влияние АБТ на микробное сообщество в толстой кишке.
После начала АБТ увеличивается количество резистентных МО и
существенно уменьшается видовое разнообразие микробиоты ЖКТ. Для
части резистентных бактерий характерна длительная персистенция.
Jernberg et al. Microbiology 2010; 156:3216
108.
Пробиотики существенно уменьшают риск диарей на фонеприема антибиотиков!
Назначение пробиотиков статистически
значимо уменьшает риск развития
антибиотик-ассоциированных диарей на
44% и КДАИ на 71%
Назначение пробиотиков значимо уменьшало
частоту антибиотик-ассоциированных
диарей на 42% (ОР 0,58, 95% ДИ 0,500,68, p<0,001; I2 54%; NNT 13,0, 95% ДИ
10,3-19,1)
Прием пробиотиков вместе с антибиотиками
у госпитализированных пациентов
существенно уменьшает риск развития ААД
(ОР 0,61, 95% ДИ 0,47-0,49) и КДАИ (ОР 0,37,
95% ДИ 0,22-0,61)
Пробиотики статистически значимо
уменьшают риск ААД во внебольничных
условиях (ОР 0,49, 95% ДИ 0,36-0,66)
109.
Систематический обзор и мета-анализ 90 генов, описанных влитературе, на экспрессию которых могут влиять пробиотики и
которые могут оказывать влияние на течение COVID-19
Применение пробиотиков может оказывать эффект на АПФ-2-опосредованное
проникновение SARS-CoV-2 в клетки, активацию системного иммунного ответа,
NLRP-опосредованные иммуномодуляторные пути, миграцию клеток иммунной
системы в дыхательную и сердечно-сосудистую системы с их последующим
повреждением, нарушение метаболизма липидов и глюкозы
Вывод авторов: пробиотики могут использоваться как
дополнительные средства в комплексной профилактике и терапии
COVID-19 инфекции
110.
Пробиотикиснижают риск
развития
острых
респираторных
инфекций
111.
Пробиотики: ключевые позициинормальная микробиота является барьером для инфицирования
многими патогенами, а также может уменьшать тяжесть
развившейся инфекции
предпочтительны пробиотические микроорганизмы, устойчивые
к обычно назначаемым антибиотикам, что позволяет
использовать их параллельно с курсом системной
антибактериальной терапии
периодический прием пробиотиков курсами от 2 недель
практически всегда полезен (даже при отсутствии явных
признаков дисбиоза)
по данным многочисленных исследований пробиотики не имеют
побочных эффектов при их правильном использовании
пробиотики необходимы всем пациентам, которым назначены
антибиотики, для уменьшения рисков антибиотикассоциированной диареи, кандидоза слизистых и профилактики
дисбиоза
112.
Играет ли роль ацетилцистеин и другиемуколитики в лечении COVID-19?
113.
Потенциально полезные эффекты N-ацетилцистеина• муколитический эффект (свободные сульфгидрильные группы разрывают
внутри- и межмолекулярные дисульфидные связи кислых мукополисахаридов
мокроты)
• замещение запасов глутатиона и нормализация окислительновосстановительного баланса в клетках, испытывающих
оксидативный стресс
– N-ацетилцистеин – предшественник цистеина, необходимого для синтеза
глутатиона
– блокирование оксидативного стресса, индуцируемого вирусом, уменьшает
гибель пораженных клеток
• увеличение пролиферативного ответа Т-лимфоцитов
• ингибирование NLRP3 инфламмасомного пути (ИЛ1b, ИЛ18)
• уменьшение концентрации ФНОа
– ограничивает провоспалительный иммунный ответ, в том
числе может блокировать длительное воспаление,
потенциально способствующее развитию фиброза легких
Poe F. & Corn J. Medical Hypothesis 2020; 143
после острого заболевания
Rangel-Mendez J.-A. & Moo-Puc R.-E. Future Microbiology 2020
114.
Предложенная эмпирически стратегия использованияN-ацетилцистеина у пациентов с COVID-19 (экстраполяция
данных in vitro, экспериментов на животных и клинических исследований
пациентов с ОРДС преимущественно не ковидной этиологии)
А есть ли данные клинических
исследований эффективности
N-ацетилцистеина у пациентов
с COVID-19?
Заявлены 6 клинических
исследований:
- 4 из них не начали набора
пациентов
- 1 – применение АЦЦ вместе
с метиленовым синим и
витамином С (трудность
интерпретации результатов)
- 1 – окончится к маю 2021 г.
Shi Z. & Puyo C. Ther Clin Risk Manag 2020; 16:1047
115.
Оценка эффективности N-ацетилцистеина упациентов с COVID-19 ассоциированным ОРДС
• двойное слепое рандомизированное плацебоконтролируемое исследование
• 135 пациентов с тяжелой COVID-19 инфекцией,
требующие неинвазивной респираторной поддержки
• N-ацетилцистеин 21 г (примерно 300 мг/кг) в течение 20
часов против 5% глюкозы
• частота перевода на ИВЛ 23,9% в группе плацебо vs
20,6% в группе N-ацетилцистеина (p=0,675)
• не обнаружено различий в двух группах по вторичным
точкам исхода (длительность ИВЛ, поступление и
длительность лечения в ОРИТ, летальность)
de Alencar J. Clin Infect Dis 2020; ciaa1443
116.
COVID-19 и другие муколитики• дискутируется роль бромгексина и его метаболита
амброксола как лекарственных средств, потенциально
ингибирующих репликацию SARS-CoV-2 и его связь
с рецептурными структурами клеток человека
• большинство опубликованных исследований
выполнены in vitro (на культурах клеток)
• убедительных клинических исследований
эффективности применения амброксола и
бромгексина для улучшения исходов COVID-19 в
настоящее время не опубликовано
Depfenhart M. et al. Internal and Emergency Medicine 2020
117.
Как правильно помочь длительно лихорадящемупациенту с COVID-19?
118.
Принципы контроля лихорадки при COVID-19лихорадка при COVID-19 на фебрильных значениях может длиться от
нескольких дней (чаще) до 1-2 недель (реже)
длительная лихорадка опасна дегидратацией, декомпенсацией
сопутствующей патологии, ухудшением функции ряда систем
(особенно респираторной и сердечно-сосудистой)
рекомендуется снижать температуру выше 38,5 С
возможно снижение температуры на более низких значениях, если
отмечается ее плохая переносимость, существенно сказывающаяся на
состоянии пациента
для купирования лихорадки чаще всего используют парацетамол или
содержащие его растворимые комбинированные лекарственные
средства (в порошках) и ибупрофен при каждом подъеме температуры
если лихорадка сохраняется длительно и на высоких цифрах возможно
назначение данных препаратов через равные интервалы времени вне
зависимости от наличия или отсутствия подъема температуры на
момент приема
119.
Что рекомендовать пациенту при лихорадке?• свободная удобная одежда
• равномерное потребление адекватного количества жидкости
– мочеиспускание у пациента должно быть примерно каждые 6 часов (цвет мочи
преимущественно бледно-желтый)
• поддерживать в палате комфортную температуру, по возможности,
регулярно проветривать помещение
• сообщить медперсоналу, если:
– имеется сильная жажда и снижение объема мочи, несмотря на
адекватное потребление жидкости
– появилась выраженные головокружение или слабость («не могу встать
сам с постели» – часто признак прогрессирующей гипоксемии)
– на фоне адекватной гидратации появились мышечные боли
чрезмерной интенсивности (рабдомиолиз?)
Минимальная суточная потребность в жидкости у здорового человека – 2030 мл/кг идеальной массы тела. На каждый градус повышения температуры
свыше 37 С следует добавлять 10 мл/кг идеальной массы тела жидкости
NHS Inform. Coronavirus (COVID-19): Self-care advice. https://www.nhsinform.scot/illnesses-and-conditions/infections-andpoisoning/coronavirus-covid-19/caring-for-a-cough-or-fever/coronavirus-covid-19-self-care-advice
120.
Интенсивная терапия у пациентов с тяжелойформой COVID-19: что является наиболее
значимым?
121.
Наиболее значимые компоненты интенсивной терапиипациентов с COVID-19
этапная респираторная поддержка (кислород интраназально / через
лицевую маску / через лицевую маску с резервуаром / неинвазивная
ИВЛ / инвазивная ИВЛ) и прон-позиция
купирование лихорадки
адекватная инфузионная терапия и профилактика дегидратации
(раздел 11.4, приказ МЗ РБ № 1195)
профилактика тромбоэмболических осложнений
(низкомолекулярный или не фракционированный гепарин)
глюкокортикостероиды и другие средства этиопатогенетической
терапии (ремдесивир, плазма реконвалесцентов, внутривенный
нормальный иммуноглобулин человека, тоцилизумаб и т.д.)
профилактика трофических нарушений, адекватная нутритивная
поддержка и профилактика делирия
раннее выявление прогрессирования / осложнений заболевания и их
коррекция (C.difficile, бактериальная пневмония, связанная с
оказанием медицинской помощи, аспергиллез и т.д.)
122.
Выжимка рекомендаций Surviving Sepsis Campaign поCOVID-19 (29/01/2021)
https://www.sccm.org/getattachment/SurvivingSepsisCampaign/Guidelines/COVID-19/SSC-COVID19-Infographic-Therapeutic-Update.pdf?lang=en-US
123.
Выжимка рекомендаций Surviving Sepsis Campaign поCOVID-19 (29/01/2021)
https://www.sccm.org/getattachment/SurvivingSepsisCampaign/Guidelines/COVID-19/SSC-COVID19-Infographic-Initial-Management-of-Hypoxic-COVID-19Patients.pdf?lang=en-US
124.
Выжимка рекомендаций Surviving Sepsis Campaign поCOVID-19 (29/01/2021)
https://www.sccm.org/getattachment/SurvivingSepsisCampaign/Guidelines/COVID-19/SSC-COVID19-Infographic-Management-of-Patients-with-COVID-19-andARDS.pdf?lang=en-US
125.
Каким именно пациентам с COVID-19 и в какихслучаях следует назначать ривароксабан?
126.
Точки приложения пероральныхантикоагулянтов
Predazzi I. et al. American Journal of Cardiovascular Drugs 2013; 13:79
127.
Роль ривароксабана при ведении амбулаторныхпациентов с COVID-19
• согласно большинству опубликованных рекомендаций, нет
убедительных данных, чтобы рекомендовать назначение
ривароксабана всем пациентам с COVID-19, которые не нуждаются
в госпитализации и не имеют дополнительных показаний для
данной группы ЛС
• профилактика венозных тромбозов ПОСЛЕ ВЫПИСКИ ИЗ
СТАЦИОНАРА не рекомендуется для пациентов c COVID-19, за
исключением группы риска по данному осложнению (AIII)
• FDA одобрило ривароксабан 10 мг ежедневно в течение 31-39 дней
у пациентов с COVID-19, имеющих факторы риска венозных
тромбоэмболических осложнений
• любое решение о назначении пероральной антикоагулятной терапии
после выписки из стационара должно приниматься на
индивидуальной основе с учетом факторов риска для конкретного
пациента
NIH COVID-19 Treatment Guidelines https://www.covid19treatmentguidelines.nih.gov/antithrombotic-therapy/
128.
Как оценить факторы риска венозныхтромбоэмболических осложнений?
Модифицированная шкала IMPROVE для оценки риска ВТЭ у пациентов не
хирургического профиля
Фактор риска
Баллы
ВТЭ в анамнезе
3
Тромбофилия (врожденная или приобретенная)
2
Паралич нижних конечностей
2
Злокачественное новообразование (в настоящее время или в
течение последних 5 лет)
2
Госпитализация в ОРИТ / отделение неотложной кардиологии
1
Возраст > 60 лет
1
• Показания для назначения профилактики ВТЭ после выписки
из стационара пациентов с COVID-19:
– балл по модифицированной шкале IMPROVE ≥ 4 или
– балл по модифицированной шкале IMPROVE ≥ 2 и уровень Д-димеров > 2
верхних границ нормы
https://www.covid19treatmentguidelines.nih.gov/antithrombotic-therapy/
129.
Большинство профессиональных медицинских сообществрекомендуют профилактику ВТЭ у выписанных из стационара
пациентов с COVID-19 только при наличии факторов риска
тромбоэмболических осложнений
Berkman S. Postgraduate Medicine 2021
130.
Исходы COVID -19 инфекции: чего ожидать увыписанных из стационара пациентов?
131.
Последствия перенесенной COVID-19• в соответствии с ВОЗ время выздоровления после легких форм
COVID-19 составляет около 2 недель, для среднетяжелых и
тяжелых – от 3 до 6 недель, однако оно может варьировать в
зависимости от возраста и предшествующей сопутствующей
патологии:
– 350 пациентов с COVID-19 в США, только 39% госпитализированных
вернулись к базовому уровню здоровья через 14-21 день от даты
постановки диагноза
– 143 пациента с COVID-19, госпитализированных в Италии (7 из них
были на ИВЛ):
• только у 13% отсутствовали какие-либо симптомы через 60 дней от
начала заболевания
• наиболее часто сохранялась слабость (53%), диспноэ (43%), боли в
суставах (27%), боли в грудной клетке (22%)
https://www.uptodate.com/contents/coronavirus-disease-2019-covid-19-clinical-features
132.
Условные стадии выздоровления после COVID-19• острая COVID-19 инфекция (acute COVID-19) – симптомы
COVID-19 инфекции, длящиеся до 4 недель с момента начала
заболевания
• продолжающаяся симптомная COVID-19 инфекция (ongoing
symptomatic COVID-19) – симптомы COVID-19, длящиеся от 4
до 12 недель с момента начала заболевания
• постковид (post-COVID-19, синонимы - “long-COVID,” “longterm COVID,” “post-acute COVID-19,” “chronic COVID-19”) –
симптомы, развивающиеся во время или после COVID-19,
продолжающиеся 12 недель и более и не объяснимые
альтернативным диагнозом
https://www.uptodate.com/contents/coronavirus-disease-2019-covid-19-evaluation-and-management-of-adults-following-acute-viralillness?search=long%20covid&source=machineLearning&graphicRef=130356#graphicRef130356
133.
Типы, удельный вес и длительностьперсистирующих симптомов после COVID-19
Meini S. et al. Eur Arch Otorhinolaryngol 2020; 277:3519
Halpin S. et al. J Med Virol 2020
Bowles K. et al. Ann Intern Med 2020
Wong A. et al. Eur Respir J 2020; 56
Nehme M. et al. Ann Intern Med 2020
Taquet M. et al. Lancet Psychiatry 2020
Carfì A. et al. JAMA 2020; 324:603
Xiong Q. et al. Clin Microbiol Infect 2020
Goërtz Y. et al. ERJ Open Res 2020; 6
Hopkins C. et al. J Otolaryngol Head Neck Surg 2020; 49:26
Kosugi E. et al. Braz J Otorhinolaryngol 2020; 86:490
Cho R. et al. Laryngoscope 2020; 130:2680
https://www.uptodate.com/contents/coronavirus-disease-2019-covid-19-evaluation-and-management-of-adults-following-acute-viralillness?search=long%20covid&source=machineLearning&graphicRef=130356#graphicRef130356
134.
У пациентов, перенесших COVID-19, могутсохраняться нейропсихиатрические отклонения на
момент выписки из стационара
• обсервационное исследование 58 пациентов с COVID-19,
госпитализированных во Франции:
• 3/58 пациентов – субклинический ишемический инсульт
(выявлен только по результатам МРТ головного мозга)
• 67% (39/58) пациентов – признаки диффузного поражения
кортикоспинальных трактов (усиленные сухожильные и
периостальные рефлексы, клонус стоп, двухсторонний симптом
Бабинского)
• 36% (14/39) пациентов на момент выписки имели
дизэкзекутивный синдром (нарушение функции планирования
целенаправленной деятельности, согласованности действий,
невнимательность, дезориентация, отсутствие гибкости в мышлении,
мнестические нарушения; связан с поражением дорсолатеральных отделов
лобных долей)
Helms J. et al. N Engl J Med 2020; 382: 2268
Ardila A. et al. Diabetes Metab Syndr 2020; 14:1377
135.
Комплекс факторов, способствующих длительномунейрокогнитивному дефициту после перенесенной COVID-19
Baker A. et al. British Journal of Anaesthesia 2021; 126:44
136.
Влияние перенесенного делирия напоследующее качество жизни пациента
Множество преморбидных факторов и факторов, воздействующих на
пациента в стационаре, предрасполагают к развитию делирия во время
острого заболевания. Следствием может быть прогрессирующие когнитивные
нарушения, депрессия и посттравматическое стрессовое расстройство,
нарушение соматического статуса, что приводит в итоге к существенному
ухудшению качества жизни по сравнению с исходным уровнем
Wilson J. et al. Nature Reviews Disease Primers 2020; 6:90
137.
Отдаленные последствия для ЦНС после перенесеннойCOVID-19
ФДГ-ПЭТ головного мозга для оценки метаболизма у двух пациентов с перенесенной
COVID-19 (через 8 недель и 7 дней от первых симптомов инфекции) и сопоставление
результатов со здоровыми субъектами
у двух пациентов обнаружен гипометаболизм в зоне обонятельной / прямой извилины ГМ
(особенно выраженный у пациента с аносмией в течение 4 недель и сохраняющимися
нарушениями памяти)
у одного пациента с сохраняющимися жалобами на боли в конечностях без объективно
определяемых чувствительных и двигательных нарушений обнаружен также гипометаболизм
в зоне амигдалы, гиппокампа, парагиппокампа, поясной извилины, пре- и постцентральной
извилины, таламуса / гипоталамуса, мозжечка, моста и продолговатого мозга
Guedj E. et al. European Journal of Nuclear Medicine and Molecular Imaging 2020
138.
Дизосмия при COVID-19: есть и хорошие новости!• многоцентровое исследование, 18 стационаров Европы, 1363
пациента с COVID-19
• оценка распространенности дизосмии и ее разрешения
• дизосмии значительно чаще регистрировалась у пациентов с легкими
формами заболевания (85,9%) по сравнению с пациентами со
среднетяжелыми и тяжелыми формами (4,5 - 6,9%, р=0,001)
• 24,1% (328/1363) не восстановили обоняние через 60 дней от начала
COVID-19
• средняя длительность сообщаемой пациентами дизосмии составила
21,6±17,9 дня
• через 6 месяцев только у 4,7% пациентов отмечались объективные
признаки аносмии / гипоосмии
• большая выраженность дизосмии в начале заболевания была строго
ассоциирована с длительно сохраняющейся дизосмией (р< 0,001).
• вывод: дизосмия разрешается у 95% пациентов в течение 6 месяцев
Lechien J. et al. Journal of Internal Medicine 2021
139.
Мультисистемный воспалительный синдром,ассоциированный с COVID-19, у взрослых (MIS-A)
• серия случаев из Великобритании и США, 27 взрослых пациента, мартавгуст 2020 г.
• только ~ ½ пациентов имели респираторную симптоматику из-за SARS-CoV2 в предшествующие 2-5 недель
• наиболее частые симптомы: лихорадка, боль в грудной клетке, сердцебиение,
диарея, абдоминальные боли, рвота, сыпь
• практически у всех пациентов – патологические отклонения на ЭКГ (аритмии
и др.), повышение уровня тропонина, ЭхоКГ признаки дисфункции левых
или правых отделов сердца
• у всех пациентов отмечались повышенные маркеры воспаления,
гиперкоагуляция и лимфопения
• подтверждение ассоциации с COVID-19 у 1/3 пациентов было возможно
только серологически
• в пандемию COVID-19 необходима настороженность в отношении
потенциальных случаев MIS-A, в том числе использование для верификации
перенесенной коронавирусной инфекции серологических методов
диагностики
Morris S. et al. MMWR 2020; 69:1450
140.
Может ли SARS-CoV-2 выступать триггером длядебюта аутоиммунных, дегенеративных,
онкологических заболеваний?
141.
COVID-19 может быть триггеромаутоиммунных заболеваний!
• После перенесенной COVID-19 инфекции имеются описания развития у
пациентов следующих состояний:
системной красной волчанки
аутоиммунной гемолитической анемии
аутоиммунной тромбоцитопении
синдрома Гийена-Барре
васкулита
рассеянного склероза
иммуновоспалительных заболеваний, включая болезнь
Кавасаки у детей
• Часть длительно сохраняющихся после COVID-19 симптомов в своей
основе также могут быть обусловлены аутоиммунитетом (слабость, боли в
суставах, миалгии, экзантемы и т.д.)
• Описано обнаружение и длительное сохранение у пациентов с COVID-19
антифосфолипидных антител, отложение иммунных комплексов,
потребление компонентов системы комплемента, антинуклеарные и антиДНК антитела
Canas C. et al. Medical Hypothesis 2020; 145:110345
142.
Возможные механизмы, запускающие аутоиммунныезаболевания у пациентов с COVID-19
SARS-CoV-2 может быть
триггером
аутоиммунитета,
связанного с состоянием
транзиторного
нарушения функции
врожденного и
приобретенного
иммунитета, при котором
иммунная система не
способна правильно
распознавать
аутоантигены.
В последующем
восстановление функции
иммунной системы
может усиливать
аномальный иммунный
ответ в фазе
реконвалесценции после
COVID-19
Canas C. et al. Medical Hypothesis 2020; 145:110345
143.
Детекция аутоантител у пациентов с COVID-19• 40 взрослых пациентов, ранее не имевших аутоиммунных
заболеваний, и 40 здоровых пациентов (группа контроля)
• оценка наличия ключевых аутоантител
• появление аутоантител de novo коррелировало с более худшим
течением и исходами COVID-19
Sacchi M. et al. Clin Transl Sci 2021
144.
COVID-19 поражает головной мозг по целому ряду механизмов:возможные триггеры нейродегенеративных заболеваний ЦНС
Verkhratsky A. et al. Biology Direct 2020; 15:28
145.
COVID-19 может способствовать конверсии«спящих» раковых клеток в активные
Реактивация «спящих» раковых клеток, их пролиферация и диссеминация может
приводить к рецидиву опухоли, ее ускоренному росту и метастазированию
Francescangeli F. et al. Front Oncol 2020; doi 10.3389/fonc.2020.592891
146.
Что мы знаем об иммунитете после перенесеннойинфекции?
Как часты повторные заражения COVID-19?
147.
Особенности иммунитета после перенесенной COVID-19• формируется практически у всех пациентов (за
исключением имеющих выраженные нарушения
функции иммунной системы из-за других заболеваний)
• имеет 2 ключевых звена:
1. гуморальное – вирус-нейтрализующие антитела,
антитела к различным антигенам вируса и В-клетки
памяти
- количество антител (титр) может постепенно снижаться,
однако их защитные свойства сохраняются обычно не менее
3-4 месяцев, по некоторым данным до 6-8 месяцев
2. клеточное - Т-клетки иммунной системы
- длительность сохранения клеточного иммунного ответа
пока неизвестна
UpToDate 2020 (Coronavirus disease 2019: Epidemiology, virology, and prevention)
148.
Как и когда появляется иммунитет послеперенесенной COVID-19 инфекции?
Иммуноглобулины
класса G
Иммуноглобулины
класса M
Sethuraman N. et al. JAMA 2020
149.
Рекомендации по серодиагностике лиц с подозрением на COVID19 Американского общества инфекционных болезней1. Не рекомендуется выполнять серологическое обследование на COVID19 в течение первых 2 недель от начала клинической симптоматики
2. Для ретроспективного подтверждения диагноза COVID-19
рекомендуется тестировать пациента на SARS-CoV-2 IgG или
суммарные антитела через 3-4 недели от начала клинической
симптоматики
3. Нет рекомендаций за или против тестирования на SARS-CoV-2 IgM
для ретроспективной диагностики COVID-19 инфекции
4. Не рекомендуется тестировать на SARS-CoV-2 IgA для
ретроспективной диагностики COVID-19 инфекции
5. Рекомендуется использовать IgG для подтверждения коронавирусной
инфекции у пациента с клинической симптоматикой, очень
подозрительной на COVID-19, но с повторно отрицательными
результатами ПЦР
https://www.idsociety.org/practice-guideline/covid-19-guideline-serology/
150.
Пациенты,переболевшие COVID19 в более тяжелой
форме, развивают более
выраженный и стойкий
иммунный ответ?
серийное определение IgM, IgG к
SARS-CoV-2 у реанимационных и
не реанимационных пациентов c
COVID-19
медиана сероконверсии IgM и IgG
8 и 10 дней, соответственно
антительный ответ гораздо более
выражен у реанимационных
пациентов по сравнению с
пациентами с более легкими
случаями заболевания
Lynch K. et al. Clinical Infectious Diseases 2021; 72
151.
Как часто встречаются повторные зараженияпри COVID-19?
• из 1038 медицинских
работников,
инфицированных
SARS-CoV-2 во
время первой волны
пандемии, ни один не
заболел повторно во
вторую волну
• иммунитет к
реинфекции длится
по меньшей мере 6
месяцев
• повторные заражения
COVID-19 могут
быть очень редки
Hanrath A. et al. Journal of Infection 2020; doi 10.1016/j.jinf.2020.12.023
152.
Как протекают повторные случаи COVID-19?• в литературе опубликован 31 подтвержденный случай реинфекции
COVID-19
• большинство повторных случаев COVID-19 протекали легче или
также, как и первичный эпизод инфекции
• неблагоприятный исход зафиксирован в двух случаях повторного
инфицирования SARS-CoV-2
• пациенты с более легким течением первого эпизода COVID-19
предрасположены к повторному инфицированию (ограниченная
эффективность выработки антител и Т-клеточного иммунитета)
• отличить реинфекцию от реактивации ранее существовавшей в
организме COVID-19 инфекции позволяют только методы
секвенирования возбудителей для каждого из эпизодов инфекции
• неясно, обладают ли мутантные штаммы SARS-CoV-2 (например,
британский вариант B.117) вызывать большую частоту повторных
случаев заболевания
Stokel-Walker C. et al. BMJ 2021; 372
153.
Профилактика инфицирования COVID-19: что унас есть на сегодня с позиций доказательной
медицины?
154.
Вакцины против COVID-19: однозначно да!Инактивированный
или ослабленный
SARS-CoV-2
Вирусный вектор,
экспрессирующий
спайковый S-протеин
SARS-CoV-2
SARS-CoV-2
S/S1RBD протеин +
адъювант
ДНК или РНК,
кодирующая
спайковый S-протеин
SARS-CoV-2
Вакцины,
использующие
данную
стратегию
Sinopharm,
Sinovac, ICMRBharat Biotech
GanSino,
Gamaleya, J&J,
AstraZeneca,
Vaxart, Merck,
Novartis
Novavax, Sanofi,
Chinese Academy
of Medical
Science (RBD)
Pfizer, Moderna,
CureVac,
Arcturus, Inovio,
Chulalongkorn U
Оценка
эффективности
вакцинации
Anti-S или antiN IgG
Anti-S IgG
Anti-S IgG (anti- Anti-S IgG
spike RBD IgG
требуется только
для RBD
вакцин)
Другие
одобренные
вакцины,
использующие
данный подход
Против кори,
эпидемического
паротита,
краснухи,
полиомиелита,
гриппа,
брюшного тифа
Против болезни
Эбола,
бешенства (для
использования в
ветеринарии)
Против гепатита
В, вируса
папилломы
человека,
столбняка и др.
В настоящее
время другие
одобренные
аналогичные
вакцины
отсутствуют
155.
Постэкспозиционная профилактика с помощьюмоноклональных антител к SARS-CoV-2: возможно да!
• бамланивимаб, касиривимаб-имдевимаб (анти-спайковые
моноклональные антитела)
• пресс-релизы результатов плацебо-контролируемых РКИ:
моноклональные антитела уменьшают частоту симптомной
COVID-19 среди резидентов домов-интернатов и
медицинского персонала, а также среди домашних контактов
заболевших лиц
• в настоящее время ожидается публикация окончательных
результатов исследований, а также изучение моноклональных
антител как средств для возможной предэкспозиционной
профилактики COVID-19
https://www.nih.gov/news-events/news-releases/clinical-trials-monoclonal-antibodies-prevent-covid-19-nowenrolling (Accessed on August 13, 2020)
https://investor.lilly.com/news-releases/news-release-details/lillys-neutralizing-antibody-bamlanivimab-ly-cov555prevented (Accessed on January 24, 2021)
https://www.prnewswire.com/news-releases/regeneron-reports-positive-interim-data-with-regen-cov-antibodycocktail-used-as-passive-vaccine-to-prevent-covid-19-301214619.html (Accessed on February 05, 2021)
156.
Гидроксихлорохин для пред- и постэкспозиционнойпрофилактики COVID-19: точно нет
открытое рандомизированное исследование, Испания
2485 лиц, контактировавших с подтвержденным случаем COVID-19
число случаев симптомной COVID-19 к 14 дню схожи в группе гидроксихлорохина
(медиана начала приема 4 дня после контакта) по сравнению со стандартным
подходом: 5,7% vs 6,2%, ОР 0,86, 95% ДИ 0,52-1,42
также не обнаружено различий в частоте SARS-CoV-2 среди подгруппы участников,
которые имели отрицательный результат ПЦР на момент включения (18,7% vs
17,8%)
частота побочных эффектов была существенно выше в группе гидроксихлорохина
(56% vs 6%, наиболее часто – гастроинтестиальные проявления, головокружение и
головная боль)
Mitjao O. et al. N Engl J Med 2021;384:417
• аналогичные результаты получены в других опубликованных работах
Boulware D. et al. N Engl J Med 2020;383:517
Rajasingham R. et al. Clin Infect Dis 2020
Barnabas R. et al. Ann Intern Med. 2020
• неэффективность гидроксихлорохина продемонстрирована и для
предэкспозиционной профилактики у медицинских работников высокого
риска в двойном слепом плацебо-контролируемом РКИ
Abella B. et al. JAMA Intern Med 2021;181:195
157.
Материалы для специалистов покоронавирусной инфекции
www.covid19center.by
Постоянно обновляемая база знаний по COVID-19
инфекции





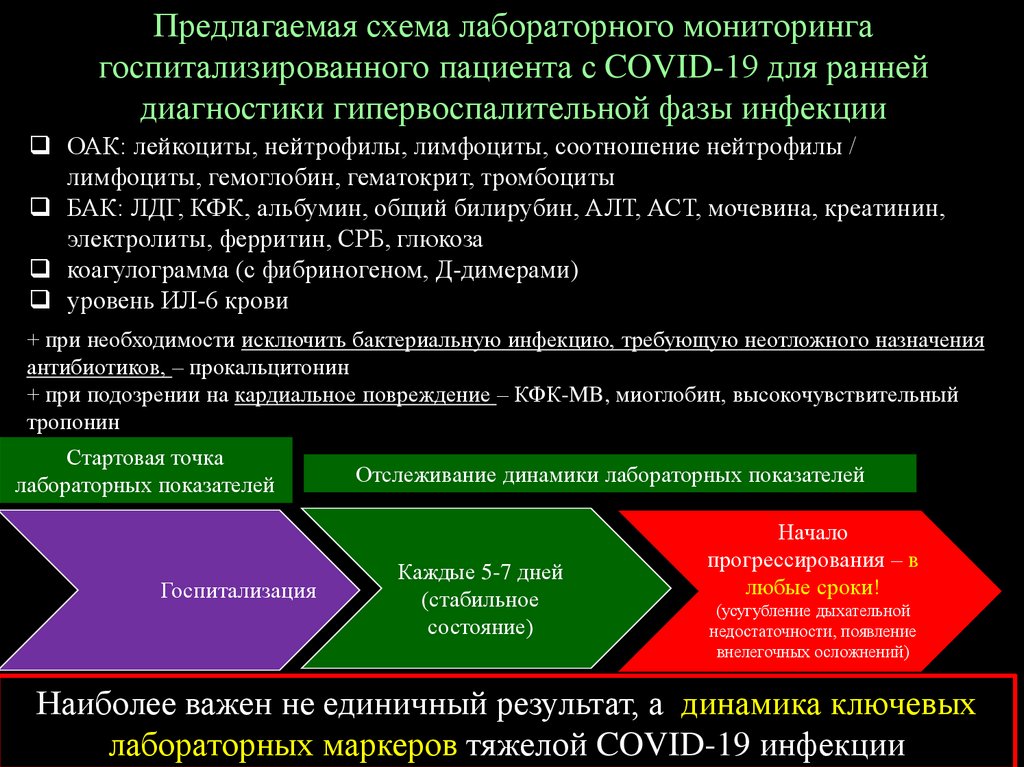

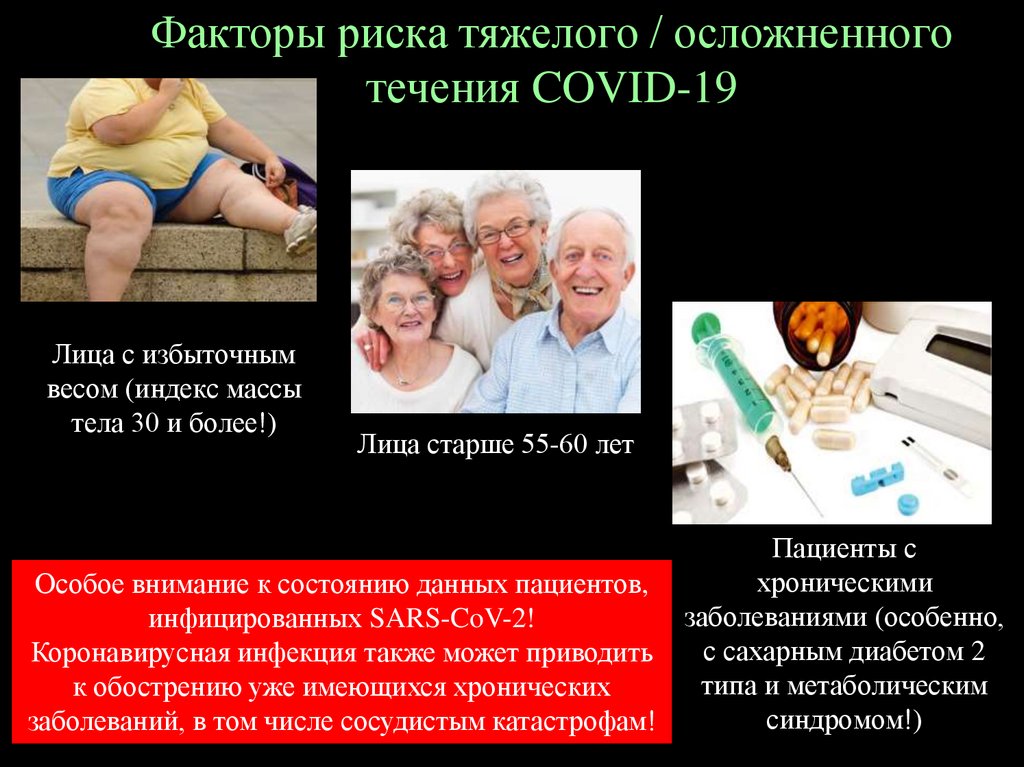




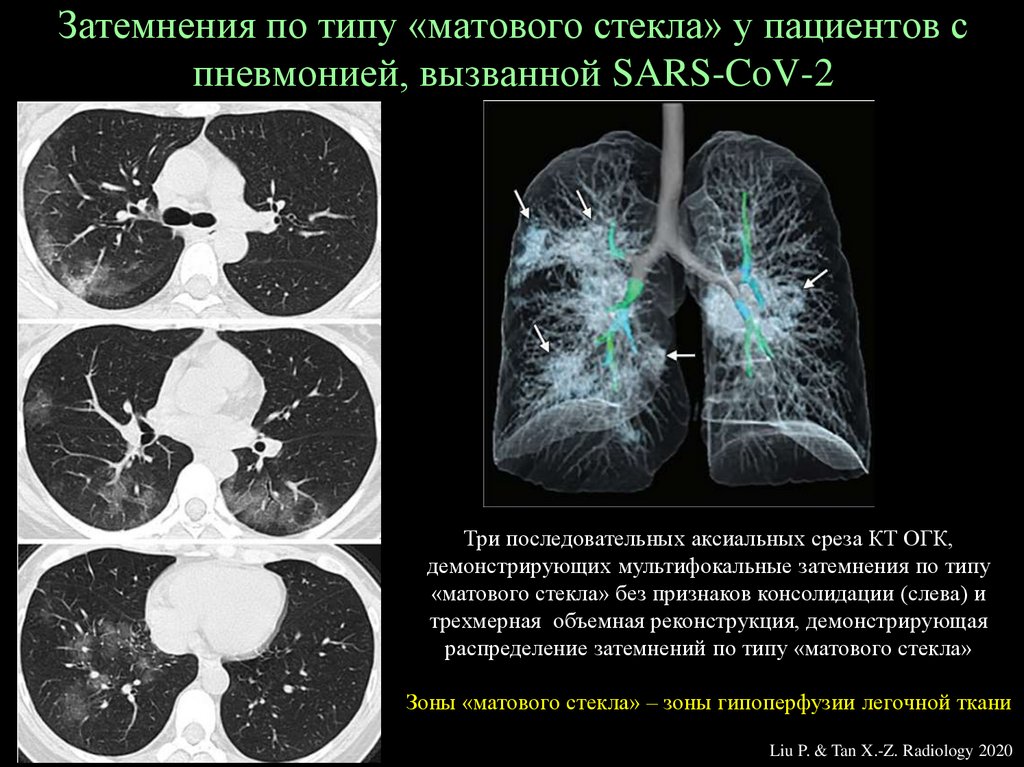


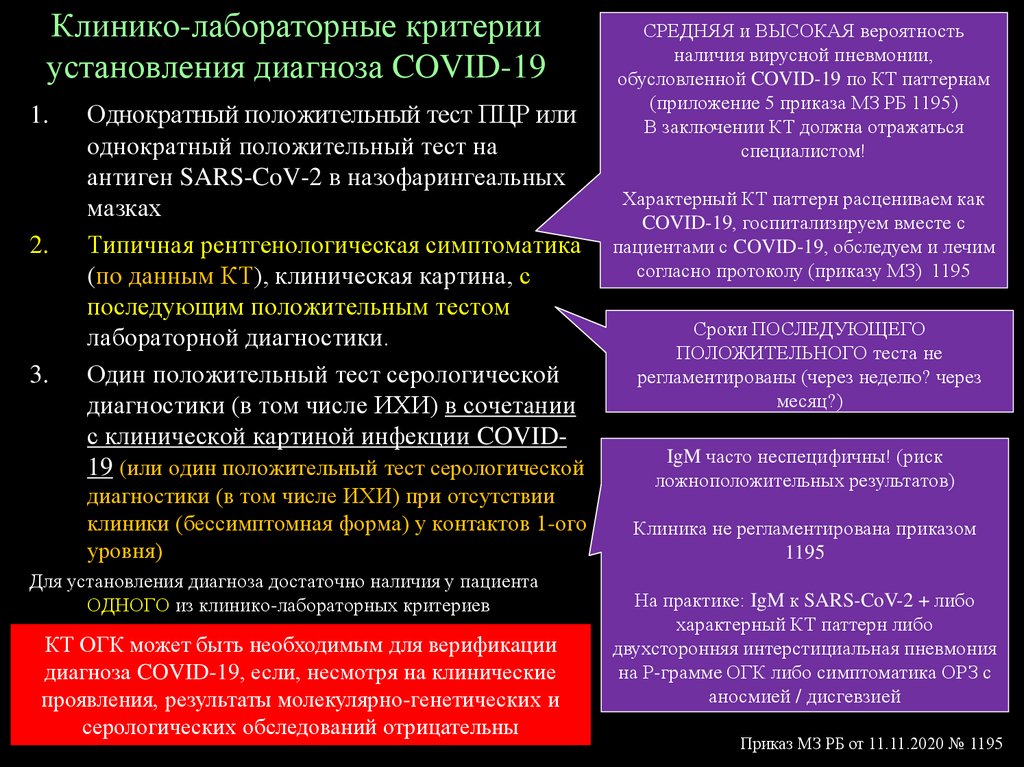

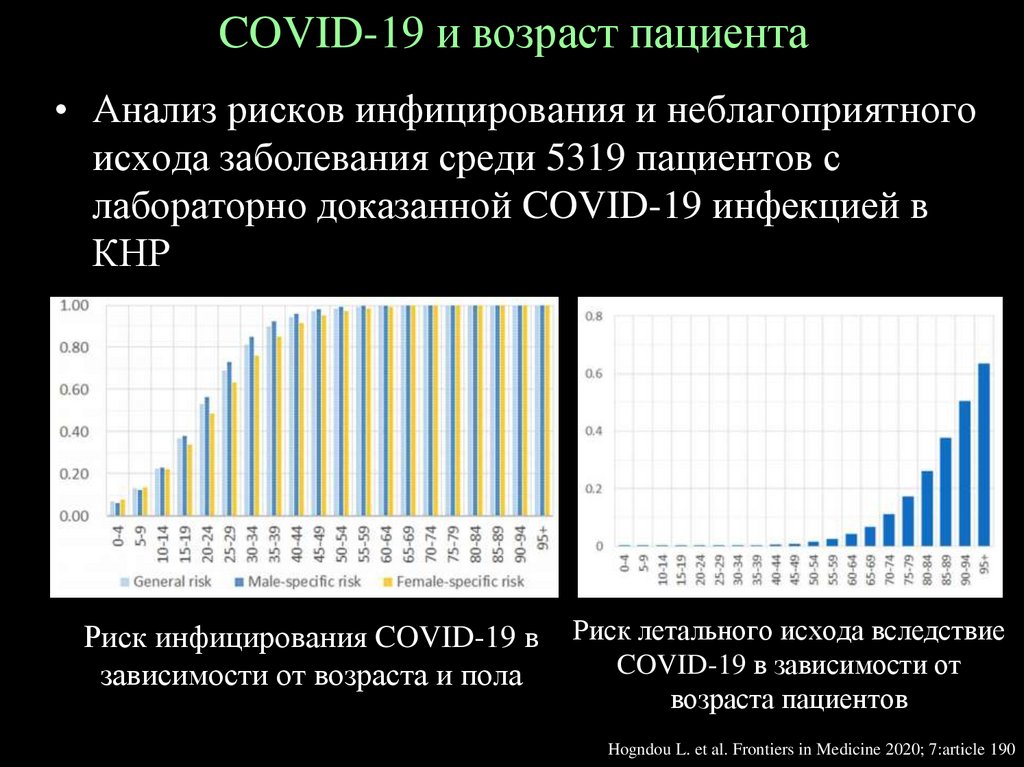
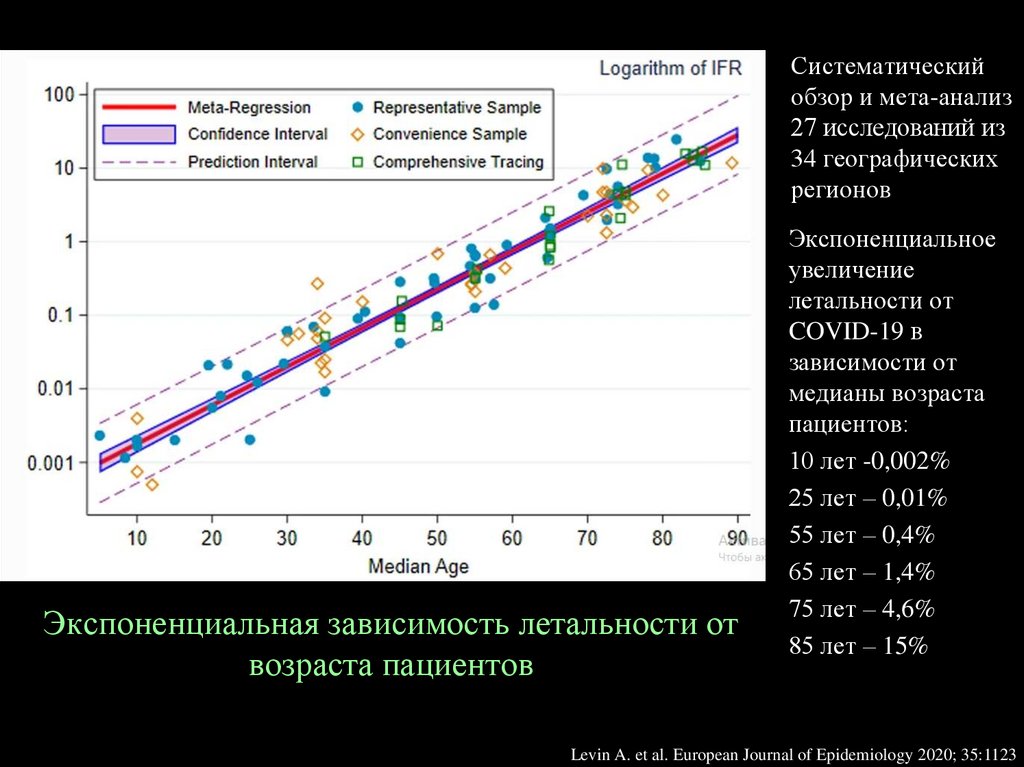



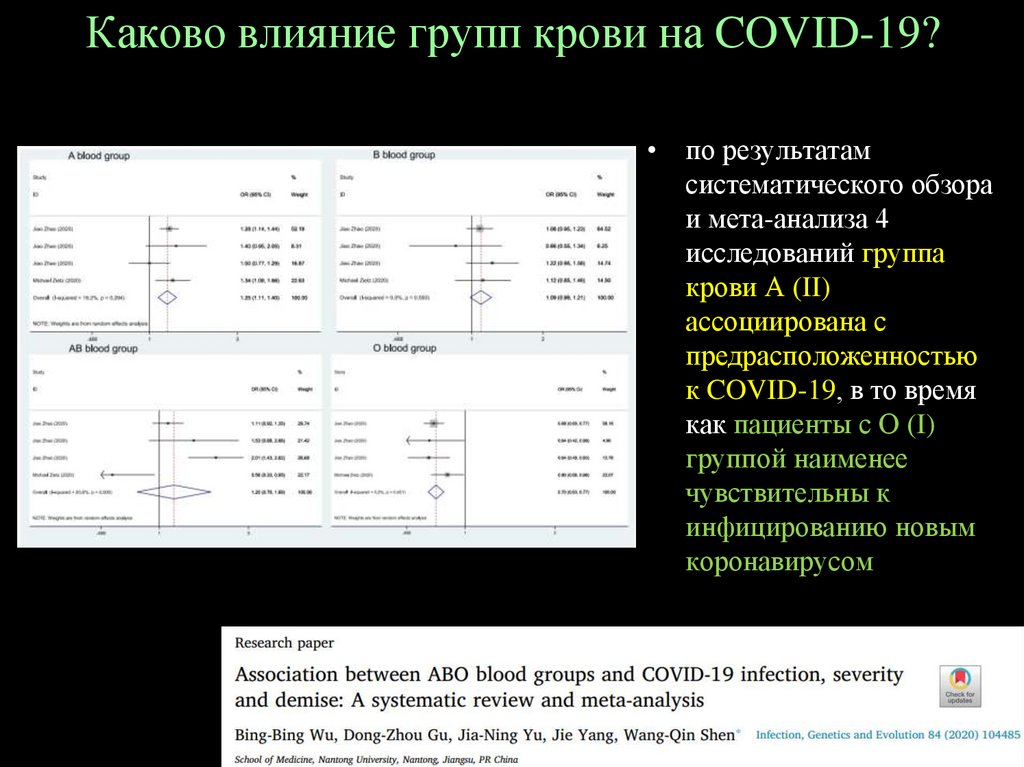


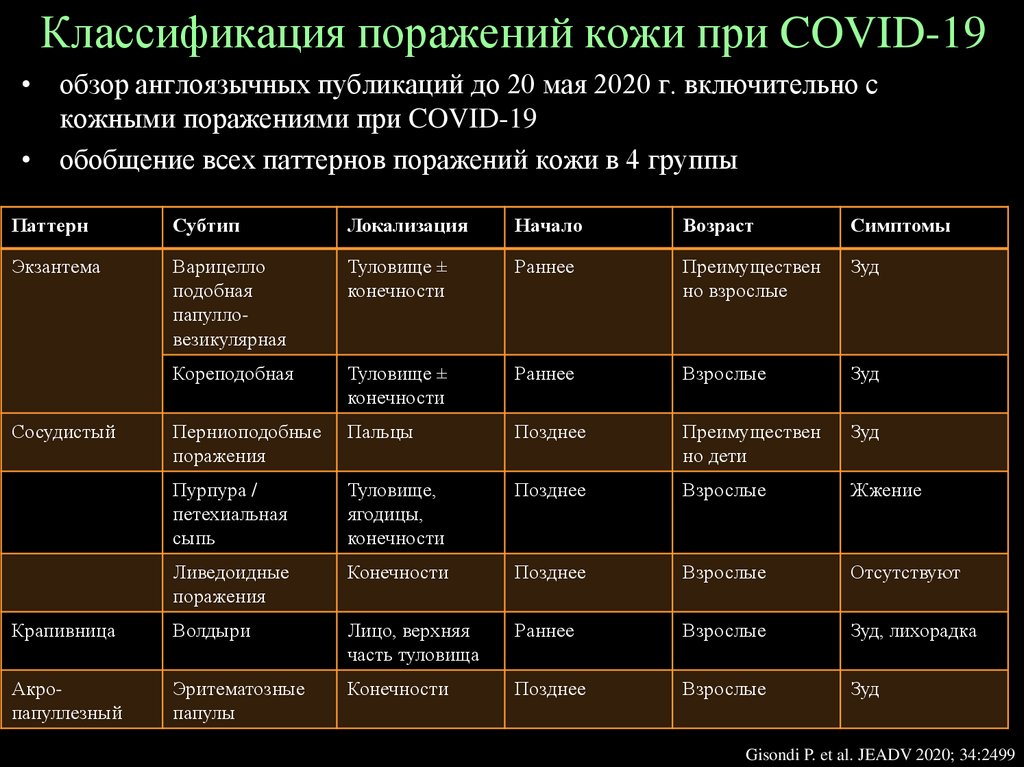
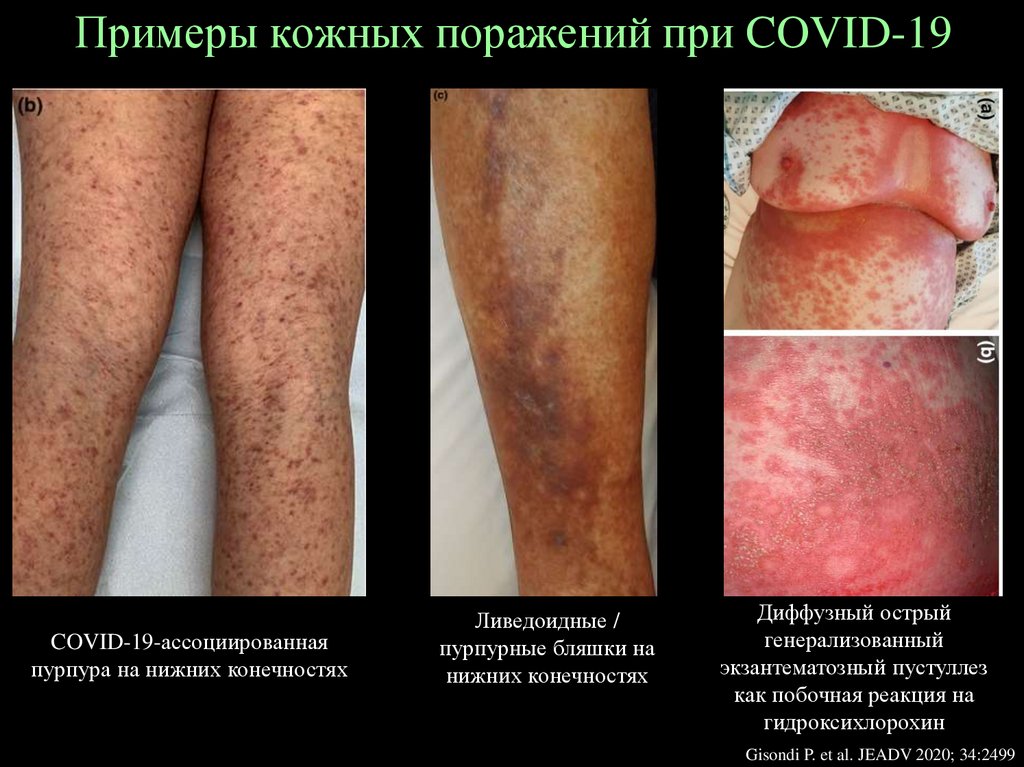


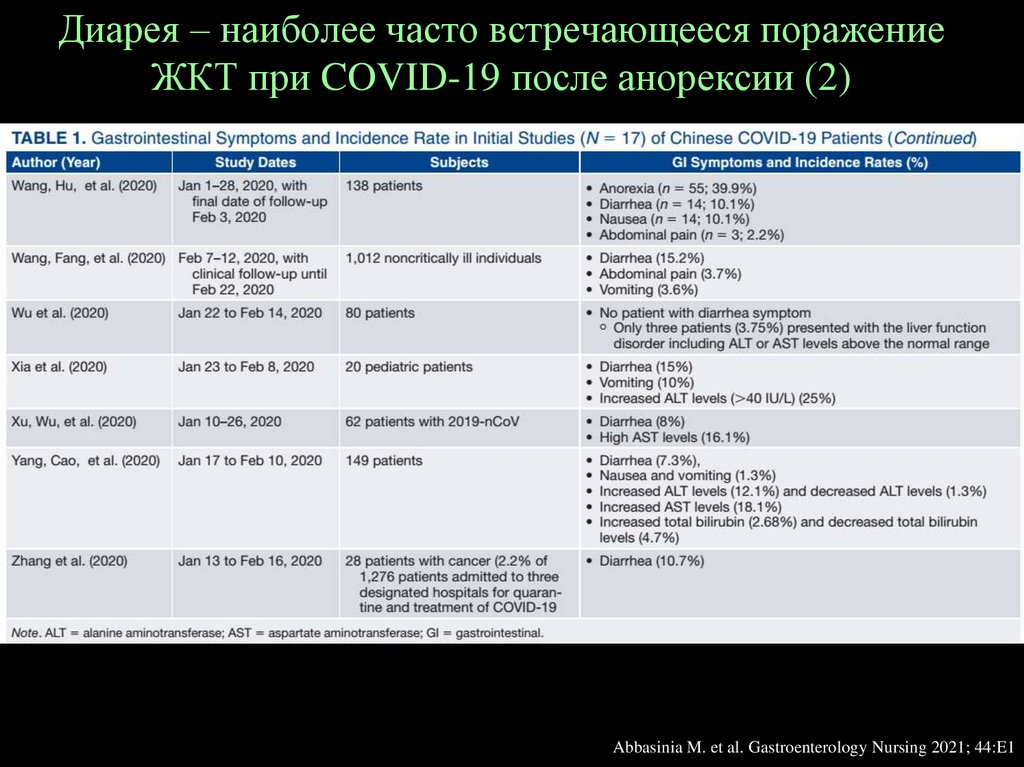

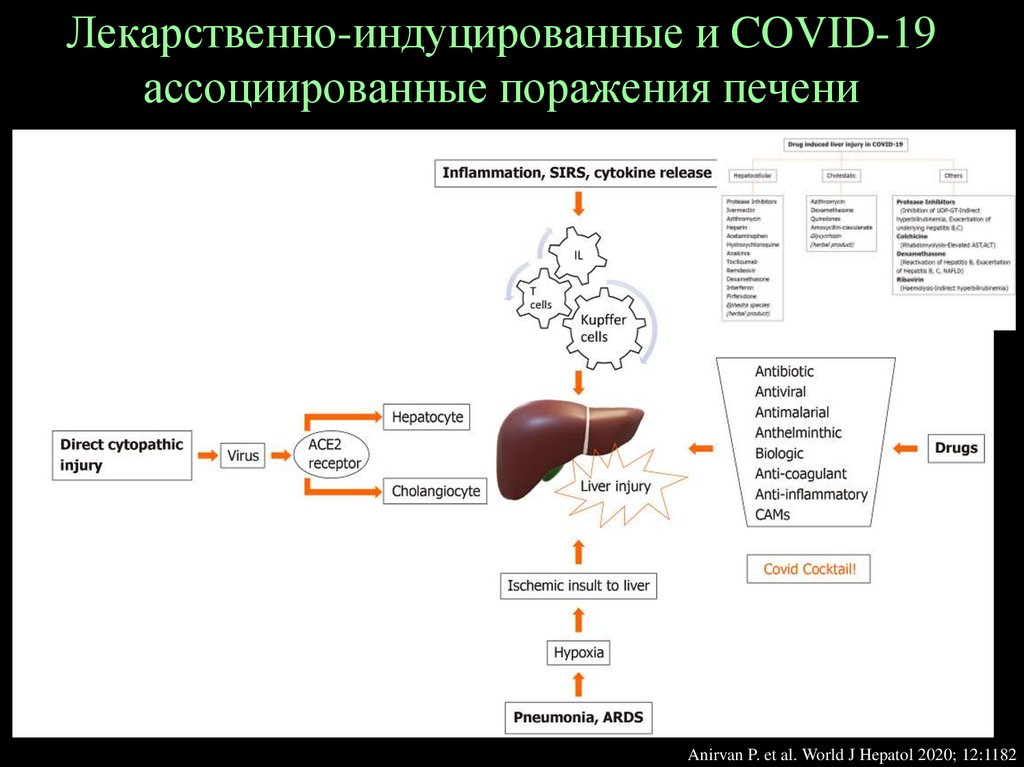





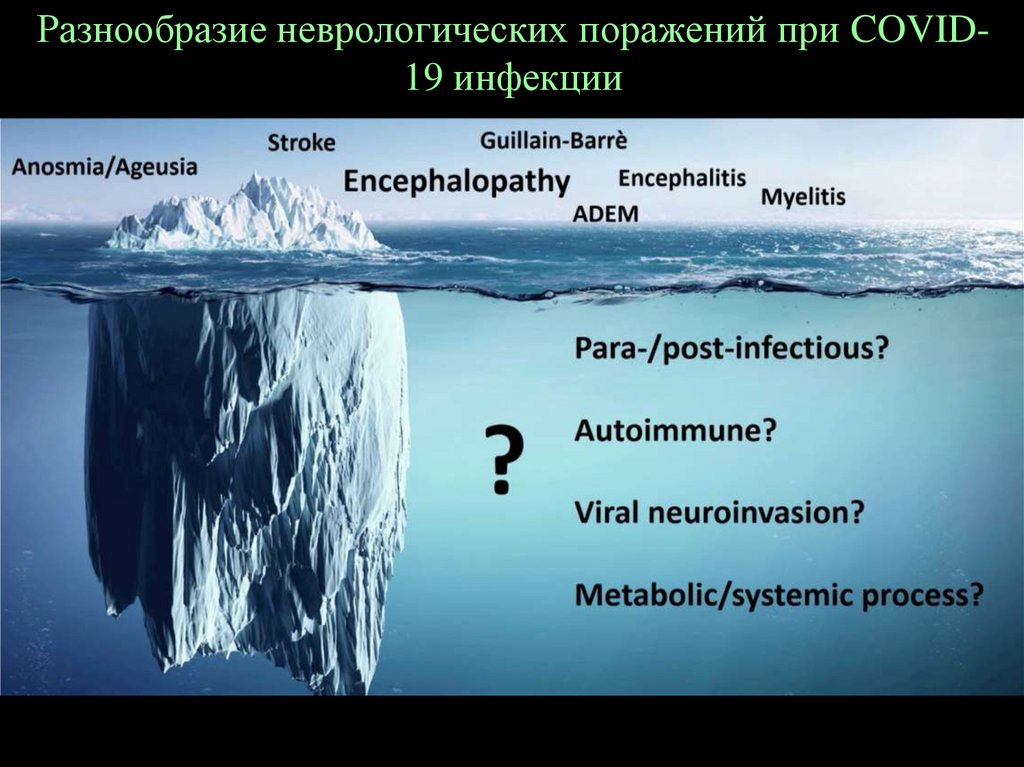

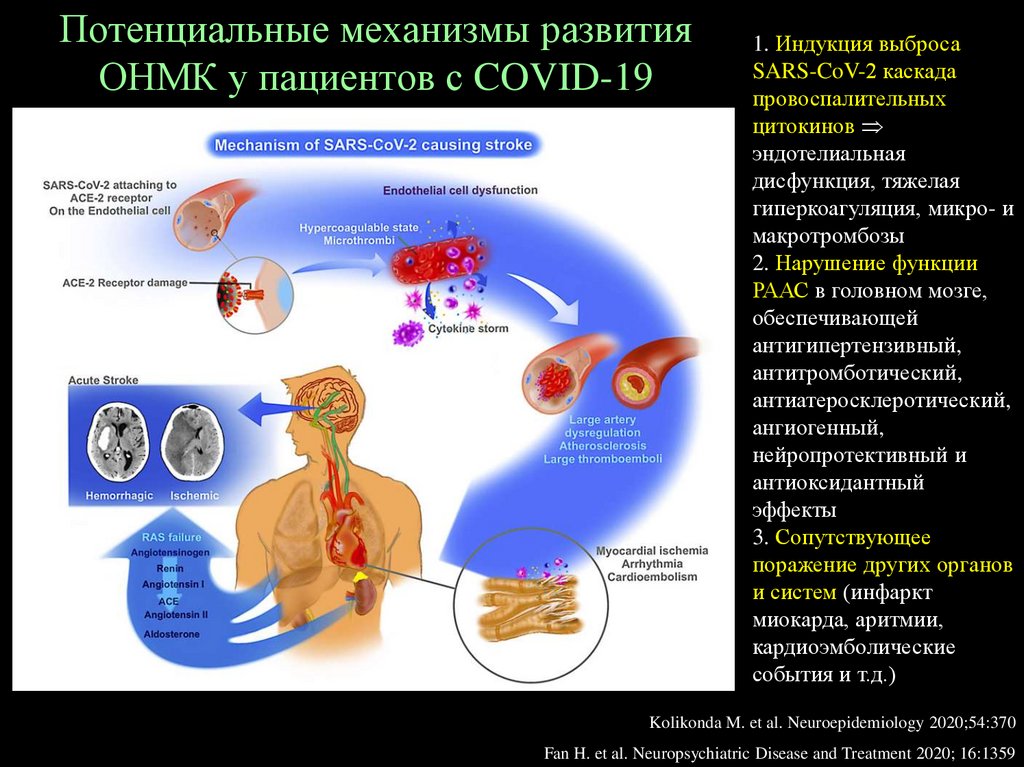










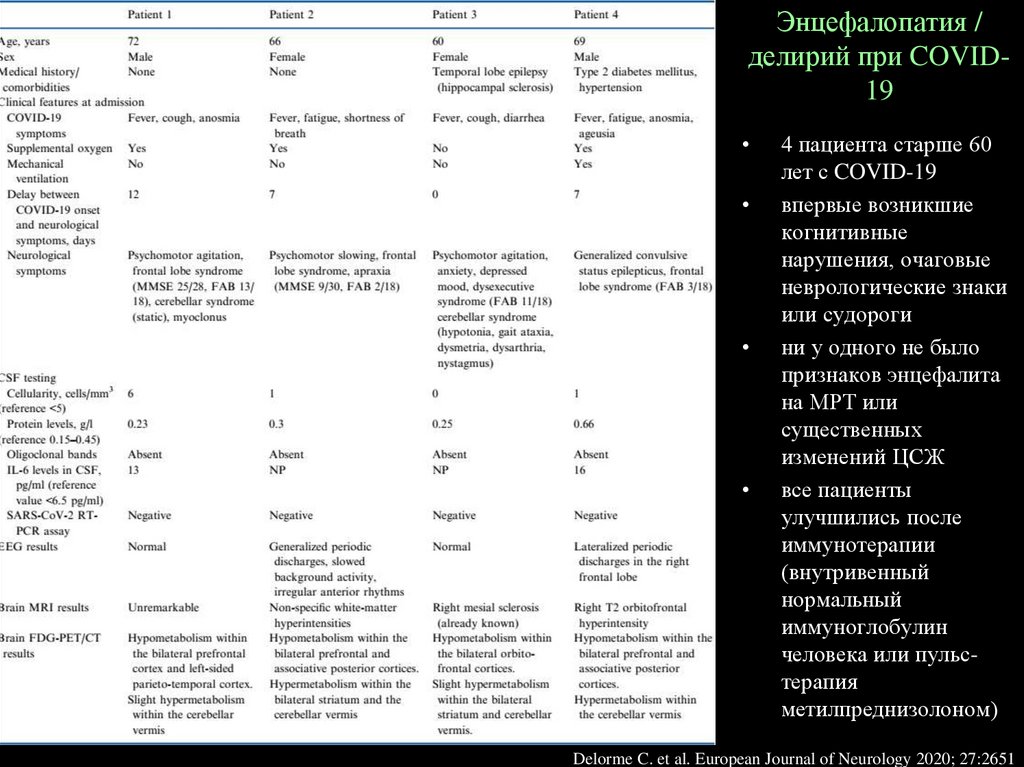









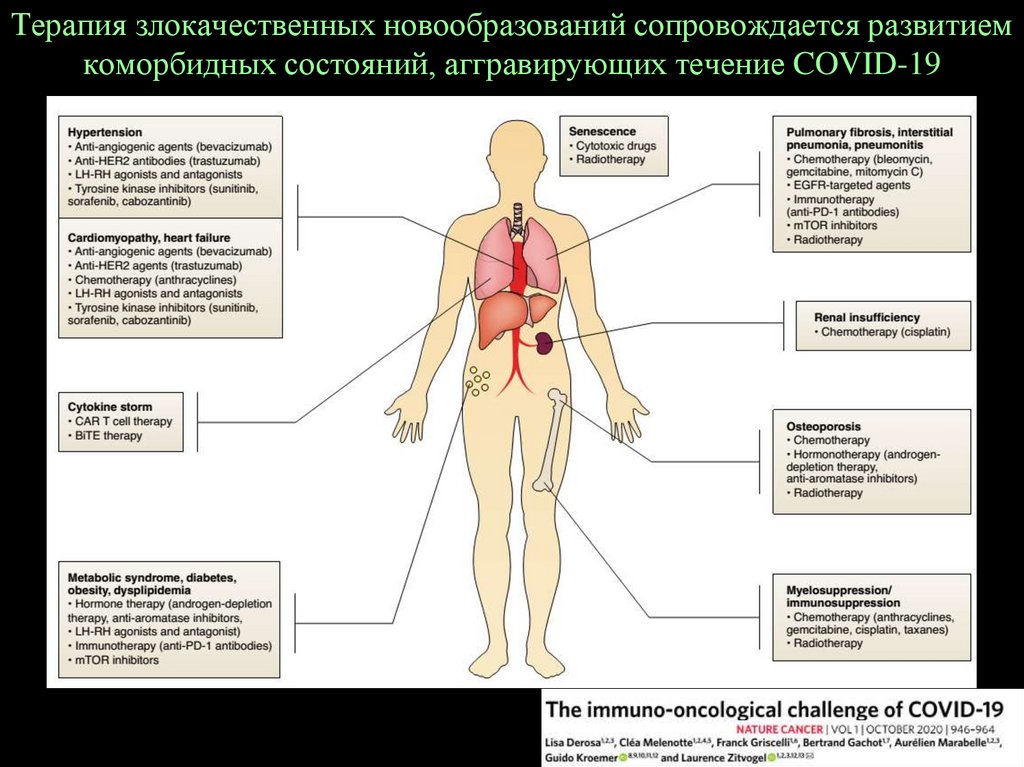















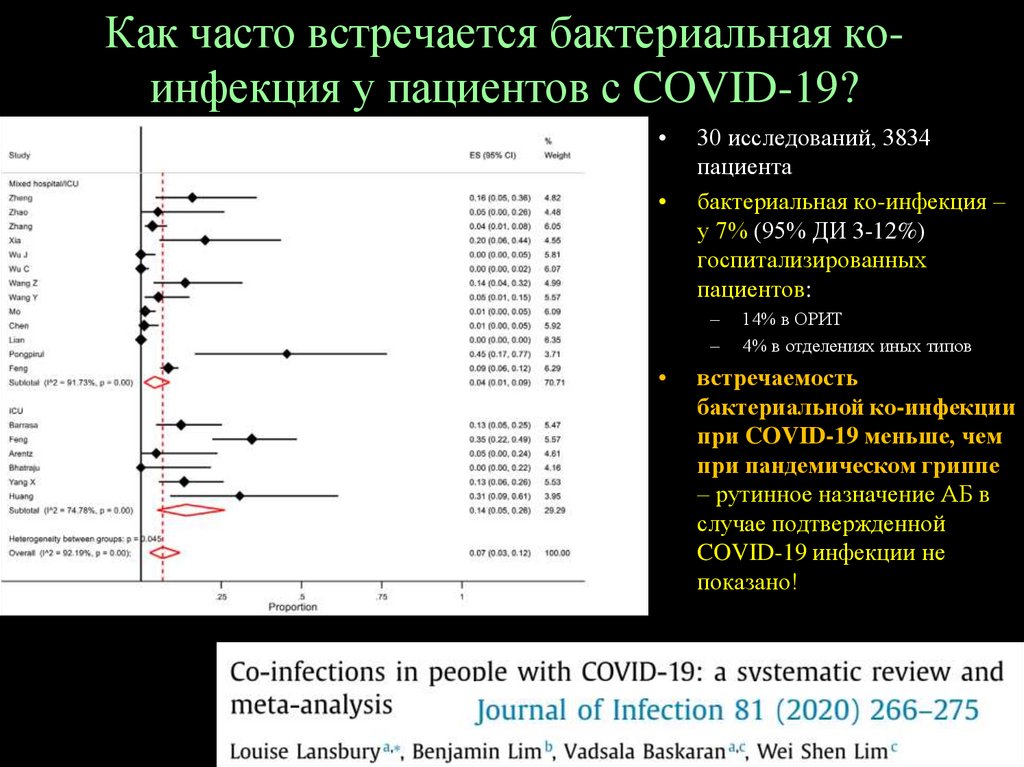















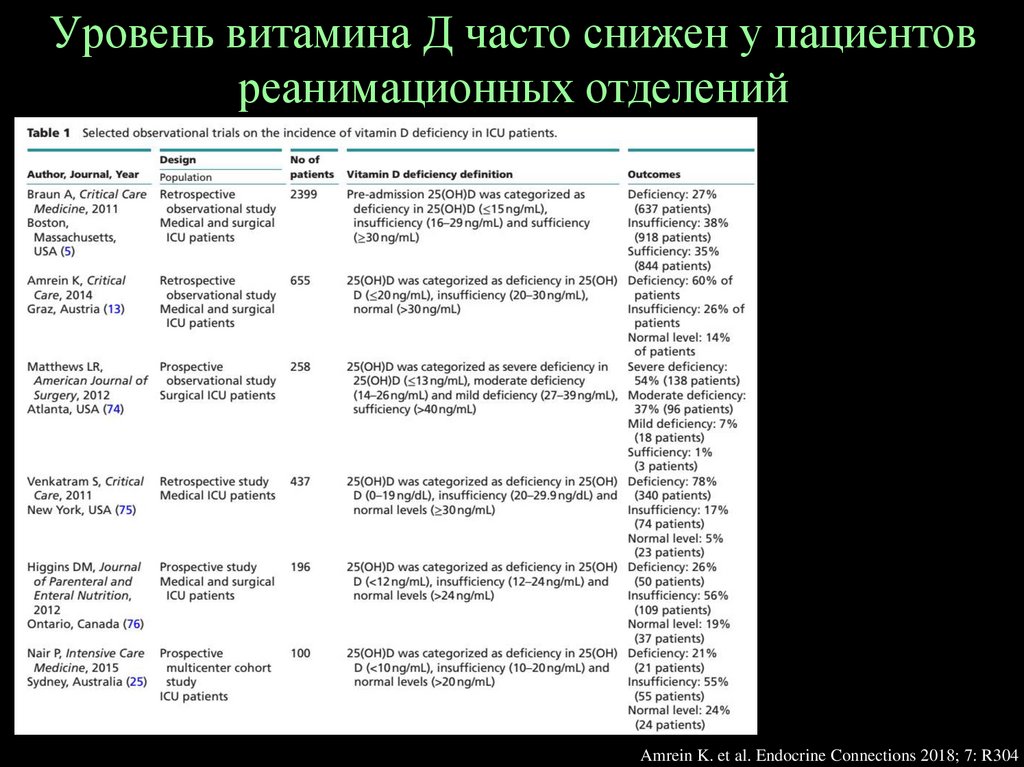
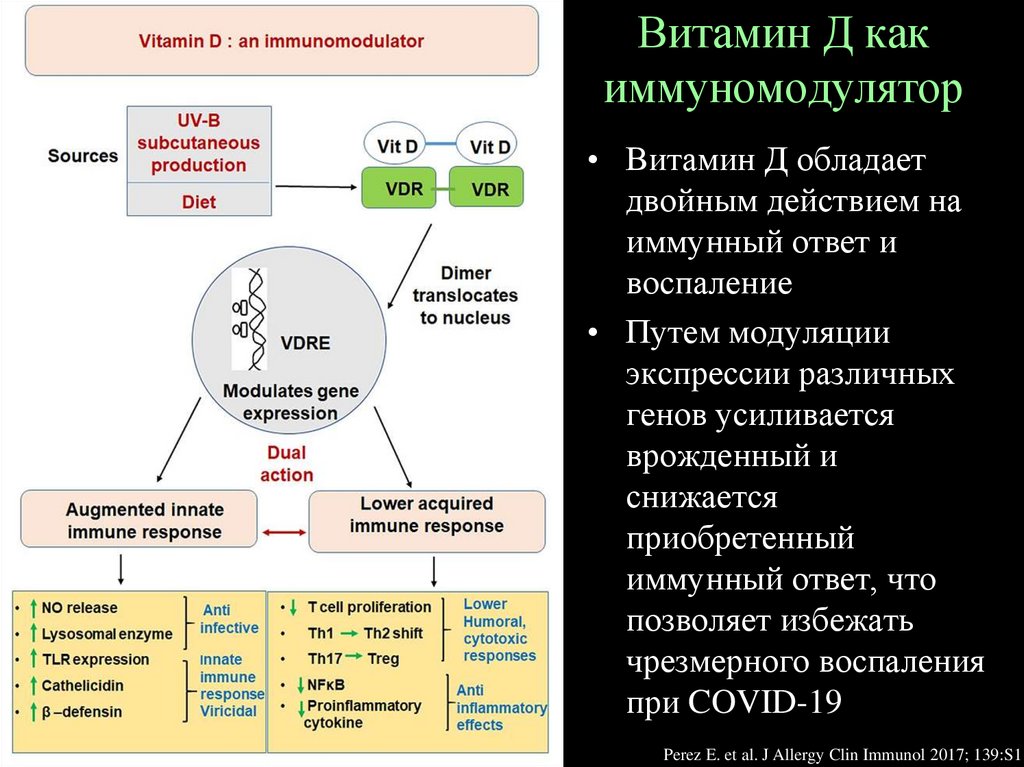
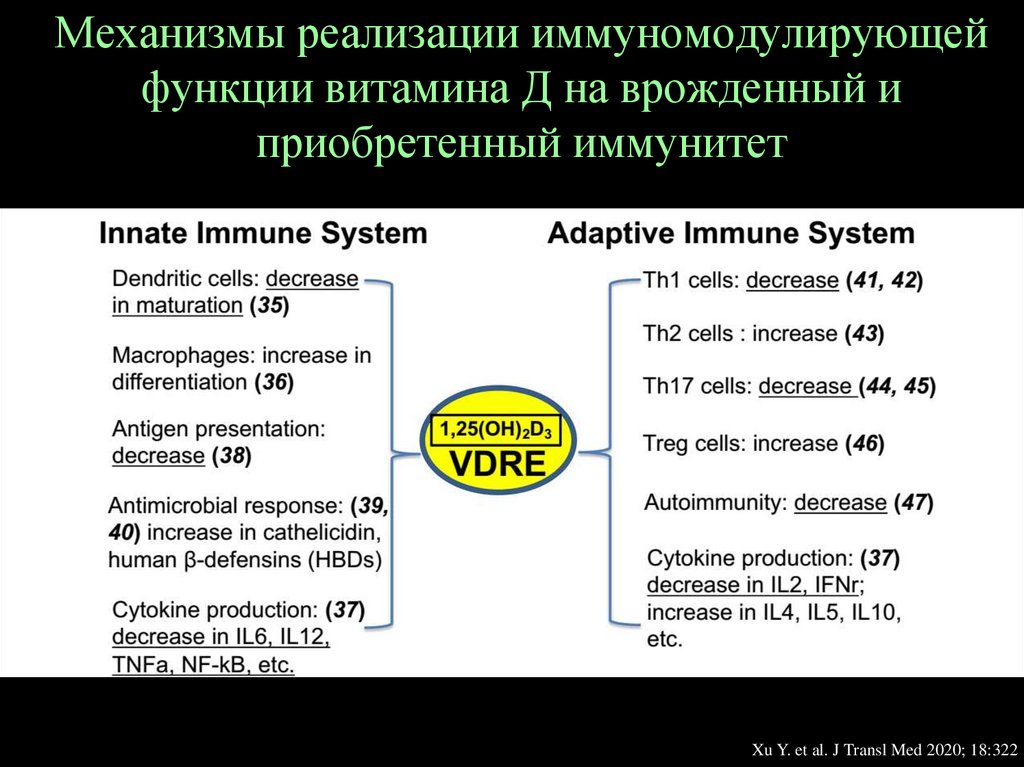
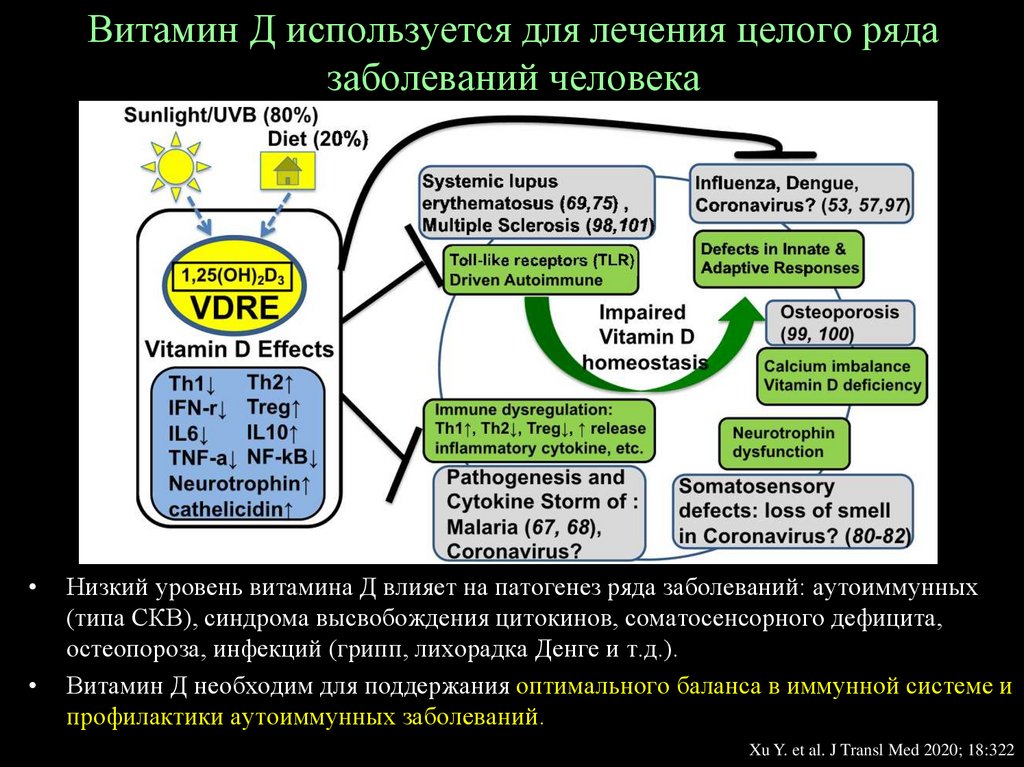









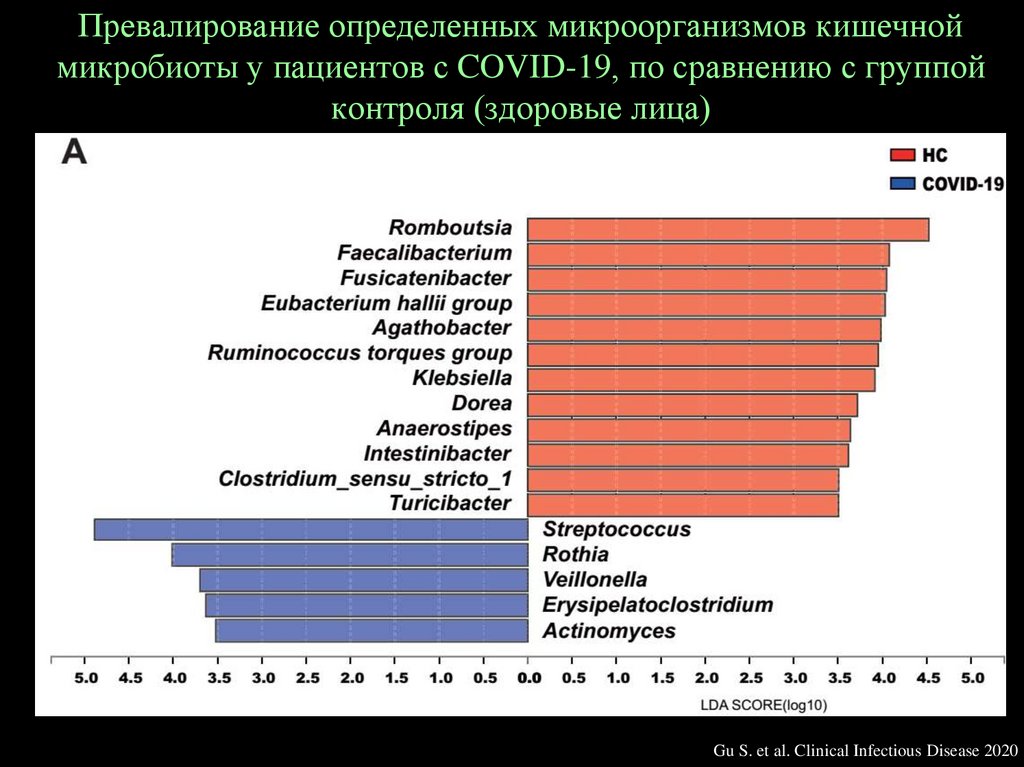



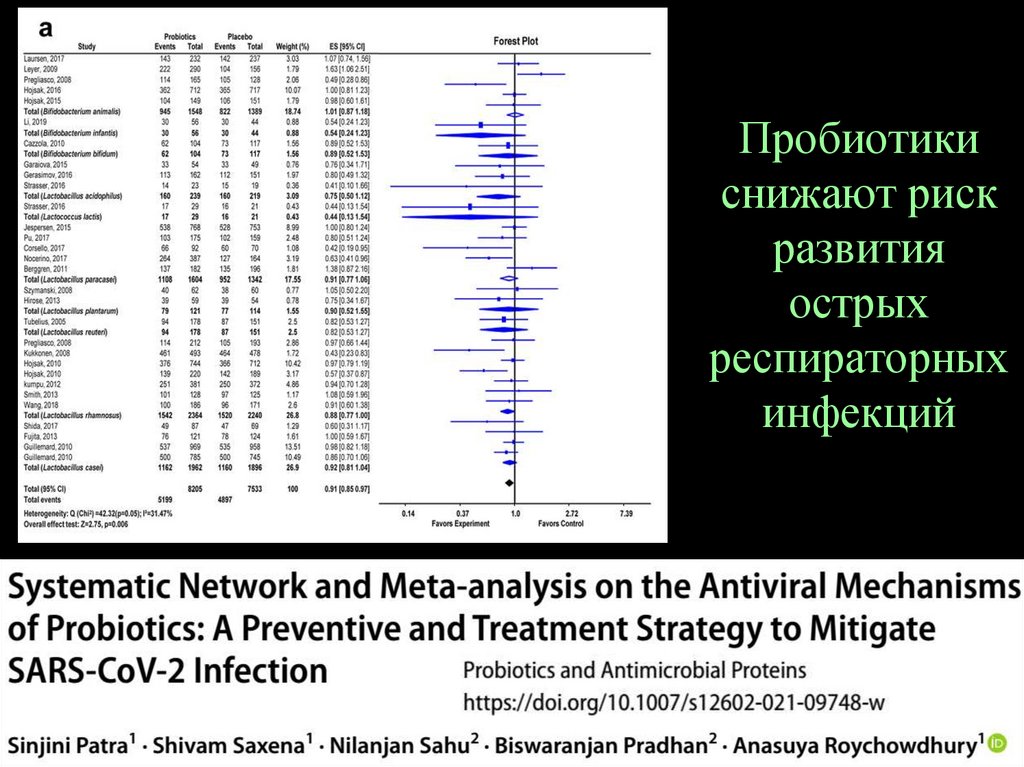



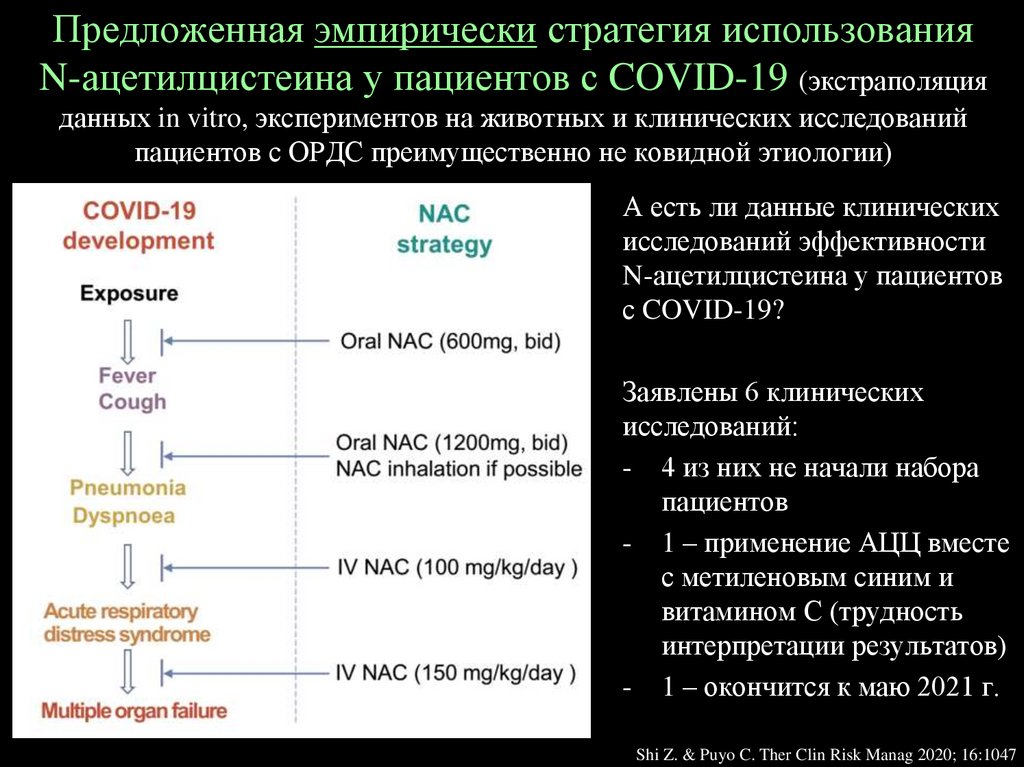











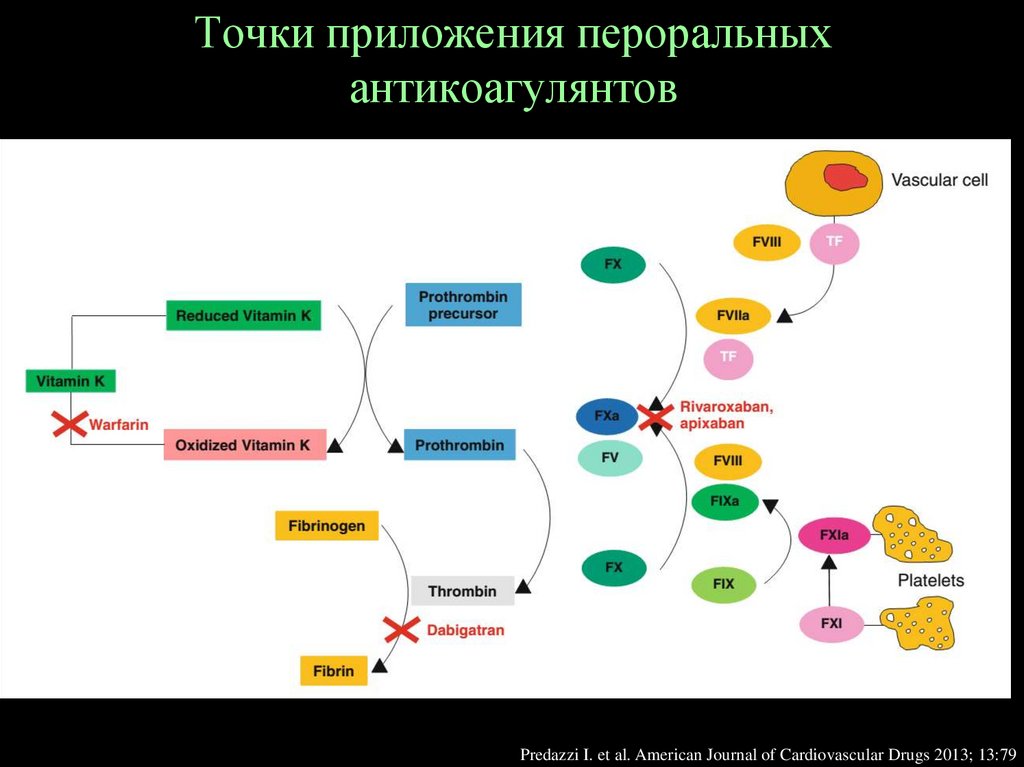









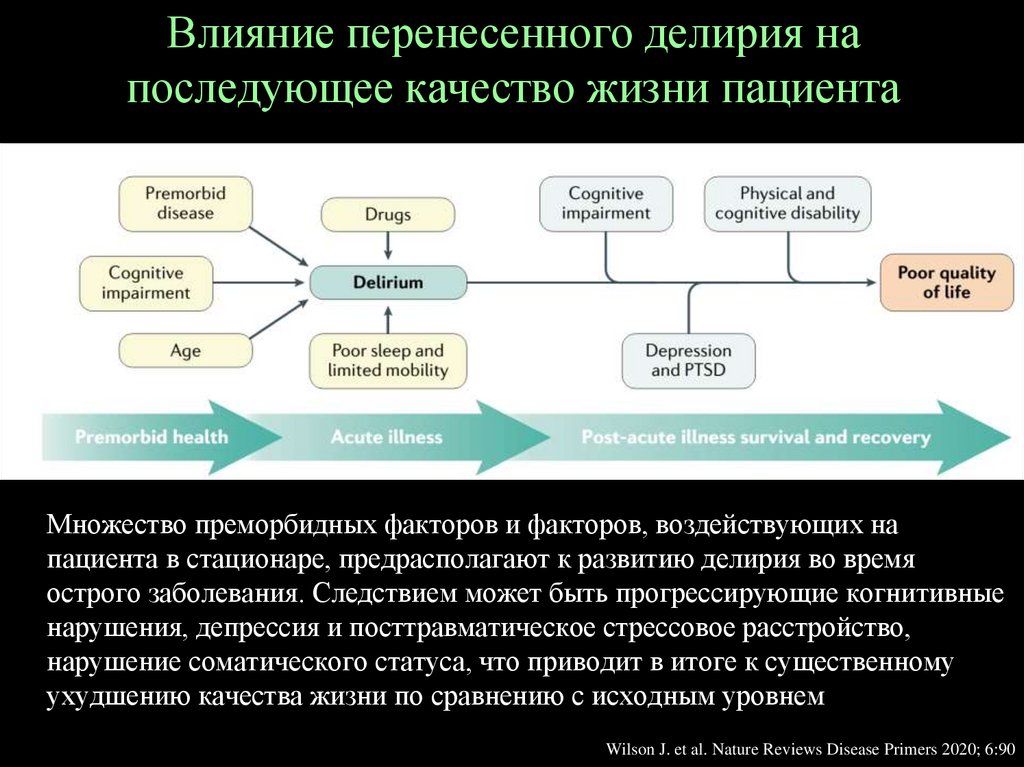
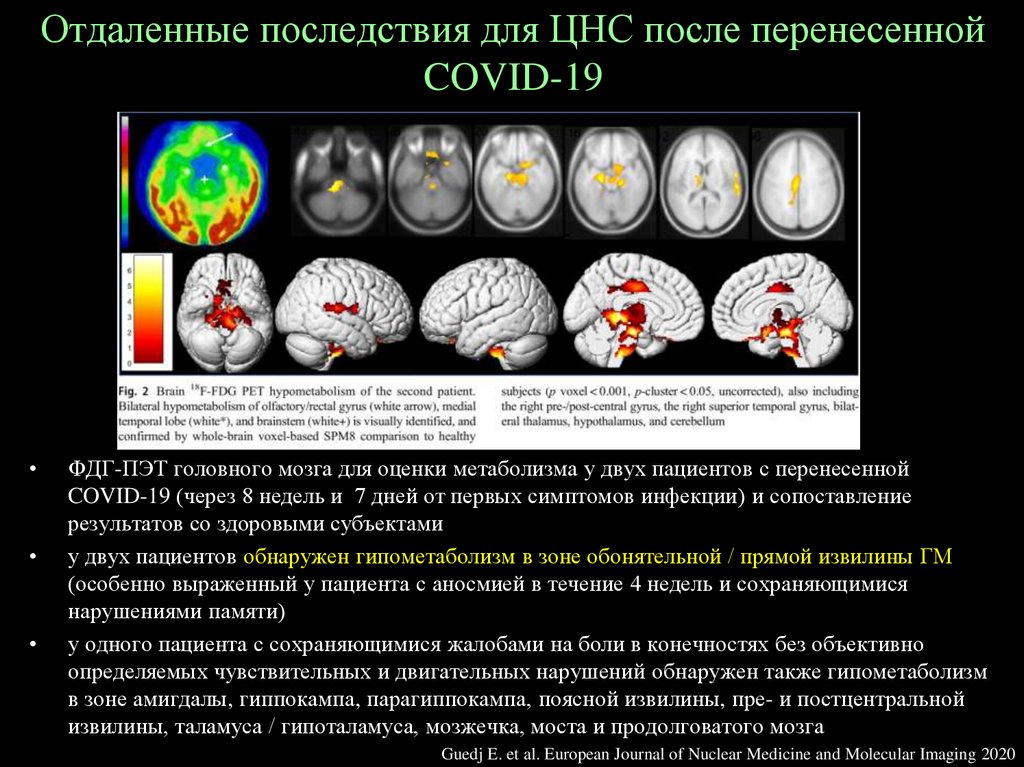





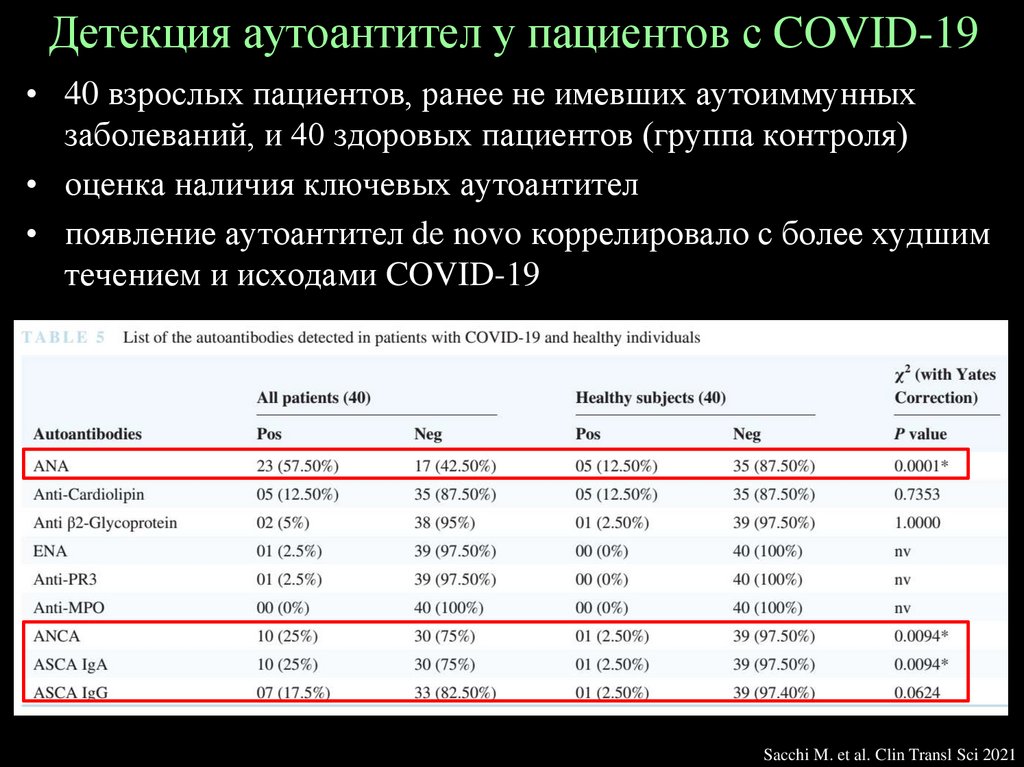
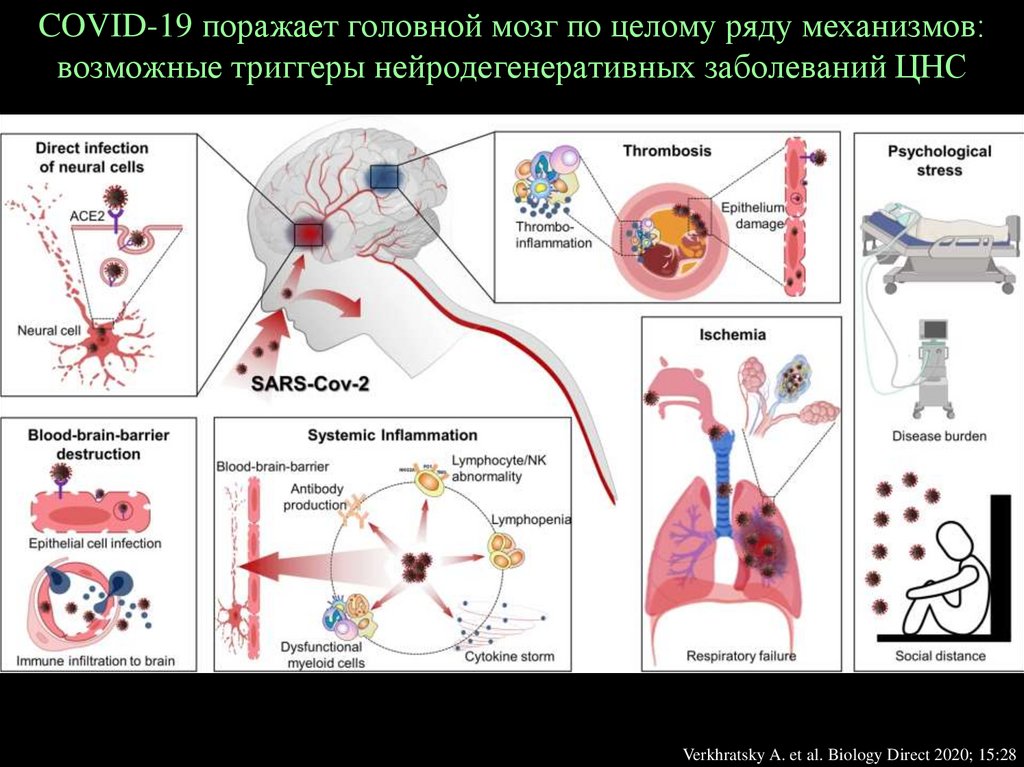





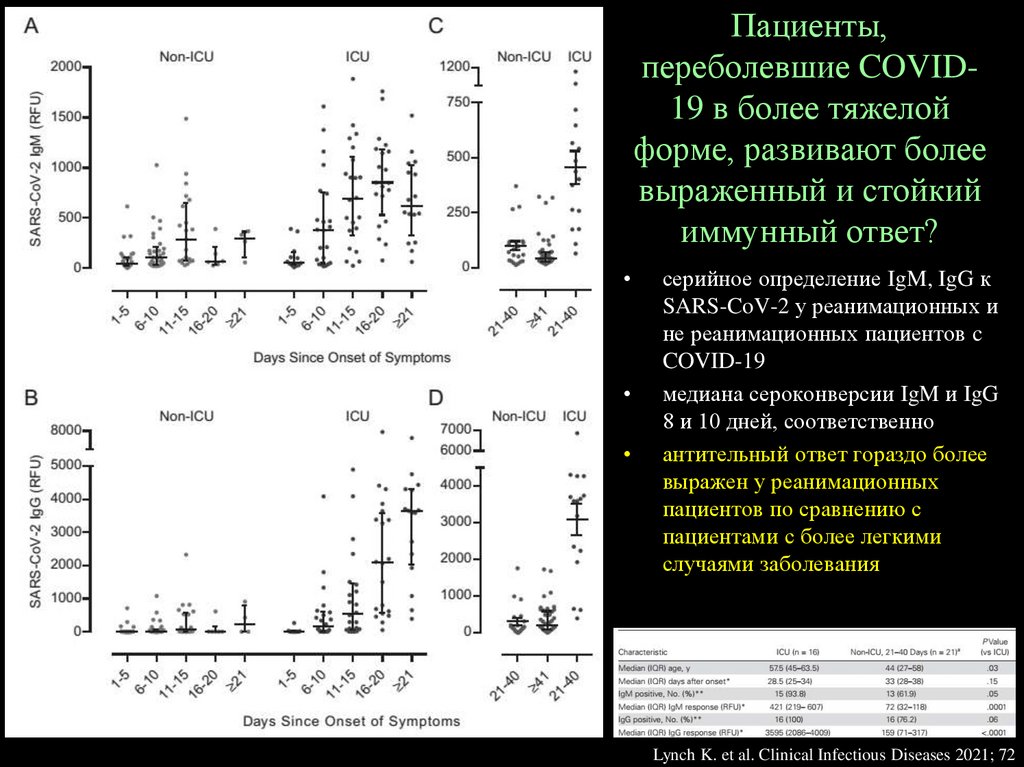



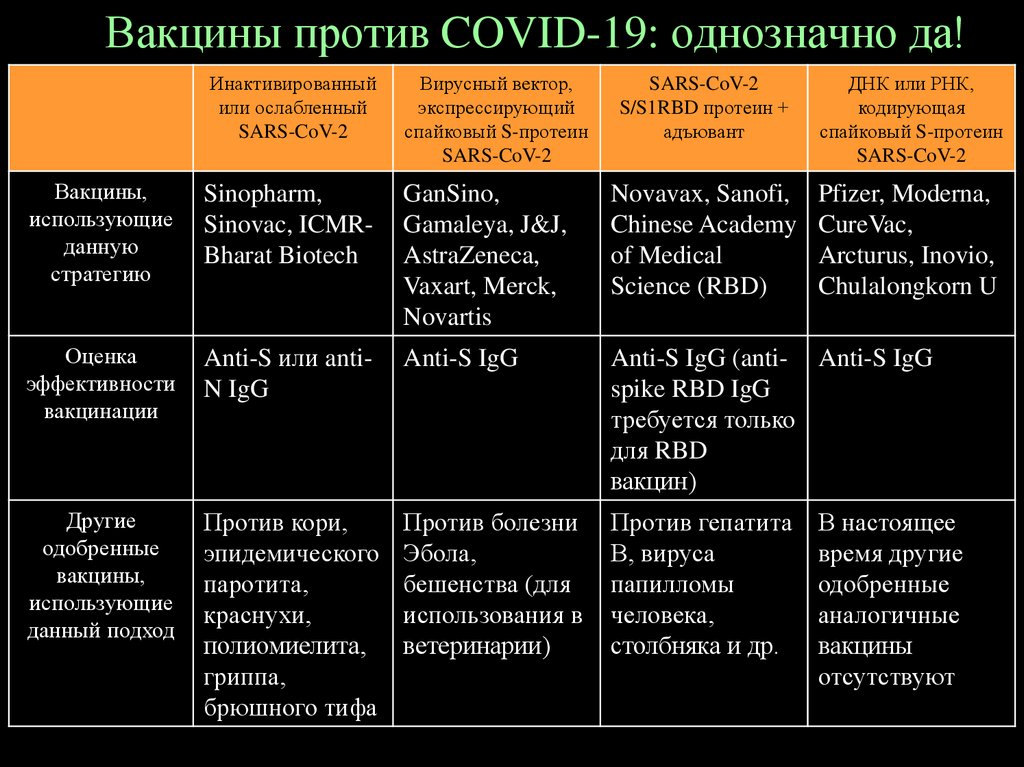



 medicine
medicine








