Similar presentations:
Ионная хроматография
1.
Ионная хроматографияВебинар
(Часть I)
Декабрь 2020 г.
2.
I. ВведениеАналиты (определяемые вещества)
Неорганические ионы (анионов и катионов)
Органические ионы
Углеводы
Гликопротеины и др.
3.
I. ВведениеОтрасли
Экологический контроль (природные и сточные воды,
метеорологический контоль, контроль промышленных выбросов и т.д.)
Водоподготовка (питьевая вода)
Энергетика (технологические среды)
Пищевая промышленность
Сельское хозяйство
Фармацевтика
Производство полупроводников
Нефтепераработка и т.д.
4.
I. ВведениеОсобенности метода
В основе - стехиометрический ионный обмен
Сорбенты (неподвижная фаза) – ионообменнкики разной силы
невысокой ёмкости
Элюенты – растворы электролитов – солей, кислот и оснований
Режим подачи растворителей - изократический
5.
I. ВведениеОсобенности метода (плюсы)
⁺
⁺
⁺
⁺
⁺
Возможность определять количественно сразу несколько компонентов
Экспрессность
Высокая чувствительность (до 10-9 г/мл без концентрирования)
Возможность частичной или полной автоматизации
Часто, отсутствие пробоподготовки
6.
I. ВведениеОсобенности метода (минусы)
-
Сложность синтеза ионообменных сорбентов
Эффективность разделения хуже, чем в стандартной обращенофазной
ВЭЖХ
Сильно коррозионная среда
Чувствительность ионообменников к органическим загрязнениям
7.
I. ИХ системаS
Inj
P
P
I
S
C
D
C
D
R
– насос - для подачи подвижной фазы (элюента) через колонку)
W
– инжектор - для введения пробы в колонку без остановки потока
– проба
– разделительная колонка
– детектор - устройство для получения аналитического сигнала, пропорционального концентрации
определяемого компонента
R – регистратор - для преобразования аналитического сигнала в форму, необходимую для
автоматического управления и расчета концентрации искомого аналита
W - слив
8.
I. Введение9.
I. Процесс разделения на колонкеCond
µS/ cm
40
30
20
10
0
Проба
Из
инжектора
1
2
3
4
5
Колонка
6
7
8 min
Детектор
Слив
10.
I. ВведениеОсновные характеристики «типичного» ИХ метода
Параметр
Величина
Размер частиц сорбента
3 – 7 мкм
Длина колонки
Внутренний диаметр колонки
Эффективность (число теоретических тарелок)
Расход элюента
Рабочее давление
Продолжительность анализа
50 – 250 мм
2 – 5 мм
10 – 20 тыс
0,1 – 2 мл/мин
50 – 200 бар (атм)
10 – 20 мин
11.
I.1. Ионный обменАктивные группы
зафиксированные ионы
Матрица
12.
I.1. Схема ионного обменаNa+
OH-
Na+
OHNa+
OHOH-
OHOH-
Анионообменник
OHOH-
+
OH-
+
+
+
OH-
+
Неподвижная фаза
+
(сорбент)
+
+
+
+ +
OH-
+
OH-
OH-
OH-
OH-
13.
I.1. Схема ионного обменаH2O
H2O
An-
An-
K+
OHOHOH-
Анионообменник
H2 O
K+
OHOH-
+
OH-
+
+
+
OH-
+
Неподвижная фаза
+
(сорбент)
+
+
+
+ +
OH-
+
OH-
OH-
OH-
OH-
14.
I.1. Схема ионного обменаРазделение анионов
Na+
Na+
OH-
OH-
Na+
OH-
OHNa+
OHOH-
OHAn-
Анионообменник
+
OH-
+
+
+
OHOH-
+
Неподвижная фаза
+
(сорбент)
+
+
+
+ +
OH-
+
OH-
OH-
OHOHAn-
15.
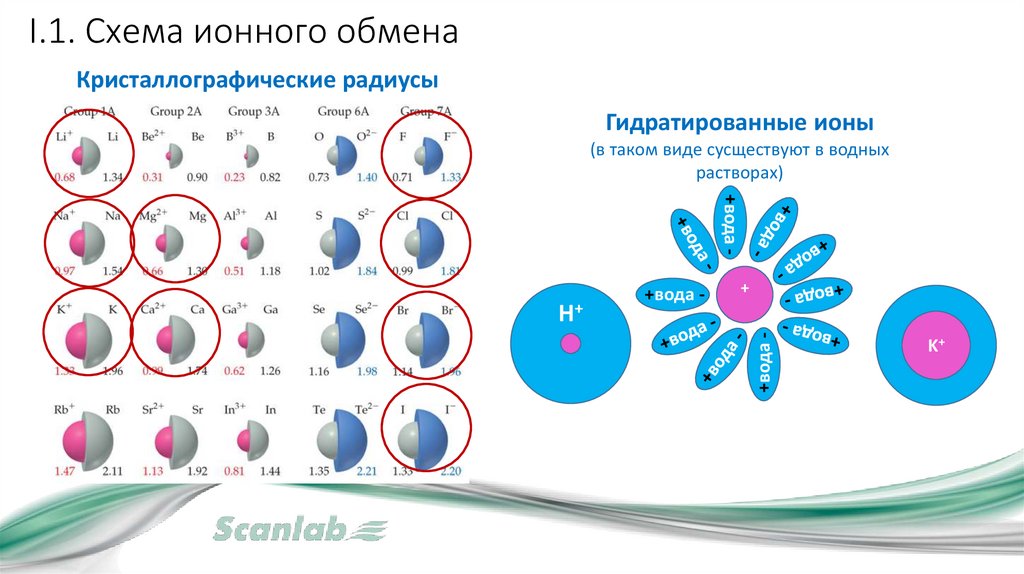
I.1. Схема ионного обменаКристаллографические радиусы
Гидратированные ионы
(в таком виде сусществуют в водных
растворах)
+вода +
+вода -
H+
+вода -
K+
16.
I.1. Схема ионного обменаСорбционный ряд катионов:
Ba+2 > Pb+2 > Ca+2 > Cu+2 > Mg+2 > Cs+ > Rb+ > K+ > NH4+ > Na+ > H+
Порядок элюирования
-
+ +
KH
Сa2+
Сорбционный ряд анионов:
цитрат > SO4-2 > HPO42- > ClO3- > NO3- > Br- > NO2- > Cl- > HCO3-> CH3COO- > OH- > FПорядок элюирования
17.
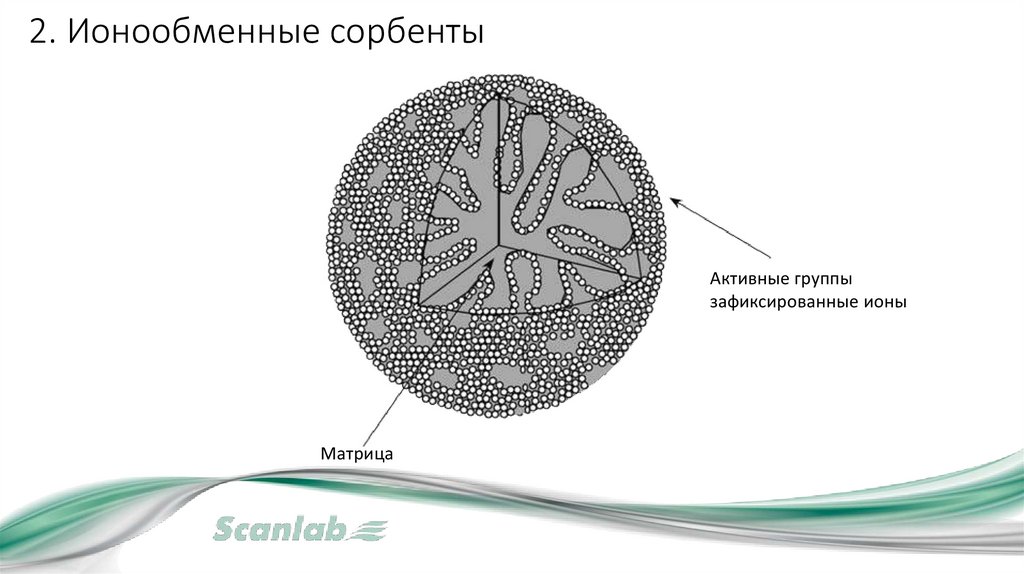
2. Ионообменные сорбентыАктивные группы
зафиксированные ионы
Матрица
18.
I.2. Ионообменные сорбенты1.2
Требования к сорбентам
Сорбент должен иметь низкую ионообменную ёмкость (ограниченное
количество активных центров):
Катиониты : 4 – 4,5 ммоль экв./г
Аниониты: 3,5-4 ммоль экв./г
Диаметр зерен сорбента не должен превышать 20 мкм, чтобы добиться
необходимого разрешен
Зерна сорбента должны обладать высокой механической прочностью и
устойчивостью к давлению
Сорбент должен обладать высокой химической устойчивостью по
отношению к подвижной фазе (элюенту)
19.
I.2. Ионообменные сорбенты. Матрицыстирол
дивинилбензол
Поливиниловый спирт
Сополимер стирола и дивинилбензола
Силикагель
Полигидроксиметакрилат
20.
I.2. Ионообменные сорбенты . Активные группыАнионообменники
Катионообменники
Сульфо-группа
Сильный
Карбоксильнаягруппа
Слабый
Вторичные или
третичные
амино-группы
Слабый
Четвертичнная
амино-группы
Сильный
Четвертичнная
амино-группы
Сильный
21.
I.3. Подвижные фазыОсобенности подвижных фаз
Практически всегда – водные растворы электролитов – солей, кислот и
оснований
Низкие концентрации (чтобы уменьшить фоновый сигнал)
Элюирующая сила меняется с изменением состава и коцентраций
Сильное влияние рН
Элюирующий ион
22.
I.3. Подвижные фазыДля анионного анализа
Наиболее распространенными элюентами в ионной хроматографии анионов являются разбавленные растворы
солей слабых кислот. Эти элюенты используют для определения анионов сильных кислот, рК которых ниже 5.
Элюент
Элюирующий иона
Элюирующая
способность
NaOH
OH-
низкая
Na2B4O7
BO3-
Очень низкая
Na2CO3
CO32-
средняя
HCO3-, CO32-
средняя
CO32-, OH-
высокая
NaHCO3 / Na2CO3
Na2CO3 / NaOH
23.
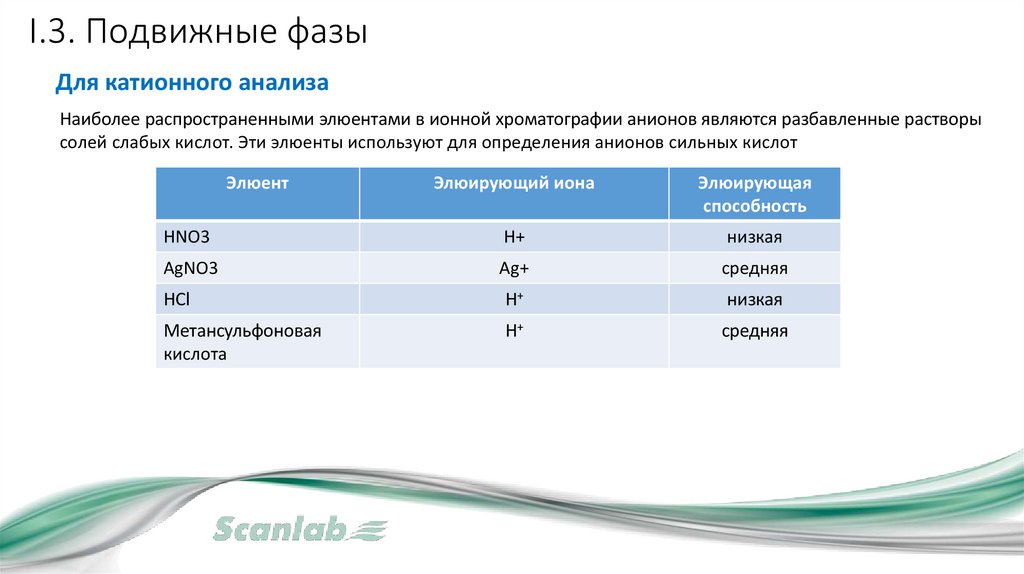
I.3. Подвижные фазыДля катионного анализа
Наиболее распространенными элюентами в ионной хроматографии анионов являются разбавленные растворы
солей слабых кислот. Эти элюенты используют для определения анионов сильных кислот
Элюент
Элюирующий иона
Элюирующая
способность
HNO3
H+
низкая
AgNO3
Ag+
средняя
HCl
H+
низкая
Метансульфоновая
кислота
H+
средняя
24.
2.1 Разделение в колонке и детектированиеПроба
Колонка
Детектор
Из
инжектора
Слив
Аналит (то, что мы ищем в пробах, например: анионы или катионы)
Загрязняющие примеси
Неудерживаемые компоненты, в т.ч. растворитель пробы. Например: вода в ИХ
25.
2.1 Разделение в колонке и детектирование26.
2.1 Защитные предколонки27.
2.1 Защитные предколонкиЗащитная
Проба предколонка
Колонка
Детектор
Из
инжектора
Слив
Аналит (то, что мы ищем в пробах, например: анионы или катионы)
Загрязняющие примеси
Неудерживаемые компоненты, в т.ч. растворитель пробы. Например: вода в ИХ

























 chemistry
chemistry








