Similar presentations:
Растворение веществ в воде. Лабораторный опыт № 5 «Изучение растворимости веществ»
1.
Тема урока: Растворение веществ в воде.Лабораторный опыт № 5 «Изучение
растворимости веществ»
2.
Цели обучения:-классифицировать вещества по растворимости в
воде
-объяснять роль растворов
повседневной жизни
в
природе
и
3.
4.
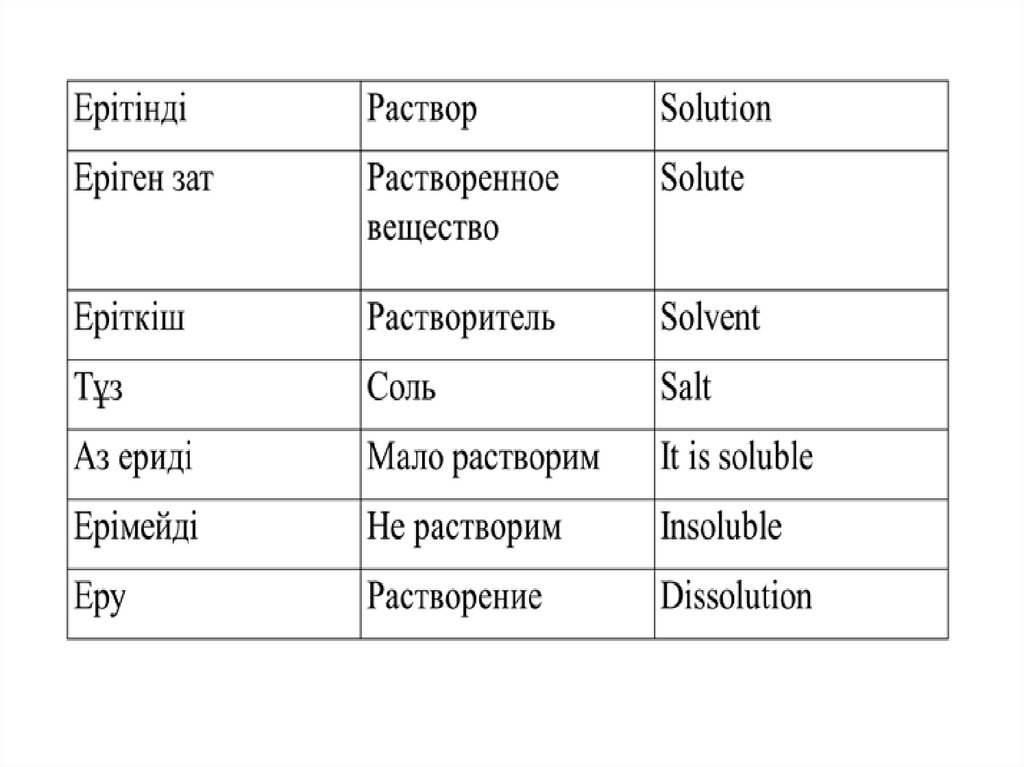
Растворы – однородные системы, состоящиеиз молекул растворителя и частиц
растворенного вещества, между которыми
происходят физические и химические
взаимодействия.
Раствор = Растворитель + Растворенное вещество
5.
РастворениеФизический процесс –
результат диффузии веществ
Химический процесс –
взаимодействие вещества с водой и
образование гидратов
Состав раствора
Растворенное вещество
Растворитель
6.
Растворимость -это способность вещества образовывать
с другими веществами (растворителями)
однородные системы – растворы
7.
Природа растворенного веществаХлорид кальция
CaCl2
Гидроксид кальция
Ca(OH)2
Карбонат
кальция CaCO3
хорошо растворимые
(в 100г H2O
больше
1г вещества)
малорастворимые
(в 100г H2O
меньше
1г вещества)
нерастворимые
(в 100г H2O
меньше 0,01г вещества)
Вещества
РАСТВОРИМОСТЬ НЕКОТОРЫХ СОЛЕЙ В 100 г ВОДЫ ПРИ 20 °С
Хорошо растворимые
Сульфат меди
Нитрат калия
Иодид натрия
CuS04
KN03
Nal
Малорастворимые
22,2
31,6
179,10
Сульфат серебра
Сульфат кальция
Иодид свинца
Практически нерастворимые
Ag2S04
CaS04
Pbl2
0,79
0,20
0,07
Бромид серебра
Хлорид серебра
Иодид серебра
AgBr
AgCl
Agl
0,0037
0,00009
0,000003
8.
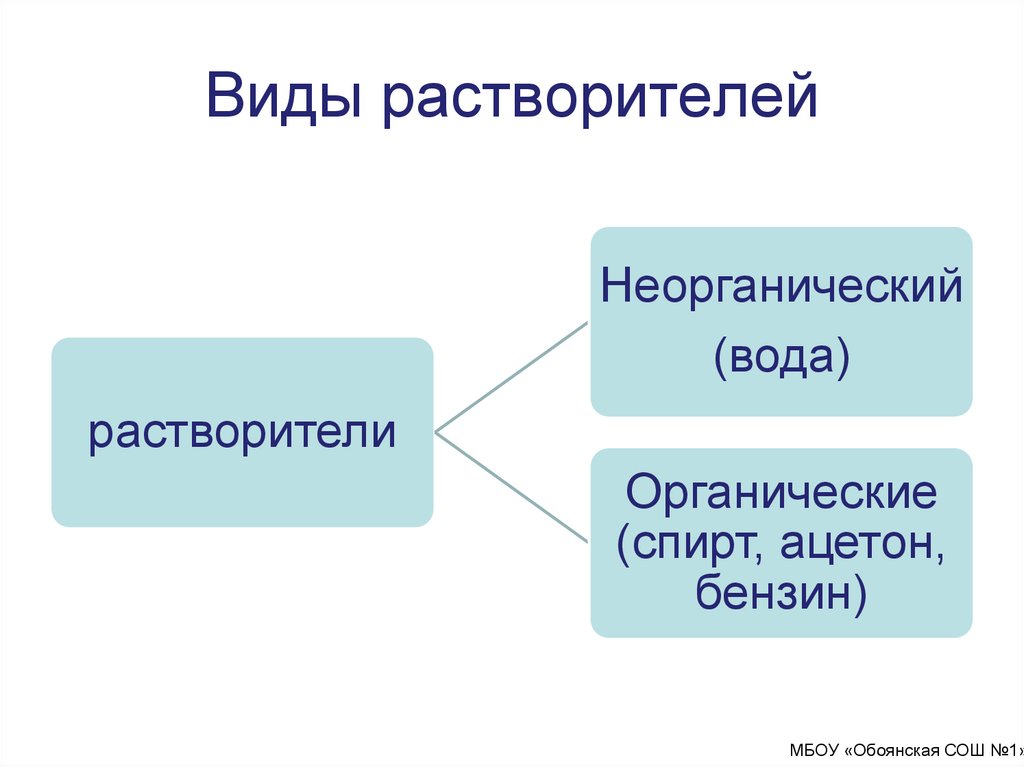
Виды растворителейНеорганический
(вода)
растворители
Органические
(спирт, ацетон,
бензин)
МБОУ «Обоянская СОШ №1»






 chemistry
chemistry








