Similar presentations:
Спирты
1.
2.
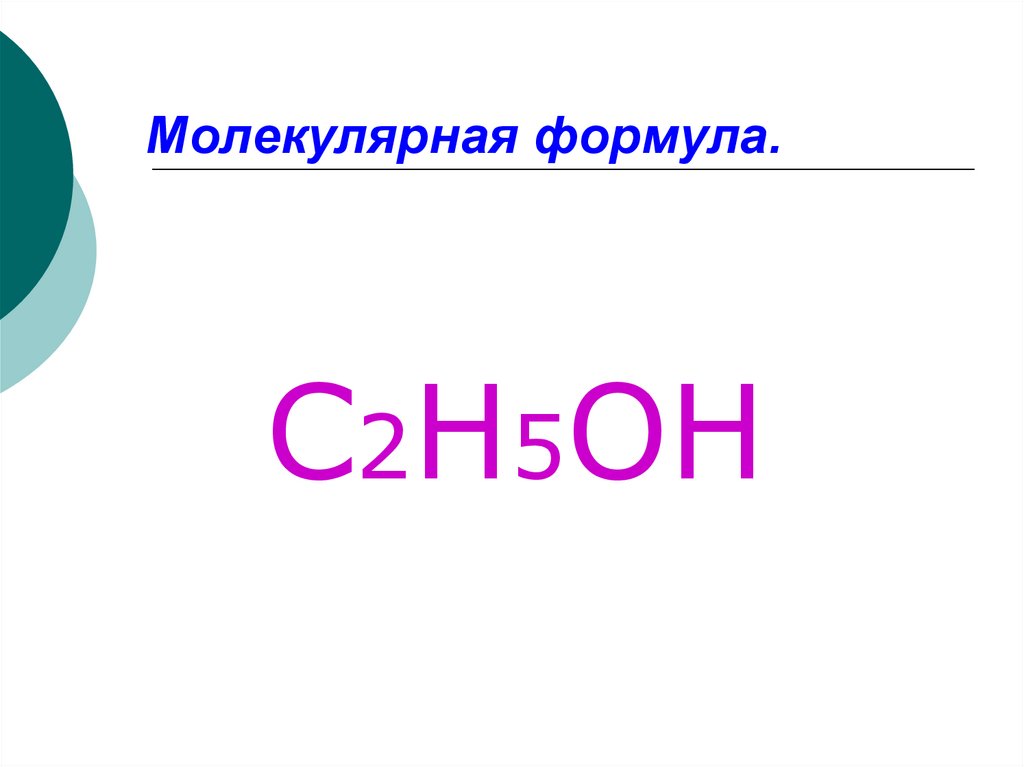
3. Молекулярная формула.
С2Н5ОН4.
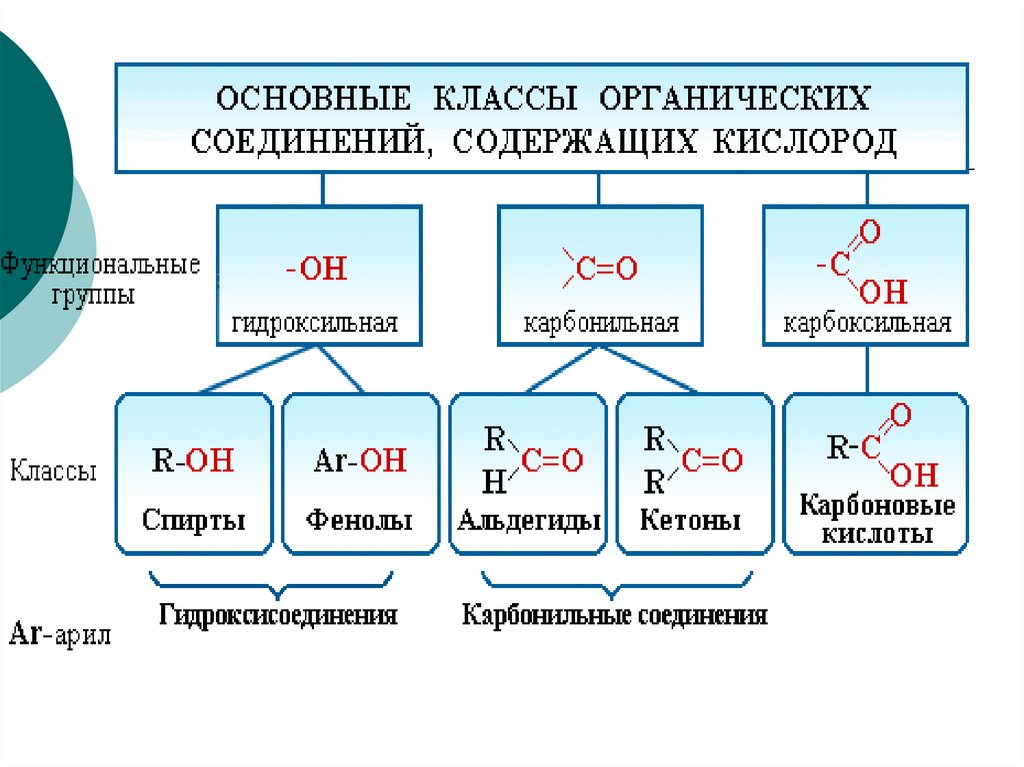
Спирты – это сложныеорганические вещества , в
молекулах которых
углеводородный радикал
связан с гидроксильной
группой –ОН.
5. Физические свойства.
Бесцветная жидкость.Своеобразный запах.
Легче воды.
Хорошо растворим в воде.
6. Общая формула гомологов.
СnH2n+1OH7.
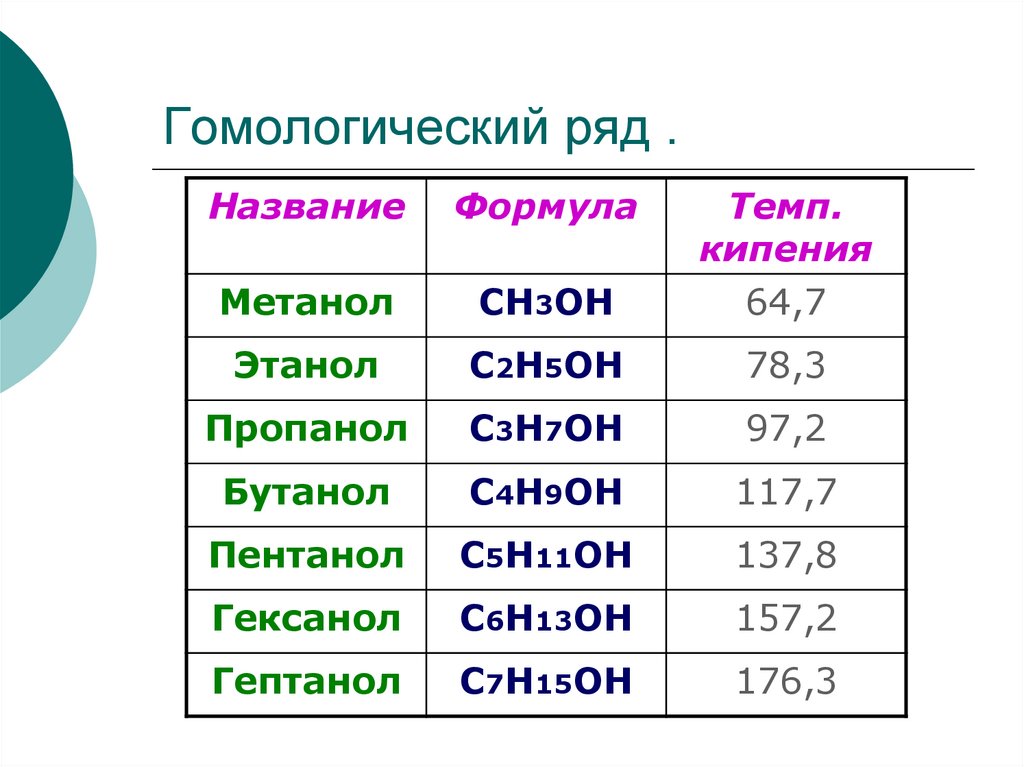
R-OH8. Гомологический ряд .
НазваниеФормула
Метанол
СН3ОН
Темп.
кипения
64,7
Этанол
С2Н5ОН
78,3
Пропанол
С3Н7ОН
97,2
Бутанол
С4Н9ОН
117,7
Пентанол
С5Н11ОН
137,8
Гексанол
С6Н13ОН
157,2
Гептанол
С7Н15ОН
176,3
9. Изомерия.
1. Углеродного скелета.СН3 – СН2 – СН2 – СН2 – ОН
бутанол -1
СН3 – СН – СН2 - ОН
СН3
2-метилпропанол-1
10.
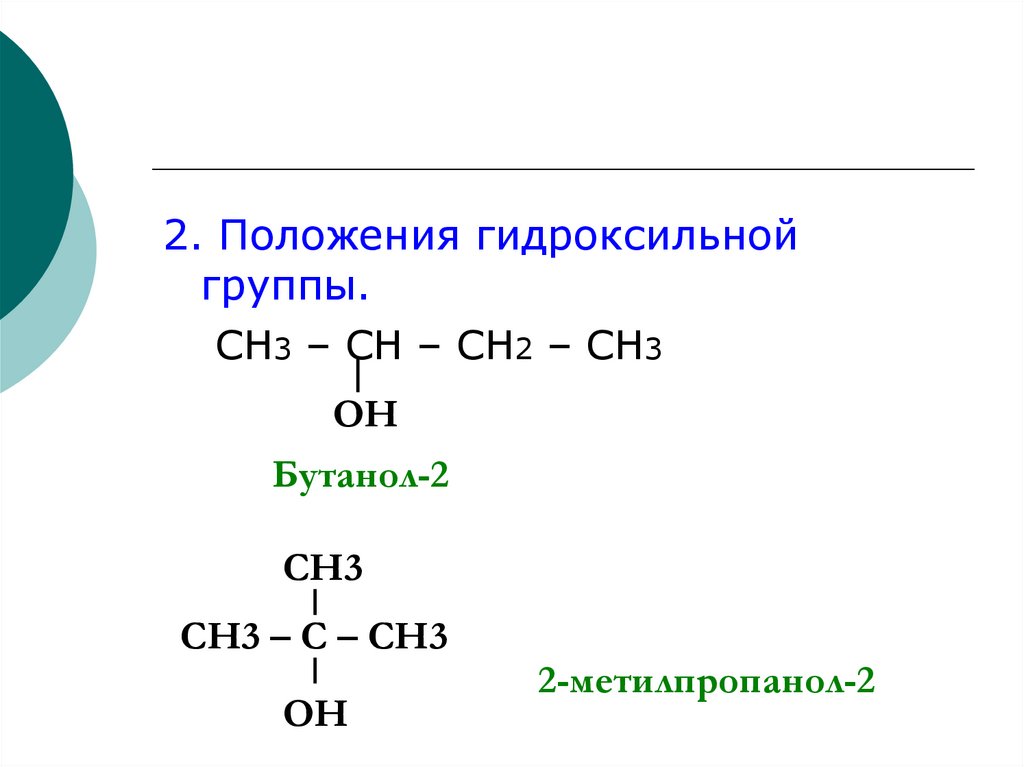
2. Положения гидроксильнойгруппы.
СН3 – СН – СН2 – СН3
ОН
Бутанол-2
СН3
СН3 – С – СН3
ОН
2-метилпропанол-2
11. Составить структурные формулы…
2-метилбутанол-13,3-диметилпентанол-2
2,3-диметилгексанол-2
2-этилгептанол-1
Пентанол-2
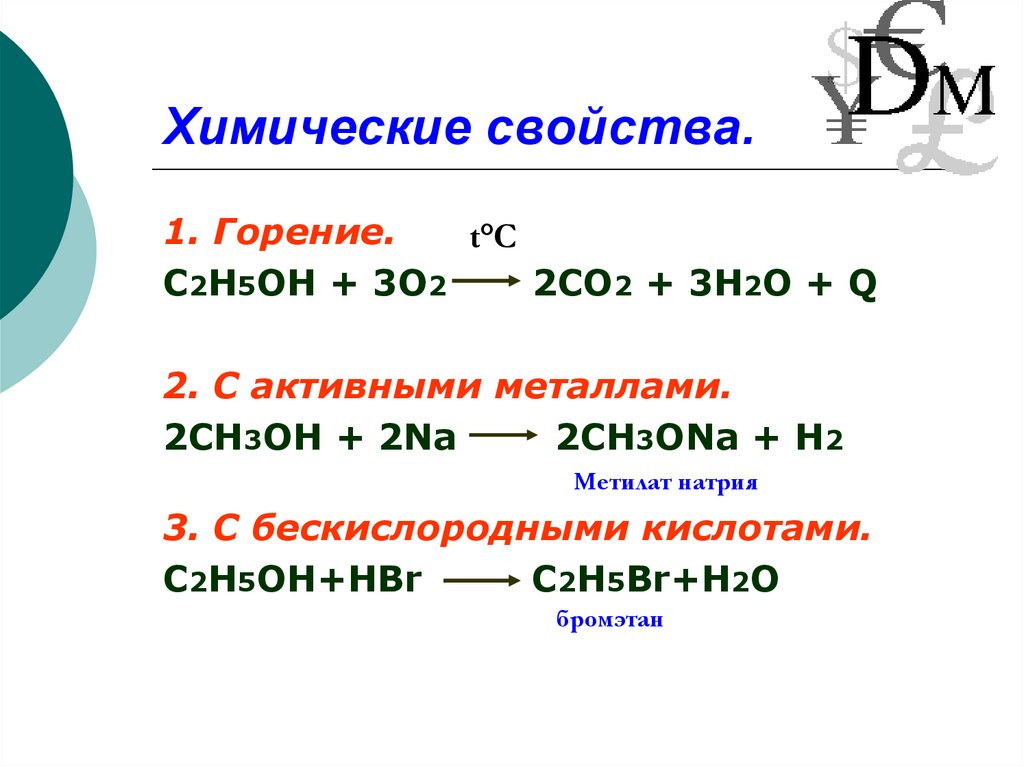
12. Химические свойства.
1. Горение.t°С
С2Н5ОН + 3О2
2СО2 + 3Н2О + Q
2. С активными металлами.
2СН3ОН + 2Na
2CH3ONa + H2
Метилат натрия
3. С бескислородными кислотами.
С2Н5ОН+HBr
C2H5Br+Н2О
бромэтан
13.
4. Дегидратация.С2Н5ОН
С2Н4 + Н2О
этилен
5. Дегидратация в избытке спирта при
+140 градусов.
С2Н5ОН + С2Н5ОН
С2Н5-О-С2Н5 + Н2О
Диэтиловый эфир
14.
Простые эфиры –органические вещества ,
молекулы которых состоят
из двух углеводородных
радикалов , соединённых
посредством атома
кислорода.
15. Применение спиртов.
1.2.
3.
4.
5.
6.
7.
В качестве растворителей.
В химической промышленности.
Для производства каучука.
В фармацевтике.
В медицине.
В пищевой промышленности.
Для производства виноводочных
изделий.
16. Водка – яд для организма.
Берегитесебя и своих
близких.
17.
Из предельныхуглеводородов
СН4
СН3Br
CH3ОН
Из непредельных
углеводородов
С2Н4
С2Н5ОН
18. Промышленный синтез метанола.
Сырьё – синтез-газ.СО + 2Н2
СН3ОН + Q
Условия реакции:
t=+250-300°С
P=10МПа













 chemistry
chemistry








