Similar presentations:
Предмет органической химии
1. Предмет органической химии
Органическая химия вполне можетсвести человека с ума. Она создает у
меня
впечатление
девственного
тропического леса, полного самых
удивительных
вещей;
из
этой
чудовищной и безграничной чащи
невозможно выбраться и в нее страшно
войти.
Ф. Велер
2. Цель урока: выявить причину существования органической химии как самостоятельного раздела химии
Цель урока:урока: выявить
выявить причину
причину
Цель
существования органической
органической химии
химии как
как
существования
самостоятельного раздела
раздела химии
химии
самостоятельного
Результаты
Результаты урока:
урока:
1.
1. Приводить
Приводитьопределения
определенияорганической
органическойхимии.
химии.
2.
2.Перечислять
Перечислятьособенности
особенностисвойств
свойств
органических
органическихвеществ,
веществ,указав
указавих
ихпричину.
причину.
3.
3.Объяснять
Объяснятьпричины
причинымногочисленности
многочисленностиии
многообразия
многообразияорганических
органическихсоединений.
соединений.
4.
4.Раскрывать
Раскрыватьсущность
сущностьопределений
определений«изомеры»
«изомеры»
ии«гомологи».
«гомологи».
5.
5.Раскрывать
Раскрыватьсущность
сущностьдоструктурных
доструктурныхтеорий.
теорий.
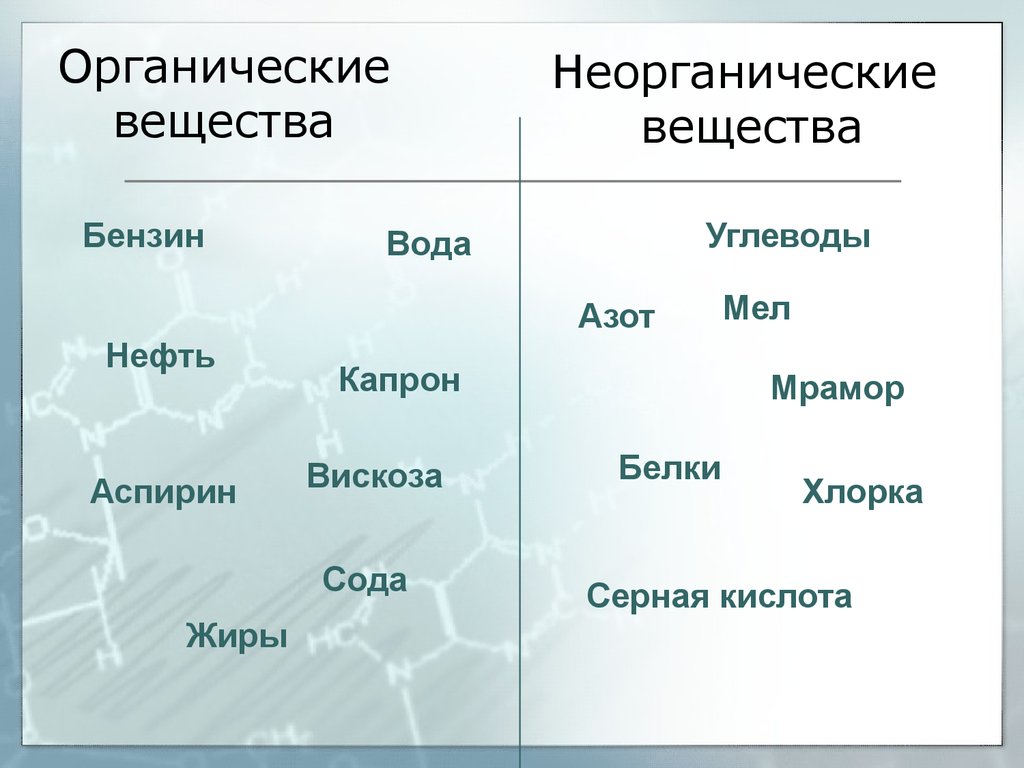
3. Органические вещества
БензинНеорганические
вещества
Углеводы
Вода
Азот
Нефть
Аспирин
Капрон
Вискоза
Сода
Жиры
Мел
Мрамор
Белки
Хлорка
Серная кислота
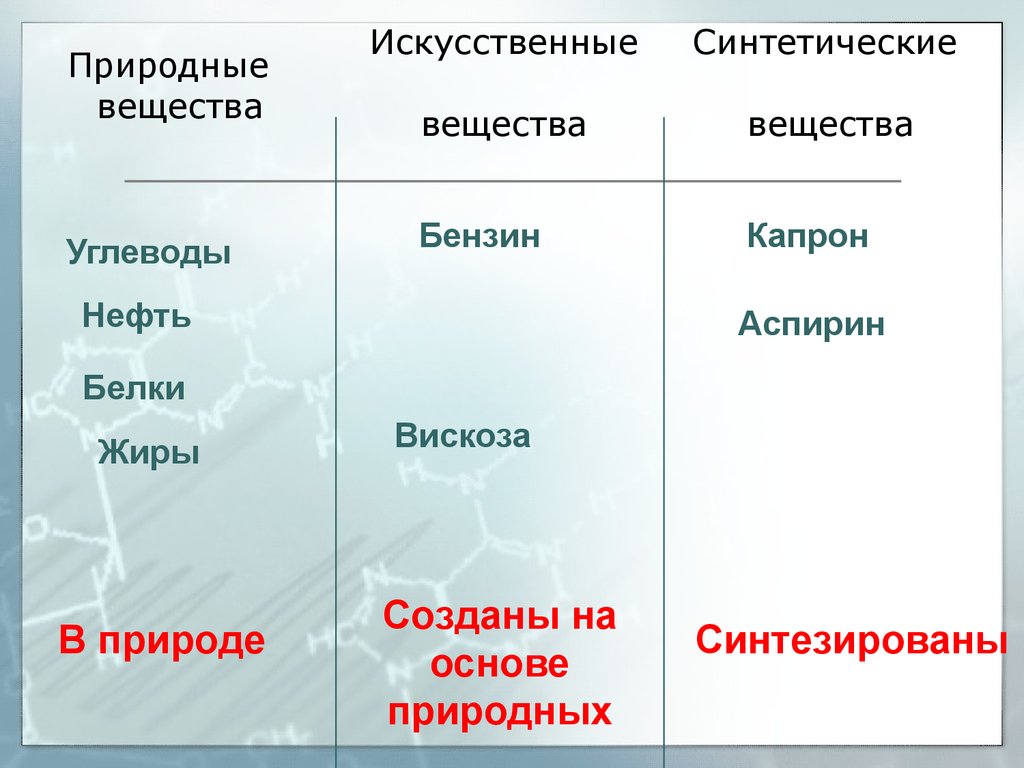
4. Природные вещества
УглеводыИскусственные
Cинтетические
вещества
вещества
Бензин
Капрон
Нефть
Аспирин
Белки
Жиры
В природе
Вискоза
Созданы на
основе
природных
Синтезированы
5.
1807 г. Берцелиус1845 г. Кекуле
1878 г. Шорлеммер
6. Органические вещества
Неорганическиевещества
CH4
C2H5OH
H2
C 2 H2
C6H12O6
H2CO3
C6H5NH2
CH3COOH
NaCl
Fe
Ca(OH)2
CO2
7. Особенности органических веществ
Характерные особенности1. В состав обязательно входят
атомы С и Н
2. Имеют низкие температуры
плавления и кипения
Примечания
Горючесть, обугливание при нагревании
Большинство имеют молекулярную
кристаллическую решетку
3. Большинство нерастворимы в
воде
Большинство образовано ковалентными
малополярными связями
4. Большинство являются
неэлектролитами
Реакции протекают медленно, чаще с
участием катализатора
5. Участники или продукты
процессов в живых организмах
6. Многочисленность
Сложные органические вещества
способны к самоорганизации
Причины:
8. Органические вещества горючи
9. Обугливаются при нагревании
ДревесинаМясо
Сахар
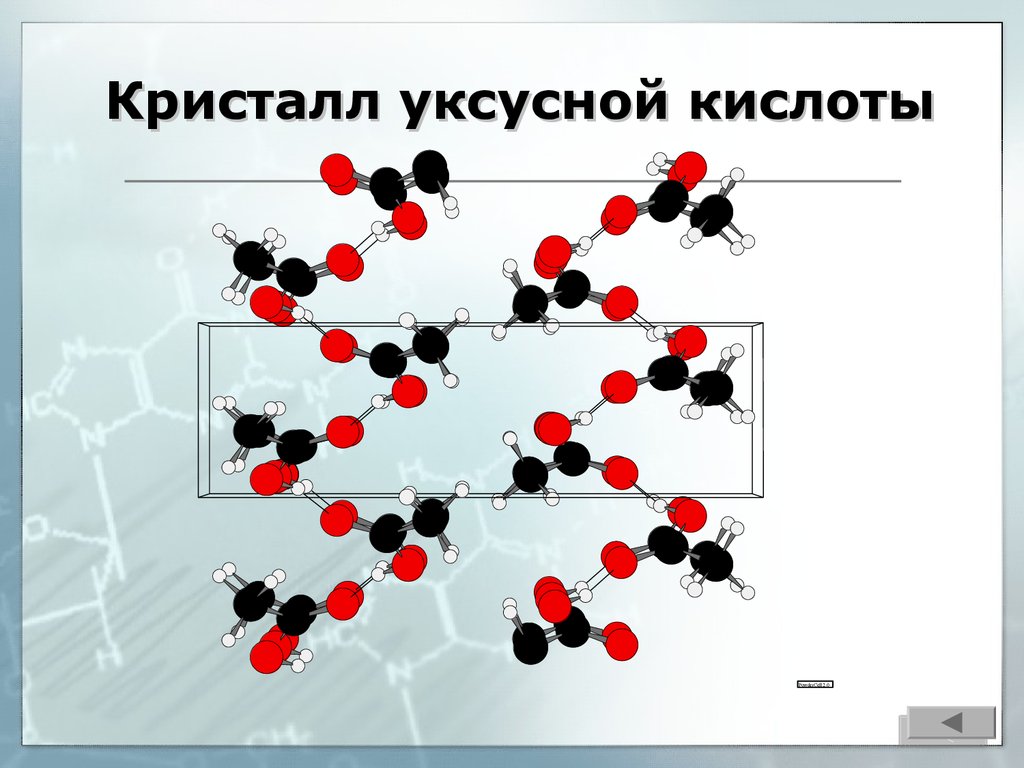
10. Кристалл уксусной кислоты
PowderCell 2.011. Большинство органических веществ не растворимо в воде
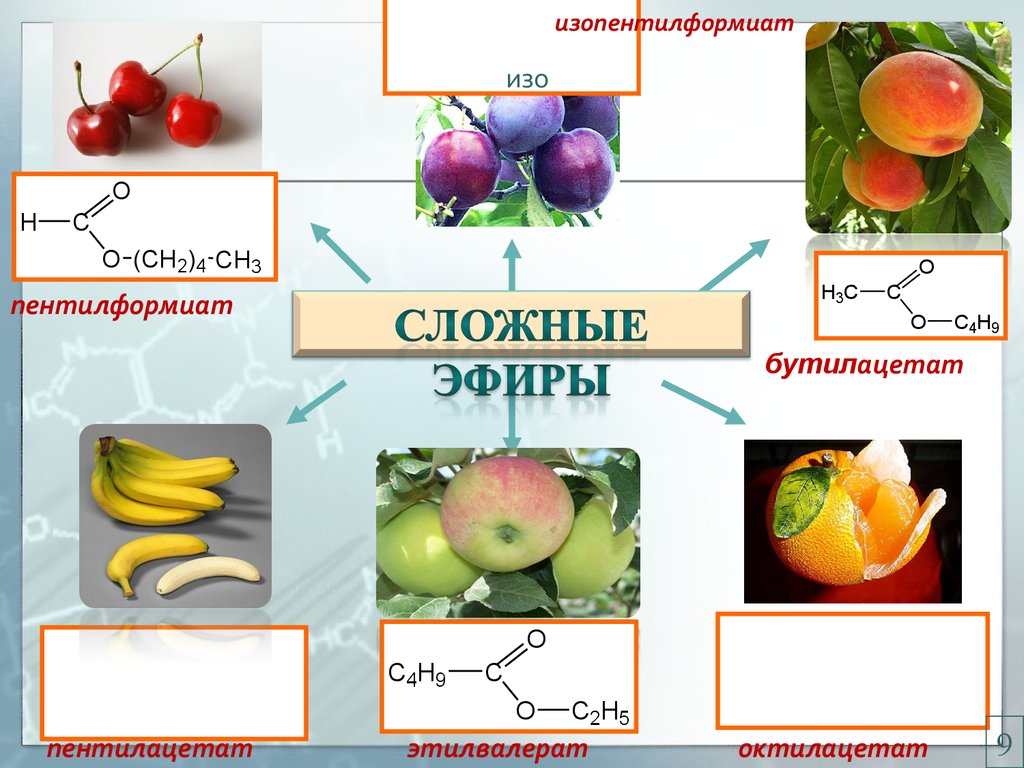
12.
изопентилформиатизо
O
H
C
O (CH2)4 CH3
O
H3C
пентилформиат
C
O
C4H9
бутилацетат
O
C4H9
C
O
пентилацетат
C2H5
этилвалерат
октилацетат
9
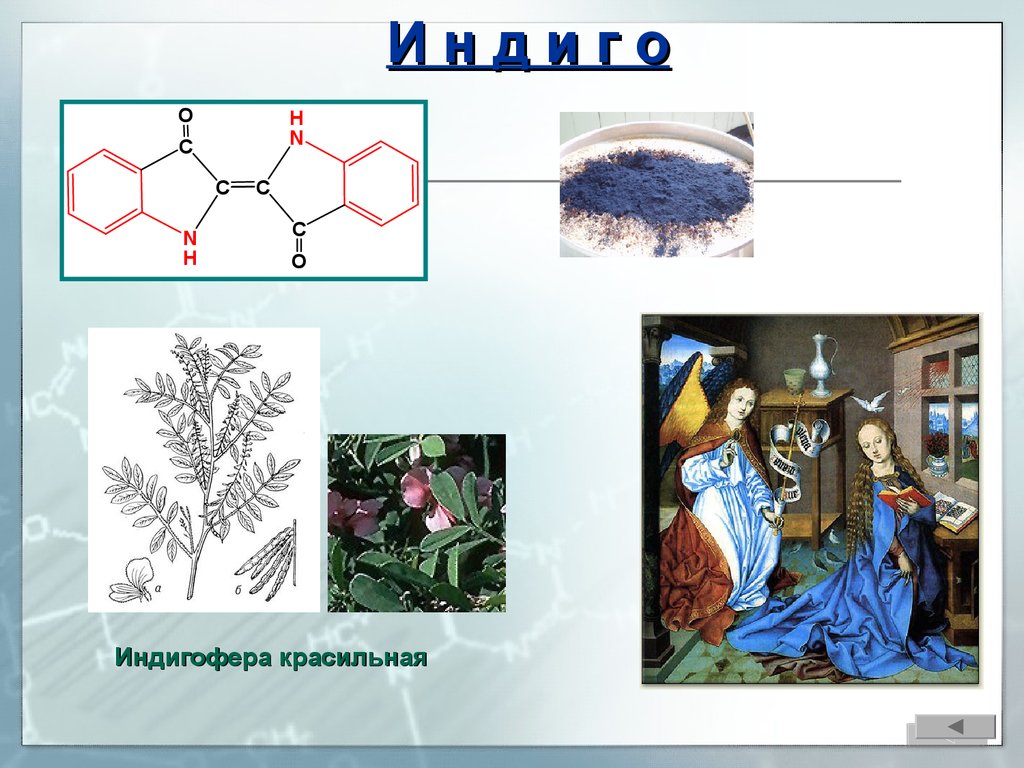
13.
ИндигоO
H
N
C
C
N
H
C
C
O
Индигофера красильная
14. Органические соединения
~ 100 млн.Неорганические соединения
~ 700 тыс.
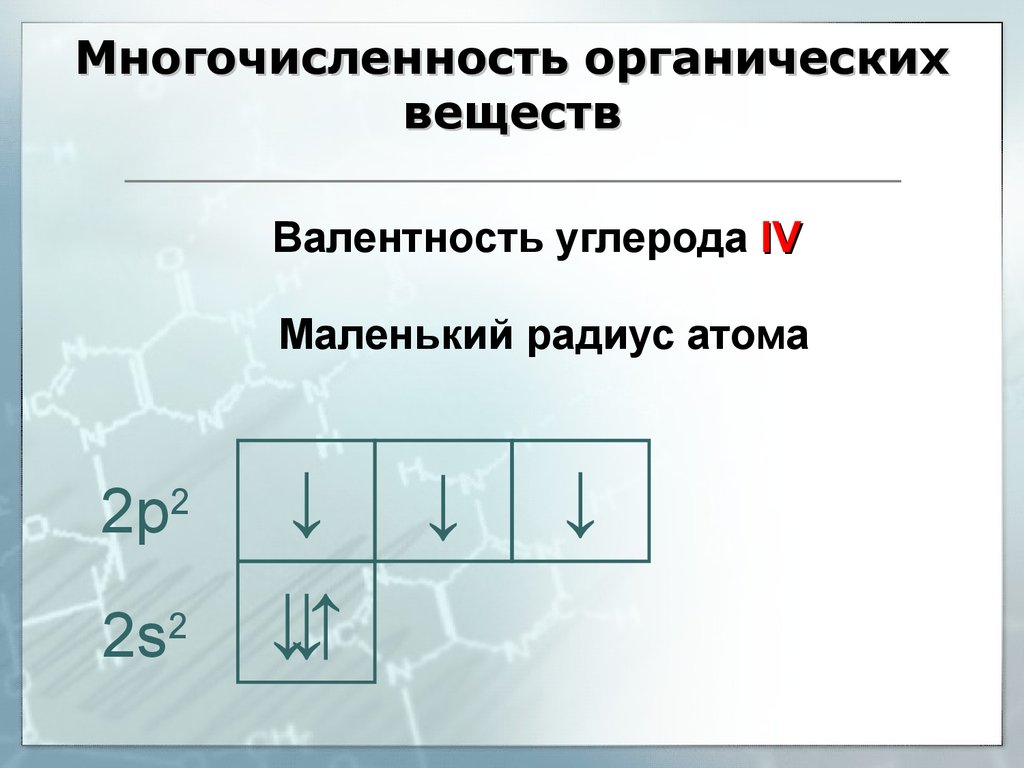
15. Многочисленность органических веществ
Валентность углерода IVМаленький радиус атома
2p2
↓
2s2
↓↑
↓
↓
↓
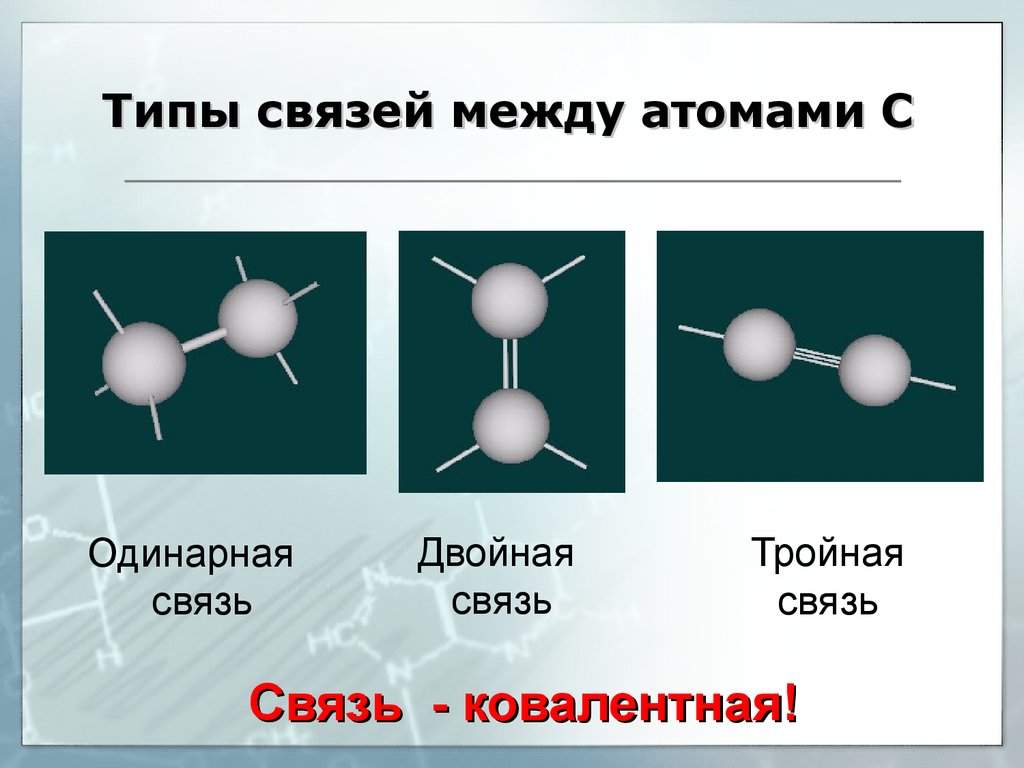
16. Типы связей между атомами С
Одинарнаясвязь
Двойная
связь
Тройная
связь
Связь - ковалентная!
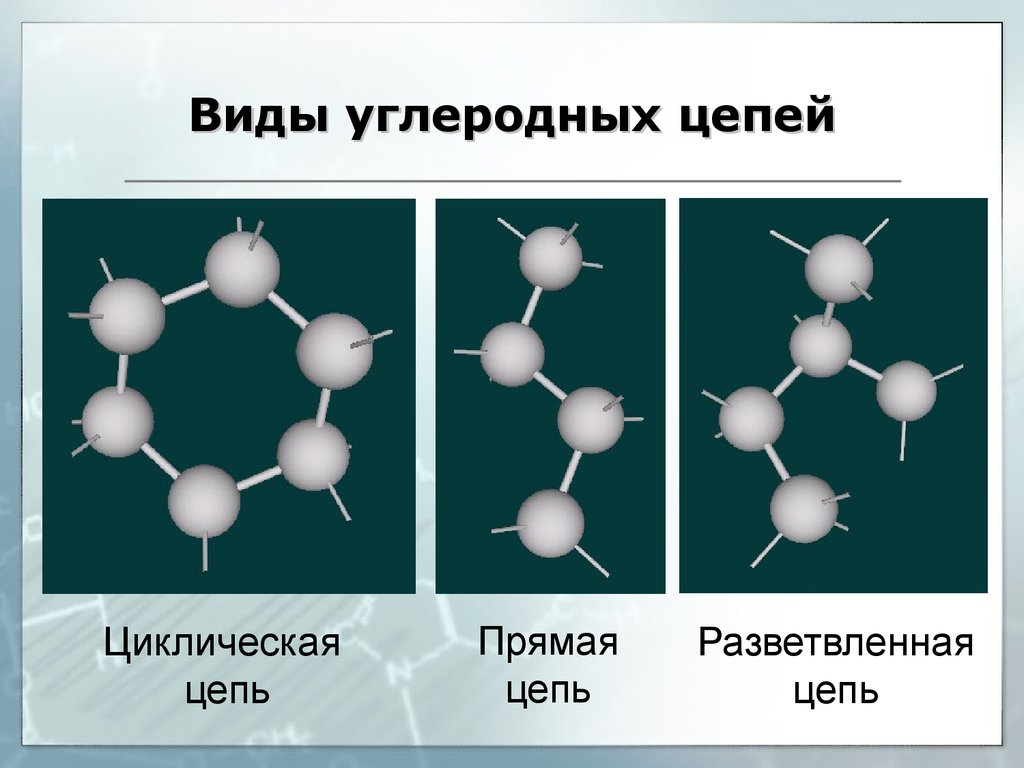
17. Виды углеродных цепей
Циклическаяцепь
Прямая
цепь
Разветвленная
цепь
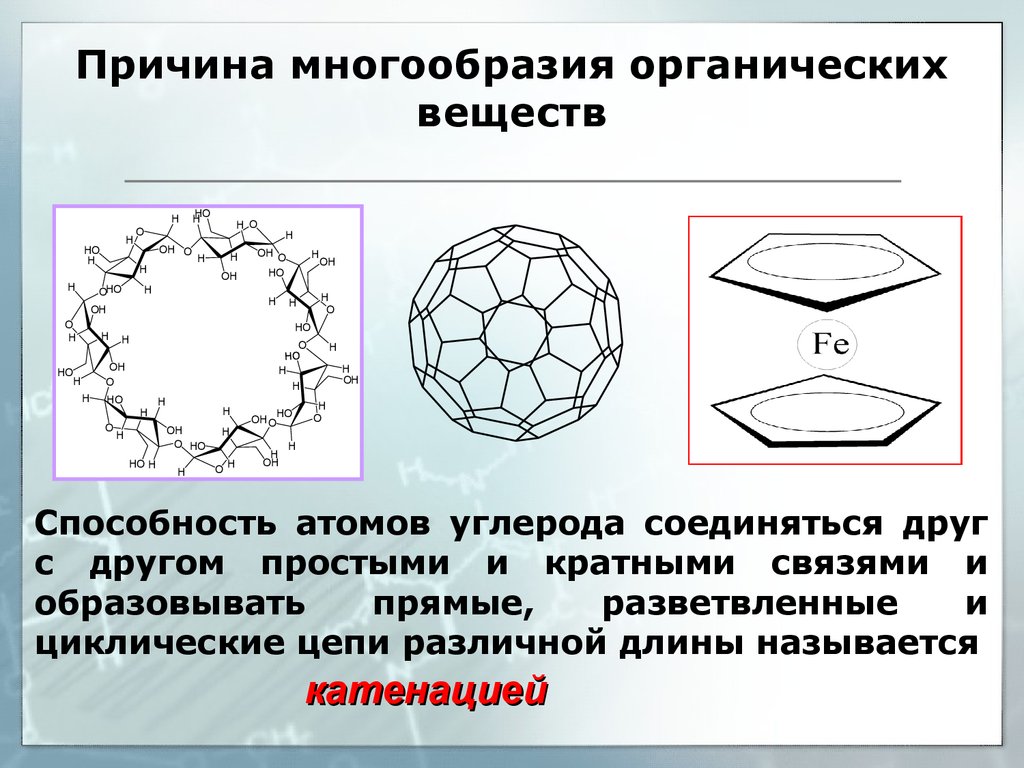
18. Причина многообразия органических веществ
HH
HO
H
H
OH O
H
OHO
HO
H
H O
O
H
H
OH
H
H
OH
O
H
H
H
OH O
HO
H
HO
HO
O
OH
H
O
H
H
O
OH
O
HO
H
H
H
H
OH
H
H
H
H
H
OH
O HO
H
HO H
H
H
O
H
OH O
HO
H
OH
H
O
H
Способность атомов углерода соединяться друг
с другом простыми и кратными связями и
образовывать
прямые,
разветвленные
и
циклические цепи различной длины называется
катенацией
19. ИЗОМЕРИЯ
ПАЛЬТОЛАПОТЬ
АПЕЛЬСИН
СПАНИЕЛЬ
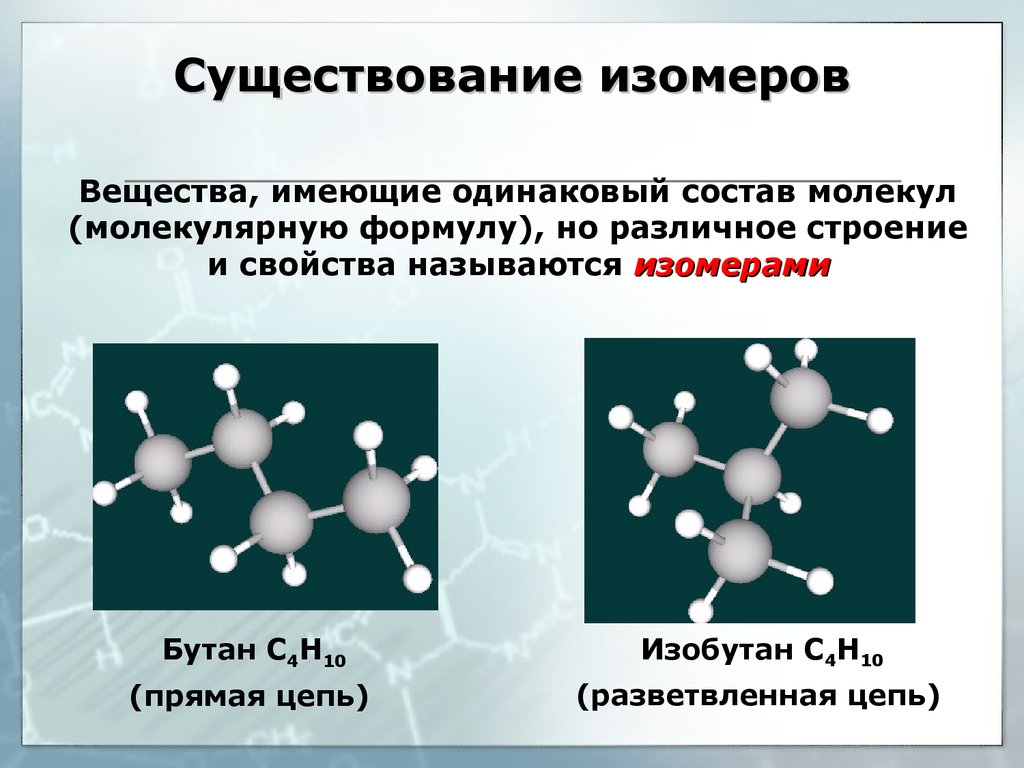
20. Существование изомеров
Вещества, имеющие одинаковый состав молекул(молекулярную формулу), но различное строение
и свойства называются изомерами
Бутан С4Н10
Изобутан С4Н10
(прямая цепь)
(разветвленная цепь)
21. Изомерия - явление существования изомеров
Молекулярнаяформула
Число возможных
изомеров
С6Н12
5
С10Н22
75
С14Н30
1858
С20Н44
366 319
22. Существование гомологов
Молекулярные формулы первых представителейгомологических рядов предельных углеводородов и
предельных одноатомных спиртов
СН4
+ СН2
СН3ОН
С2Н6
+ СН2
С2Н5ОН + СН
С3Н8
+ СН2
С3Н7ОН
С4Н10
+ СН2
С4Н9ОН + СН
+ СН2
2
+ СН2
2
Вещества, имеющие одинаковый качественный состав, сходное
строение и свойства, отличающиеся на одну или несколько
гомологических разниц - гомологи
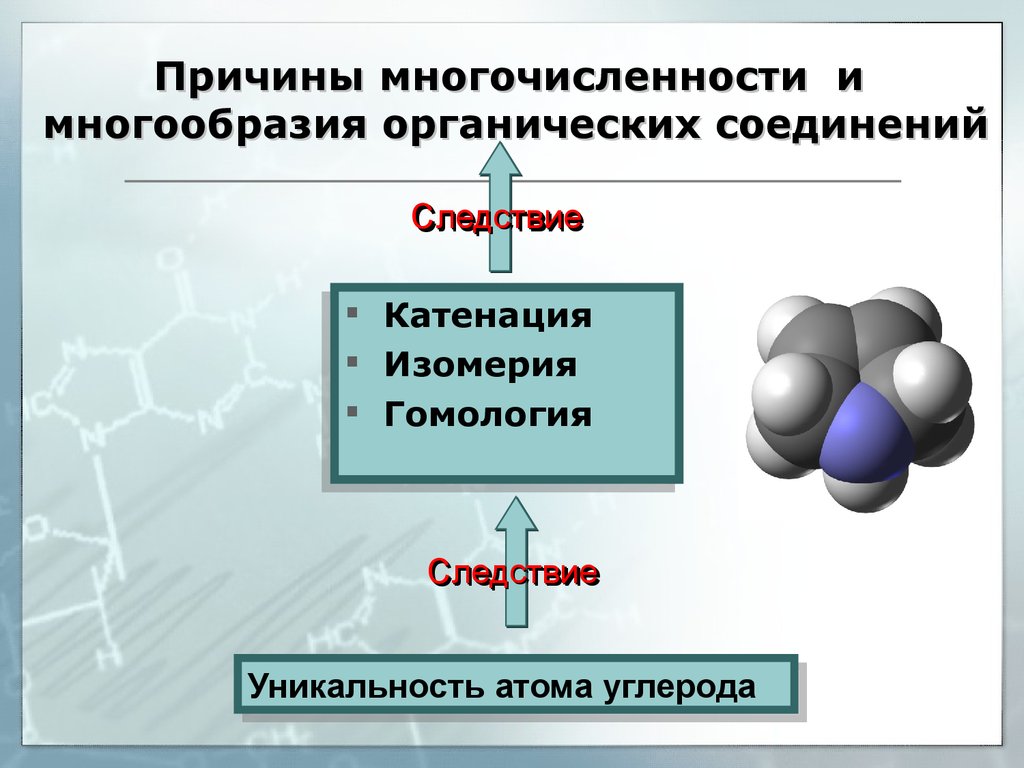
23. Причины многочисленности и многообразия органических соединений
СледствиеКатенация
Катенация
Изомерия
Изомерия
Гомология
Гомология
Следствие
Уникальность
Уникальность атома
атомауглерода
углерода
24.
Основные классы органическихвеществ
6
C
УГЛЕРОД
12,011
CH4
O
CH3-CH2-CH3
CH2 C
OH
NH2
CH3─CH2─NO2
H2C=CH─CH2─CH3
HC≡C─CH2─CH3
H2C=CH─CH=CH2
CH3─CH2─NH2
CH3
H3C
C
O
CH2
CH3
CH3
O
O
CH3 C
CH3─CH2─OH
OH
H3C
C
CH3
O
O
CH3 C
H
OH
H3C-O-CH3
25. Первые попытки объяснения строения органических веществ
26. Теория витализма
Название образовано от словосочетания“Vis vitalis”-(Лат.)- жизненная сила.
Теория, основанная на предположении о
том, что для синтеза органического
вещества нужна часть живого организма.
Сторонниками этого учения были многие
учёные 19 века.
27. Теория радикалов
Ю. ЛибихФ. Велер
Я. Берцелиус
Все молекулы состоят из двух частейположительно заряженного радикала и
отрицательно заряженной частицы.
+:
Существование устойчивых группировок
атомов- радикалов, переходящих в
неизменном виде из одного соединения в
другое.
-:
Абсолютная неизменность и
самостоятельное существование
радикала.
Упрощённое представление о полярности
молекулы.
Противоречие с теорией замещения.
28. Теория типов
Ш. ЖерарО. Лоран
Существует несколько типов, на
которые классифицируют
вещества
+:
Формула и классификация близки
к современным.
-:
Допускалась множественность
формул одного вещества.
Внутреннее строение молекул
признавалось принципиально
непознаваемым.
29. Домашнее задание
§ 1, записи в тетрадиПринести тетрадь 12 л в обложке для
практических работ.
Готовиться к самостоятельной экспресс-работе.
30. Экспресс-работа
ВопросБаллы
1. В чем причина особенностей свойств органических
веществ? Конкретизируйте.
3 балла
2. Как доказать, что предлагаемые вещества
являются изомерами?
2 балла
3. Почему теория радикалов и теория типов являются
доструктурными теориями?
3 балла
4. Чем можно объяснить многообразие и
многочисленность органических веществ?
2 балла
5. Как доказать, что выданное вещество относится к
органическим веществам?
1 балл
6. Приведите примеры изомеров и гомологов
2 балла
7. Обоснуйте несостоятельность определений
органической химии, предложенных Берцеллиусом и
Кукуле
2 балла
8. Приведите примеры, доказывающие явление
катенации
2 балла
31. Цель: понимание сущности и методологического значения теории органических веществ А.М. Бутлерова
Цель:Цель: понимание
понимание сущности
сущности ии методологического
методологического
значения
значения теории
теории органических
органических веществ
веществ А.М.
А.М.
Бутлерова
Бутлерова
Результаты урока
1. Перечислять
Перечислятьпредпосылки
предпосылки создания
созданиятеории
теориистроения
строения
1.
органическихвеществ.
веществ.
органических
2. Объяснять
Объяснятьиииллюстрировать
иллюстрироватьпримерами
примерами основные
основные
2.
положениятеории
теориистроения
строенияорганических
органическихвеществ
веществА.М.
А.М.
положения
Бутлерова.
Бутлерова.
3. Раскрывать
Раскрыватьметодологическое
методологическоезначение
значение теории
теорииА.М.
А.М.
3.
Бутлерова
Бутлерова
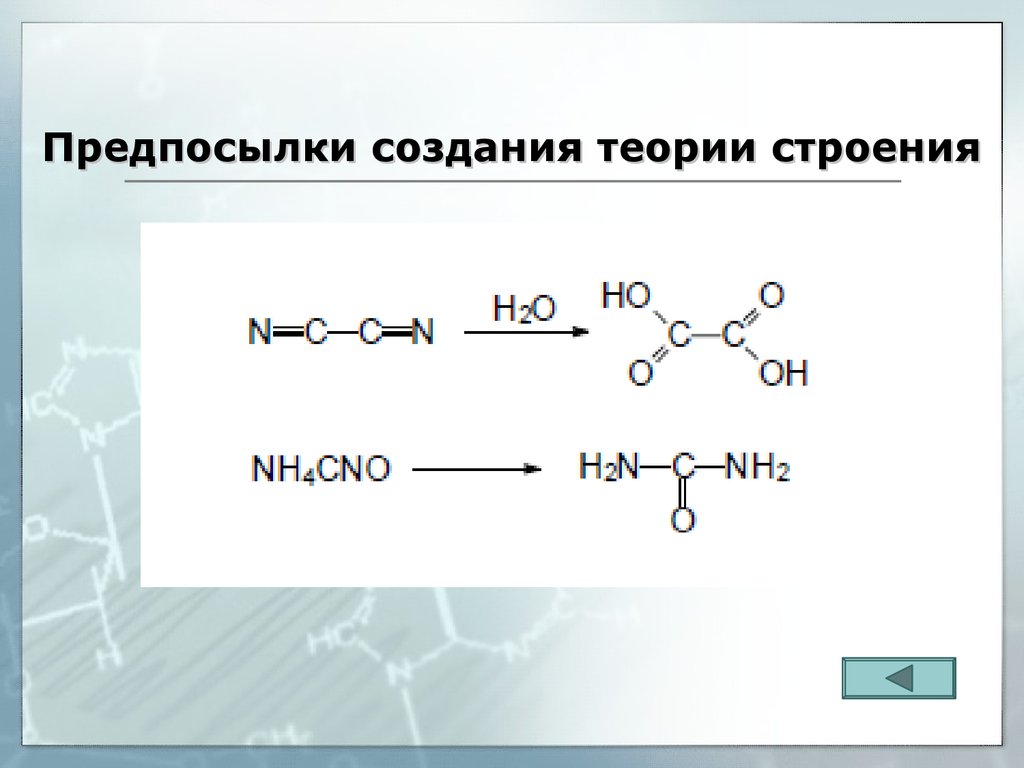
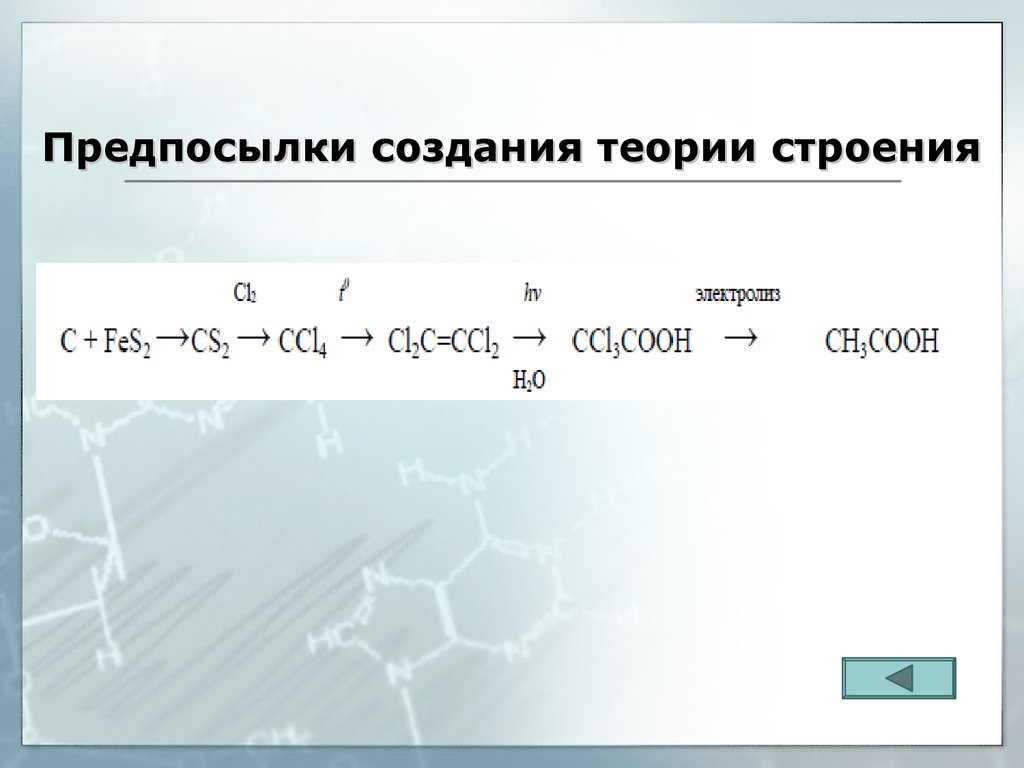
32. Предпосылки создания теории строения
ТеоретическиеЭкспериментальные
Доструктурные теории
1824 г – синтез щавелевой
кислоты Ф.Велер
1830 г – Й. Берцелиус ввел понятие
«изомерии»
1828 г – синтез мочевины Ф.
Велер
1852 г. – Э. Франкланд открыл
валентность
1842 г – синтез анилина Н.Н.
Зинин
1857 г. – А. Кекуле развил
представление о
четырехвалентности С
1845 г – синтез уксусной
кислоты А.Кольбе
1858 г. – Ф. Кекуле и А. Купер
1854 г – синтез жира М.
сделали вывод о возможности С–С Бертло и А. Шарль
1860 г. – атомно-молекулярное
учение на съезде химиков в
Карлсруэ
1861 г – синтез сахаристого
вещества А.М. Бутлеров
Личностные качества А.М. Бутлерова
33. Предпосылки создания теории строения
34. Предпосылки создания теории строения
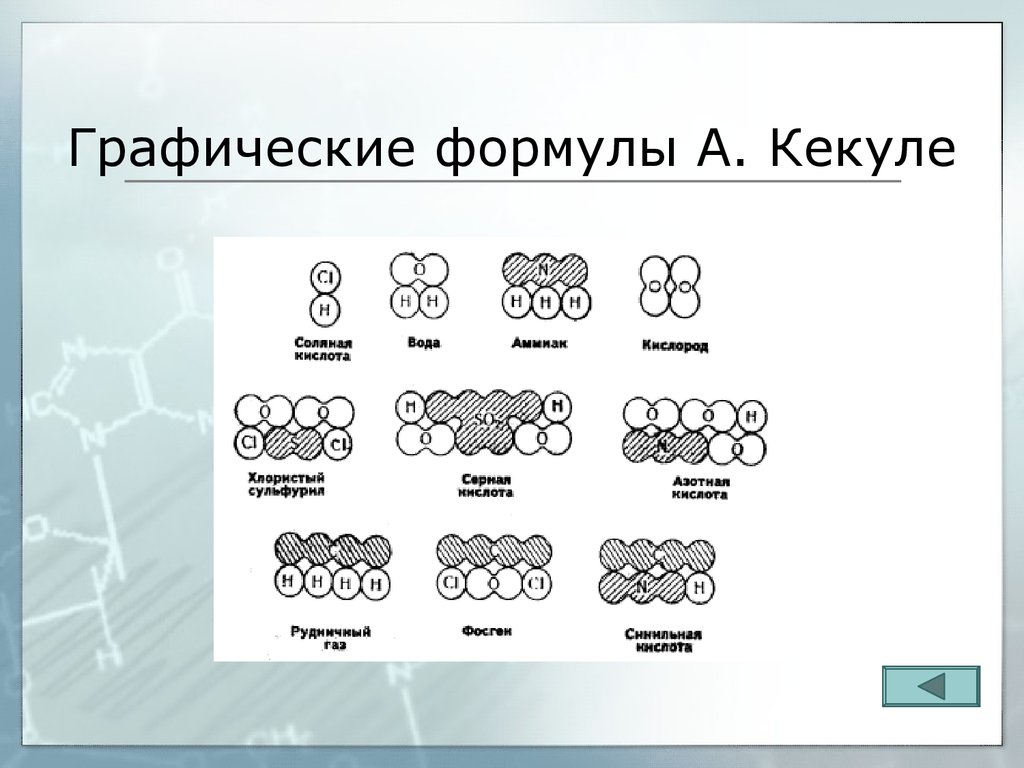
35. Графические формулы А. Кекуле
36. Химические формулы А. Купера
37.
1861 г. А.М. БутлеровСъезд немецких
естествоиспытателей г. Карлсруэ
«Исходя из мысли, что каждый химический атом, входящий в
состав тела, принимает участие в образовании этого
последнего и действует здесь определенным количеством
принадлежащей ему химической силы (сродства), я называю
химическим строением распределение действия этой силы,
вследствие которого химические атомы, посредственно или
непосредственно влияя друг на друга, соединяются в
химическую частицу».
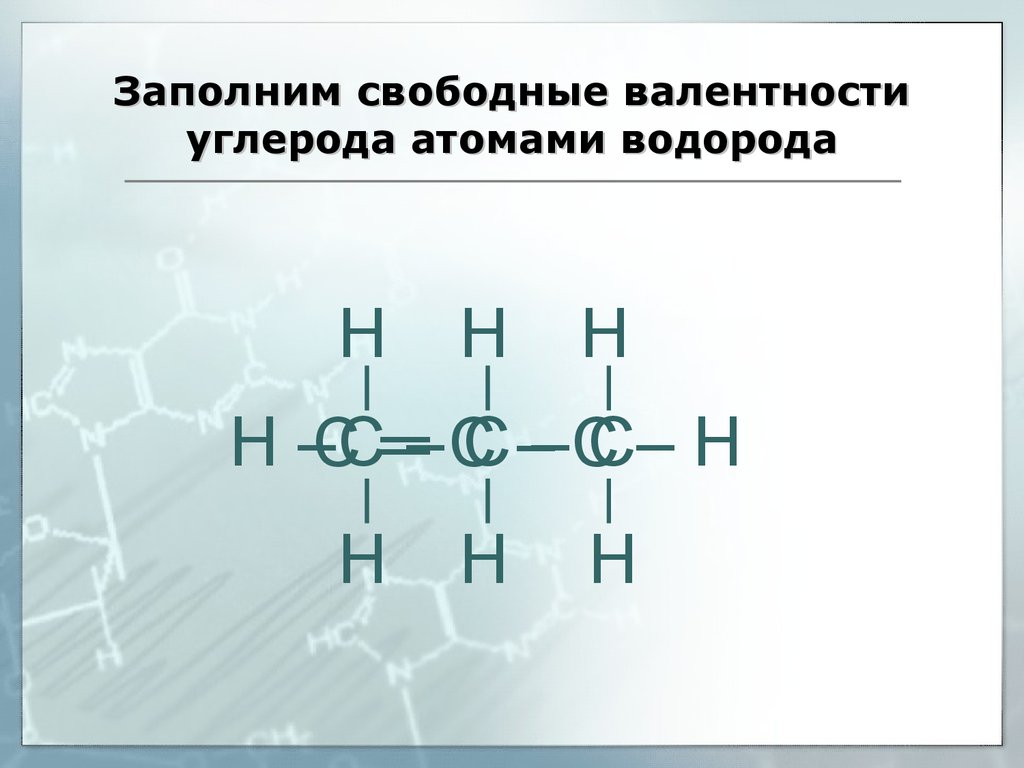
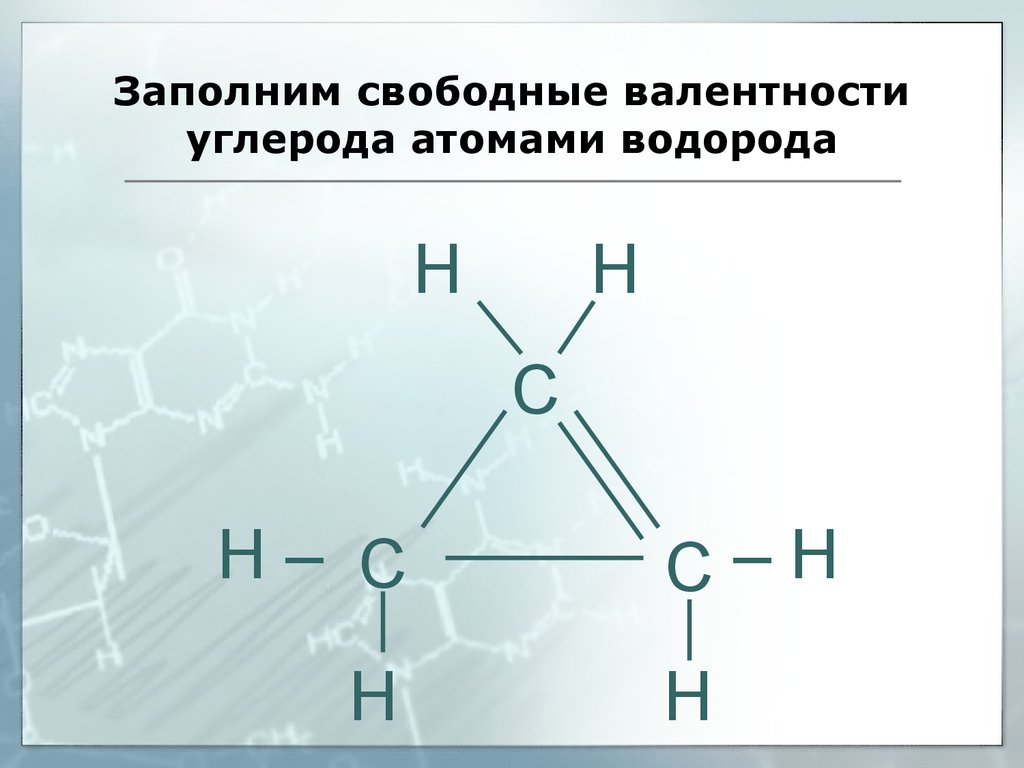
38. Заполним свободные валентности углерода атомами водорода
НН
Н
Н –СС═– С
С –– СС– Н
Н
Н
Н
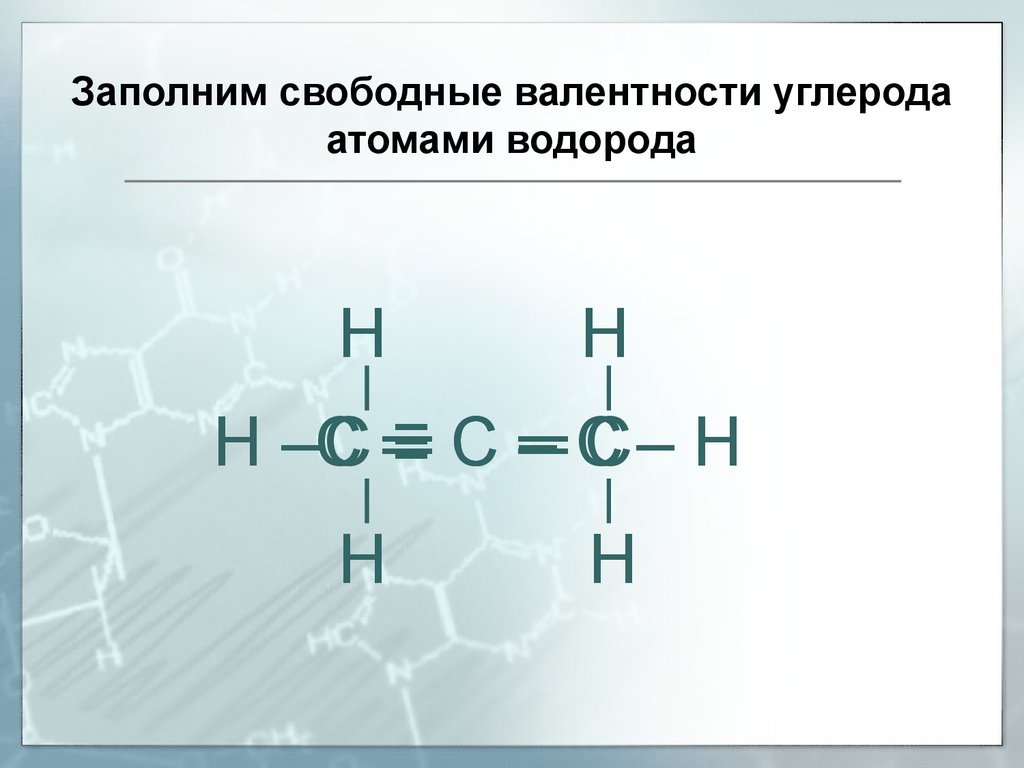
39.
Заполним свободные валентности углеродаатомами водорода
Н
Н
Н –С
С═
≡С–
═С
С– Н
Н
Н
40.
Заполним свободные валентностиуглерода атомами водорода
Н
Н
С
Н– С
Н
С–Н
Н
41.
1861 г. А.М. Бутлеров«Всякое органическое соединение имеет
единственную(!)
химическую
формулу,
отражающую порядок связывания атомов в
молекуле и определяющую его свойства (!!)».
Свойства веществ определяются
их
строением и наоборот, зная строение, можно
прогнозировать свойства
Состав
Строение
Свойства
42. Идентификация, установление состава и строения
1.Элементный анализ – определение содержания
атомов различных элементов.
2. Измерение физических свойств – плотности,
температуры плавления, показателя преломления.
3. Физические методы.
а) Спектроскопия:
ИК – идентификация функциональных групп по
частотам колебаний;
ЯМР – определение числа структурно различных
атомов по их поведению в постоянном магнитном
поле.
б) Масс-спектрометрия. Измерение молекулярных масс
фрагментов молекулы.
43. Луи Пастер: исследования 1848-1854 гг.
HOO C-CH(OH)-CH( OH) -CO OHДве формы винной кислоты идентичны по
всем свойствам, исключая:
(1) способности отклонять плоскость
поляризации плоско поляризованного
света
(2) усваиваться микроорганизмами
Оптическая изомерия
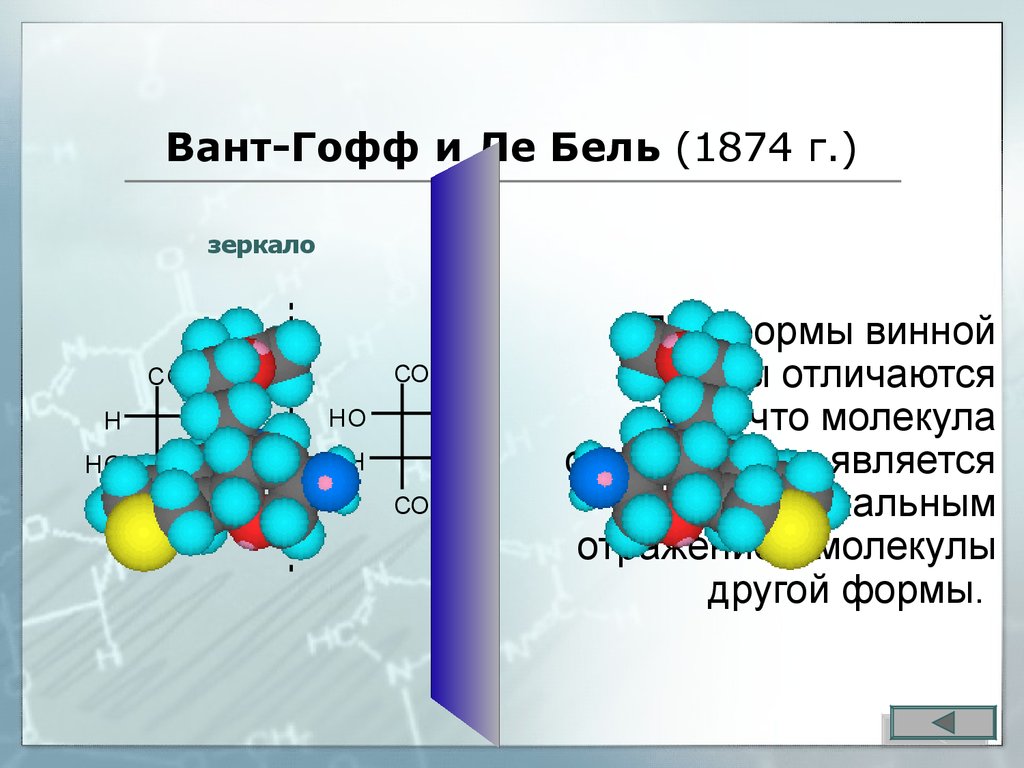
44. Вант-Гофф и Ле Бель (1874 г.)
зеркалоCO OH
COOH
H
HO
OH
H
COOH
HO
H
H
OH
CO OH
Две формы винной
кислоты отличаются
тем, что молекула
одной формы является
зеркальным
отражением молекулы
другой формы.
45.
«когда четыре сродства атома углерода насыщенычетырьмя различными одновалентными группами,
можно получить два и только два различных
тетраэдра, относящихся друг к другу как предмет и
его зеркальное отражение».
46. Л. Полинг «Теория резонанса»
все молекулы имеют одинаковую геометрию и электроннуюструктуру, но эта последняя такова, что не может быть
представлена какой-либо одной валентной схемой с
локализованными связями. Однако ее можно достаточно
хорошо представить усреднением двух этих схем, взятых с
определенными статистическими весами. Можно сказать, что
основное состояние молекулы будет соответствовать
«резонансу» между структурами А и В, которые мы
будем именовать «резонансными структурами».
47. Домашнее задание
1.Приготовиться кк устномуустному ответу
ответу
1.Приготовиться
по материалам
материалам урока
урока
по
2. Приготовиться
Приготовиться кк сам.
сам. работе
работе
2.
3.Задачи
3.Задачи
48. Состав органических веществ
2CuOС → CO2 + 2Cu
CuO + ...
Cu






























 chemistry
chemistry








