Similar presentations:
Сильные и слабые электролиты. Кислотность среды. 9 класс
1.
11.11.2020Сильные и слабые электролиты
2.
Цель: уметь раскрывать смысл понятий «сильныйэлектролит», «слабый электролит».
3.
Кто такие электролиты?Электролиты – это вещества, растворы или расплавы которых
проводят электрический ток,
в следствие того, что диссоциируют (распадаются на ионы)
Вещества каких классов являются электролитами?
Кислоты, основания, соли
Какие из них слабые, а какие сильные электролиты?
4.
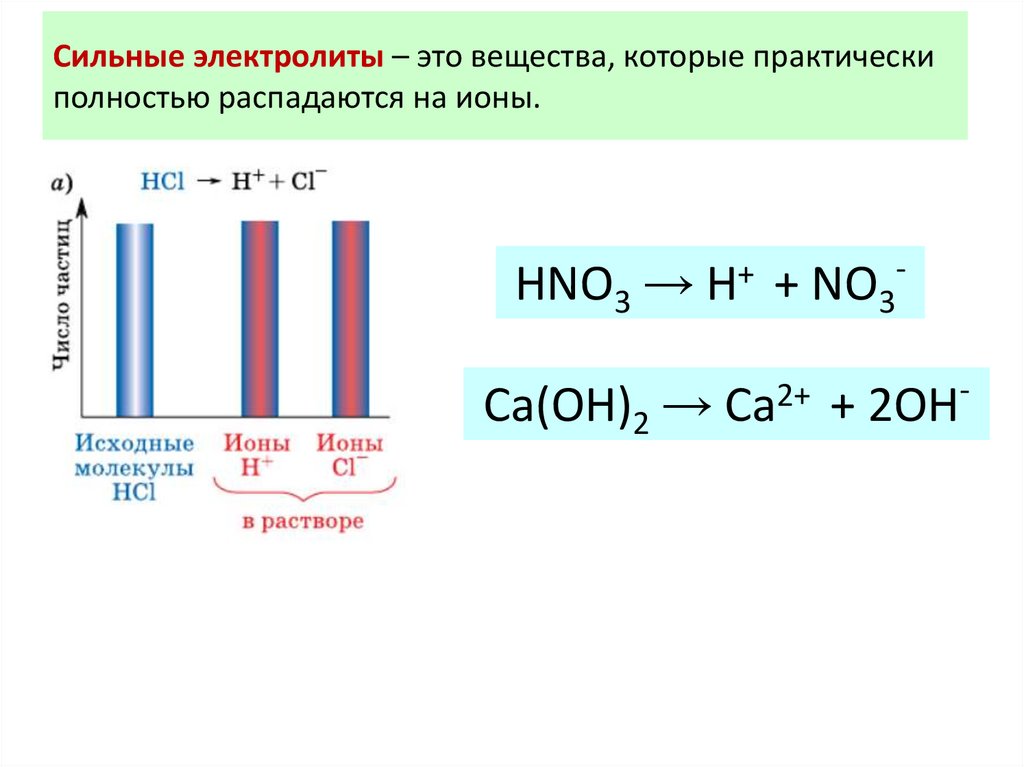
Сильные электролиты – это вещества, которые практическиполностью распадаются на ионы.
HNO3 → H+ + NO3-
Ca(OH)2 →
Ca2+
-
+ 2OH
5.
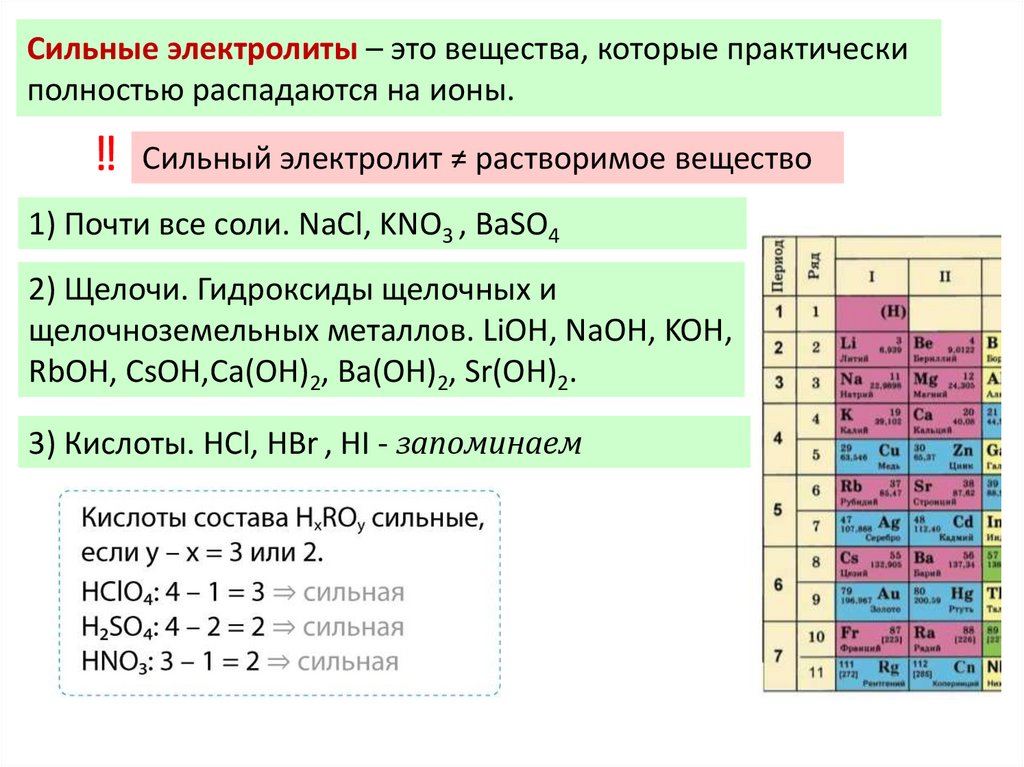
Сильные электролиты – это вещества, которые практическиполностью распадаются на ионы.
‼
Сильный электролит ≠ растворимое вещество
1) Почти все соли. NaCl, KNO3 , BaSO4
2) Щелочи. Гидроксиды щелочных и
щелочноземельных металлов. LiOH, NaOH, KOH,
RbOH, CsOH,Ca(OH)2, Ba(OH)2, Sr(OH)2.
3) Кислоты. НCl, НBr , НI - запоминаем
6.
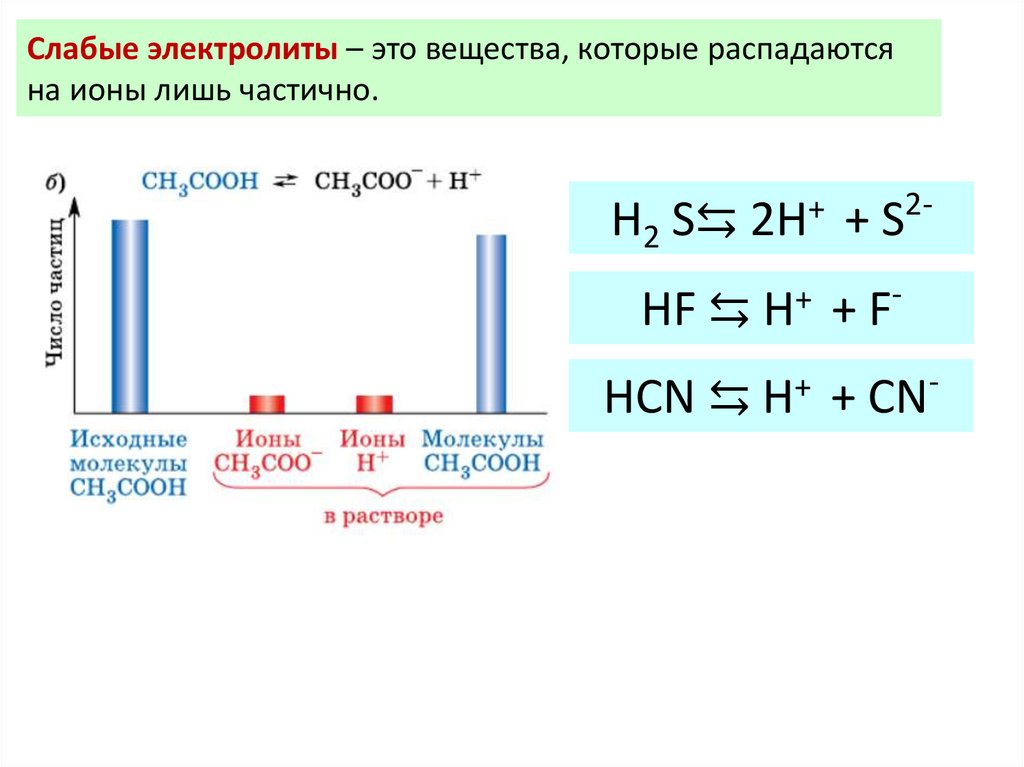
Слабые электролиты – это вещества, которые распадаютсяна ионы лишь частично.
H2 S⇆
2H+
HF ⇆
H+
+S
+F
2-
-
HCN ⇆ H+ + CN-
7.
Слабые электролиты – это вещества, которые распадаютсяна ионы лишь частично.
1) Вода
2) Нерастворимые в воде основания. Сu(OH)2 , Fe(OH)2 .
Амфотерные гидроксиды Zn(OH)2 , Al(OH)3 , Fe(OH)3 .
3) Водный раствор аммиака NH3
4) Все кислоты, что не вошли в группу сильных
8.
Степень диссоциацииэто отношение количества вещества, распавшегося на
ионы, к общему количеству растворенного вещества.
α=
ν
νобщ
α=
ν
νобщ
∙ 100%
У сильных электролитов α ≈ 50-100% (0,5 - 1)
У слабых электролитов α ≈ 10% (меньше 0,1)
9.
10.
Дома: В водном растворе фосфата железа (II) содержится 0,1 моль фосфатионов. Сколько граммов соли использовали для приготовления раствора?11.
итог• Электролиты, которые полностью распадаются на ионы,
называют сильными.
• К ним относят все соли, гидроксиды щелочных и
щелочноземельных металлов, некоторые кислоты –
соляную, серную, азотную.
• Электролиты, которые лишь частично распадаются на
ионы, называются слабыми.
• Это вода, такие слабые кислоты, как сероводородная,
уксусная нерастворимые основания
12.
Дома:Изучать §11;
выучить вещества (группы веществ), которые
относятся к сильным и слабым электролитам;
упр.2,3;
*В водном растворе нитрата железа (II) содержится
0,1 моль нитрат-ионов. Сколько граммов соли
использовали для приготовления раствора?
Домашнюю работу оформляем на двойном листке.
Работу подписываем.
Указываем номер параграфа и номера заданий.
Приходим в школу на консультацию и относим листок в лаборантскую химии
(можно под дверь).
До субботы работы должны быть сданы!







 chemistry
chemistry








