Similar presentations:
Дисперсные системы. Лиофобные дисперсные системы (часть 2)
1. Дисперсные системы. Лиофобные дисперсные системы часть 2
Физическая и коллоидная химия1
2.
Молекулярно-кинетические свойства- свойства, обусловленные числом (концентрацией)
частиц, участвующих в тепловом движении.
В истинных растворах числом молекул или
ионов
В дисперсных системах числом частиц
дисперсной фазы
размеры частиц в ДС (и молекул
ВМС) много больше размеров
обычных молекул,
они двигаются медленнее;
связанные с движением
молекулярно-кинетические
свойства менее выражены.
2
3.
Изобретение ультрамикроскопа (1903) позволило непосредственно наблюдатьдвижение отдельных коллоидных частиц и связать интенсивность движения с
размером частиц
*
Молекулярно-кинетические свойства ДС – важнейший раздел коллоидной химии.
«зримый отблеск мира молекулярного хаоса» (В. Оствальд).
3
4.
Молекулярно-кинетические свойства (общие):• диффузия,
• осмотическое давление,
• понижение давления пара над раствором,
• изменение температур кипения и замерзания
+ проявление в дисперсных системах
• броуновское движение,
• седиментация
4
5.
Осмос -движение растворителячерез мембрану в
направлении выравнивания
концентраций
Осмотическое давление
В истинных растворах
Росм = СRT
С – молярная концентрация растворенного вещества (моль/м3)
В коллоидных растворах Росм = СкRT
Ск – молярная концентрация частиц (моль частиц/м3)
5
6.
Скмоль частиц
.
3
м
моль коллоидных частиц
в единице объема системы
Cмасс массовая концентрация
общее число частиц n
Ск
n
N AV
m дисп.фазы
m ед N AV
m дисп.фазы
Vед N AV
m дисп.фазы
4 r 3 N AV
3
С масс
4 r 3 N A
3
mед
Vед
число частиц (моль) масса частицы объем частицы
Pосм
1
r
3
При равных Смасс
Pосм определяется размерами
частиц. При укрупнении частиц
(коагуляция) Pосм уменьшается
Росм1 r23
3
Росм 2 r1
6
7.
Диффузияраспространение вещества вследствие теплового движения
его частиц. Ведёт к равномерному распределению вещества
по всему занимаемому им объёму (к выравниванию
химического потенциала).
Коэффициент
диффузии
RT 1
D
N A 6 h r
D — коэффициент диффузии (м2/c)
η — вязкость дисперсионной среды,
r — радиус частицы
1
D
r
7
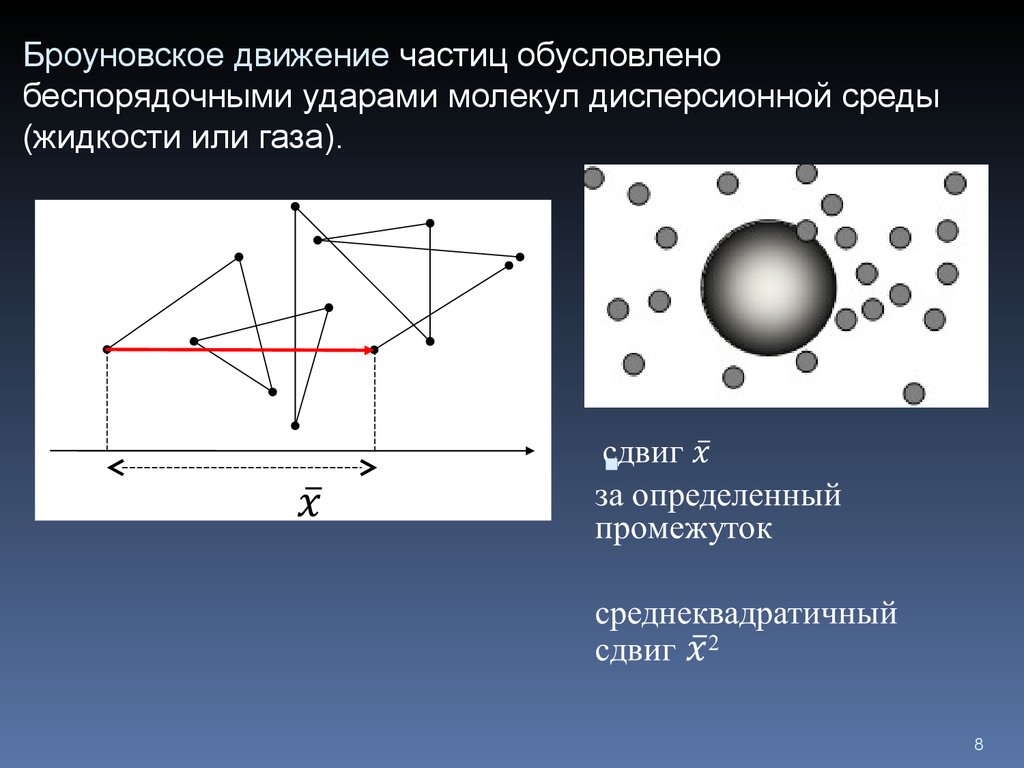
8.
Броуновское движение частиц обусловленобеспорядочными ударами молекул дисперсионной среды
(жидкости или газа).
8
9.
А. Эйнштейн, 1905 г.М. Смолуховский,
Связь среднеквадратичного
сдвига частицы с коэффициентом
диффузии
RTt
Dx 2 Dt
N A 3 h r
2
Выполнимость этого уравнения показали
опыты Ж. Б. Перрена,
что явилось экспериментальным
подтверждением количественной теории
броуновского движения и
доказательством существования атомов
и молекул.
1
Dx
r
2
9
Ж. Б. Перрен
10.
Седиментация –оседание частицВ состоянии равновесия
F тяж = F сопр (вязкость),
скорость оседания u = const
Fсопр 6 rhu
( - 0 )
u
×
6 rh
mg
(через массу частицы)
Fтяж (m - m0 ) g
( - 0 )
V ( - 0 )g m
g
2r 2 g ( - 0 )
u
9h
(через радиус частицы)
ρ и ρ0 — плотности частиц и среды
10
11.
Седиментационный анализ – определение размера(массы) частиц по скорости оседания
2r 2 g ( - 0 )
u
9h
9hu
r
2g( - о)
Скорость u - путь, пройденный частицей (высота) h, деленный
на время оседания τ.
Измеряя время, за которое частица оседает под действием
силы тяжести на фиксированную высоту, можно вычислить
размер отельных частиц.
В поле силы тяжести определяются частицы 1-100мкм
11
12.
частицы r 1мкм оседают в поле силы тяжести нанесколько см за сутки,
в центрифуге – несколько см за секунды
Лабораторная центрифуга
500-3000 об/мин
Ультрацентрифуга Optima L100 XР
100 000 об/мин
802 400 g
12
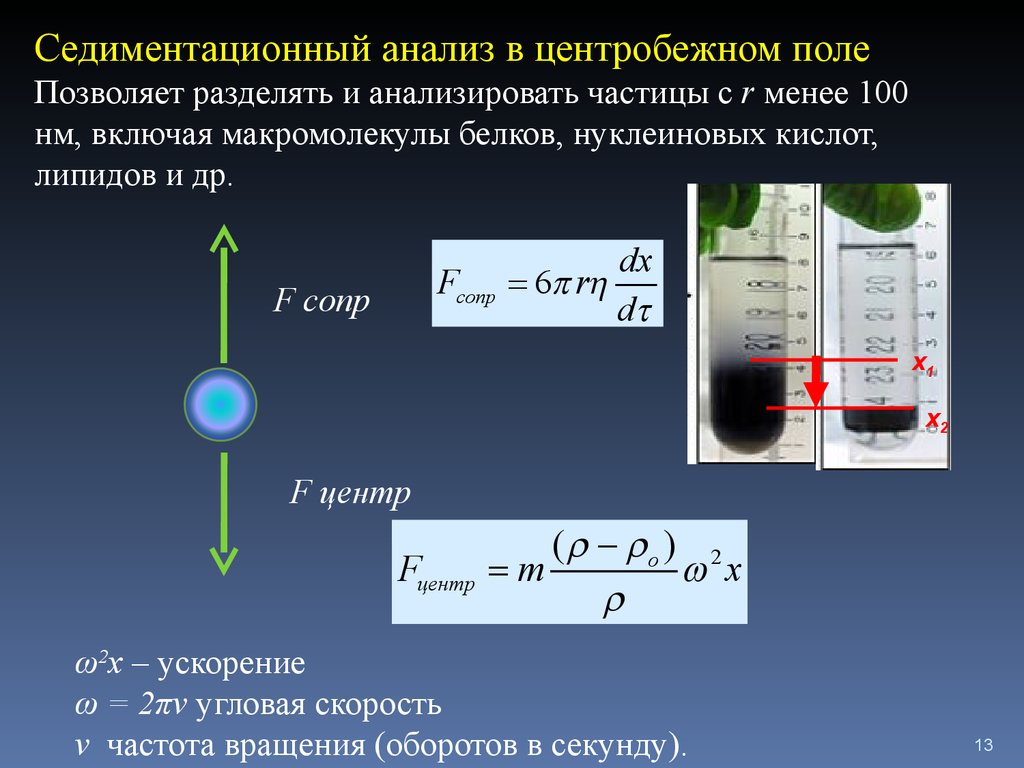
13.
Седиментационный анализ в центробежном полеПозволяет разделять и анализировать частицы с r менее 100
нм, включая макромолекулы белков, нуклеиновых кислот,
липидов и др.
Fсопр
F cопр
dx
6 rh
dt
x1
x2
F центр
Fцентр
( - o ) 2
m
w x
ω2x – ускорение
ω = 2πν угловая скорость
ν частота вращения (оборотов в секунду).
13
14.
( - 0 ) 2dx
m
w x 6 rh
dt
D
m× NA M
RT
6 rhN A
dx
RT dt
mN A
× 2 ×
D w x ( - 0 )
14
15.
dxСоотношение
dt
S
w2 x
скорости оседания dx/dτ к ускорению ω2x называют коэффициентом седиментации:
Отношение скорости оседания dx/dτ к ускорению ω2x
называют коэффициентом седиментации:
dx
S d2t
w x
Коэффициент седиментации — важнейшая
характеристика,
используемая
при
определении
молекулярной
массы
полимеров и белков:
Theodor Svedberg.
RTS
M
×
D ( - 0 )
1 S (Сведберг) = 10-13 с
15
16.
Седиментационная устойчивость – устойчивость к оседанию•Вследствие оседания на дне сосуда
концентрация частиц увеличится, а в
верхней части уменьшится.
Диффузия
•Гипсометрический закон
Лапласа — Перрена
h1
2
RT ln 2
4 r 3 gN A ( - 0 )
3
Седиментация
h1/2- гипсометрическая высота
на которой концентрация частиц
уменьшается в 2 раза
17. Оптические свойства дисперсных систем Взаимодействие дисперсной системы со светом
λ380- 450- 480- 500450 480 500 560
560590
590620
620760 нм
17
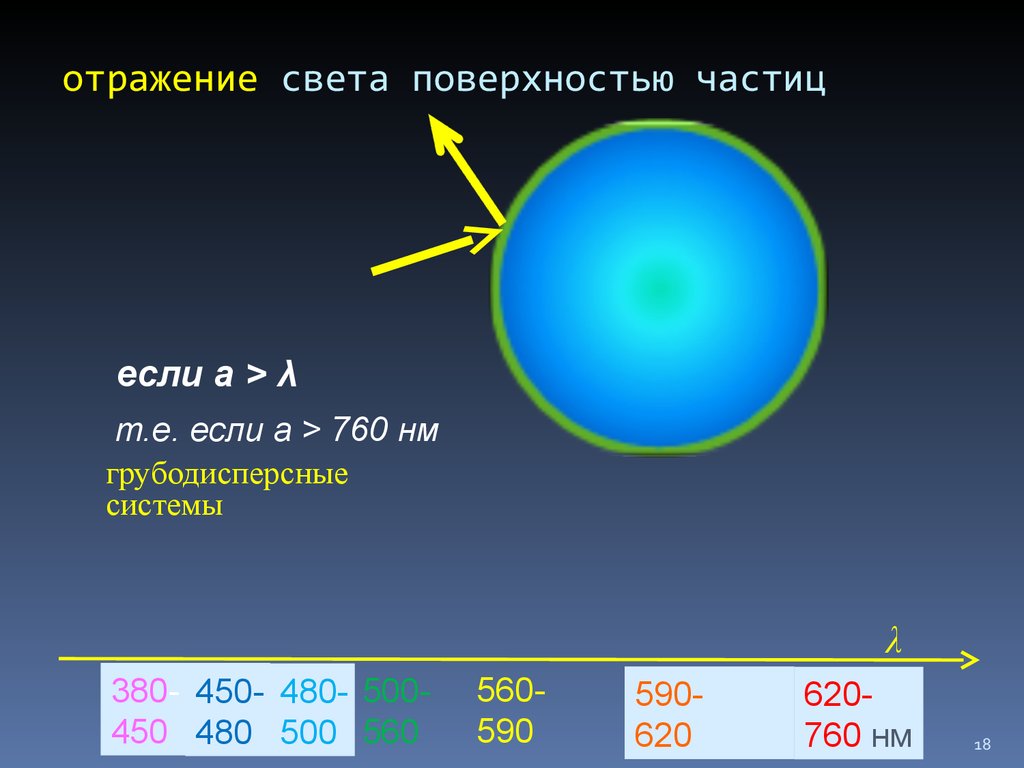
18. отражение света поверхностью частиц
если а > λт.е. если а > 760 нм
грубодисперсные
системы
λ
380- 450- 480- 500450 480 500 560
560590
590620
620760 нм
18
19. прохождение света через систему
если а << λ(менее 10 нм = низкомолекулярные растворы =
дисперсионная среда,
малая концентрация частиц дисперсной фазы)
19
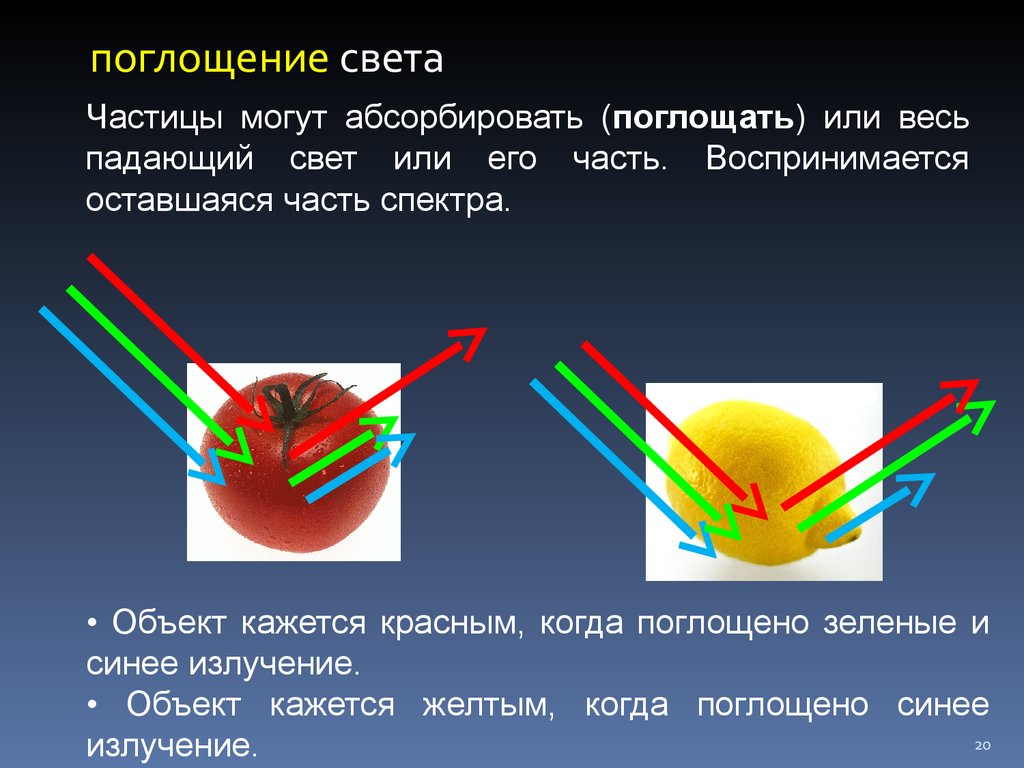
20. поглощение света
Частицы могут абсорбировать (поглощать) или весьпадающий свет или его часть. Воспринимается
оставшаяся часть спектра.
• Объект кажется красным, когда поглощено зеленые и
синее излучение.
• Объект кажется желтым, когда поглощено синее
20
излучение.
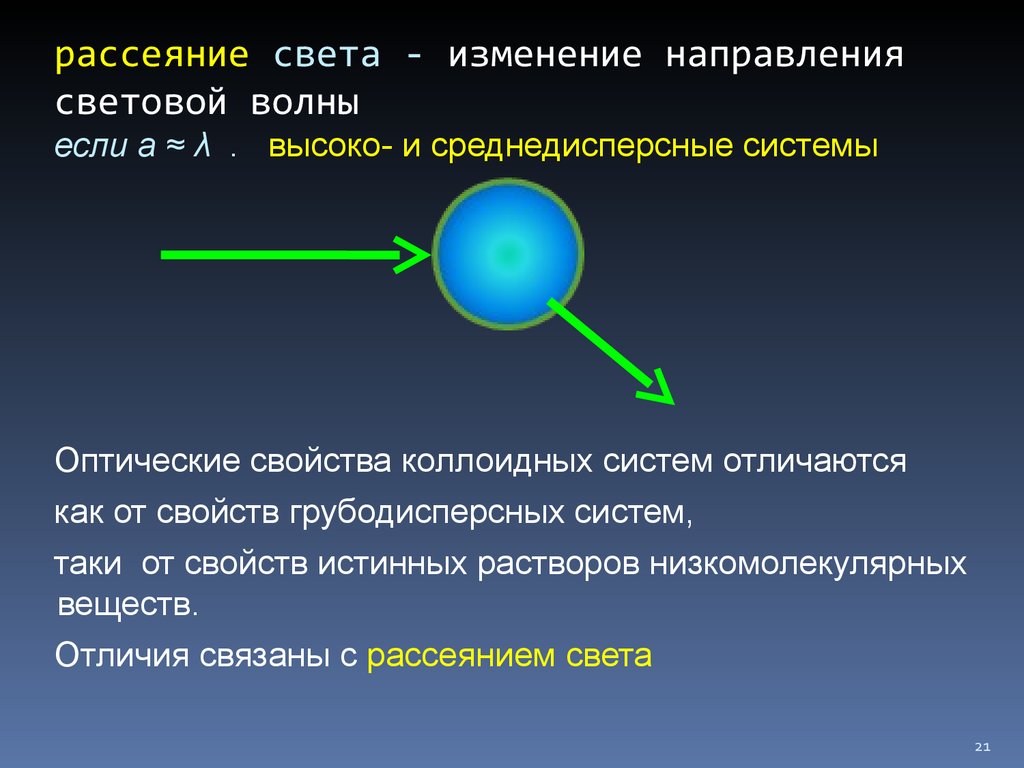
21. рассеяние света - изменение направления световой волны если а ≈ λ . высоко- и среднедисперсные системы
рассеяние света - изменение направлениясветовой волны
если а ≈ λ . высоко- и среднедисперсные системы
Оптические свойства коллоидных систем отличаются
как от свойств грубодисперсных систем,
таки от свойств истинных растворов низкомолекулярных
веществ.
Отличия связаны с рассеянием света
21
22. В высоко- и среднедисперсной системе падающий свет распределяется на три части: поглощенный, рассеянный и прошедший
(I – интенсивность светового потока )золь
Падающий
Поглощенный
I0
Iпогл
Прошедший
Iпр
Рассеянный
Iрас
22
23. Характерные проявления оптических свойств дисперсных систем
опалесценция,эффект Тиндаля,
окраска
окраска определяется
•рассеянием света (если нет поглощения света )
•поглощением (адсорбцией) света.
23
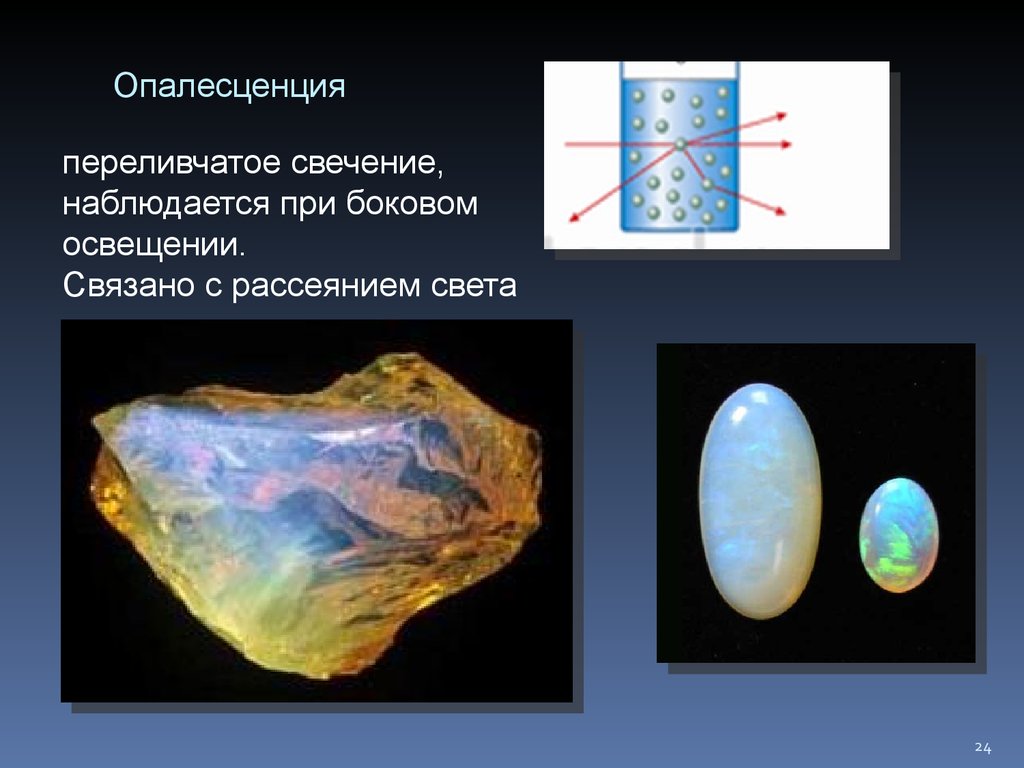
24. Опалесценция
переливчатое свечение,наблюдается при боковом
освещении.
Связано с рассеянием света
24
25. Эффект Тиндаля
John TyndallЭффект связан с рассеянием света
При освещении коллоидного
раствора сбоку пучком света
наблюдается яркий светящийся
след — конус Тиндаля, или
эффект Тиндаля).
в случае низкомолекулярного раствора жидкость кажется
оптически пустой
25
26. Эффект Тиндаля в воздушной среде
2627.
Интенсивность рассеяния светаö
24 æ n2 - nсV
1
3
I рас I 0
l
4
2
2
уравнение
Рэлея
2
ç 2
2 ÷
è n2 + 2n1 ø
Строго –
для a ≤ 0,1λ
Iрас — интенсивность рассеянного света ;
I0 — интенсивность падающего света;
λ — длина волны падающего света;
n1 и n2 — показатели преломления дисп. среды и
дисп. фазы;
V — объем одной частицы (V = πd3/6);
с — массовая концентрация,
ρ — плотность частиц дисперсной фазы.
27
28.
Измеряя Iрас можноэкспериментально определить
концентрацию C
или их размер d
Нефелометрия .
Приборы, применяемые для
измерения интенсивности
рассеянного света Iрас —
нефелометры.
28
29.
Лучше рассеивается короткая (красная)часть спектраIрас
≈
1
λ4
29
30. Оптические методы исследования дисперсных систем Оптический микроскоп
Оптические методы исследования дисперсныхсистем
Разрешающая способность (различимое
Оптический микроскоп
расстояние между точками) :
l
l
S
2А
2n sin a
λ — длина волны; 2
n — показатель преломления среды;
α — угол между крайними лучами,
попадающими в объектив.
А = n sin(α/2) - числовая апертура объектива.
А≈1-1.5
S
l
760нм
S> 100 нм - среднедисперсные системы
253нм
2A
1 × 1,5
30
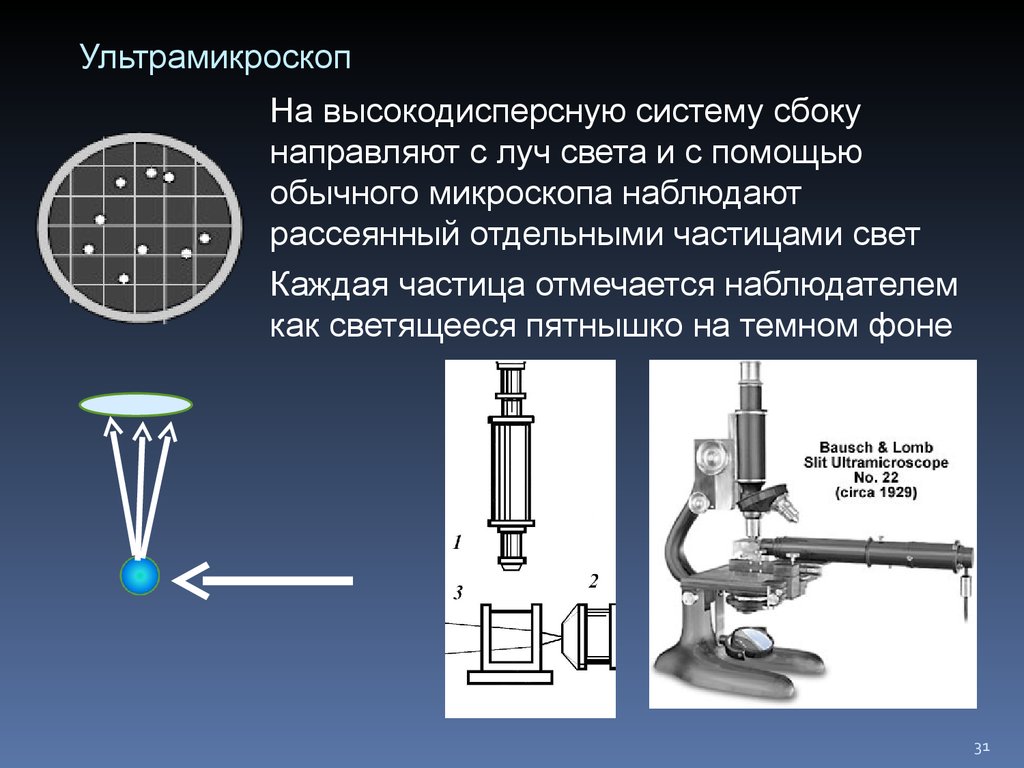
31. Ультрамикроскоп
На высокодисперсную систему сбокунаправляют с луч света и с помощью
обычного микроскопа наблюдают
рассеянный отдельными частицами свет
Каждая частица отмечается наблюдателем
как светящееся пятнышко на темном фоне
31
32.
3233. Электронный микроскоп
Длина волны электрона 5 ∙ 10-11м.l 5 ×10-11
Sм
1,7 ×10-11
2 A 2 ×1,5
(теоретически)
на практике 0,2-0,3 нм
Ход лучей в целом такой же,
как в обычном микроскопе,
а роль оптических стеклянных
или кварцевых линз в нем
выполняют электромагниты.
Получаемое изображение
фиксируется на экране.
33
34. Просвечивающие электронные микроскопы
3435. Сканирующий электронный микроскоп
Принцип работы :сканирование поверхности
образца электронным пучком,
анализ отраженных от
поверхности частиц и
возникающего излучения
трехмерный
эффект
воспроизведения
рельефа образца
35
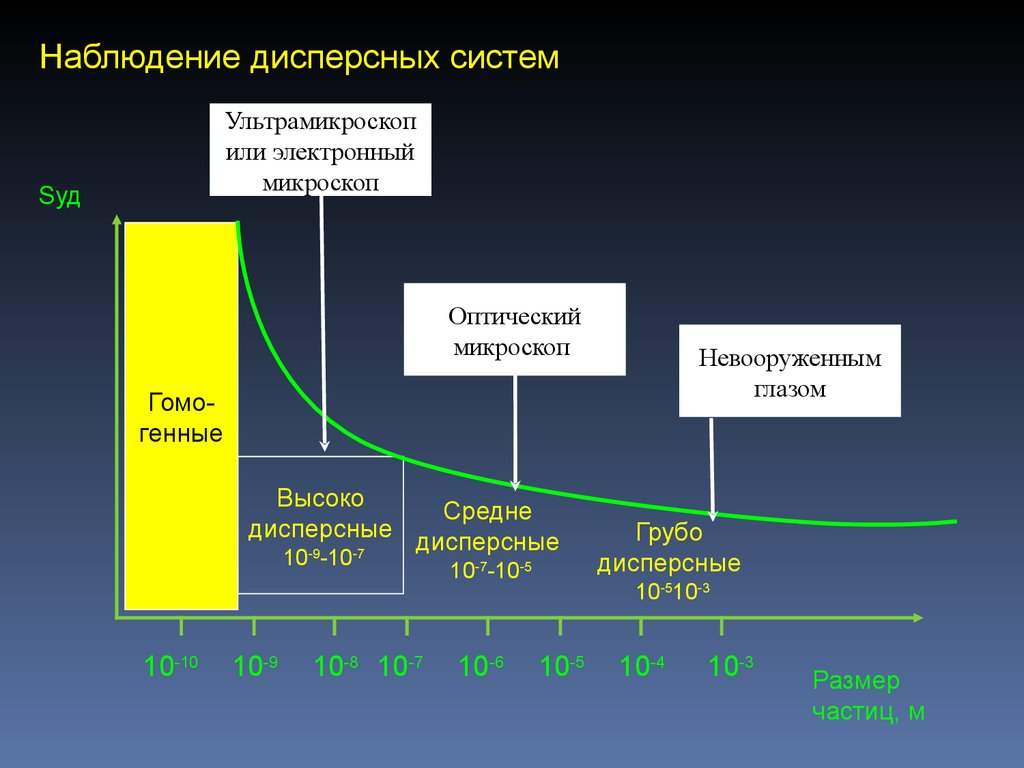
36. Наблюдение дисперсных систем
Ультрамикроскопили электронный
микроскоп
Sуд
Оптический
микроскоп
Невооруженным
глазом
Гомогенные
Высоко
дисперсные
10 -10
-9
10-10
10-9
-7
Средне
дисперсные
10-8 10-7
10-7-10-5
10-6
Грубо
дисперсные
10-510-3
10-5
10-4
10-3
Размер
частиц, м



























 physics
physics chemistry
chemistry








