Similar presentations:
Дисперсные системы. Лиофобные дисперсные системы (часть 1)
1. Дисперсные системы. Лиофобные дисперсные системы часть 1
Физическая и коллоидная химия1
2. Дисперсные системы – гетерогенные системы с высокой степенью дисперсности (раздробленности) одной из фаз. Признаки: гетерогенность диспе
Дисперсные системы – гетерогенные системы свысокой степенью дисперсности (раздробленности)
одной из фаз.
Граница раздела фаз
Признаки:
(чем мельче частицы, тем больше S)
гетерогенность
дисперсность
Избыточная поверхностная энергия
Термодинамическая неустойчивость
Поверхностные явления, поверхностные
свойства
Пример обозначения: Т/Ж
(твердая дисперсная фаза/ жидкая дисперсионная среда)
3.
Классификация ДС по агрегатному состоянию фаз.
Система
Примеры
Т/Ж Золи, суспензии,
пасты
Химические осадки, пасты, краски
Ж/Ж Эмульсии
Нефть, молоко, масло, кремы
Г/Ж Пены
Мыльные, флотационные пены и др.
Т/Т
Минералы, сплавы, строительные и
композиционные материалы,
Твердые золи
Ж/Т Капиллярно-
Влажные почвы, влажные строительные
материалы, древесина, опал, жемчуг
Г/Т
Пористые тела
(твердые пены)
Адсорбенты, катализаторы, пенопласты,
пемза, пенобетон, хлеб
Т/Г
Аэрозоли, порошки Дым, пыль, сухие строительные материалы,
песок, ткани, мука.
пористые тела,
твердые эмульсии
Ж/Г Туман
Г/Г -
Облака, туман, спрей
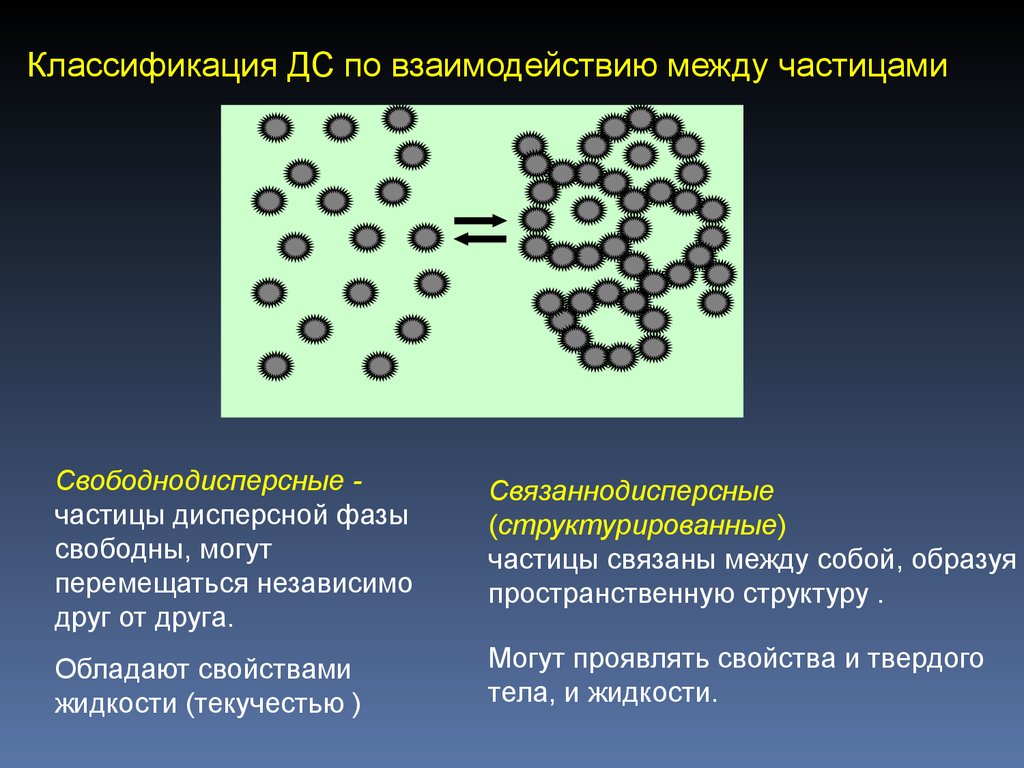
4. Классификация ДС по взаимодействию между частицами
Свободнодисперсные частицы дисперсной фазысвободны, могут
перемещаться независимо
друг от друга.
Связаннодисперсные
(структурированные)
частицы связаны между собой, образуя
пространственную структуру .
Обладают свойствами
жидкости (текучестью )
Могут проявлять свойства и твердого
тела, и жидкости.
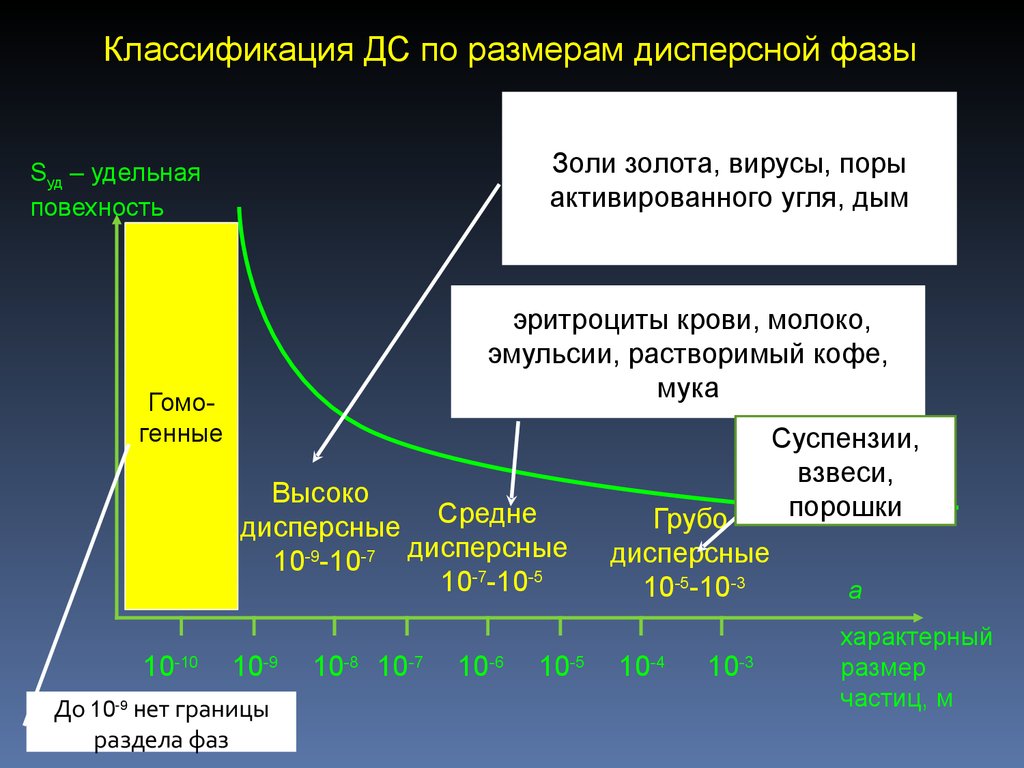
5. Классификация ДС по размерам дисперсной фазы
Золи золота, вирусы, порыактивированного угля, дым
Sуд – удельная
повехность
эритроциты крови, молоко,
эмульсии, растворимый кофе,
мука
Гомогенные
Высоко
дисперсные Средне
10-9-10-7 дисперсные
10-7-10-5
10-10
10-9
До 10-9 нет границы
раздела фаз
10-8 10-7
10-6
10-5
Грубо
дисперсные
10-5-10-3
10-4
10-3
Суспензии,
взвеси,
порошки
a
характерный
размер
частиц, м
6.
Классификация ДС по интенсивности взаимодействиямежду д. фазой и жидкой д. средой
лиофобные
лиофильные
(золи, эмульсии )
(ПАВ)
взаимодействие
между фазами
граница раздела
избыт. пов. энергия
термодинамич.
устойчивость
оч. слабое/нет
четкая
высокая
неустойчивы
сильное
размыта
низкая
устойчивы, обр-ся
самопроизвольно
6
7.
Характерные размеры - размеры дисперсной фазы,которые отражают раздробленность.
трехмерные
порошки
эмульсии
золи
двумерные
нити
капилляры
одномерные
пленки
7
8.
Дисперсность D — величина, обратная характерномуразмеру:
1
D
размерность м-1.
a
Удельная поверхность Sуд — площадь границы раздела фаз
S, приходящаяся на единицу массы m:
S уд
S
,
m
размерность м2/кг или м2/г.
Удельная поверхность частиц сферической формы:
S уд
.
2
S
n
S
6 d n
6
ед
3
m Vед n d n d
8
9.
910. различные виды мельниц - помол до 1-10 мкм
Механическоедиспергирование
различные виды мельниц
- помол до 1-10 мкм
Механизм диспергирования
Под действием деформирующих
сил (давление, удар, трение) на
поверхности тв. тела образуется
микротрещина.
Развитие микротрещин происходит
значительно легче при адсорбции
веществ — понизителей твердости
(ионы, молекулы ПАВ), которые
стремятся раздвинуть микрощель,
облегчая диспергирование.
Эффект адсорбционного понижения
твердости – эффект Ребиндера
10
11. (для твердых тел и жидкостей)
Ультразвуковоедиспергирование
(для твердых тел и жидкостей)
Ультразвук упругие колебания и
волны с частотами
от 15 кгц до 1 Ггц.
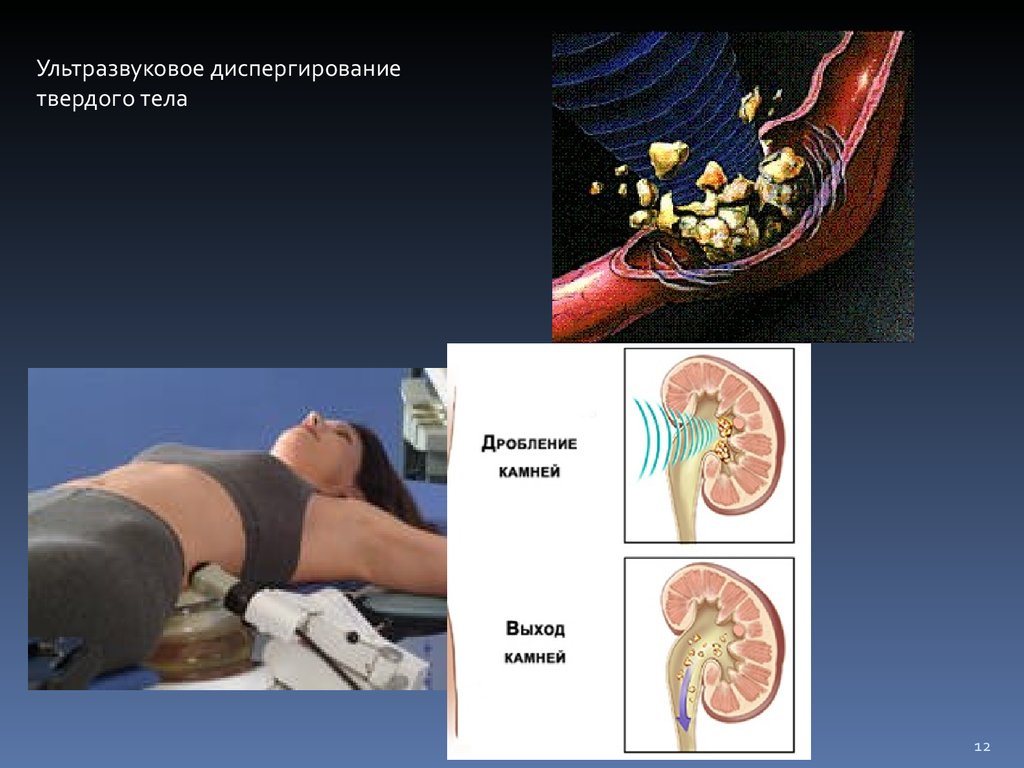
Кавитации -локальные быстро
чередующиеся сжатия и расширения
вещества, приводящие к образованию
мельчайших полостей и их разрушению.
11
12.
Ультразвуковое диспергированиетвердого тела
12
13.
Ультразвуковоедиспергирование жидкости
Ультразвуковой ингалятор
13
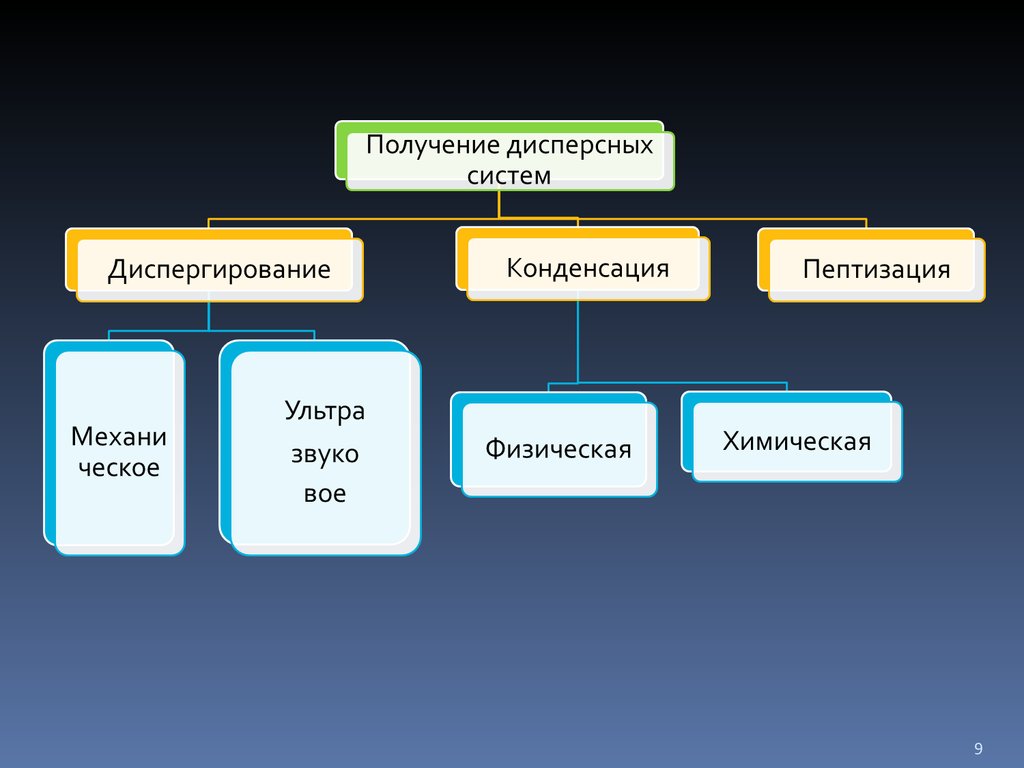
14. Методы конденсации – образование новой фазы из отдельных атомов или молекул
Методы физическойконденсации
Метод замены
растворителя
Конденсация из паров
и др.
Методы химической
конденсации
связаны с протеканием
химических реакций,
приводящих к
образованию новой
фазы (выпадению
осадка).
14
15.
Пептизация — процесс перехода вещества из геля(осадка)в золь под влиянием диспергирующих веществ
(пептизаторов).
При пептизации происходит разрушение связей между
слипшимися, но сохранившими самостоятельность мелкими
частичками дисперсной фазы: частицы приобретают заряд
и начинают отталкиваться друг от друга.
Виды пептизации:
промыванием осадка - «вымывание» электролита,
адсорбционная пептизация – ионы пептизатора
-электролита адсорбируются на поверхности частиц,
химическая пептизация – пептизатор химически
взаимодействует с веществом осадка; образующиеся в
результате реакции ионы придают частице заряд .
.
15
16. Пептизация под действием пептизатора заряд частиц увеличивается – отталкивание – образование золя
17.
Золи - лиофобные высокодисперсные системы Т/Ж.как правило, получают методом химической конденсации.
Реакции обмена, восстановления, окисления, гидролиза и
т. д.
Образованию золя способствуют
малые концентрации реагентов,
присутствие стабилизирующих веществ,
большое количество центров зародышеобразования.
.
17
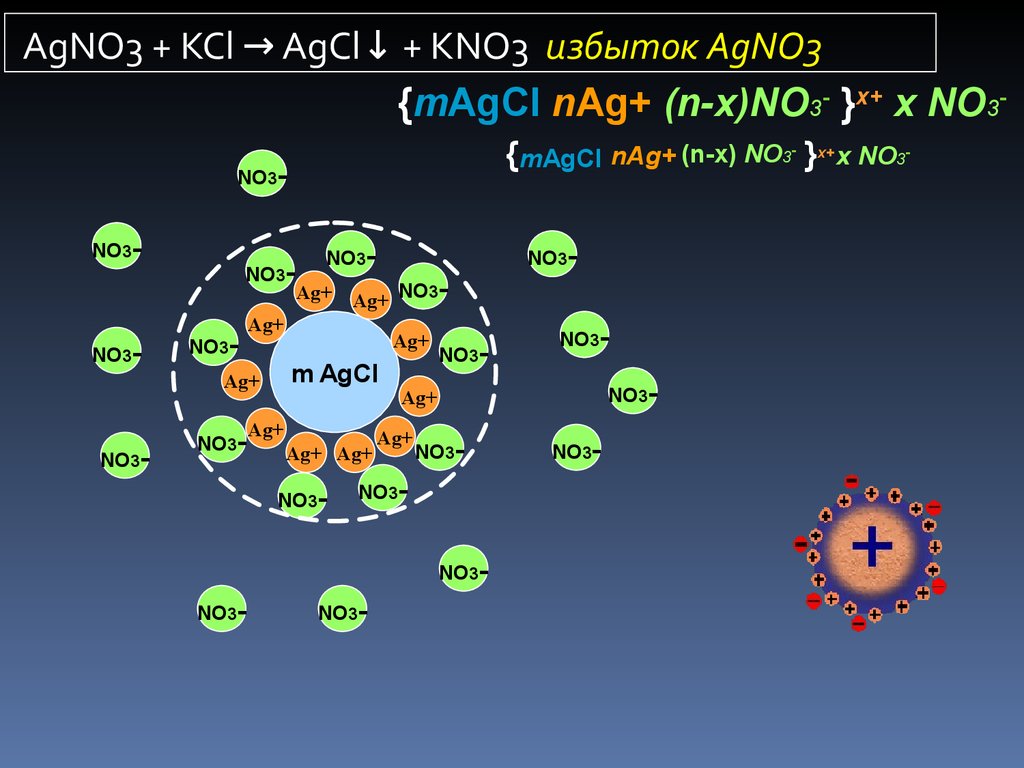
18.
AgNО3 + KCl → AgCl↓ + KNО3 избыток AgNО3{mAgCl nAg+ (n-x)NO3- }x+ x NO3{mAgCl nAg+ (n-x) NO3- }x+ x NO3-
NO3NO3-
NO3-
NO3NO3-
NO3-
Ag+
NO3-
Ag+ NO3-
Ag+
Ag+
m AgCl
Ag+
NO3-
NO3-
Ag+
Ag+ Ag+
NO3-
NO3-
NO3-
Ag+
Ag+
NO3-
NO3NO3-
NO3-
NO3-
NO3-
NO3-
19.
AgNО3 + KCl → AgCl↓ + KNО3 избыток KCl{mAgCl nCl- (n-x)K+}x- x K+
K
K+
{mAgCl nCl-
+
K
Cl-
K
K+
Cl
K+
-
K+
Cl
Cl- K+
K+
Cl- m AgCl
ClCl- K+
K+ Cl
Cl Cl
K+
K+
-
+
K+
+
K+
K+
K+
K+
K+
K+
(n-x)K+
}x- x K+
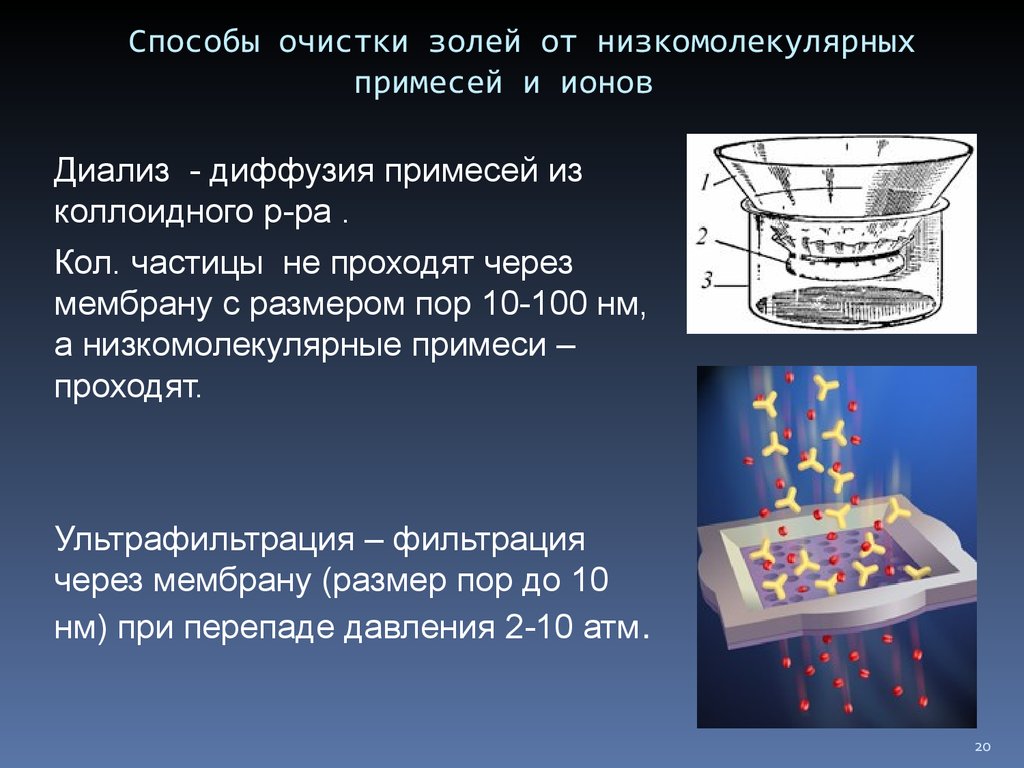
20. Способы очистки золей от низкомолекулярных примесей и ионов
Диализ - диффузия примесей изколлоидного р-ра .
Кол. частицы не проходят через
мембрану с размером пор 10-100 нм,
а низкомолекулярные примеси –
проходят.
Ультрафильтрация – фильтрация
через мембрану (размер пор до 10
нм) при перепаде давления 2-10 атм.
20
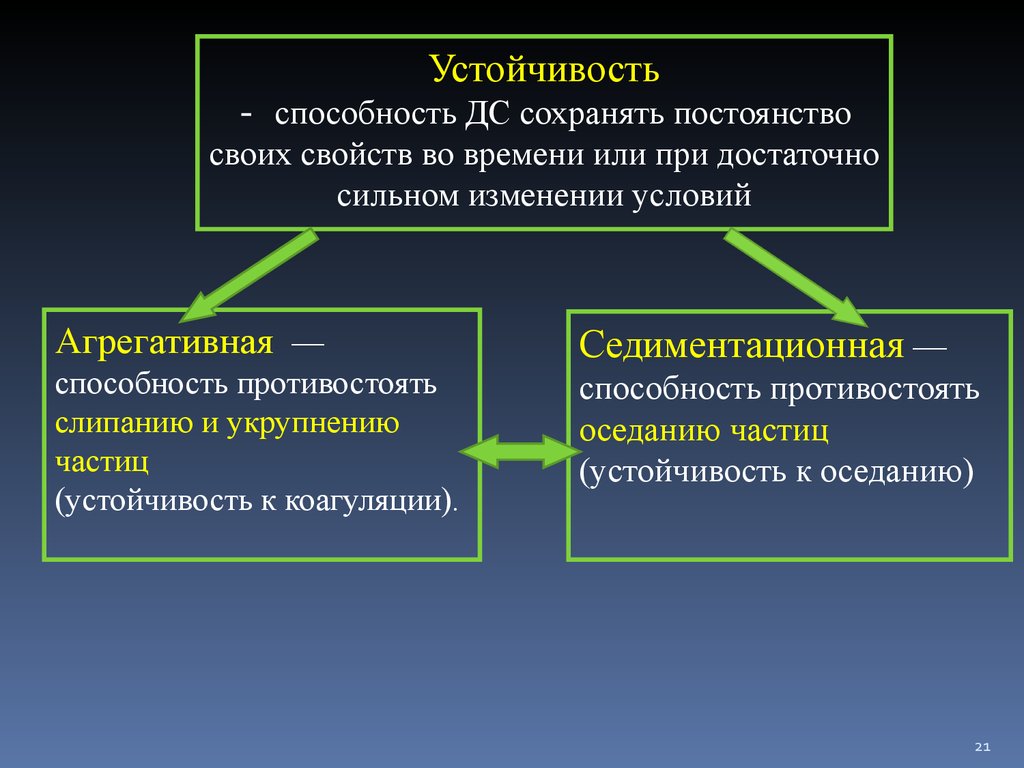
21. Устойчивость - способность ДС сохранять постоянство своих свойств во времени или при достаточно сильном изменении условий
Агрегативная —способность противостоять
слипанию и укрупнению
частиц
(устойчивость к коагуляции).
Седиментационная —
способность противостоять
оседанию частиц
(устойчивость к оседанию)
21
22.
Е отТеория (агрегативной) устойчивости
дисперсных систем -теория ДЛФО
«Энергетический (потенциальный)
барьер», его высота определяется
зарядом частиц
h
расстояние
между частицами
Е пр
«Ближний
минимум»
«Дальний
минимум»
Суммарная Е
22
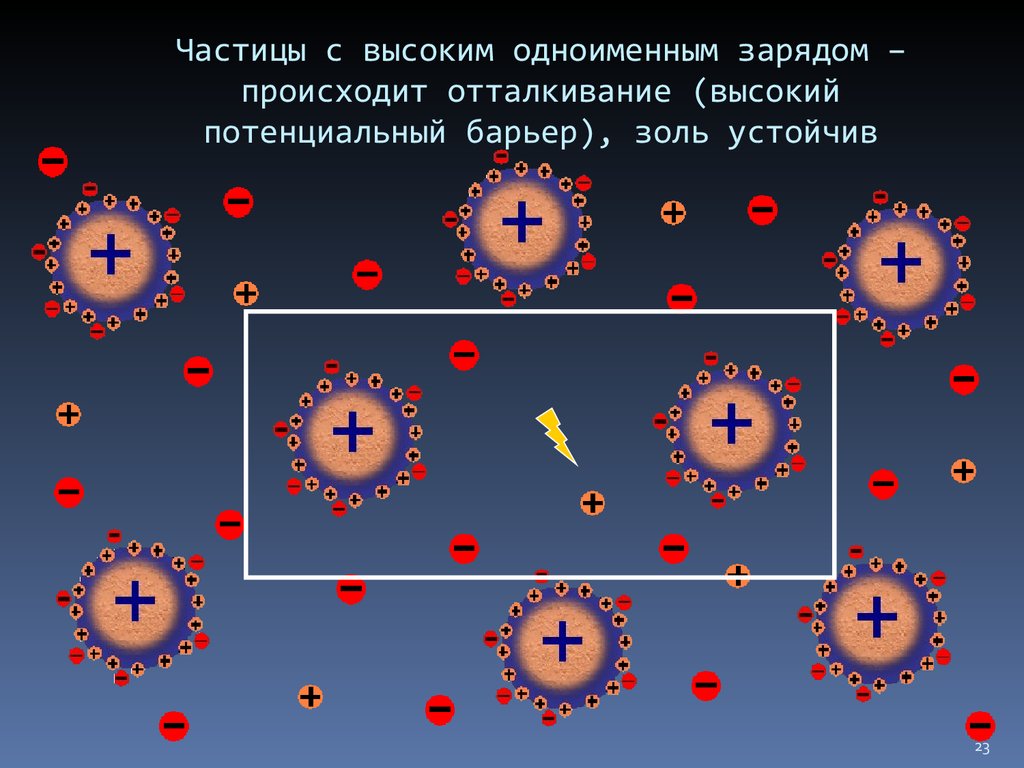
23. Частицы с высоким одноименным зарядом – происходит отталкивание (высокий потенциальный барьер), золь устойчив
2324.
Коагуляция - самопроизвольное укрупнение частицтвердой дисперсной фазы в золях (чаще - под действием
электролита).
Порог коагуляции Ск
наименьшая концентрация электролита, при которой
начинается коагуляция.
С эл Vэл
Ск
V золя Vэл
24
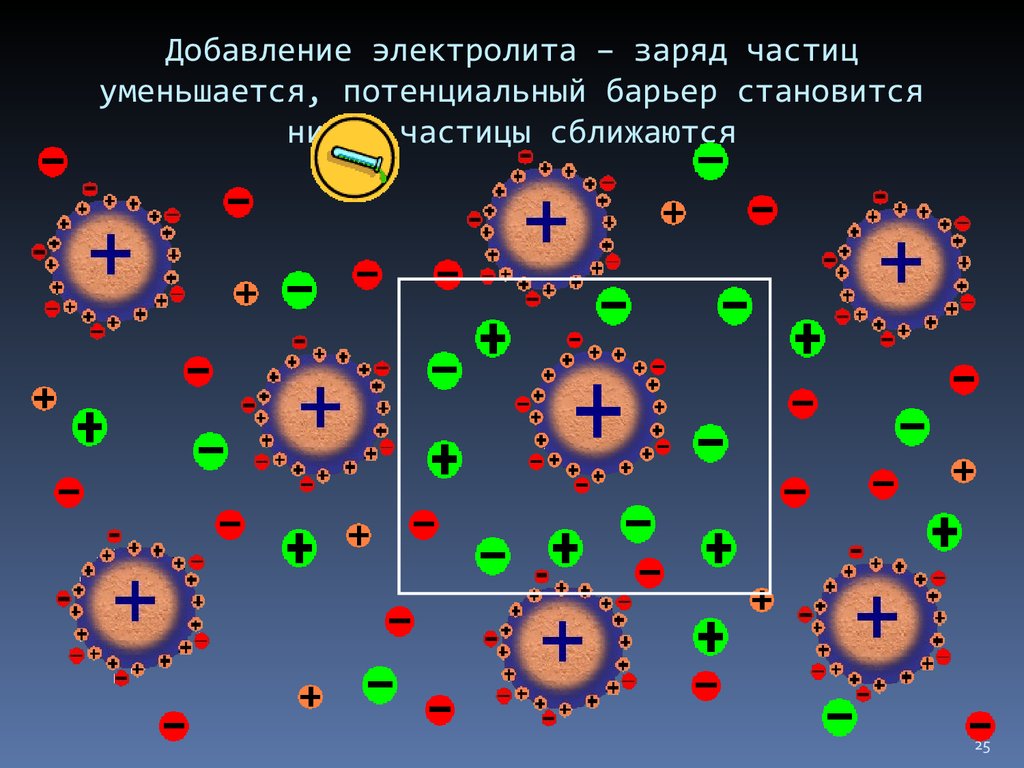
25. Добавление электролита – заряд частиц уменьшается, потенциальный барьер становится ниже, частицы сближаются
2526. Частицы притягиваются - КОАГУЛЯЦИЯ
2627.
Коагулирующее действие оказывают только ионы,противоположные по заряду ядру коллоидной частицы.
1. Концентрационная
коагуляция
(увеличим
концентрацию K+) –
больше ионов в
(изоэлектрическое состояние:
плотном слое
{mAgI ∙nI – ∙ nK+}.
2. Коагуляция при добавлении
+
+
+
+
+
Li
,
Na
,
K
,
Rb
,
Cs
,
гидратированных ионов
–
–
–
– –
F
,
Сl
,
Вr
,
NO
,
I
,
CNS
.
3
меньшего размера
– маленькие вытесняют крупные
27
28.
3. Коагуляция золей электролитами, содержащимимногозарядный ион
может произойти перезарядка золя
{mAg
· n I– ·(n – x) Zn2+ }2(n–х)+ ·(n – x) Zn2+.
28
29.
Правило Шульце — Гарди:коагулирующая способность иона тем больше, чем
больше его заряд:
1
Ск 6
z
Ск1: Ск2 :Ск3 =
1
1
6
1
2
6
:
1
3
6
1 : 0,016 : 0,0014 729 : 64 : 1.
С эл Vэл
С
Ск — порог коагуляции, напоминнание: к V
золя V эл
z — заряд иона-коагулятора (1, 2 или 3)
29
30.
Гетерокоагуляция –взаимодействие частиц, различных по заряду и величине.
Взаимная коагуляция происходит при смешивании золей с
разноименно заряженными коллоидными частицами.
30
31.
Коллоидная защита — повышениеагрегативной устойчивости золя
путем введения в него
поверхностно-активных
соединений, адсорбирующихся на
поверхности частицы.
Количественная характеристика защитного действия
Золотое число — это масса вещества (мг), которую нужно
прибавить к 10 мл 0,0006% красного золя золота для
предотвращения его перехода в синий золь при
добавлении 1 мл 10% раствора NaCl.
31






















 physics
physics chemistry
chemistry