Similar presentations:
Биологическое окисление
1. Биологическое окисление
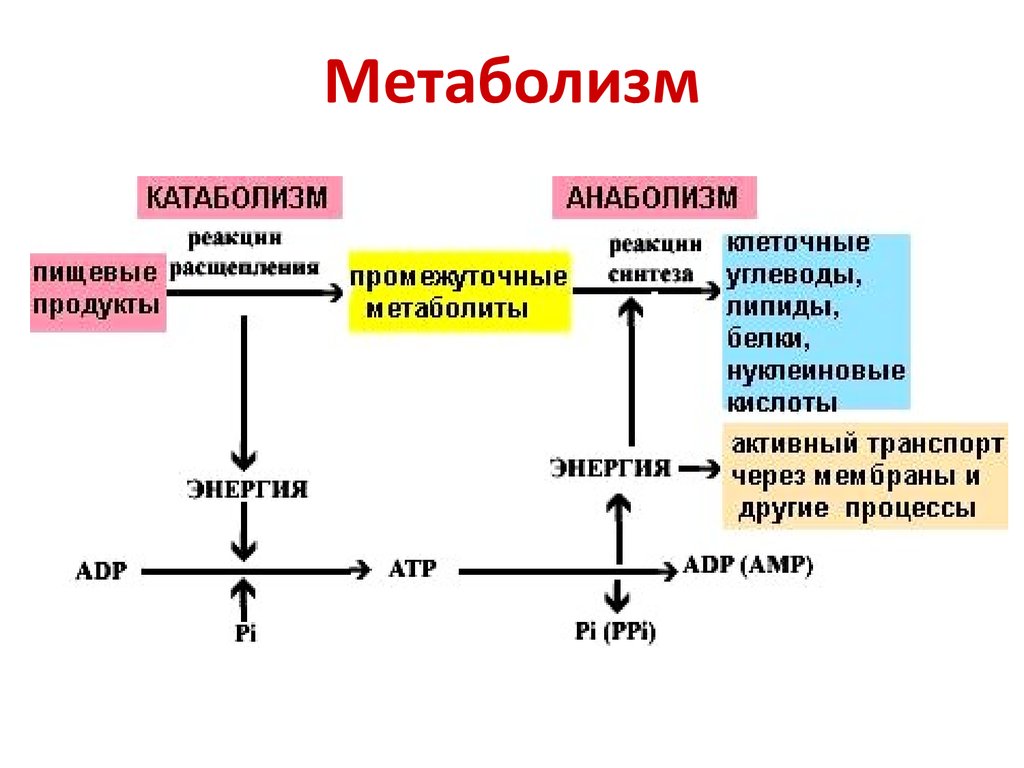
2. Метаболизм
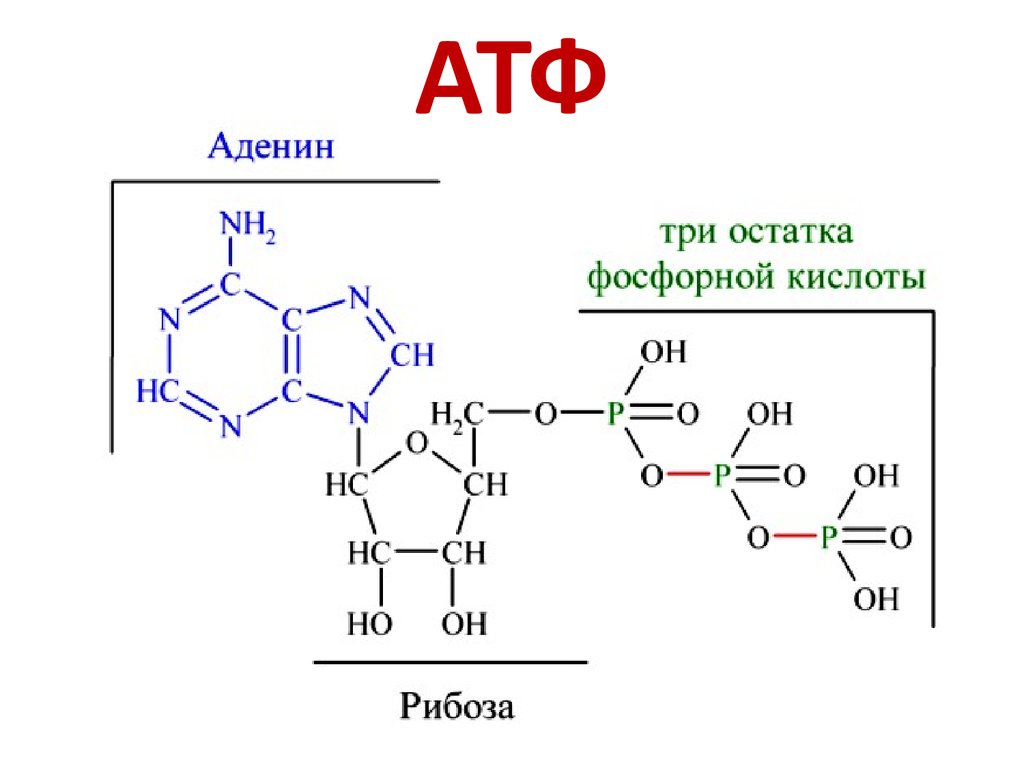
3. АТФ
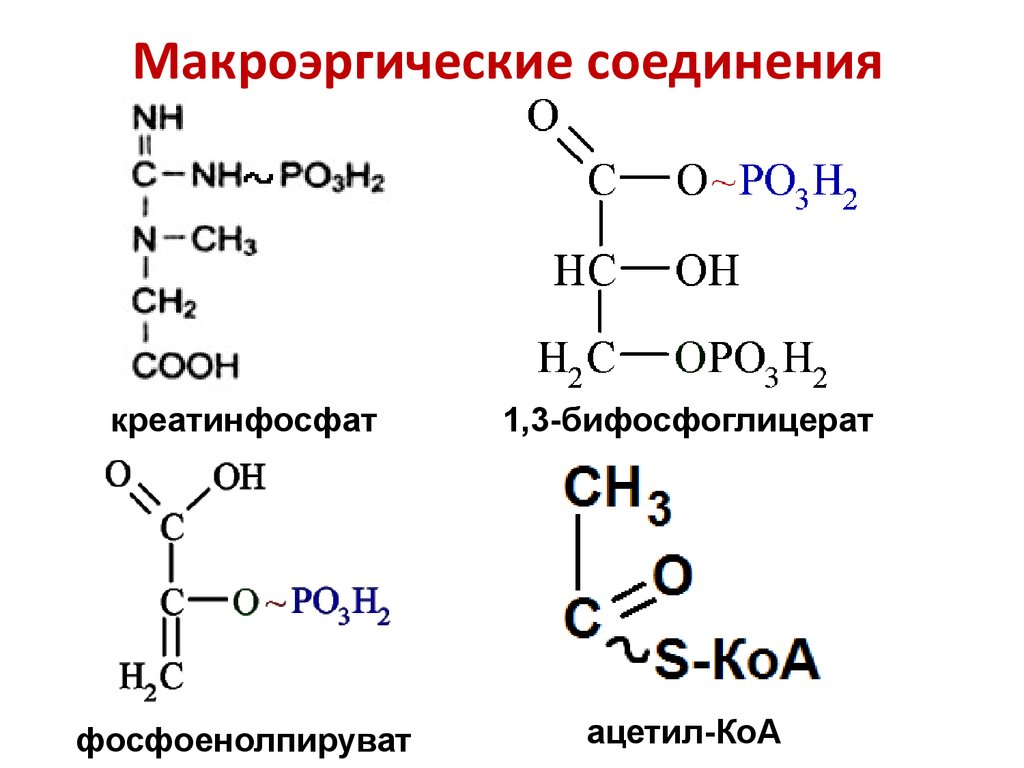
4. Макроэргические соединения
креатинфосфат1,3-бифосфоглицерат
фосфоенолпируват
ацетил-КоА
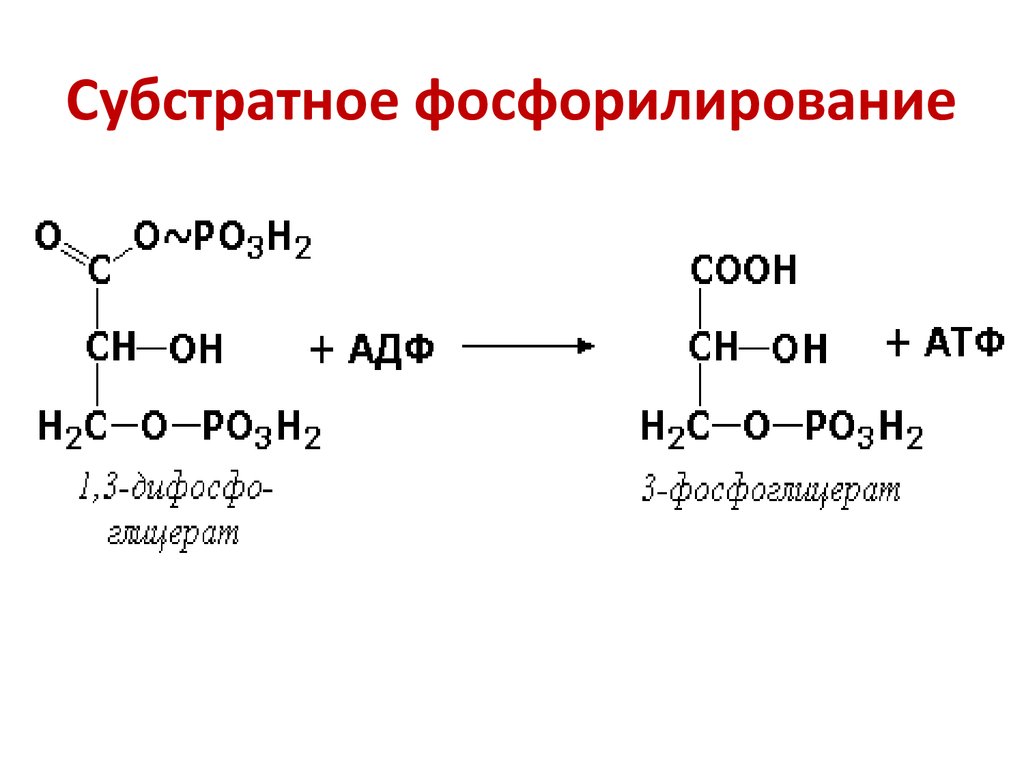
5. Субстратное фосфорилирование
6. Клеточное дыхание Окислительное фосфорилирование
С6Н12О6 + 6Н2О + 12А = 6 СО2 + 12АН212АН2 + 6О2 = 12Н2О + 12А
С6Н12О6 + 6О2 = 6 СО2 + 6Н2О
7. Антуан Лоран Лавуазье
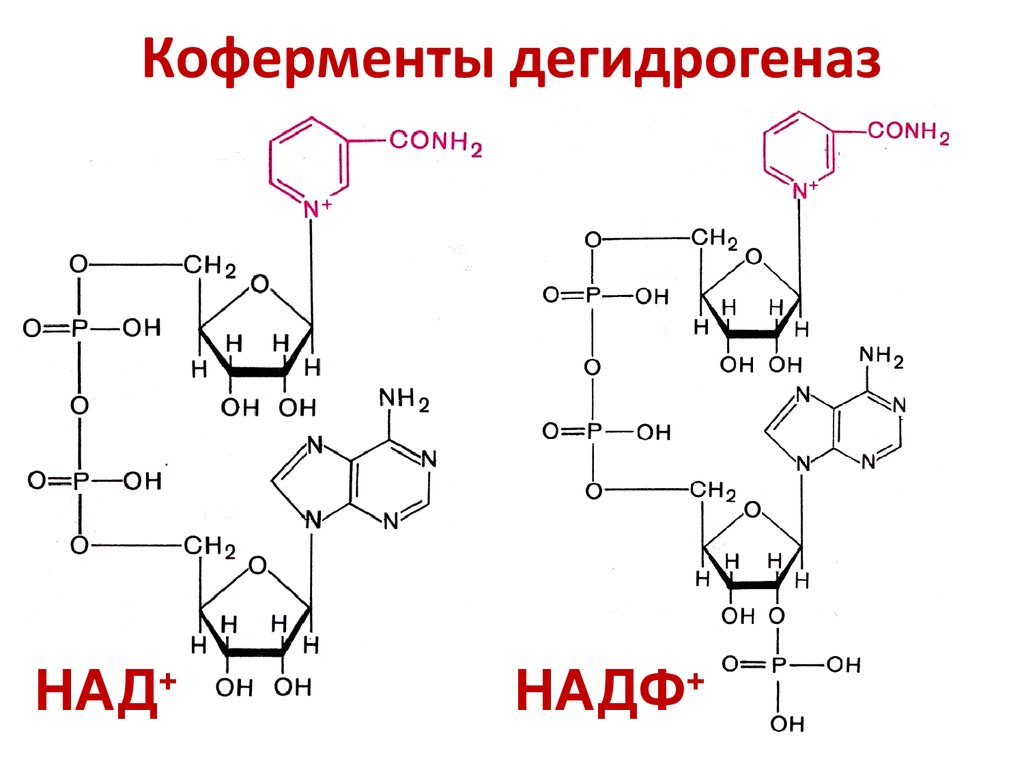
8. Коферменты дегидрогеназ
НАД+НАДФ+
9.
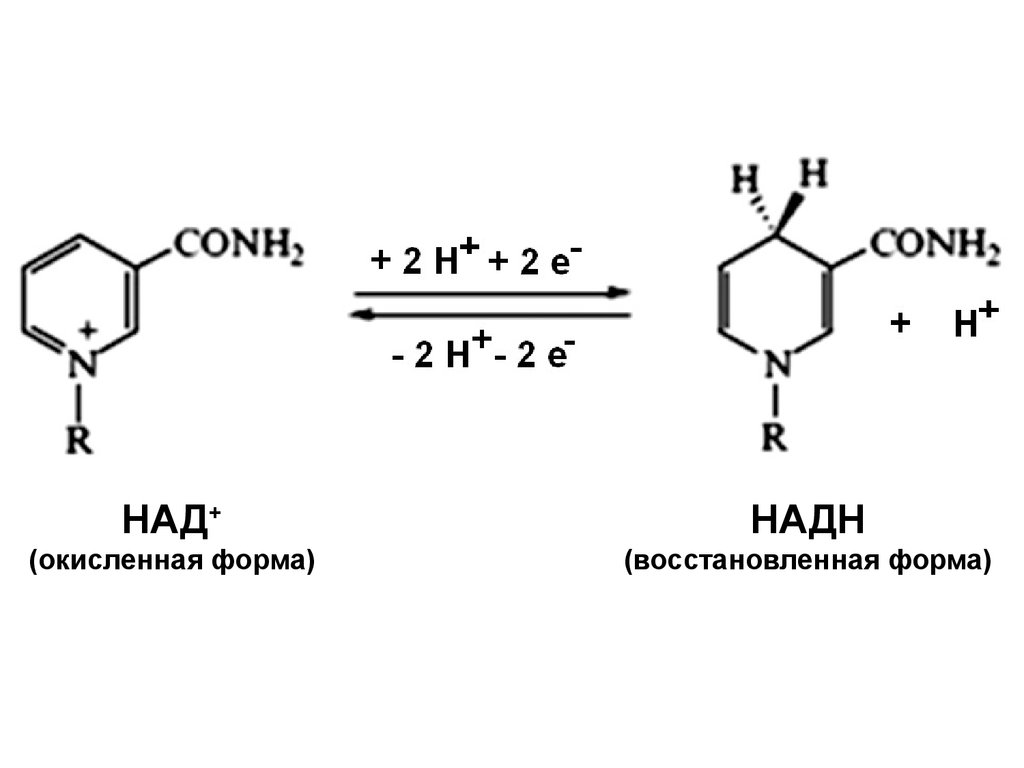
НАД+НАДН
(окисленная форма)
(восстановленная форма)
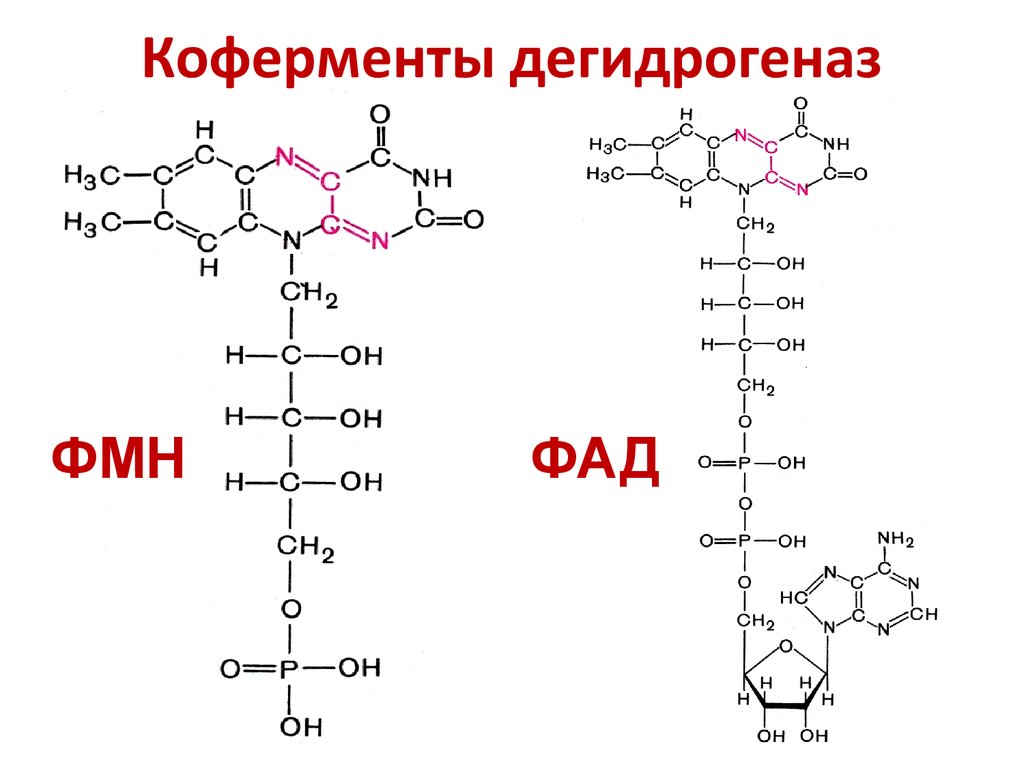
10. Коферменты дегидрогеназ
ФМНФАД
11.
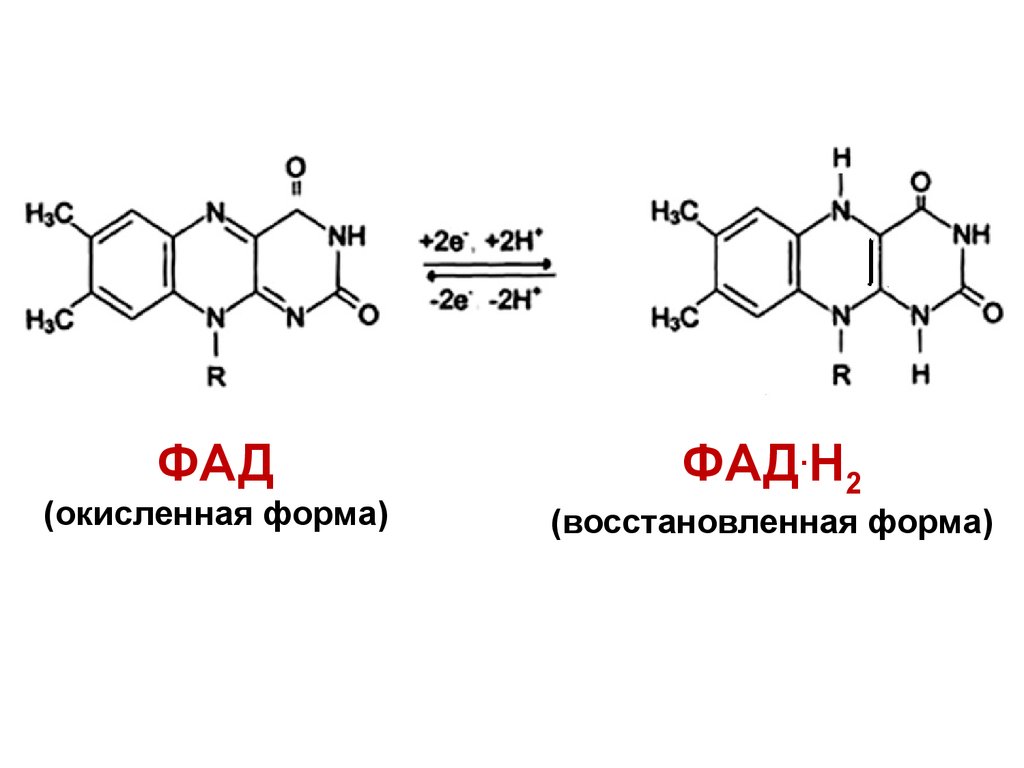
ФАД(окисленная форма)
ФАД.Н2
(восстановленная форма)
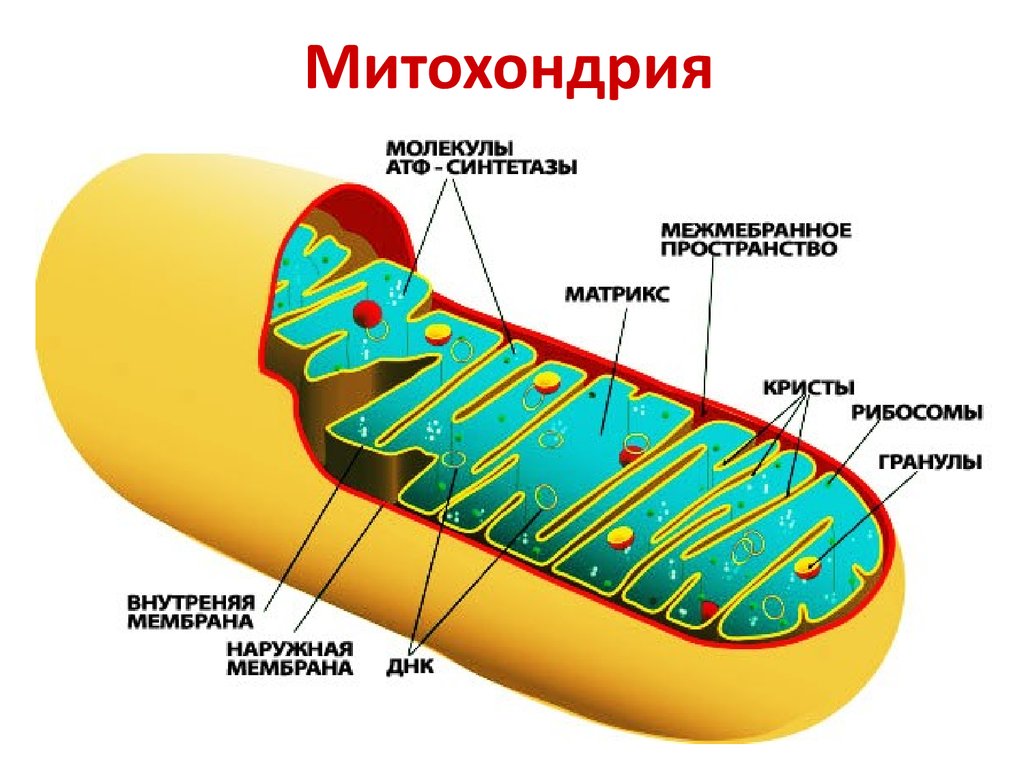
12. Митохондрия
13. Состав комплексов дыхательной цепи
Комплекс I (НАДН-дегидрогеназа):ФМН, железосерный белок FeS.
Комплекс II (сукцинатдегидрогеназа):
ФАД, FeS.
Комплекс III (QН2-дегидрогеназа):
цитохромы b и с1, FeS.
Комплекс IV (цитохром с оксидаза):
цитохромы a и a3, ионы меди.
14. Строение гема цитохромов а и с
Цитохром аЦитохром с
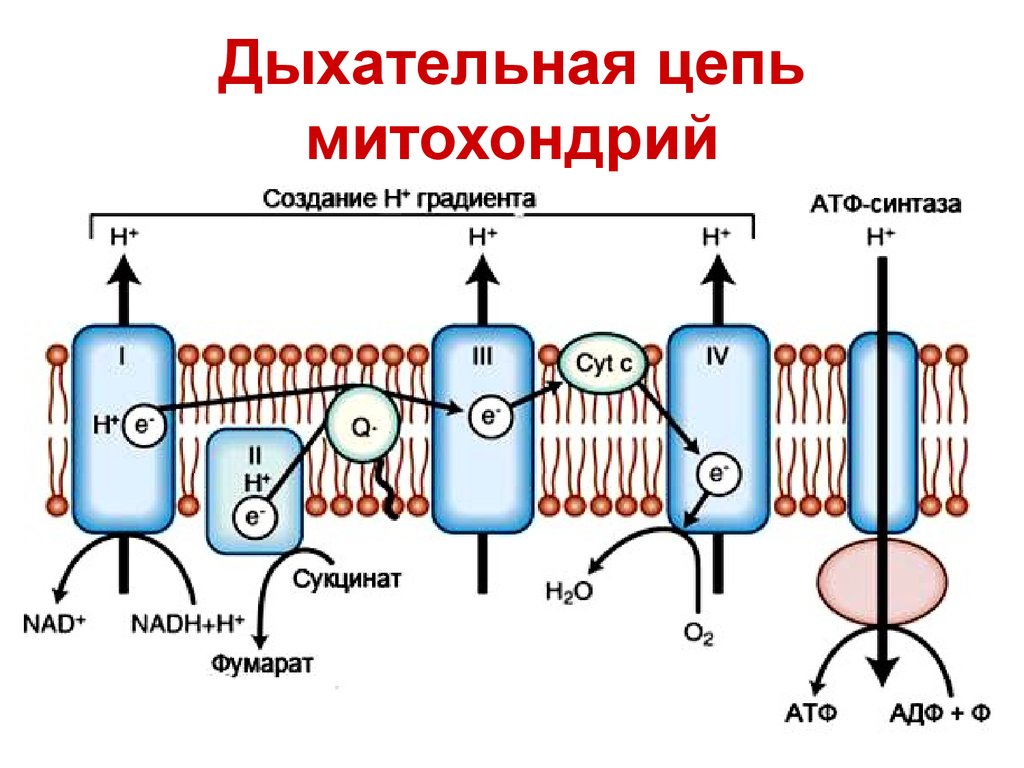
15.
Дыхательная цепьмитохондрий
16. АТФ-синтаза
17. Питер Деннис Митчелл – автор хемиосмотической концепции
(Нобелевская премия 1978 г.)18. Гипотеза П. Бойера и Дж. Уокера (Нобелевская премия, 1997 г.)
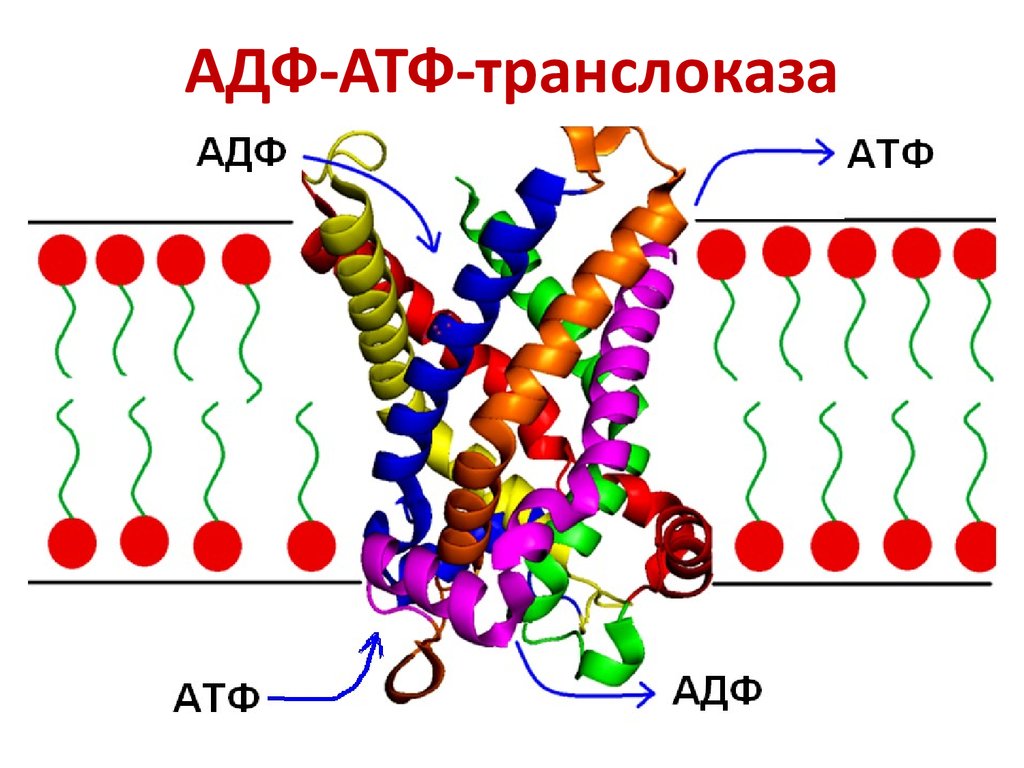
19. АДФ-АТФ-транслоказа
20. Энергетический заряд клетки (ЭЗК):
1/2[ÀÄÔ] [ÀÒÔ]ÝÇÊ
[ÀÌÔ] [ÀÄÔ] [ÀÒÔ]
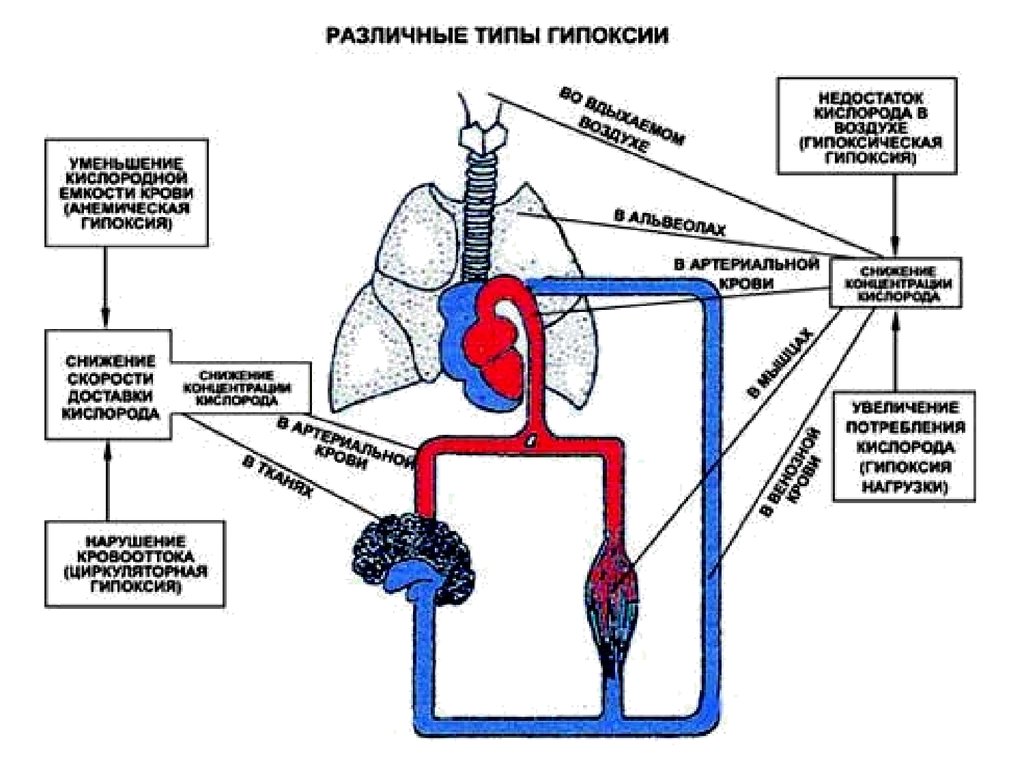
21. Гипоэнергетические состояния
1. Алиментарные2. Гипоксические:
- экзогенная гипоксия
- легочная (дыхательная) гипоксия
- гемодинамическая гипоксия
3. Митохондриальные.
22.
23. Разобщение дыхания и фосфорилирования
24.
25. Бурый жир
26. Разобщение дыхания и фосфорилирования
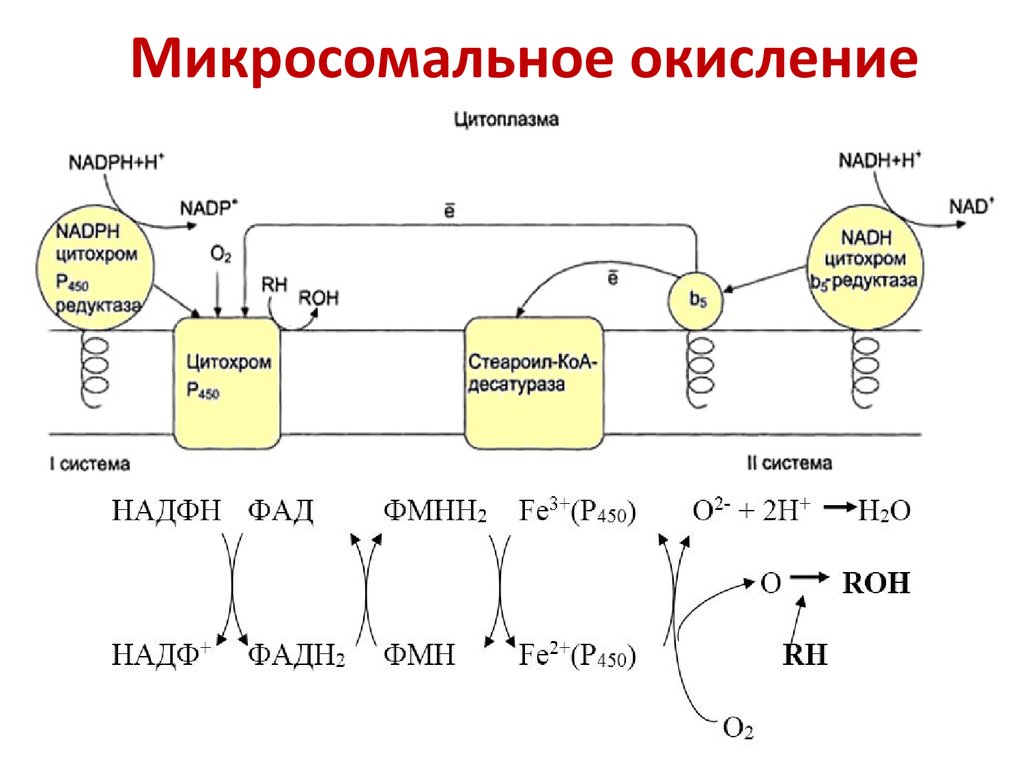
27. Микросомальное окисление
RH + O2 + NADPH + H+ → ROH + H2O + NADP+1. NADPH-P450 - цитохром Р450- редуктаза,
цитохром Р450
2. NADH-цитохром-b5 редуктаза, цитохром b5,
стеароил-КоА-десатураза
Цитохром Р450
28. Микросомальное окисление
29. Примеры реакций, катализируемых цитохромом Р-450
30. Изоферменты цитохрома Р-450
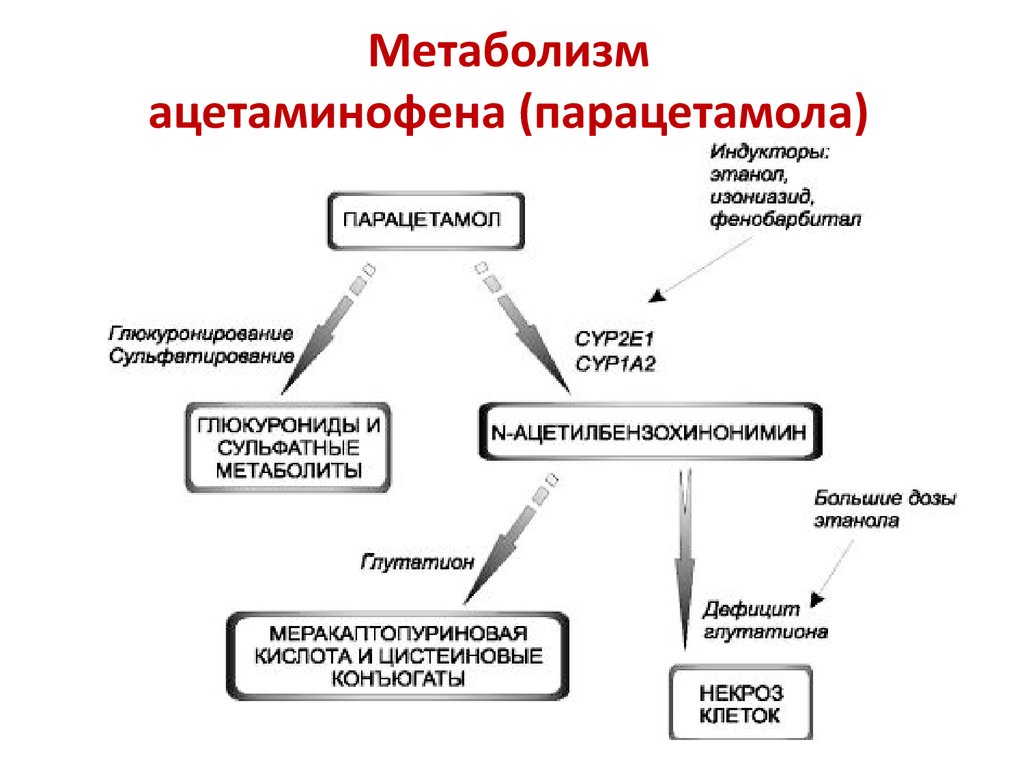
31. Метаболизм ацетаминофена (парацетамола)
Метаболизмацетаминофена (парацетамола)
32. Кислород и его активные формы
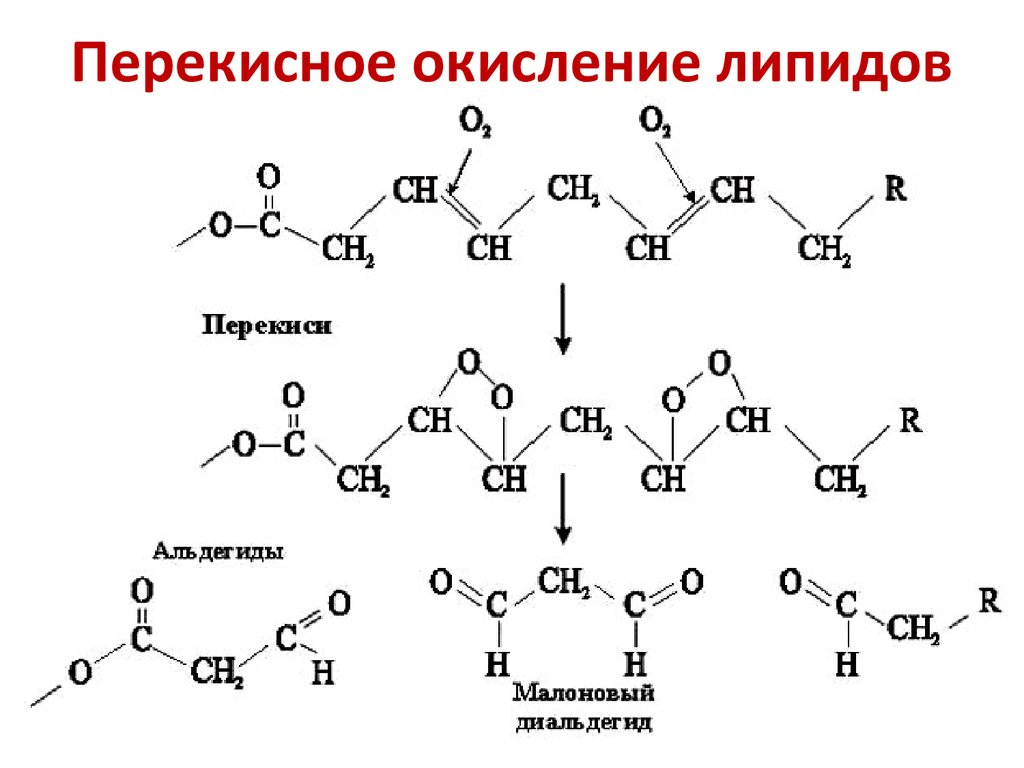
33. Перекисное окисление липидов
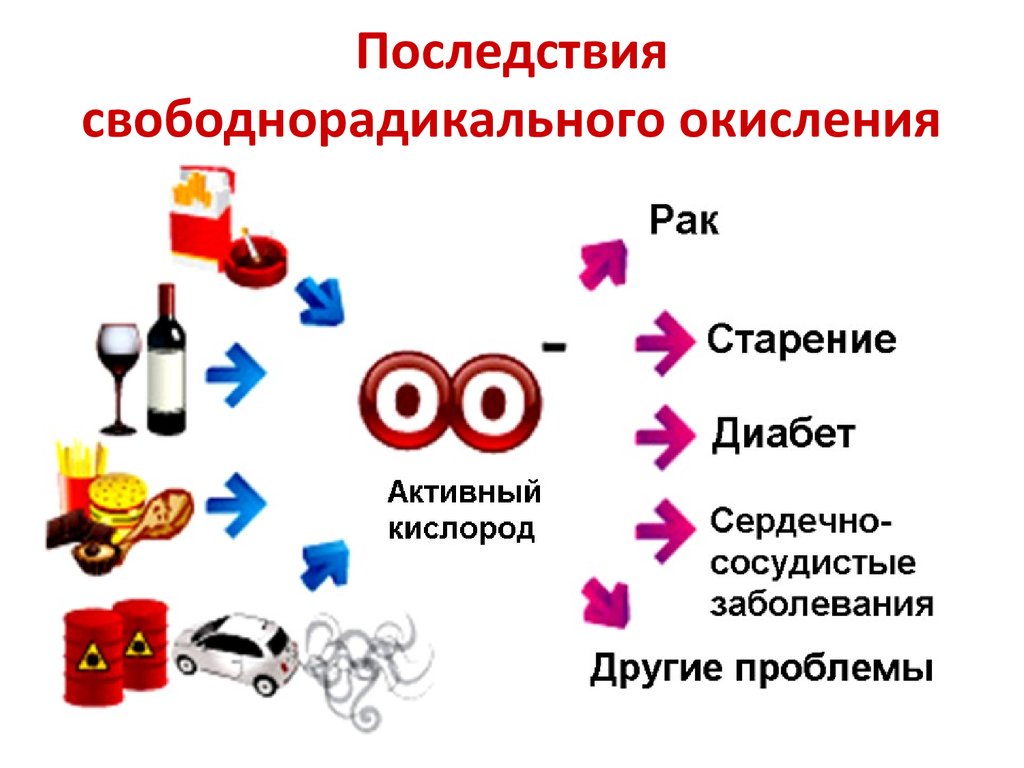
34. Последствия свободнорадикального окисления
35. АНТИОКСИДАНТНАЯ СИСТЕМА
Ферментативные АОНеферментативные АО
Первичные Е
(СОД, каталаза,
глутатионпероксидаза)
Жирорастворимые
(витамины Е, К, А,
каротиноиды)
Вторичные Е
(глутатионредуктаза,
глюкозо-6фосфатдегидрогеназа)
Водорастворимые
(витамин С,
флавоноиды, пептиды
(глутатион, карнозин,
таурин), Se, Zn
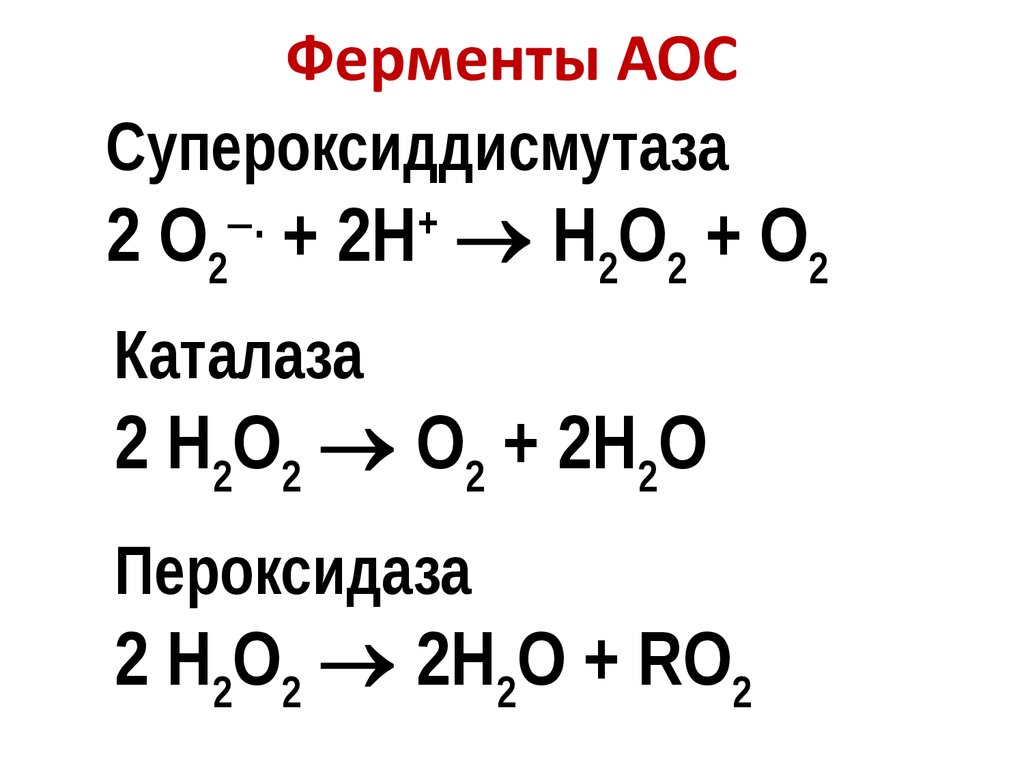
36. Ферменты АОС
Супероксиддисмутаза2 O + 2Н H2O2 + O2
.
2
+
Каталаза
2 H2O2 O2 + 2H2О
Пероксидаза
2 H2O2 2H2О + RO2
37. Глутатион как компонент антиоксидантной системы
38. Механизм действия антиоксидантов
39. Болезнь Паркинсона
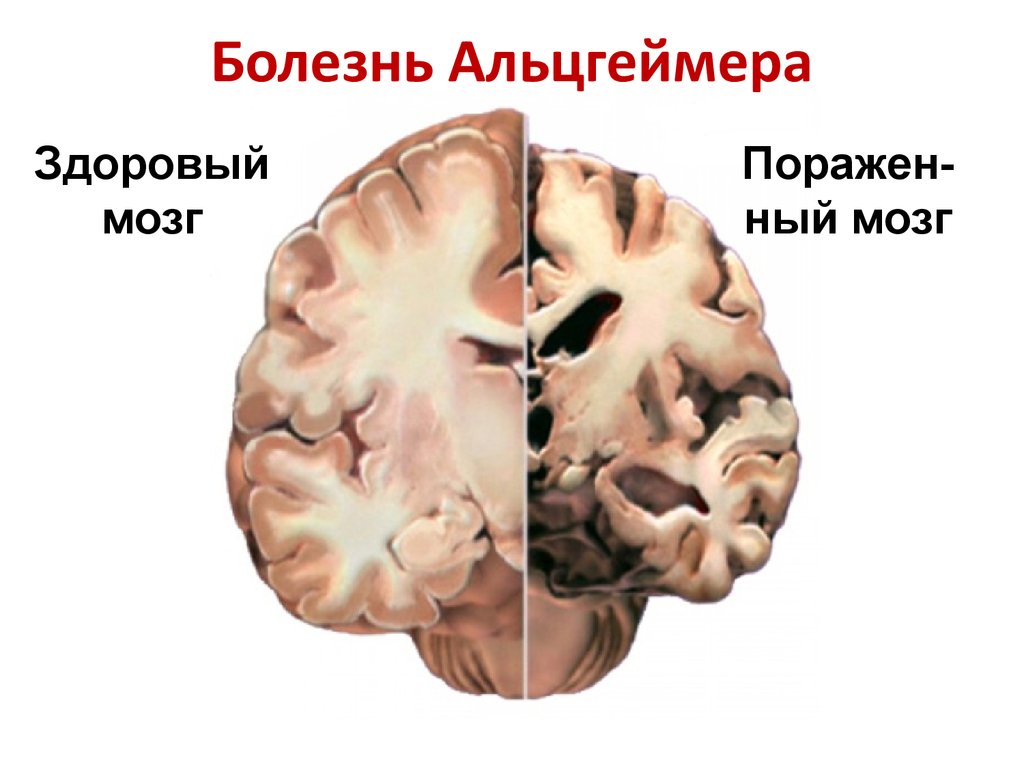
40. Болезнь Альцгеймера
Здоровыймозг
Пораженный мозг






















 biology
biology chemistry
chemistry








