Similar presentations:
Газовая хроматография
1.
Газовая хроматографияЛектор
доцент Шаповалова Елена Николаевна
2.
Газовая хроматография – метод разделения иопределения летучих термостабильных
соединений
Разделение проводится в виде газа или паров
В качестве подвижной фазы используется газ, для
которого характерна малая вязкость и большие
скорости диффузии
• Большая эффективность
• Экспрессный и многокомпонентный анализ
3.
Достоинства газовой хроматографии :- сравнительная
простота аппаратурного оформления;
- весьма широкие границы применимости (можно определять
соединения, для которых достигается давление насыщенного пара
0,001-1 мм рт.ст.);
- возможность определения с высокой точностью малых количеств
газов органических соединений;
- быстрота анализа;
- широкий выбор сорбентов и неподвижных фаз;
- большие возможности изменения условий разделения;
возможность
осуществления
химических
реакций
в
хроматографической колонке или детекторе, что расширяет круг
определяемых соединений (реакционная газовая хроматография);
- повышение информативности при сочетании с различными
инструментальными
методами
(масс-спектрометрией
и
ИК(Фурье)спектрометрией).
4.
• В основе хроматографического разделениялежат сорбционные процессы в неподвижную
фазу
• Сорбция – поглощение газов, паров твердыми
или жидкими поглотителями
• Сорбаты – поглощаемые вещества
• Варианты газовой хроматографии:
• Газо-адсорбционная
Неподвижная фаза
Адсорбенты – твердые вещества с развитой
поверхностью
• Газо-жидкостная
Неподвижная фаза
Абсорбенты – вязкие жидкости
5.
ВЗАИМОДЕЙСТВИЯ В ГАЗОВОЙ ХРОМАТОГРАФИИОриентационное (силы Кеезома) возникает при взаимодействии
молекул, обладающих постоянными диполями
Индукционное (силы Дебая) возникает при взаимодействии
молекул с постоянным диполем с молекулами, не обладающими
постоянным диполем; возникает наведенный диполь. Обычно это
слабые взаимодействия.
Дисперсионное (силы Лондона) обусловлено тем, что
неполярные молекулы обладают виртуальными диполями,
индуцирующими у других неполярных молекул диполи такого рода.
Уменьшается с увеличением валентных электронов и
электрического момента взаимодействующих молекул.
Специфическое обусловлено либо комплексообразованием,
либо образованием водородной связи
F-H…F O-H…O N-H C-H…C
6.
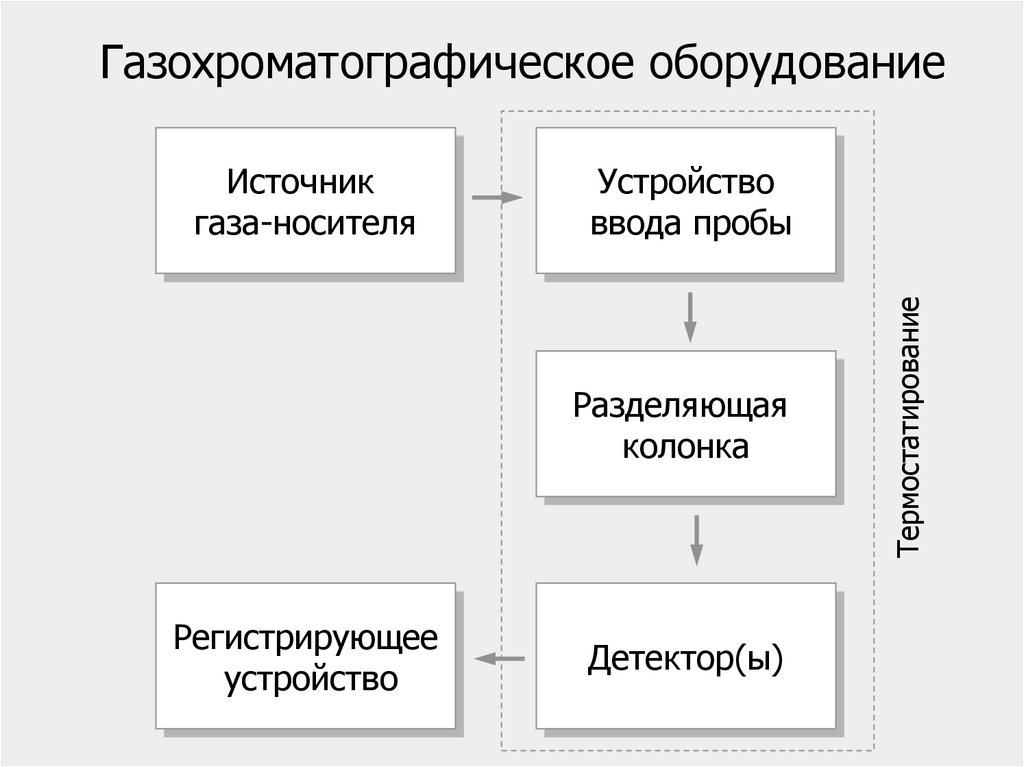
Газохроматографическое оборудованиеУстройство
ввода пробы
Разделяющая
колонка
Регистрирующее
устройство
Детектор(ы)
Термостатирование
Источник
газа-носителя
7.
Газ-носительНе должен химически взаимодействовать с
компонентами пробы или частями хроматографа
Быть термически инертным
Удовлетворять требованиям детектирования
Иметь высокую чистоту
Азот, Водород, Гелий, Аргон
(из баллонов или генераторов газов)
Необходимость очень точного дозирования
(расхода) газа
8.
9.
Ввод пробыИспаритель:
1- корпус, 2 – канал испарения
пробы,
3 – термостойкое уплотнение из
резины,
4 – прижимная гайка
10.
Условия ввода пробы•минимальный объем
•количество вещества в пробе должно быть намного
меньше емкости колонки
•проба не должна быть направлена навстречу потоку
газа-носителя и искажать характеристики потока
•проба должна быть воспроизводима с большой
степенью точности
•вещество должно испаряться без разложения
•смеси компонентов должны вводиться и испаряться
без изменения состава
11. Дозаторы
Шприцы (газовые и микрошприцы)Пробоотборная петля
Специальные дозирующие устройства :
• дозирование давлением,
• микродозатор (микродиппер) < 1 мкл
• устройство для ввода твердых проб
• герметичные пробоотборные
колонки
12. Парофазный анализ
Позволяет судить о составе конденсированной фазы(жидкость, твердое вещество) по химической информации,
содержащейся в газовой фазе
• Две группы методов парофазного анализа:
• Статические – равновесные газовая и конденсированная
фазы образуют замкнутые системы
• Динамические – контакт между фазами происходит в
открытой системе и газ продувается через слой жидкости
или гранулированной твердой фазы
А.Г. Витенберг, Б.В. Иоффе Газовая экстракция в хроматографическом
анализе. Л., Химия , 1982
13. Парофазный анализ
Коэффициент распределенияp
Ki
i pi
р – общее давление в системе
γi- экстраполированный коэффициент
активности аналита
рi –парциальное давление паров аналита
14.
Парофазное дозирование проб1. Отбор с помощью шприцев
2. Введение пробы с помощью газового крана,
дозируемый объем которого заполняется за счет
изменения давления в системе
3. Пневматическое парафазное дозирование проб
осуществляется созданием перепада давления между
сосудом с анализируемым образцом и
хроматографической колонкой
15. Оборудование для парофазного анализа
Парофазнаяустановка «Фаза»
(Россия)
16.
Детекторыв газовой хроматографии
17.
Требования к детекторам вхроматографии
Высокая чувствительность
Малая инерционность
(зона компонента проходит через детектор
за секунды или менее)
Линейная зависимость «отклик-концентрация»
Воспроизводимость результатов
Простота в использовании и доступность
18.
ДетекторыИнтегральный
-регистрирует изменение во времени
суммарного количества всех компонентов
Дифференциальный
–
измеряет
мгновенную
концентрацию кмпонентов
Время
Время
Концентрационный сигнал определяется текущей концентрацией в
ячейке и многократно регистрируется, зависит от скорости потока
Детектор такого типа – катарометр
Потоковый детектор регистрирует сигнал однократно, сигнал
определяется мгновенным значением концентрации, не зависит от
скорости потока
Пример такого детектора – пламенно-ионизационный детектор
19. Катарометр (детектор по теплопроводности)
Смин 10-4%Принцип действия основан на измерении температуры
нагретых нитей (чувствительных элементов) в зависимости
от теплопроводности окружающего газа, определяемой его
составом
Сигнал детектора основан на различии в теплопроводности
чистого газа-носителя и смеси газа-носителя с веществом:
λ – теплопроводность, α – молярная доля компонентов
20.
Ячейка катарометра21.
Факторы, влияющие начувствительность катарометра
- отношение ∆λ/λ (зависит от газа-носителя;
удельного сопротивления
термочувствительных нитей; уменьшается с
увеличением температуры)
- напряжение по диагонали моста
(S=kU2 )
- величина фонового сигнала
- геометрические характеристики
термочувствительного элемента
22.
Относительная теплопроводностьвеществ
Вещество
Четыреххлористый
углерод
Бензол
Гексан
Аргон
Метанол
Азот
Гелий
Водород
Относительная
теплопроводность
0.05
0.11
0.12
0.12
0.13
0.17
1.00
1.28
23.
Вариантыдетектора по теплопроводности
Термисторный ДТП
чувствительный элемент - термистор (шарик диаметром
0,5 мм из смеси окислов Mn, Co,Ni)
Преимущества: малый объем ячейки, высокий
температурный коэффициент
Недостаток – инерционность
Термохимический детектор
Преимущество – высокая чувствительность,
Недостаток – нестабильность, недолговечность
24.
Ионизационные детекторыПринципы ионизационного
детектирования
Сигнал – изменение ионного тока, вызванное
введением в детектор анализируемого вещества
Ионный ток возникает под действием источника
ионизации
и
электрического
поля
между
электродами детектора.
25.
Принципы ионизационного детектированияВ любой момент времени в детекторе скорость
образования заряженных частиц (ионов и
электронов)
равна
сумме
скоростей
рекомбинации и сбора заряженных частиц на
электродах детектора.
Плотность (концентрация) заряженных частиц,
либо
скорость
переноса
частиц
в
электрическое поле зависит от состава газа в
камере детектора
26.
Принципы ионизационного детектированияI,A
I
II
III
E
I – слабое поле, режим неполного сбора заряженных частиц;
ток определяется скоростью переноса частиц в направлении
поля
II – участок насыщения, полный сбор зарядов; ток
определяется скоростью образования зарядов
27.
Принципы ионизационного детектированияЗависимость сигнала ионизационного детектора от
концентрации вещества на первом (а) и втором (б)
участке вольтамперной кривой
28.
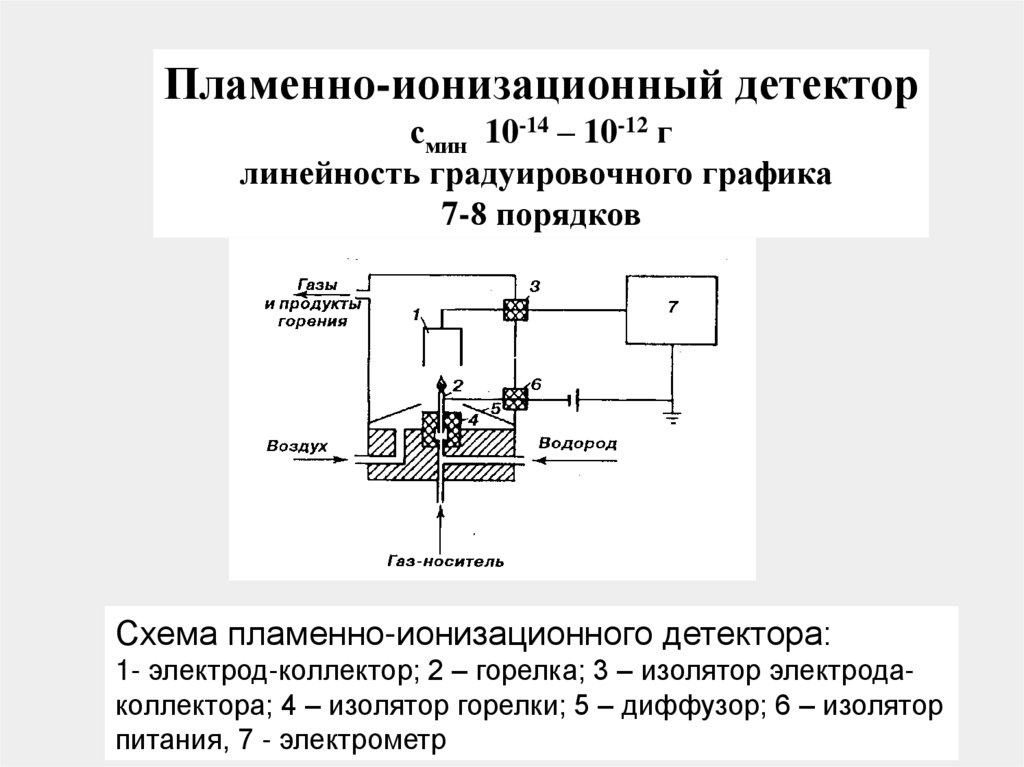
Пламенно-ионизационный детекторсмин 10-14 – 10-12 г
линейность градуировочного графика
7-8 порядков
Схема пламенно-ионизационного детектора:
1- электрод-коллектор; 2 – горелка; 3 – изолятор электродаколлектора; 4 – изолятор горелки; 5 – диффузор; 6 – изолятор
питания, 7 - электрометр
29.
Процессы в пламени1/2 H2 + O2 O +OH
Пиролиз вещества обеспечивает наличие СН
СН • + O CHO+ + e –
обеспечивает протекание тока
Негативное влияние оказывают
O, Hal, S, P, N
СН• + O2 CHO+ + O
CHO+ + OHCHO • + OH
CHO+ + H2O CO + H3O+
30.
Влияние природы определяемого веществана чувствительность ПИД
Зависит от эффективного углеродного числа (ЭУЧ)
Атом
Тип соединения
Вклад в ЭУЧ
С
С
С
С
С
С
О
О
О
О
Cl
Алифатические
Ароматические
Олефиновые
Ацетиленовые
Карбонильные
Нитрильный
Эфирный
Первичный спирт
Вторичный спирт
Третичный спирт
Два или более на один
алифатический С
На один олефиновый С
1,0
1,0
0,95
1,30
0
0,3
- 1,0
- 0,6
0,75
0,25
- 0,12
(на каждый)
+ + 0,05
Cl
31.
Термоионный детекторСмин 10-14г/сек
линейность ГГ - 102
Процессы в пламени
32. Пламенно-фотометрический детектор (ПФД)
• Принцип действия основан на возбуждениианализируемых соединений в обогащенном
по водороду пламени. При возвращении
возбужденных молекул в основное
состояние возникает эмиссия света на
определенной длине волны, характерной
для данного соединения.
• Интенсивность света характеристической
длины волны зависит от количества
определяемого соединения.
33.
• ПФД является селективным по отношению кфосфор- и серосодержащим веществам.
• Различие условий сжигания в ПФД и ДИП
состоит в том, что в ПФД пламя обогащено
водородом, в то время как в ДИП оно
обогащено кислородом.
34. Пульсирующий ПФД
работает в пульсирующем режиме,а не в режиме непрерывного пламени
Преимущества по сравнению с
обычным пламенно-фотометрическим детектором:
♦ Более высокая чувствительность
♦ Более высокая селективность
(по отношению к углеводородам)
♦ Пониженный расход водорода и сжатого воздуха
35.
Стадии работы ППФД36.
Детектор электронного захватаСмин 10-14г/сек
линейность ГГ - 102-5•102
Процессы, определяющие ток ионизации:
TG – газ-носитель
Схема детектора: 1 – электроды;
2 – радиоактивный источник
37.
Влияние состава аналитовна чувствительность ЭЗД
38.
Влияние состава аналитовна чувствительность ЭЗД и ПИД
39. Гелиевый ионизационный детектор
• Принцип действияГаз-носитель (инертный газ – гелий) ионизируется в камере с
высокой напряженностью электрического поля. Под действием
ионизирующего излучения электроны ускоряются и возбуждают
атомы инертного газа до метастабильного состояния
• А+e–
→ А* + e –1
При взаимодействии метастабильного возбужденного атома с
нейтральным или возбужденным атомом постороннего газа
образуются новые носители заряда и ток возрастает
Если присутствуют вещества, энергия ионизации которых ниже, они
также ионизируются в результате переноса заряда,
• А* + В → А + В* + e – (механизм Пеннинга)
с ростом их концентрации ток увеличивается
40. Гелиевый ионизационный детектор
Гелиевый ионизационный детектор –наиболее чувствительный детектор
для определения неорганических газов
Необходимые условия работы:
• использование особо чистых газов
• газонепроницаемые соединения
(стальные трубки и детектор)
1 - тритий на циркониевой фольге • удаление влаги из газовых соединений
2 – анод
• используют лишь ГАХ
3 – катод
4 – ввод газа из колонки
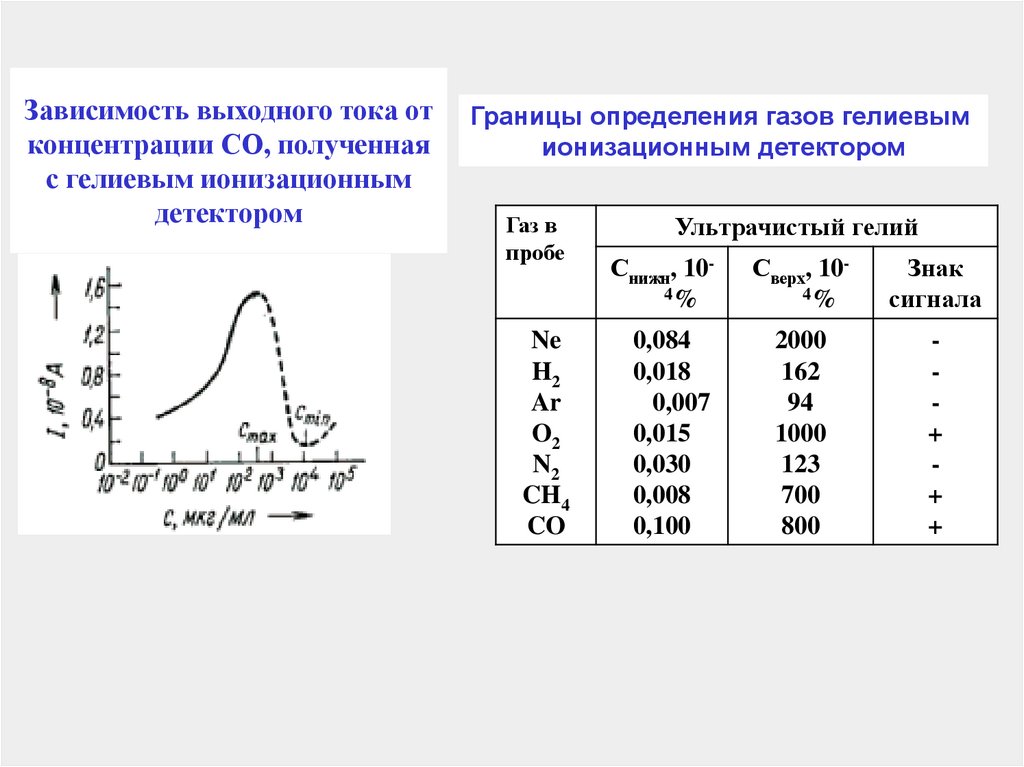
41. Зависимость выходного тока от концентрации СО, полученная с гелиевым ионизационным детектором
Границы определения газов гелиевымионизационным детектором
Газ в
пробе
Ne
H2
Ar
O2
N2
CH4
CO
Ультрачистый гелий
Снижн, 104%
0,084
0,018
0,007
0,015
0,030
0,008
0,100
Сверх, 104%
Знак
сигнала
2000
162
94
1000
123
700
800
+
+
+
42.
Фотоионизационный детекторПринцип действия
Молекулы аналитов ионизируются под действием УФизлучения и измеряется возникающий ионный ток
Схема фотоионизационного детектора:
1 – входной канал; 2 – основание детектора;
3 – ионизационная камера; 4 – коаксиальные
электроды; 5 – УФ-лампа; 6 – защитный кожух;
7 – изоляторы; 8 – канал для поддувочного
газа.
43.
Стадии ионизации:1. Прямая ионизация молекул определяемых веществ (АВ)
АВ + hν
АВ+ + e
2. Ионизация молекул АВ возбужденными молекулами
газа-носителя С
С + hν
АВ + С*
С*
АВ+ + e + С
3. Ионизация фотонами с промежуточным переходом
молекул АВ в возбужденное состояние
АВ + hν
АВ*
АВ*
АВ+ + e
4. Побочные процессы, ответственные за рекомбинацию
заряженных частиц
АВ+ + e
АВ+ + С–
АВ;
АВ + С
С+е
С-;
44.
Масс-спектрометрическийдетектор (GC-MS)
Детектирование по отношению массы иона к его заряду
(m/z)
Принцип
действия детектора:
при ионизации молекулы в вакууме образуется группа
характеристических ионов;
число образующихся ионов пропорционально количеству
поступающего вещества;
регистрируется изменение полного ионного тока, который
пропорционален числу ионов.
45. Масс-спектрометрический детектор
Одновременно с записью хроматограммы(зависимости полного ионного тока от
времени) в любой ее точке, обычно на
вершине хроматографического пика,
может быть зарегистрирован масс-спектр
(зависимость интенсивности ионного тока
от массы иона).
46.
Масс-спектрометрическийдетектор (GC-MS)
Достоинства
•Очень высокая чувствительность (фемтограммы)
• Возможность идентификации соединения
• Установление структуры неизвестного соединения
• Анализ биополимеров (до 100 000 Da)
• Возможность анализа очень сложных смесей
• Диапазон линейности градуировочного графика
- до 7 порядков
47.
Общие особенности ГХ и МС– в обоих методах анализ вещества проводится в
газовой фазе;
- количество вещества, необходимое для одного
анализа, составляет мкг;
- скорости выполнения анализов в обоих методах
могут быть согласованы таким образом, что в
процессе элюирования одного
хроматографического пика можно измерить
несколько полных масс-спектров.
48.
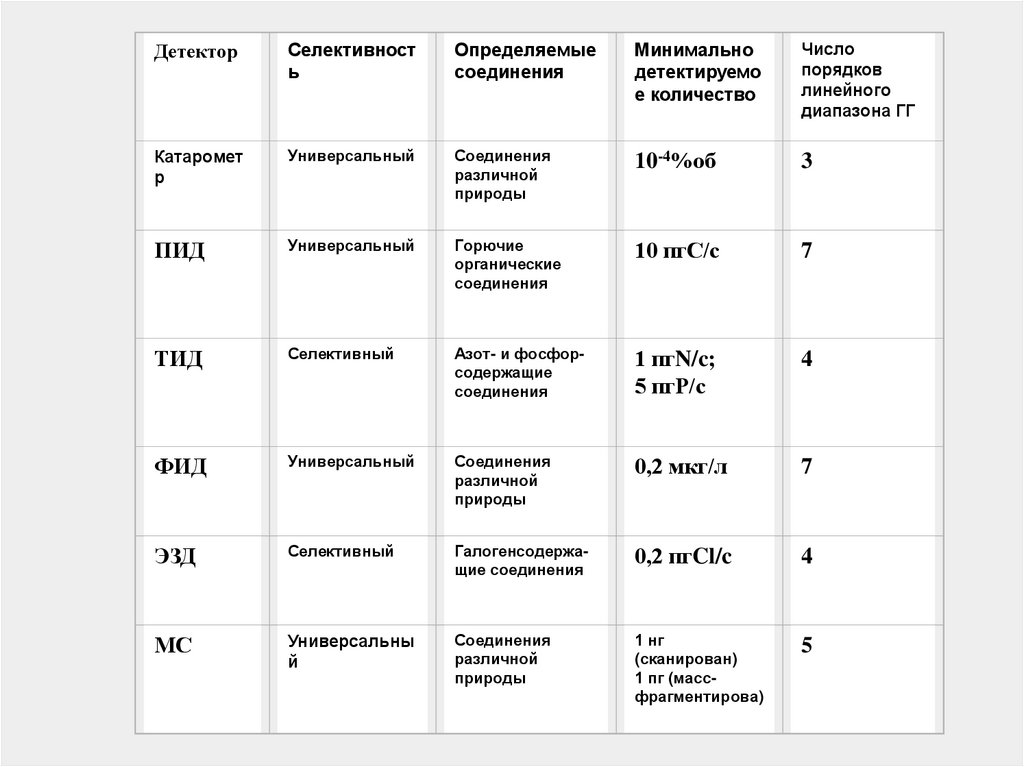
ДетекторСелективност
ь
Определяемые
соединения
Минимально
детектируемо
е количество
Число
порядков
линейного
диапазона ГГ
Катаромет
р
Универсальный
Соединения
различной
природы
10-4%об
3
ПИД
Универсальный
Горючие
органические
соединения
10 пгС/с
7
ТИД
Селективный
Азот- и фосфорсодержащие
соединения
1 пгN/c;
5 пгР/с
4
ФИД
Универсальный
Соединения
различной
природы
0,2 мкг/л
7
ЭЗД
Селективный
Галогенсодержащие соединения
0,2 пгCl/c
4
МС
Универсальны
й
Соединения
различной
природы
1 нг
(сканирован)
1 пг (массфрагментирова)
5
49.
Способы расчета концентрации (содержания)определяемого компонента
Метод абсолютной калибровки
Метод внутренней нормализации
Метод внутреннего стандарта
50.
Идентификация компонентов смеси51.
Легколетучие органические соединения, загрязняющие воздКласс
соединений
Индивидуальные
вещества
ПДК,
мг/м3
Возможные
варианты
детектирования
Альдегиды
Акролеин
Формальдегид
Капроновый альдегид
Ацетальдегид
Бензальдегид
0,03
0,035
0,02
0,01
0,02
ПИД, МС
Кетоны
Ацетон
Метилэтилкетон
0,35
0,1
ПИД, МС
Ароматические
углеводороды
Бензол
Метилбензолы
Нитробензол
Толуол
Нитротолуолы
Ксилолы
Стирол
Изопропилбензол
Нафталин
Антрацен
1,5
0,01-0,03
ПИД, МС
0,6
0,2
0,04
0,01
0,003
ПИД, ТИД, МС
ПИД
ТИД, МС
ПИД, МС
52.
ХлоруглеводородыДибензофуран
Хлороформ
1,2-Дихлорэтан
Метилхлороформ
Трихлорэтилен
Тетрахлорэтилен
1,1,1-Трихлорэтан
Тетрахлорид углерода
0,03
3
4
0,5
2
4
Трифторхлорметан (фр11)
Дифтордихлорметан
(фр12)
Трифтортрихлорметан
100
100
Спирты
Метанол
Этанол
Изобутанол
1
5
0,1
Олефины
Пентены
Гексены
0,4
Этилацетат
0,1
Фреоны
Эфиры
ПИД, ЭЗД, МС
ЭЗД, МС
ЭЗД, МС
8
ПИД, МС
ПИД, МС
ПИД, МС
53.
Газо-адсорбционнаяхроматография
Основана
на адсорбции веществ из газовой
фазы на твердом сорбенте
Обычно используют для разделения и
определения атмосферных газов
(O2, N2, Ar, CO2, H2S, CO, SОx, CH4.)
54.
Неподвижные фазы в ГАХУдельная
Химическая
поверхностная энергия
Структура
поверхности
характер взаимодействий адсорбент-адсорбат
Адсорбционная
активность
Удельная поверхность Структура
Адсорбента
Количественные характеристики
адсорбционных процессов
55. Классификация по химической природе
•Неорганические•Неорганические модифицированные
•Органические, пористые
56.
Классификация адсорбентов поих геометрической структуре
Адсорбент
Пористый
Непористый
тип 1
Кристаллический NaCl,
графитированная
термическая cажа
Однороднопористый
Однородноширокопористый,
тип 2
Гели кремневой
кислоты, дурапак С
Неоднороднопористый, тип 4
В ГХ не используют
Однородноузкопористый,
тип 3
Углеродные молекулярные сита,
Пористые угли, органические полимеры
57.
Структура пустот играет большую рольПараметры оценки структуры пор:
•геометрическая площадь поверхности стенок пор
•общий объем пор
•средний диаметр пор
•распределение пор по величине диаметра
58.
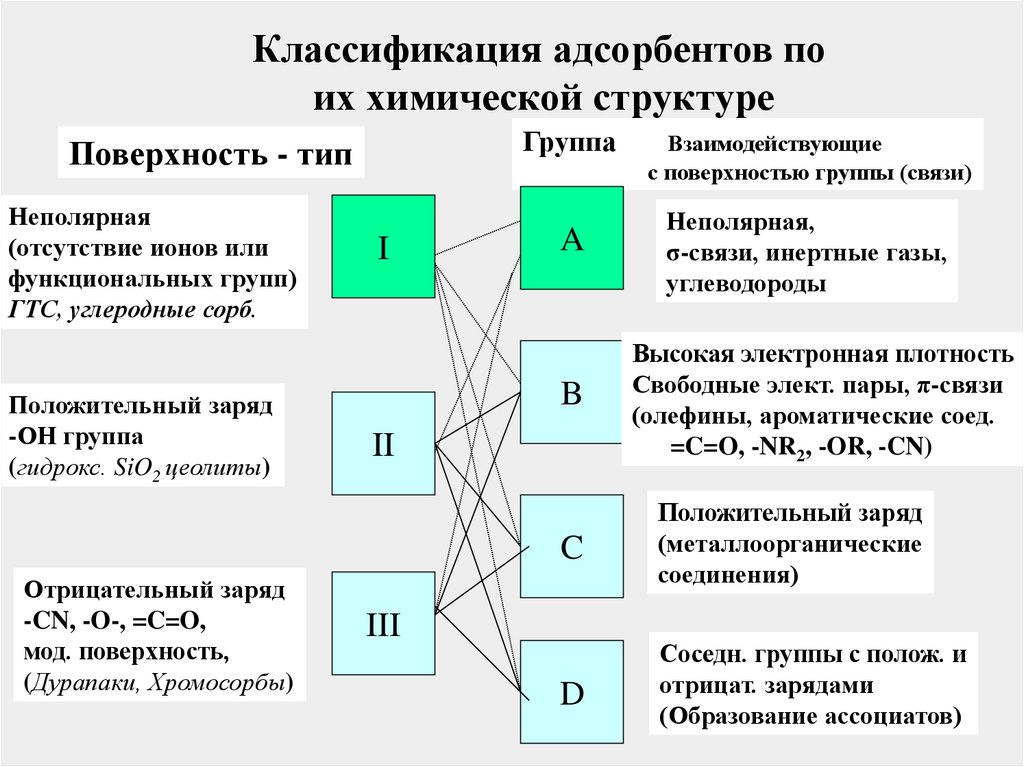
Классификация адсорбентов поих химической структуре
Группа
Поверхность - тип
Неполярная
(отсутствие ионов или
функциональных групп)
ГТС, углеродные сорб.
Положительный заряд
-ОН группа
(гидрокс. SiO2 цеолиты)
Отрицательный заряд
-CN, -O-, =C=O,
мод. поверхность,
(Дурапаки, Хромосорбы)
I
A
B
II
Взаимодействующие
с поверхностью группы (связи)
Неполярная,
σ-связи, инертные газы,
углеводороды
Высокая электронная плотность
Свободные элект. пары, π-связи
(олефины, ароматические соед.
=C=O, -NR2, -OR, -CN)
C
Положительный заряд
(металлоорганические
соединения)
D
Соседн. группы с полож. и
отрицат. зарядами
(Образование ассоциатов)
III
59.
Адсорбенты в ГАХ(углеродные материалы)
Адсорбент
Геометрическая
структура
поверхности
адсорбента
Величина
удельной
поверхност
и, м2/г
Химический
характер
поверхности
адсорбента
Разделяемые
классы
соединений
Графитированная
термическая
сажа
Непористая
6 – 12
Неспецифический, инертный
Предельные,
непредельные и
ароматические
углеводороды,
альдегиды,
кетоны, спирты,
амины
Активированный уголь
Развитая,
пористая
800 – 1000
Углеродные
молекулярные
сита
Микропористый
(исключительно
чистая
поверхность)
1000 – 1200
Неспецифический
Неспецифический
малополярный
Постоянные газы,
легкие
углеводороды
Низшие (С1-С5)
спирты и жирные
кислоты, вода
60. Коммерческие углеродные адсорбенты
Графитированные сажиКарбопаки В, С, Х,Y, Z
Углеродные молекулярные сита
Карбоксены, Карбоксивы
61.
62.
63.
Адсорбенты в ГАХ(полярные сорбенты)
Адсорбент
Геометрическая
структура
поверхности
адсорбента
Величина
удельной
поверхности,
м2/г
Химический
характер
поверхности
адсорбента
Разделяемые
классы соединений
Силикагель
Пористый
2 – 500
Специфический
Газы, средне- и
высококипящие
соединения с
высокой электронной плотностью
Цеолитовые
молекулярные
сита
Микропористый,
Регулярная система
пор: набор
одинаковых
«больших пустот»
связанных
однородными
микропорами
≈ 200
Специфический
гидрофильный
Газовые смеси
Оксид
алюминия
Пористый
Специфический,
гетерополярный
Сложные смеси
углеводородов
64.
Типы гидроксильных групп на поверхности силикагеляМодифицирование силикагеля:
Si
OH
+
Cl
Si(CH3)3
Si
O Si(CH3)3
+
H Cl
65.
Цеолитовые молекулярные ситаM2/nO•Al2O3•xSiO2•yH2O
Структура элементарной
ячейки цеолитов
Разделение газовой смеси на
молекулярном сите 5А: а) Mg-форме, б)
Li-форме
66.
Эффекты, определяющие адсорбционные свойствацеолитов
1. Стерический или геометрический
Внутрь пор цеолита могут попасть молекулы, диаметр которых меньше
или равен эффективной ширине поры применяемого цеолита
2. Термодинамический или энергетический
Из-за ионного гетерополярного характера внутренняя поверхность пор
электростатически взаимодействует с адсорбатом. Селективность можно
менять варьируя заряд, величину и положение катиона
3. Кинетический
Разделение может осуществляться вследствие различия в кинетике
сорбции, т.е. различия в скорости диффузии
67. Коммерческие полярные сорбенты
Цеолиты:NaA, NaX, CaA, CaX
Диатомитовые носители:
Хромосорбы, Целиты, Хроматроны,
Инертоны, Хезасорбы, Стерхамолы,
Цветохромы, Порохромы,
Сферохромы
68.
Адсорбенты в ГАХ(полимерные сорбенты)
Адсорбе
нт
(Хромосорб)
Матрица
Величина
удельной
поверхности,
м2/г
Полярность
Область
применения
101
Стирол-ДВБ
30 – 40
Неполярная
Эфиры, спирты,
кетоны,альдегид
ы гликоли
102
104
«
Полиакрила
т с сетчатой
структурой
300 – 400
400 – 500
«
постоянные
газы, НМС, КСС
Слабополярная
формальдегид,
серусодержащие
газы
Среднеполярная
Разделение
газов и
полярных
соединений
(воды, спиртов,
альдегидов,
кетонов,
гликолей)
«
107
100 – 200
69.
Схема получения пористых полимеровстирола и дивинилбензола (а) и дивинилбензола (б)
70. Коммерческие полимерные сорбенты
• Поропак Q, R, N, S• Haye Sep Q, N, R, P, S, A, B, C, D
• Хромосорб 101, 102, 103,104, 105, 106,
107, 108
• Полисорб 1, 10
• Тенакс
71.
Полимерный cорбент Тенакс- GCУдельная поверхность 20 м2/г, пред. температура 3750С
Поли-(2,6-дифенил-п-фениленоксид)
Преимущества:
- малое время удерживание, благодаря низкой удельной поверхности;
- устойчивая нулевая линия;
- отсутствие необратимого взаимодействия с полярными соединениями;
- устойчивость по отношению к кислороду и воде;
- стабильность
Недостаток:
- более низкая эффективность, чем при использовании сополимеров
стирола и дивинилбензола
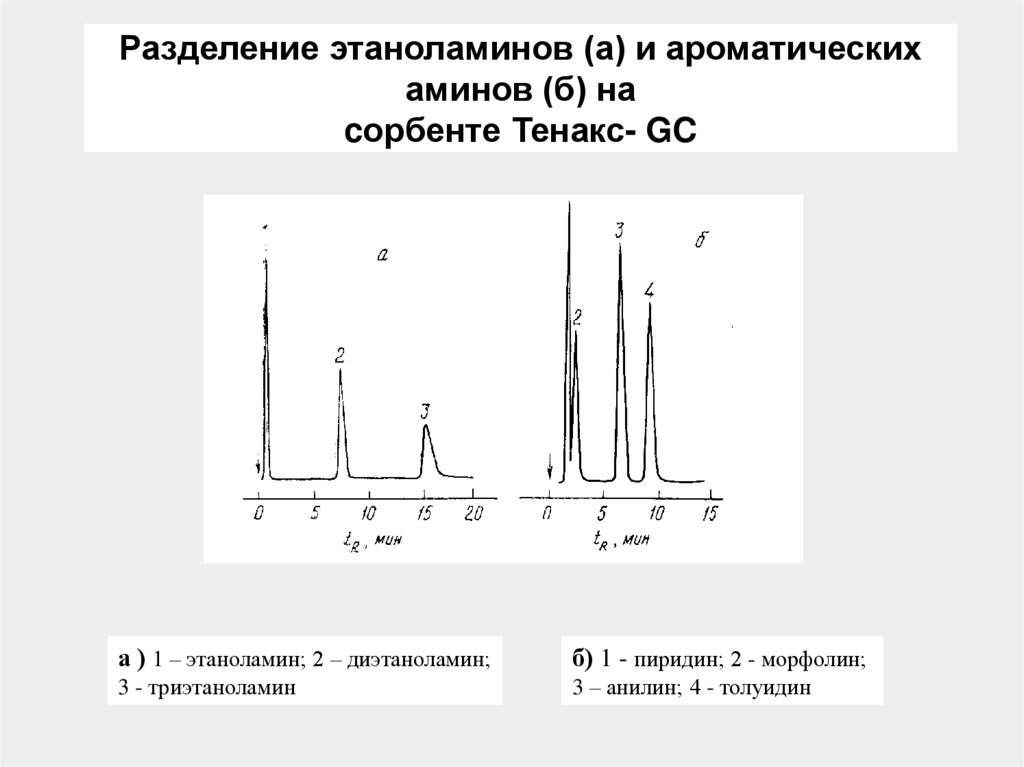
72. Разделение этаноламинов (а) и ароматических аминов (б) на cорбенте Тенакс- GC
а ) 1 – этаноламин; 2 – диэтаноламин;б) 1 - пиридин; 2 - морфолин;
3 - триэтаноламин
3 – анилин; 4 - толуидин
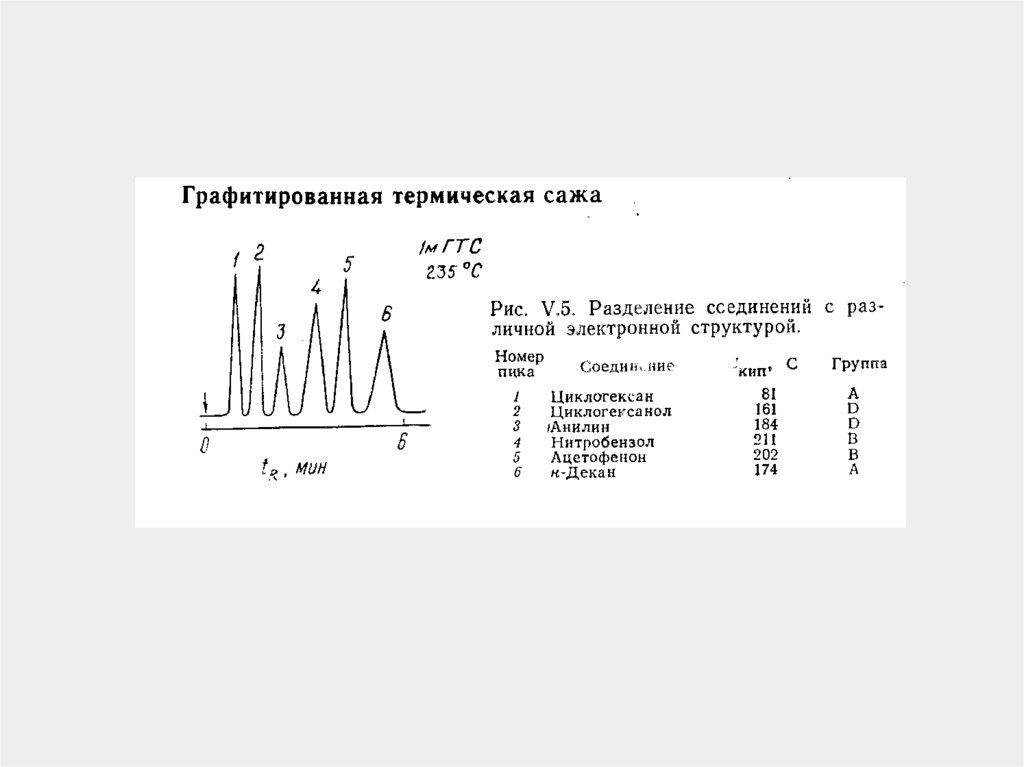
73.
Использование ГАХАнализ смеси углеводородов: 1 – метан;
2 – этан; 3 – пропен; 4 – пропан;
5 – изобутан; 6 – бутен-1; 7 – изо-бутен;
8 - н-бутан;9 – цис-бутен-2;
10 – транс-бутен-2
на адсорбенте стерлинг МТ.
74.
Использование ГАХSiO2
Углеродные сита
Разделение газообразных углеводородов на порасиле В (а)
и поропаке N (б)
75.
Разделение серусодержащихсоединений на порапаке QS
Программирование температуры,
начальная 300С
Определение примесей H2S, SO2,
и COS в воздухе
Неподвижная фаза – карбоксив S
1 – воздух, 2 - H2S, 3 - SO2
4 – COS.
76.
Достоинства и недостатки ГАХДостоинства
• Простой метод определения неорганических газов
• Возможна реализация дополнительного эффекта –
распределение молекул по размерам
• Пригоден для разделения несложных смесей
молекулярных органических веществ, стабильных
при очень высоких температурах (до 300 0С)
Недостатки
• Изотерма сорбции часто нелинейна
• Алюмосиликаты и цеолиты – кислоты Льюиса,
следовательно, реакционноспособны
• Неоднородность поверхности сорбента приводит к
«хвостованию» пиков
• Метод чувствителен к парам воды
77.
Газо-жидкостнаяхроматография
78.
Механизм основан на различном распределенииопределяемых компонентов в газовой и жидкой фазах
Селективность зависит
от температуры кипения вещества
и от его растворимости в неподвижной фазе
A/B – коэффициент селективности разделения
компонентов А и В
0
0
A/B = DA/DB = KA/KB = pB B / p A A
K=
p / p N
0
i
p - парциальное давление;
pi0
- давление насыщенного пара;
N - мольная доля;
- коэффициент активности
Чем ниже температура кипения вещества, тем слабее удерживание
• Чем лучше растворяется в-во в неподвижной фазе, тем сильнее
удерживание
79.
Требования к носителям в ГЖХ• Достаточно малый размер (20-40 мкм)
• Механическая прочность
• Легкая смачиваемость жидкостью
• Термостойкость и химическая инертность
80.
НосителиДиатомиты : SiO2 90-92%
Al2O3 4-5%
Fe2O3 0,1-2,0%
CaO 1,0-1,5%
MgO 0,4%
1 тип
S 2 м2/г Хроматон, Газохром,
Сферохром
2 тип
S 0,3 м2/г Кизельгур, Шималит
Стеклянные шарики
Силикагель
Политетрафторэтилен
Поверхность носителя
0,5 – 3,0 м2/г
Размеры пор
(0,5 – 1,5) 10 –3 мм
Активность носителя
Способы уменьшения
1) химическое модифицирование
обработка кислотами, щелочами,
хлорсиланами, алкидсиланами)
2) физическое модифицирование
насыщение анализируемыми
соединениями
81.
Сравнение активности носителей:а – необработанный, б – промытый кислотой,
в – промытый кислотой и обработанный
диметилдихлорсиланом
4
82.
Требования к неподвижной фазе в ГЖХ• Малая летучесть (Ткип на 2000C выше Т колонки)
• Устойчивость при рабочих температурах
• Химическая инертность
• Определенная растворяющая способность
(принцип «подобное растворяется в подобном»)
• Способность хорошо смачивать носитель
(образование тонкой пленки)
83.
Методы нанесения ЖНФ•Фильтрации
•Фронтальный
•Отгонки
•Пропитка в парах или
распыление на носитель
в «кипящем слое»
84.
Влияние степени пропиткина зависимость высоты,
эквивалентной теоретической
тарелке (ВЭТТ) от скорости
газа-носителя:
а – 45%, б – 30 %, в – 15%,
г – 5%
(шамотный кирпич 0,3 мм,
пропитанный н-гексадеканом)
85.
Полярностьсвойства, обуславливающие селективность за
счет физического взаимодействия молекул с
функциональными группами НФ
Включается сумма неразрывно связанных
взаимодействий, например, взаимная
ориентация диполей, индуктивные и
дисперсионные силы, образование водородных
мостиков
86. Индексы удерживания Ковача
Индекс удерживания вещества – умноженное на 100 числоатомов углерода в гипотетическом н-алкане с таким же
исправленным временем удерживания
- исправленное время удерживание вещества
исправленное время удерживания н-алкана, элюирующегося
до вещества
исправленное время удерживания н-алкана, элюирующегося
после вещества
87.
Система РоршнайдераΔI = Iполярн - Iнеполярн
ΔI= ax+by+cz+du+es,
где a -мера донорных сил переноса заряда,
b - мера донорных сил переноса протона,
с - мера акцепторных сил переноса заряда,
d - мера акцепторных сил переноса протона,
e - мера ориентационных взаимодействий,
факторы, характеризующие специфичность
анализируемых соединений
x,e,z,u,s - константы Роршнайдера
неподвижных фаз
88. Оценка полярности неподвижных фаз
P = (X + Y + Z + U + S)/5X = I(бензол) – индукционные взаимодействия
Y = I(бутанол) - протон-донорные и протонакцепторные взаимодействия
Z = I(нитропропан) – диполь-дипольные
взаимодействия
U = I(пентанон-2) - диполь-дипольные
взаимодействия
S = I(пиридин) – протон-акцепторные
взаимодействия
89.
Важнейшие неподвижные фазы90.
УГЛЕВОДОРОДЫНеароматические углеводороды
Сквалан
Парафиновое масло
Апиезоновые смазки
Ароматические углеводороды
Алкилнафталин
Полифениловый эфир
91.
СиликоныМетилсиликоны
Фенилсиликоны
Фторалкилсиликоны
Нитрилсиликоны
Полиэфирсиликоны
92.
Спирты , эфиры и производные углеводовПолигликоли
HO-CH2-[-CH2-OC-CH2-CH2-CO-CH2]n-CH2OH
HO-[-CH2-CH2-O0]n-H
Сложные эфиры
Фталаты
Адипаты
Фосфаты
Нитрилы и нитрилоэфиры
93.
Неподвижные фазы, применяемые для разделениясоединений различных классов
Класс соединений
Неподвижная фаза
Алкалоиды
Силиконы Е-30, F-1
Амины алифатические
Карбовакс 400 + КОН
Амины ароматические
Карбовакс 400 + КОН
Аминокислоты
Силиконы OV-1, OV-101
Эфиры жирных кислот
Нитрилсиликоны
Полихлорированные бифенилы
Метилфенилсиликоны
ПАУ
Метилфенилсиликоны
Гербициды
Метилсиликоны
Инсектициды
Силиконы SE-30, SE-54
Спирты С1-С5
Карбовакс 1500
Пестициды
Силиконы SE-30, SE-50
Фенолы
Силиконы, SP-1000
Углеводороды
Апиезоны L,M, силикон Е-52
Эфиры
Силиконы, карбоваксы
Металлорганические соединения
Силиконы
94.
Капиллярная газовая хроматографияРуденко Б.А., Руденко Г.И. Высокоэффективные
хроматографические процессы. Т.1.
Высокоэффективная газовая хроматография
Редактор К. ХАЙВЕР
95.
Колонки в газовой хроматографииКапиллярные –
внутренний диаметр
0.25-0.5 мм., l = 100 м
Неподвижная фаза
нанесена на стенки.
Высокая эффективность
(до 1*106 ТТ/м),
иногда недостаточная
селективность
Набивные (насадочные) –
внутренний диаметр
3-10 мм., l = 10 м
Неподвижная фаза
нанесена на сорбент.
Высокая селективность,
часто недостаточная
эффективность
(~ 1*105 ТТ/м)
96.
Вывод Голея:реализовать потенциальную высокую эффективность
газохроматографического процесса возможно только
при использовании колонки в форме гладкой трубки
с достаточно большим отношением длины к диаметр
97.
Критерий Рейнольдсаdv
Re
d — характеристический размер канала;
v — скорость течения; ρ — плотность среды;
η — ее вязкость.
характер течения любой среды резко изменяется от ламинарного
к турбулентному, когда критерий Рейнольдса достигает
«критического значения», равного приблизительно 2300
98.
Характеристики капиллярной колонкиДиаметр 0,25—0,50 мм.
Длина 25—50 м.
Перепад давлений 1—2 атм
Времена удерживания компонентов, не превышают 1—2
Количество газа 1—5 мл/мин
с линейной скоростью 0,5— 1,0 м/сек.
Значение критерия Рейнольдса 3—50
поток газа - строго ламинарный
99.
Эффективность, где
B
H C g u Cl u
u
B - продольная диффузия;
Cg , C l
- сопротивление
массопереносу в газовой и жидкой фазе
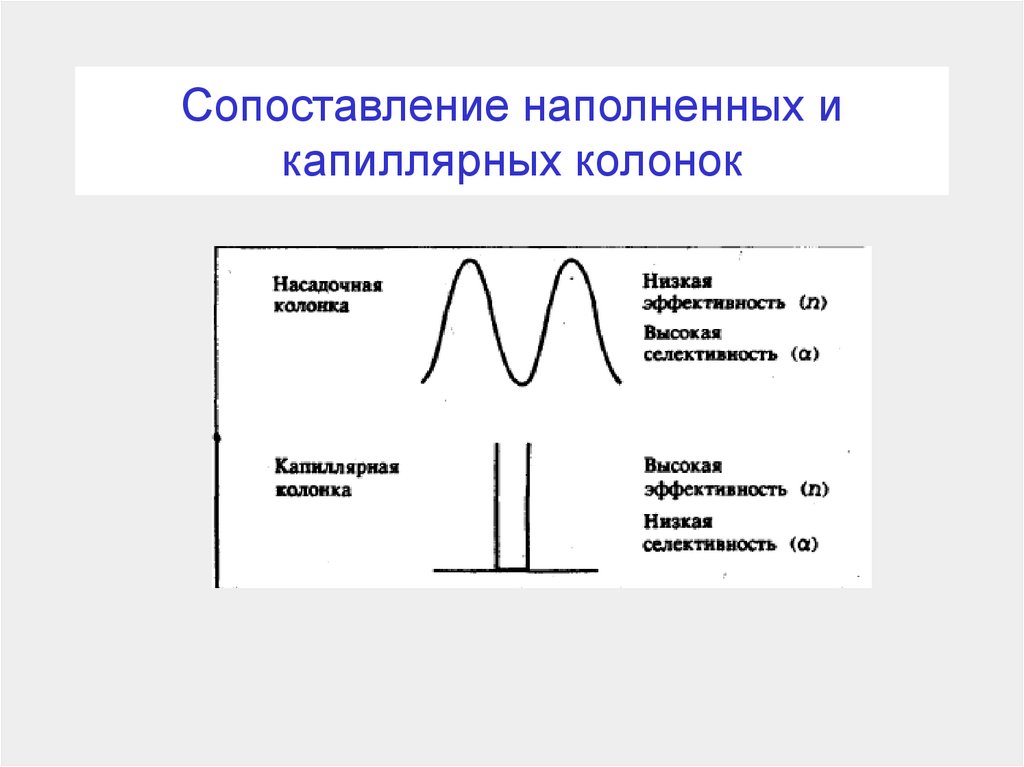
100. Сопоставление наполненных и капиллярных колонок
101.
Требования к капиллярам длякапиллярных колонок
– капилляр должен иметь определенную длину и
постоянный диаметр по всей длине, причем эти параметры
не должны изменяться под действием температуры и
давления;
– внутренняя поверхность капилляра должна быть
химически однородной, на ней не должно быть больших
трещин и пор;
– поверхность должна адсорбировать сорбаты, жидкие
неподвижные фазы и газ-носитель в минимальной степени;
– поверхность должна прочно и равномерно смачиваться
неподвижной фазой, т.е. на поверхности должен быть
гомогенный разделяющий слой неподвижной фазы;
– капилляры должны обладать необходимой механической
102.
Этапы подготовки капилярной колонки-изготовление капилляра;
-подготовка внутренней поверхности капилляра
травлением или дезактивацией;
-нанесение неподвижной фазы;
- кондиционирования и испытания капиллярной
колонки
103.
Устройство для изготовления капилляра104.
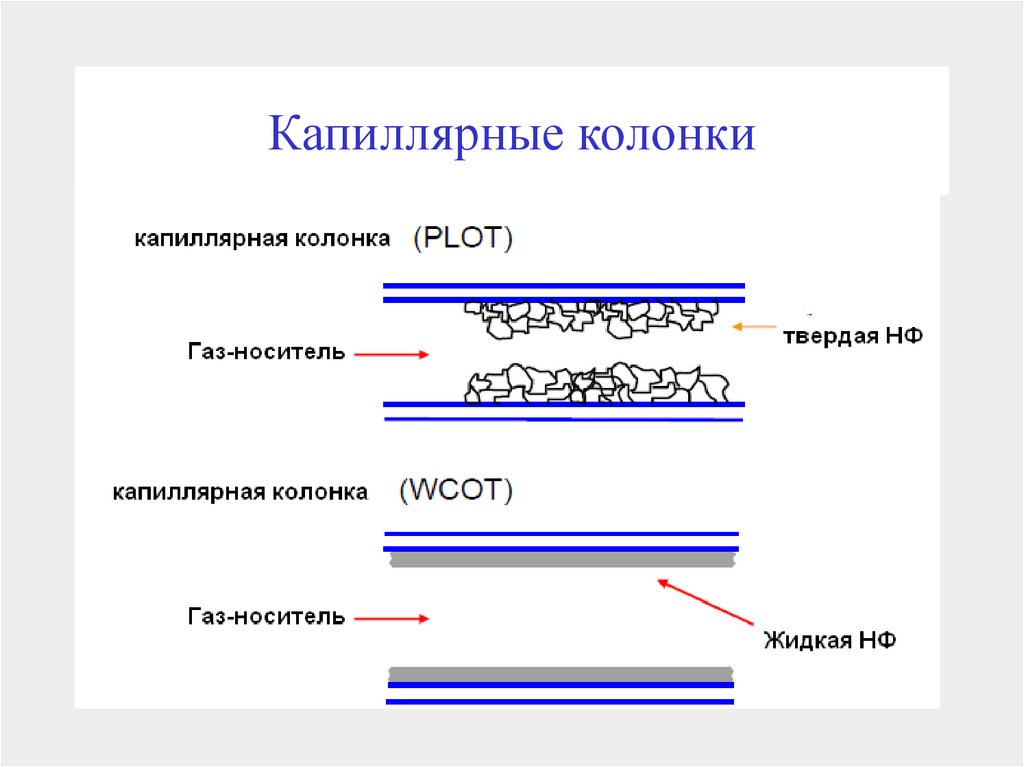
Классификация капиллярных колонок1. Капиллярные колонки(WCOT)
Тонкая пленка неподвижной фазы нанесена непосредственно
на внутреннюю поверхность колонки
толщина пленки 0,01-1 мкм;
внутренний диаметр и толщина стенок - n.10-n.100 мкм
2. Капиллярные колонки с пористым
слоем(SCOT)
На внутренних стенках расположен слой носителя, несущего
неподвижную фазу
толщина пленки 1 - 5 мкм
3. Капиллярные колонки с твердым
носителем (PLOT)
На внутренних стенках напылен слой твердого носителя
толщина пленки 10 мкм
4. Колонки с химически привитой неподвижной фазой
105. Капиллярные колонки
106.
Сравнение параметров длякварцевых WCOT
капиллярных колонок
107. Влияние природы газа-носителя на эффективность капиллярных колонок
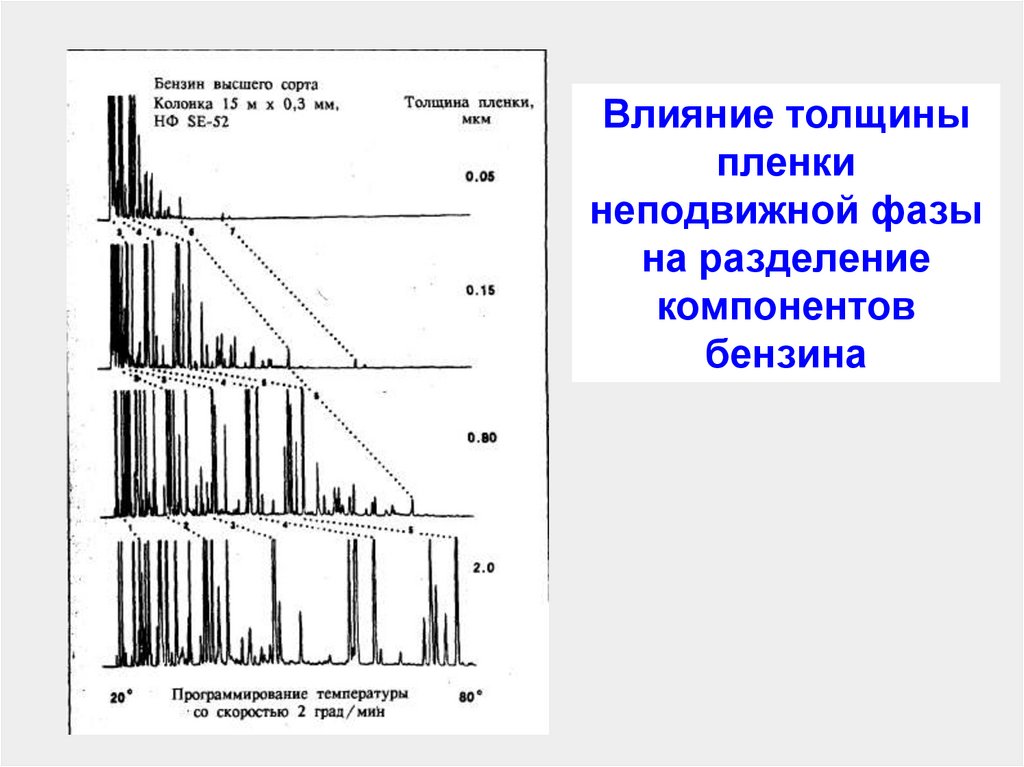
108.
Влияние толщиныпленки
неподвижной фазы
на разделение
компонентов
бензина
109.
Влияние промывкиколонки на разделение
пестицидов
110.
Изменение формы пиков додеканола и м-пентадеканапри увеличении объема пробы
111.
Недостатки КГХСложность изготовления капилляров
Сложность аппаратуры (деление
потока)
112.
Узел ввода пробы в капиллярную колонкуработающий в режиме деления потока
113. Способы ввода пробы в капиллярную колонку
Ввод пробы с делителем потока
Ввод пробы без делителя потока
Ввод пробы в колонку
Прямой ввод пробы (ввод мгновенно испаренной вне
колонки пробы)
• Ввод пробы с программированием температуры
испарителя
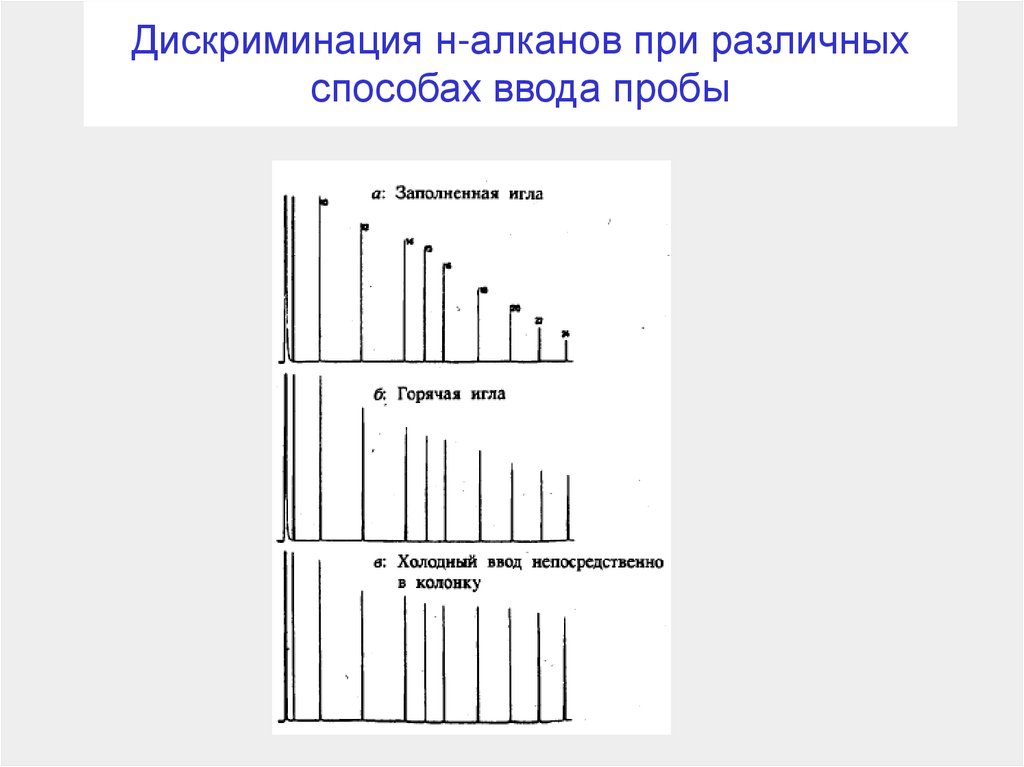
114. Дискриминация н-алканов при различных способах ввода пробы
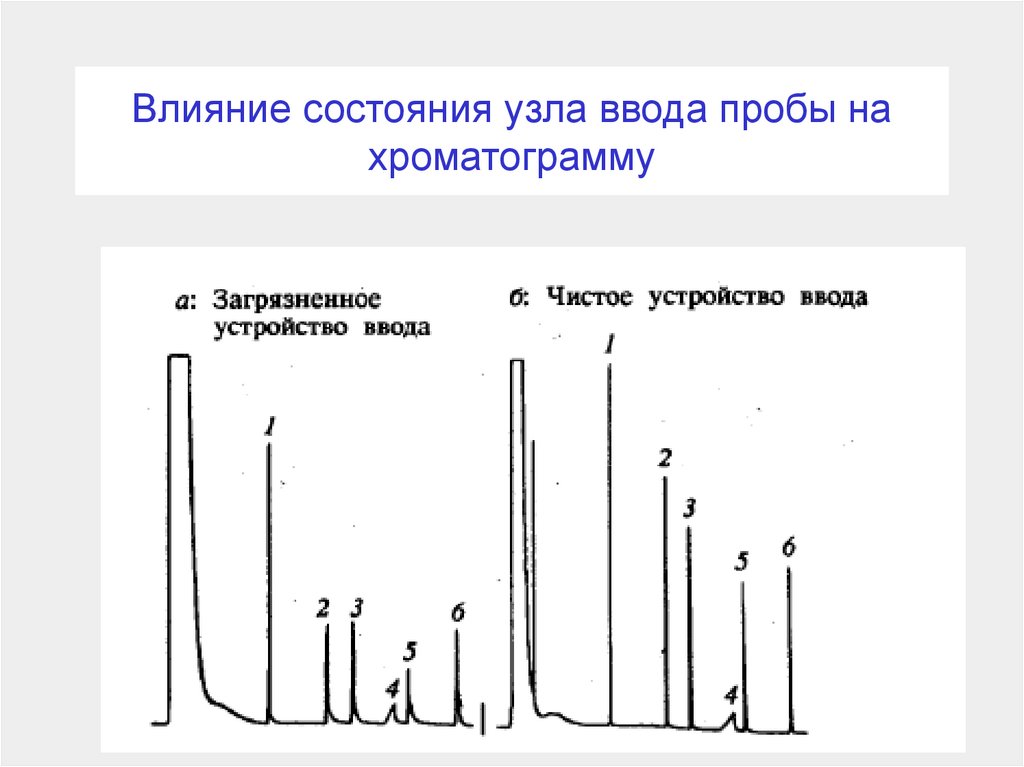
115. Влияние состояния узла ввода пробы на хроматограмму
116.
Хроматограмма извлеченных из почвы остаточных количеств азот/фосфорсодержащихпестицидов, полученная с селективным термоионным детектором:
1 – дихлофос; 2 – ЕРТС; 3 – бутилат; 4 – мевинфос; 5 – вернолат; 6 – пебулат; 7 – тебутирон;
8 – молинат; 9 – этопрон; 10 – циклоат; 11 – хлорпропам; 12 – атратон; 13 – симазин; 14 – прометон;
15 – атразин;16 – промазин; 17 – тербуфос; 18 – пронамид; 19 – диазинон; 20 – дисульфотон; 21 –
тербацил; 22 – метрибузин; 23 – симетрин; 24 – алахлор; 25 – аметрин; 26 – прометрин; 27 –
тербутрин; 28 – бромацил; 29 – метолахлор; 30 – тридемефон; 31 – МЖК-264; 32 – дигенамид; 33 –
стирофос; 34 – бутахлор; 35 – фенаминос; 36 – напрпамид; 37 – трициклазол; 38 – мерфос; 39 –
карбоксин; 40 – норфлуразон; 41 – гексазинон; 42 – фенаримол; 43 – флуридон.
117.
Разделение смеси ПАУ капиллярнойгазовой хроматографией
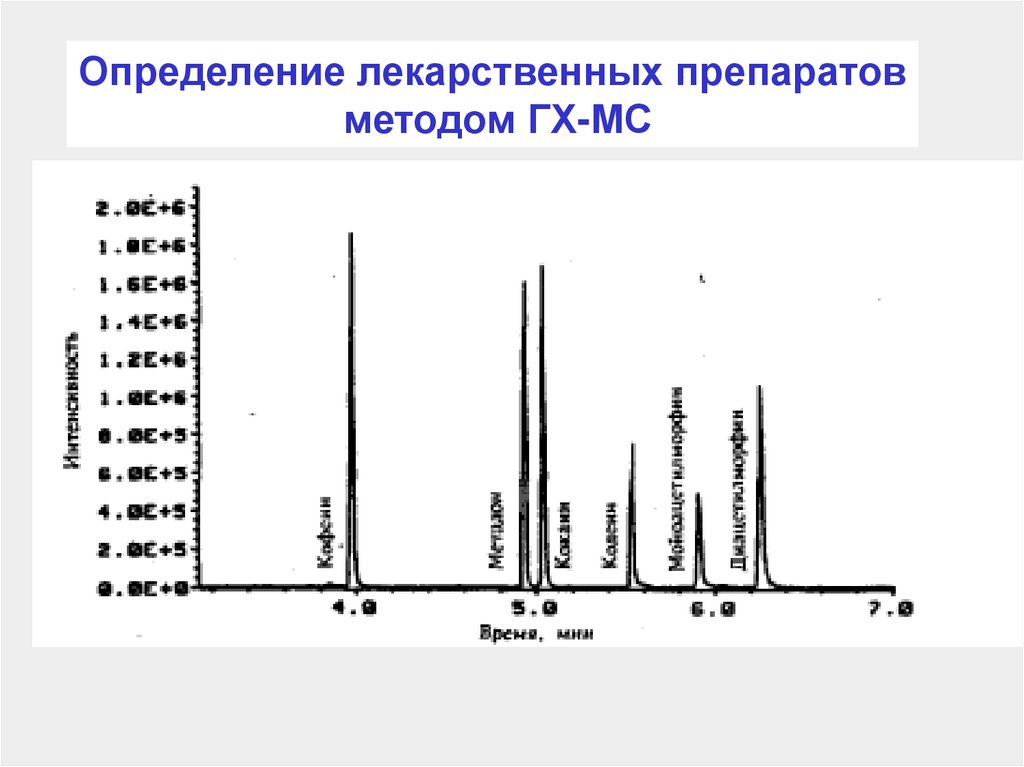
118.
Определение лекарственных препаратовметодом ГХ-МС
119.
Зависимость ВЭТТ (по ундекану) от линейнойскорости газа-носителя для капиллярных
колонок различного диаметра
120.
Поликапиллярные колонкиМикрофотографии поперечного среза ПКК.
Число капилляров 1375, диаметр – 40 мкм.
а) общий вид; б) при увеличении в 480 раз
121.
Зависимость ВЭТТ для металлоорганическихсоединений от скорости потока:
1,2,3 – капиллярная колонка;
4,5,6 – поликапиллярная колонка
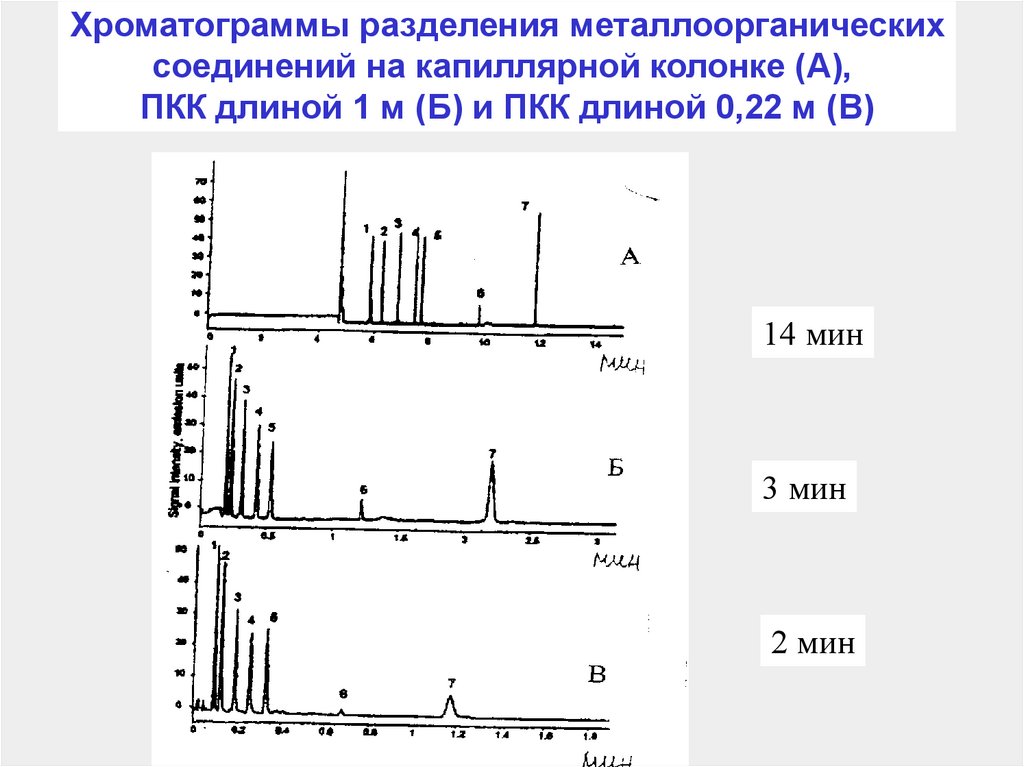
122.
Хроматограммы разделения металлоорганическихсоединений на капиллярной колонке (А),
ПКК длиной 1 м (Б) и ПКК длиной 0,22 м (В)
14 мин
3 мин
2 мин
123.
Разделение легких углеводородов на ПККРазделение углеводородов
на газоадсорбционной ПКК:
1 - метан; 2 – этилен; 3 – этилен;
4 – пропан; 5 – ацетилен;
6 – пропилен; 7 – изобутан;
8 – бутан; 9 – транс-бутен;
10 –изобутен; 11 – бутен-1;
12 – цис-бутен
15 сек
Разделение
метана(1), этана (2),
этилена (3), пропана (4) и
ацетилена (5)
на газоадсорбционной ПКК
8 сек
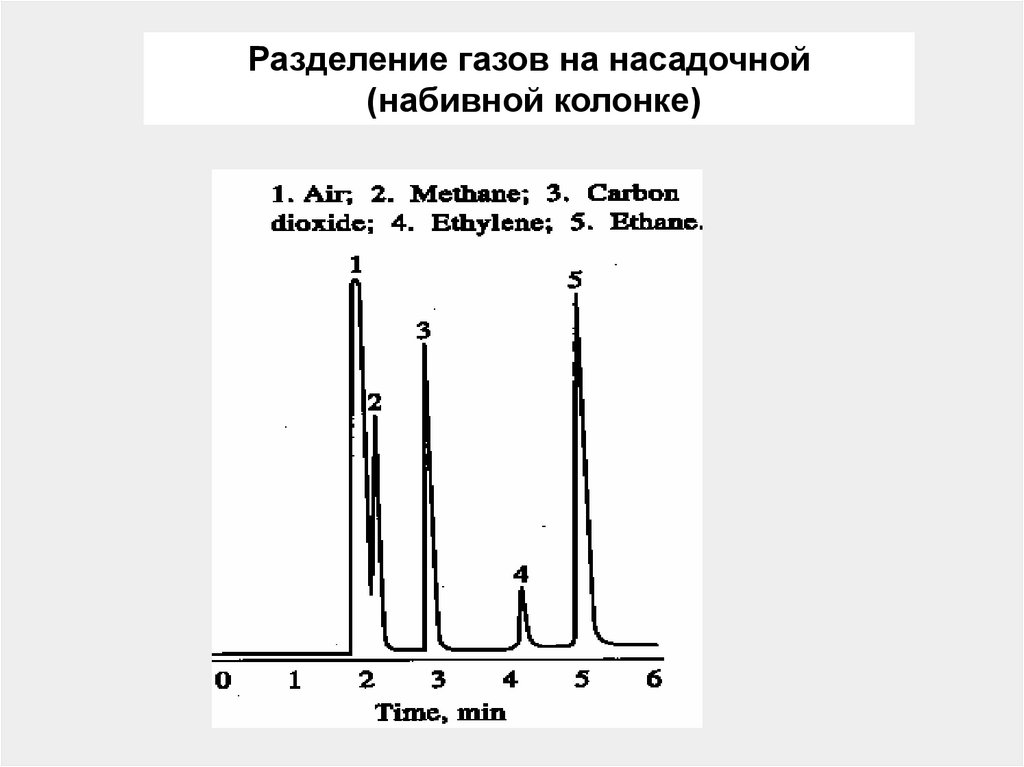
124.
Разделение газов на насадочной(набивной колонке)
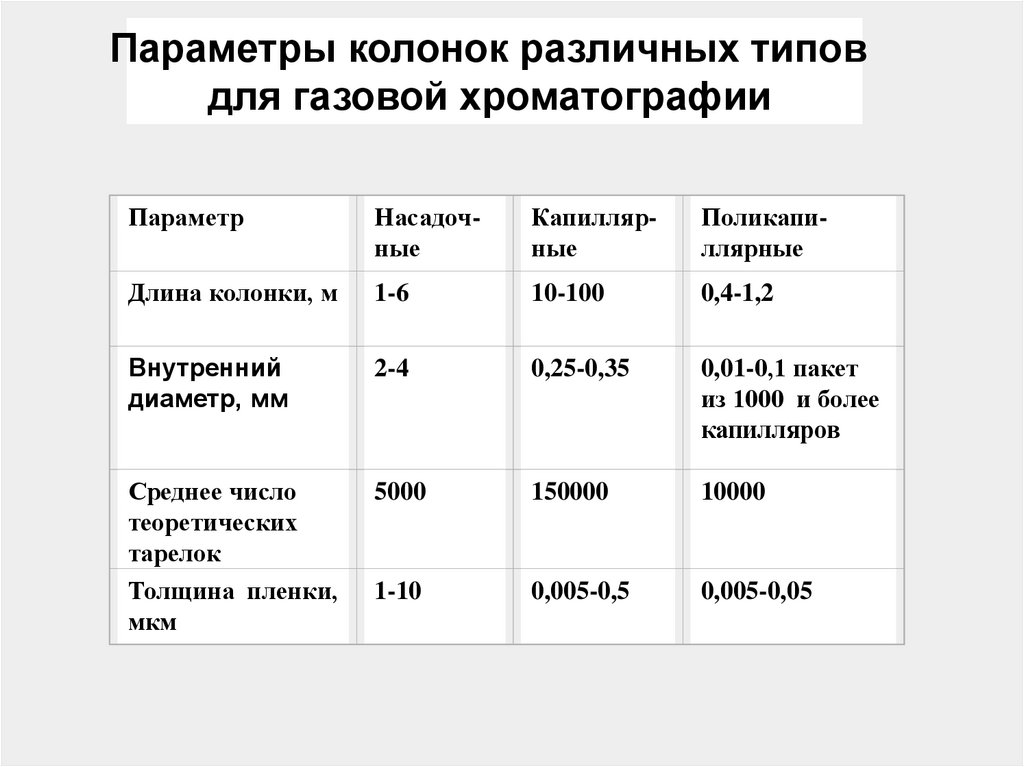
125.
Параметры колонок различных типовдля газовой хроматографии
Параметр
Насадочные
Капиллярные
Поликапиллярные
Длина колонки, м
1-6
10-100
0,4-1,2
Внутренний
диаметр, мм
2-4
0,25-0,35
0,01-0,1 пакет
из 1000 и более
капилляров
Среднее число
теоретических
тарелок
Толщина пленки,
мкм
5000
150000
10000
1-10
0,005-0,5
0,005-0,05
126.
Двумерная ГХ-ГХ хроматография127.
Двумерная ГХ-ГХ хроматографияСхематическое изображение направления
для четырехходового крана
128.
Двумерная ГХ-ГХ хроматографияХроматограмма лигроиновой
фракции нефти после
прохождения через
предколонку
Хроматограмма лигроиновой
фракции нефти после
прохождения через предколонку
и аналитическую колонки
129.
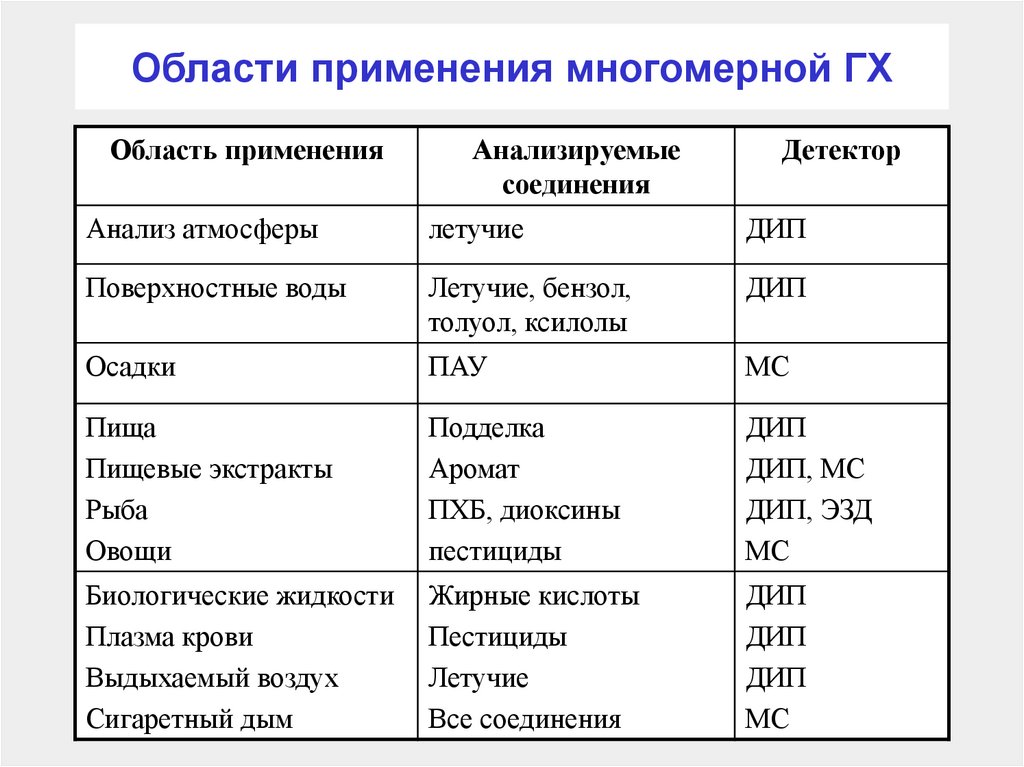
Двумерная ГХ-ГХ хроматография130. Области применения многомерной ГХ
Область примененияАнализируемые
соединения
Детектор
Анализ атмосферы
летучие
ДИП
Поверхностные воды
Летучие, бензол,
толуол, ксилолы
ДИП
Осадки
ПАУ
МС
Пища
Пищевые экстракты
Рыба
Овощи
Подделка
Аромат
ПХБ, диоксины
пестициды
ДИП
ДИП, МС
ДИП, ЭЗД
МС
Биологические жидкости
Плазма крови
Выдыхаемый воздух
Сигаретный дым
Жирные кислоты
Пестициды
Летучие
Все соединения
ДИП
ДИП
ДИП
МС
131.
Реакционная газовая хроматогафия (РГХ)Используются направленные химические
превращения:
нелетучих соединений в летучие,
неустойчивых соединений в устойчивые
132.
Варианты РГХХимическое образование
производных
Пиролитическая РГХ
Метод «вычитания»
133.
Положительные особенности РГХРасширение области применения ГХ
Улучшение разделения анализируемых соединений,
т.к индивидуальные свойства соединений более
заметно проявляются в образующихся производных,
чем в исходных соединениях
Существенное улучшение количественных
характеристик аналитических определений
Увеличение чувствительности детектирования
Лучшая сохранность хроматографической колонки
134.
Недостатки РГХУсложнение анализа
Ухудшение эффективности
разделения
Увеличение времени анализа
135. Условия получения производных
• Количественное (или, по крайней мере,воспроизводимое) образование производных
• Перевод всего аналита (95-100%) в получаемое
производное (заметно отличающееся по свойствам от
исходных веществ)
• Реакция должна проходить быстро и желательно по
простой и четкой методике
• Продукты дериватизации должны легко экстрагировать
из реакционной смеси
• Необходимо контролировать: полноту протекания
реакции; температуру и продолжительность
проведения дериватизации; термостабильность
производных; возможность протекания побочных
процессов; чистоту исходных реактивов; хорошую
селективность хроматографического разделения
136.
Основные способы полученияпроизводных
1. Получение силильных производных
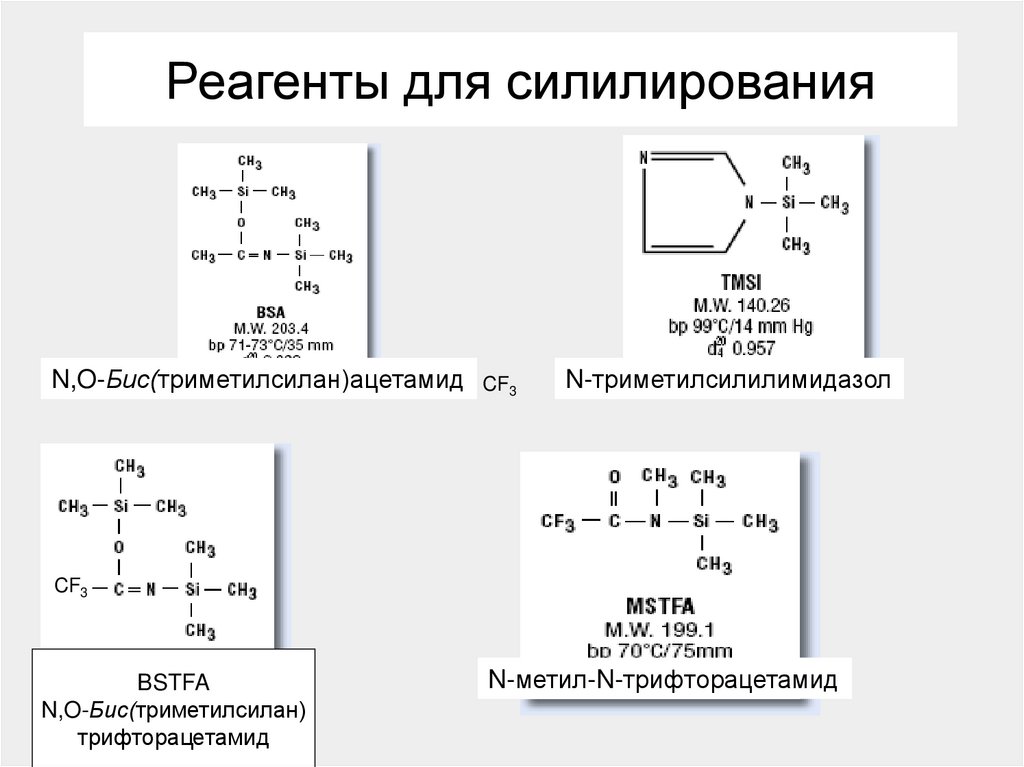
137. Реагенты для силилирования
N,O-Бис(триметилсилан)ацетамидCF3
N-триметилсилилимидазол
CF3
BSTFA
N,O-Бис(триметилсилан)
трифторацетамид
N-метил-N-трифторацетамид
138. 2. Алкилирование
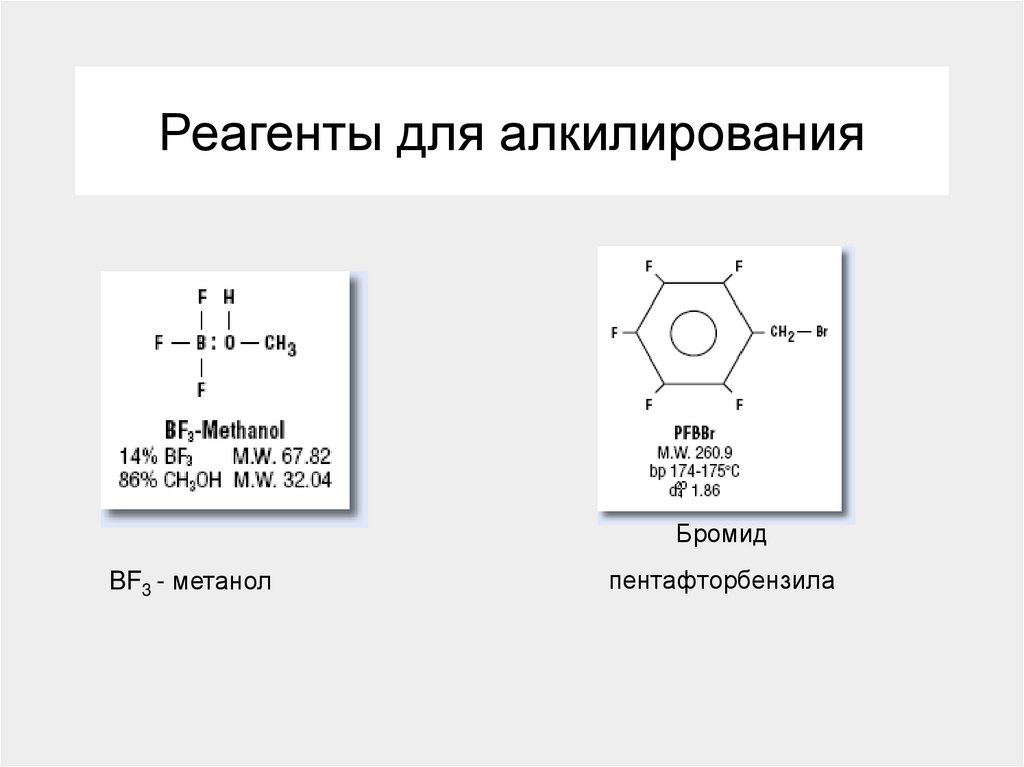
139. Реагенты для алкилирования
БромидBF3 - метанол
пентафторбензила
140.
3. Получение сложных эфировДиазометановый метод
RCOOH + CH2N2 → RCOOCH3 + N2
Метанольный метод
RCOOH + CH3OH → RCOOCH3
Пиролитический метод
RCOOH + (CH3)4NOH RCOOCH3 + H2O +(CH3)3N
4. Получение простых эфиров
ROH + CH3I →ROCH3 + HI
141.
5. Получение ацильных производныхацилирующие реагенты─ ангидриды
соответствующих кислот
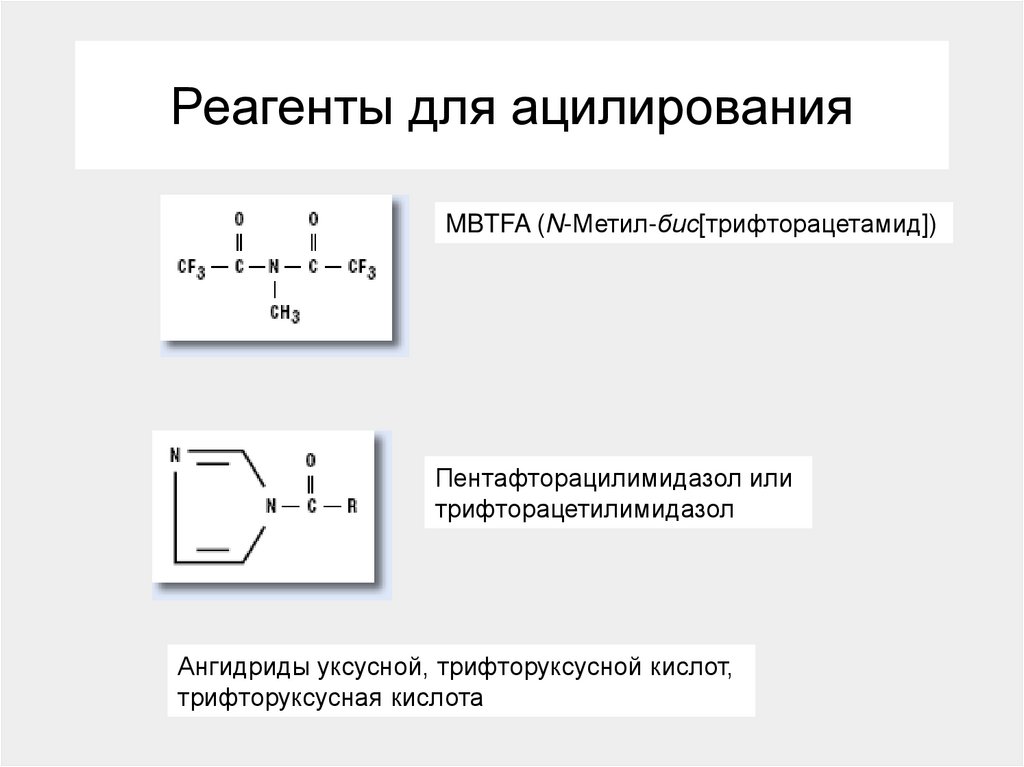
142. Реагенты для ацилирования
MBTFA (N-Метил-бис[трифторацетамид])Пентафторацилимидазол или
трифторацетилимидазол
Ангидриды уксусной, трифторуксусной кислот,
трифторуксусная кислота
143.
6. Образование оксимов и гидразинов7. Образование производных
неорганических соединений
(летучих хелатов металлов, алкилпроизводных ртути ,
гидридов, хлоридов)
144.
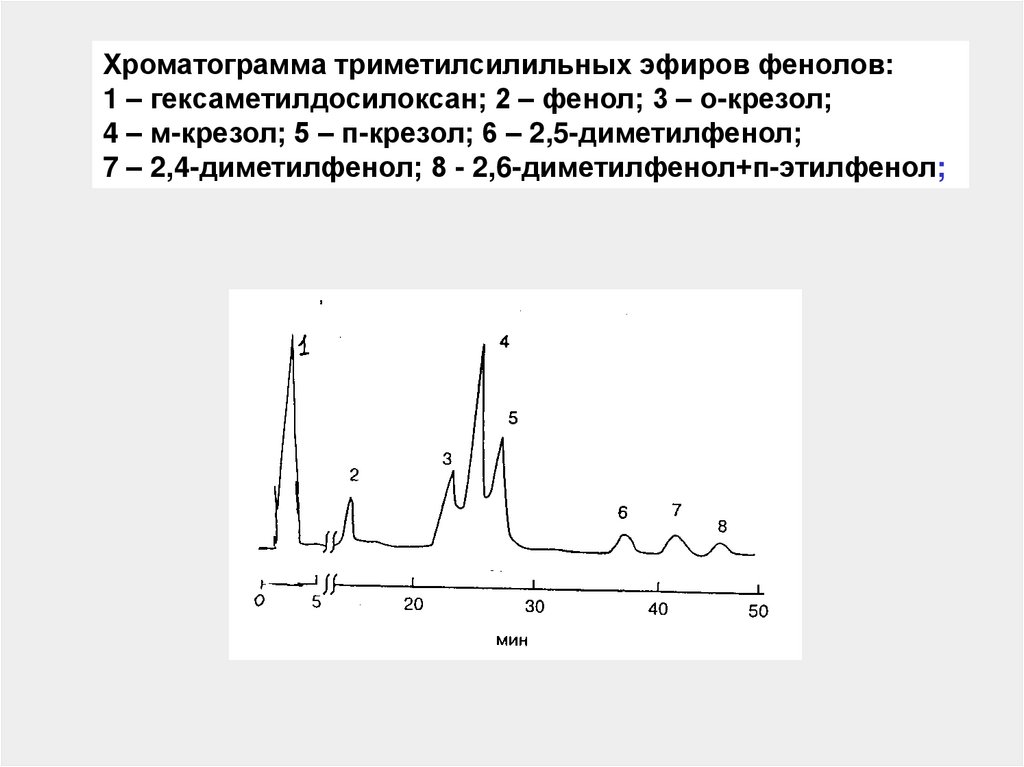
Хроматограмма триметилсилильных эфиров фенолов:1 – гексаметилдосилоксан; 2 – фенол; 3 – о-крезол;
4 – м-крезол; 5 – п-крезол; 6 – 2,5-диметилфенол;
7 – 2,4-диметилфенол; 8 - 2,6-диметилфенол+п-этилфенол;
145.
Определение фенолов методомреакционной газовой хроматографии
Проба
Фенолы
Фенолы в
коптильном дыме
и табаке
Фенолы
Фенол, гваякол,
крезолы
Производные
2,4-динитрофениловые эфиры
Триметисилильные
Гептафторбутирильные
Ацетаты
Определяемые
содержания
Детектор
пг
ЭЗД
нг
ПИД
пг
ЭЗД
0,005-10 мг/м3
ПИД
146.
Определение альдегидовНаиболее популярный способ дериватизации с
2,4-динитрофенилгидразином
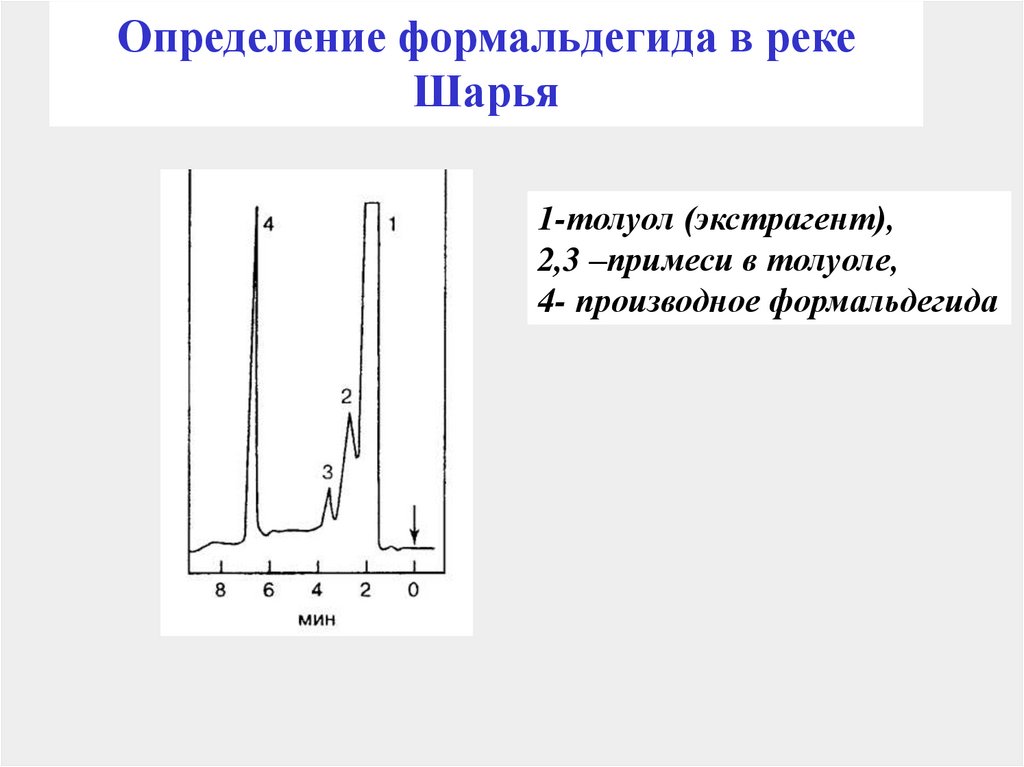
147. Определение формальдегида в реке Шарья
1-толуол (экстрагент),2,3 –примеси в толуоле,
4- производное формальдегида
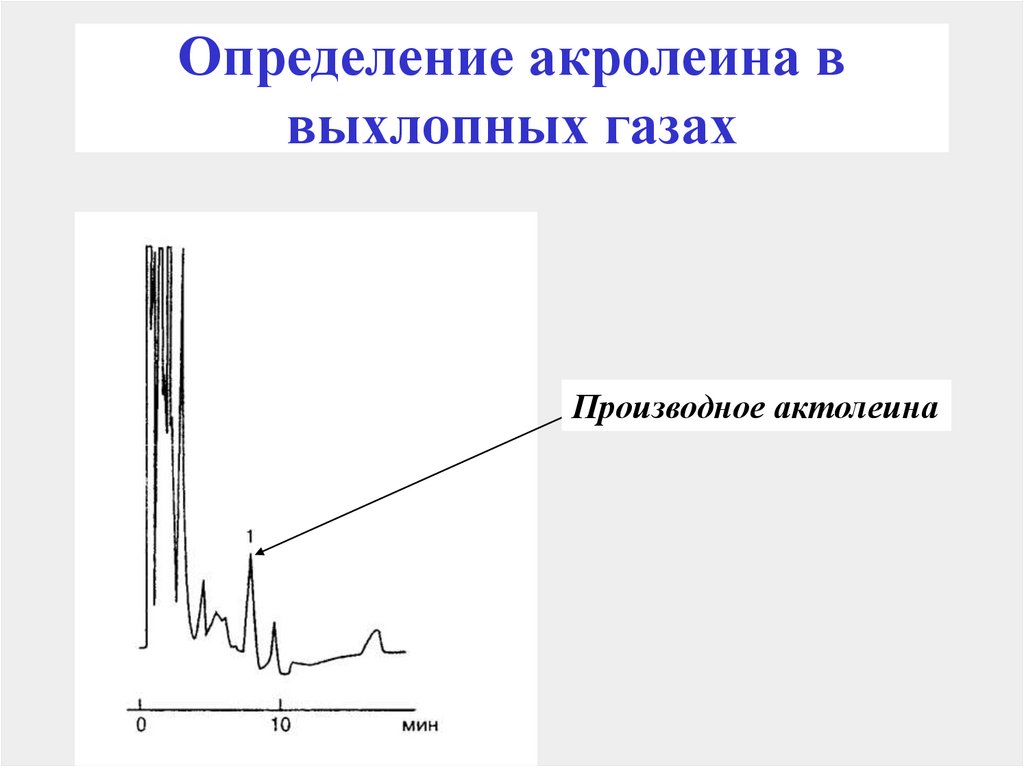
148. Определение акролеина в выхлопных газах
Производное актолеина149.
Хроматограмма производных альдегидовв экстракте из конденсата сигаретного дыма
150. Пиролитическая (пиролизная) хроматография
151.
Пиролизная хроматография – метод, которыйсочетает процесс пиролиза и
хроматографическое разделение
образовавшихся низкомолекулярных
продуктов деструкции, реализованные в
единой хроматографической системе
Чаще всего задача исследователя состоит
в установлении эмпирической корреляции
между строением исследуемого соединения и
получаемым в результате пиролиза спектром
низкомолекулярных соединений
152. Типы пиролизеров
• Постоянного нагрева: заданная температура в зонепиролиза поддерживается постоянной с помощью внешнего
обогрева, а исследуемый образец, находящийся
первоначально при комнатной температуре, вводят с
помощью специального устройства в заранее нагретую до
заданной температуры зону пиролиза
• Импульсного типа: термоэлемент-держатель пробы
кратковременно нагревают. за счет подачи импульса энергии
в течение непродолжительного периода времени (несколько
сек)
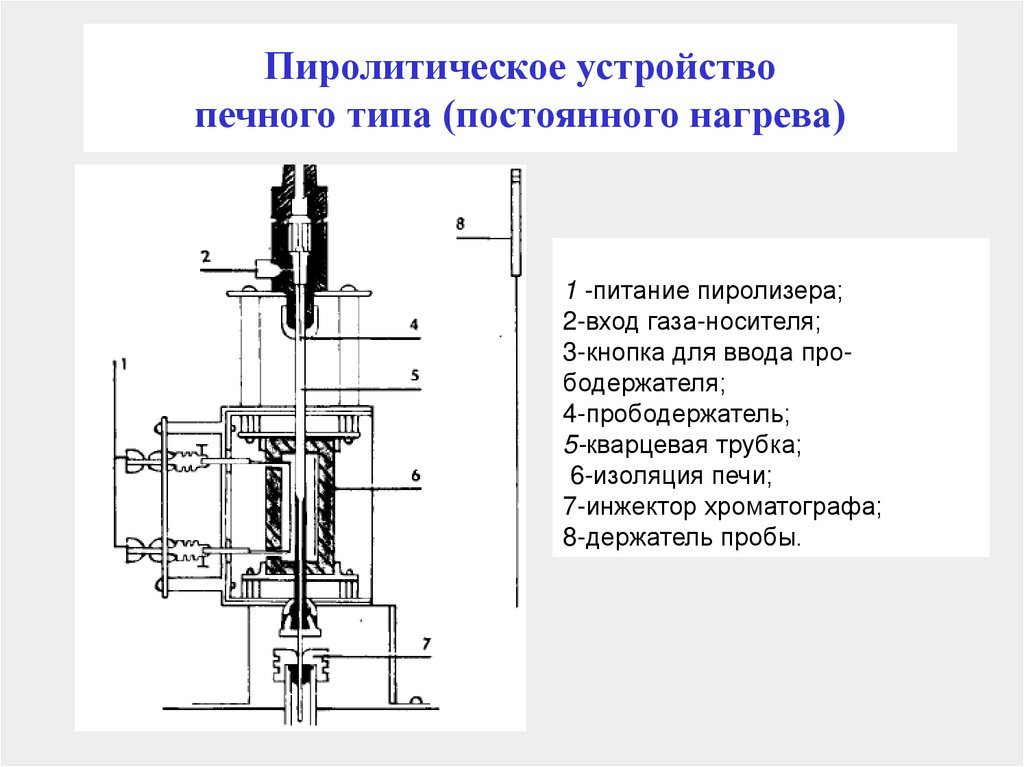
153. Пиролитическое устройство печного типа (постоянного нагрева)
1 -питание пиролизера;2-вход газа-носителя;
3-кнопка для ввода прободержателя;
4-прободержатель;
5-кварцевая трубка;
6-изоляция печи;
7-инжектор хроматографа;
8-держатель пробы.
154.
Пиролизер филаментного типа.
1 -держатели;
2-стеклянный изолятор;
3-накидная гайка;
4-уплотнительная прокладка;
5-реактор;
6-штуцер для ввода газа-носителя;
7-корпус пиролизера;
8-филамент из нихрома;
9-гайка для крепления пиролизера и
соединение его с колонкой;
10-уплотнительная втулка;
11 –хроматографическая колонка,
12 - термостат
155. Области применения ПГХ
Криминалистика• Идентификация компонентов образцов разной степени
сложности, содержащие высокомолекулярные
органические соединения, неполимерные продукты
(битумы, смазки и др.), а также натуральные
высокомолекулярные соединения
Краски и различные декоративные покрытия
Адгезивы
Яды, лекарства, наркотики
Бактерии и грибки
Волосы
Синтетические и натуральные волокона
Источники возгорания при пожарах
156. Области применения ПГХ
Биохимические исследования• идентификации микроорганизмов
Медицина
• диагностика болезней (в том числе раковых) и слежение за
их развитием и лечением
• лекарственных препаратов в выделениях человека и
физиологических жидкостях
Фармакология
Определение барбитуратов, сульфамидов, пенициллинов,
цефалоспоринов и др. препаратов
Геология
• Топлива и их источники
• гумусовы вещества
• органического вещества в грунтах других планет с целью
установления внеземной жизни
Загрязнение окружающей среды
157.
Метод вычитания158.
Реагенты, используемые в методе вычитанияУлавливаемые
соединения
н-Парафины, н-олефины, άолефины
Реагенты
Молекулярные сита, карбамид
Ароматические углеводороды Оксид алюминия, молекулярные сита
10Х
Сопряженные диены
Малеиновый ангидрид
Олефины
Серная кислота на силикагеле, бром
на угле
Альдегиды
Алюмо- и боргидриды лития
Амины
Фосфористая кислота
Фенолы
Гидроксид натрия на кварце
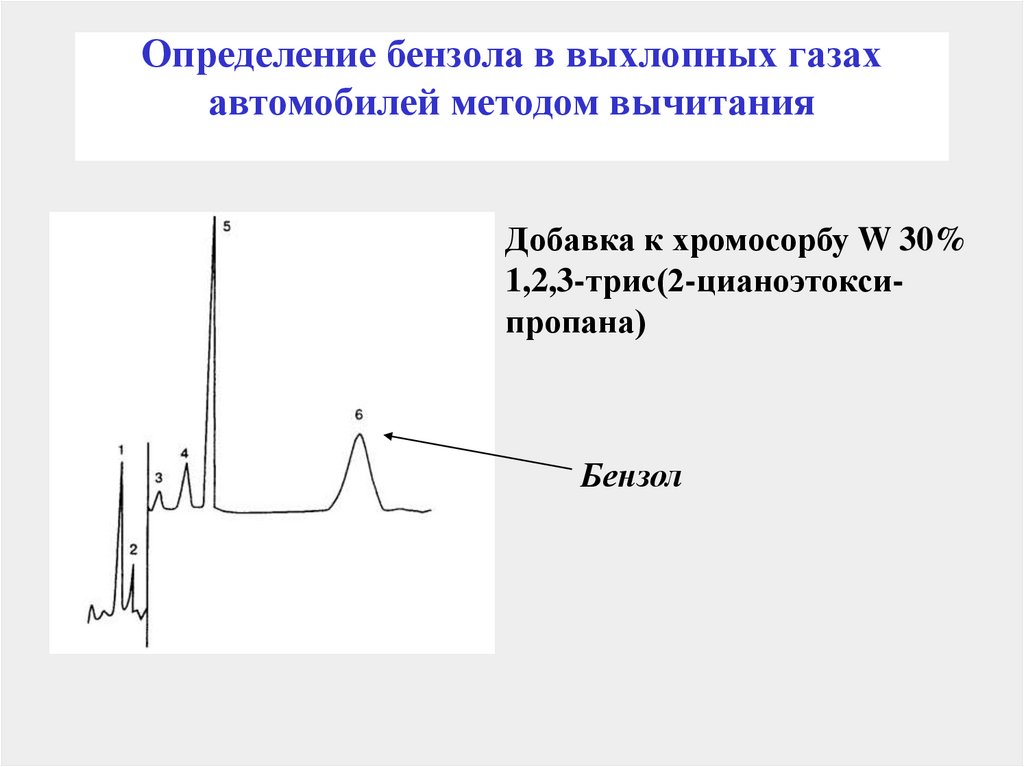
159. Определение бензола в выхлопных газах автомобилей методом вычитания
Добавка к хромосорбу W 30%1,2,3-трис(2-цианоэтоксипропана)
Бензол
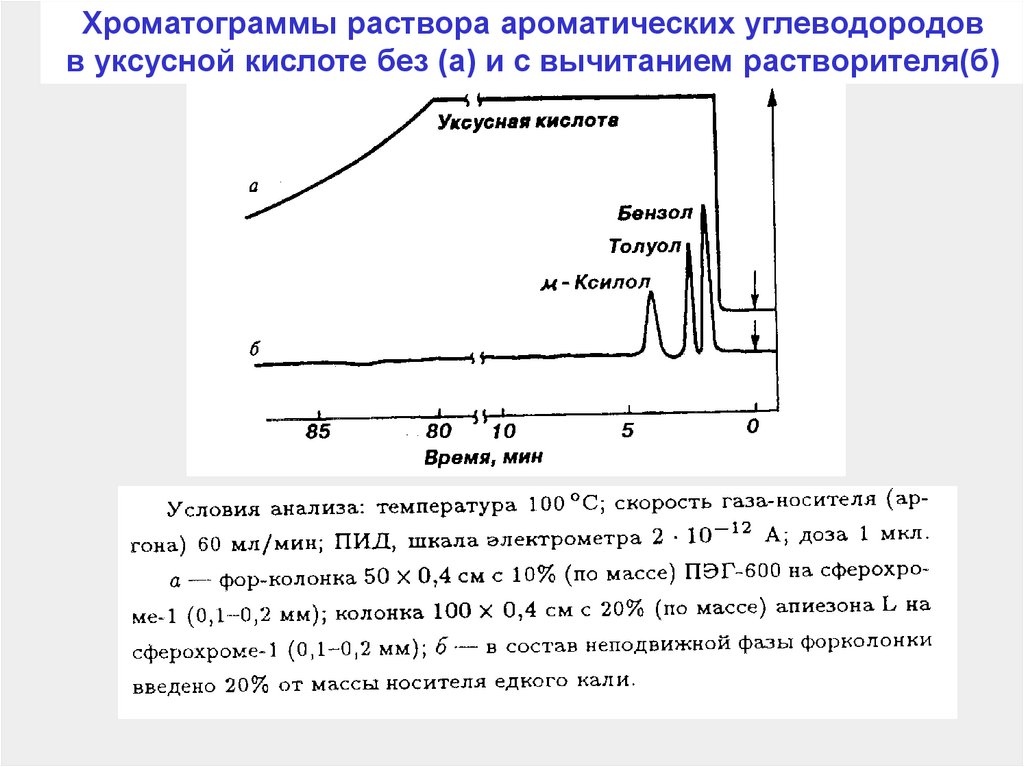
160.
Хроматограммы раствора ароматических углеводородовв уксусной кислоте без (а) и с вычитанием растворителя(б)
161.
Идентификация винилхлорида в смесиЛОС
в воздухе рабочей зоны при производств искусственной
кожи на основе ПВХ: а – в обычном варианте; б – после
пропускания воздуха через форколонку с цеолитом 5А и серной
кислотой.
1 – винилхлорид; 11 – толуол (экстрагент); пики 2-10 не
идентифицировались.
162.
Сверхкритическая флюидная хроматография(СКФХ, super-critical fluid chromatography)
Метод, в котором подвижной фазой является вещество,
находящееся в сверхкритическом состоянии - флюид
163.
Подвижные фазы для СКФХФлюид
Т крит, 0С
Р крит, атм
крит, г/мл
CO2
31,3
72,9
0,47
NH3
132,5
112,5
0,24
н-C5H12
196,6
33,3
0,23
Свойства газа, жидкости и флюида
Подв. фаза
Плотность,
г/мл
Вязкость, Пз
К диффузии,
см2/с
Газ
СКФ
Жидкость
0,001
0,3
0,9
10-4
10-3
10-2
10-1
10-4
10-5
164.
Свойства флюида• По вязкости ближе к газу
• По плотности и растворяющей способности ближе к
жидкости
Преимущества СКФХ
• Быстрота разделения при сохранении высокой
селективности, достоинство по сравнению с ВЭЖХ
• Гибкость анализа
• Возможность анализа нестабильных и малолетучих
соединений, расширяет возможности анализа по сравнению
с газовой хроматографией
165.
Схема установки для СКФХ166.
Хроматографы для СКФХ167.
Рабочие параметры в СКФХПодвижная фаза - флюид
Коэффициенты емкости меняются с изменением
плотности подвижной фазы и давления
При высоких плотностях невозможно осуществлять
программирование плотности и поэтому для ускорения
элюирования сорбатов необходимо добавлять в
подвижную фазу небольшие количества (1%) полярных
модификаторов
168.
Рабочие параметры в СКФХНеподвижная фаза - сорбент
Выбор ограничен из-за сильной растворяющей
способности флюидов
Используют Al2O3; SiO2; полистирол; силикагель,
химически модифицированный октадецильными и
аминопропильными группами
169.
Сопоставление методов СКФХ, ГХ иВЭЖХ
170.
Особенности СКФХ1. Флюиды способны растворять вещества с высокой
молекулярной массой и слабой летучестью
2. Низкая вязкость позволяет в значительной степени
уменьшить давление на входе в колонку для данной
скорости потока (по сравнению с ВЭЖХ)
4. Повышенная проницаемость позволяет увеличить
длину колонки и анализировать сложные смеси, которые
нельзя разделить путем оптимизации селективности
подвижной фазы в ВЭЖХ
5. Величина коэффициентов диффузии сорбатов в
сверхкритических флюидах приводит к уменьшению
времени анализа в ряду ВЭЖХ СКФХ ГХ
171.
Хроматограммы лекарственных веществЖидкостная
хроматография
Сверхкритическая
флюидная
хроматография
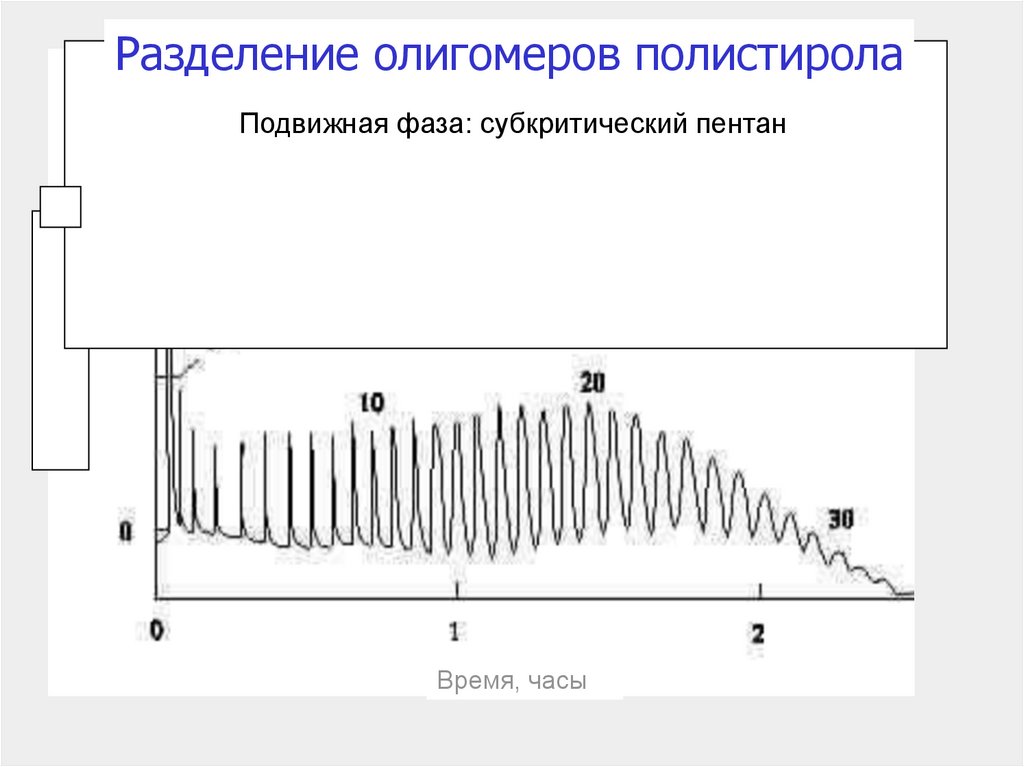
172.
Разделение олигомеров полистиролаПодвижная фаза: субкритический пентан
Время, часы
173. Литература
1.2.
3.
4.
5.
6.
Руководство по газовой хроматографии. В 2-х ч. Пер. с нем.
Под ред. Э.Лейбница, Х.Г.Штруппе. М.: Мир, 1988
Столяров Б.В. и др. Практическая газовая и жидкостная
хроматография. – С.-Пт.: С.-Петербургский университет, 1998
Руденко Б.А., Руденко Г.И. Высокоэффективные
хроматографические процессы. В 2-ух томах. – М.: Наука, 2003
Другов Ю.С., Родин А.А. Газохроматографическая
идентификация загрязнений воздуха, воды и почвы.
Практическое руководство. С.-Пт.: Теза, 1999, 622с.
Другов Ю.С., Родин А.А. Газохроматографический анализ
газов. Практическое руководство. С.-Пт.: Анатолия, 2001, 425с.
Сверхкритическая флюидная хроматография/ Под ред.
Р.Смита. М.: Мир, 1991г.
174. Статика сорбции
Закон Генрисс = К•с
сс – концентрация вещества на поверхности
с – концентрация вещества в растворе
К – истинный коэффициент Генри
k‘= масса сорбата в 1 см слоя сорбента D V
масса сорбата в 1 см раствора
V
k‘ – частный коэффициент Генри
3
s
3
m
175. Кинетика сорбции
•Внешний массообменМиграция молекул сорбата из канала между
частицами сорбента к их поверхности
•Внутренняя диффузия
Диффузия внутрь зерна по систтеме пор
адсорбента или пленки абсорбента
•Акт сорбции
176. Распределение концентраций при лимитирующей стадии внешнего (а) и внутреннего (б) массообмена
-ln(1-F)=Kc•tF-степень достижения равновесия
Kc – константа скорости процесса
F=Kc•t1/2
С -концентрация
177.
Основные элементы системы: газовыйхроматограф – масс-спектрометр – компьютер
178.
Разделение ароматических углеводородовна модифицированной ГТС
(карбопак С + 0,34% 2,4,5,7 – тетранитрофлуоренона)
1 – бензол, 2 – толуол, 3 – этилбензол,
4 – изопропилбензол, 5 – м-ксилол,
6 – п-ксилол, 7 – о-ксилол, 8 – стирол,
9 – н-пропилбензол























































































































































 physics
physics








