Similar presentations:
Конденсированные состояния вещества. Лекция 14
1.
Физика. Лекция 14Конденсированные состояния
вещества
В.И. Читайкин
кандидат физико-математических наук
доцент
2.
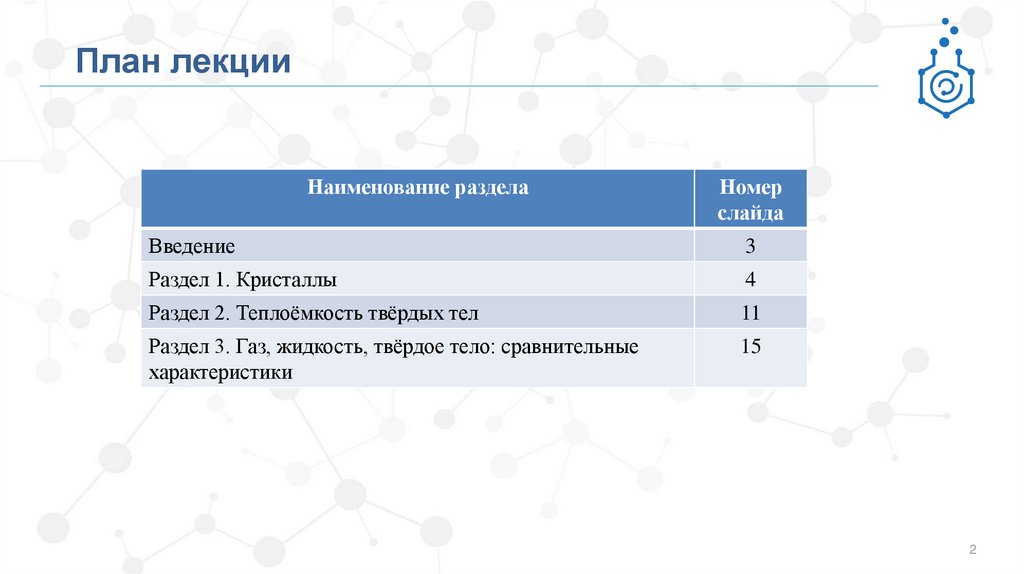
План лекцииНаименование раздела
Номер
слайда
Введение
3
Раздел 1. Кристаллы
4
Раздел 2. Теплоёмкость твёрдых тел
11
Раздел 3. Газ, жидкость, твёрдое тело: сравнительные
характеристики
15
2
3.
ВведениеОбщие замечания
Лекция 14 посвящена основам конденсированного состояния вещества – твёрдому
телу, жидкости. Тематика первых двух разделов лекции отличается от привычной
«газовой» тематики (идеальный/реальный газ), но, в то же время, является
естественным развитием молекулярно-кинетической теории строения вещества.
Определение: конденсированное состояние вещества – это такое состояние, в
котором частицы вещества (атомы, молекулы, ионы) связаны между собой силами
электромагнитного взаимодействия. Причём, энергии теплового движения частиц не
хватает на самопроизвольный разрыв этой связи. Поэтому конденсированное тело
сохраняет свой объём и даже форму (в случае твёрдого тела).
В определённом смысле, конденсированное состояние вещества – понятие,
объединяющее твёрдые тела и жидкости в противопоставлении их газу.
В разделе 3 дано физическое сравнение твёрдых тел, жидкостей и газа.
3
4.
Конденсированное состояниеРаздел 1. Кристаллы
4
5.
1. Кристаллы1.1 Определения и понятия
Кристалл – это твёрдое тело, имеющее правильную геометрическую форму.
Правильная геометрическая форма обусловлена упорядоченным расположением частиц,
повторяющимся в трёхмерном пространстве. Такая структура расположения частиц называется
кристаллической решёткой. Другими словами, каждый кристалл имеет кристаллическую
решётку, которая образована повторяющимся в трёхмерном пространстве расположением
частиц.
Частицы в кристалле находятся в узлах кристаллической решётки. Эти узлы – есть
устойчивые центры положения частиц, вокруг которых частицы совершают хаотические
тепловые колебания, оставаясь в среднем на
одном месте.
Кристалл имеет кристаллическую решётку с
геометрически строгой структурой.
При отсутствии строгой геометрической
структуры – НЕКРИСТАЛЛ.
5
6.
1. Кристаллы1.2 Монокристаллы, поликристаллы.
Кристалл, в основе которого лежит одна и та же
кристаллическая решётка с постоянными по пространству параметрами, называется монокристаллом.
NaCl
Вырастить дома можно
Твёрдое тело, состоящее из множества беспорядочно ориентированных мелких кристаллических зерён,
называется поликристаллом.
Поликристалл состоит из кристаллических зёрен
одного и то же вещества. Важно, чтобы эти зёрна были
беспорядочно ориентированы.
C
Вырастить дома нельзя
Кристаллогидраты
Я не знаю, можно ли их вырастить дома.
6
7.
1. Кристаллы1.3.1 Типы структур кристаллов
Наука о кристаллах – кристаллография. В основе кристаллографии лежит классификация
кристаллов по структуре их кристаллических решёток.
Структура кристаллических решёток определяется свойством симметрии, т.е.
возможностью их совмещения с собой при параллельном переносе, повороте, отражении и
некоторых других комбинациях. Всего возможно 230 комбинаций симметричных структур,
некоторые их них очень сложны и труднопредставимы.
Кристаллические решётки с различной симметрией (простые примеры)
7
8.
1. Кристаллы1.3.2. Типы структур кристаллов. Переносная симметрия.
Элементарная ячейка.
Наиболее практически значимой является переносная симметрия кристаллической
решётки, которая получается путём совмещения с собой при параллельном переносе.
Самое важное свойство переносной симметрии: существуют элементарные ячейки, из
которых может быть составлена любая пространственная кристаллическая структура методом
повторения этой ячейки во всех трёх направлениях.
Элементарная ячейка – параллелепипед, построенный на рёбрах а, b и с с углами
между ними α, β и γ. Величины а, b и с называются периодами решётки.
Элементарная ячейка полностью и однозначно определяется совокупностью
параметров: а, b, с и α, β и γ.
Пример «построения» монокристалла (а)
из одной элементарной ячейки (б):
8
9.
1. Кристаллы1.3.3. Типы структур кристаллов. Переносная симметрия.
Характеристики кристаллической решётки.
Период кристаллической решётки (величины а, b и с) – это расстояние между
центрами ближайших однотипных частиц в элементарной ячейке в каждом из трёх
направлений.
Координационное число – это число однотипных частиц, находящихся на
приблизительно равном и наименьшем расстоянии от данной частицы.
Коэффициент компактности (плотность упаковки) – это отношение объёма, занятого
частицами, ко всему объёму элементарной ячейки.
Пример: объёмно-центрический кристалл (ОЦК).
Характеристики кристаллической решётки ОЦК:
Период:
а, b, с (или: а, если а=b=с)
Координационное число:
К8
Коэффициент компактности: 68%
9
10.
1. Кристаллы1.3.4.Типы структур кристаллов. Переносная симметрия.
Сингония.
Число переносных симметрий кристаллической решётки относительно немного и все они
разделяются по семи кристаллографическим системам или сингониям.
Хорошая, наглядная таблица сингоний с рисунками
содержится в учебнике Т.И.Трофимовой, §71, с.133.
10
11.
Конденсированное состояниеРаздел 2. Теплоёмкость твёрдых тел
11
12.
2. Теплоёмкость твёрдых тел2.1 Тепловое движение частиц в твёрдом теле
Как известно (см., напр., сл.5), узлы кристаллической решетки определяют средние,
равновесные положения частиц. Сами же частицы (ионы, атомы или молекулы) непрерывно
колеблются около этих средних положений, причем интенсивность колебаний растет с
температурой.
Для большинства твёрдых тел при нормальных и умеренно высоких температурах энергии
теплового движения частиц не хватает на самопроизвольный разрыв связи, т.е. частица
колеблется во всех трёх направлениях вокруг положения равновесия, но покинуть «строй» не
может.
Наглядный образ колебаний частиц вокруг узлов кристаллической решётки может быть
таким:
или таким:
12
13.
2. Теплоёмкость твёрдых тел2.2 Число степеней свободы и внутренняя энергия
-
Число степеней свободы частицы в твёрдом теле:
поступательных – 0, т.к. поступательного движения частицы нет;
вращательных – 0, т.к. вращение у одной частицы отсутствует;
колебательных – 3, т.к. частица колеблется равновероятно во всех трёх направлениях
вокруг положения равновесия (узла кристаллической решётки).
Всего: iчаст = iпост + iвращ + 2iколеб = 6 (см. лекция 10, раздел 3).
Внутренняя энергия
Внутренняя энергия на каждую степень свободы составляет ½kT (см. лекция 10, раздел 3).
Внутренняя энергия на частицу составляет Uчаст = iчаст × ½kT = 3kT.
Внутренняя энергия 1 моля твёрдого тела составляет Um = Uчаст × NA = 3NAkT = 3RT.
13
14.
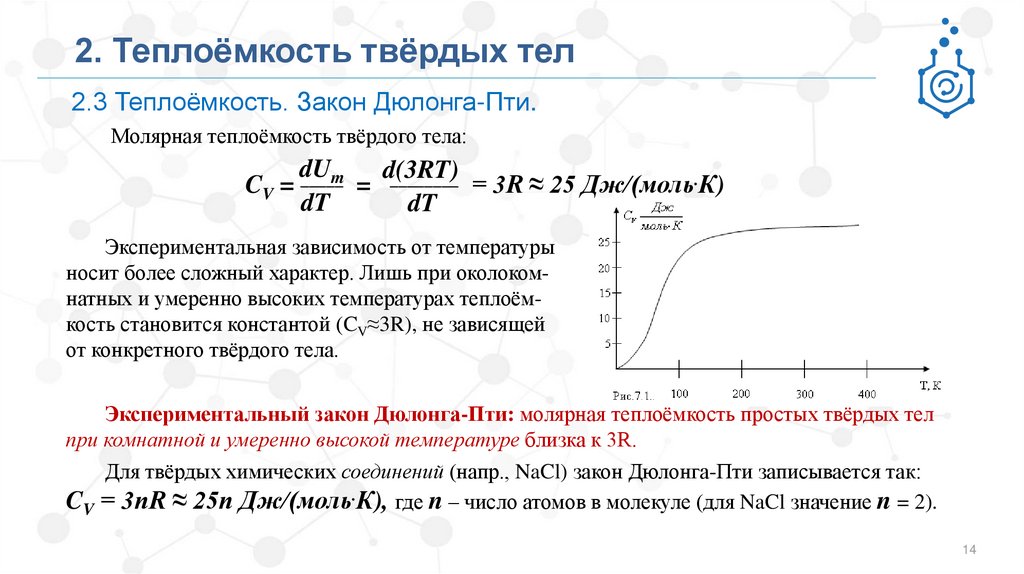
2. Теплоёмкость твёрдых тел2.3 Теплоёмкость. Закон Дюлонга-Пти.
Молярная теплоёмкость твёрдого тела:
dU
d(3RT)
m
_____
CV =
= ________ = 3R ≈ 25 Дж/(моль.К)
dT
dT
Экспериментальная зависимость от температуры
носит более сложный характер. Лишь при околокомнатных и умеренно высоких температурах теплоёмкость становится константой (CV≈3R), не зависящей
от конкретного твёрдого тела.
Экспериментальный закон Дюлонга-Пти: молярная теплоёмкость простых твёрдых тел
при комнатной и умеренно высокой температуре близка к 3R.
Для твёрдых химических соединений (напр., NaCl) закон Дюлонга-Пти записывается так:
CV = 3nR ≈ 25n Дж/(моль.К), где n – число атомов в молекуле (для NaCl значение n = 2).
14
15.
Конденсированное состояниеРаздел 3. Газ, жидкость, твёрдое тело:
сравнительные характеристики
«The last but not the least»
(Раздел последний, но не по важности)
15
16.
3. Газ, жидкость, твёрдое тело: сравнительныехарактеристики
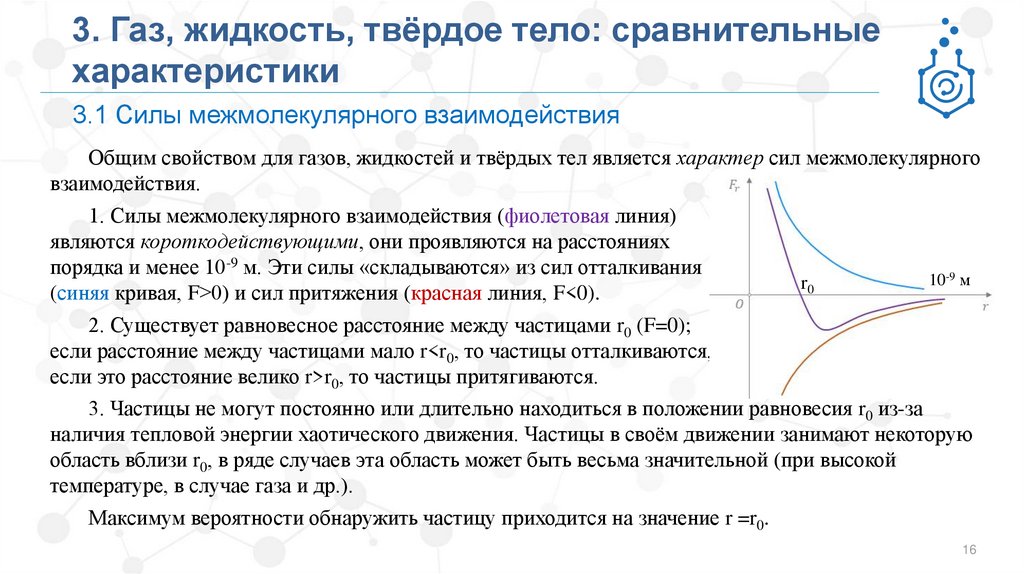
3.1 Силы межмолекулярного взаимодействия
Общим свойством для газов, жидкостей и твёрдых тел является характер сил межмолекулярного
взаимодействия.
1. Силы межмолекулярного взаимодействия (фиолетовая линия)
являются короткодействующими, они проявляются на расстояниях
порядка и менее 10-9 м. Эти силы «складываются» из сил отталкивания
10-9 м
r0
(синяя кривая, F>0) и сил притяжения (красная линия, F<0).
2. Существует равновесное расстояние между частицами r0 (F=0);
если расстояние между частицами мало r<r0, то частицы отталкиваются,
если это расстояние велико r>r0, то частицы притягиваются.
3. Частицы не могут постоянно или длительно находиться в положении равновесия r0 из-за
наличия тепловой энергии хаотического движения. Частицы в своём движении занимают некоторую
область вблизи r0, в ряде случаев эта область может быть весьма значительной (при высокой
температуре, в случае газа и др.).
Максимум вероятности обнаружить частицу приходится на значение r =r0.
16
17.
3. Газ, жидкость, твёрдое тело: сравнительныехарактеристики
3.2 Потенциальная энергия межмолекулярного взаимодействия
Общим свойством для газов, жидкостей и твёрдых тел также является
характер поведения потенциальной энергии межмолекулярного взаимодействия.
Минимум потенциальной энергии достигается в точке r0, т.е. в точке равновесного положения частиц; в этой точке находится максимум вероятности обнаружения частицы.
В зависимости от соотношения между тепловой энергии
частицы (kT) и «глубины потенциальной ямы» (mod{Eп0}) можно
получить различное агрегатное состояние вещества (таблица).
Соотношение между тепловой энергией
и глубиной потенциальной ямы
Положение частицы
kT < mod{Eп0}
Частица колеблется около положения равновесия r0
kT ≈ mod{Eп0}
Частица может удаляться от положения равновесия на
расстояние ≈ 2r0, продолжая колебаться
kT > mod{Eп0}
Частица может перемещаться на значительное удаление,
положения равновесия не существует
Агрегатное
состояние
Твёрдое тело
Жидкость
Газ
17
18.
3. Газ, жидкость, твёрдое тело: сравнительныехарактеристики
3.3 Порядок расположения частиц
Агрегатное
состояние
Твёрдое
тело
Жидкость
Газ
Поведение частиц в веществе
Характеристика
порядка
Частицы постоянно находятся строго вблизи своих положений равновесия, совершая
вблизи них небольшие колебания. Переходы частиц из одного положения в другое
отсутствуют.
Частицы образуют довольно чёткий «строй» (напр., кристалл), в котором упорядоченное
расположение частиц повторяется на больших расстояниях.
Сохраняются объём и форма твёрдого тела.
Дальний
порядок
Частицы в течение длительного времени находятся вблизи своих положений равновесия,
совершая вблизи них небольшие колебания. Затем частицы совершают быстрый переход в
другое положение. И так далее.
Чёткий «строй» отсутствует, упорядоченное расположение частиц повторяется на малых
расстояниях, сопоставимых с межмолекулярным.
Жидкость сохраняет объём, но не сохраняет форму.
Ближний
порядок
Частицы могут перемещаться на значительное удаление, положения равновесия не сущест- Беспорядок
вует. Характер движения частиц – хаотический. Объём и форма газа не сохраняются.
хаос
18
19.
Курс лекций по физике для студентов 1-ого курсав весеннем семестре завершён.
Желаю успешного завершения учебного года!
19

















 physics
physics








