Similar presentations:
Катиондар мен аниондардың сапалық талдануы. Заттар талдануында қолданылатын электролиттер ертіндісінің теориясы
1.
Катиондар мен аниондардың сапалықталдануы.Заттар талдануында қолданылатын
электролиттер ертіндісінің теориясы
Орындаған:Қуанышбай А
Қабылдаған:Раманова Л
2. Жоспары
I.КіріспеII.Негізгі бөлім
Катиондар сапалық реакция
Аниондарга сапалық реакция
Сапалық талдау қадамдары
III.Қорытынды
3.
Катионоң зарядталған
сондықтан электролиз жағ
дайында катод, яки теріс
зарядталған электрод төңір
егінде шоғырланатын ион.
Электролиттердің электролизі
кезінде катодқа қарай
тартылады.
Құрамында катионы бар және
жұпталмаған электрондары бар
бөлшектер катиондаррадикалдар деп аталады.
Бос күйінде плазманың газ фазасында және аниондармен бірге көптеген
тұздардың құрамында болады. Бейтарап бөлшектерден бір немесе
бірнеше электронды қатты қыздыру, электрлік заряд, иондаушы сәуле, тағы
басқа нәтижесінде айырып алады.
4.
Мұнда катиондардың ортақ тобы:I топ: Ag + , Hg 2 2+ , Pb 2+
1 М HCl-де шоғырланған
II топ: Би 3+ , Cd 2+ , Cu 2+ , Hg 2+ , Pb 2+ , Sb 3+және Sb 5+ ,
Sn 2+ және Sn 4+
0,1 МДа 2 С ерітіндісінде рН 0,5-де шоғырланған
III топ: Al 3+ , Cd 2+ , Co 2+ , Cr 3+ , Fe 2+ және Fe 3+ , Mn 2+ ,
Ni 2+ , Zn 2+
РН 9 кезінде 0,1 МДа 2 С ерітіндісінде тұндыру
IV топ: Ba 2+ , Ca 2+ , K + , Mg 2+ , Na + , NH 4 +
Ba 2+ , Ca 2+ және Mg 2+ 0,2 М (NH 4 ) 2 CO 3ерітіндісінде рН
10 кезінде тұндыруда; басқа иондардың еруі мүмкін
5.
Сапалық талдаудың қадамдары•Үлгі қатты (тұз) ретінде ұсынылса, кез-келген кристалдардың
пішіні мен түсін атап өту маңызды.
•Реагенттер катиондарды тиісті элементтер тобына бөлуге
арналған.
•Топтағы иондар бір-бірінен бөлінеді. Әр бөлек сатысынан кейін
белгілі бір иондардың шынымен жойылғанын растау үшін сынақ
орындалады. Сынақ бастапқы үлгіде орындалмайды!
•Бөлу әр түрлі иондардың сипаттамаларына сүйенеді. Олар тотығу
күйін өзгерту үшін қышқылдықты, негізді немесе судағы
дифференциалдық ерігіштігін немесе кейбір иондарды тұндыру
үшін редоксидтік реакцияларды тудыруы мүмкін.
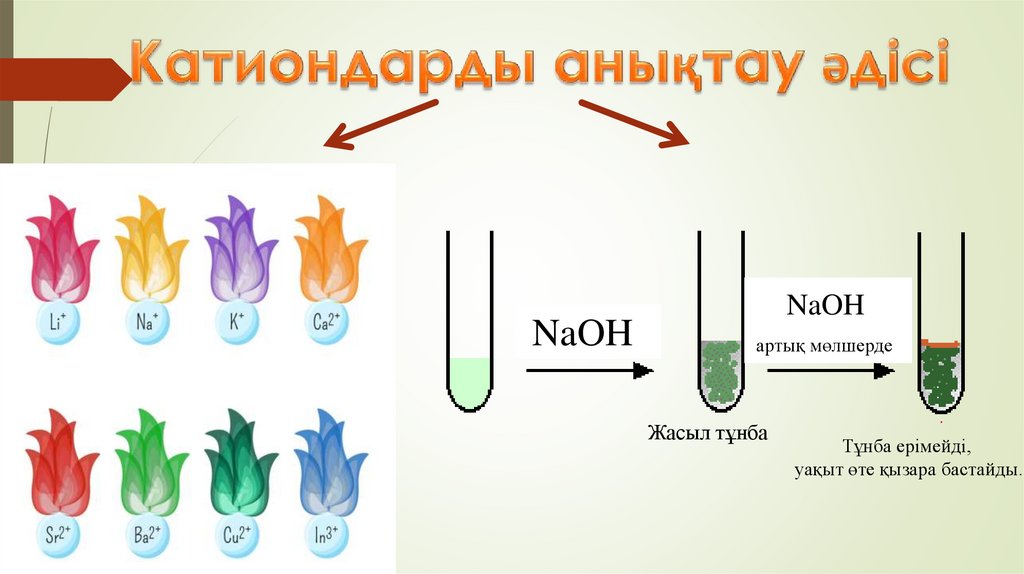
6.
NaOHNaOH
артық мөлшерде
Жасыл тұнба
Тұнба ерімейді,
уақыт өте қызара бастайды.
7.
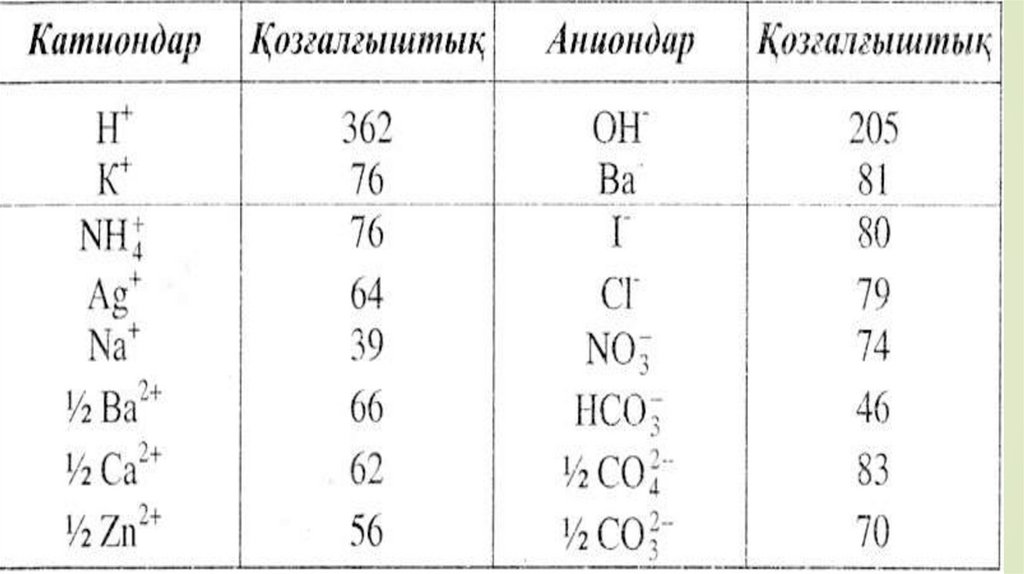
Теориялық матрицаКатиондар
Li+
Na+
Ba2+
Cu2+
Fe2+
Fe3+
Тұнба түзу реакциясы
(NaOH ерітіндісімен реакция)
өзгеріс байқалмайды
өзгеріс байқалмайды
өзгеріс байқалмайды
көк түсті тұнба түзіледі
артық мөлшерде қою көк түсті
тұнба түзеді
жасыл түсті тұнба түзіледі
артық мөлшерде ерімейді
қою қоңыр түсті тұнба түзіледі
артық мөлшерде ерімейді
Жалынды бояу
әдісі
қызыл
сары
ашық жасыл
көк жасыл
сары
сары
8.
9.
10. Пайдаланылған əдебиеттер
Пайдаланылған әдебиеттерАналитикалық химия оқулығы Ю.Я.Хоритонов
Ebooks.ru
Stid.kz
infourok








 chemistry
chemistry








