Similar presentations:
Антимикробная терапия нейтропенической лихорадки
1.
Антимикробная терапиянейтропенической лихорадки
С.Б.Ляпустин
2. Терминология
Нейтропеническая лихорадка (НИ) –
кратковременное повышение температуры тела
выше 38,0*С в течение одного часа и более у
пациентов с нейтропенией (количество
нейтрофилов < 0,5 х 109/л или < 1,0 х 109/л с
прогнозируемым падением в ближайшее время,
обусловленной заболеванием или проведением
химио- или лучевой терапии
В 80% связана с инфекцией
Подтверждается микробиологически в 40%
N.B.! Лихорадка может быть единственным
симптомом инфекции!
С.Б.Ляпустин 2008
3. Основные возбудители НИ
• Грам+: Staphylococcus aureus,Staphylococcus epidermidis, стрептококки,
энтерококки
• Грам-: E. coli Klebsiella pneumonia
Pseudomonas aeruginosa
Доля грам+ возбудителей растёт на фоне
использования в/в устройств и
химиотерапии.
На фоне массивной а/б терапии, в/в
устройств и парентерального питания –
Candida, Aspergillus)
С.Б.Ляпустин 2008
4. Антибактериальная терапия НИ
• А/синегнойный β-лактам (цефтазидим,цефоперазон, цефаперазон/сульбактам, цефепим,
имипенем, меропенем) ± АГ (амикацин)
• При высоком риске грам+ возбудителей:
ванкомицин + цефтазидим или цефепим
• При неэффективности а/б терапии или высоком
риске грибковой инфекции – антимикотики
(флюконазол, амфотерицин, вориконазол,
каспофунгин)
А/б терапию продолжают до 7 дней или до
эрадикации возбудителя (или до исчезновения
симптомов).
Отмену антибиотиков желательно проводить при
условии, что число нейтрофилов > 0,5 х 109/л
Диапазон: от меро+ванко+каспо до амоксиклав+ципро
С.Б.Ляпустин 2008
5.
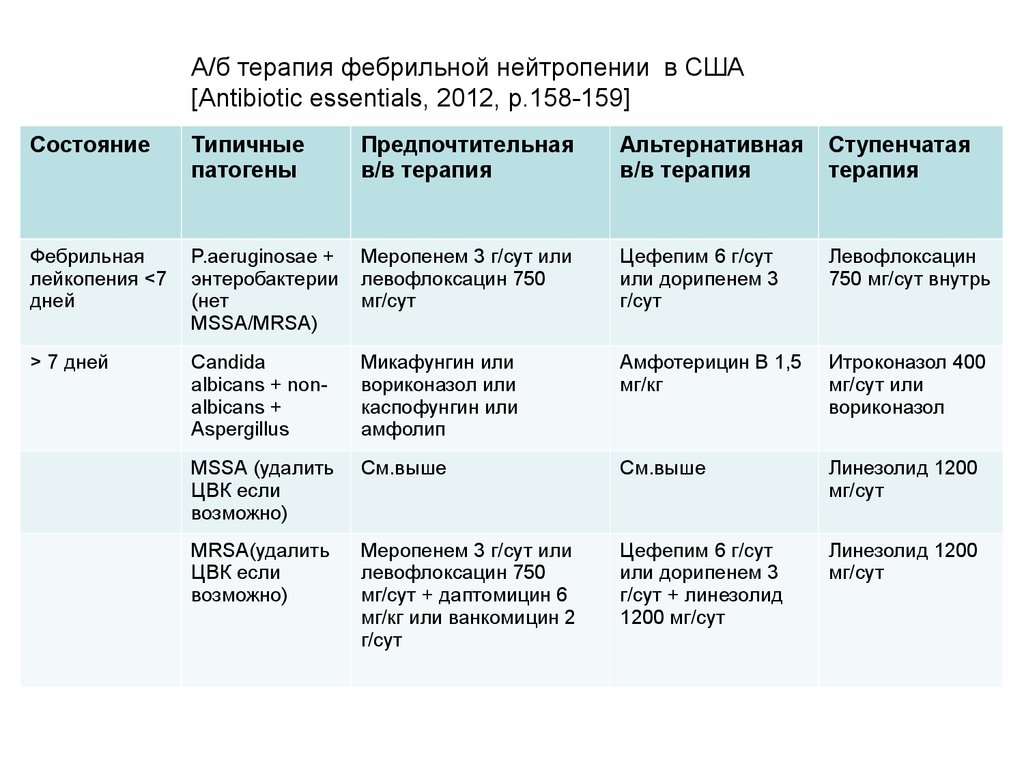
А/б терапия фебрильной нейтропении в США[Antibiotic essentials, 2012, p.158-159]
Состояние
Типичные
патогены
Предпочтительная
в/в терапия
Альтернативная
в/в терапия
Ступенчатая
терапия
Фебрильная
лейкопения <7
дней
P.aeruginosae +
энтеробактерии
(нет
MSSA/MRSA)
Меропенем 3 г/сут или
левофлоксацин 750
мг/сут
Цефепим 6 г/сут
или дорипенем 3
г/сут
Левофлоксацин
750 мг/сут внутрь
> 7 дней
Candida
albicans + nonalbicans +
Aspergillus
Микафунгин или
вориконазол или
каспофунгин или
амфолип
Амфотерицин В 1,5
мг/кг
Итроконазол 400
мг/сут или
вориконазол
MSSA (удалить
ЦВК если
возможно)
См.выше
См.выше
Линезолид 1200
мг/сут
MRSA(удалить
ЦВК если
возможно)
Меропенем 3 г/сут или
левофлоксацин 750
мг/сут + даптомицин 6
мг/кг или ванкомицин 2
г/сут
Цефепим 6 г/сут
или дорипенем 3
г/сут + линезолид
1200 мг/сут
Линезолид 1200
мг/сут
6.
7.
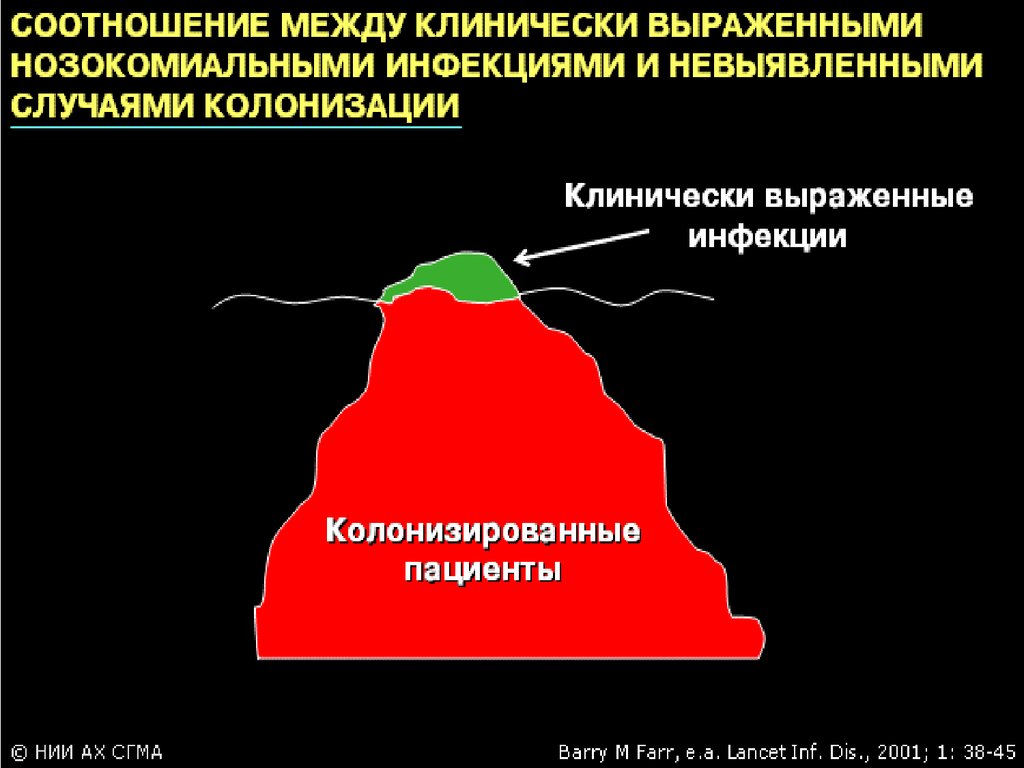
8. Нозокомиальные инфекции
С.Б.Ляпустин9.
10.
11.
12.
13.
14.
15.
16.
17.
18. Инфекции связанные с медицинской помощью
Любые клинически распознаваемыеинфекционные заболевания, которые
развиваются у пациента в результате его
обращения в больницу за лечебной помощью
или пребывания в ней, а также любые
инфекционные заболевания сотрудника
больницы, развившиеся вследствие его
работы в данном учреждении, вне
зависимости от времени появления
симптомов
19.
20.
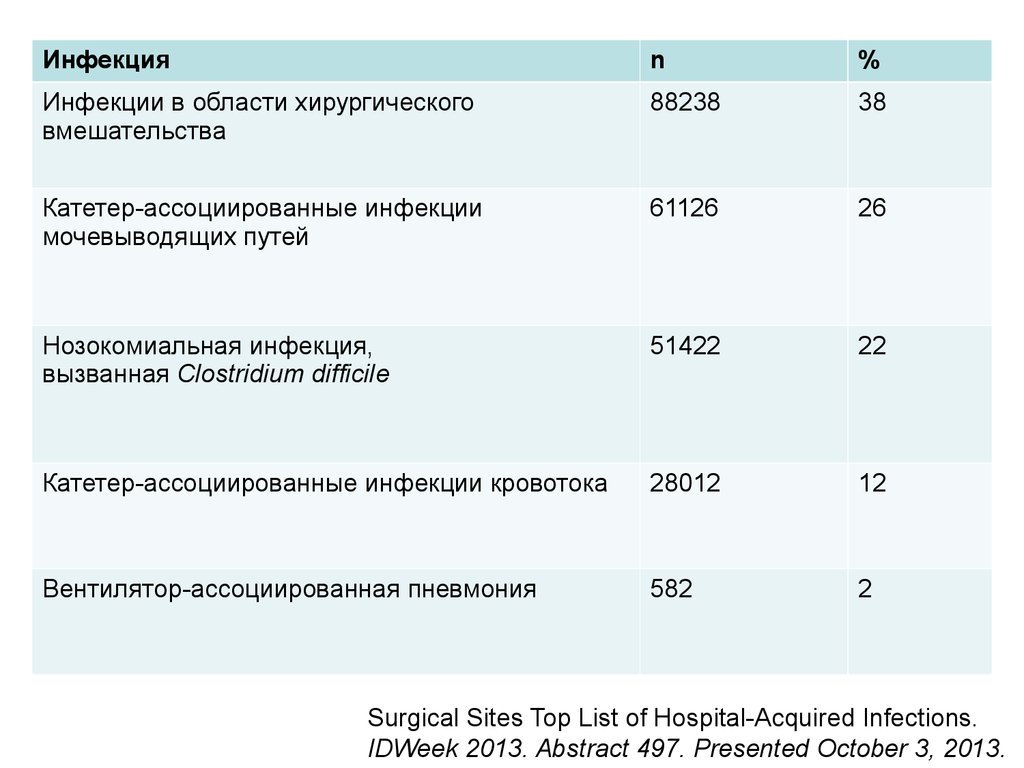
Инфекцияn
%
Инфекции в области хирургического
вмешательства
88238
38
Катетер-ассоциированные инфекции
мочевыводящих путей
61126
26
Нозокомиальная инфекция,
вызванная Clostridium difficile
51422
22
Катетер-ассоциированные инфекции кровотока
28012
12
Вентилятор-ассоциированная пневмония
582
2
Surgical Sites Top List of Hospital-Acquired Infections.
IDWeek 2013. Abstract 497. Presented October 3, 2013.
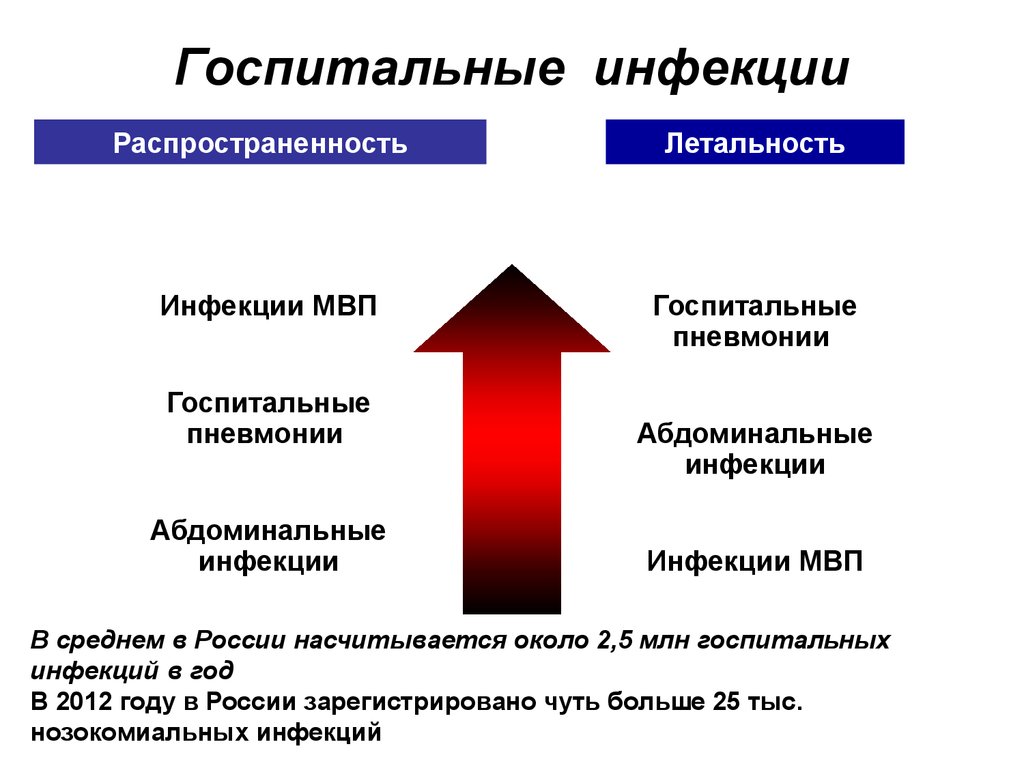
21. Госпитальные инфекции
РаспространенностьИнфекции МВП
Госпитальные
пневмонии
Абдоминальные
инфекции
Летальность
Госпитальные
пневмонии
Абдоминальные
инфекции
Инфекции МВП
В среднем в России насчитывается около 2,5 млн госпитальных
инфекций в год
В 2012 году в России зарегистрировано чуть больше 25 тыс.
нозокомиальных инфекций
22. Факторы, способствующие развитию ГИ
Общее состояние и возраст больного
Тип отделения (хирургия/терапия/ОРИТ)
Длительность пребывания в стационаре
Широкое использование антибиотиков
Наличие/отсутствие инвазивных устройств
Использование антисекреторных средств
Иммуносупрессия или нейтропения
Вид возбудителя
Хирургические факторы
«Резервуар» ГИ: выписанные пациенты и персонал
23.
«ESKAPE»-патогеныEnterococcus
faecium
Третий наиболее частый возбудитель госпитальных инфекций
кровеносного русла. Отмечена возрастающая резистентность
к ванкомицину.
Staphylococcus
aureus (MRSA)
Рост резистентности к современным препаратам. Недостаток
пероральных препаратов для проведения ступенчатой терапии.
Klebsiella
pneumoniae,
Escherichia coli
Микроорганизмы, продуцирующие бета-лактамазы расширенного
спектра действия, встречающиеся с увеличивающейся частотой
и вызывающие тяжёлые, с высокой частотой летальных исходов,
инфекции. K. pneumoniae, продуцирующая карбапенемазы,
вызывает тяжёлые инфекции в отделениях длительного ухода.
Имеется несколько эффективных антибактериальных
препаратов, новые препараты на этапе разработки отсутствуют.
Acinetobacter
baumannii
Доля данного микроорганизма увеличивается повсеместно,
в последнее время вызывает нозокомиальные вспышки. Очень
высокий уровень летальности. Резистентность к карбапенемам.
Pseudomonas
aeruginosa
Повсеместное увеличение числа случаев инфекций,
вызванных P. aeruginosa. Резистентность к карбапенемам,
фторхинолонам, аминогликозидам.
Enterobacter
spр.
Мультирезистентность, обусловленная выработкой беталактамаз расширенного спектра, карбапенемаз,
24.
Особенности в стандартизацииантибактериальной терапии
• Внебольничные
инфекции
– Ограниченный
перечень возбудителей
– Известный уровень
устойчивости
– Стандартизация
целесообразна
• Госпитальные
инфекции
– Более широкий круг
потенциальных
патогенов
– Непредсказуемый
уровень устойчивости
– Возможности
стандартизации
ограничены
Антибиотики для лечения госпитальных инфекций
не должны рутинно назначаться при
внебольничных инфекциях
25.
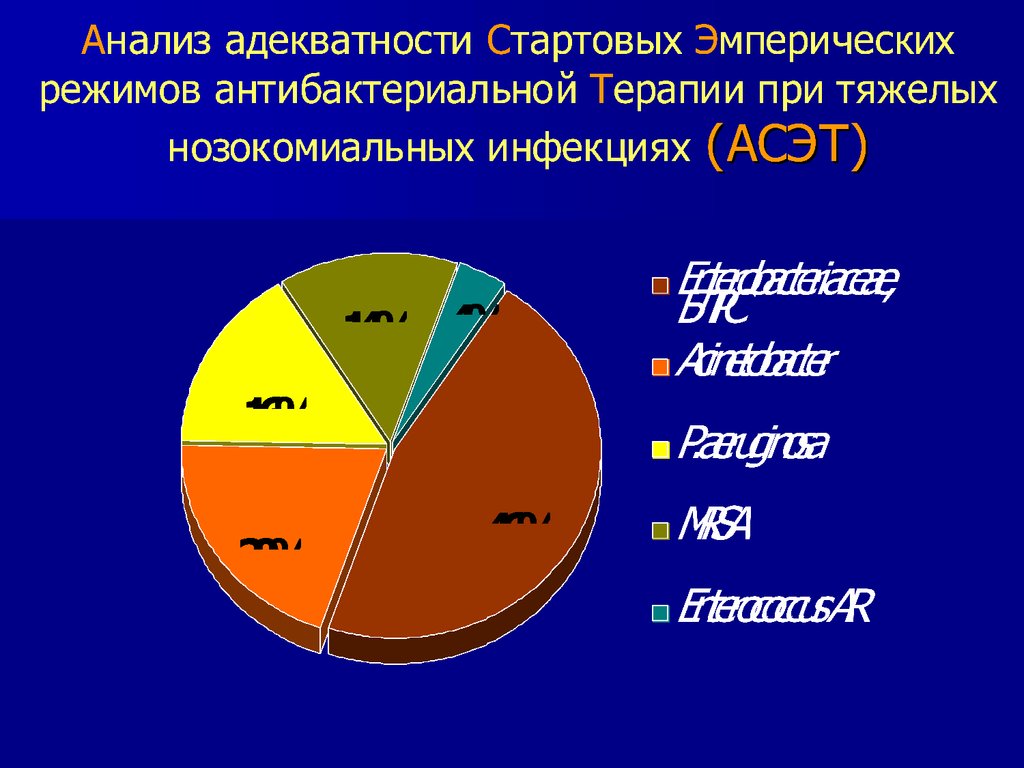
Структура возбудителей НИ в ОРИТ(РЕВАНш 2006 г)
Enterobacteriaceae
32,0%
P. aeruginosa
27,3%
Staphylococcus spp.
18,8%
Acinetobacter baumannii
10,4%
Enterococcus spp.
5,7%
Stenotrophomonas maltophilia
1,5%
Другие
4,3%
26.
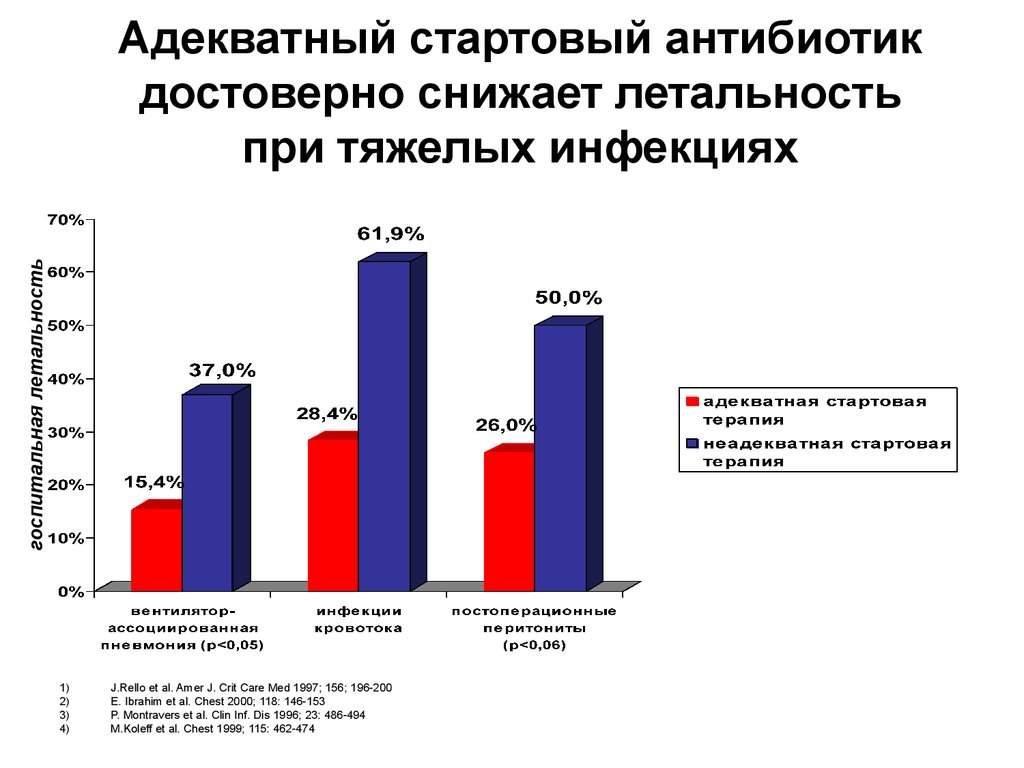
27. Адекватный стартовый антибиотик достоверно снижает летальность при тяжелых инфекциях
госпитальная летальностьАдекватный стартовый антибиотик
достоверно снижает летальность
при тяжелых инфекциях
1)
2)
3)
4)
J.Rello et al. Amer J. Crit Care Med 1997; 156; 196-200
E. Ibrahim et al. Chest 2000; 118: 146-153
P. Montravers et al. Clin Inf. Dis 1996; 23: 486-494
M.Koleff et al. Chest 1999; 115: 462-474
28.
29.
Основной механизм устойчивости Грам(-) бактерий кбета-лактамам – продукция бета-лактамаз
Клинически значимые бета-лактамазы Грам(-) бактерий
Класс А
широкого
расширенного
спектра
спектра
Класс С
Тип
TEM, SHV
TEM, SHV, CTX-M
AmpC
Локализация
генов
плазмидная
плазмидная
Субстратный
профиль
Амп, Цеф I(II) Амп, Цеф I-IV
Амп, Цеф I-III
Чувствит-ть к
ингибиторам
Да
Нет
Сохраняют эфф-ть
Карб, ЦефIII-IV Карб, Цеф/СБ
Да
хромосомная
Цефепим, Карб
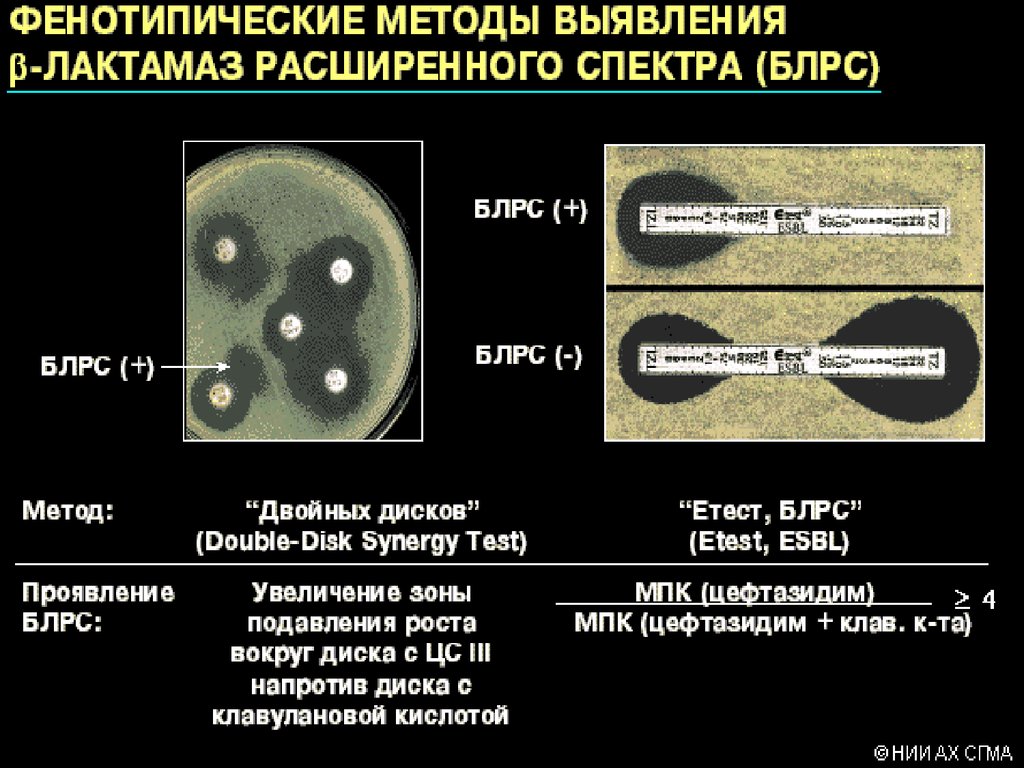
30.
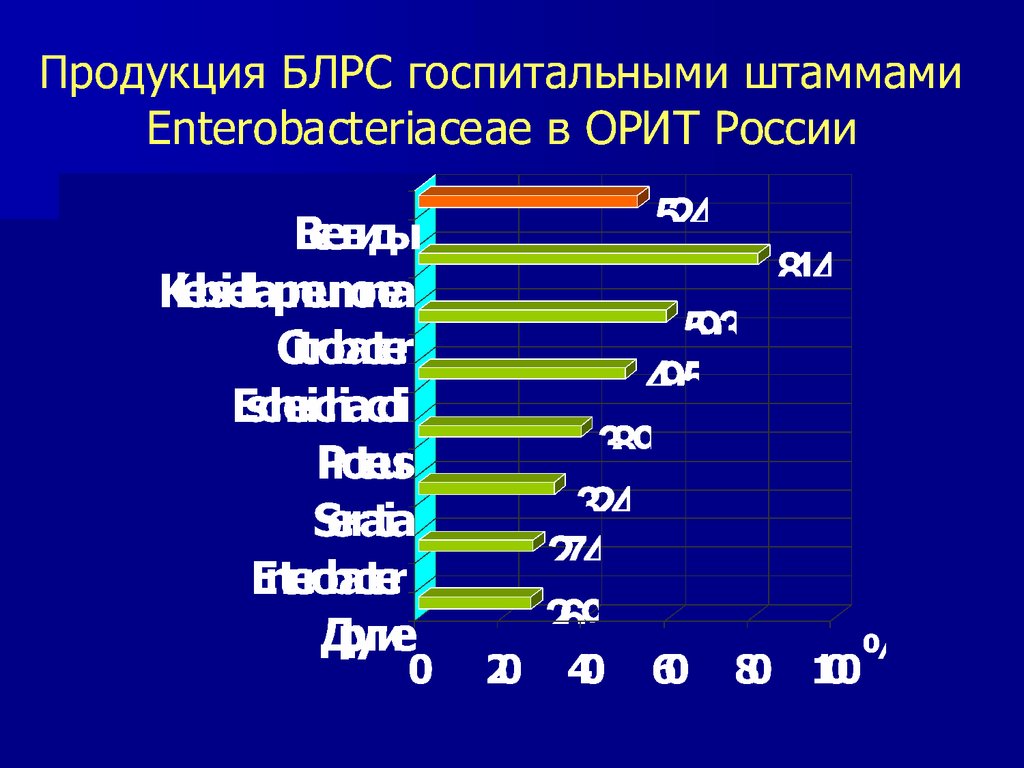
Бета-лактамазы расширенного спектра• Наиболее часто выявляются у нозокомиальных штаммов
Klebsiella spp., E.coli, P.mirabilis
– Частота продукции БЛРС в ОРИТ 53-88%
• Снижение клинической эффективности всех
цефалоспоринов при формальной чувствительности (МПК 28 мкг/мл)
• Высокий уровень ассоциированной устойчивости
(>50%) к аминогликозидам и фторхинолонам
• Практически важно:
– При выявлении устойчивости хотя бы к одному
цефалоспорину III
интерпретировать как устойчивость
ко всем цефалоспоринам
31.
32.
33.
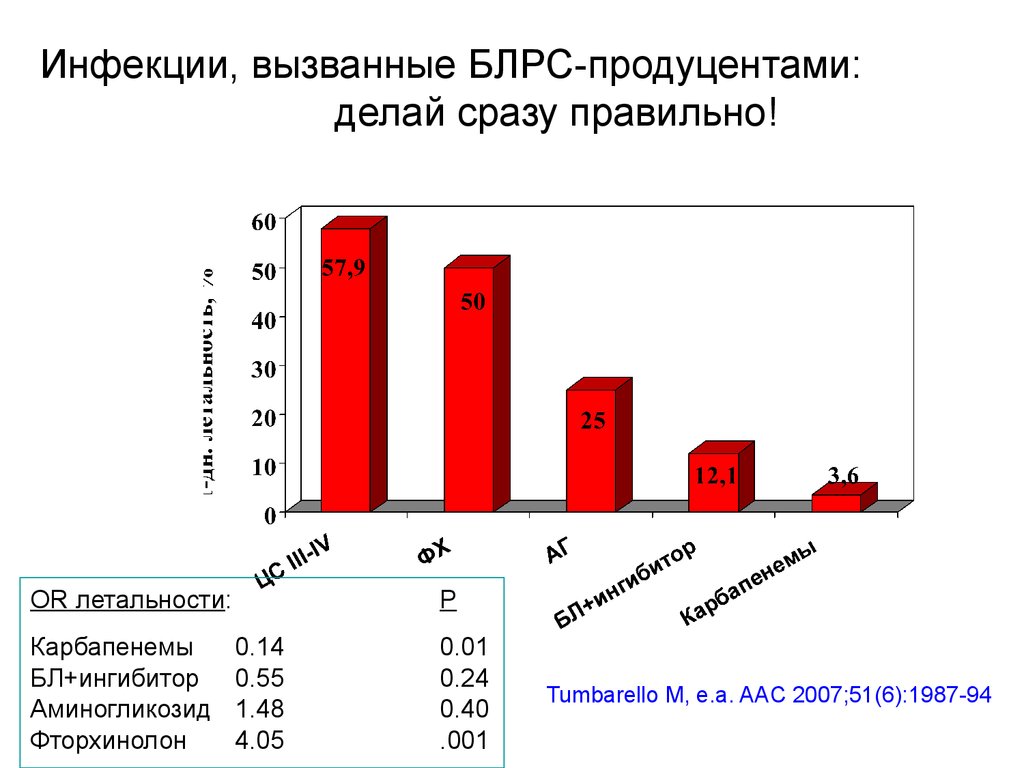
Инфекции, вызванные БЛРС-продуцентами:делай сразу правильно!
OR летальности:
Карбапенемы
БЛ+ингибитор
Аминогликозид
Фторхинолон
Р
0.14
0.55
1.48
4.05
0.01
0.24
0.40
.001
Tumbarello M, e.a. AAC 2007;51(6):1987-94
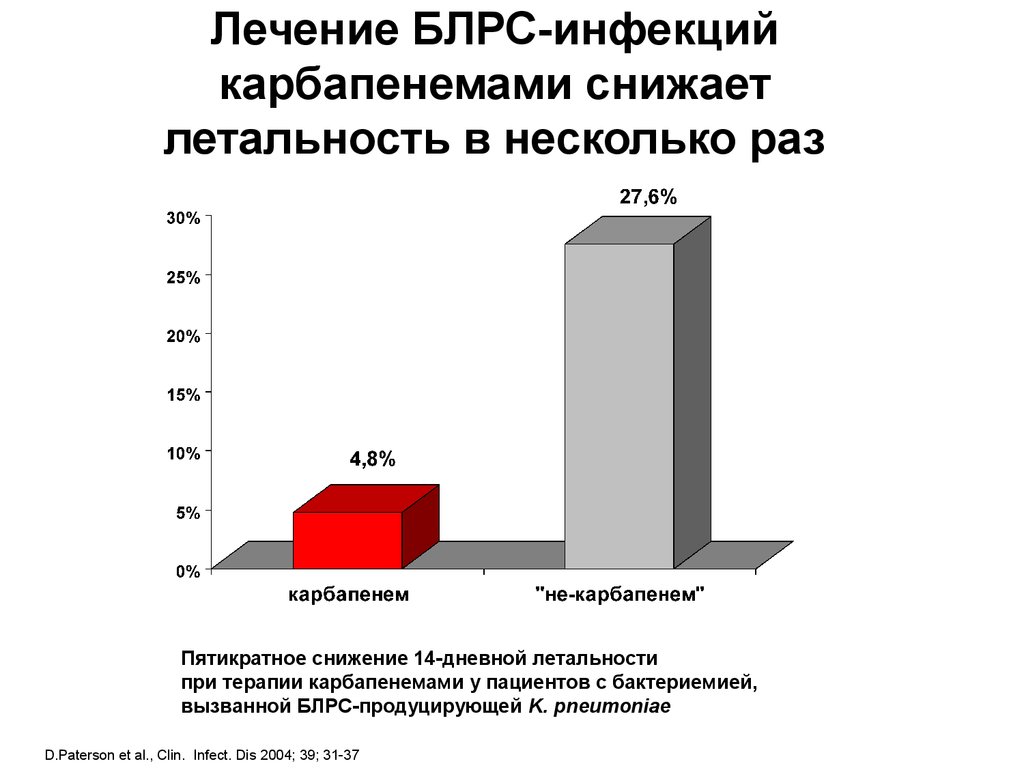
34. Лечение БЛРС-инфекций карбапенемами снижает летальность в несколько раз
Пятикратное снижение 14-дневной летальностипри терапии карбапенемами у пациентов с бактериемией,
вызванной БЛРС-продуцирующей K. pneumoniae
D.Paterson et al., Clin. Infect. Dis 2004; 39; 31-37
35.
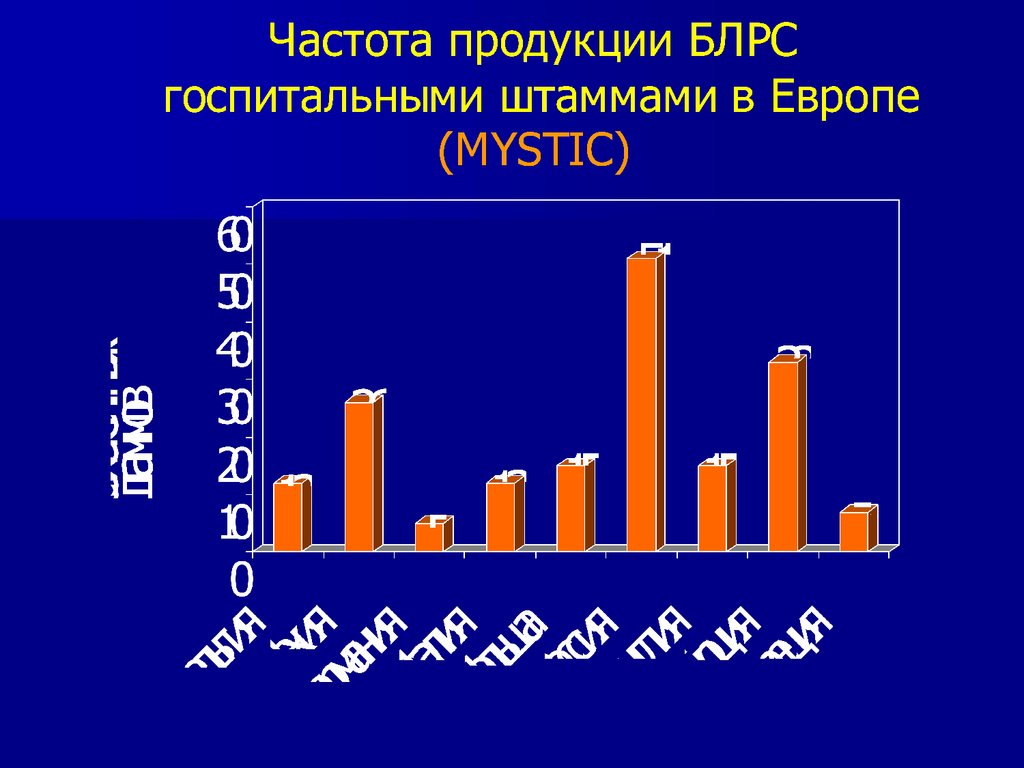
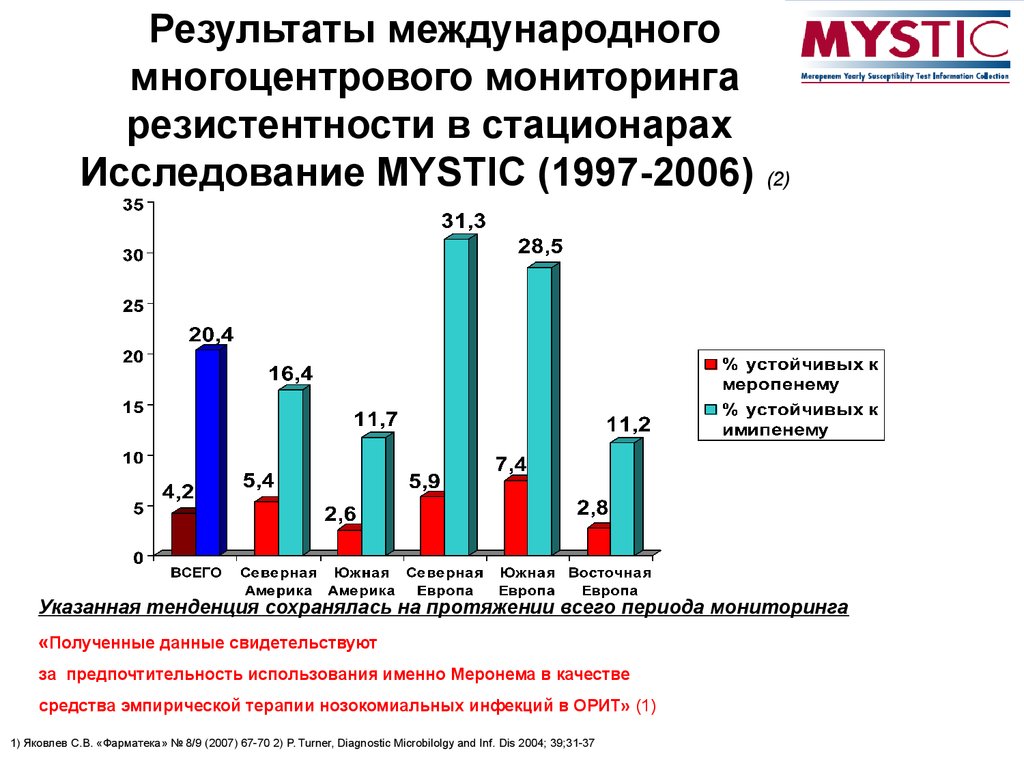
36. Результаты международного многоцентрового мониторинга резистентности в стационарах Исследование MYSTIC (1997-2006) (2)
Указанная тенденция сохранялась на протяжении всего периода мониторинга«Полученные данные свидетельствуют
за предпочтительность использования именно Меронема в качестве
средства эмпирической терапии нозокомиальных инфекций в ОРИТ» (1)
1) Яковлев С.В. «Фарматека» № 8/9 (2007) 67-70 2) P. Turner, Diagnostic Microbilolgy and Inf. Dis 2004; 39;31-37
37.
38.
Резистентный стафилококкMethicillin ((O
Oxacillin
xacillin))
R esistant
S taphylococcus
A ureus
Оксациллин
Цефазолин
Цефтриаксон
Имипинем
Гентамицин
Клиндомицин
Ванкомицин
Линезолид
R
R
S
S
R
S
R
R
R
S
S
• Механизм устойчивости: модификация мишени действия всех
бета-лактамных антибиотиков – пенициллинсвязывающего белка
• MRSA – устойчивы ко всем беталактамным антибиотикам
• Ассоциированная устойчивость
Аминогликозиды
Линкозамины
Макролиды
Тетрациклины
39.
Распространение МRSA в России принозокомиальных инфекциях
Диапазон
В среднем
1995 – 1996
0 – 40%
9.5%
2000 – 2001
0 – 89.5%
33.5%
[С.В. Сидоренко]
[А.В. Дехнич]
2004 – Москва
[Сидоренко и соавт]
64.9%
В настоящее время в ОРИТ России – 41%
При выделении из крови – 63%
40.
41.
42.
ХУЖЕ НЕ БЫВАЕТ?- Карбапенемазы (KPC и др.)
- VISA и VRSA
- VRE
- C.difficile
- MDR >1 препарата из 3-х и более классов а/б
- ХDR > 1 препарата из всех классов а/б
- PDR > ко всем известным а/б
Дефицит новых антибиотиков
10 X ‘20: ID EXPERTS CALL FOR 10 NEW ANTIBIOTICS BY 2020
Infectious Diseases Society of America Urges Development of New Antibiotics
to Address Global Drug Resistance Crisis
ARLINGTON, Va. — The Infectious Diseases Society of America (IDSA) has asked
for a commitment from the Obama administration and the European Union to further
the Society’s mission to achieve the development of 10 new antibiotics within the
next 10 years, known as the 10 x ’20 Initiative. The World Health Organization
(WHO) has identified antimicrobial resistance as one of the three greatest threats to
human health.
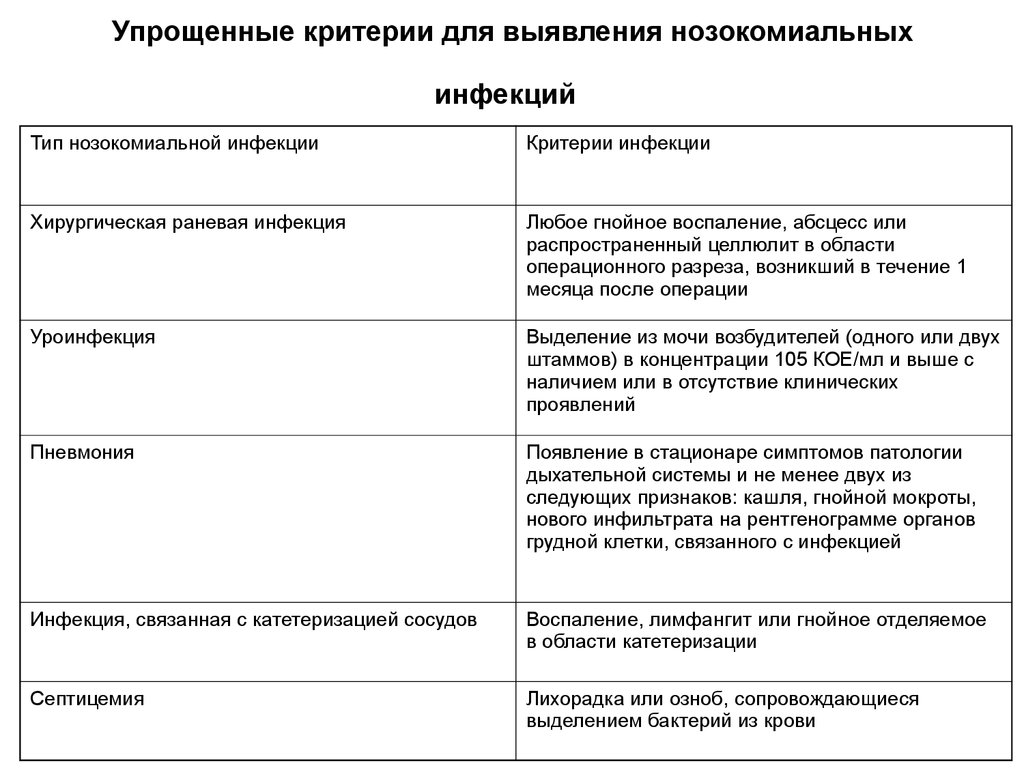
43. Упрощенные критерии для выявления нозокомиальных инфекций
Тип нозокомиальной инфекцииКритерии инфекции
Хирургическая раневая инфекция
Любое гнойное воспаление, абсцесс или
распространенный целлюлит в области
операционного разреза, возникший в течение 1
месяца после операции
Уроинфекция
Выделение из мочи возбудителей (одного или двух
штаммов) в концентрации 105 КОЕ/мл и выше с
наличием или в отсутствие клинических
проявлений
Пневмония
Появление в стационаре симптомов патологии
дыхательной системы и не менее двух из
следующих признаков: кашля, гнойной мокроты,
нового инфильтрата на рентгенограмме органов
грудной клетки, связанного с инфекцией
Инфекция, связанная с катетеризацией сосудов
Воспаление, лимфангит или гнойное отделяемое
в области катетеризации
Септицемия
Лихорадка или озноб, сопровождающиеся
выделением бактерий из крови
44.
Контроль антибиотикорезистентностиМаксимальная терапия с учетом разумной достаточности
– Де-эскалация
– Исключить профилактическое лечение
– Не лечить колонизацию
– Сокращение длительности курсов АБ терапии
– Интраоперационная профилактика в хирургии
– Своевременное удаление инородных тел (катетеры)
Контроль переноса инфекций, эпид
эпид.. мероприятия
Фармакодинамическое обоснование режимов дозирования
Формуляр и химиотерапевтическая служба
Мониторинг возбудителей и их резистентности в конкретном
отделении
Реальное взаимодействие микробиологической службы и
клиницистов
45.
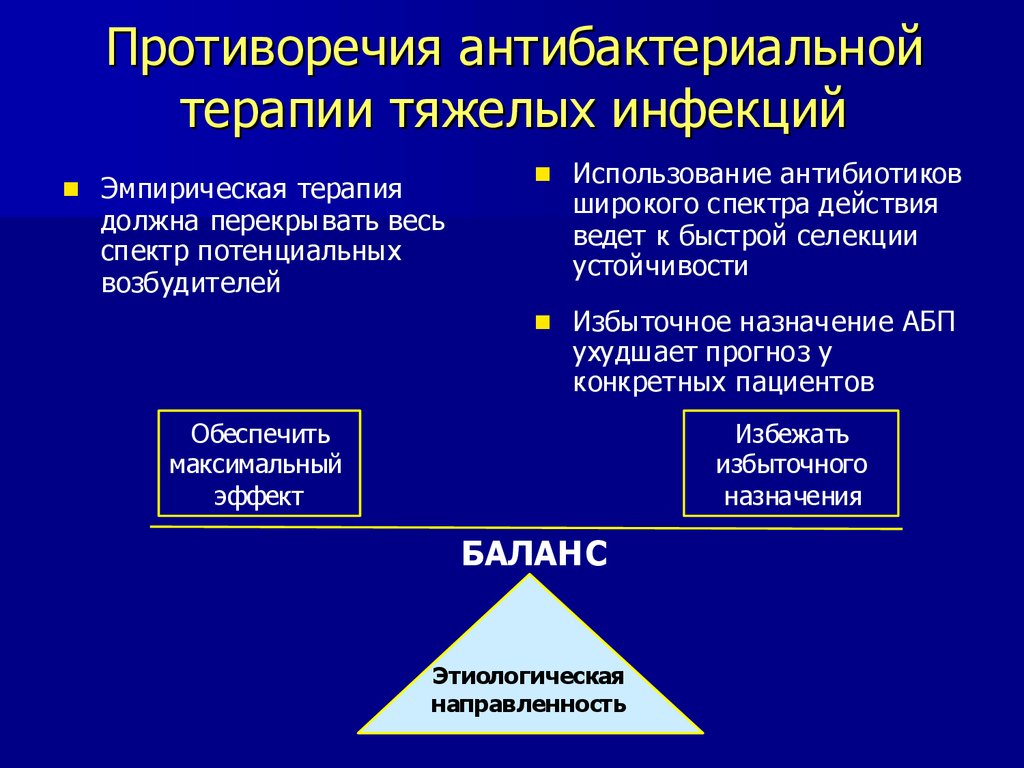
Противоречия антибактериальнойтерапии тяжелых инфекций
Эмпирическая терапия
Использование антибиотиков
должна перекрывать весь
спектр потенциальных
возбудителей
широкого спектра действия
ведет к быстрой селекции
устойчивости
Избыточное назначение АБП
ухудшает прогноз у
конкретных пациентов
Обеспечить
максимальный
эффект
Избежать
избыточного
назначения
БАЛАНС
Этиологическая
направленность
46.
47.
48.
49.
50.
Профилактика нозокомиальных инфекций в ОРИТ (общие требования)- Изоляция
- Сокращение койко-дня
- 1 больной – 1 медсестра
- Мытьё рук персоналом!!!!!
- Уменьшение «инвазивности»
- Дезинфекция и стерилизация
- Ограничение необоснованной и эскалационной антибактериальной терапии
- Профилактика аспирации
- Микробиологически безопасная интубация и трахеостомия (удаление
надманжеточной жидкости снижает время пребывания в ОРИТ)
- Микробиологический мониторинг
- Отмена а/б терапии при клиническом и лабораторном улучшении (PCT< 2
нг/мл)
- Уменьшение седации
51. Профилактика нозокомиальных инфекций в ОРИТ (частные требования)
• Профилактика госпитальной пневмонии: приподнятыйголовной конец на 30-45*, специальные ЭТТ и ТСТ,
неинвазивная ИВЛ, постоянное ПДКВ, стерильное
увлажнение, уменьшение седации в дневное время,
использование протоколов отлучения от ИВЛ, увеличение
давления в манжете
• Профилактика инфекций кровотока: строгая асептика при
установке и использовании катетера, своевременное
удаление, использование современных материалов,
безигольных коннектеров и пластиковых инфузионных
пакетов
• Профилактика госпитальной уроинфекции: анестезия во
время установки катетера, замкнутая дренажная система,
отказ от промывания
• Профилактика инфекций кожи и мягких тканей и
пролежней: использования р-ров с антисептиками для
мытья, адекватная нутритивная поддержка, п/пролежневые
матрасы, увеличение нагрузки на сестер, спец. повязки и
гидрогели
• Антибиотикопрофилактика в хирургии
52.
53.
54.
55. ДВА СЛУЧАЯ ГОСПИТАЛЬНОГО СЕПСИСА, АССОЦИИРОВАННОГО С PSEUDOMONAS AERUGINOSA В ИНФЕКЦИОННОМ СТАЦИОНАРЕ Ляпустин С.Б., Карпунина Т.И., Кузнецова М.В. (ГУ
ДВА СЛУЧАЯ ГОСПИТАЛЬНОГО СЕПСИСА, АССОЦИИРОВАННОГО СPSEUDOMONAS AERUGINOSA В ИНФЕКЦИОННОМ СТАЦИОНАРЕ
Ляпустин С.Б., Карпунина Т.И., Кузнецова М.В.
(ГУЗ «ККИБ» г.Пермь, ПГМА им. ак. Е.А.Вагнера, ИЭГМ УрО РАН)
56. Клинические наблюдения
Пациент Г. 52 лет, ОРИТ ККИБ с 11.06.06. по 10.09.06 с диагнозом:Клещевой энцефалит, менингоэнцефалополиомиелитическая форма,
тяжелое течение (Ig М к вирусу КЭ в СМЖ и крови от 11.06.06.)
Пациент Б., 17 лет, ОРИТ ККИБ с 10.08.06 по 27.08.06 с диагнозом:
Вирусный гепатит А (аВГА IgM +), острый, тяжелое течение +
нейтропения.
Пациентка К., 53 лет, диагностическое отделение ККИБ с 28.08.06 по
12.09.06 с диагнозом: Рожистое воспаление левой голени,
эритематозная форма. Трофическая язва левой голени. Сахарный
диабет I типа. Диабетическая остеоартропатия левой стопы.
Хронический лимфостаз. Хронический остеомиелит плюсневых
костей, свищевая форма.
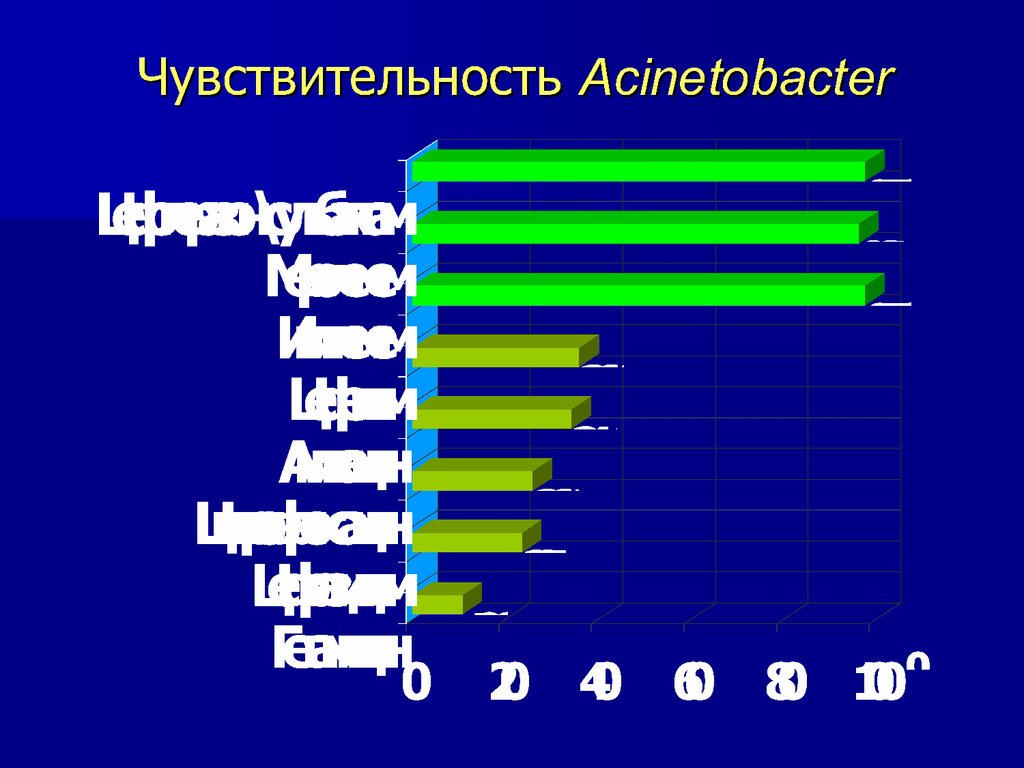
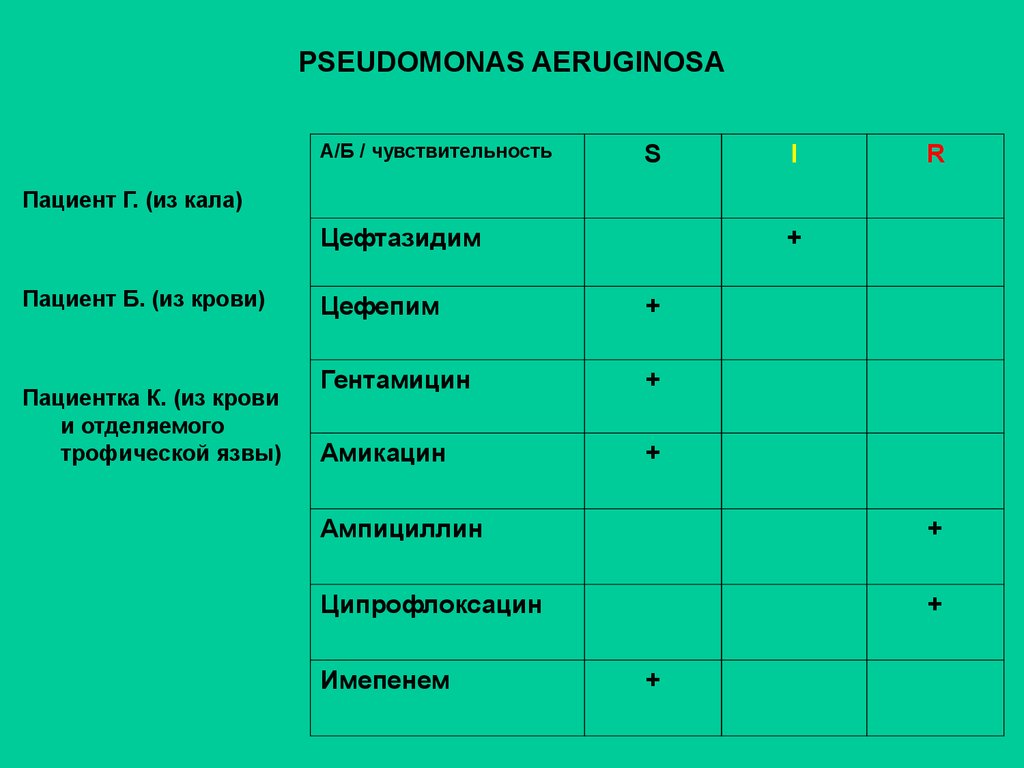
57. PSEUDOMONAS AERUGINOSA
А/Б / чувствительностьS
I
R
Пациент Г. (из кала)
Цефтазидим
Пациент Б. (из крови)
Пациентка К. (из крови
и отделяемого
трофической язвы)
+
Цефепим
+
Гентамицин
+
Амикацин
+
Ампициллин
+
Ципрофлоксацин
+
Имепенем
+
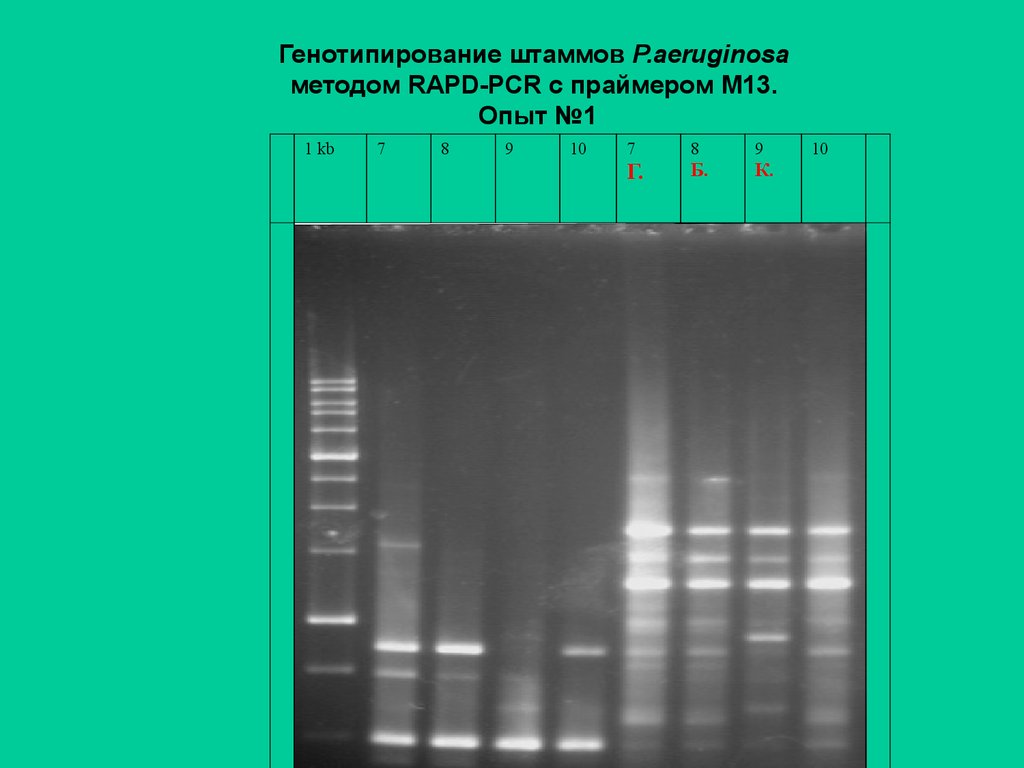
58. Генотипирование штаммов P.aeruginosa методом RAPD-PCR с праймером М13. Опыт №1
1 kb7
8
9
10
7
8
9
Г.
Б.
К.
10
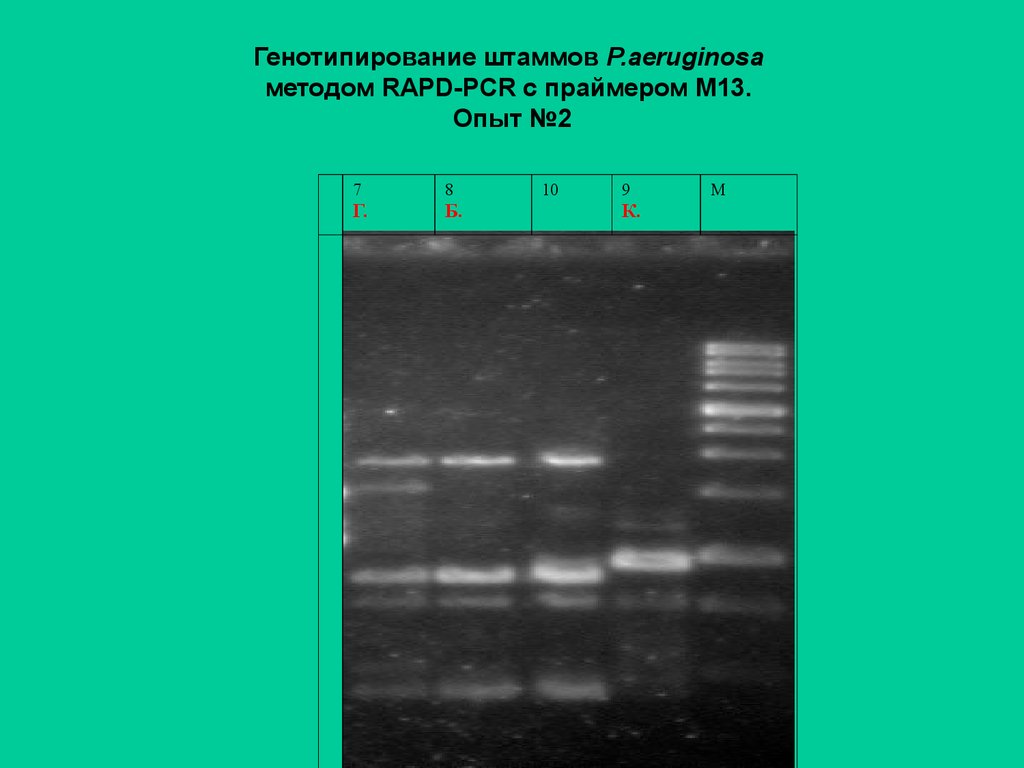
59. Генотипирование штаммов P.aeruginosa методом RAPD-PCR с праймером М13. Опыт №2
78
Г.
Б.
10
9
К.
М
60. Эпидемиологическое расследование
Обследование всех сотрудников ОРИТ ККИБ: носительство
P.aeruginosa не выявлено
При исследовании смывов с медицинского оборудования и
инструментария ОРИТ P.aeruginosa не обнаружена
61. Выводы
Проявления внутрибольничной инфекции маскируются
воспалительной симптоматикой основного заболевания,
послужившего поводом для госпитализации.
Формирование и циркуляция госпитальных штаммов в
инфекционных стационарах может приводить к формированию
некультивируемых форм бактерий
Для подтверждения нозокомиальной природы изолируемых
бактериальных культур, их этиологической значимости, в
особенности в случае летального исхода, молекулярногенетические методы исследования могут быть приоритетными.
62.
63.
64.
65.
66.
67.
ПЕРСПЕКТИВЫ-А/б терапия: новые препараты?; рациональное использование «старых»,
тайм-ауты в а/б терапии, использование а/б вне стационара и т.д.
-Вакцинация
-бактериофаги
-Уменьшение инвазивности
-Донорская микробиота кишечника для лечения C.difficile









































 medicine
medicine








