Similar presentations:
Иммунотерапия + клинический случай
1. Иммунотерапия + клинический случай
Старые проблемы - новые решения!Иммунотерапия + клинический случай
Черепова Евгения Владимировна
Студентка 5 курса 13 группы
Сеченовский Университет ИЗД
04 ноября 2019 г.
2. Иммунная система человека
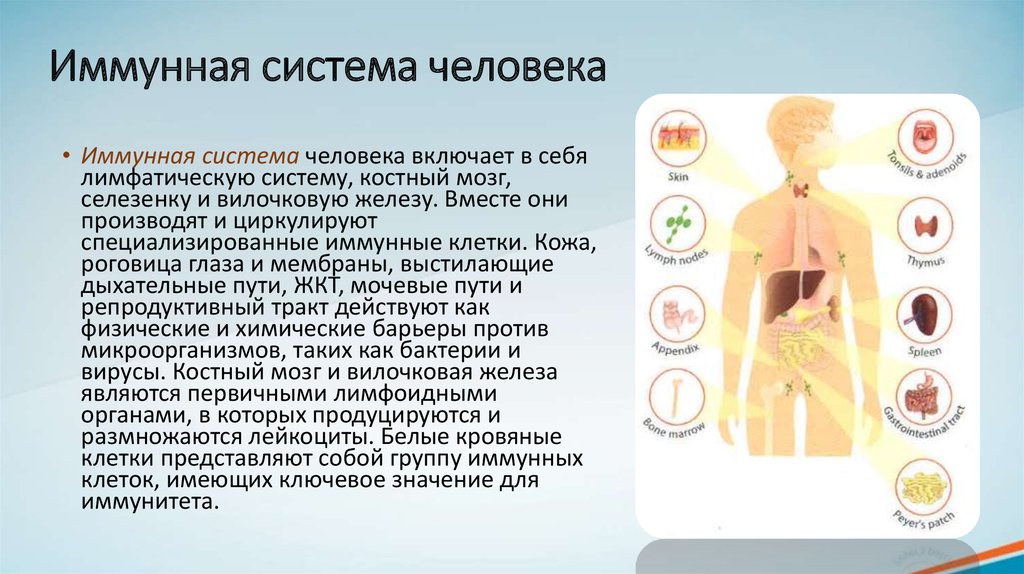
• Иммунная система человека включает в себялимфатическую систему, костный мозг,
селезенку и вилочковую железу. Вместе они
производят и циркулируют
специализированные иммунные клетки. Кожа,
роговица глаза и мембраны, выстилающие
дыхательные пути, ЖКТ, мочевые пути и
репродуктивный тракт действуют как
физические и химические барьеры против
микроорганизмов, таких как бактерии и
вирусы. Костный мозг и вилочковая железа
являются первичными лимфоидными
органами, в которых продуцируются и
размножаются лейкоциты. Белые кровяные
клетки представляют собой группу иммунных
клеток, имеющих ключевое значение для
иммунитета.
3.
Роль иммунной системы заключается в защите организма от чужеродныхили опасных захватчиков, включая микроорганизмы (бактерии, вирусы,
грибы) и раковые клетки. Чтобы сделать это избирательно, иммунная
система должна уметь различать свои (нормальные клетки,
принадлежащие человеку) и чужие (аномальные клетки или частицы,
которые чужды человеку).
• Нормальный иммунный ответ включает в себя:
1. Распознавание потенциально вредных антигенов.
Они могут возникнуть вне тела, например, от вторгающихся бактерий, или
изнутри тела, например нормальные клетки, которые мутировали и
потенциально могли стать, или уже стали злокачественными.
2. Активация и мобилизация защиты клеток и антител.
3. Атака против захватчика или аномальной клетки.
4. Прекращение атаки после противодействия угрозе.
4.
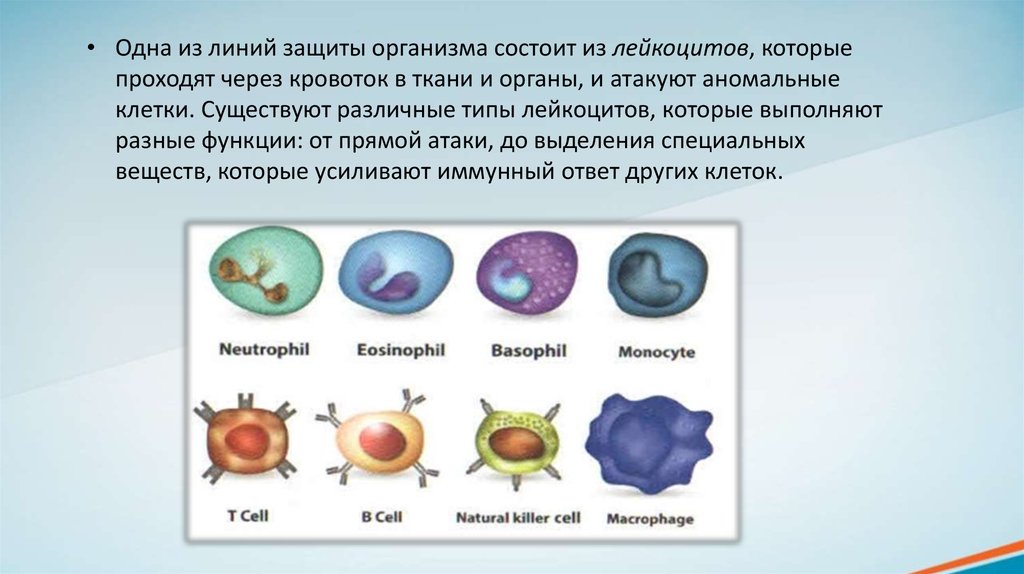
• Одна из линий защиты организма состоит из лейкоцитов, которыепроходят через кровоток в ткани и органы, и атакуют аномальные
клетки. Существуют различные типы лейкоцитов, которые выполняют
разные функции: от прямой атаки, до выделения специальных
веществ, которые усиливают иммунный ответ других клеток.
5.
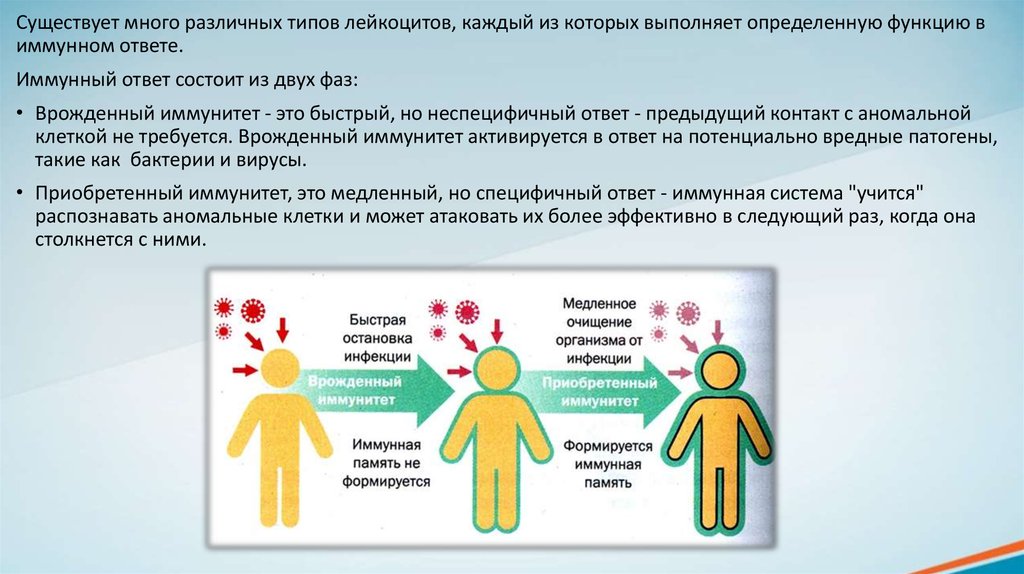
Существует много различных типов лейкоцитов, каждый из которых выполняет определенную функцию виммунном ответе.
Иммунный ответ состоит из двух фаз:
• Врожденный иммунитет - это быстрый, но неспецифичный ответ - предыдущий контакт с аномальной
клеткой не требуется. Врожденный иммунитет активируется в ответ на потенциально вредные патогены,
такие как бактерии и вирусы.
• Приобретенный иммунитет, это медленный, но специфичный ответ - иммунная система "учится"
распознавать аномальные клетки и может атаковать их более эффективно в следующий раз, когда она
столкнется с ними.
6. Иммуннотерапия
• Иммунотерапия — это лечение, подразумевающее искусственное воздействиена иммунитет при помощи лекарственных препаратов. Принципы метода
заключаются в стимуляции защитных функций или подавлении неспецифичных
функций. При активизации естественной защиты организма применяют
лекарственные средства, стимулирующие скрытые резервы для борьбы с
болезнью.
• Действие лекарственных препаратов иммунотерапии заключается в
естественном противораковом иммунном ответе организма на атаку, в то время
как химиотерапия влияет непосредственно на рост и пролиферацию
опухолевых клеток. Иммунные контрольные точки предназначены для
отключения иммунного ответа и предотвращения повреждения здоровых
клеток. Но опухолевые клетки перенимают этот механизм и деактивируют Тклетки. Ингибиторы контрольных точек и ингибиторы пути предотвращают эту
дезактивацию и увеличивают противоопухолевый иммунный ответ организма.
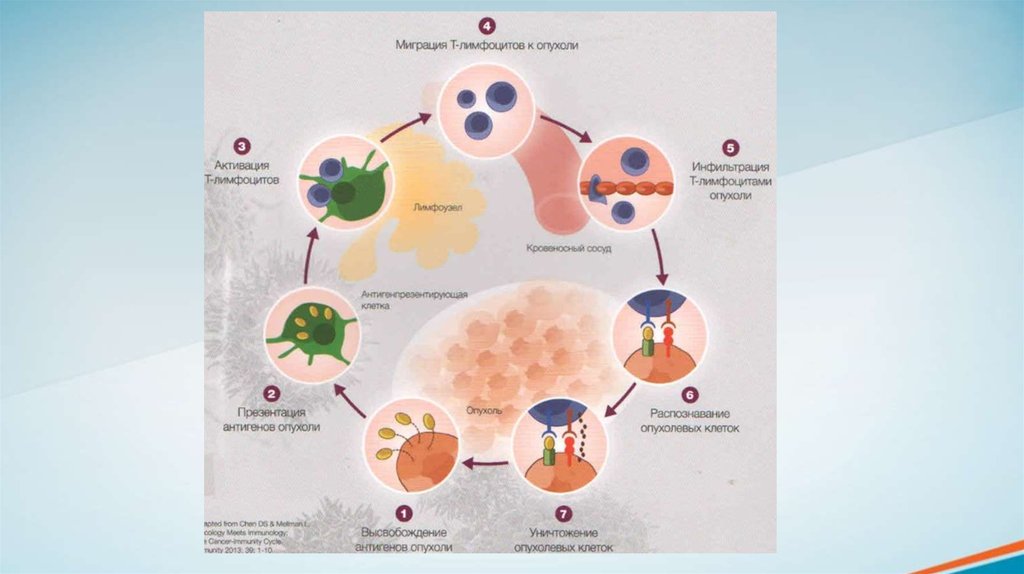
7. Противоопухолевый иммунный ответ
Цикл противоопухолевого иммунного ответа состоит из нескольких этапов:1.
Высвобождение антигенов опухоли. Наличие опухолевых антигенов является пусковым механизмом для запуска
противоопухолевого иммунного ответа.
2.
Презентация антигенов опухоли. Антигены, выделяемые опухолью, не активируют Т-лимфоциты напрямую, а
захватываются антигенпрезентирующими клетками, например, дендритными клетками, макрофагами, Влимфоцитами. Антигенпрезентирующие клетки поглощают и перерабатывают антигены (процессинг). После
процессинга, антигенпрезентирующие клетки представляют фрагменты антигенов на своей поверхности с помощью
главного комплекса гистосовместимости.
3.
Активация Т-лимфоцитов. Для активации Т-лимфоцитов необходимо 2 сигнала:
• Т-клеточный рецептор взаимодействует с опухолевым антигеном (с участием главного комплекса гистосовместимости)
• Костимулирующий рецептор CD28 на Т-лимфоците, связывается с CD80 и CD86, на антигенпрезентирующей клетке.
• Затем происходит пролиферация активированных T-лимфоцитов.
4.
Миграция Т-лимфоцитов к опухоли.
5.
Инфильтрация Т-лимфоцитами опухоли.
6.
Распознавание опухолевых клеток. Происходит благодаря связыванию Т-клеточного рецептора с распознанным
опухолевым антигеном на главном комплексе гистосовместимости.
7. Уничтожение опухолевых клеток. Т-лимфоцит уничтожает опухолевую клетку, что приводит к выбросу опухолевых
антигенов и цикл противоопухолевого иммунного ответа повторяется.
8.
9.
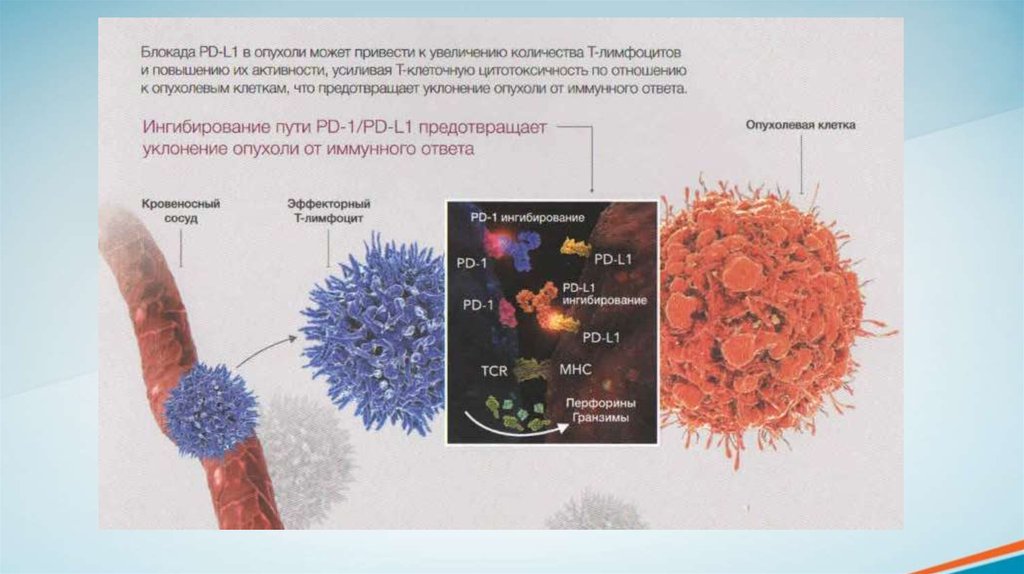
Опухолевые клетки используют различные механизмы уклонения от иммунногоответа. Один из них иммунные контрольные точки.
Иммунные контрольные точки являются рецепторами на поверхности Т-лимфоцитов и
других иммунокомпетентных клеток. Данные рецепторы связываются с
соответствующими лигандами, которые располагаются на опухолевых и других клетках и
подавляют Т-клеточный иммунный ответ.
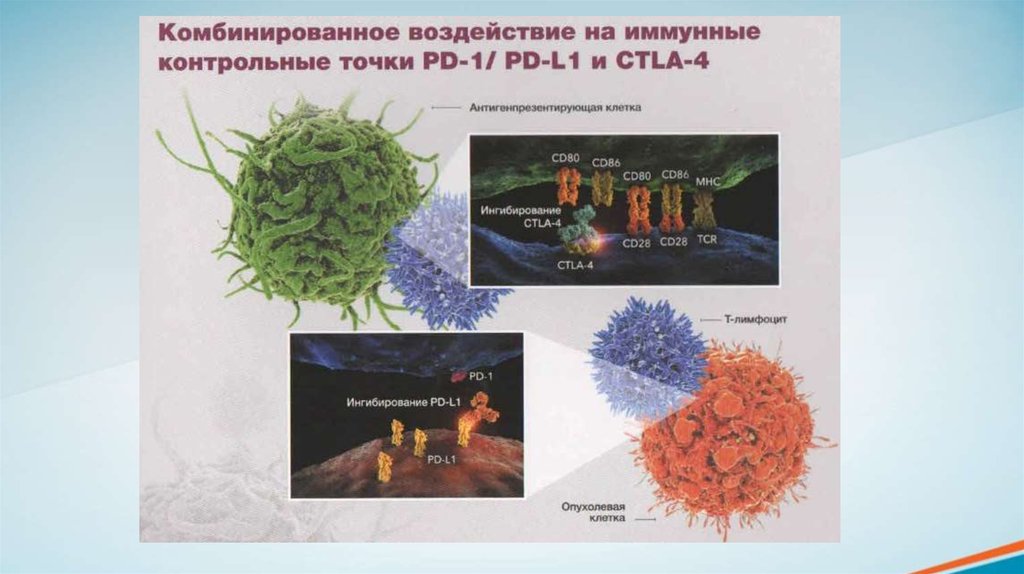
PD-1 (рецептор запрограммированной клеточной гибели 1) и СТLA-4 (ассоциированный с
цитотоксическими Т-лимфоцитами антиген 4) — наиболее изученные иммунные
контрольные точки, которые экспрессируются преимущественно Т-лимфоцитами.
CTLA-4 блокирует активацию Т-лимфоцитов на 3 этапе противоопухолевого иммунного
ответа.
Активация пути передачи сигналов от рецептора PD-1 происходит на завершающих
этапах цикла, после инфильтрации Т-лимфоцитами опухоли. Данные сигналы приводят к
инактивации Т-лимфоцитов.
10.
11.
12.
ИнгибированиеCTLA-4
13.
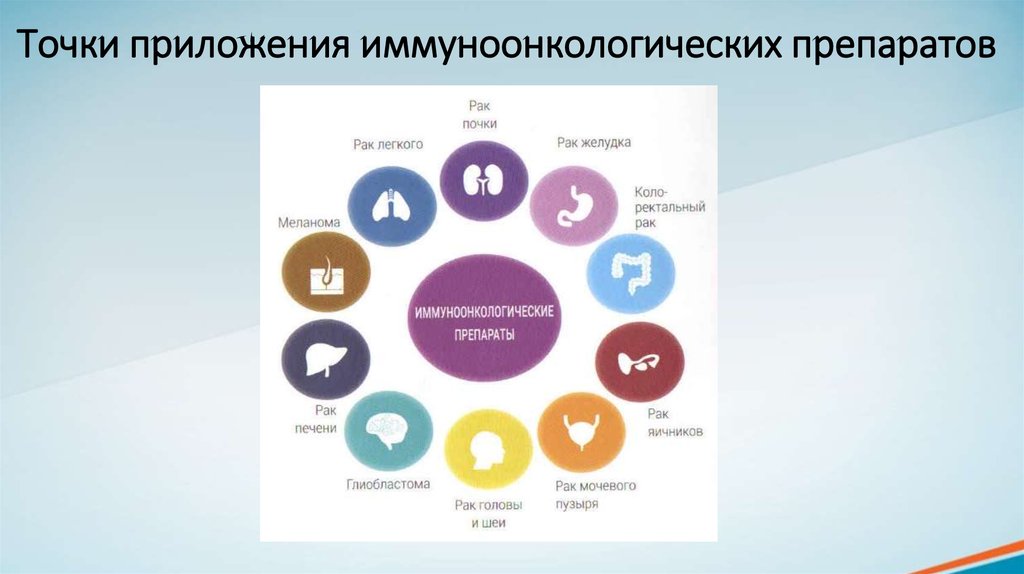
14. Точки приложения иммуноонкологических препаратов
15.
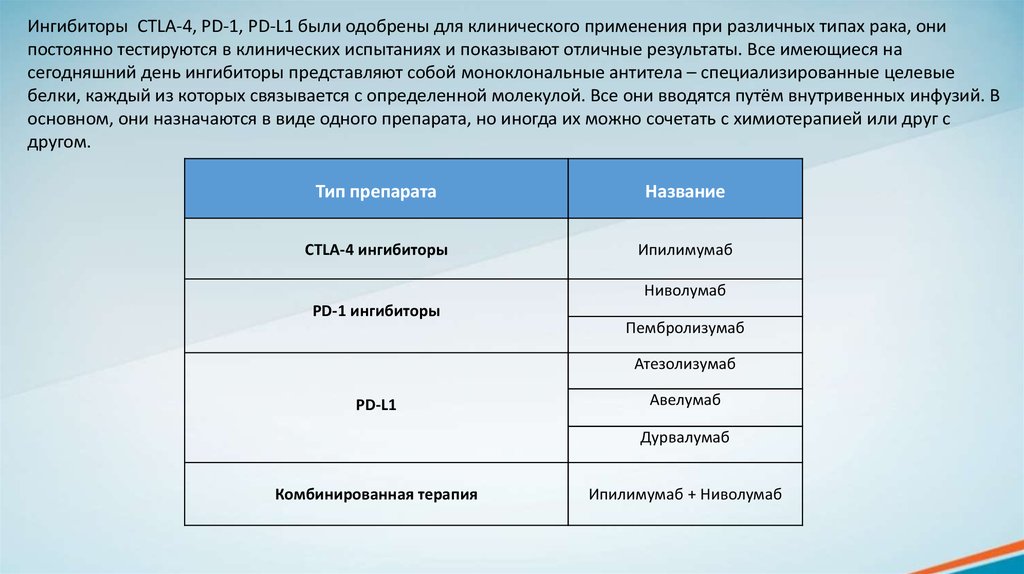
Ингибиторы CTLA-4, PD-1, PD-L1 были одобрены для клинического применения при различных типах рака, онипостоянно тестируются в клинических испытаниях и показывают отличные результаты. Все имеющиеся на
сегодняшний день ингибиторы представляют собой моноклональные антитела – специализированные целевые
белки, каждый из которых связывается с определенной молекулой. Все они вводятся путём внутривенных инфузий. В
основном, они назначаются в виде одного препарата, но иногда их можно сочетать с химиотерапией или друг с
другом.
Тип препарата
Название
CTLA-4 ингибиторы
Ипилимумаб
Ниволумаб
PD-1 ингибиторы
Пембролизумаб
Атезолизумаб
PD-L1
Авелумаб
Дурвалумаб
Комбинированная терапия
Ипилимумаб + Ниволумаб
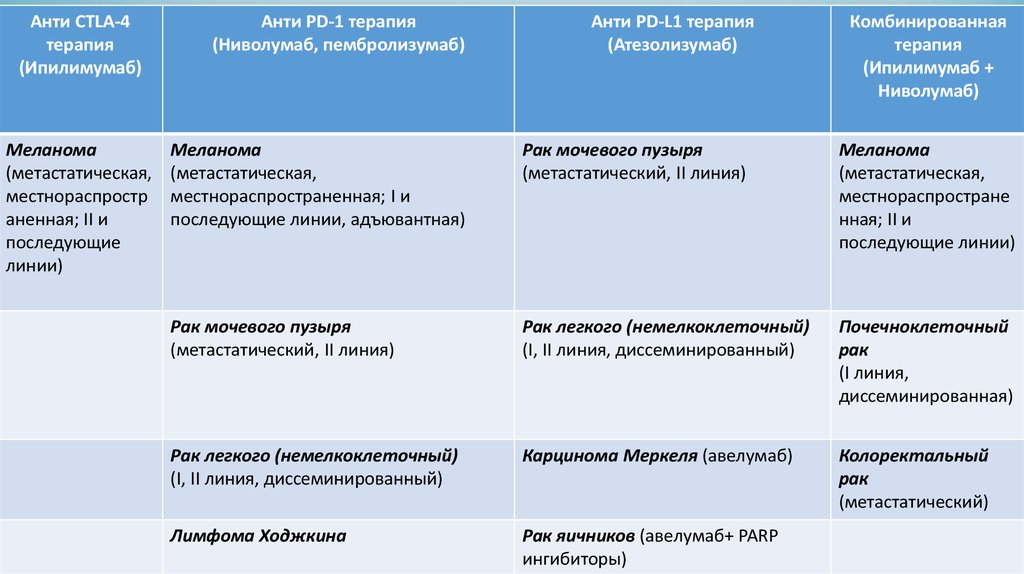
16.
Анти CTLA-4терапия
(Ипилимумаб)
Меланома
(метастатическая,
местнораспростр
аненная; II и
последующие
линии)
Анти PD-1 терапия
(Ниволумаб, пембролизумаб)
Анти PD-L1 терапия
(Атезолизумаб)
Комбинированная
терапия
(Ипилимумаб +
Ниволумаб)
Меланома
(метастатическая,
местнораспространенная; I и
последующие линии, адъювантная)
Рак мочевого пузыря
(метастатический, II линия)
Меланома
(метастатическая,
местнораспростране
нная; II и
последующие линии)
Рак мочевого пузыря
(метастатический, II линия)
Рак легкого (немелкоклеточный)
(I, II линия, диссеминированный)
Почечноклеточный
рак
(I линия,
диссеминированная)
Рак легкого (немелкоклеточный)
(I, II линия, диссеминированный)
Карцинома Меркеля (авелумаб)
Колоректальный
рак
(метастатический)
Лимфома Ходжкина
Рак яичников (авелумаб+ PARP
ингибиторы)
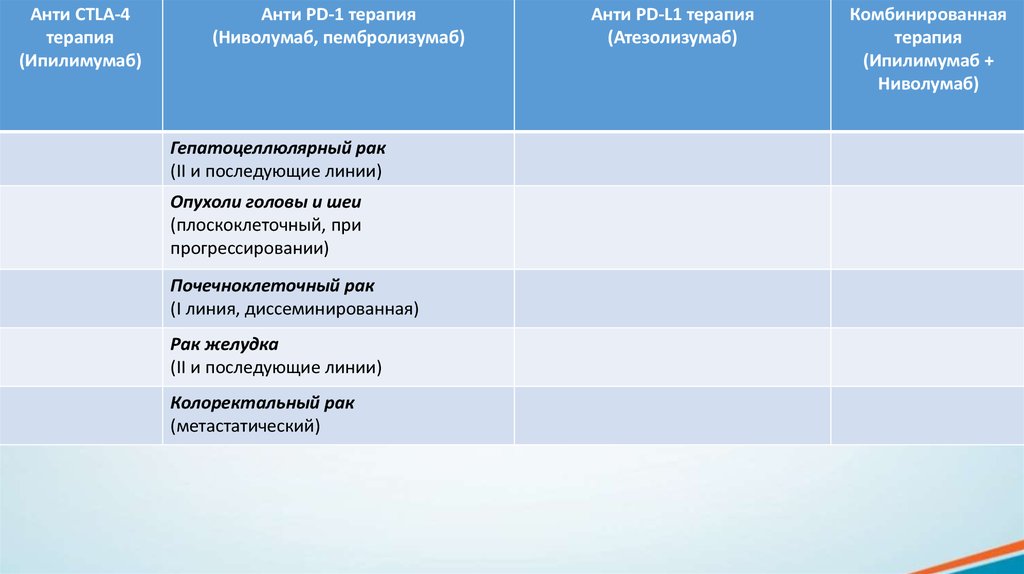
17.
Анти CTLA-4терапия
(Ипилимумаб)
Анти PD-1 терапия
(Ниволумаб, пембролизумаб)
Гепатоцеллюлярный рак
(II и последующие линии)
Опухоли головы и шеи
(плоскоклеточный, при
прогрессировании)
Почечноклеточный рак
(I линия, диссеминированная)
Рак желудка
(II и последующие линии)
Колоректальный рак
(метастатический)
Анти PD-L1 терапия
(Атезолизумаб)
Комбинированная
терапия
(Ипилимумаб +
Ниволумаб)
18.
Препараты, блокирующиеконтрольные точки
иммунного ответа,
потенциально могут
вызвать
иммуноопосредованные
нежелательные явления с
поражением любых
органов и систем.
19.
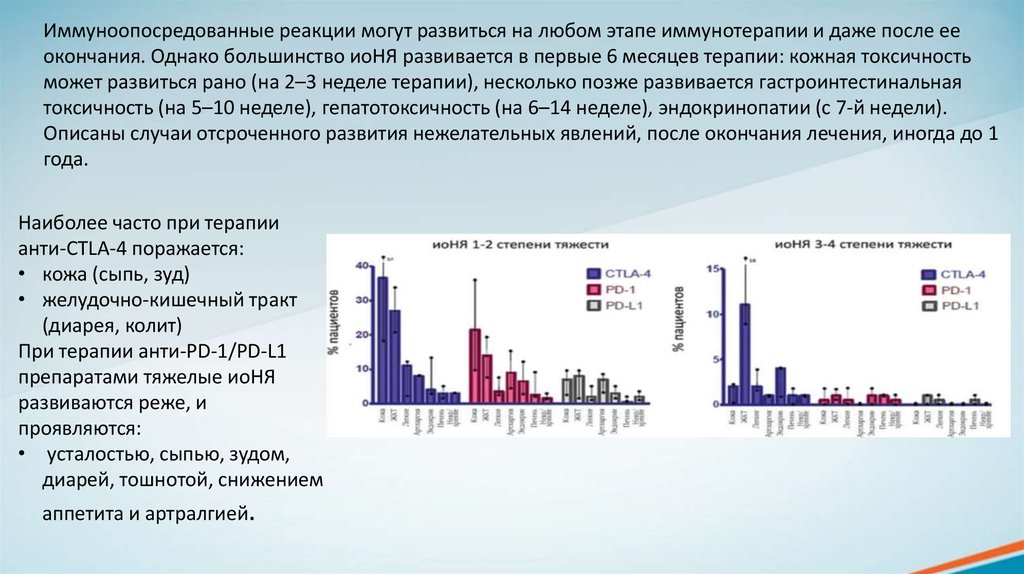
Иммуноопосредованные реакции могут развиться на любом этапе иммунотерапии и даже после ееокончания. Однако большинство иоНЯ развивается в первые 6 месяцев терапии: кожная токсичность
может развиться рано (на 2–3 неделе терапии), несколько позже развивается гастроинтестинальная
токсичность (на 5–10 неделе), гепатотоксичность (на 6–14 неделе), эндокринопатии (с 7-й недели).
Описаны случаи отсроченного развития нежелательных явлений, после окончания лечения, иногда до 1
года.
Наиболее часто при терапии
анти-CTLA-4 поражается:
• кожа (сыпь, зуд)
• желудочно-кишечный тракт
(диарея, колит)
При терапии анти-PD-1/PD-L1
препаратами тяжелые иоНЯ
развиваются реже, и
проявляются:
• усталостью, сыпью, зудом,
диарей, тошнотой, снижением
аппетита и артралгией.
20.
КЛИНИЧЕСКИЙ СЛУЧАЙПациент Д., 21 год.
Диагноз: Меланома кожи pT2aN2aM0 стадия III A
Анамнез заболевания:
Узловое образование кожи спины выявлено в июле 2017 года.
15.08.2017 - иссечение опухоли и регионарных лимфатических узлов.
Гистология (Молдова)-пигментная меланома. Мутация в гене BRAF- не
выявлено.
Пересмотр гистопрепаратов и иммуногистохимия в ЛРЦ – узловая
пигментная эпителиойдноклеточная меланома кожи, толщина опухоли по
Бреслоу 1,78 мкм, без изъязвления, метастаз меланомы pT2aN2a.
Выполнено молекулярно-генетическое исследование в ЛРЦ: не выявлена
мутация в гене BRAF, KIT (пересмотр в КГБ 62)
21.
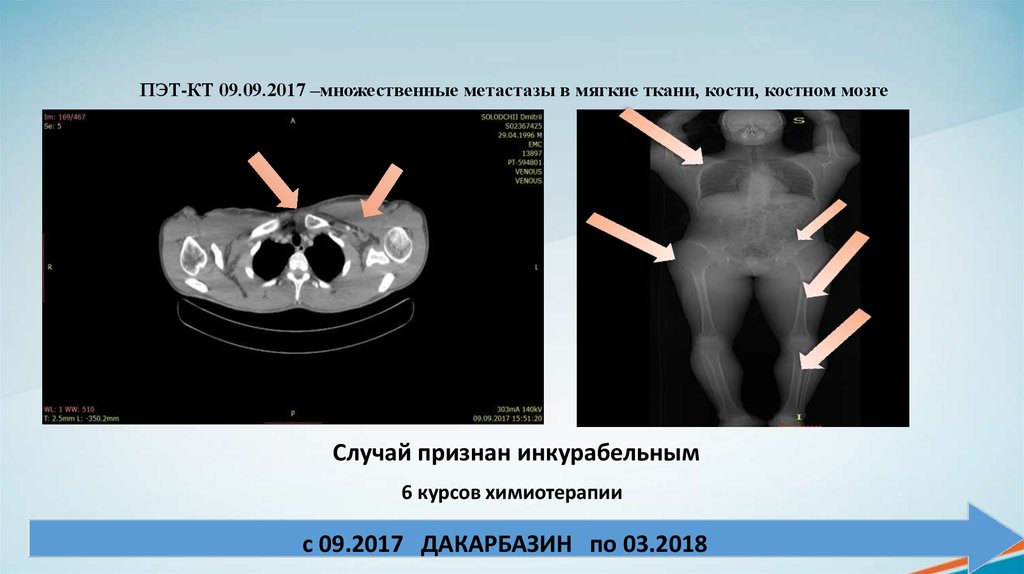
ПЭТ-КТ 09.09.2017 –множественные метастазы в мягкие ткани, кости, костном мозгеСлучай признан инкурабельным
6 курсов химиотерапии
c 09.2017 ДАКАРБАЗИН по 03.2018
22.
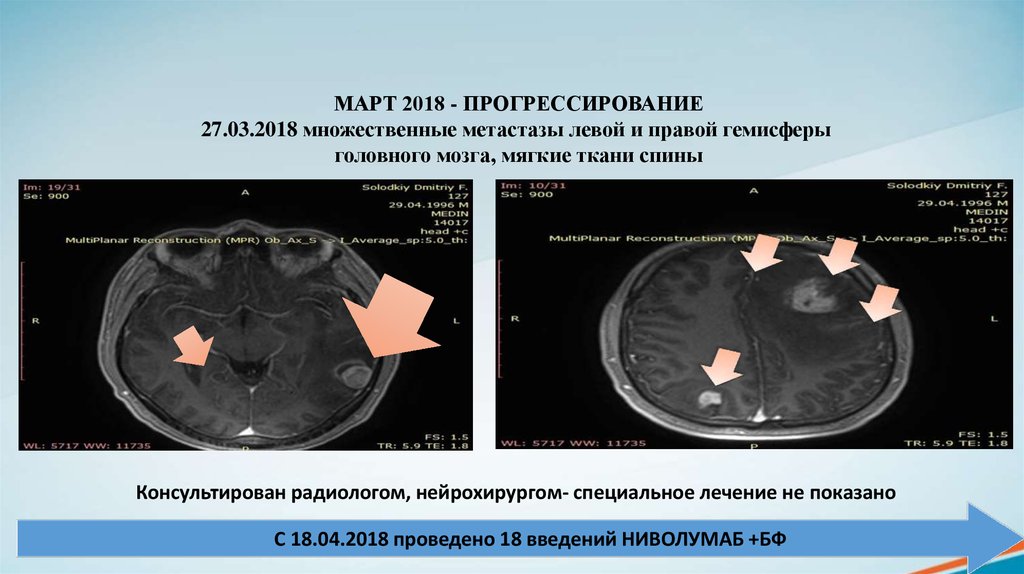
МАРТ 2018 - ПРОГРЕССИРОВАНИЕ27.03.2018 множественные метастазы левой и правой гемисферы
головного мозга, мягкие ткани спины
Консультирован радиологом, нейрохирургом- специальное лечение не показано
С 18.04.2018 проведено 18 введений НИВОЛУМАБ +БФ
23. ПЭТ-КТ – сентябрь 2018- выраженное уменьшение метастазов головного мозга и снижение уровня их метаболической активности.
Исчезновение патологической метаболическойактивности в образованиях мягких тканей, костях, костном мозге.
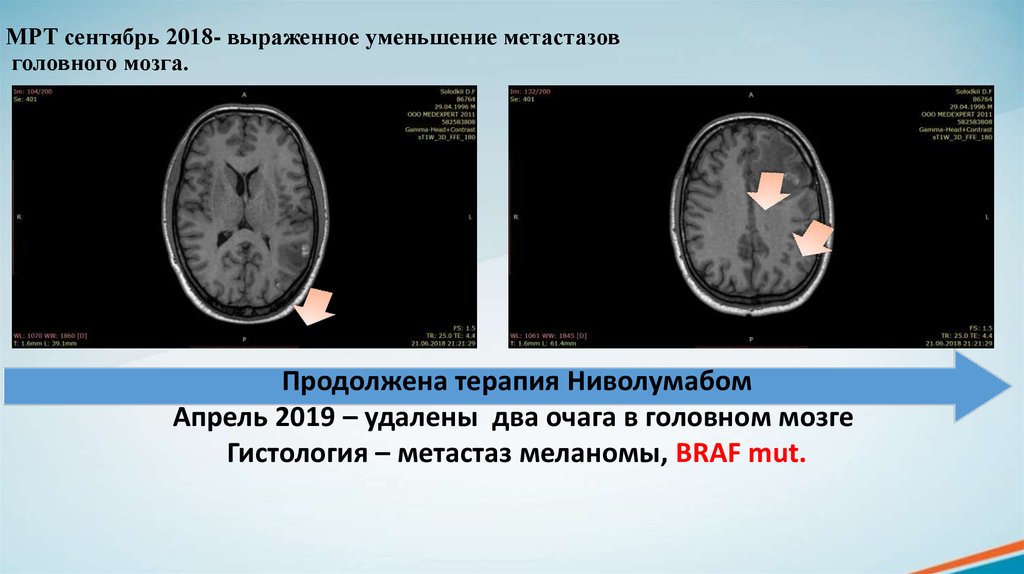
24. МРТ сентябрь 2018- выраженное уменьшение метастазов головного мозга.
Продолжена терапия НиволумабомАпрель 2019 – удалены два очага в головном мозге
Гистология – метастаз меланомы, BRAF mut.
25.
Проведено 22 курса иммунотерапии по схеме ниволумабКТ в июле 2019г – метастазы печени, селезенки, грудины, грудных и
поясничных позвонков, правой подвздошной кости
МРТ ГМ – образования без динамики, отек правой лобной области
2 курса вемурафениб
Сентябрь 2019г – прогрессирование: рост метастазов в головном мозге,
новые очаги
Проведен 1 курс химиотерапии по схеме: Темозоломид
03.10.19г – удаление метастаза головного мозга
Прогрессирование: продолженный рост метастазов гм, кровоизлияние из
метастаза в левую гемисферу мозжечка, медикаментозный синдром Кушинга,
тромбоцитопения 3 ст.
Симптоматическая терапия
26.
27.
Клинический случайПациент, 44 года
28. Клинический случай Пациент, 44 года
Диагноз: рак ротоглоткиT3N2bM0; IVА ст.
Гистология: плоскоклеточный
неороговевающий рак
Назначено: 3 курса неоадъювантной
ПХТ по схеме TPF (Доцетаксел +
цисплатин + 5-фторурацил)
Курс лучевой терапии по
радикальной программе на
ротоглотку СОД 70Гр на фоне
еженедельного введения
карбоплатина 150мг
Полный регресс опухоли.
Динамическое наблюдение
Данные ПЭТ/КТ: очаги в мягких тканях
носоглотки слева SUV5,25, размерами
около 2,2х1,2 см
Гистология: низкодифференцированный
плоскоклеточный рак носоглоточного
типа
Диагноз: Рак носоглотки T1N0M0; I ст.
Назначено: цисплатин 180 мг + курс
лучевой терапии по радикальной
программе на область носоглотки СОД
66ГР.
Полный регресс опухоли.
Динамическое наблюдение.
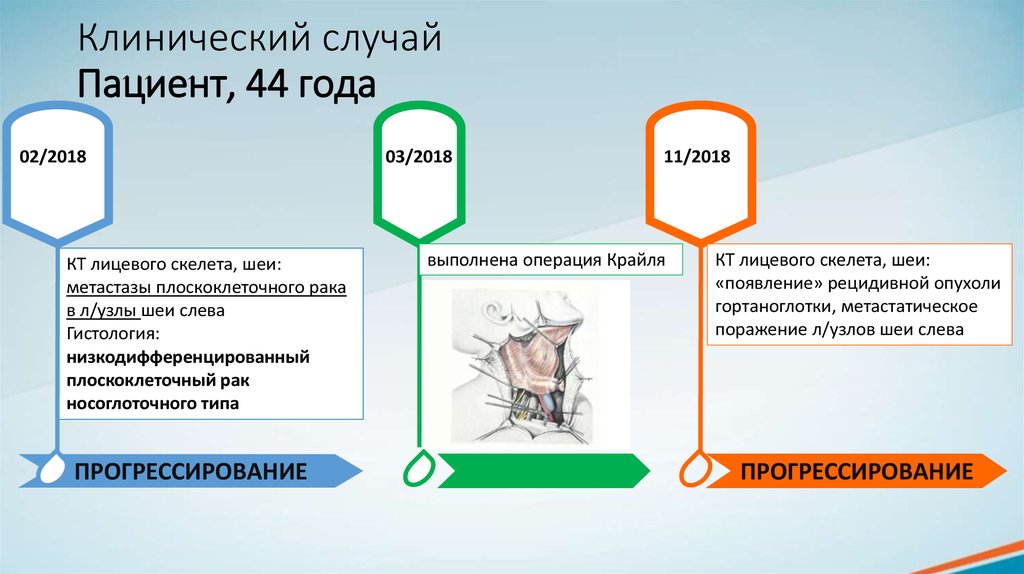
29. Клинический случай Пациент, 44 года
02/2018КТ лицевого скелета, шеи:
метастазы плоскоклеточного рака
в л/узлы шеи слева
Гистология:
низкодифференцированный
плоскоклеточный рак
носоглоточного типа
ПРОГРЕССИРОВАНИЕ
03/2018
11/2018
выполнена операция Крайля
КТ лицевого скелета, шеи:
«появление» рецидивной опухоли
гортаноглотки, метастатическое
поражение л/узлов шеи слева
ПРОГРЕССИРОВАНИЕ
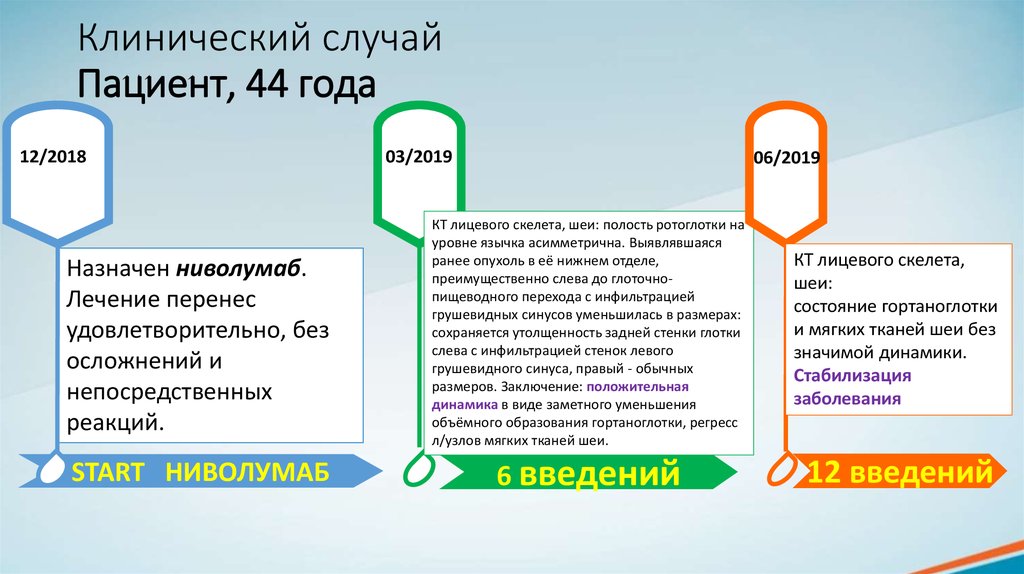
30. Клинический случай Пациент, 44 года
12/2018Назначен ниволумаб.
Лечение перенес
удовлетворительно, без
осложнений и
непосредственных
реакций.
START НИВОЛУМАБ
03/2019
06/2019
КТ лицевого скелета, шеи: полость ротоглотки на
уровне язычка асимметрична. Выявлявшаяся
ранее опухоль в её нижнем отделе,
преимущественно слева до глоточнопищеводного перехода с инфильтрацией
грушевидных синусов уменьшилась в размерах:
сохраняется утолщенность задней стенки глотки
слева с инфильтрацией стенок левого
грушевидного синуса, правый - обычных
размеров. Заключение: положительная
динамика в виде заметного уменьшения
объёмного образования гортаноглотки, регресс
л/узлов мягких тканей шеи.
КТ лицевого скелета,
шеи:
состояние гортаноглотки
и мягких тканей шеи без
значимой динамики.
Стабилизация
заболевания
6 введений
12 введений
31. Клинический случай Пациент, 44 года
09/2019Лечение перенес удовлетворительно, без
осложнений и непосредственных реакций
КТ лицевого скелета, шеи:
! после 18 введений !
По сравнению с 11.03.19г. и 11.06.19г. –
полный регресс опухоли
гортаноглотки.
18 введений
















 medicine
medicine








