Similar presentations:
Теория горения и взрыва
1.
ФГБОУ ВО«ГОСУДАРСТВЕННЫЙ АГРАРНЫЙ УНИВЕРСИТЕТ СЕВЕРНОГО ЗАУРАЛЬЯ»
______________________________________
КАФЕДРА ТЕХНОСФЕРНОЙ БЕЗОПАСНОСТИ
Ст.преподаватель
Александрой В.И.
2018 год
2.
Дисциплина3.
Литература1. Теория горения и взрыва: практикум: учебное пособие / В.А. Девисилов,
Т.И. Дроздова, С.С. Тимофеева / под общ. ред. В.А. Девисилова. - М.:
ФОРУМ, 2012. - 352 с. - (Высшее образование).
2. Портола, В.А.. Расчет процессов горения и взрыва [Текст]: учеб. пособие
для вузов / В.А. Портола, Н.Ю. Луговцова, Е.С.Торосян. – Томск: Изд-во ТПУ,
2012. – 107 с.
3. Адамян, В.Л. Теория горения и взрыва [Электронный ресурс]: учебное
пособие / В.Л. Адамян. — Электрон. дан. — Санкт-Петербург : Лань, 2018.
— 116 с. — Режим доступа: https://e.lanbook.com/book/109508. — Загл. с
экрана.
4.
5.
6.
7.
1.2.
3.
Вопросы лекции
Горение . Условия для возникновения горения.
Горючее вещество. Группы горючих веществ или материалов
Полное и неполное горение.
8.
9.
10.
11.
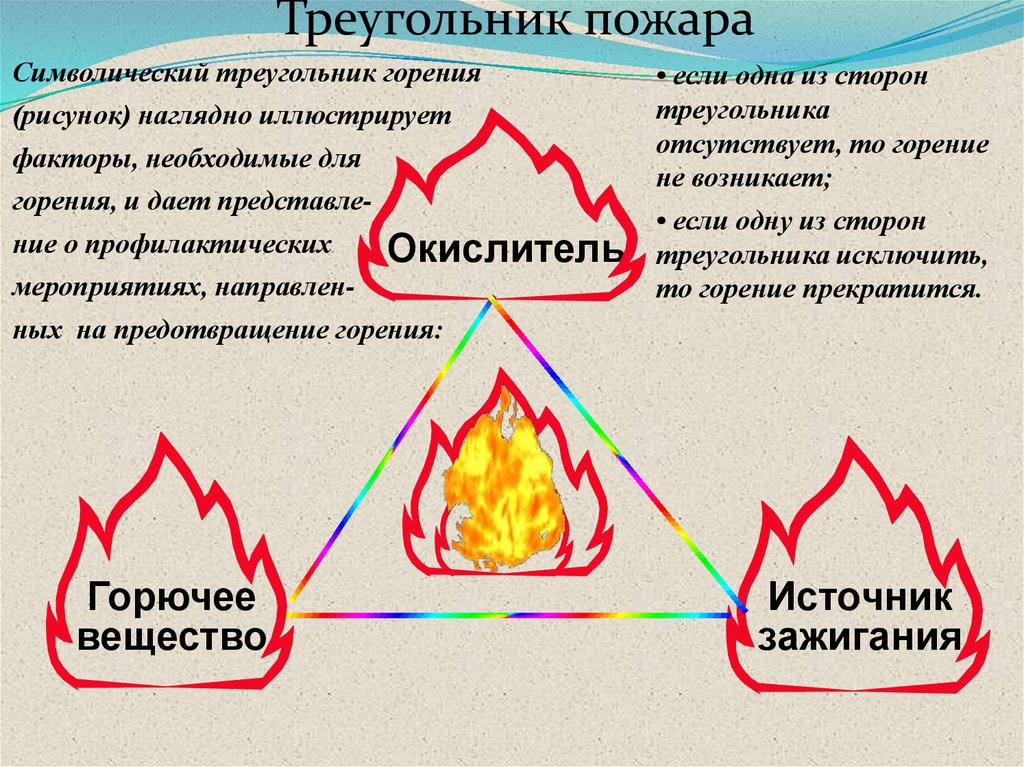
Треугольник пожараСимволический треугольник горения
(рисунок) наглядно иллюстрирует
факторы, необходимые для
горения, и дает представление о профилактических
Окислитель
мероприятиях, направленных на предотвращение горения:
Горючее
вещество
• если одна из сторон
треугольника
отсутствует, то горение
не возникает;
• если одну из сторон
треугольника исключить,
то горение прекратится.
Источник
зажигания
12.
13.
14.
Органические горючие вещества – это всевещества
на
основе
углерода,
представляющие
собой
материалы
растительного и животного происхождения,
или
же
ископаемые
вещества,
т.е.
добываемые
из
недр
земли.
Все
они
применяются как в натуральном виде, так и
после соответствующей
Неорганические
горючиеобработки.
вещества
и
материалы
представляют
собой
все
простые и сложные вещества неорганической
природы, способные к реакциям горения. По
современной химической классификации это
металлы
и
неметаллы,
их
различные
производные.
15.
К горючим металлам и их производнымотносятся все щелочные и щелочноземельные металлы, а также металлы
других групп периодической системы
Д.И. Менделеева и их производные -
карбиды, сульфиды и т.п.
К
горючим
неметаллам
и
их
производным относятся бор, кремний,
фосфор, мышьяк, сера, селен, теллур,
их карбиды, гидриды, сульфиды и т.д.
По агрегатному состоянию горючие
вещества и материалы подразделяются
на газообразные, жидкие и твердые.
16.
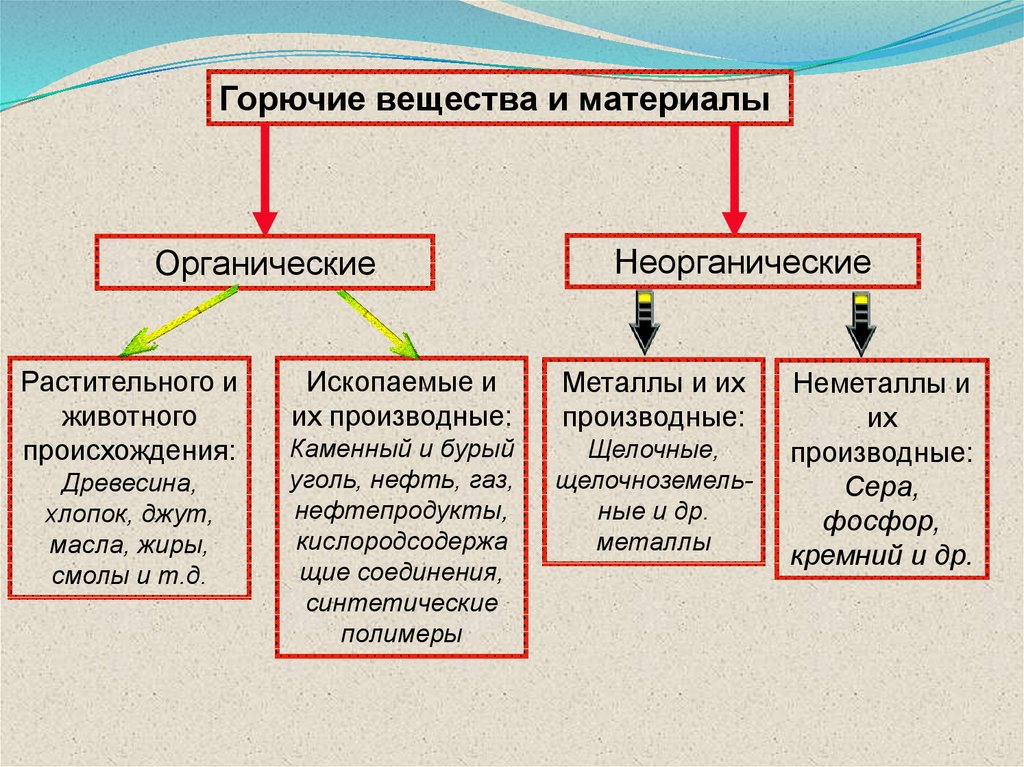
Горючие вещества и материалыОрганические
Растительного и
животного
происхождения:
Древесина,
хлопок, джут,
масла, жиры,
смолы и т.д.
Неорганические
Ископаемые и
их производные:
Металлы и их
производные:
Каменный и бурый
уголь, нефть, газ,
нефтепродукты,
кислородсодержа
щие соединения,
синтетические
полимеры
Щелочные,
щелочноземельные и др.
металлы
Неметаллы и
их
производные:
Сера,
фосфор,
кремний и др.
17.
18.
K = 4 × n(C) + 4 × n(S ) + n(H ) + n(N ) - 2 × n(O)- 2 × n(Cl) - 3 × n(F ) - 5 × n(Br)
где:
n(C), n(S), n(H), n(N), n(O), 2 n(Cl), n(F), n(Br) –
число атомов углерода, серы, водорода,
азота, кислорода, хлора, фтора и брома в
молекуле вещества.
Если
больше
коэффициент
единицы
является
горючести
(К 1),
горючим;
при
то
К
вещество
значении
К
18
меньше единицы (К < 1) – вещество
19.
Расчет коэффициента горючестиПример 1.
Рассчитать коэффициент горючести
С6Н5NH2 и хлорной кислоты HClO4.
анилина
Решение:
В молекуле анилина n(C) = 6; n(Н) = 7; n(N) = 1;
К = 4 × 6 + 7 + 1 = 32
К > 1, следовательно, анилин – горючее вещество.
В молекуле хлорной кислоты n(Н) = 1; n(Cl) = 1; n(О) = 4;
К=1–2×4–2×1=-9
К < 1, хлорная кислота – негорючее вещество.
20.
Пример 2. Определить горючесть этиламина(C2H5NH2).
Решение. Рассчитываем коэффициент горючести
этиламина:
n(C) = 2; n(H = 7; п(N) = 1;
Кг = 4 ⸱ 2 + 7 + 1 = 16; Кг > 1.
Ответ. Этиламин - горючее вещество.
Пример 2. Определить горючесть закиси азота
(N2О).
Решение. Рассчитываем коэффициент закиси
азота: п(О) = 1; п(N) = 2;
Кг = 2 -2 · 1 = О; Кг < 1.
Ответ. Закись азота - негорючее вещество.
21.
22.
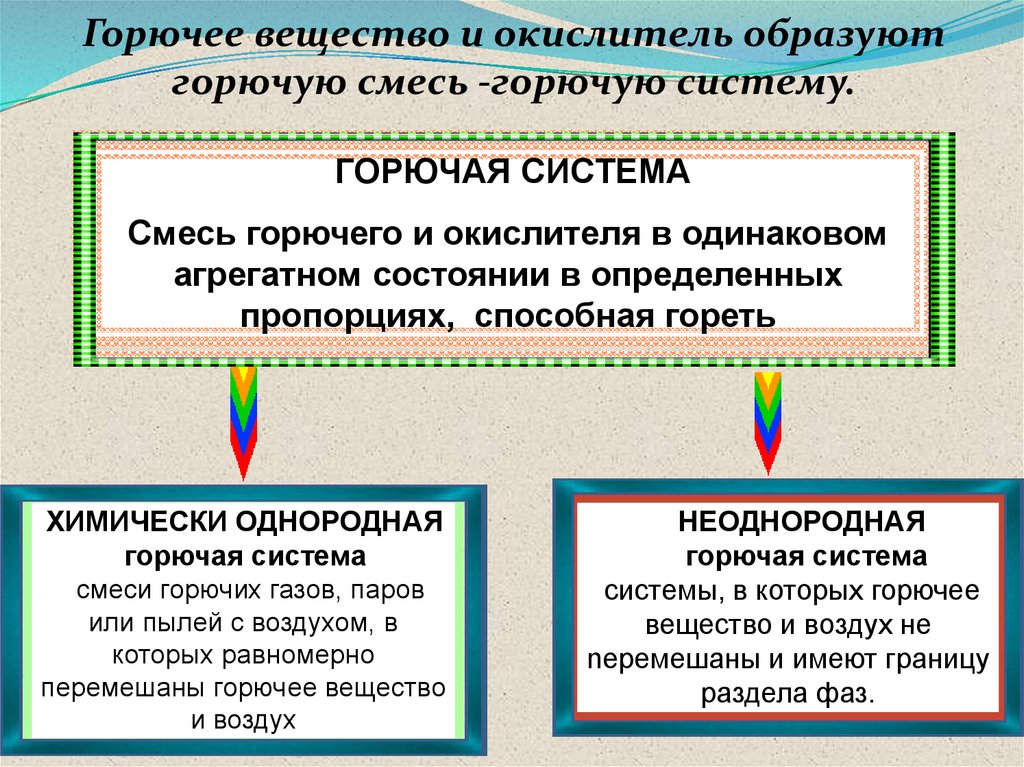
Горючее вещество и окислитель образуютгорючую смесь -горючую систему.
ГОРЮЧАЯ СИСТЕМА
Смесь горючего и окислителя в одинаковом
агрегатном состоянии в определенных
пропорциях, способная гореть
ХИМИЧЕСКИ ОДНОРОДНАЯ
горючая система
смеси горючих газов, паров
или пылей с воздухом, в
которых равномерно
перемешаны горючее вещество
и воздух
НЕОДНОРОДНАЯ
горючая система
системы, в которых горючее
вещество и воздух не
nеремешаны и имеют границу
раздела фаз.
23.
24.
Горючие вещества могут быть в трехагрегатных состояниях: жидком, твердом,
газообразном. Отдельные твердые вещества при
нагревании плавятся и испаряются, другие –
разлагаются и выделяют газообразные продукты
и твердый остаток в виде угля и шлака, третьи не
разлагаются и не плавятся.
Горение отличается многообразием видов и
особенностей,
обусловливаемых
процессами
теплообмена,
газодинамическими
эффектами,
кинетикой химических превращений, а также
обратной связью между внешними условиями и
характером развития горения.
25.
К внешним проявлениям горения относится пламя,которое характеризуется свечением и выделением
теплоты. При горении конденсированных систем
(систем, состоящих только из твердых или жидких фаз
или их смесей) пламя может и не возникнуть. Такое
горение называют беспламенным горением или тлением.
26.
27.
28.
29.
ОкислителиГалогены:
Хлор,
фтор,
бром,
йод.
Кислород и
кислород
воздуха
Соли
кислородсодержащих
кислот:
Нитраты,
хлораты
Окислители - это вещества, атомы которых в
химических превращениях принимают электроны. Среди
простых веществ к ним относятся все галогены и
30.
31.
32.
33.
34.
35.
P2O5Оксид фосфора
Na2O
K2O
36.
Л37.
38.
39.
40.
41.
42.
43.
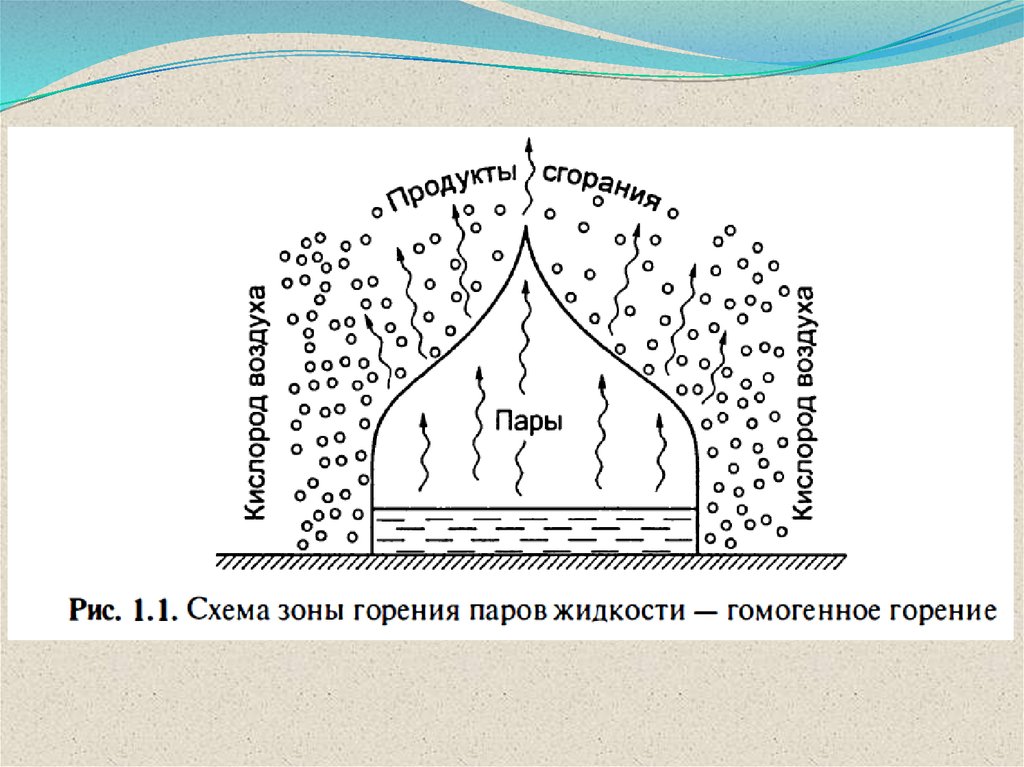
Виды и режимы горенияГОМОГЕННОЕ
горение
оба компонента находятся в
одной фазе (однородные
горючие смеси)
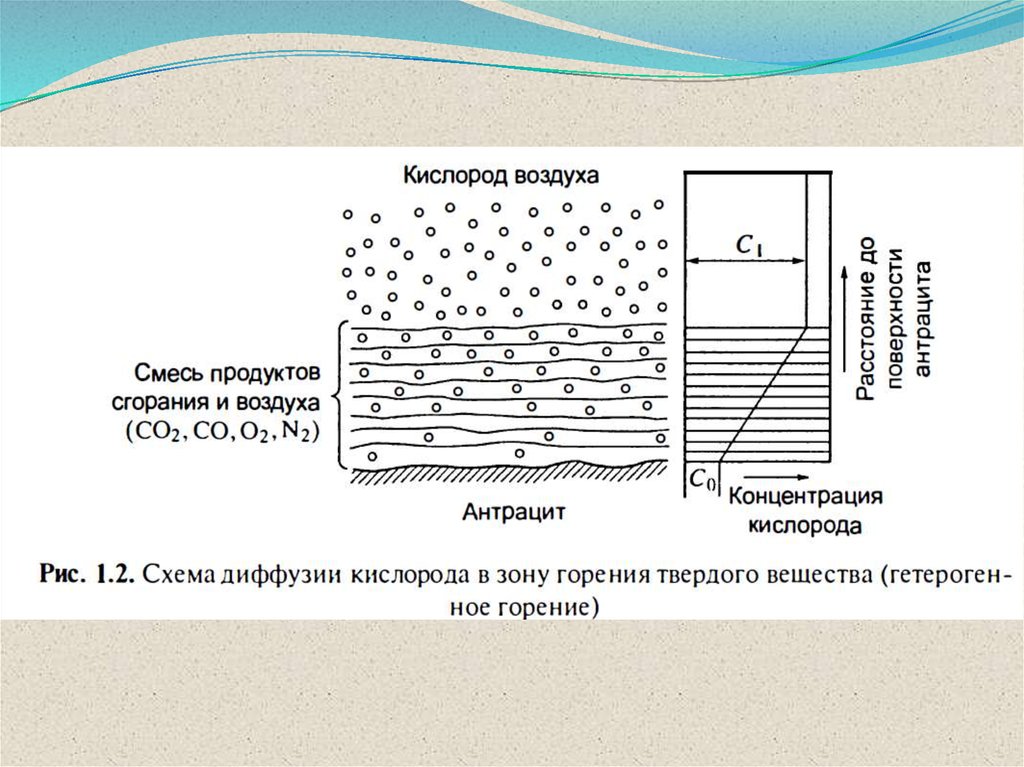
ГЕТЕРОГЕННОЕ
горение
агрегатное
состояние
у
компонентов горючей системы
различное
(неоднородные
горючие
смеси).Пример
–
тление ТГМ.
44.
ГОМОГЕННОЕ ГОРЕНИЕКИНЕТИЧЕСКОЕ
горение
ДИФФУЗИОННОЕ
горение
это горение предварительно
перемешанной горючей смеси,
т.е. однородной смеси.
Скорость
горения
определяется только кинетикой
окислительновосстановительной реакции.
это
горение
неоднородной
смеси,
когда
горючее
и
окислитель предварительно не
перемешаны.
В этом случае, смешивание
горючего
и
окислителя
происходит во фронте пламени
за счет диффузии.
Воздух
Воздух
Воздух
Воздух
Гор. газ
Гор. газ
45.
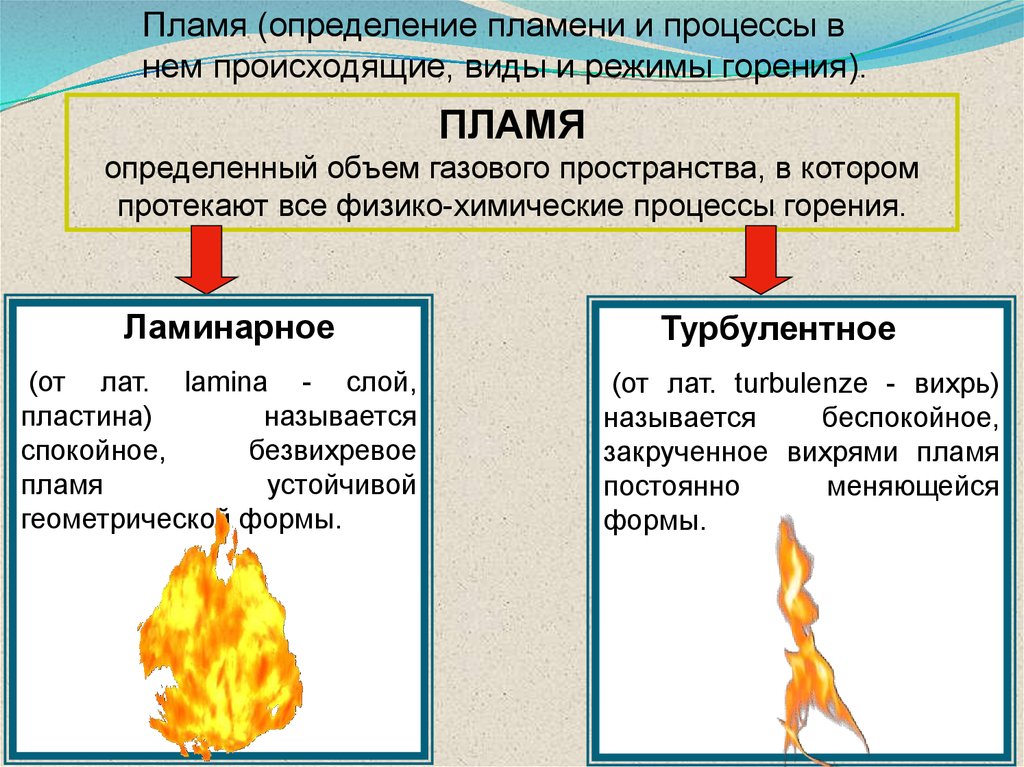
Пламя (определение пламени и процессы внем происходящие, виды и режимы горения).
ПЛАМЯ
определенный объем газового пространства, в котором
протекают все физико-химические процессы горения.
Ламинарное
(от лат. lamina - слой,
пластина)
называется
спокойное,
безвихревое
пламя
устойчивой
геометрической формы.
Турбулентное
(от лат. turbulenze - вихрь)
называется
беспокойное,
закрученное вихрями пламя
постоянно
меняющейся
формы.
46.
Структура пламениФРОНТ
ПЛАМЕНИ
(δпл.)
–
тонкий
поверхностный слой, ограничивающий пламя,
непосредственно в котором
протекают
окислительно-восстановительные реакции.
Зона максимальных
температур
δпл.≈0,5•10-3 см.
47.
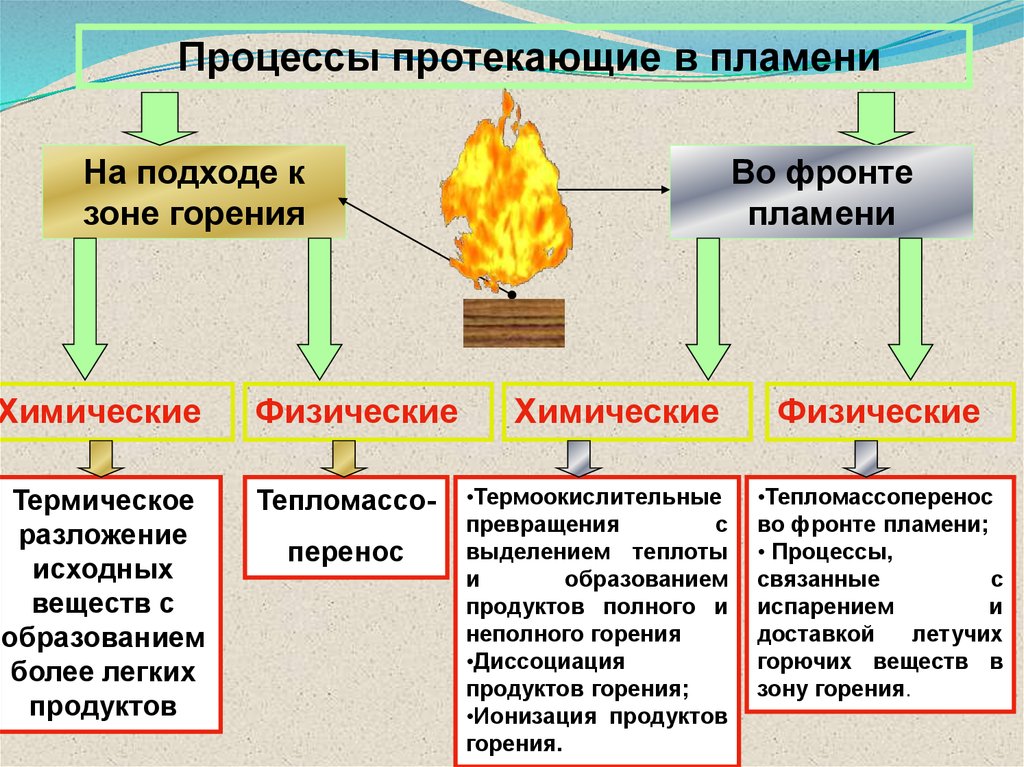
Процессы протекающие в пламениНа подходе к
зоне горения
Химические
Физические
Термическое
разложение
исходных
веществ с
образованием
более легких
продуктов
Тепломассоперенос
Во фронте
пламени
Химические
•Термоокислительные
превращения
с
выделением теплоты
и
образованием
продуктов полного и
неполного горения
•Диссоциация
продуктов горения;
•Ионизация продуктов
горения.
Физические
•Тепломассоперенос
во фронте пламени;
• Процессы,
связанные
с
испарением
и
доставкой
летучих
горючих веществ в
зону горения.
48.
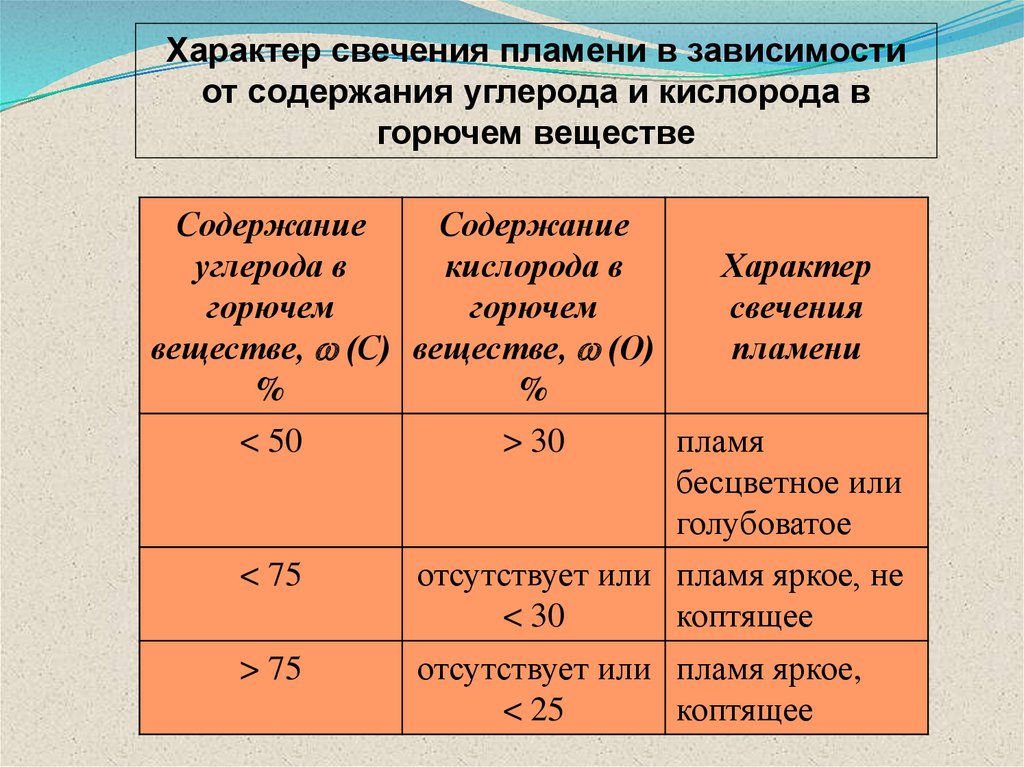
Характер свечения пламени в зависимостиот содержания углерода и кислорода в
горючем веществе
Содержание
Содержание
углерода в
кислорода в
горючем
горючем
веществе, (С) веществе, (О)
%
%
< 50
< 75
> 75
Характер
свечения
пламени
пламя
бесцветное или
голубоватое
отсутствует или пламя яркое, не
< 30
коптящее
> 30
отсутствует или пламя яркое,
< 25
коптящее
49.
Рассчитать коэффициент горючести следующихвеществ
50.
метионин С5Н11NO2S, азотная кислота HNO3, глюкозаС6Н12O6, угольная кислота H2СO3, дихлорэтилен С2Н4Cl2,
лимонная кислота С6H8O7, дихлорметан СН2Cl2, уксусная
кислота С2H4O2, глутамин С5Н10N2O3, хлорметан СH3Cl,
аспартам С14Н18N2O5, фосген СОCl2, хинин С20Н24O2N2,
серная кислота Н2SO4, аспарагин С4Н8N2O3, хлорметан
СН3Cl, нитробензол С6Н5NO2, сероуглерод СS2, метан
СН4, мочевина NН2СОNН2, диоксид хлора СlO2, винная
кислота Н2С4Н4О6, сернистая кислота H2SO3, формамид
НСОNН2, хлористая кислота HClO2, глицин С2Н5NО2,
циклогексан С6H12, бутиловый спирт С4Н9ОН, ацетилен
С2H2, диэтиловый эфир С4Н10О ,толуол С7H8, фенол
С6Н5ОН, кетен СH2СО,
нитрат аммония NH4NO3,
антрацен С14H10, стеариновая кислота С18Н36О2, этилен
С2H4, диметилсульфид СН3SCH3, бензол С6H6









































 life safety
life safety








