Similar presentations:
Химическая связь
1. Химическая связь
2. Вещества молекулярного и немолекулярного строения
3. Виды химической связи
Ковалентная• неполярная
• полярная
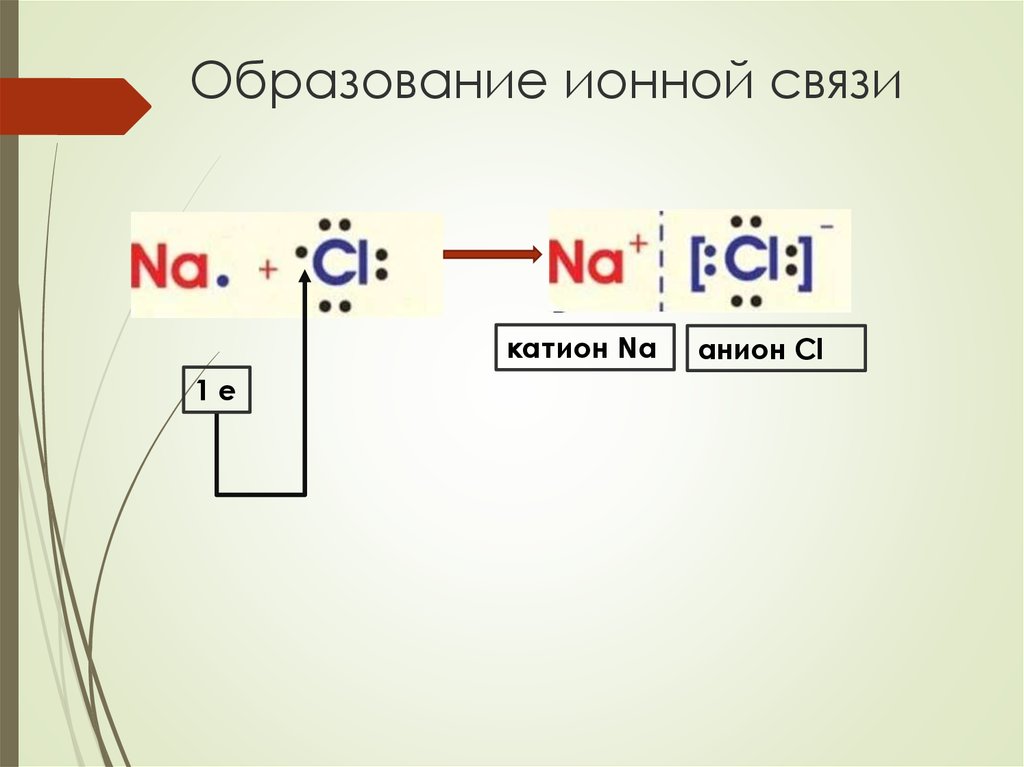
Ионная
Металлическая
Межмолекулярная
• водородная
• ван-дер-ваальсова
4. Химическая связь
1) имеет электромагнитнуюприроду
2) в результате образования
связи происходит понижение
энергии системы
5. 1. Ковалентная связь
Наиболее прочный тип химической связиЕсв до 800 кДж/моль
6.
Ковалентная связьвозникает:
̶ между атомами неМе
̶ за счет перекрывания атомных
электорнных орбиталей
7. Ковалентная связь при этом образуются: ̶ общая для двух атомов электронная пара, ̶ молекулярная орбиталь.
8. Электроотрицательность (ЭО)
это способность атомов,принимающих участие в образовании
ковалентной связи, притягивать к себе
общую электронную пару
количественно описывает
неметаллические свойства атома
значение ЭО можно рассчитать
9. Электроотрицательность (ЭО)
чем больше разница в значениях ЭОсвязанных атомов, тем больше
полярность ковалентной связи
10. Фрагмент ряда относительной ЭО элементов
BaNa
Mn
Al
Cu
Si
H
0,89 0,93 1,55 1,61 1,90 1,90 2,1
P
2,2
C
S
Br
Cl
O
2,55 2,58 2,96 3,16 3,44
F
max
ЭО
11. 1а. Ковалентная неполярная связь
12. Ковалентная неполярная связь
образуется между одинаковыми атомами неМеобщая е-пара:
расположена симметрично относительно
центров атомов
в равной мере принадлежит обоим атомам, т.к.
их ЭО одинакова (примеры: простые вещества
H2, O2, О3 …)
13. Схема образования молекул водорода и хлора с использованием формул Льюиса: точками обозначаются электроны внешнего уровня
графическая формула молекулы водорода Н – Нграфическая формула молекулы хлора
Cl – Cl
14. 1б. Ковалентная полярная связь
15. Ковалентная полярная связь
образуется между атомами неМе сразличной ЭО
общая е-пара:
сдвинута в сторону атома с большим
значением ЭО (более сильного неметалла)
примеры: HCl, H2O, SO2, PCl5





















 chemistry
chemistry








