Similar presentations:
Термодинамика химических процессов
1. Тема: ТЕРМОДИНАМИКА ХИМИЧЕСКИХ ПРОЦЕССОВ
2. План
Энергетика химических и фазовых превращений1.1 Основные понятия термодинамики: система, энергия
(внутренняя, тепловая, механическая), параметры
состояния системы, компоненты системы, фаза, процесс.
Первый закон (начало) термодинамики.
1.2 Тепловые эффекты реакций и термохимические
уравнения. Закон Гесса. Понятие энтальпии. Теплота
(энтальпия) образования вещества.
1.3 Энтропия и второе начало (закон) термодинамики
1.4 Энергия Гиббса (изобарно-изотермический потенциал).
Критерии самопроизвольного протекания процессов.
Вычисления по термохимическим уравнениям
3.
ТЕРМОДИНАМИКА ХИМИЧЕСКИХ ПРОЦЕССОВОсновные понятия:
Химическая термодинамика – раздел химии,
изучающий энергетику химических и фазовых
превращений,
направление
и
протекание
процессов
в
физико-химических
системах,
химические и фазовые равновесия
Термодинамика (дословно – наука об изменении
тепла) базируется не на постулатах, а на
экспериментально подтвержденных объективных
закономерностях, сформулированных в основных
началах (или законах)
4.
ТЕРМОДИНАМИКА ХИМИЧЕСКИХ ПРОЦЕССОВОсновные понятия:
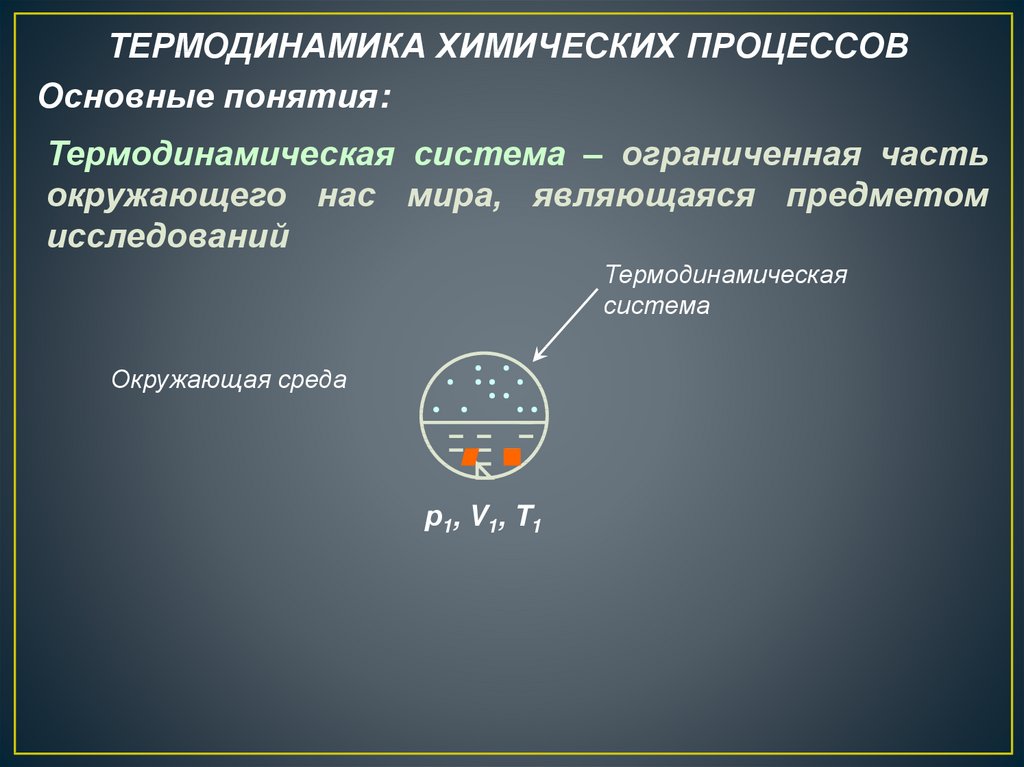
Термодинамическая система – ограниченная часть
окружающего нас мира, являющаяся предметом
исследований
Термодинамическая
система
Окружающая среда
р1, V1, T1
5.
ТЕРМОДИНАМИКА ХИМИЧЕСКИХ ПРОЦЕССОВОсновные понятия:
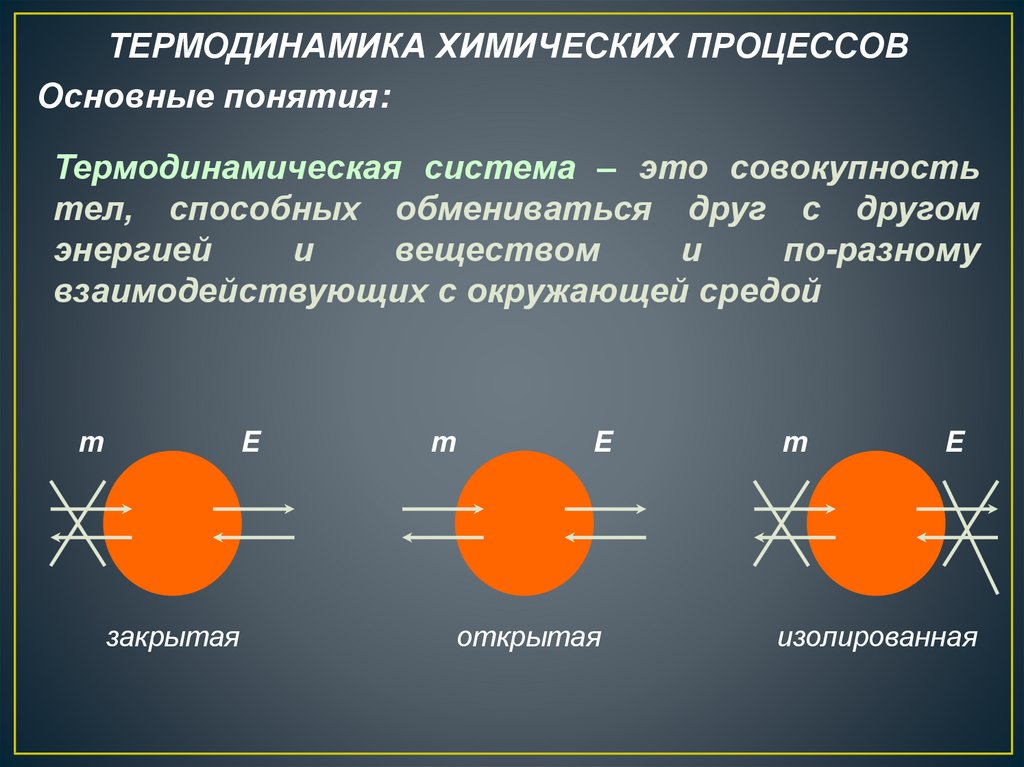
Термодинамическая система – это совокупность
тел, способных обмениваться друг с другом
энергией
и
веществом
и
по-разному
взаимодействующих с окружающей средой
m
E
закрытая
m
E
открытая
m
E
изолированная
6.
ТЕРМОДИНАМИКА ХИМИЧЕСКИХ ПРОЦЕССОВОсновные понятия:
Термодинамические параметры – это величины,
характеризующие термодинамическую систему
Интенсивные параметры (их величина не зависит
от количества вещества):
- температура (T);
- давление (р);
- молярная концентрация (См).
Экстенсивные параметры (их величина зависит от
количества вещества):
- масса (m);
- объем (V).
7.
ТЕРМОДИНАМИКА ХИМИЧЕСКИХ ПРОЦЕССОВОсновные понятия:
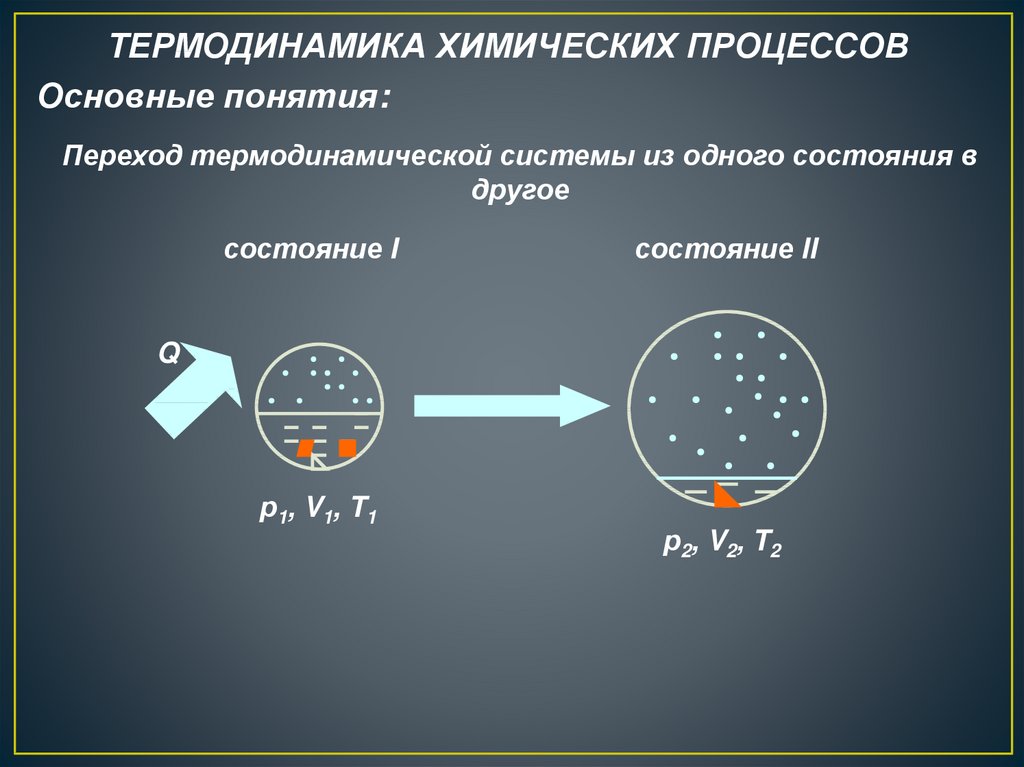
Переход термодинамической системы из одного состояния в
другое
состояние I
состояние II
Q
р1, V1, T1
р2, V2, T2
8.
ТЕРМОДИНАМИКА ХИМИЧЕСКИХ ПРОЦЕССОВОсновные понятия:
Внутренняя энергия системы (U) определяется
суммарным запасом энергии составляющих систему
молекул, атомов, электронов, ядер и т.д. и
складывается, в основном, из кинетической энергии
этих частиц и энергии взаимодействия между ними
U = U2 – U1
Внутренняя энергия изолированной системы ( Q = 0; A = 0;
U = 0) есть величина постоянная
9.
ПЕРВЫЙ ЗАКОН ТЕРМОДИНАМИКИA = p V
Q = U + A + W + E
– совершаемая системой работа
– подведенная к системе теплота
Первый закон термодинамики:
теплота Q, сообщаемая системе извне, расходуется
на увеличение внутренней энергии закрытой
системы U и на совершаемую системой работу A:
Q = U + A
* Первый закон термодинамики вытекает
сохранения энергии М.В. Ломоносова.
из
закона
10.
ТЕРМОДИНАМИКА ХИМИЧЕСКИХ ПРОЦЕССОВОсновные понятия:
Энтальпия, Н – функция состояния, равная
сумме U + pV:
H U + pV
Для изобарного процесса:
H = U + p V
При р = const и при отсутствии других видов
работ, кроме работы расширения, теплота равна
изменению энтальпии с противоположным знаком:
Qр = U + p V = - H
Для изохорного процесса (V = const ) и в отсутствии
других видов работ:
QV = U
11.
ТЕРМОДИНАМИКА ХИМИЧЕСКИХ РЕАКЦИЙОсновные понятия:
Тепловые эффекты и термохимические уравнения
реакций
Раздел химической термодинамики, в котором
изучают теплоты (±Q) химических реакций и их
зависимость от различных физико-химических
параметров, называется термохимией
Термохимическое уравнение реакции – уравнение
реакции, в котором наряду с ее участниками
указывается тепловой эффект реакции как один из
продуктов взаимодействия
В термохимическом уравнении реакции обязательно
указывается агрегатное состояние вещества
12.
ТЕПЛОВЫЕ ЭФФЕКТЫ РЕАКЦИЙИ ТЕРМОХИМИЧЕСКИЕ УРАВНЕНИЯ
Пример: Реакция образования воды из простых
веществ
выражается
термохимическим
уравнением:
H2 (г) + ½ O2 (г) = H2O (г) + 242 кДж
При экзотермическом процессе Qр-ции > 0, Нр-ции < 0.
При эндотермическом процессе Qр-ции < 0, Нр-ции > 0.
13.
ЗАКОН ГЕССА– установлен экспериментально в 1840 г. русским химиком Г.
И. Гессом
Изменение энтальпии Нр-ции (изменение теплового
эффекта Qр-ции) химической реакции не зависит от
промежуточных стадий реакции (пути протекания
процесса), а определяется только состоянием
исходных веществ и продуктов реакции
14.
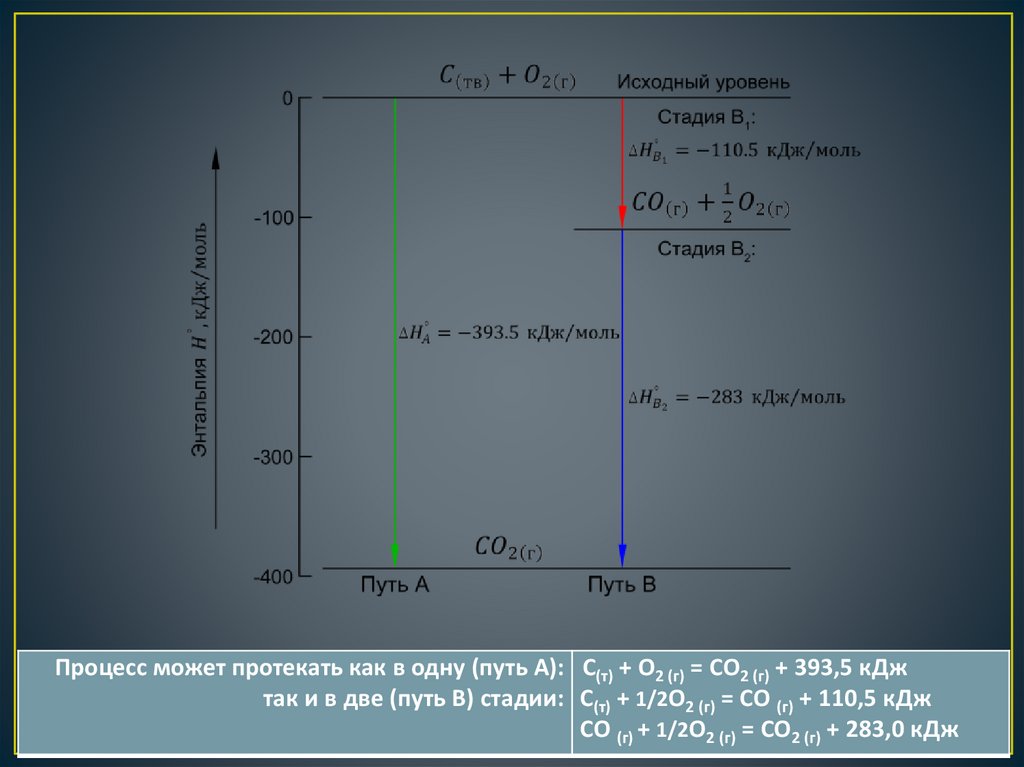
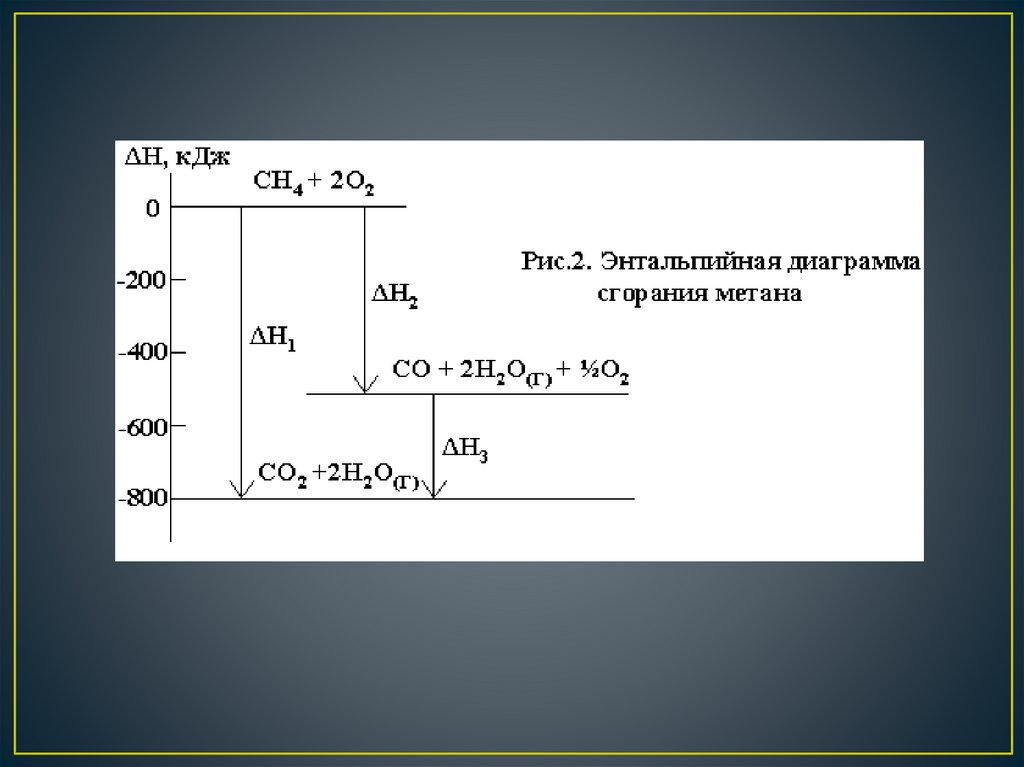
Процесс может протекать как в одну (путь А): С(т) + О2 (г) = СО2 (г) + 393,5 кДжтак и в две (путь В) стадии: С(т) + 1/2О2 (г) = СО (г) + 110,5 кДж
СО (г) + 1/2О2 (г) = СО2 (г) + 283,0 кДж
15.
16.
ЗАКОН ГЕССАПример: Определить изменение энтальпии Hх в реакции
взаимодействия газообразного аммиака с раствором
хлороводородной кислоты с образованием хлорида аммония:
NH3 (г) + HCl (р) = NH4Cl (р);
Hх
(ӿ)
если известны величины Hi следующих реакций:
1) образование твердого хлорида аммония из газообразного аммиака и
хлороводорода ( H1):
NH3 (г) + HCl (г) = NH4Cl (тв) ,
H1
(1)
2) образование раствора хлорида аммония (aq – означает растворение
в воде с образованием бесконечно разбавленного раствора) ( H2):
NH4Cl (тв) + aq = NH4Cl (р),
H2
(2)
3) образование раствора хлороводородной кислоты ( H3):
HCl (г) + aq = HCl (р)
H3
(3)
Комбинируя реакции 1, 2 и 3, получаем интересующую нас реакцию (ӿ),
для которой:
Hх = H1 + H2 + H3
17.
ЗАКОН ГЕССА,следствие, математическое выражение:
ΔНºр-ции = Σ ni ∙ΔНºf (прод.) – Σ nj ∙ΔНºf (исх. в-в),
где ni и nj – стехиометрические коэффициенты в уравнении
реакции; i – для продуктов реакции; j – для исходных веществ;
ΔНºf – стандартная энтальпия образования вещества, кДж/моль
Стандартная энтальпия образования вещества (ΔНºf, кДж/моль)
– изменение энтальпии в реакции образования 1 моль вещества
из простых веществ в стандартных условиях (при температуре
25 С (298,15 К) и давлении 1 атм = 760 мм рт. ст. = 101,3 кПа)
Пример: для реакции
Al2O3 (тв) + 3SO3 (г) = Al2(SO4)3 (тв)
ΔНºр-ции = ΔНºf [Al2(SO4)3 (тв)] – {ΔНºf [Al2O3 (тв)] + 3ΔНºf [SO3 (г)]}
= -3444,1 кДж – {-1676,8 кДж + 3(-376,2 кДж)} = -638,7 кДж
Al2O3 (тв) + 3SO3 (г) = Al2(SO4)3 (тв) + 638,7 кДж
18.
ТЕРМОДИНАМИКА ХИМИЧЕСКИХ РЕАКЦИЙОсновные понятия:
Энтропия (S) – функция состояния системы, такая
же фундаментальная и универсальная, как энергия
В классической термодинамике под энтропией понимают такое
свойство системы, изменение которого при обратимом
процессе численно равно отношению теплоты к температуре
протекания процесса:
dS = dQ/Т
S k ln qU ,V
где qU,V – термодинамическая вероятность данного состояния
системы при определенном запасе внутренней энергии U и объеме V;
k – постоянная Больцмана, равная 1,38 10-23 Дж/К.
19.
ВТОРОЕ НАЧАЛО (ЗАКОН) ТЕРМОДИНАМИКИР. Клаузиус, 1850 г.; У. Томпсон (лорд Кельвин), 1851 г.
• Предпосылки: исследования французского военного
инженера С. Карно (1824 г.) принципов действия
тепловых двигателей с целью повышения их
коэффициента полезного действия (КПД).
• Формулировки второго начала термодинамики:
1. Невозможен самопроизвольный переход тепла от тела
менее нагретого к телу более нагретому (Р. Клаузиус).
2. Невозможно превратить теплоту в работу, не
производя никакого другого действия, кроме охлаждения
источника тепла (У. Томпсон, М. Планк).
3. Вечный двигатель второго рода невозможен
(В. Оствальд).
20.
ВТОРОЕ НАЧАЛО (ЗАКОН) ТЕРМОДИНАМИКИВ изолированных системах самопроизвольно идут те
процессы, при которых происходит увеличение энтропии
( Sизолир > 0)
– Все системы самопроизвольно стремятся
достигнуть состояния с наибольшей
разупорядоченностью (с бóльшим беспорядком).
Энтропия (S) – мера неупорядоченности в системе,
или вероятности ее состояния.
При протекании необратимых процессов энтропия
увеличивается и стремится к максимальному
значению: ΔS > 0.
* Энтропия идеального кристалла индивидуального
вещества при температуре абсолютного нуля (0 К) равна
нулю
21.
ИЗМЕНЕНИЕ ЭНТРОПИИ, ΔSS i S j S
0
0
i
0
j
Энтропия всегда увеличивается (ΔS > 0) в процессах:
при переходе из конденсированного состояния
(твердого) в жидкое, из жидкого в газообразное;
при растворении твердого или жидкого вещества;
при диссоциации электролита; чем больше степень
диссоциации, тем заметней увеличивается энтропия;
в химических реакциях, идущих с образованием
газообразных веществ.
* Чем сложнее состав вещества, тем больше его
энтропия S°.
22.
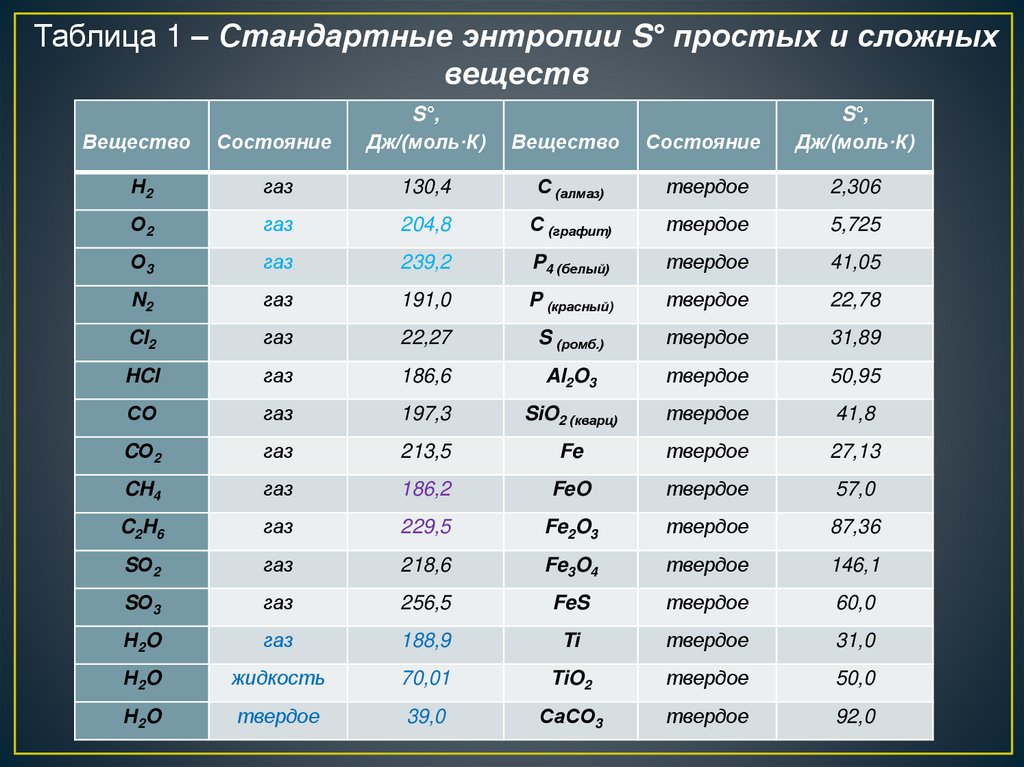
Таблица 1 – Стандартные энтропии S° простых и сложныхвеществ
Вещество
Состояние
S°,
Дж/(моль·К)
Вещество
Состояние
S°,
Дж/(моль·К)
Н2
газ
130,4
С (алмаз)
твердое
2,306
О2
газ
204,8
С (графит)
твердое
5,725
О3
газ
239,2
P4 (белый)
твердое
41,05
N2
газ
191,0
P (красный)
твердое
22,78
Cl2
газ
22,27
S (ромб.)
твердое
31,89
HCl
газ
186,6
Al2O3
твердое
50,95
СО
газ
197,3
SiO2 (кварц)
твердое
41,8
CО2
газ
213,5
Fe
твердое
27,13
CH4
газ
186,2
FeO
твердое
57,0
C2H6
газ
229,5
Fe2O3
твердое
87,36
SО2
газ
218,6
Fe3O4
твердое
146,1
SО3
газ
256,5
FeS
твердое
60,0
Н2O
газ
188,9
Ti
твердое
31,0
Н2O
жидкость
70,01
TiO2
твердое
50,0
Н2O
твердое
39,0
СаСО3
твердое
92,0
23.
ТЕРМОДИНАМИКА ХИМИЧЕСКИХ РЕАКЦИЙОсновные понятия:
Энергия
Гиббса
(G)
(изобарно-изотермический
потенциал, свободная энергия, Дж, кДж, кДж/моль) –
функция состояния термодинамической системы,
если давление и температура – независимые
параметры (р = const, Т = const):
G = H – TS.
Изменение энергии Гиббса:
ΔG0 = ΔH0 – TΔS0
ΔG – критерий самопроизвольного протекания
процессов.
Для самопроизвольно протекающих процессов:
ΔG0 < 0
G0 = ( H0 – T S0) < 0
24.
Таблица 2 – Критерии возможности самопроизвольногопротекания процессов
Ограничения,
накладываемые на
систему
Функция состояния
Изолированная
система
Неизолированная
система,
T, p = const
S
G
Определение
изменения функции
состояния
Критерий
самопроизвольного
протекания
процесса
Условие равновесия
G = H – T S
S
Qобр
T
S > 0
G < 0
S = 0; максимум S G = 0, минимум G
25.
ИЗМЕНЕНИЕ ЭНЕРГИИ ГИББСА0
0
0
G298
i G298
j G298
i
0
G298
Стандартные значения
справочных таблицах.
ΔНºf
j
0
H 298
ΔНºf,
0
298 S 298
Sº,
ΔGºf
приведены
в
и ΔGºf – характеристики термодинамической
стабильности веществ: чем более отрицательное значение
они имеют, тем устойчивее вещество, то есть тем легче
оно образуется из исходных простых веществ и тем
труднее разлагается на исходные вещества.
26.
Таблица 3 – Возможность и условия протекания реакцийв зависимости от характера изменения энтальпии ΔНº ,
энтропии ΔSº, энергии Гиббса ΔGº
Изменение функции
1
ΔH0
ΔS0
ΔG0
–
+
–
Принципиальная возможность
и условия протекания реакции
Возможна при любой температуре
2
+
–
–
3
–
–
–+
Принципиально
не
возможна.
Возможна в обратном направлении
(для обратимых реакций).
Возможна при низких температурах
4
+
+
+–
Возможна при высоких температурах





















 chemistry
chemistry








