Similar presentations:
Рибофлавин, тиамин, кислота аскорбиновая, натрия хлорид. Состав лекарственной формы. Анализ в аптечных условиях
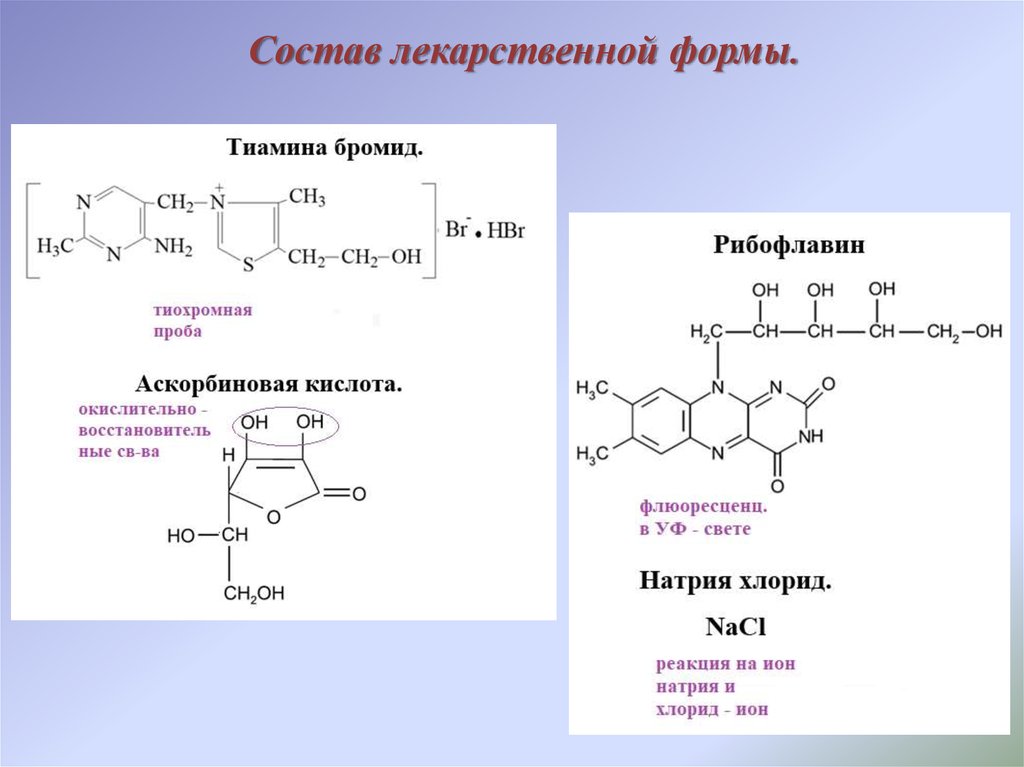
1. КУРСОВАЯ РАБОТА ЛФ состава: Рибофлавина Тиамина бромида по 0,002 Кислоты аскорбиновой 0,05 Натрия хлорида 0,08 Воды очищенной
до 10 млЦель работы заключается в изучении методик анализа
компонентов сложной ЛФ при совместном присутствии
Выполнила студентка АГМУ 053 группы
Кузнецова Юлия Владиславовна
2. Состав лекарственной формы.
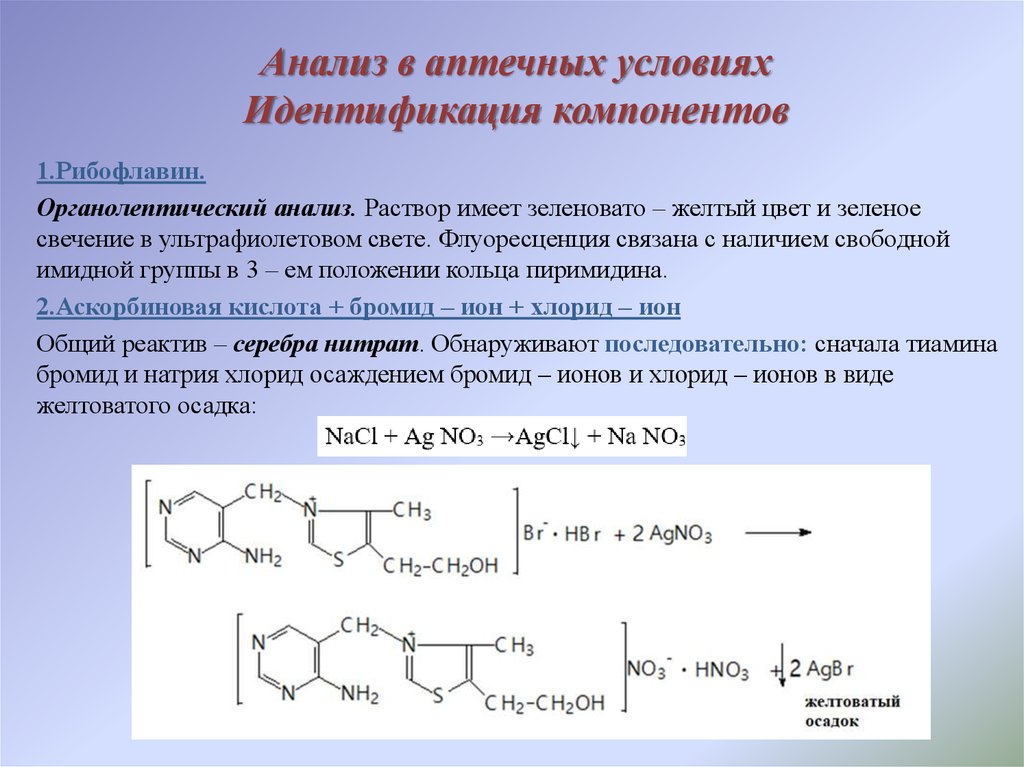
3. Анализ в аптечных условиях Идентификация компонентов
1.Рибофлавин.Органолептический анализ. Раствор имеет зеленовато – желтый цвет и зеленое
свечение в ультрафиолетовом свете. Флуоресценция связана с наличием свободной
имидной группы в 3 – ем положении кольца пиримидина.
2.Аскорбиновая кислота + бромид – ион + хлорид – ион
Общий реактив – серебра нитрат. Обнаруживают последовательно: сначала тиамина
бромид и натрия хлорид осаждением бромид – ионов и хлорид – ионов в виде
желтоватого осадка:
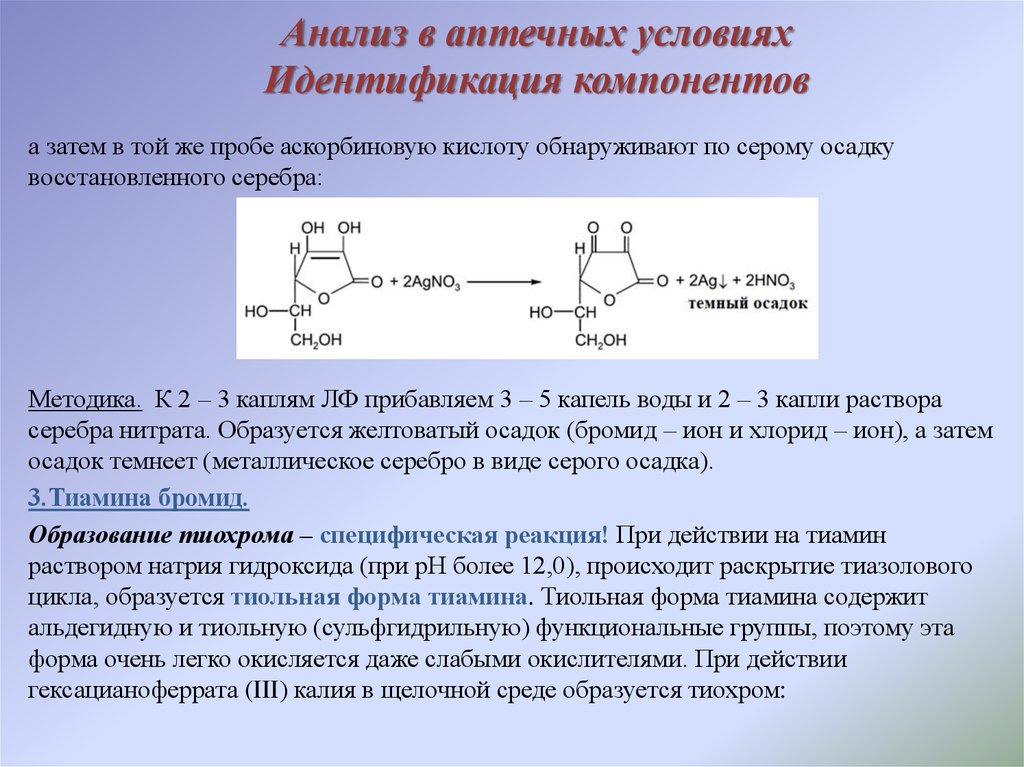
4. Анализ в аптечных условиях Идентификация компонентов
а затем в той же пробе аскорбиновую кислоту обнаруживают по серому осадкувосстановленного серебра:
Методика. К 2 – 3 каплям ЛФ прибавляем 3 – 5 капель воды и 2 – 3 капли раствора
серебра нитрата. Образуется желтоватый осадок (бромид – ион и хлорид – ион), а затем
осадок темнеет (металлическое серебро в виде серого осадка).
3.Тиамина бромид.
Образование тиохрома – специфическая реакция! При действии на тиамин
раствором натрия гидроксида (при рН более 12,0), происходит раскрытие тиазолового
цикла, образуется тиольная форма тиамина. Тиольная форма тиамина содержит
альдегидную и тиольную (сульфгидрильную) функциональные группы, поэтому эта
форма очень легко окисляется даже слабыми окислителями. При действии
гексацианоферрата (III) калия в щелочной среде образуется тиохром:
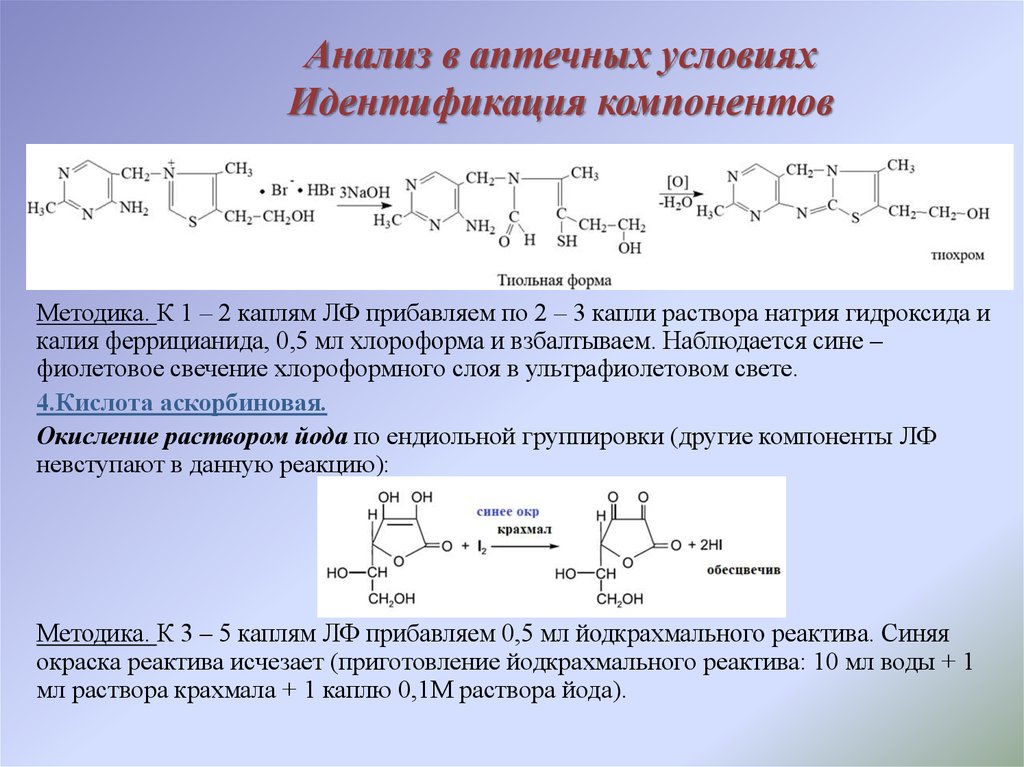
5. Анализ в аптечных условиях Идентификация компонентов
Методика. К 1 – 2 каплям ЛФ прибавляем по 2 – 3 капли раствора натрия гидроксида икалия феррицианида, 0,5 мл хлороформа и взбалтываем. Наблюдается сине –
фиолетовое свечение хлороформного слоя в ультрафиолетовом свете.
4.Кислота аскорбиновая.
Окисление раствором йода по ендиольной группировки (другие компоненты ЛФ
невступают в данную реакцию):
Методика. К 3 – 5 каплям ЛФ прибавляем 0,5 мл йодкрахмального реактива. Синяя
окраска реактива исчезает (приготовление йодкрахмального реактива: 10 мл воды + 1
мл раствора крахмала + 1 каплю 0,1М раствора йода).
6. Анализ в аптечных условиях Идентификация компонентов
Образования турнбулевой сини, основана на окислении кислоты аскорбиновой поендиольной группировки железа (III) хлоридом (другие компоненты смеси данной
реакции не дают):
Методика. К 5 каплям раствора прибавляем по 2 капли растворов ферроцианида калия и
железа (III) хлорида. Появляется синее окрашивание.
5.Ион натрия.
Окрашивание пламени. Часть раствора на графитовой палочке вносят в бесцветное
пламя. Пламя окрашивается в желтый цвет.
7. Анализ в аптечных условиях Количественное определение компонентов
Проводят без разделения компонентов.1.Рибофлавин. ФЭК – измерение оптического поглощения раствора в видимой области
спектра по собственной желтой окраски, т.е предварительные реакции окрашивания не
проводим!
Методика. К 0,5 мл ЛФ прибавляем 9,5 мл воды и измеряем оптическую плотность (А1)
полученного раствора при длине волны около 445 нм в кювете с толщиной слоя 10 мм.
Раствор сравнения: вода.
Параллельно измеряем оптическую плотность раствора (А2), содержащего 2,5 мл 0,004%
стандартного раствора рибофлавина (0,0001 г) и 7,5 мл воды.
Содержание рибофлавина (X) в граммах вычисляем по формуле стандартного
раствора:
Х = А1 • 0,0001 • 10
А2• 0,5
Где 0,5 – навеска, взятая на анализ, гр; 10 – объем ЛФ, мл
8. Анализ в аптечных условиях Количественное определение компонентов
2.Кислота аскорбиновая. Йодометрия. Аскорбиновая кислота окисляется поендиольной группировке стандартным раствором йода в нейтральной, слабокислой или
слабощелочной среде до кислоты дегидроаскорбиновой (индикатор — раствор
крахмала)
Методика. К 1 мл ЛФ прибавляем 1 мл воды и титруют 0,02 М раствором йода (А мл)
до буро – синего окрашивания (индикатор — крахмал).
Содержание кислоты аскорбиновой (X) в граммах вычисляем по формуле:
Хг = 0,00176 ∙ Амл ∙ K ∙ 10
1,0
10 – объем ЛФ по прописи, мл; 1,0 – объем ЛФ, взятый на анализ, мл; А – объем 0,02М
раствора йода, пошедшего на титрование, мл.
9. Анализ в аптечных условиях Количественное определение компонентов
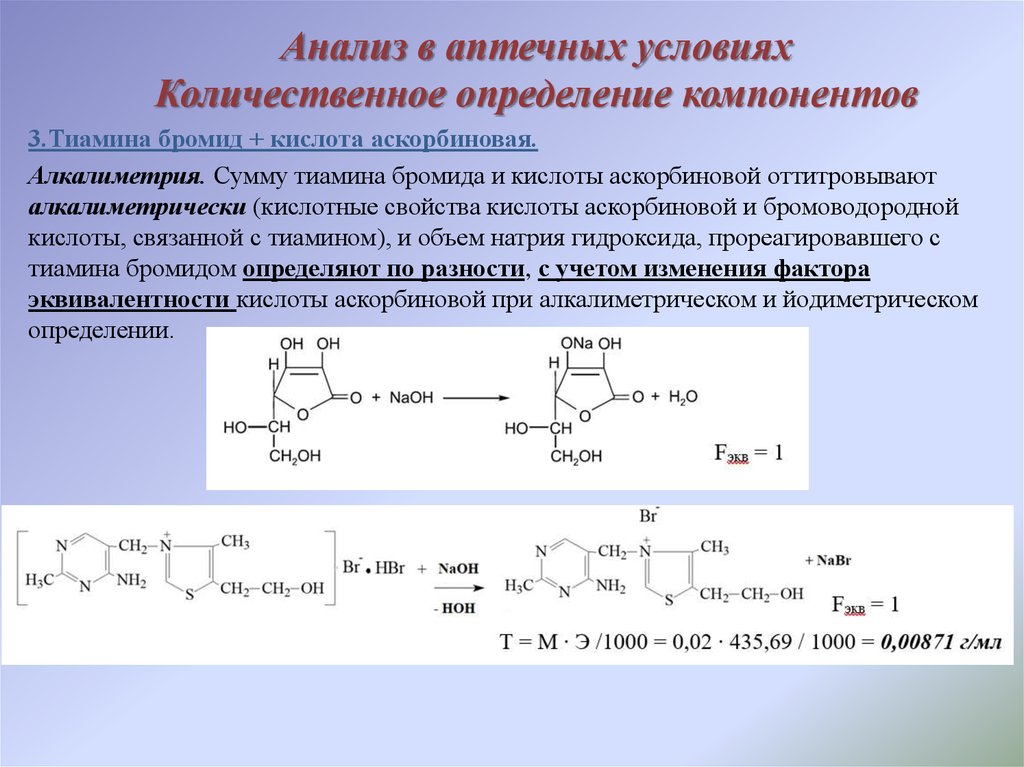
3.Тиамина бромид + кислота аскорбиновая.Алкалиметрия. Сумму тиамина бромида и кислоты аскорбиновой оттитровывают
алкалиметрически (кислотные свойства кислоты аскорбиновой и бромоводородной
кислоты, связанной с тиамином), и объем натрия гидроксида, прореагировавшего с
тиамина бромидом определяют по разности, с учетом изменения фактора
эквивалентности кислоты аскорбиновой при алкалиметрическом и йодиметрическом
определении.
10. Анализ в аптечных условиях Количественное определение компонентов
Методика. Титруем в 1 мл ЛФ сумму тиамина бромида и кислоты аскорбиновой 0,02М раствором натрия гидроксида (Б мл) до появления розового окрашивания
(индикатор – фенолфталеин).
Количество 0,02М раствора натрия гидроксида, израсходованного на титрование
тиамина бромида (Х мл) рассчитываем по разности:
Х = Б – А /2
где А/2 – учет изменения эквивалентов кислоты аскорбиновой при
алкалиметрическом титровании и йодометрическом.
Содержание тиамина бромида (X) в граммах вычисляем по формуле:
Хг = 0,00871 ∙ Хмл ∙ 10
1,0
10 – объем ЛФ по прописи, мл; 1,0 – объем ЛФ, взятый на анализ, мл; Х – объем
0,02М раствора натрия гидроксида, пошедшего на титрование только тиамина
бромида, мл.
11. Анализ в аптечных условиях Количественное определение компонентов
4.Натрия хлорид + тиамина бромид.Аргентометрия (видоизмененный метод Фольгарда). Метод заключается во введении
в анализируемый раствор 0,1 мл 0,1М раствора NH4SCN и железоаммониевых квасцов
для получения роданида железа, имеющего кроваво – красную окраску и последующим
прямым титрованием серебра нитратом.
После осаждения бромидов серебра нитрат будет взаимодействовать с роданидом
железа.
В точке эквивалентности красная окраска исчезает, но расход титранта будет завышен на
0,1 мл, то есть, на объем раствора аммония роданида, который был введен для
образования индикатора. Поэтому в расчетах из объема серебра нитрата,
израсходованного на титрование, вычитают 0,1 мл 0,1М раствора NH4SCN.
12. Анализ в аптечных условиях Количественное определение компонентов
Методика. К 1 мл ЛФ прибавляем по 1 мл разведенной кислоты азотной и железо –аммониевых квасцов, 0,1 мл 0,1М раствора роданида аммония и титруем сумму
галогенидов (хлорид – ион + бромид – ион) раствором серебра нитрата (В мл) до
исчезновения красной окраски.
Количество 0,1М раствора серебра нитрата, израсходованного на титрование только
натрия хлорида (Х1) рассчитываем по разности:
Х1 = В – 0,1 – Х / 5
где В – объем раствора серебра нитрата, пошедший на титрование суммы
галогенидов, мл; 0,1 – объем взятого на анализ 0,1М раствора роданида аммония, мл;
Х – количество 0,02М раствора натрия гидроксида, израсходованного на титрование
тиамина бромида, мл; 5 – учет разности молярности титрантов (0,1М / 0,02 М = 5
раз)
Содержание натрия хлорида (X) в граммах вычисляем по формуле:
Хг = 0,005844 ∙ Х1 ∙ 10
1,0
10 – объем ЛФ по прописи, мл; 1,0 – объем ЛФ, взятый на анализ, мл; Х1 – количество
0,1М раствора серебра нитрата, израсходованного на титрование только натрия
хлорида, мл
13. Анализ в лабораторных условиях
Метод ТСХ основан на способностижидкой фазы, продвигающейся по слою
сорбента (силикагель), перемещать
компоненты разделяемой смеси с
разными скоростями. Положение пятен
разделяемых витаминов на
хроматограмме характеризуют
значением Rf.
Ход опыта. В угол силуфоловой
пластинки на расстоянии 2 см от каждой
стороны наносят раствор ЛФ и
стандартные образцы (растворов
тиамина, аскорбиновой кислоты и
рибофлавина). Используют подвижную
фазу (бензол – этанол – уксусная кислота
– ацетон; 70:20:5:5), затем подсушивают и
выявляют пятна отдельных витаминов в
ультрафиолетовом свете, используя
значения Rf
14. Анализ в лабораторных условиях
Определение подлинности (идентификация)1.Раствор имеет зеленовато – желтый цвет и зеленое свечение в ультрафиолетовом
свете (рибофлавин)
2. К 1 – 2 каплям ЛФ прибавляем по 2 – 3 капли раствора натрия гидроксида и
калия феррицианида, 0,5 мл хлороформа и взбалтываем. Наблюдается сине –
фиолетовое свечение хлороформного слоя в ультрафиолетовом свете (тиамин)
3.К 3 – 5 каплям ЛФ прибавляем 0,5 мл йодкрахмального реактива. Синяя окраска
реактива исчезает (кислота аскорбиновая)
5.Часть раствора на графитовой палочке вносят в бесцветное пламя. Пламя
окрашивается в желтый цвет (ион натрия)
Подлинность и количественное содержание (ВЭЖХ).
Высокоэффективная жидкостная хроматография является удобным, быстрым
способом разделения, и проведения качественного и количественного анализа.
Исследуемый образец вводят в колонку хроматографа. Анализируя полученную
хроматограмму, идентифицируют вещества и рассчитывают их количество.
Идентификацию проводят по параметрам удерживания, сравнивая их с
параметрами удерживания стандартов. Определяют время от момента ввода пробы
до появления максимума пика на хроматограмме
15. Анализ в лабораторных условиях
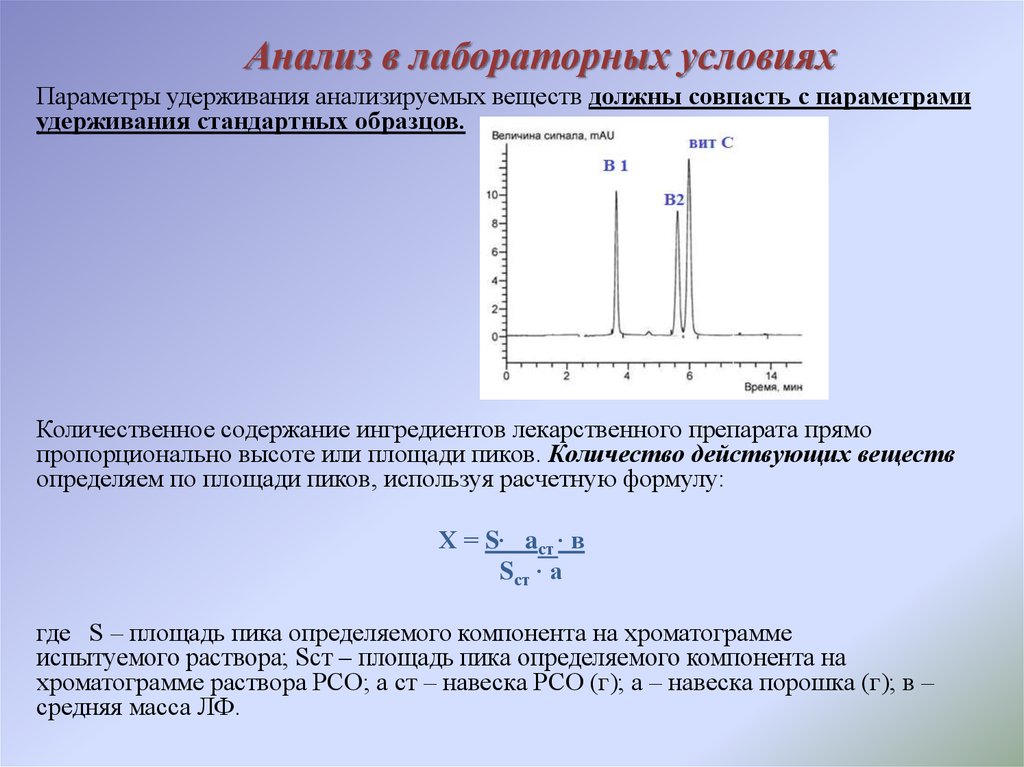
Параметры удерживания анализируемых веществ должны совпасть с параметрамиудерживания стандартных образцов.
Количественное содержание ингредиентов лекарственного препарата прямо
пропорционально высоте или площади пиков. Количество действующих веществ
определяем по площади пиков, используя расчетную формулу:
Х = S∙ aст ∙ в
Sст ∙ а
где S – площадь пика определяемого компонента на хроматограмме
испытуемого раствора; Sст – площадь пика определяемого компонента на
хроматограмме раствора РСО; a ст – навеска РСО (г); a – навеска порошка (г); в –
средняя масса ЛФ.









 medicine
medicine chemistry
chemistry








