Similar presentations:
Окислительно-восстановительные реакции. Подготовка к К/Р. 9 класс
1.
Урок 9 классаОкислительно-восстановительные
реакции.
Подготовка к К/Р
21.11.2016
1е занятие 2го триместра
2.
Подготовка к К/РНа следующем уроке у нас будет контрольная!
Она будет посвящена степеням окисления,
окислительно-восстановительным
реакциям
и
электронно-ионному
методу
расставления
коэффициентов.
У Вас будет 10 реакций, если правильно сделано:
10-8 – отлично;
7-6 – хорошо;
5-3 – трояк.
3.
Подготовка к К/РПоследовательность действий на к/р:
1) Проверяем является ли реакция окислительновосстановительной (ОВР).
Чем ОВР отличается от других реакций?
4.
Подготовка к К/РПоследовательность действий на к/р:
1) Проверяем является ли реакция окислительновосстановительной (ОВР).
Cl2 + O3 ClO3
NaBr + AgNO3 AgBr + NaNO3
5.
Подготовка к К/РПоследовательность действий на к/р:
1) Проверяем является ли реакция окислительновосстановительной (ОВР).
Cl2 + O3 ClO3
NaBr + AgNO3 AgBr + NaNO3
6.
Подготовка к К/РПоследовательность действий на к/р:
1) Проверяем является ли реакция окислительновосстановительной (ОВР).
2) Расставляем степени окисления над элементомокислителем и элементом-восстановителем.
7.
Подготовка к К/РПоследовательность действий на к/р:
1) Проверяем является ли реакция окислительновосстановительной (ОВР).
2) Расставляем степени окисления над элементомокислителем и элементом-восстановителем.
Cl2 + H2O(пар) + С(кокс) CO2 + HCl
8.
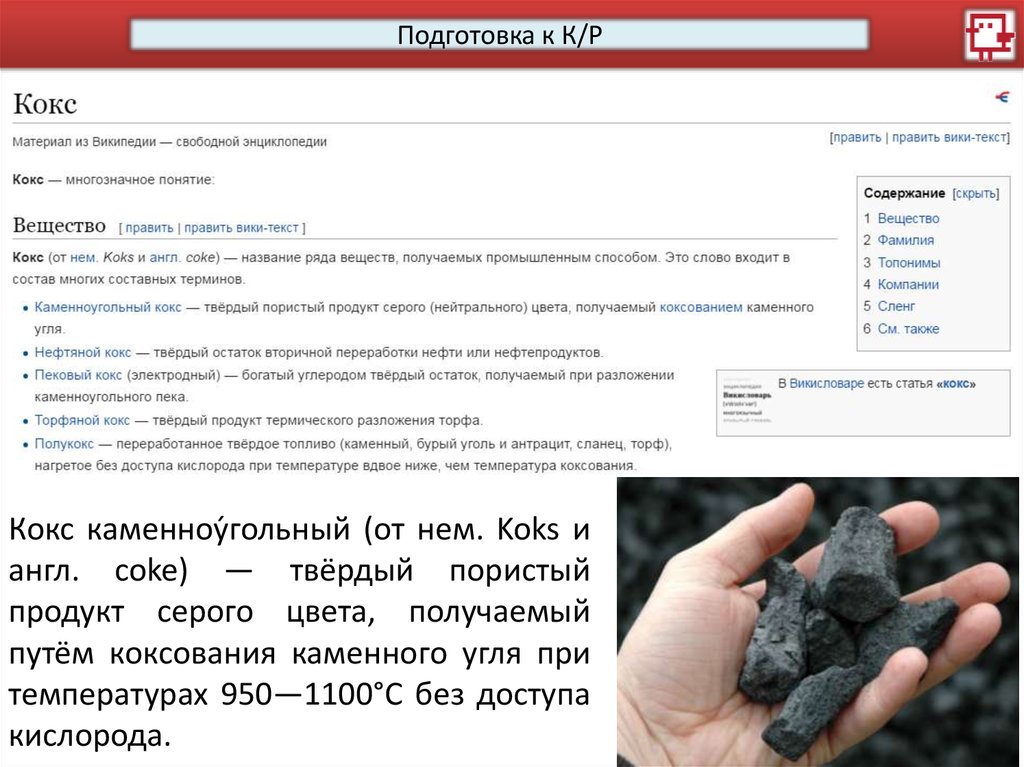
Подготовка к К/РКокс каменноу́гольный (от нем. Koks и
англ. coke) — твёрдый пористый
продукт серого цвета, получаемый
путём коксования каменного угля при
температурах 950—1100°С без доступа
кислорода.
9.
Подготовка к К/РПоследовательность действий на к/р:
1) Проверяем является ли реакция окислительновосстановительной (ОВР).
2) Расставляем степени окисления над элементомокислителем и элементом-восстановителем.
Cl2 + H2O(пар) + С(кокс) CO2 + HCl
10.
Подготовка к К/РПоследовательность действий на к/р:
1) Проверяем является ли реакция окислительновосстановительной (ОВР).
2) Расставляем степени окисления над элементомокислителем и элементом-восстановителем.
+4
-1
0
0
Cl2 + H2O(пар) + С(кокс) CO2 + HCl
11.
Подготовка к К/РПоследовательность действий на к/р:
1) Проверяем является ли реакция окислительновосстановительной (ОВР).
2) Расставляем степени окисления над элементомокислителем и элементом-восстановителем.
3) Записываем часть электронного уравнений
(полу-реакций) для окислителя и восстановителя:
0
0
+4
-1
Cl2 + H2O(пар) + С(кокс) CO2 + HCl
Окислитель: Сl2 ClВосстановитель: С CO2
12.
Подготовка к К/РПоследовательность действий на к/р:
4) Качественно уравниваем полу-реакции:
Cl2 + H2O(пар) + С(кокс) CO2 + HCl
Окислитель: Сl2 + A Cl- + B
Восстановитель: С + X CO2 + D
13.
Подготовка к К/РПоследовательность действий на к/р:
4) Качественно уравниваем полу-реакции:
Cl2 + H2O(пар) + С(кокс) CO2 + HCl
Окислитель: Сl2 ClВосстановитель: С + H2O CO2 + Н+
14.
Подготовка к К/РПоследовательность действий на к/р:
4) Качественно уравниваем полу-реакции.
5) Количественно уравниваем полу-реакции:
Cl2 + H2O(пар) + С(кокс) CO2 + HCl
Окислитель: Сl2 ClВосстановитель: С + H2O CO2 + Н+
15.
Подготовка к К/РПоследовательность действий на к/р:
4) Качественно уравниваем полу-реакции.
5) Количественно уравниваем полу-реакции:
Cl2 + H2O(пар) + С(кокс) CO2 + HCl
Окислитель: Сl2 2ClВосстановитель: С + 2H2O CO2 + 4Н+
16.
Подготовка к К/РПоследовательность действий на к/р:
4) Качественно уравниваем полу-реакции.
5) Количественно уравниваем полу-реакции.
6) Считаем заряды и уравниваем их электронами:
Cl2 + H2O(пар) + С(кокс) CO2 + HCl
Окислитель: Сl2 2Cl-
Восстановитель: С + 2H2O CO2 + 4Н+
17.
Подготовка к К/РПоследовательность действий на к/р:
4) Качественно уравниваем полу-реакции.
5) Количественно уравниваем полу-реакции.
6) Считаем заряды и уравниваем их электронами:
Cl2 + H2O(пар) + С(кокс) CO2 + HCl
+2е-
Окислитель: Сl2 2Cl-4е-
Восстановитель: С + 2H2O CO2 + 4Н+
18.
Подготовка к К/РПоследовательность действий на к/р:
4) Качественно уравниваем полу-реакции.
5) Количественно уравниваем полу-реакции.
6) Считаем заряды и уравниваем их электронами.
7) Вычисляем коэффициенты пропорциональности
по электронном для каждой полу-реакции:
+2е-
Сl2 2Cl- -4еС + 2H2O CO2 + 4Н+
2
1
19.
Подготовка к К/РПоследовательность действий на к/р:
8)
Складываем
полу-реакции
коэффициентов:
Сl2 2ClС + 2H2O CO2 + 4Н+
2
1
с
учётом
20.
Подготовка к К/РПоследовательность действий на к/р:
8)
Складываем
полу-реакции
коэффициентов:
Сl2 2ClС + 2H2O CO2 + 4Н+
с
учётом
2
1
2Сl2 + C + 2H2O = CO2 + 4Cl- + 4H+
4HCl
Ура!
21.
Подготовка к К/РSO2 + SeO2 + H2O Se + H2SO4
22.
Подготовка к К/РH2SO4(конц) + Zn H2S + H2O + ZnSO4





















 chemistry
chemistry








