Similar presentations:
Химиялық тепе-теңдік
1. Химиялық тепе-теңдік
2.
Химиялық тепе-теңдік күйгеәрекеттесетін заттардың
концентрациясы, температура
ал газ күйіндегі заттарға қысым
әсер етеді.
Реакциялаушы жүйенің бір тепе
теңдік күйден басқа тепе-теңдік
күйге ауысуын химиялық тепетеңдіктің ығысуы деп аталады.
1884жылы химиялық тепетеңдіктің ығысу заңдылығы
қортындыланып шығарылады.
Бұл заңдылықты
«Ле Штателье»деп атайды.
3.
Химиялық тепе-теңдікБірдей жағдайда қарама-қарсы екі
бағытта жүретін реакциялар
қайтымды реакциялар деп
аталады.
Fe₃O₄ + 4H₂ 3Fe + 4H₂O
Солдан оңға қарай жазылған
реакция тура, ал оңнан солға қарай
жазылған реакция кері реакция деп
аталады.
4.
Қайтымды реакциядарда, тура және керіреакциялардың жылдамдықтары
теңескен күйді химиялық тепе-теңдік
деп атайды.
Химиялық тепе-теңдік кезінде реакйиядар
тоқтап қалмайды, тек қарама-қарсы
реакцияладың жылдамдықтары ғана
теңесетін процесс. Сондықтан оны
жылжымалы немесе динамикалық тепе–
теңдік деп атайды
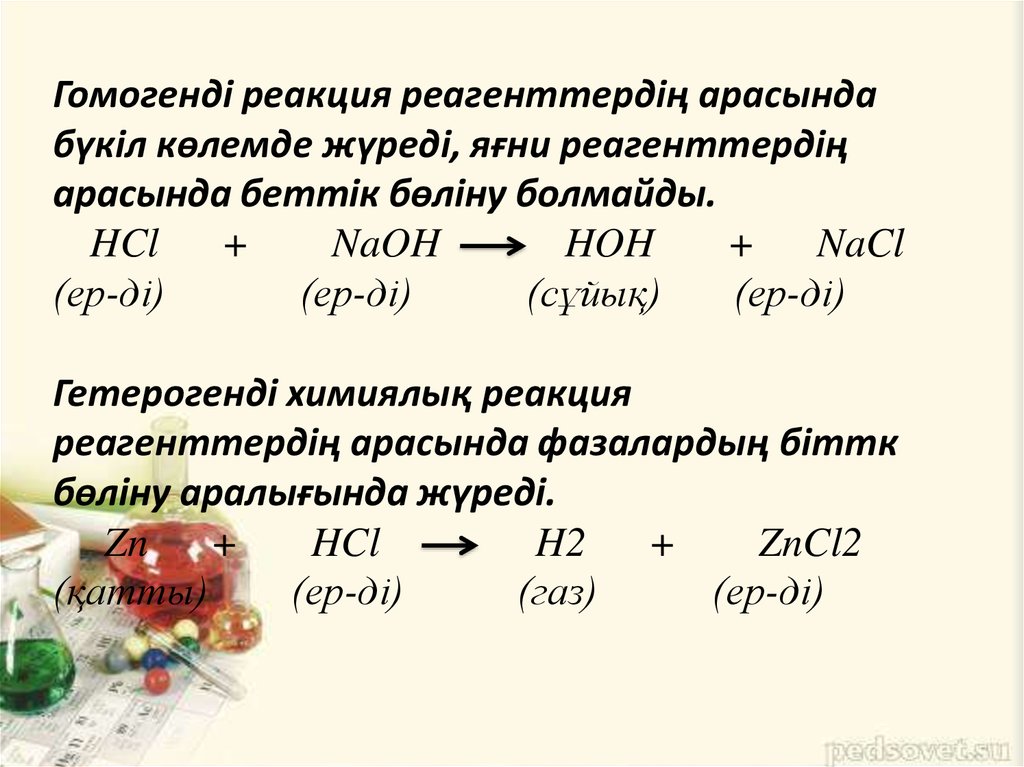
5. Гомогенді реакция реагенттердің арасында бүкіл көлемде жүреді, яғни реагенттердің арасында беттік бөліну болмайды. HCl + NaOH
HOH+
NaCl
(ер-ді)
(ер-ді)
(сұйық)
(ер-ді)
Гетерогенді химиялық реакция
реагенттердің арасында фазалардың біттк
бөліну аралығында жүреді.
Zn +
HCl
H2 +
ZnCl2
(қатты)
(ер-ді)
(газ)
(ер-ді)
6. Гомогенді реакциялардың жылдамдығы жүйенің көлем бірлігінде және кесімді уақытта реакцияға түскен немесе реакция нәтижетсінде
түзілген заттардыңмөлшерімен өлшенеді.
Гетерогенді реакциялардың жылдамдығы
фазалар айырығының аудан беті бірлігінде
және кесімді уақытта реакцияға түскен
немесе реакция нәтижесінде тузілген
заттардың мөлшерімен өлшенеді.





 chemistry
chemistry








