Similar presentations:
Регуляция обмена веществ. Гормоны
1. Регуляция обмена веществ. Гормоны
2. Гормо́ны (греч. Ορμόνη) (греч. hormao — возбуждаю, побуждаю) — биологически активные сигнальные химические вещества, выделяемые
эндокринными железами непосредственно ворганизме и оказывающие дистанционное сложное
и многогранное воздействие на организм в целом
либо на определённые органы и ткани-мишени.
Гормоны служат гуморальными (переносимыми с
кровью) регуляторами определённых процессов в
различных органах и системах.
3. ОСНОВНЫЕ СИСТЕМЫРЕГУЛЯЦИИ МЕТАБОЛИЗМА И МЕЖКЛЕТОЧНОЙ КОММУНИКАЦИИ
Для нормального функционирования многоклеточногоорганизма необходима взаимосвязь между отдельными
клетками, тканями и органами. Эту взаимосвязь
осуществляют 4 основные системы регуляции.
Центральная и периферическая нервные системы через нервные
импульсы и нейромедиаторы;
Эндокринная система через эндокринные железы и гормоны,
которые секретируются в кровь и влияют на метаболизм
различных клеток мишеней;
Паракринная и аутокринная системы посредством различных
соединений, которые секретируются в межклеточное
пространство и взаимодействуют с рецепторами либо
близлежащих клеток, либо той же клетки ( простагландины,
гормоны ЖКТ, гистамин и др. )
Иммунная система через специфические белки ( цитокины,
антитела).
4.
Долгое время оставалось неясным, как гормонымогут оказывать столь разные эффекты на
различные физиологические процессы. В последние
годы было выяснено, что биологическое действие
гормонов, например, кортизола направлено на
проницаемость клеточных мембран и на ферменты,
причем действие на ферменты развивается в двух
направлениях: влияние на активность ферментов и
на синтез de novo.
5.
6. Роль гормонов в регуляции обмена веществ.
Интегрирующими регуляторами , связывающимиразличные регуляторные механизмы и метаболизм в
разных органах , являются гормоны . Они
функционируют как химические посредники ,
переносящие сигналы , возникающие в различных
органах и ЦНС . Ответная реакция клетки на действие
гормона разнообразна и определяется как химическим
строением гормона , так и типом клетки , на которую
направлено действие гомона.
В крови гормоны присутствуют в очень низкой
концентрации. Для того , чтобы передавать сигналы в
клетки , гормоны должны распознаваться и связываться
особыми белками клетки – рецепторами , обладающими
высокой специфичностью .
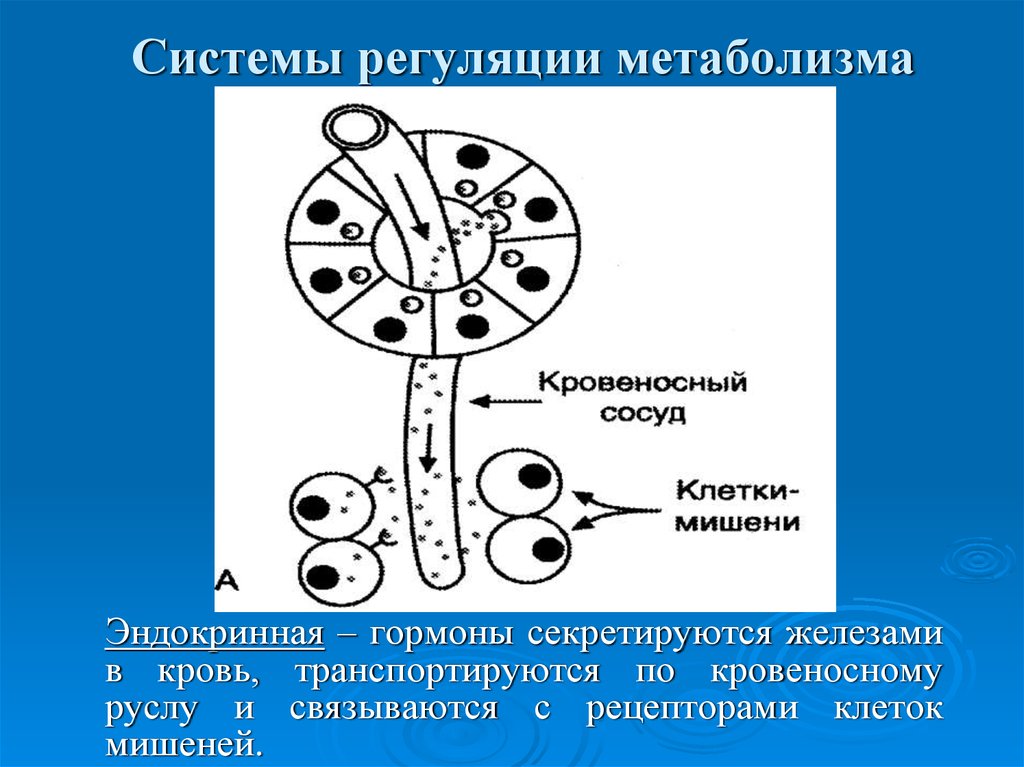
7. Системы регуляции метаболизма
Эндокринная – гормоны секретируются железамив кровь, транспортируются по кровеносному
руслу и связываются с рецепторами клеток
мишеней.
8.
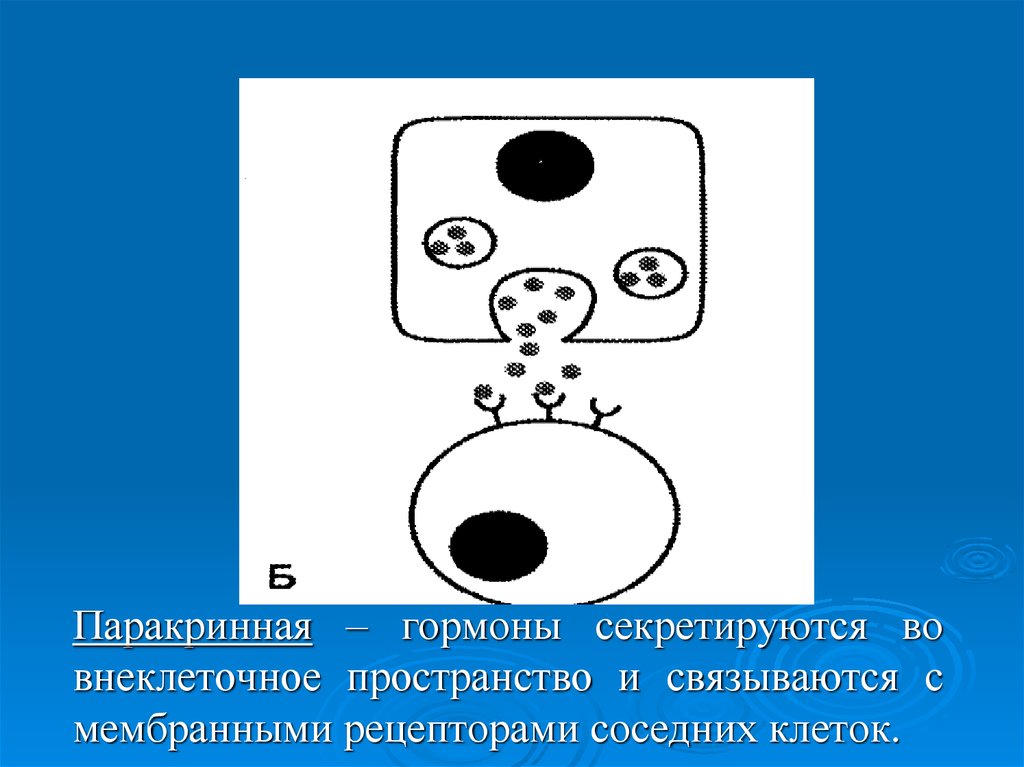
Паракринная – гормоны секретируются вовнеклеточное пространство и связываются с
мембранными рецепторами соседних клеток.
9.
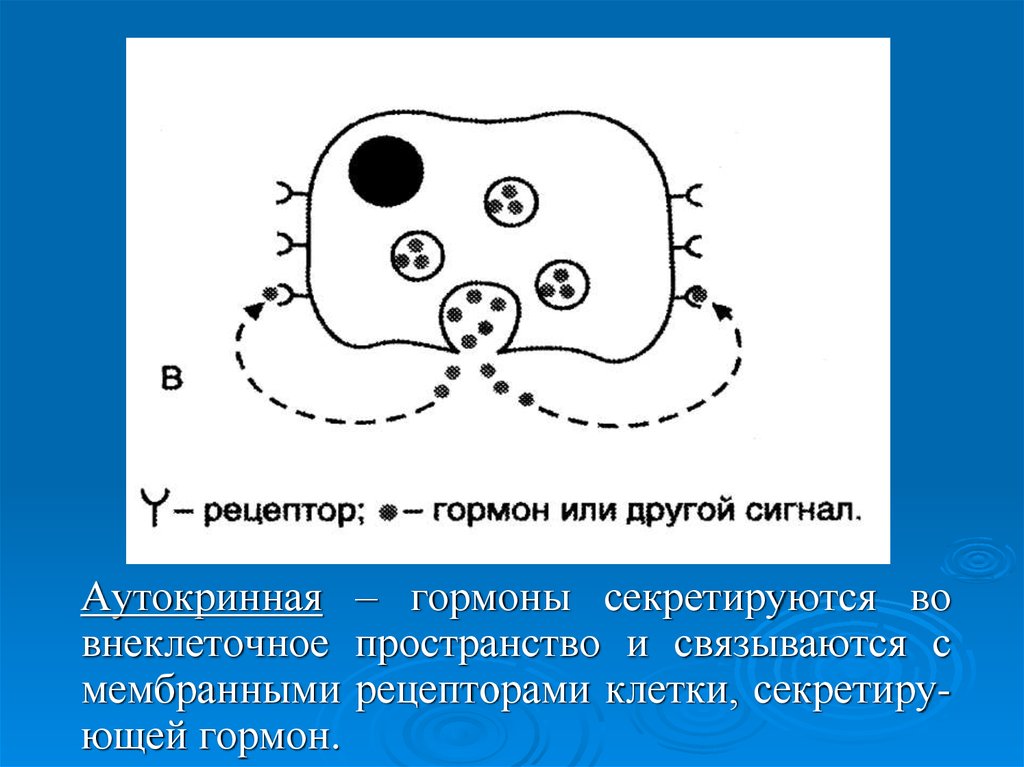
Аутокринная – гормоны секретируются вовнеклеточное пространство и связываются с
мембранными рецепторами клетки, секретирующей гормон.
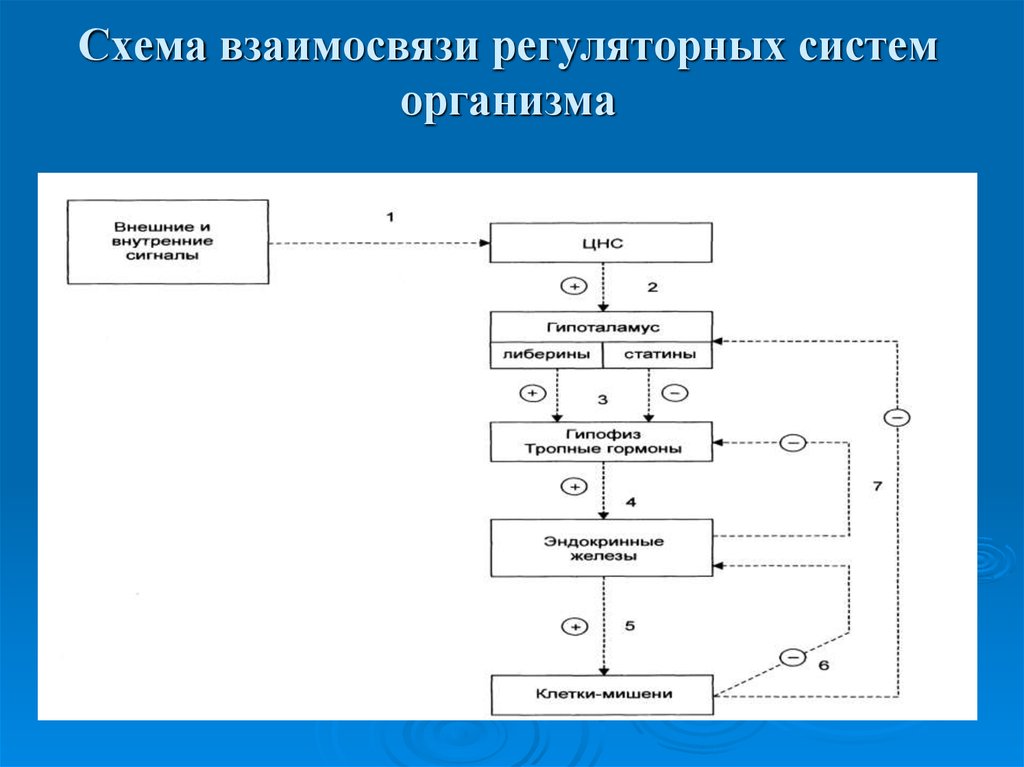
10. Схема взаимосвязи регуляторных систем организма
11.
Клетки-мишени - это клетки, которыеспецифически взаимодействуют с
гормонами с помощью специальных
белков-рецепторов.
Эти белки-рецепторы располагаются на
наружной мембране клетки, или в
цитоплазме, или на ядерной мембране и на
других органеллах клетки.
12. Клеточные рецепторы гормонов
Рецепторы пептидных гормонов иадреналина располагаются на поверхности
клеточной мембраны . Рецепторы
стероидных и тиреоидных гормонов
находятся внутри клетки.
Рецепторы по своей природе являются
белками . Состоят из нескольких доменов.
13. Рецепторы инсулина.
Рецепторы инсулина локализованы на внешнейповерхности клеточной мембраны. Они вступают во
взаимодействие
с
инсулином
и
передают
соответствующую
информацию
внутриклеточным
компонентам,
ответственным
за
биологическое
действие
гормона.
Первым
этапом
действия
инсулинрецепторного комплекса является снижение
активности аденилатциклазы, а все последующие
влияния связаны с уменьшением содержания
внутриклеточного цАМФ. Во всех изученных тканях
рецепторы
инсулина
обладают
одинаковой
специфичностью
связывания.
В
клинических
исследованиях изучение рецепторов к инсулину
проводится на моноцитах крови. Изменения в
инсулиновых
рецепторах
моноцитов
отражают
состояние инсулинового аппарата в наиболее важных
тканях-мишенях, в частности печеночной и жировой.
14. Структура мембранных рецепторов
Выделяют 3 функционально разных участка:1.Домен узнавания- расположен в N-концевой части
полипептидной цепи на внешней стороне клеточной
мембраны . Содержит гликозилированные участки и
обеспечивает узнавание и связывание гормона.
2.Трансмембранный домен:
а)у рецепторов , сопряженных с G-белками, состоит из 7
плотно упакованных α-спиральных полипептидных
последовательностей
б)одна α-спирализованная полипептидная цепь
3.Цитоплазматческий домен- создает химический сигнал
в клетке , который сопрягает узнавание и связывание
гормона с определенным внутриклеточным ответом.
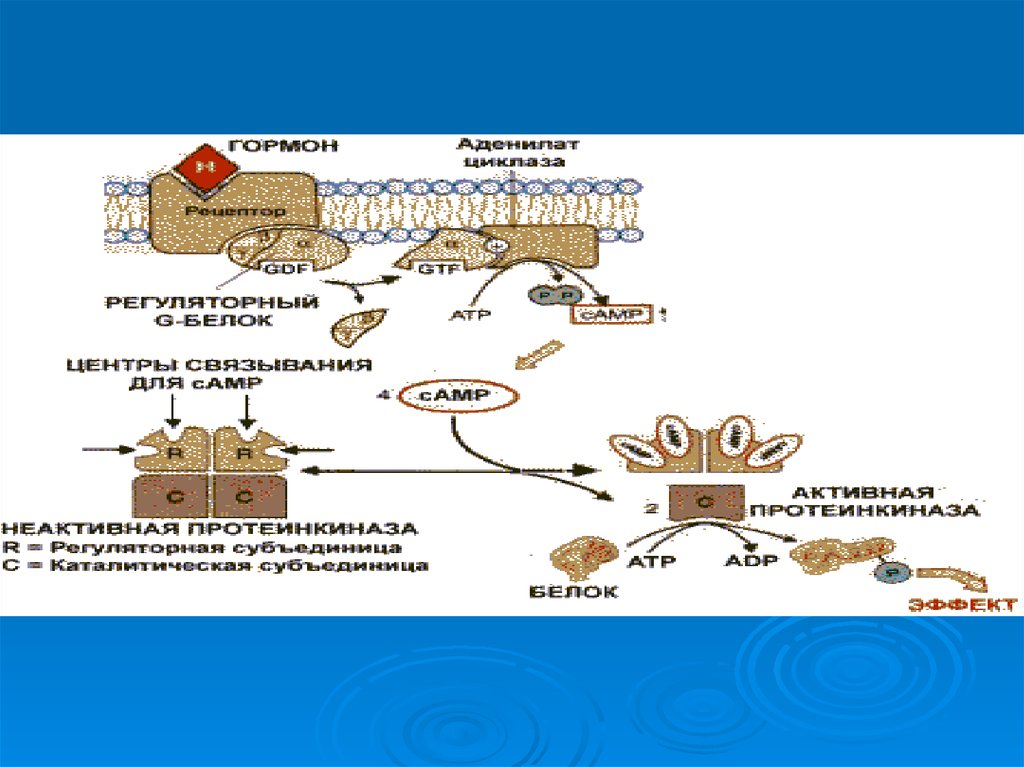
15. По механизму действия гормоны делятся на:
1 гормоны , взаимодействующие смембранными рецепторами (пептидные
гормоны, адреналин, цитокины,
эйкозаноиды)
2 гормоны , взаимодействующие с
внутриклеточными рецепторами
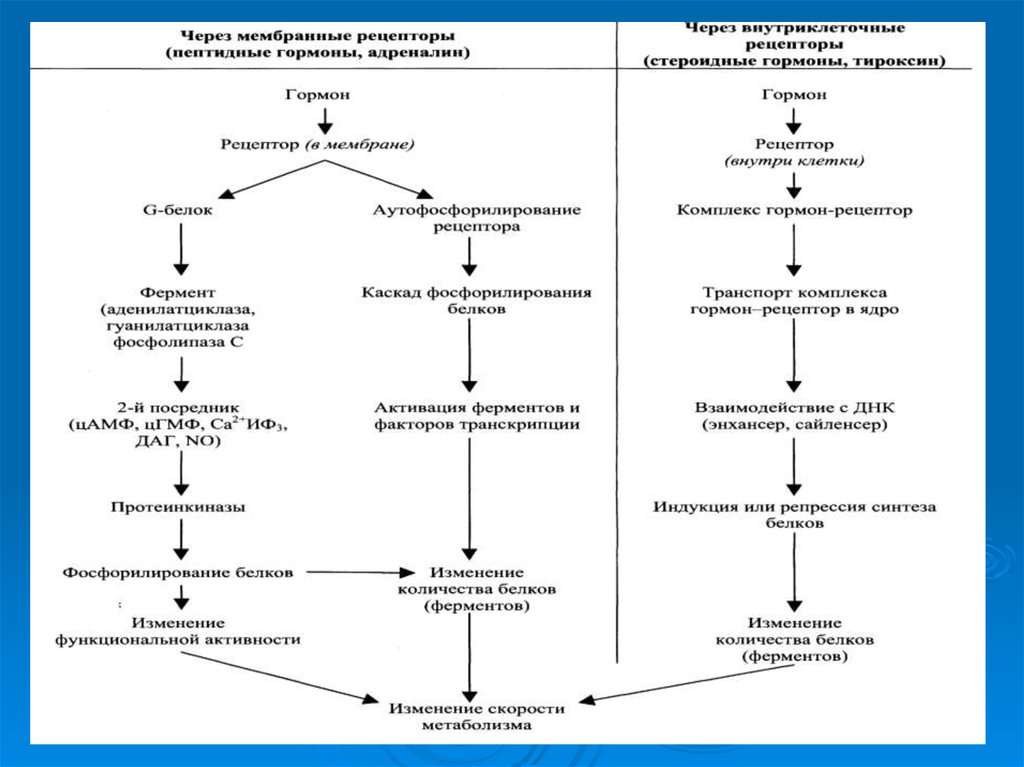
16. Основные этапы передачи гормональных сигналов
17.
18.
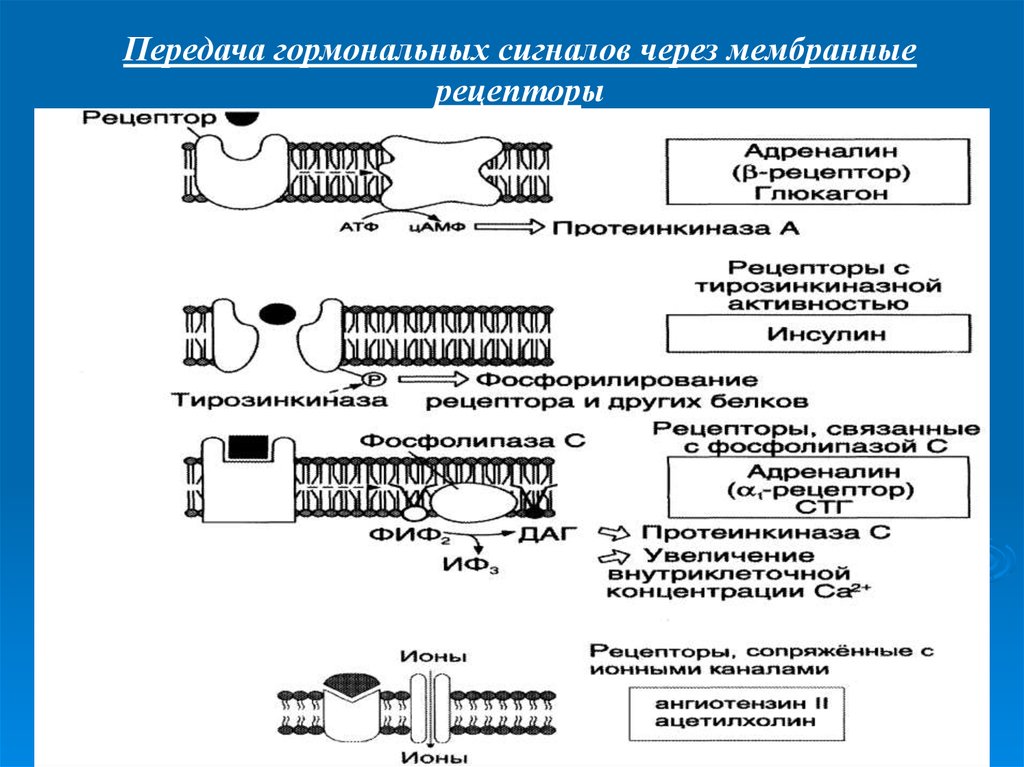
Передача гормональных сигналов через мембранныерецепторы
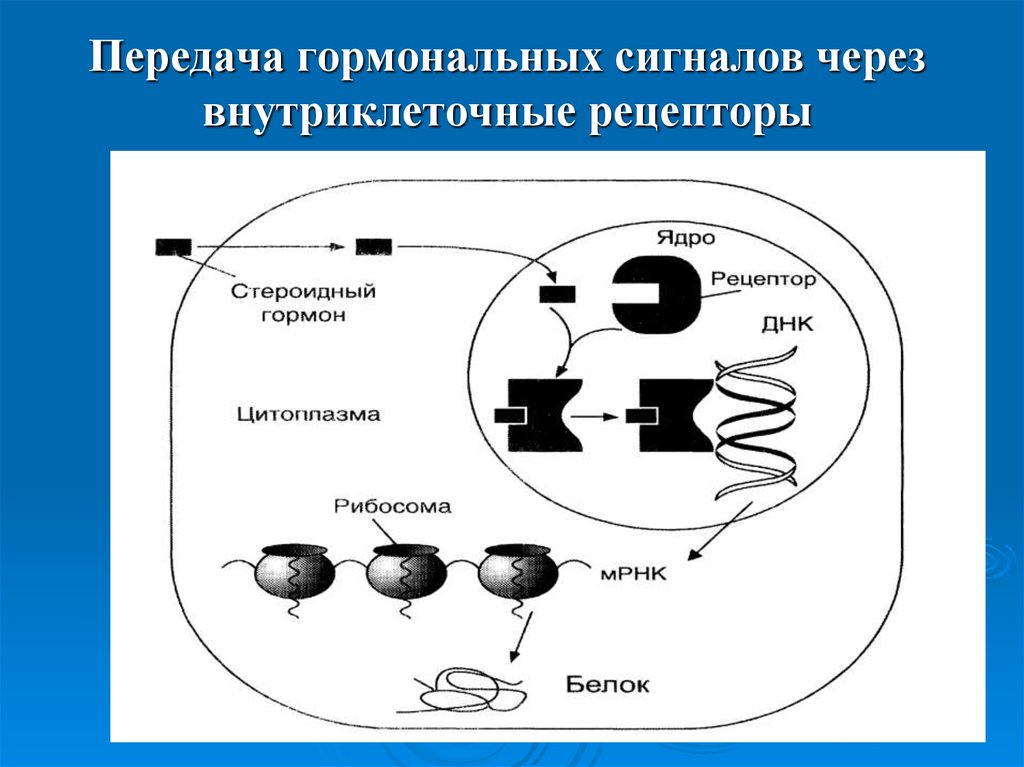
19. Передача гормональных сигналов через внутриклеточные рецепторы
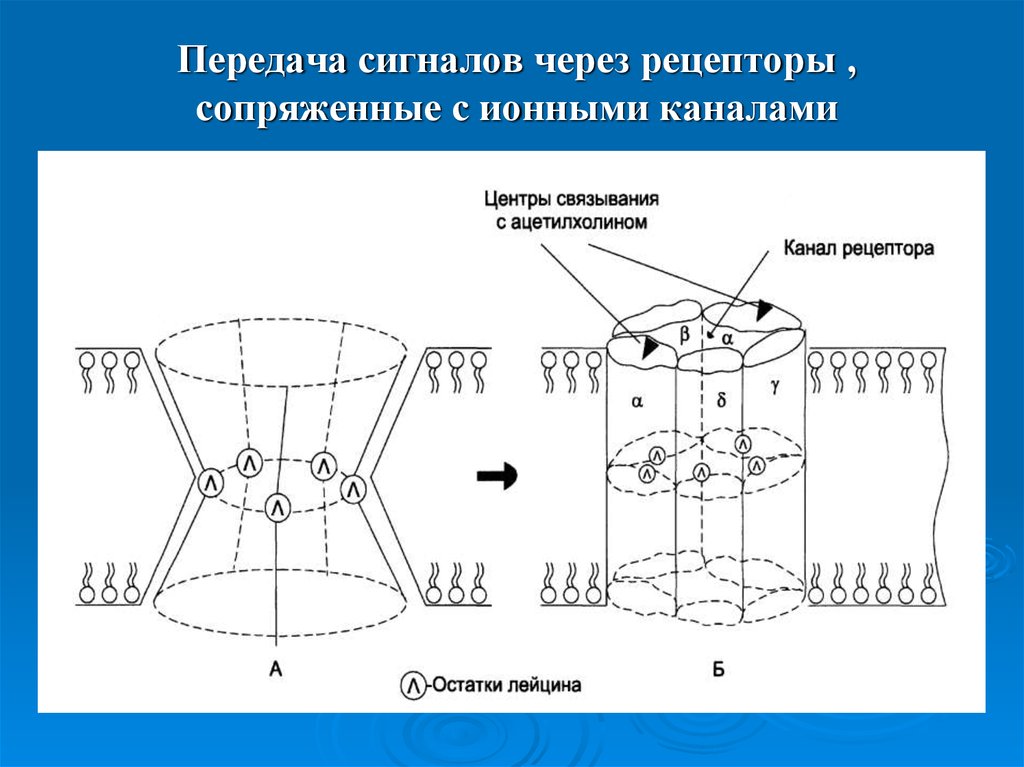
20. Передача сигналов через рецепторы , сопряженные с ионными каналами
21. Гормоны гипоталамуса – гормоны пептидной природы. Образование происходит по механизму частичного протеолиза .
1. Тиреолиберин – выполняет функцию нейромедиатора ,повышающего двигательную активность и АД.
2. Кортиколиберин – выполняет роль медиатора , участвуя в
ответной реакции на стрессовые ситуации.
3. Гонадолиберин – стимулирует синтез и секрецию ЛГ и ФСГ.
4. Соматолиберин – стимулирует синтез и секрецию
соматотропина. Соматолиберин применяют в клинической практике
для диагностики нарушений функции гипофиза.
5. Соматостатин – состоит из 14 аминокислотных остатков и имеет
циклическую структуру , так же может состоять из 28 аминокислотных
остатков. Синтезируется в желудке , в кишечнике , поджелудочной
железе , в области периферических нервных окончаниях , в плаценте ,
надпочечниках , сетчатке . Выполняет функции гормона и медиатора.
22. Механизмы регуляции внутренней секреции.
Все процессы, происходящие в организме,имеют специфические механизмы регуляции.
23.
Ведущее место в регуляции эндокринныхжелез принадлежит центральной нервной
системе.
Существует несколько механизмов
регуляции:
1) нервный. Прямые нервные влияния
играют определяющую роль в работе
иннервируемых органов (мозгового слоя
надпочечников, нейроэндокринных зон
гипоталамуса и эпифиза);
2) нейроэндокринный, связанный с
деятельностью гипофиза и гипоталамуса.
24.
3) эндокринный (непосредственное влияниеодних гормонов на биосинтез и секрецию
других (тропные гормоны передней доли
гипофиза, инсулин, соматостатин);
4) нейроэндокринный гуморальный.
Осуществляется нейрогормональными
метаболитами, оказывающие регулирующее
действие на железы (глюкозой,
аминокислотами, ионами калия, натрия,
простагландинами).
25.
В гипоталамусе происходит трансформация нервногоимпульса в специфический эндокринный процесс,
приводящий к синтезу гормона и его выделению в особых
зонах нервно-сосудистого контакта.
Выделяют два типа нейроэндокринных реакций:
а) образование и секрецию рилизинг-факторов – главных
регуляторов секреции гормонов гипофиза (гормоны
образуются в мелкоклеточных ядрах подбугровой области,
поступают в область срединного возвышения, где
накапливаются и проникают в систему портальной
циркуляции аденогипофиза и регулируют их функции);
б) образование нейрогипофизарных гормонов (гормоны сами
образуются
в
крупноклеточных
ядрах
переднего
гипоталамуса, спускаются в заднюю долю, где депонируются,
оттуда поступают в общую систему циркуляции и действуют
на периферические органы);
26. Гормоны поджелудочной железы
Поджелудочной железа выполняет в организмедве важнейшие функции:
1) Экзокриная- обеспечивает синтез, секрецию
ферментов и ионов, необходимых для
процессов пищеварения
2) Эндокриная- выполняют клетки островкового
аппарата, поджелудочной железы, которые
секретируют гормоны, участвующие в
регуляции многих процессов в организме.
27. В островковой части поджелудочной железы (островки Лангерханса) выделяют 4 типа клеток:
αклетки- глюкагон
β клетки- инсулин
δ клетки- соматостатин
G клетки- гастрин
F клетки- секретируют
панкреатический полипептид
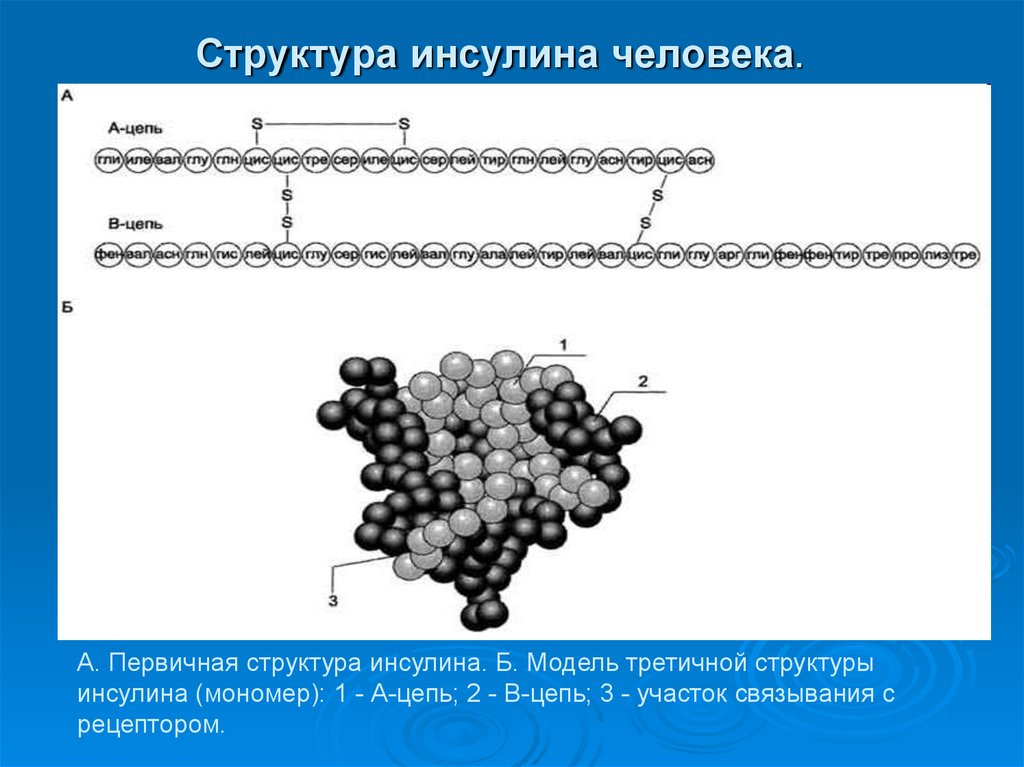
28. Структура инсулина человека.
А. Первичная структура инсулина. Б. Модель третичной структурыинсулина (мономер): 1 - А-цепь; 2 - В-цепь; 3 - участок связывания с
рецептором.
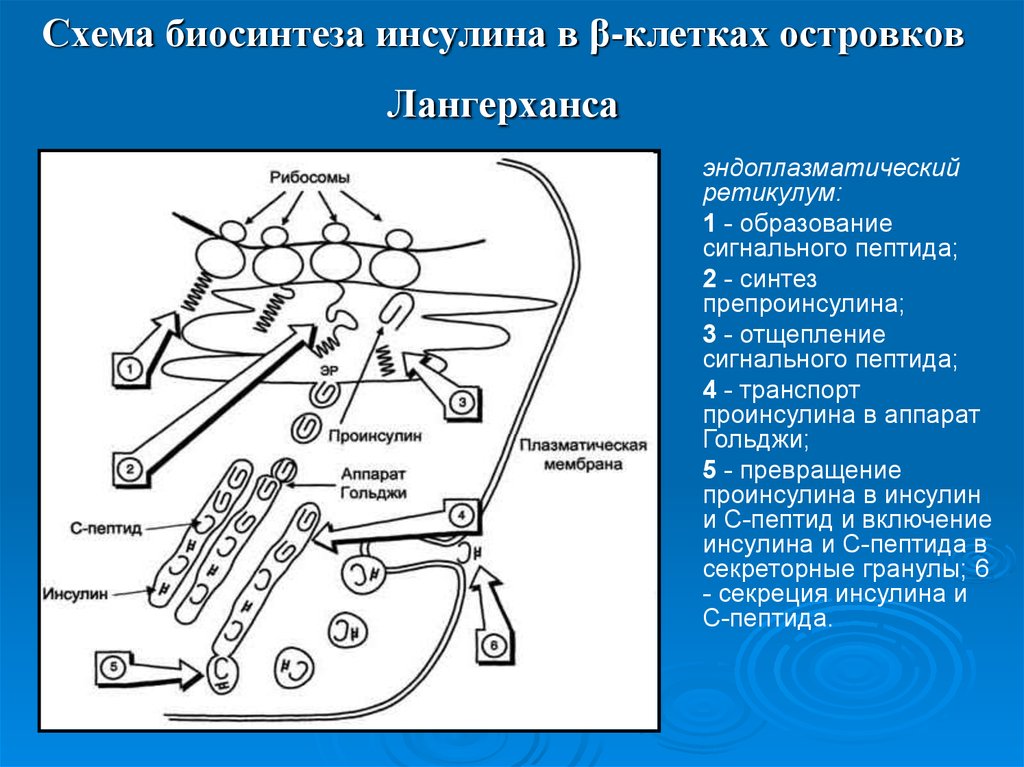
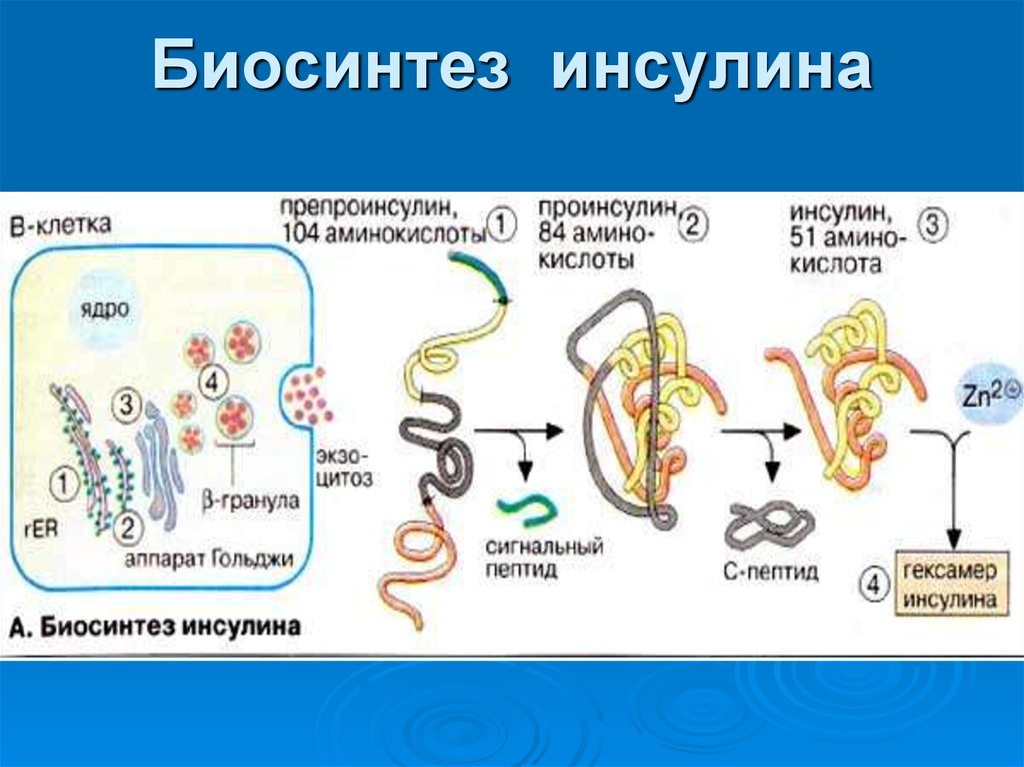
29. Схема биосинтеза инсулина в β-клетках островков Лангерханса
эндоплазматическийретикулум:
1 - образование
сигнального пептида;
2 - синтез
препроинсулина;
3 - отщепление
сигнального пептида;
4 - транспорт
проинсулина в аппарат
Гольджи;
5 - превращение
проинсулина в инсулин
и С-пептид и включение
инсулина и С-пептида в
секреторные гранулы; 6
- секреция инсулина и
С-пептида.
30. Биосинтез инсулина
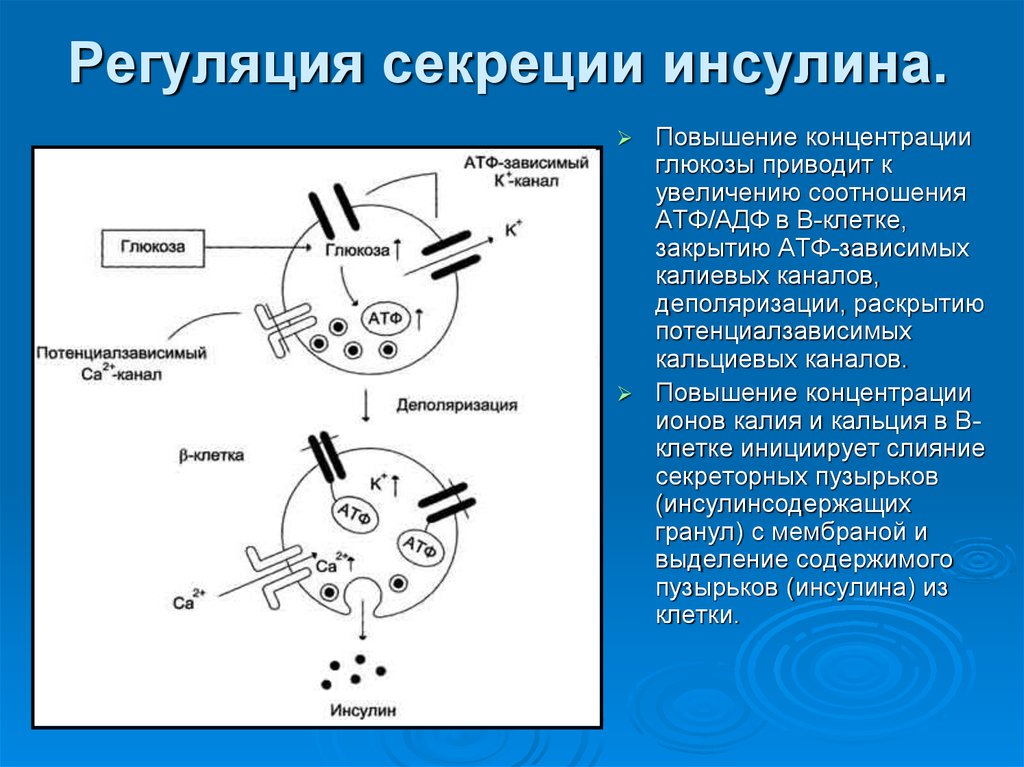
31. Регуляция секреции инсулина.
Повышение концентрацииглюкозы приводит к
увеличению соотношения
АТФ/АДФ в В-клетке,
закрытию АТФ-зависимых
калиевых каналов,
деполяризации, раскрытию
потенциалзависимых
кальциевых каналов.
Повышение концентрации
ионов калия и кальция в Вклетке инициирует слияние
секреторных пузырьков
(инсулинсодержащих
гранул) с мембраной и
выделение содержимого
пузырьков (инсулина) из
клетки.
32. Биологические функции инсулина
1.2.
3.
4.
5.
6.
7.
8.
главный анаболический гормон
участвует в регуляции метаболизма
усиливает окисление глюкозы в клетках
влияет на процессы репликации и
транскрипции
влияет на ключевые ферменты
метаболизма
усиливает синтез гликогена
усиливает синтез ЖК
тормозит глюконеогенез
33. Механизм действия инсулина
Действие инсулина начинается с его связывания соспецифическим гликопротеиновым рецептором на поверхности
клетки-мишени.Рецепторы инсулина обнаружены почти во всех
типах клеток, но больше всего их в гепатоцитах и клетках
жировой ткани.
Так как концентрация инсулина в крови составляет ~10-10 М,
Инсулиновый рецептор (IR) постоянно синтезируется и
разрушается. Т1/2 рецептора составляет 7-12 ч.
При высокой концентрации инсулина в плазме крови, например, при
ожирении, число инсулиновых рецепторов может уменьшаться, и
клетки-мишени становятся менее чувствительными к инсулину, что
может быть одной из причин сахарного диабета II типа
34. Механизм снижение чувствительности
Снижение чувствительности клеток к гормону(десенситизация) опосредуется 2 механизмами.
1.
Утрату рецепторов путём их интернализации.
(Комплекс инсулин-рецептор захватывается
внутрь клетки эндоцитозом. В результате
интернализации часть рецепторов
подвергается разрушению в лизосомах, а часть
возвращается в плазматическую мембрану)
2.
Ковалентная модификация рецептора в
результате фосфорилирования.
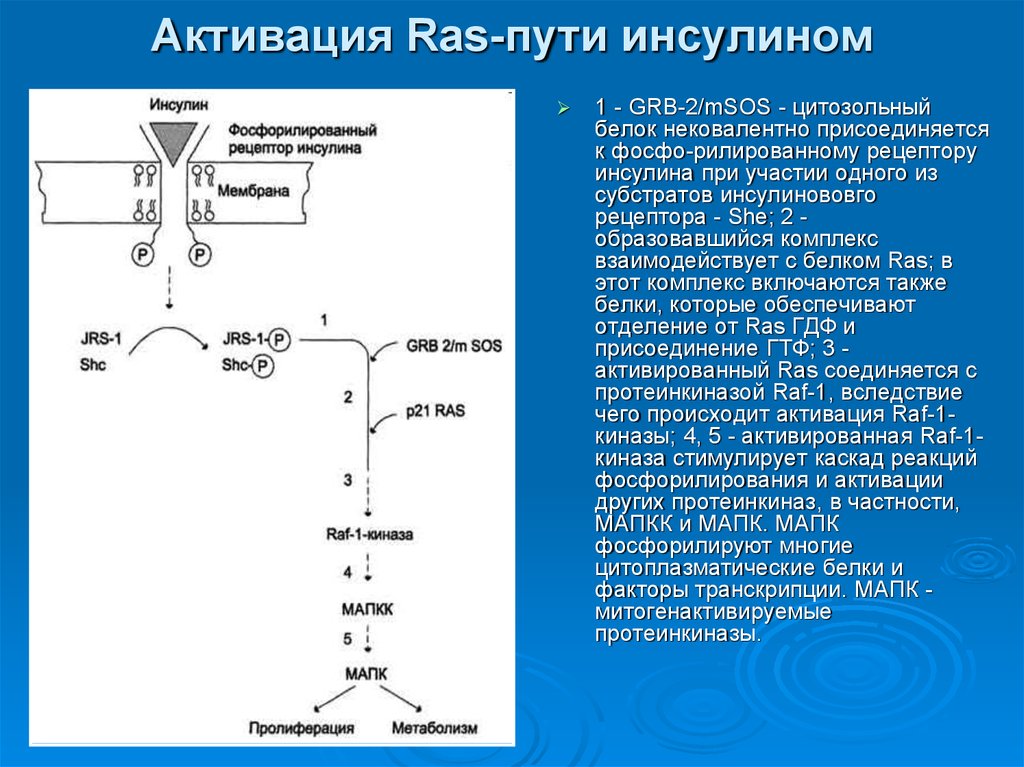
35. Активация Ras-пути инсулином
1 - GRB-2/mSOS - цитозольныйбелок нековалентно присоединяется
к фосфо-рилированному рецептору
инсулина при участии одного из
субстратов инсулинововго
рецептора - She; 2 образовавшийся комплекс
взаимодействует с белком Ras; в
этот комплекс включаются также
белки, которые обеспечивают
отделение от Ras ГДФ и
присоединение ГТФ; 3 активированный Ras соединяется с
протеинкиназой Raf-1, вследствие
чего происходит активация Raf-1киназы; 4, 5 - активированная Raf-1киназа стимулирует каскад реакций
фосфорилирования и активации
других протеинкиназ, в частности,
МАПКК и МАПК. МАПК
фосфорилируют многие
цитоплазматические белки и
факторы транскрипции. МАПК митогенактивируемые
протеинкиназы.
36. Активация фосфоинозитол-3-киназы
Активация фосфоинозитол-3-киназы (ФИ-3-киназы). Этотфермент катализирует фосфорилирование ФИ, ФИ-4-фосфата
и ФИ-4,5-бисфосфата в положении 3, образуя
полифосфоинозитиды: ФИ-3-фосфат, ФИ-3,4-бисфосфат, ФИ3,4,5-трифосфат, которые в разных клетках стимулируют
мобилизацию Са2+ и активацию специфических протеинкиназ
Активация ФИ-3-киназы стимулирует транслокацию ГЛЮТ-4 в
плазматическую мембрану и таким образом ускоряет
трансмембранный перенос глюкозы в клетки жировой и
мышечной ткани.
В жировой ткани активация ФИ-3-киназы приводит к
торможению липолиза. Снижение скорости липолиза
происходит в результате активации фосфодиэстеразы и
уменьшения внутриклеточной концентрации цАМФ
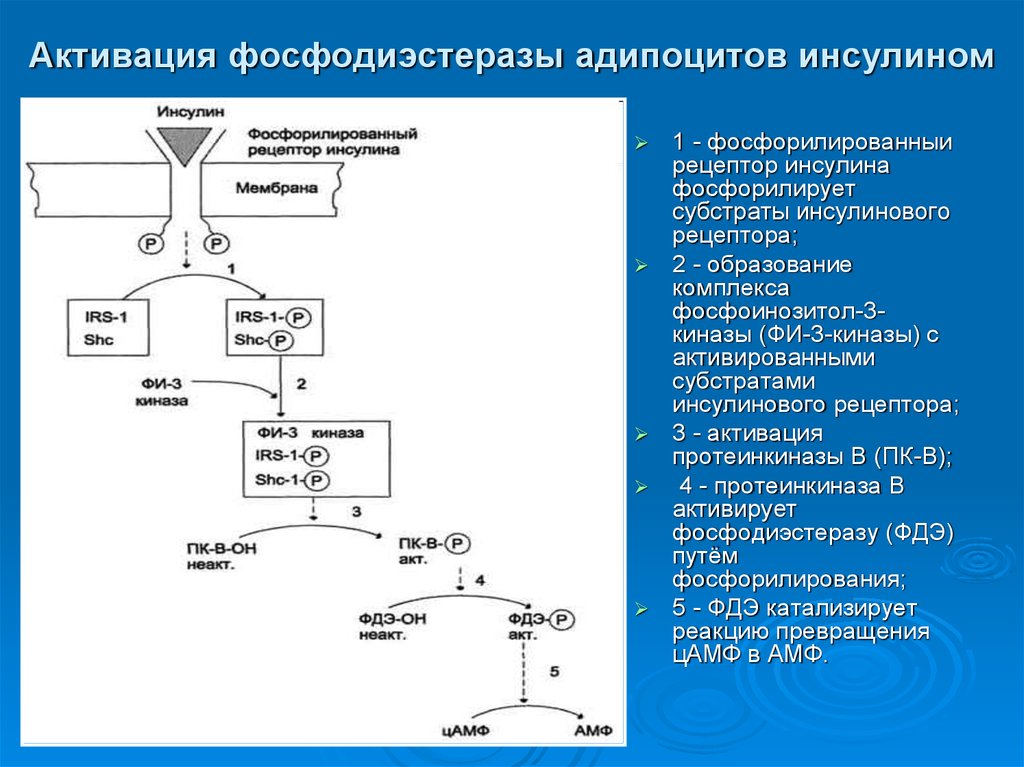
37. Активация фосфодиэстеразы адипоцитов инсулином
1 - фосфорилированныирецептор инсулина
фосфорилирует
субстраты инсулинового
рецептора;
2 - образование
комплекса
фосфоинозитол-3киназы (ФИ-3-киназы) с
активированными
субстратами
инсулинового рецептора;
3 - активация
протеинкиназы В (ПК-В);
4 - протеинкиназа В
активирует
фосфодиэстеразу (ФДЭ)
путём
фосфорилирования;
5 - ФДЭ катализирует
реакцию превращения
цАМФ в АМФ.
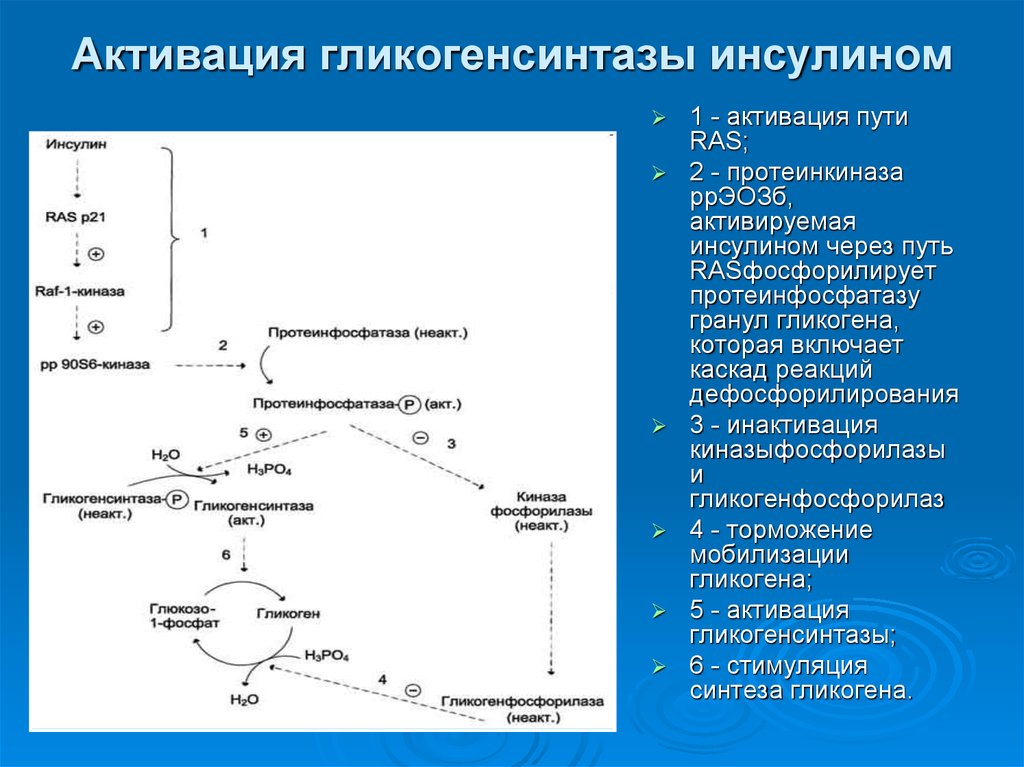
38. Активация гликогенсинтазы инсулином
1 - активация путиRAS;
2 - протеинкиназа
ррЭОЗб,
активируемая
инсулином через путь
RASфосфорилирует
протеинфосфатазу
гранул гликогена,
которая включает
каскад реакций
дефосфорилирования
3 - инактивация
киназыфосфорилазы
и
гликогенфосфорилаз
4 - торможение
мобилизации
гликогена;
5 - активация
гликогенсинтазы;
6 - стимуляция
синтеза гликогена.
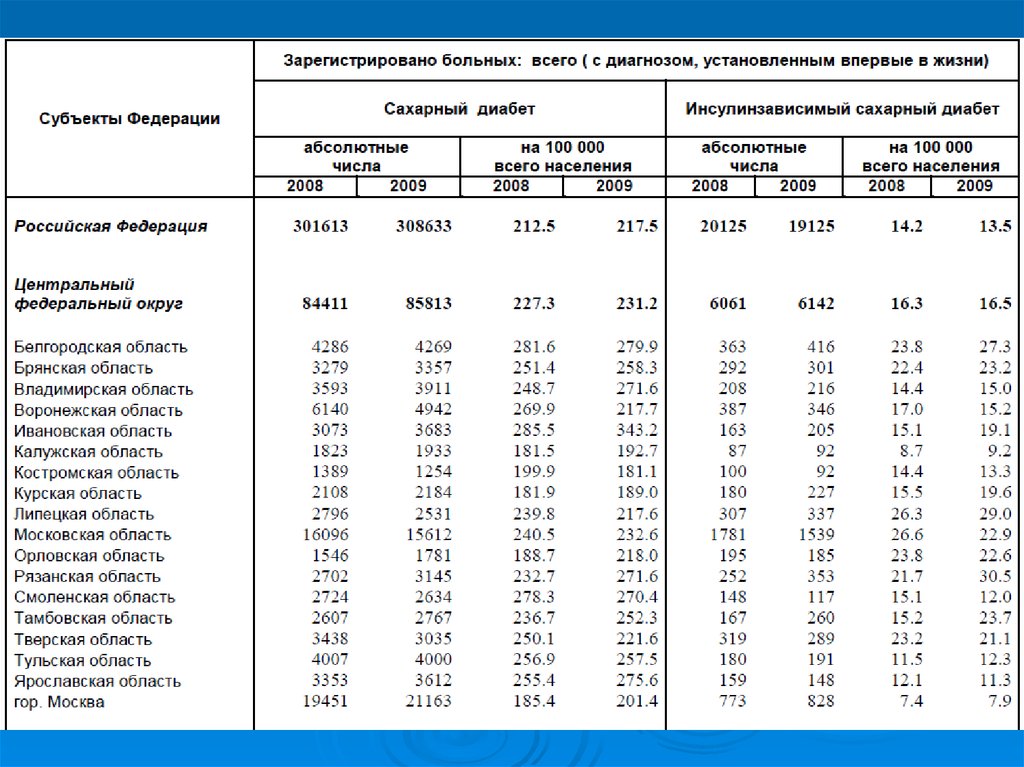
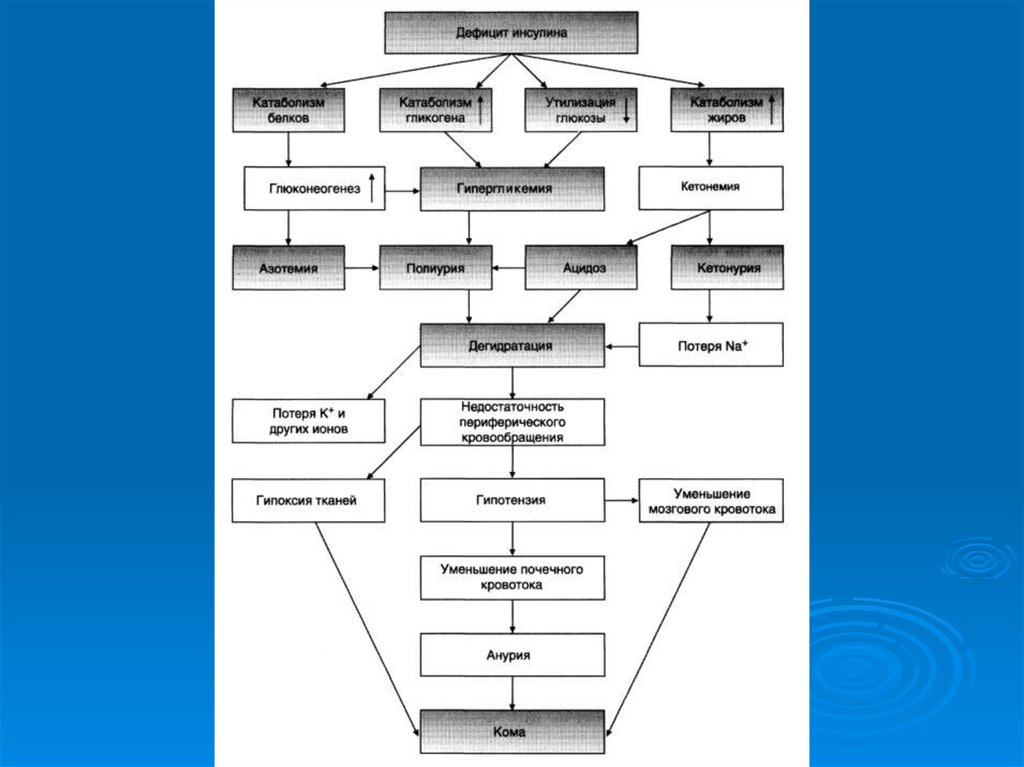
39. Инсулинзависимый сахарный диабет
Инсулинозависимый диабет сахарный связывают саутоиммунным поражением инсулин-образующих клеток
островков поджелудочной железы, приводящим к дистрофии
этих клеток, сморщиванию самих островков и почти полному
прекращению образования инсулина. Считают, что пусковыми
механизмами такого аутоиммунного процесса у людей с
наследственной предрасположенностью к диабету сахарному, т.
е. факторами риска в отношении инсулинзависимого диабета
сахарного, служат вирусные инфекции (краснуха, вирусный
гепатит, эпидемический паротит и др.) или некоторые
интоксикации. При инсулинзависимом диабете сахарном
содержание инсулина в крови резко снижено (вплоть до
полного его отсутствия). Отмечаются выраженные обменные
нарушения.
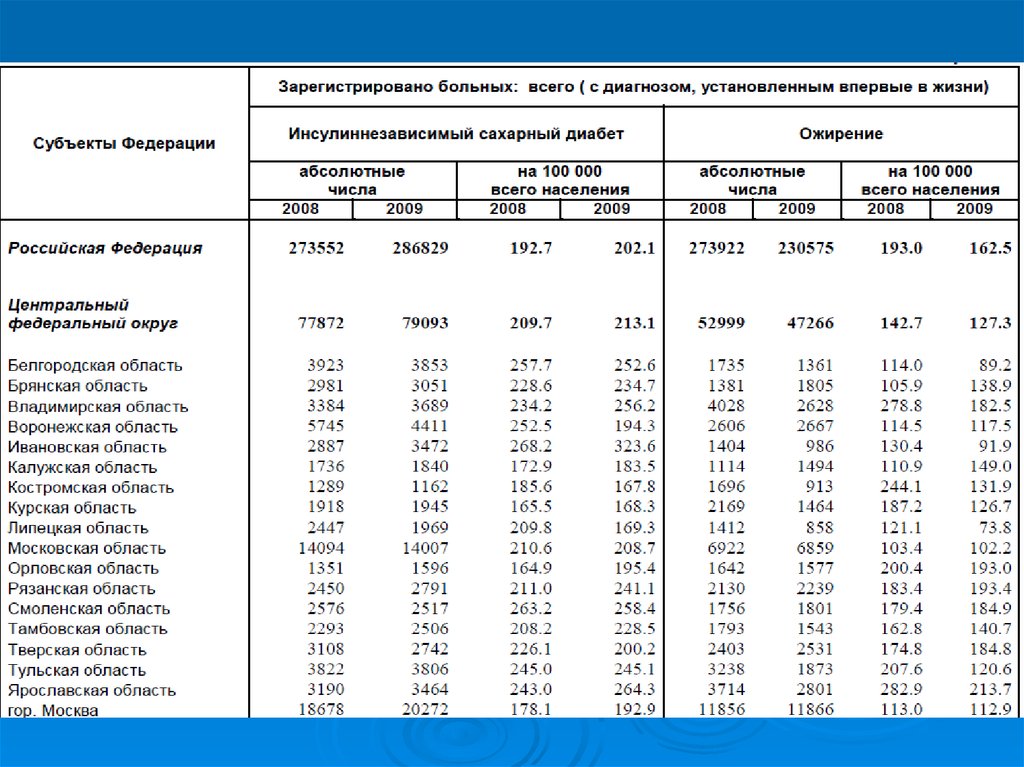
40. Инсулиннезависимый сахарный диабет
Инсулиннезависимый диабет сахарный связывают главным образом спонижением чувствительности специфических клеточных рецепторов
тканей к инсулину или с поступлением в кровоток неактивного гормона
из-за полного отсутствия или понижения активности фермента,
катализирующего так наз. ограниченный протеолиз проинсулина, т. е.
отщепление от его молекулы С-пептида. Не связанный с клеткой
инсулин не может проявить своего действия, и глюкоза не поступает
внутрь клетки. Однако инсулинобразующие клетки и сама ткань
островков при инсулиннезависимом диабете сахарном не изменены,
секреция инсулина в ответ на воздействие глюкозы суммарно не
меняется, и содержание гормона в крови соответствует норме или
бывает чуть ниже или выше нормы. При этом типе диабета сахарного
также отмечают гипергликемию и глюкозурию, но высокую
концентрацию кетоновых тел в крови наблюдают редко.
Инсулиннезависимым диабетом сахарным чаще болеют лица старше 50
лет (особенно женщины).
41.
42.
43.
44. Сахарный диабет может привести к неблагоприятным последствиям, если его плохо контролировать
ОрганЧто происходит?
Последствия
Нервная система
Поражение нервов из-за нарушения
обмена глюкозы.
Слабость в ногах ируках. Уменьшение
чувствительности и боль в руках и
ногах, параличи.
Кровь
Нарушение функция белых клеток
крови (лейкоциты).
Увеличение риска развития инфекций
(снижение иммунитета).
Почки
Поражение сосудов почек
Почечная недостаточность,
гипертония.
Глаза
Поражение сосудов сетчатки глаз.
Уменьшение остроты зрения вплоть до
слепоты
Происходит повреждение стенок
кровеносных сосудов. Высокий уровень
сахара в крови ведет к сужению просвета
сосудов . В результате нарушается
Сосуды
доставка кислорода к тканям
организма.
Нарушение работы сердца (инфаркт),
инсульт и т.п.
Уменьшение размера сосудов вызывает сн
ижение притока крови к различным
участкам организма человека.
Кожа
Нарушения кровоснабжения кожи.
Трофические язвы.
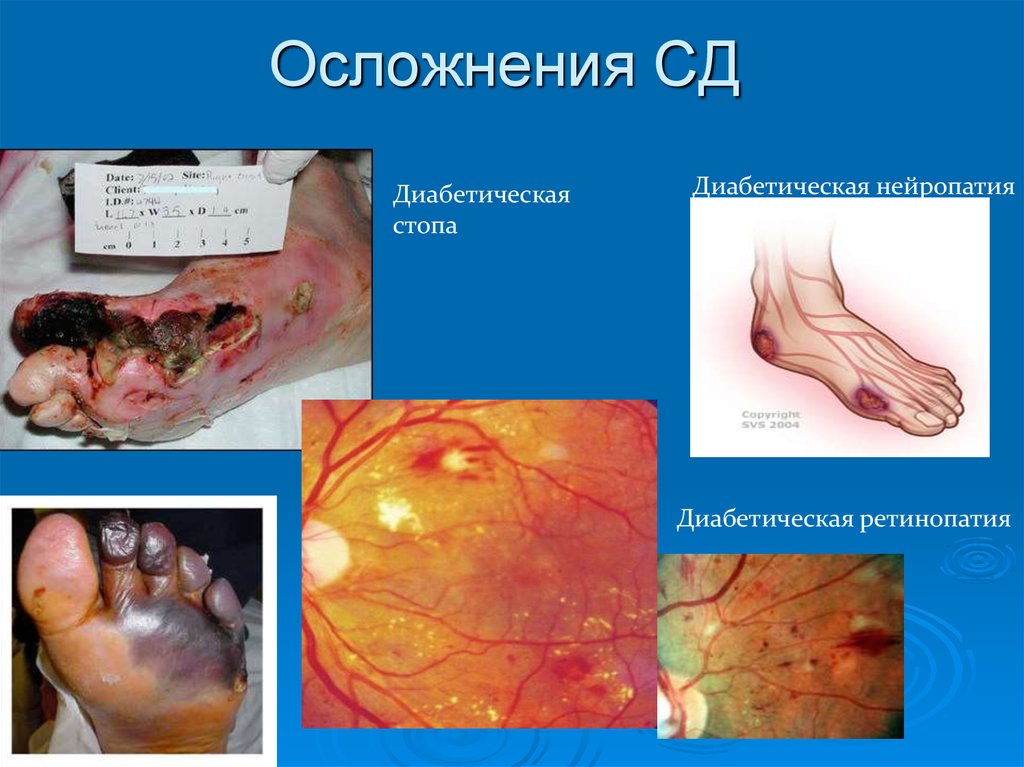
45. Осложнения СД
Диабетическаястопа
Диабетическая нейропатия
Диабетическая ретинопатия
46. Глюкагон
Глюкагон - одноцепочечный полипептид, состоящий из 29 аминокислотных остатков.Биосинтез глюкагона происходит в α-клетках островков Лангерханса, в
нейроэндокринных клетках кишечника и в некоторых отделах ЦНС. Неактивный
предшественник проглюкагон в результате частичного протеолиза превращается в
несколько пептидов. В клетках поджелудочной железы главный пептид - глюкагон; в
клетках кишечника образуются глюкагонопо-добные пептиды: GLP-1, GLP-2,
глицентин и другие. GLP-1 ингибирует секрецию глюкагона и стимулирует синтез и
секрецию инсулина.
На секрецию глюкагона влияют и многие другие соединения, включая аминокислоты,
ЖК, кетоновые тела и нейромедиаторы. При приёме пищи, богатой углеводами,
секреция глюкагона снижается. Белковая пища стимулирует секрецию инсулина и
глюкагона; однако некоторые аминокислоты в большей степени влияют на секрецию
одного из них. Например, аланин стимулирует секрецию глюкагона, но не инсулина.
В плазме крови глюкагон не связан с каким-либо транспортным белком. Т1/2
гормона составляет ~5 мин. В печени глюкагон быстро разрушается под
действием специфических протеаз.
Эффекты глюкагона в основном противоположны эффектам инсулина.
Контринсулярный гормон. Основные клетки-мишени глюкагона - печень и жировая
ткань. Связываясь с рецепторами на плазматической мембране клеток-мишеней,
глюкагон повышает содержание цАМФ. В гепатоцитах это приводит к активации
фосфорилазы гликогена и к снижению активности гликогенсинтазы. В результате
ускоряется мобилизация гликогена. Фосфорилирование пируваткиназы и БИФ
вызывает торможение гликолиза и ускорение глюконеогенеза. Кроме того, глюкагон
стимулирует глюконеогенез, индуцируя синтез ферментов: глюкозо-6-фосфатазы,
фосфоенол-пируваткарбоксикиназы, фруктозо-1,6-бисфосфатазы. В клетках жировой
ткани глюкагон через аденилатциклазный каскад активирует гормончувствительную
ТАГ-липазу и стимулирует липолиз. Таким образом, в противоположность инсулину
глюкагон стимулирует мобилизацию основных энергоносителей - углеводов и жиров.
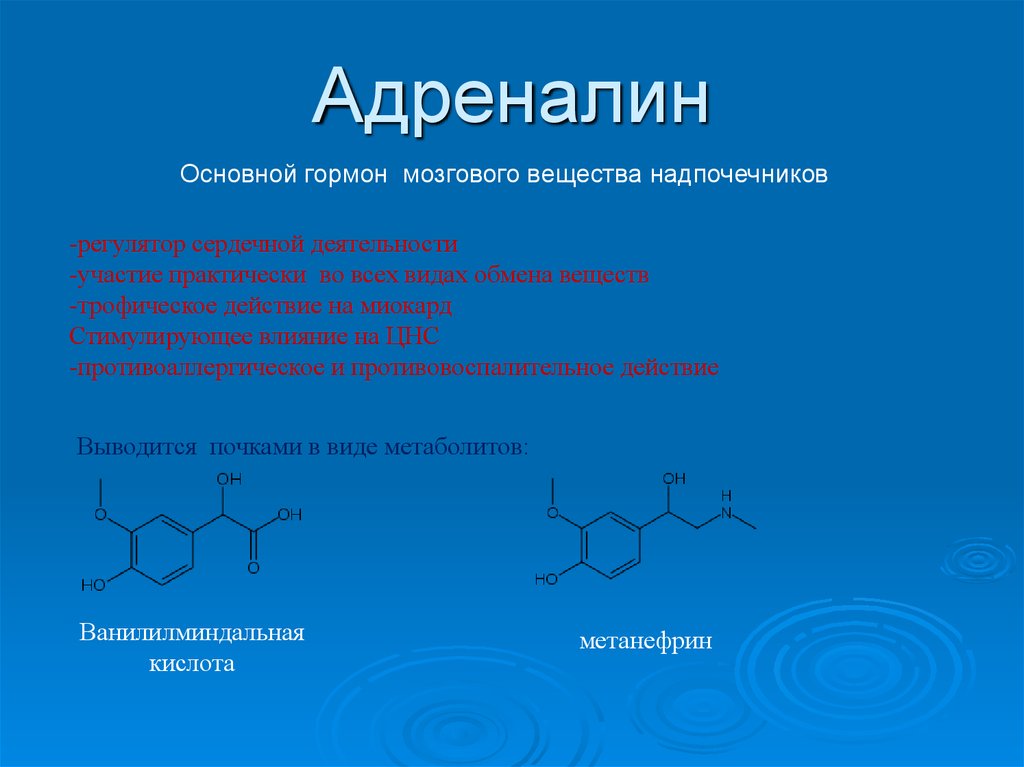
47. Адреналин
Основной гормон мозгового вещества надпочечников-регулятор сердечной деятельности
-участие практически во всех видах обмена веществ
-трофическое действие на миокард
Стимулирующее влияние на ЦНС
-противоаллергическое и противовоспалительное действие
Выводится почками в виде метаболитов:
Ванилилминдальная
кислота
метанефрин
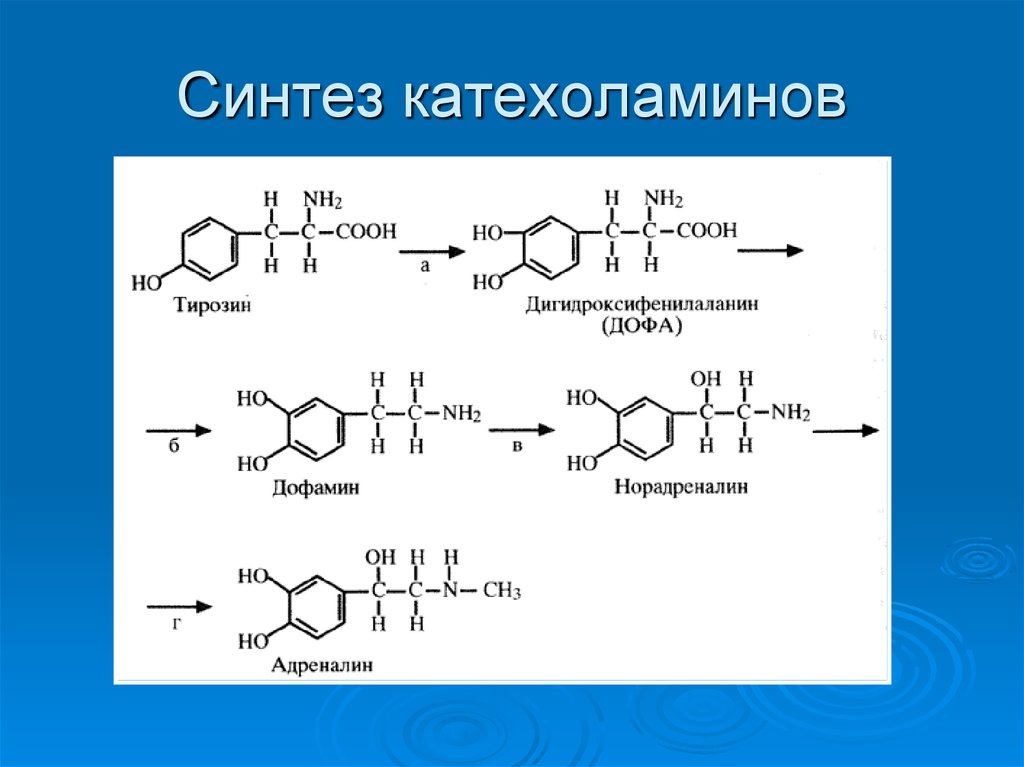
48. Синтез катехоламинов
49. Синтез и секреция катехоламинов
Синтез катехоламинов происходит в цитоплазме игранулах клеток мозгового слоя надпочечников.
Катехоламины поступают в гранулы путём АТФ-зависимого
транспорта и хранятся в них в комплексе с АТФ. Разные
гранулы содержат разные катехоламины: некоторые только
адреналин, другие - норадреналин, третьи - оба гормона.
Секреция гормонов из гранул происходит путём экзоцитоза.
Катехоламины и АТФ освобождаются из гранул.
В плазме крови катехоламины образуют непрочный комплекс с
альбумином. Адреналин транспортируется в основном к печени
и скелетным мышцам. Норадреналин образуется в основном в
органах, иннервируемых симпатическими нервами.
Норадреналин лишь в незначительных количествах достигает
периферических тканей. Т1/2 катехоламинов - 10-30 с.
Основная часть катехоламинов быстро метаболизируется в
различных тканях при участии специфических ферментов.Лишь
небольшая часть адреналина (~ 5%) выделяется с мочой.
50.
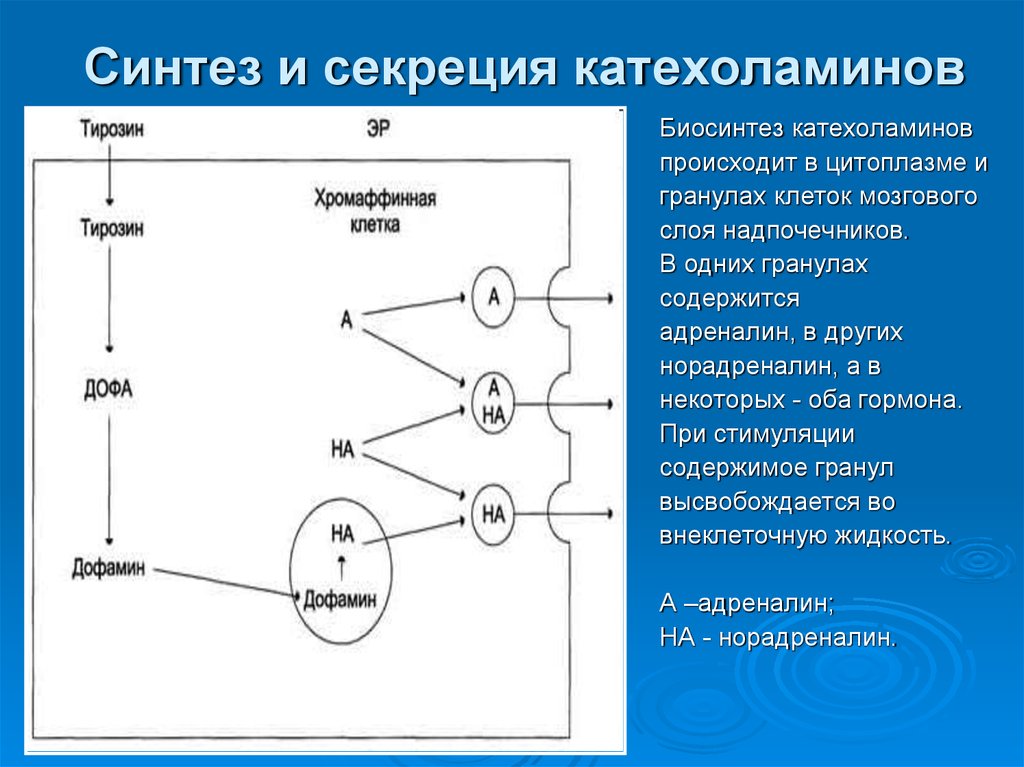
Метаболизм катехоламинов51. Синтез и секреция катехоламинов
Биосинтез катехоламиновпроисходит в цитоплазме и
гранулах клеток мозгового
слоя надпочечников.
В одних гранулах
содержится
адреналин, в других
норадреналин, а в
некоторых - оба гормона.
При стимуляции
содержимое гранул
высвобождается во
внеклеточную жидкость.
А –адреналин;
НА - норадреналин.
52. Механизм действия и биологические функции катехоламинов
Катехоламины действуют на клетки-мишени через рецепторы,локализованные в плазматической мембране. Выделяют 2
главных класса таких рецепторов: α-адренергические и βадренергические. Все рецепторы катехоламинов гликопротеины, которые являются продуктами разных генов,
различаются сродством к агонистам и антагонистам и передают
сигналы в клетки с помощью разных вторичных посредников.
Это определяет характер их влияния на метаболизм клетокмишеней.
Адреналин взаимодействует как с α-, так и с β-рецепторами;
норадреналин в физиологических концентрациях главным
образом взаимодействует с α-рецепторами.
Взаимодействие гормона с β-рецепторами активирует
аденилатциклазу, тогда как связывание с α2-рецептором её
ингибирует. При взаимодействии гормона с α1-рецептором
происходит активация фосфолипазы С и стимулируется
инозитолфосфатный путь передачи сигнала
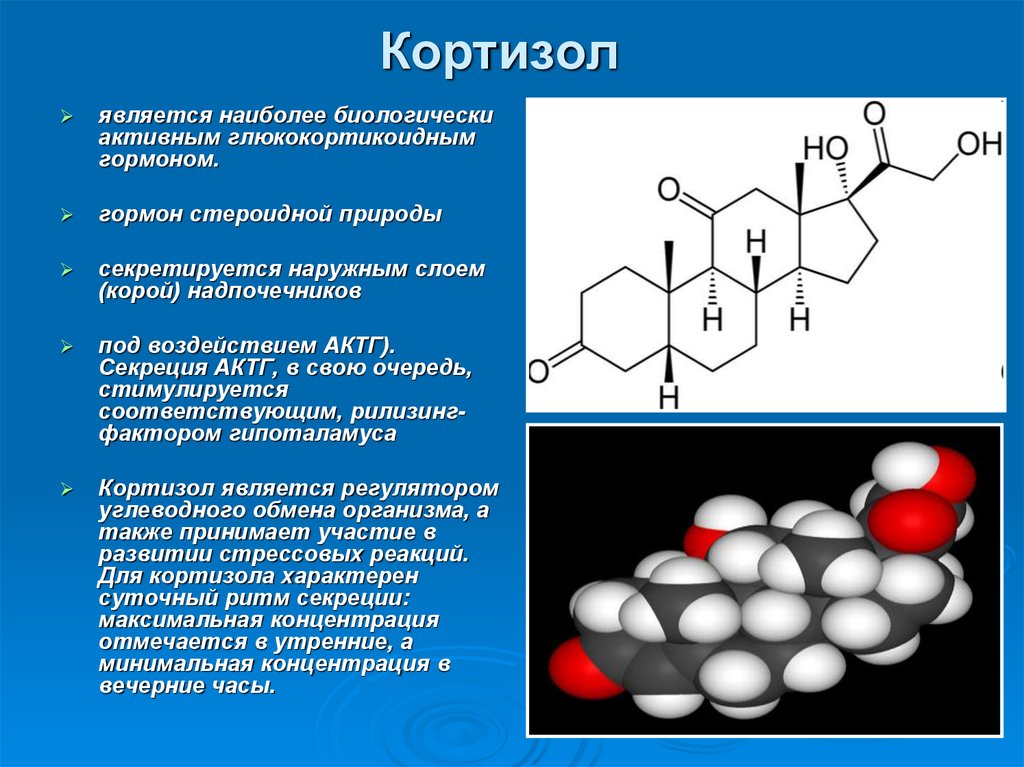
53. Кортизол
является наиболее биологическиактивным глюкокортикоидным
гормоном.
гормон стероидной природы
секретируется наружным слоем
(корой) надпочечников
под воздействием АКТГ).
Секреция АКТГ, в свою очередь,
стимулируется
соответствующим, рилизингфактором гипоталамуса
Кортизол является регулятором
углеводного обмена организма, а
также принимает участие в
развитии стрессовых реакций.
Для кортизола характерен
суточный ритм секреции:
максимальная концентрация
отмечается в утренние, а
минимальная концентрация в
вечерние часы.
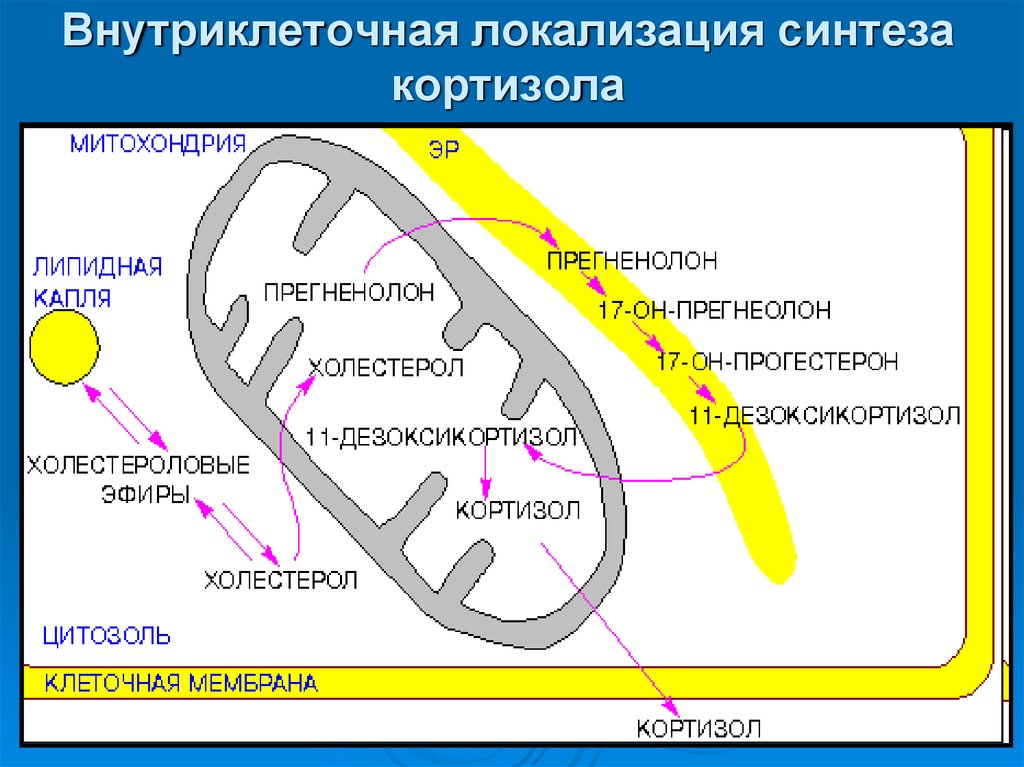
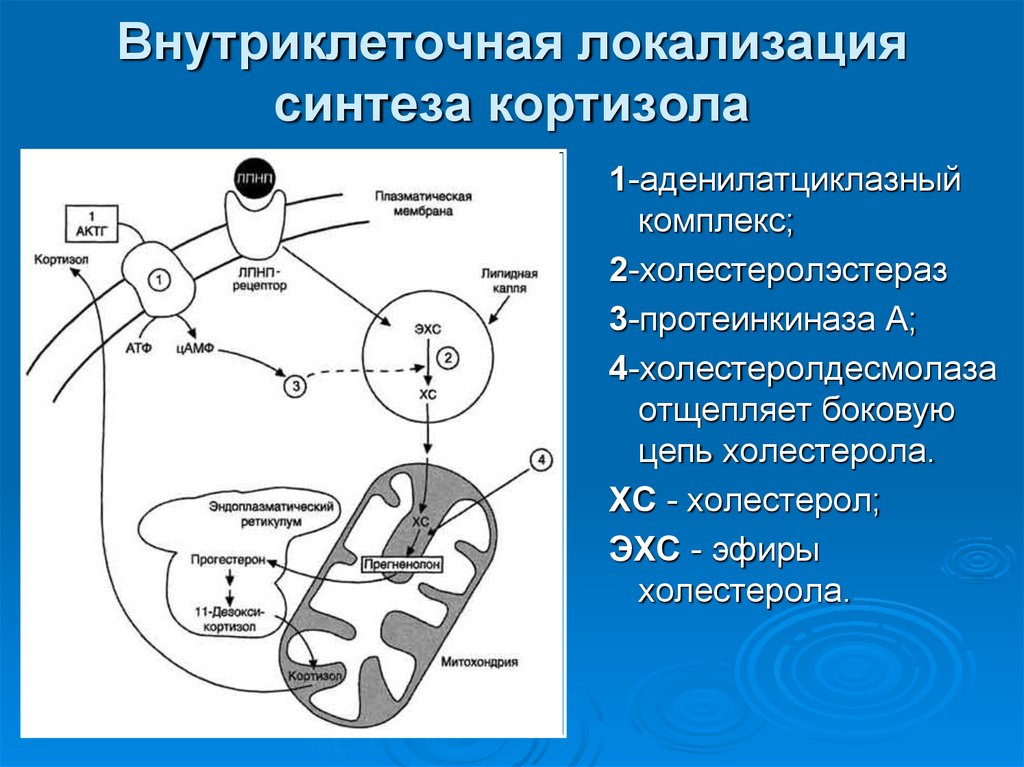
54. Внутриклеточная локализация синтеза кортизола
55. Внутриклеточная локализация синтеза кортизола
1-аденилатциклазныйкомплекс;
2-холестеролэстераз
3-протеинкиназа А;
4-холестеролдесмолаза
отщепляет боковую
цепь холестерола.
ХС - холестерол;
ЭХС - эфиры
холестерола.
56. РЕГУЛЯЦИЯ ОБМЕНА ОСНОВНЫХ ЭНЕРГОНОСИТЕЛЕЙ
Основные пищевые вещества (углеводы, жиры, белки) окисляются ворганизме с освобождением свободной энергии, которая используется в
анаболических процессах и при осуществлении физиологических функций.
Энергетическая ценность основных пищевых веществ выражается в
килокалориях и составляет: для углеводов - 4 ккал/г, для жиров - 9 ккал/г,
для белков - 4 ккал/г. Взрослому здоровому человеку в сутки требуется
2000-3000 ккал (8000-12 000 кДж) энергии.
При обычном ритме питания промежутки между приёмами пищи
составляют 4-5 ч с 8-12-часовым ночным перерывом.
Во время пищеварения и абсорбтивного периода (2-4 ч) основные
энергоносители, используемые тканями (глюкоза, жирные кислоты,
аминокислоты), могут поступать непосредственно из пищеварительного
тракта. В постабсорбтивном периоде и при голодании энергетические
субстраты образуются в процессе катаболизма депонированных
энергоносителей.
Изменения в потреблении энергоносителей и энергетических затратах
координируются путём чёткой регуляции метаболических процессов в
разных органах и системах организма, обеспечивающей энергетический
гомеостаз.
Основную роль в поддержании энергетического гомеостаза играют
гормоны инсулин и глюкагон. а также другие контринсулярные гормоны адреналин, кортизол, йодтиронины и соматотропин. Инсулин и
глюкагон играют главную роль в регуляции метаболизма при смене
абсорбтивного и постабсорбтивного периодов и при голодании.
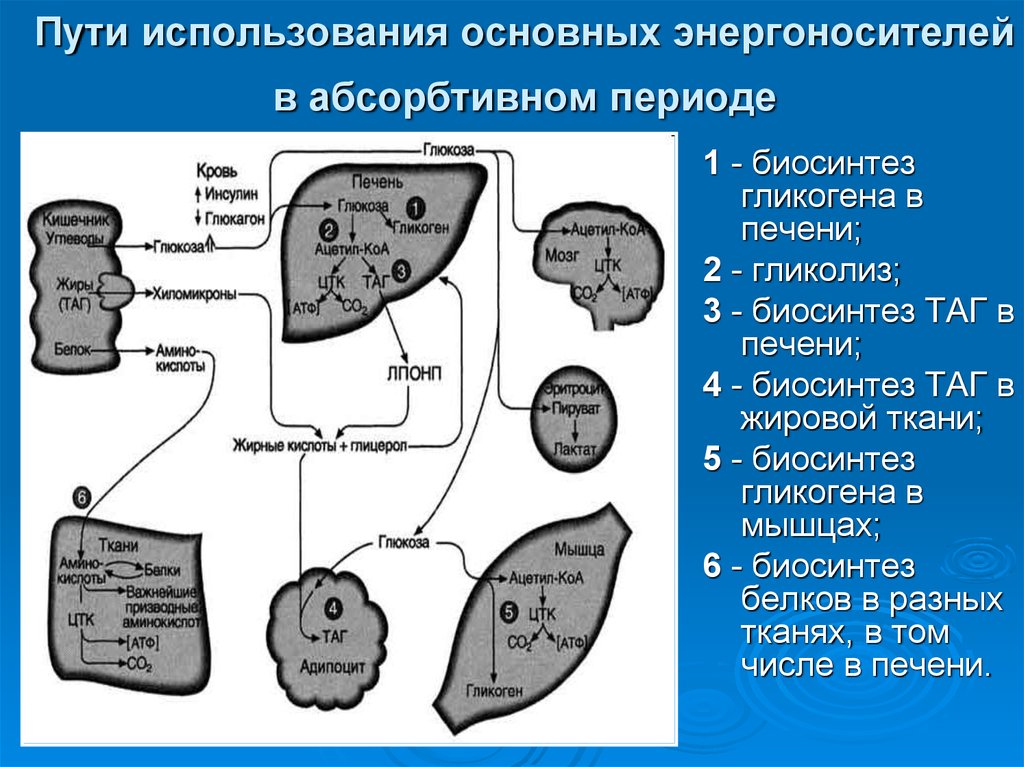
57. Пути использования основных энергоносителей в абсорбтивном периоде
1 - биосинтезгликогена в
печени;
2 - гликолиз;
3 - биосинтез ТАГ в
печени;
4 - биосинтез ТАГ в
жировой ткани;
5 - биосинтез
гликогена в
мышцах;
6 - биосинтез
белков в разных
тканях, в том
числе в печени.
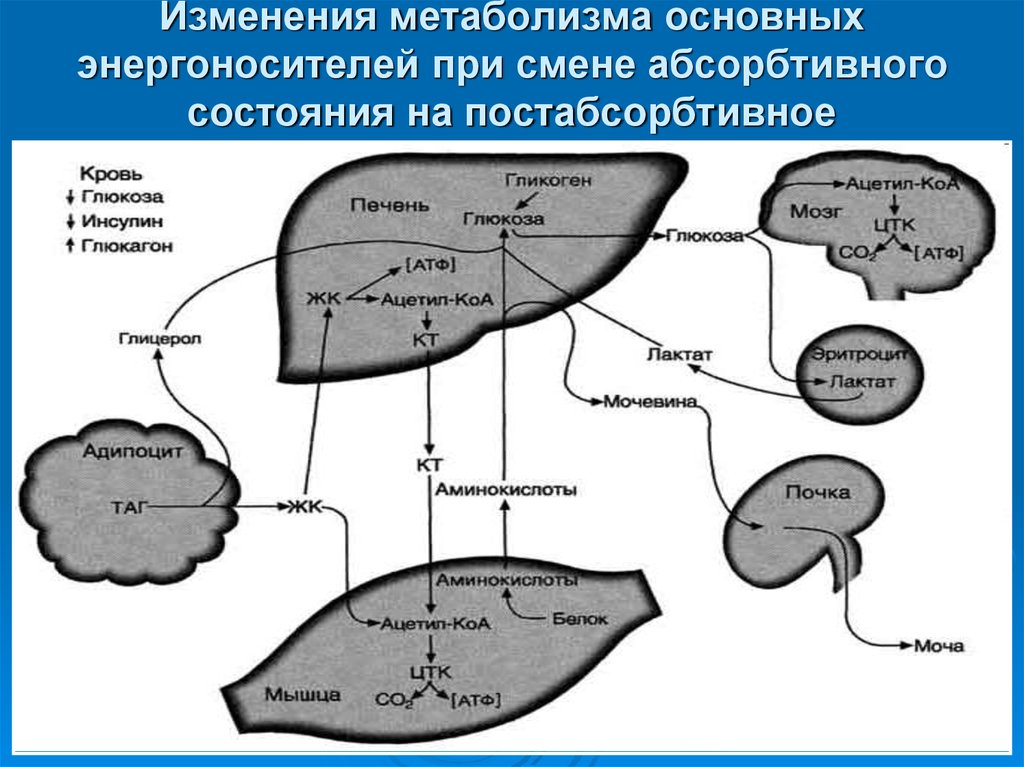
58. Изменения метаболизма основных энергоносителей при смене абсорбтивного состояния на постабсорбтивное
59. Изменение гормонального статуса и метаболизма при голодании
Голодание может быть кратковременным, в течение суток (I фаза),продолжаться в течение недели (II фаза) или нескольких недель (III
фаза).
В отсутствие пищи в крови снижается уровень глюкозы, аминокислот и
триацилглицеролов.
Инсулинглюкагоновый индекс снижается, и повышается концентрация
контринсулярных гормонов, в первую очередь кортизола. В этих
условиях возникает состояние, для которого характерно преобладание
процессов катаболизма жиров, гликогена и белков на фоне общего
снижения скорости метаболизма.
Под влиянием контринсулярных гормонов в этот период происходит
обмен субстратами между печенью, жировой тканью, мышцами и
мозгом. Этот обмен служит двум целям:
1) поддержанию концентрации глюкозы в крови для обеспечения
глюкозозависимых тканей (мозга, эритроцитов);
2) мобилизации других источников энергии, в первую очередь жиров,
для обеспечения энергией всех других тканей. Вследствие
переключения метаболизма на режим мобилизации энергоносителей
даже после 5-6 нед голодания концентрация глюкозы в крови
составляет не менее 60 мг/дл.
60.
1. Обмен углеводов Так как за счёт мобилизации гликогена обеспечиваетсятолько кратковременное голодание, основным источником глюкозы при длительном
голодании служит глюконеогенез, а основными субстратами глюконеогенеза аминокислоты, лактат и глицерол. При низкой концентрации инсулина глюкоза
используется только инсулиннезависимыми тканями, в основном мозгом,
эритроцитами.
2. Обмен жиров Жирные кислоты,становятся основными источниками энергии для
большинства органов в первый период голодания. Во II фазе мобилизация жиров
продолжается, и концентрация жирных кислот в крови увеличивается в 3-4 раза по
сравнению с постабсорбтивным состоянием. Синтез кетоновых тел начинается в
первые дни голодания. Во II фазе голодания скорость синтеза кетоновых тел
значительно возрастает. Концентрация кетоновых тел в крови в этот период может
достигать 20-30 мг/дл (в норме 1-3 мг/дл). Используются кетоновые тела, в основном,
в мышцах. В этот период голодания часть энергетических потребностей мозга
обеспечивается кетоновыми телами, а скорость окисления кетоновых тел в мышцах
снижается.
3. Обмен белков В течение нескольких первых дней голодания быстро распадаются
мышечные белки - основной источник субстратов для глюконеогенеза. При голодании
более 3 нед скорость катаболизма белков стабилизируется и составляет примерно 20
г в сутки. В этот период увеличивается потребление мозгом кетоновых тел, а скорость
глюконеогенеза снижается. Снижение скорости глюконеогенеза способствует
сбережению белков. В этот период и для мозга кетоновые тела становятся
значительным источником энергии. Однако для окисления кетоновых тел необходимы
оксало-ацетат и другие компоненты ЦТК. В норме они образуются из глюкозы и
аминокислот, а при голодании - только из аминокислот. При продолжительности
голодания более 4 недель развиваются атрофические процессы, в результате
которых происходит потеря значительного количества белков. В теле человека
массой 70 кг масса белков составляет 15 кг. При потере 1/3-1/2 белков наступает
смерть.
61. Изменения метаболизма при гипо- и гиперфункции коры надпочечников
Заболевания коры надпочечников могут проявиться симптомамикак гипо-, так и гиперпродукции гормонов.
Большинство клинических проявлений надпочечниковой
недостаточности обусловлено дефицитом глюкокортикоидов
и минералокортикоидов.
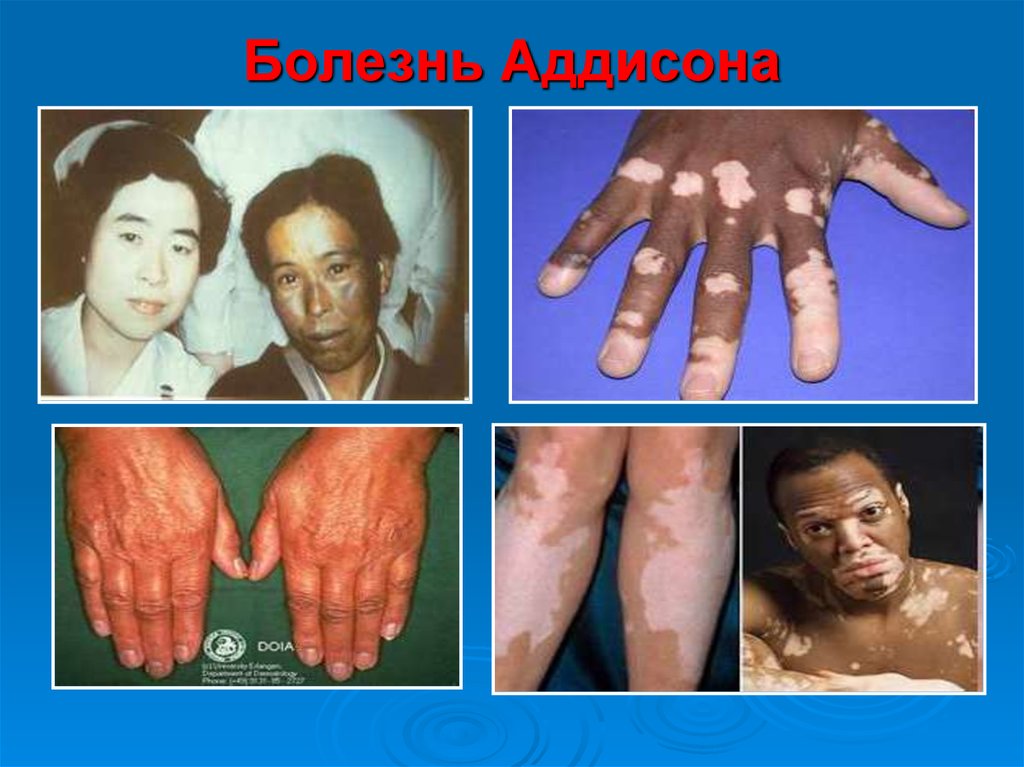
Первичная недостаточность надпочечников (болезнь Аддисона) развивается в
результате поражения коры надпочечников туберкулёзным или аутоиммунным процессом.
Основные клинические проявления выражаются в снижении массы тела, общей слабости,
снижении аппетита, тошноте, рвоте, снижении АД и типичной для первичной
надпочечниковой недостаточности гиперпигментацйи кожи ("бронзовая болезнь") . Причина
гиперпигментации - повышение продукции ПОМК - предшественника АКТГ и
меланоцитстимулирующего гормона.
Вторичная недостаточность надпочечников может развиться при дефиците АКТГ, что, в
свою очередь, может быть следствием опухоли или инфекционного поражения гипофиза. При
вторичной недостаточности надпочечников, отсутствует гиперпигментация.
При врождённой гиперплазии надпочечников нарушается синтез кортизола. В 95%
случаев при этой патологии обнаруживается дефект 21-гидроксилазы (реже 11-гидроксилазы).
Снижение продукции кортизола сопровождается увеличением секреции АКТГ, накоплением
промежуточных продуктов синтеза кортикостероидов, в частности, предшественников
андрогенов. Избыток андрогенов ведёт к усилению роста тела, раннему половому созреванию
у мальчиков и развитию мужских половых признаков у девочек (адреногенитальный синдром).
При частичной недостаточности 21-гидроксилазы у женщин может нарушаться
менструальный цикл.
62. Болезнь Аддисона
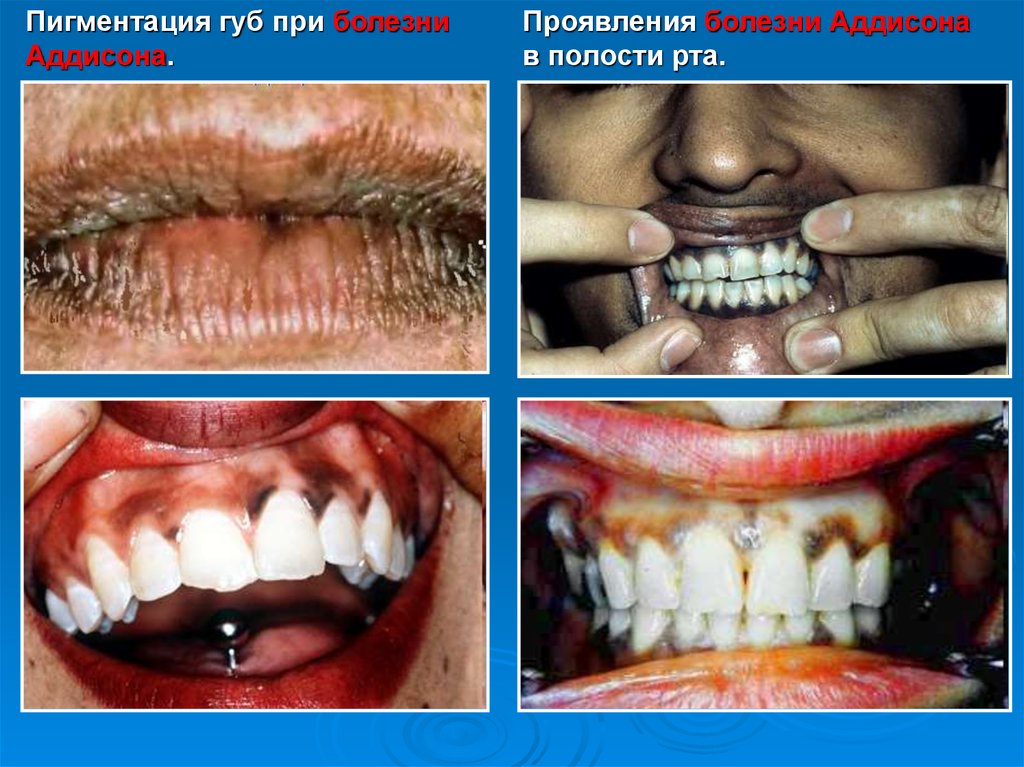
63.
Пигментация губ при болезниАддисона.
Проявления болезни Аддисона
в полости рта.
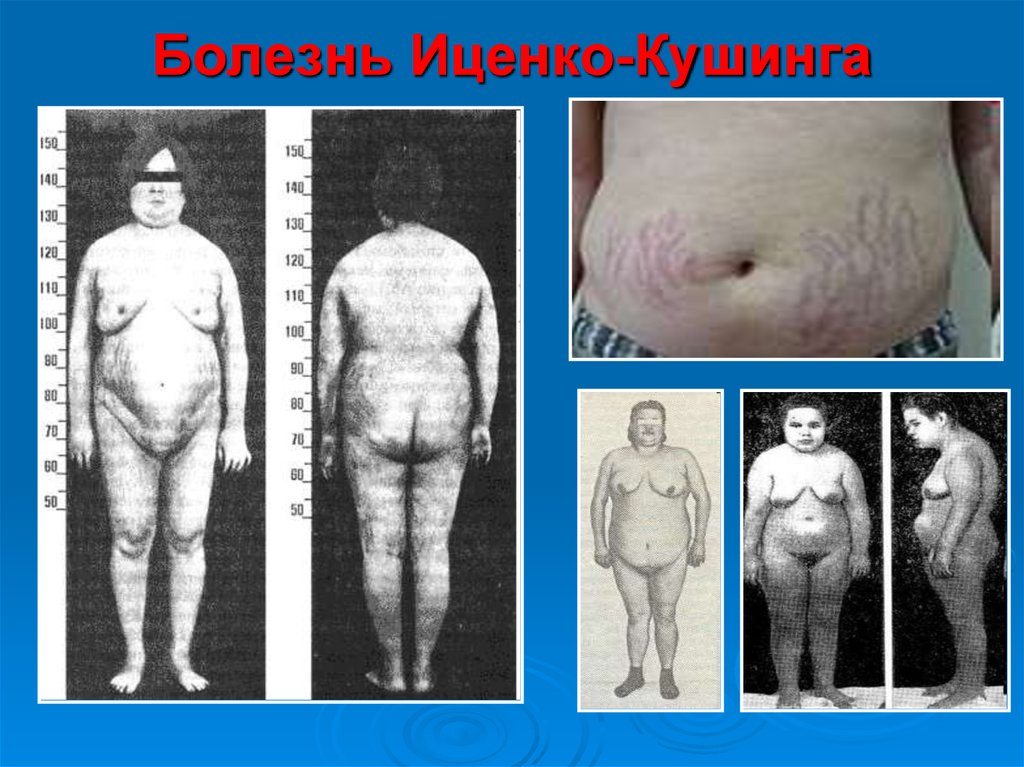
64. Гиперпродукция глюкокортикоидов (гиперкортицизм)
может быть следствием повышения уровня АКТГ при опухолях гипофиза (болезньИценко-Кушинга) и опухолях других клеток (бронхов, тимуса, поджелудочной
железы), вырабатывающих кортикотропинподобные вещества, или избыточного синтеза
кортизола при гормонально-активных опухолях коры надпочечников (синдром
Иценко-Кушинга).
При гиперкортицизме наблюдаются гипергликемия и снижение толерантности к глюкозе,
обусловленные стимуляцией глюконеогенеза ("стероидный диабет"), усиление
катаболизма белков, уменьшение мышечной массы, истончение кожи, остеопороз,
инволюция лимфоидной ткани. Характерно своеобразное перераспределение
отложений жира ("лунообразное лицо", выступающий живот). Гипернатриемия,
гипертензия, гипокалиемия обусловлены некоторой минералокортикоидной активностью
кортизола, которая проявляется при его избытке.
Для выявления первичной причины гиперкортицизма, помимо определения
концентрации АКТГ в плазме крови, используют тесты с применением высоких доз
синтетического глюкокортикоида дексаметазона (структурного аналога кортизола).
Дексаметазон подавляет секрецию АКТГ по механизму отрицательной обратной связи.
Для болезни Иценко-Кушинга характерно снижение концентрации кортизола после
применения дексаметазона более чем на 50%. Отсутствие реакции на введение
дексаметазона может указывать на наличие опухоли надпочечников или
внегипофизарной секреции АКТГ.



































 biology
biology