Similar presentations:
Лекция 3. Химическое равновесие
1. Лекция 3
Лекция3
ХИМИЧЕСКОЕ
РАВНОВЕСИЕ
2. План
3.1. Кинетическое итермодинамическое описание
химического равновесия
3.2. Смещение химического
равновесия (принцип Ле
Шателье).
3.3. Равновесие в биосредах.
3.
3.1 Обратимыминазываются химические
реакции и физико-химические
процессы, самопроизвольно
протекающие как в прямом,
так и в обратном направлении
4.
аА + вВ ⇄ сС + dDN2 + 3 H2
⇄ 2 NH3
NH4Cl + H2O ⇄ NH4 OH + HCl
Hb + O2
⇄ HbO2
5.
Изучая реакции выпадения осадков израстворов,
Бертолле
первым пришел к выводу
об обратимости химических
процессов
К.Л.Бертолле (1748-1822)
6.
Участвуя в Египетском походефранцузской армии как научный
консультант Наполеона, Бертолле
обнаружил отложения Na2CO3 на
берегу озер с соленой водой, что
позволило ему сделать вывод об
обратимости изученной ранее
химической реакции:
Na2CO3 + CaCl2
⇄ CaCO3 + 2 NaCl
7.
Пределом протеканияобратимых процессов
является состояние
химического
равновесия
8.
Химическое равновесие- это такое состояние
обратимого процесса, в
котором скорость
прямой и обратной
реакций равны между
собой.
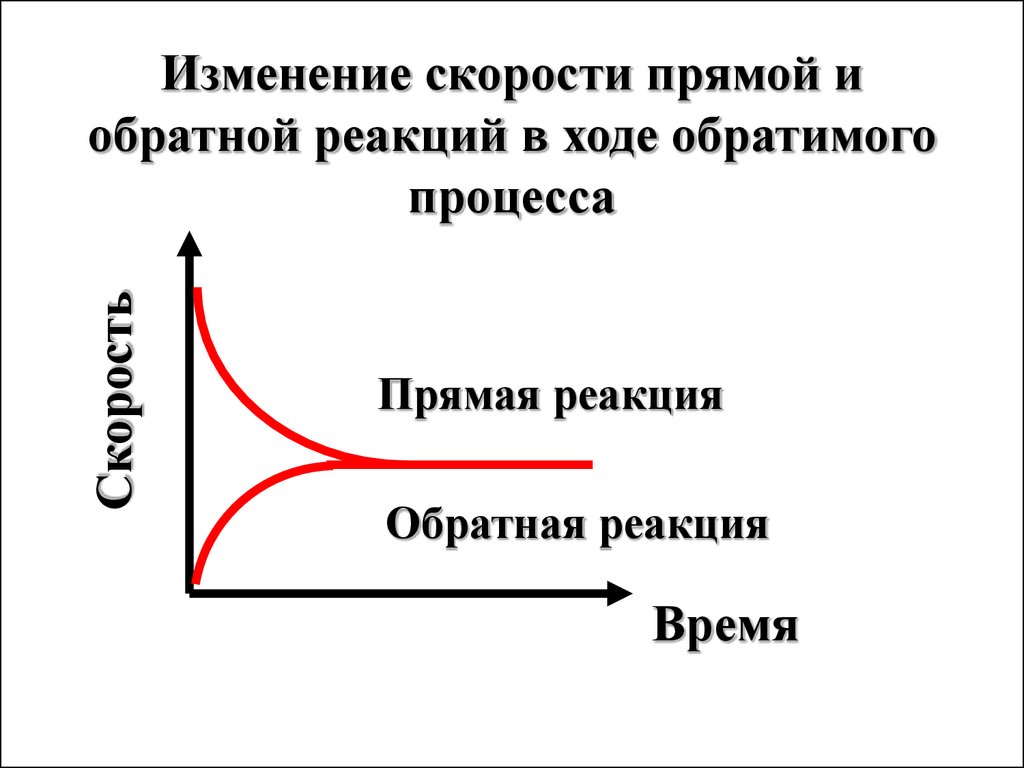
9. Изменение скорости прямой и обратной реакций в ходе обратимого процесса
СкоростьИзменение скорости прямой и
обратной реакций в ходе обратимого
процесса
Прямая реакция
Обратная реакция
Время
10.
Признакомхимического
равновесия является
постоянство во времени
концентраций всех
веществ, участвующих
в процессе.
11.
Концентрации веществв состоянии
химического
равновесия
называются
равновесными: [Ā],
моль/л.
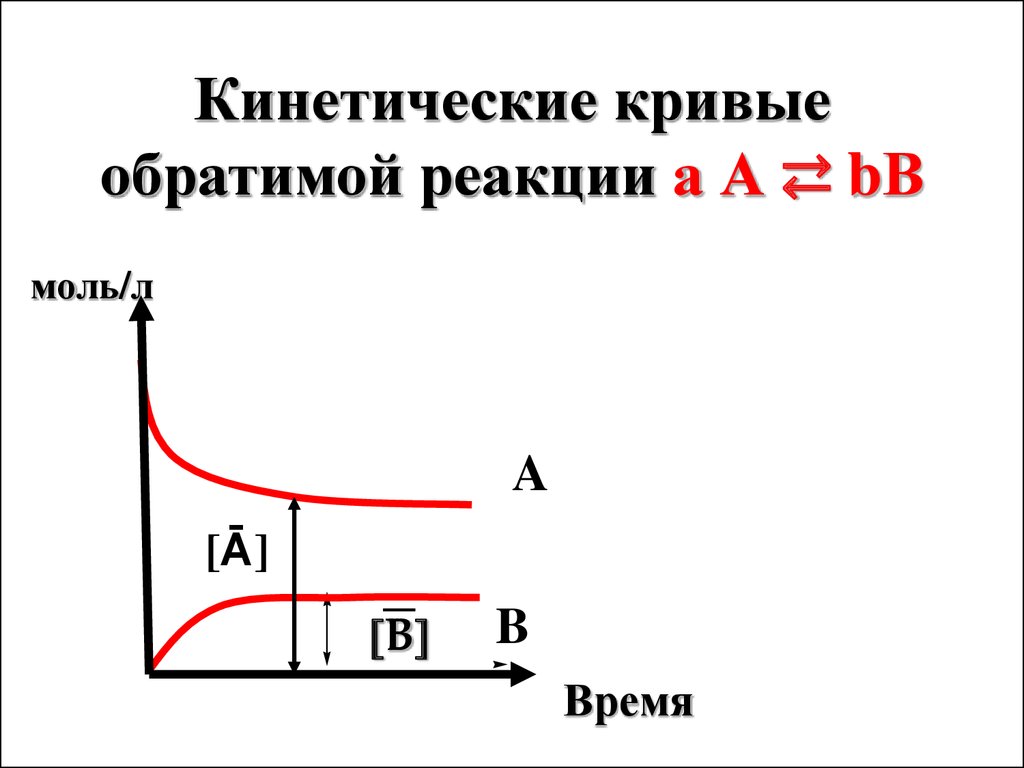
12. Кинетические кривые обратимой реакции а А ⇄ bВ
моль/лA
[Ā]
B
B
Время
13.
Кинетическое описаниехимического равновесия основано
на законе действующих масс:
скорость реакции прямо
пропорциональна
произведению концентраций
реагирующих веществ
(Гульдберг-Вааге,1884)
14.
В состоянии равновесияυпр =
a
kпр[A]
υобр =
c
kобр[C]
b
[B]
d
[D]
k - константа скорости
15. υпр =
Так какυ υ
пр =
обр,
следовательно
kпр_
kобр
=
c
d
[C] [D]
a
b
[A] [B]
16.
kпрkобр
=
Кc
где Kс – концентрационная
константа равновесия
17.
Закон действующихмасс для обратимой
реакции
Kc =
c
[C]
d
[D]
a
[A]
b
[B]
18.
Например:Hb + O2 ⇄ HbO2
[HbO2]
Кс = ----------- = 1300
[Hb][O2]
19.
Если в химическойреакции участвуют
газообразные, жидкие и
твердые вещества, то для
расчета Кс используют
только равновесные
концентрации газов
20.
Например:CO2(г) + 2 NH3(г) ⇄H2O (г) + CO(NH2)2 (к)
Kc =
___ H2O ___
2
CO2 × NH3
21.
Для описания обратимыхгазофазных реакций
используют константу
химического равновесия,
обозначаемую Kp:
22.
сК
р
d
рС ×
рD
=
а
рА
b
×
рВ
p – равновесное парциальное
давление газа в смеси
23.
Соотношение Kс и Крописывается уравнением:
Кс = Кр (RT)
(а+b-c-d)
24.
Если К >> 1 →равновесие
смещено
вправо, υпр > υобр;
Если К << 1 →
равновесие
смещено
влево, υпр< υобр
25. В основе термодинамического описания обратимого процесса лежит уравнение изотермы химической реакции
C DRT ln
a
b
A B
c
G G
0
d
26.
Всостоянии
химического
равновесия
Δ G = 0,
а концентрации веществ А, В,
С, D являются равновесными.
Соответственно
o
ΔG
= - RT ln K
- уравнение химического
сродства
27.
Термодинамический расчетконстанты равновесия:
- G0 /RT
K=e
K зависит только от
температуры и природы
реагирующих веществ
28.
3.2 Состояние химическогоравновесия является наиболее
энергетически выгодным
состоянием обратимого
процесса, так как
характеризуется минимальным
запасом внутренней энергии
системы(G min)
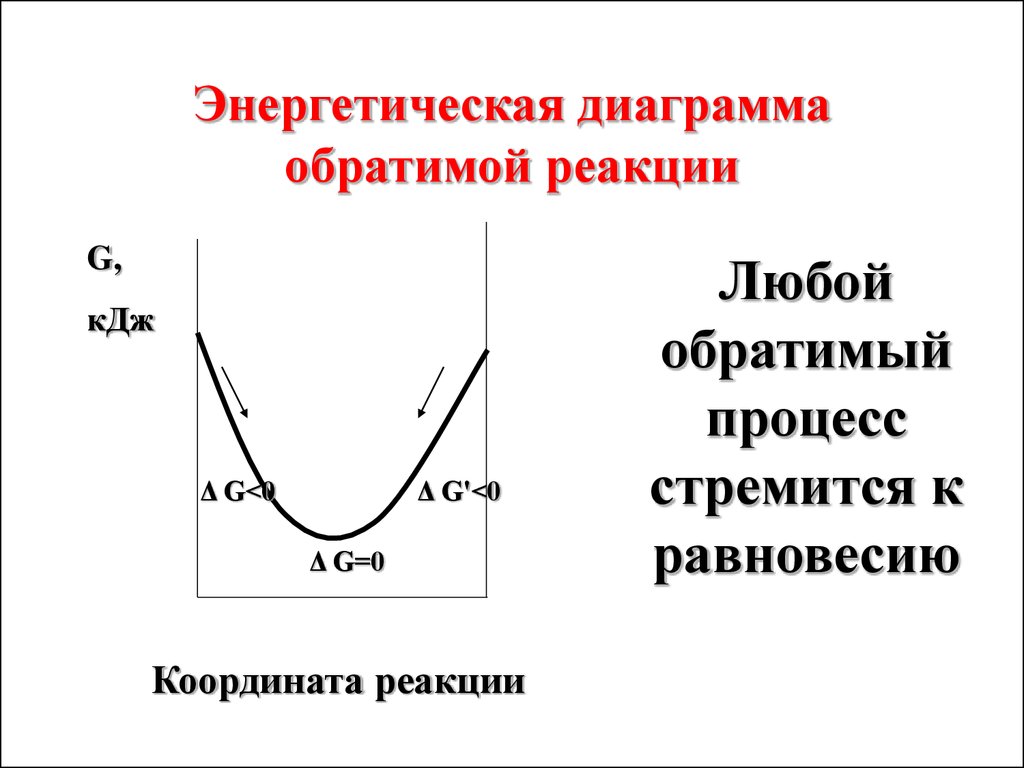
29. Энергетическая диаграмма обратимой реакции
Энергетическая диаграммаобратимой реакции
G,
кДж
Δ G<0
Δ G'<0
Δ G=0
Координата реакции
Любой
обратимый
процесс
стремится к
равновесию
30.
В 1884 г.французский
физико-химик
и металлург
Ле Шателье
сформулировал
общий закон
смещения
химического
равовесия
Анри Луи Ле Шателье
(1850–1936)
31.
Принцип Ле Шателье: «Если насистему, находящуюся в состоянии
химического равновесия, оказать
внешнее воздействие (изменив
температуру, давление или
концентрации веществ), то
положение равновесия сместится
таким образом, чтобы ослабить
внешнее воздействие».
32.
В любом случае равновесие будетсмещаться до тех пор, пока не
наступит новое положение
равновесия, которое соответствует
новым условиям. Этот принцип
позволяет предсказать
качественные изменения в
равновесной системе при
изменении условий
33.
Частные случаи принципаЛе Шателье
A)повышение температуры
смещает равновесие в сторону
эндотермической, а
понижение температуры - в
сторону экзотермической
реакции
34.
Смещение равновесия in vivoHb + O2 ⇄ HbO2,
Δ rН = - 10 кДж
При повышении температуры
равновесие смешается влево (кровь
отдает кислород тканям), при
понижении температуры
равновесие смещается вправо
(кровь обогащается кислородом).
35.
Частные случаи принципа Ле ШательеБ) при
повышении давления
равновесие смещается в
сторону меньшего количества
газообразных веществ, а при
понижении давления - в
сторону их большего
количества.
36.
Изменение давления не влияет насмещение химического
равновесия, если:
•В реакции не участвуют газы;
•Реакция протекает без изменения
количества газообразных веществ
N 2 + O2
⇄ 2 NO
37.
Смещение равновесия in vivoHb + O2 ⇄ HbO2
Венозная кровь поступает в легкие, где
испытывает повышенное давлении О2.
В результате равновесие смещается
вправо (кровь насыщается
кислородом). Артериальная кровь,
поступающая в ткани, оказывается при
пониженном давлении кислорода, в
результате чего равновесие смещается
влево (кровь отдает кислород тканям).
38.
Частные случаи принципа Ле ШательеB) при
увеличении
концентрации вещества,
участвующего в обратимом
превращении, равновесие
смещается в сторону той
реакции, которая протекает с
убылью этого вещества (и
наоборот).
39.
Смещение равновесия in vivoHb + O2
⇄ HbO2
При увеличении содержания
гемоглобина в крови равновесие
смещается вправо (ткани
обогащаются кислородом). При
недостатке гемоглобина (анемия)
равновесие смещается влево
(больной страдает от кислородной
недостаточности).
40.
3.3 Важнейшейбиосредой является вода.
Описание процессов,
протекающих в водных
растворах, возможно с
позиций теории
химического равновесия.
41.
Многие процессы,играющие важную роль в
метаболизме живых
организмов, связаны с
обратимым переносом
протонов (протолитические
равновесия).
42.
Диссоциация водыВода – слабый электролит,
диссоциацию которого можно
представить схемой:
H2O ⇄
+
H +
OH
43.
При комнатнойтемпературе из
5 млн. молекул воды
на ионы
диссоциирует только
одна
44.
Поскольку+
H2O >> H ( OH ),
то можно считать, что
H2O = const
45.
Kc =+
H × OH
----------------------------------------------------
Кс [H2O] =
H2O
+
[H ][OH ]
46.
Kс [H2O] = KwKw - ионное произведение воды,
константа равновесия, описывающая
обратимую диссоциацию воды.
Кw =
+
[H ][OH ]
(t =
o
25 C)
=
-14
10
47.
Для воды и водных растворов:+
H
Kw
------- OH
=
OH
=
Kw
-------- H+
48. Диссоциация слабых кислот
Диссоциация слабых кислотCH3COOH⇄ CH3
Ka =
COO
+H
+
H+ × CH3COO-
________________________________
CH3COOH
Ka - константа равновесия, называемая
константой кислотности
49.
Диссоциация слабых основанийNH4OH
⇄
+
NH4 +
NH4 ×
+
Kb =
OH
OH
NH4OH
Kb-константа равновесия,
называемая константой
основности
50.
Чем больше Ка иKb, тем сильнее
диссоциируют
кислоты и
основания в
водных растворах
51. Гидролиз (гидролитическое разложение) – это реакция разложения сложных веществ на более простые под воздействием воды
Гидролиз(гидролитическое
разложение)
– это реакция разложения
сложных веществ на более
простые под воздействием
воды
52. Гидролиз солей - это реакция ионного обмена между составными частями соли и воды, протекающая с изменением кислотности раствора
53.
Гидролиз соли, образованнойслабым основанием и
сильной кислотой
NH4Cl+ H2O ⇄ NH4OH + HCl
NH4
+
+ H2O ⇄ NH4OH +
+
H
54.
Кг ==
NH4OH × H+
__________________________________
NH4+
NH4OH ×Kw
________________________________
NH4+ × OH-
=
Kw
=
___________
Kb
Кг – константа равновесия,
называемая константой гидролиза
55.
Гидролиз соли, образованнойслабой кислотой и сильным
основанием
CH3COONa + H2O
⇄ CH3COOH + NaOH
CH3COO- + H2O
Кг =
⇄ СH3COOH + OHKw
Ka
56.
Гидролиз соли, образованнойслабым основанием и слабой
кислотой
CH3COONH4 + H2O
Кг =
⇄ NH4OH + CH3COOH
Kw
Ka × Kb
57.
Способность соли к гидролизухарактеризуется при помощи
степени гидролиза (h):
h=
Количество гидролизуемой соли
_______________________________________________________________________________________________
Общее количество соли в
растворе
58.
h = √ Кг / CMЧем больше константа
гидролиза, тем сильнее
гидролизуется соль.
59.
Гидролиз солей один из факторов,регулирующих
кислотность
внутренней среды
организма.
60.
Благодаримза
внимание!!!









































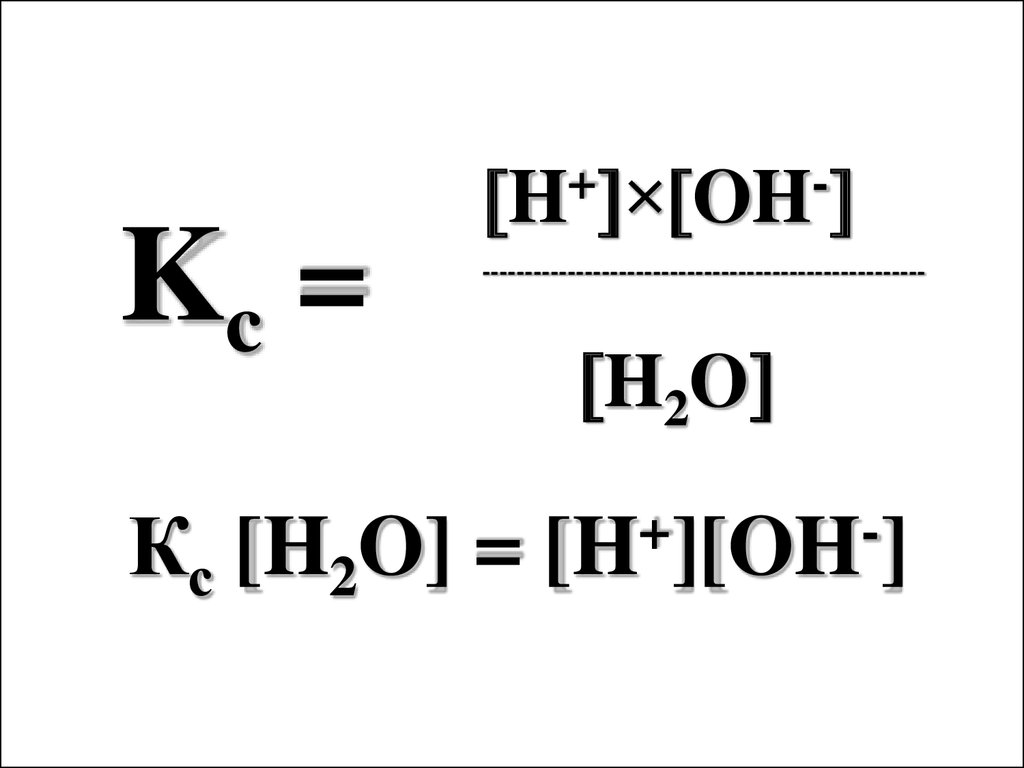















 chemistry
chemistry








