Similar presentations:
Микробиология
1.
ГОСУДАРСТВЕННЫЙ МЕДИЦИНСКИЙ УНИВЕРСИТЕТ Г.СЕМЕЙВыполнила:Жумаканова Т.М
Специальность: Стоматология
Дисциплина: Микробиология
Проверила:Заворохина О.А
Семей 2016
2.
1.Введение2.Основная часть
2.1Исторические этапы развития
микробиологии
2.2Молекулярно-генетические методы
2.3Генная инженерия в медицинской
микробиологии
3.Заключение
4.Список литератур
3.
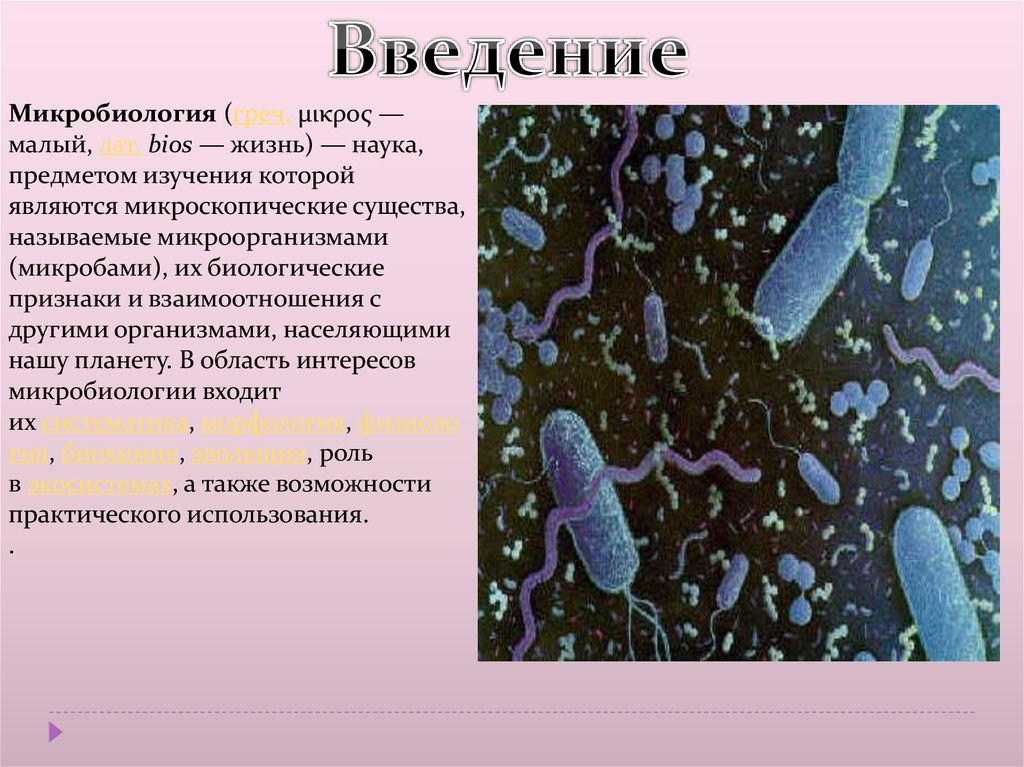
Микробиология (греч. μικρος —малый, лат. bios — жизнь) — наука,
предметом изучения которой
являются микроскопические существа,
называемые микроорганизмами
(микробами), их биологические
признаки и взаимоотношения с
другими организмами, населяющими
нашу планету. В область интересов
микробиологии входит
их систематика, морфология, физиоло
гия, биохимия, эволюция, роль
в экосистемах, а также возможности
практического использования.
.
4.
Историю развития микробиологии можно разделить на 5этапов:
1)ЭВРИСТИЧЕСКИЙ – начинается с момента, когда
Гиппократ (3-4 век до н.э.) высказал догадку (эвретикадогадка, домысел), что болезни передающиеся от человека к
человеку, вызываются невидимыми неживыми веществами
(миазмами). До открытия микробов, люди пользовались
плодами деятельности микробов – виноделие, пивоварение,
сыроделие, выпечка хлеба. В 15 – 16 в Джералимо
Фракасторо, выразил мнение, что вызывают болезни “живые
контагии” передающие болезни через воздух или предметы,
живущие в окружающей среде, для борьбы с болезнями
вызываемом “живыми контагиями” необходимо изолировать
больного, уничтожить контагии.
5.
2) морфологический – с конца 17 – начало 18 века.Левенгук открыл бактерии, создал микроскоп (ув 150-300
раз). Рассматривая (воду, кровь, налет с зубов) он
обнаружил живые микроорганизмы (анималькумосы).
После открытия Левунгука начали открываться новые
бактерии, грибы, простейшие, в конце 19 были открыты
вирусы. В 18 веке в микробиологии зародилась
деонтология. В течении 18-20 столетия были открыты
новые возбудители инфекционных болезней. В 1892
Ивановский открыл царство вирусов (при изучении
мозаичной болезни Шабака).
3) физиологический – после обнаружения микробов, возник вопрос об
их устройсте, биосвойствах, процессах жизнедеятельности, этиологии.
Важную роль в этот период сыграли работы Луи Пастера, он открыл:
природу брожения,
анаэробиоз,
опроверг теорию самозарождения,
основал принцип стерилизации,
разработал принцип вакцинации и способы получения вакцин.
Так же внес свой вклад Роберт Кох: предложил окраску бактерий,
микрофотосъемку, способ получения ЧК. Изучение биологических и
физиологических свойств микроорганизмов продолжалось с конца 19 в и
в течении 20 в.
6.
4) иммунологический – этот период связан с Пастером, Мечниковым иЭрлиха. Их можно называть основоположником иммунологии. Этот период
начался во второй половине 19 в, встал вопрос, как можно защищаться от
патогенных микробов, вызывающих инфекционные болезни. В конце 19 века
Пастер обосновал принцип вакцинации и способ получения вакцины.
Пастер показал, что ослабленный (температурой) возбудитель холеры кур,
бешенства, сибирской язвы, потерявший вирулентные патогенные свойства,
при введение в организм создает специфическую невосприимчивость к
возбудителю. В 1983 Монтанье открыл ВИЧ.
5) молекулярно-генетический – развивался во второй половине 20 веке, в
генетике, биотехнологии, генной инженерии, цитологии дало толчок к
развитии микробиологии и иммунологии (молекул и генетических
аспектов). Была расшифрована молекулярная структура бактерий и вирусов,
строение и состав генома, структура факторов иммунной защиты. В
результате достижения в микробиологии и иммунологии 20 века в
обеспечили успехи в борьбе с инфекционными болезнями, открыли новые
пути и методы диагностики и терапии неинфекционных болезней,
связанных с нарушением иммунной системы.
7.
Молекулярно-генетические методыизучения наследственности человека
– это большая группа методов,
позволяющих выявлять варианты
структуры исследуемого участка
ДНК. В основе методов лежат
различные манипуляции с ДНК и
РНК.
8.
Выделение ДНКПервым этапом любого молекулярно-генетического исследования
является выделение нуклеиновых кислотиз образца ткани. Для
выделения ДНК пригодны любые ядросодержащие клетки
организма. Чаще всего на практике используется периферическая
кровь (лейкоциты).
Выделенная из клеток ДНК представляет собой весь геном организма
(геномная ДНК). Для выделения ДНК применяется обработка крови
солевыми растворами различной концентрации для разрушения
плазматической мембраны и ядерной оболочки и очистка
препаратов. Выделенная ДНК пригодна для любых молекулярногенетических исследований и может продолжительное время
сохраняться в замороженном виде.
В большинстве случаев для анализа (например, для диагностики
болезни) достаточно исследования небольшого фрагмента генома.
Для этого исследуемый фрагмент необходимо получить в большом
количестве копий (амплифицикация). Амплифицировать фрагмент
ДНК можно при помощи методов молекулярного клонирования и
полимеразной цепной реакции (ПЦР).
9.
10.
Полимеразная цепная реакция (ПЦР)Метод амплификации (увеличение количества копий) ДНК invitro.
Метод позволяет в течение нескольких часов получить большое
количество копий исследуемой ДНК.
Возможность осуществления репликации ДНК в пробирке давно
интересовала ученых. Особенно интересной представлялась
возможность накопления большого количества копий ДНК для
последующих исследований. Этот процесс стал возможным после
открытия термостабильной Tag-полимеразыиз термофильных
бактерийThermisaquaticus. Принцип метода ПЦР был разработан
Кэри Мюллисом (США) в 1983 году и в настоящее время используется
как для научных целей, так и для диагностики в практическом
здравоохранении. В основе метода ПЦР лежит комплементарное
достраивание ДНК-матрицы, осуществляемоеinvitroс помощью
фермента ДНК-полимеразы (т.е. осуществляется репликация).
Обычная ДНК-полимераза не может работать при высоких
температурах. Оптимум работыTag-полимеразы находится в области
70-72 С, что позволило сделать процесс репликации циклическим.
При многократном повторении циклов синтеза происходит
экспоненциальное увеличение числа копий специфического
фрагмента ДНК, что позволяет из небольшого количества
анализируемого материала (не определяемое современными
методами) получить достаточное количество копий ДНК для
идентификации их методом электрофореза.
11.
Комплементарное достраивание цепи начинается не в любой точкепоследовательности ДНК, а только в определенных стартовых блоках –
коротких двунитевых участках. При присоединении таких блоков к
специфическим участкам ДНК можно направлять процесс синтеза новой
цепи только в этом участке, а не по всей длине цепи. Для создания
стартовых блоков в заданных участках ДНК используют две
олигонуклеотидные затравки – праймеры. Праймеры комплементарны
последовательностям ДНК на левой и правой границах специфического
фрагмента и ориентированы таким образом, что достраивание новой
цепи ДНК протекает только между ними. Таким образом, метод ПЦР
представляет собой многократное увеличение числа копий
(амплификация) специфического участка ДНК, катализируемое
ферментом ДНК-полимеразой.
12.
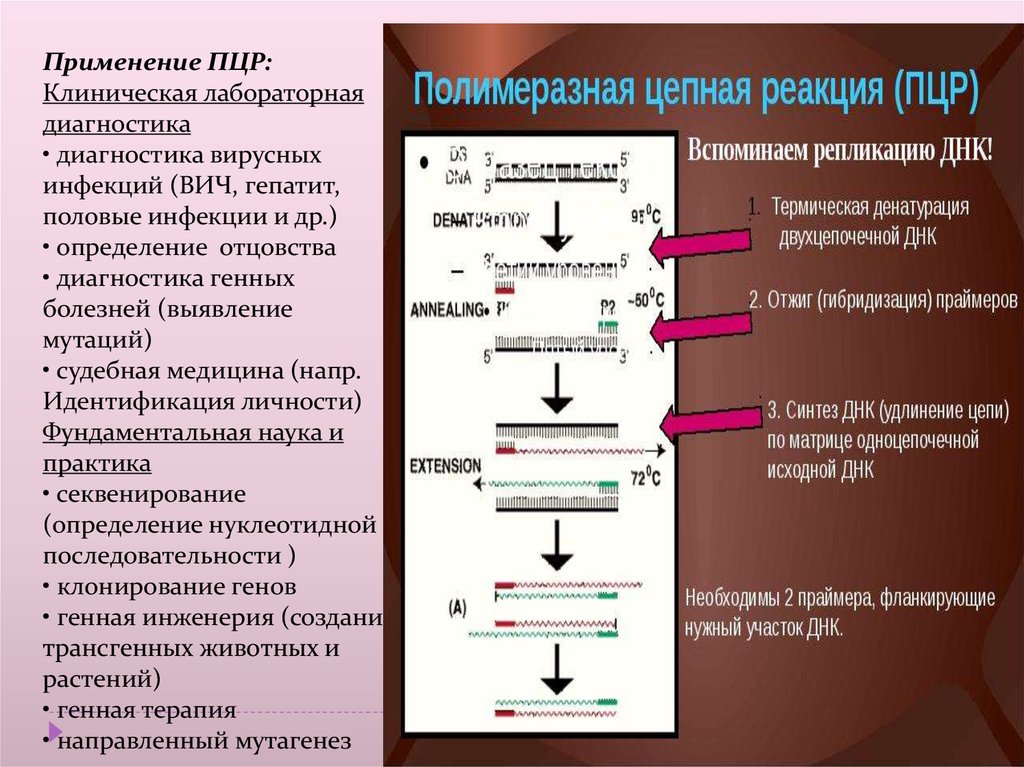
Применение ПЦР:Клиническая лабораторная
диагностика
• диагностика вирусных
инфекций (ВИЧ, гепатит,
половые инфекции и др.)
• определение отцовства
• диагностика генных
болезней (выявление
мутаций)
• судебная медицина (напр.
Идентификация личности)
Фундаментальная наука и
практика
• секвенирование
(определение нуклеотидной
последовательности )
• клонирование генов
• генная инженерия (создание
трансгенных животных и
растений)
• генная терапия
• направленный мутагенез
13.
Генная инженерия в медицинской микробиологииВ медицинской микробиологии все шире используются методы генной инженерии, с
помощью которых «заставляют» микроорганизмы продуцировать нужные
медицинской практике препараты (вакцины, гормоны, интерфероны, цитокины и
др.), путем внесения в их геном соответствующего гена, т.е. получения
рекомбинантного штамма с нужными свойствами путем «направленной»
рекомбинационной изменчивости. Разберем принципиальный алгоритм такого
методы на примере получения рекомбинантной вакцины для профилактики гепатита
В.
А. Из генома вируса гепатита В вырезают ген, детерминирующего синтез HBs-Ag –
белка, индуцирующего иммунный ответ против вируса. Затем внедряют его с
помощью одного из видов рекомбинационной изменчивости в геном дрожжевой
клетки (как вариант может использоваться кишечная палочка).
Б. Затем добиваются манифестациягена – его дерепрессии, так как экзогенный
генетический материал, интегрированный в хромосому, как правило,
репрессируется. С дерепрессированного же гена снимается информация, и
рекомбинантная клетка начинает продуцировать соответствующий белок.
В. Клональная культура, содержащая рекомбинантные клетки, выращивается в
хемостате, где синтезирует большое количество HBs-Ag.
Г. Затем отделяют культуральную среду от микробных клеток и
проводят очистку HBs-Ag.
Д. В результате получается вакцина, содержащая HBs-Ag, но не содержащая ни самих
вирусных частиц, ни их фрагментов.
14.
Микробиология (греч. μικρος — малый, лат. bios —жизнь) — наука, предметом изучения которой
являются микроскопические существа, называемые
микроорганизмами (микробами), их биологические
признаки и взаимоотношения с другими организмами,
населяющими нашу планету. В область интересов
микробиологии входит
их систематика, морфология, физиология, биохимия, э
волюция, роль в экосистемах, а также возможности
практического использования.
15.
1.google2 studfiles.ru












 biology
biology








