Similar presentations:
Теплообмен при фазовых переходах
1.
Теплообмен при фазовых переходахФазовый переход – образование новой фазы при изменении
термодинамических параметров (температуры и/или давления).
Фазовые переходы I рода:
1. Существует теплота перехода
2. Образование границы раздела фаз энергетически выгодно
3. Термодинамические параметры (например, энтальпия) меняются
скачкообразно.
Примеры: парообразование, конденсация, плавление, кристаллизация,
сублимация, десублимация.
Фазовые переходы II рода:
1. Отсутствует теплота перехода
2. Образование границы раздела фаз энергетически невыгодно
3. Термодинамические параметры меняются непрерывно, но их производные
(например, теплоемкость) – скачкообразно.
Примеры: переход из нормального в сверхпроводящее состояние, переход
жидкого гелия из нормального в сверхтекучее состояние.
2.
Межфазная поверхность и ее свойствах
ρ
δ
х
Приближение Гиббса: поверхность не имеет толщины, но обладает
некоторыми избыточными свойствами.
U = U1 + U 2 + U изб
dU изб = TdSизб + s dF + å mi dM iизб
i
S – энтропия, σ – поверхностное натяжение, F – площадь поверхности,
μ и М – химический потенциал и масса i-го компонента.
Поверхностное натяжение зависит от
природы фаз и является функцией
температуры.
d é
-3 2
¢
¢¢
s ( r - r ) ù = const
û
dT ë
3.
Тонкие пленки1
δ = 0,1 – 10 мкм
2
3
Уравнение Гиббса для фазы 2:
dU 2 = TdS 2 - pdV2 + s S dF + å mi dM i
s S = s 12 + s 23
i
При малой толщине переходные слои 1 – 2 и 2 – 3 перекрываются, фаза 2 в
чистом виде не возникает. Тогда в состоянии термодинамического равновесия
12,23
dU = dU1 + dU 3 + dU изб
12,23
1 ¶U изб
p1 = p3 = p2 F2 ¶d
12,23
1 ¶U изб
P=– расклинивающее давление в тонком слое жидкости,
F2 ¶d которое может как способствовать, так и препятствовать
P: d
-3
дальнейшему снижению толщины пленки.
4.
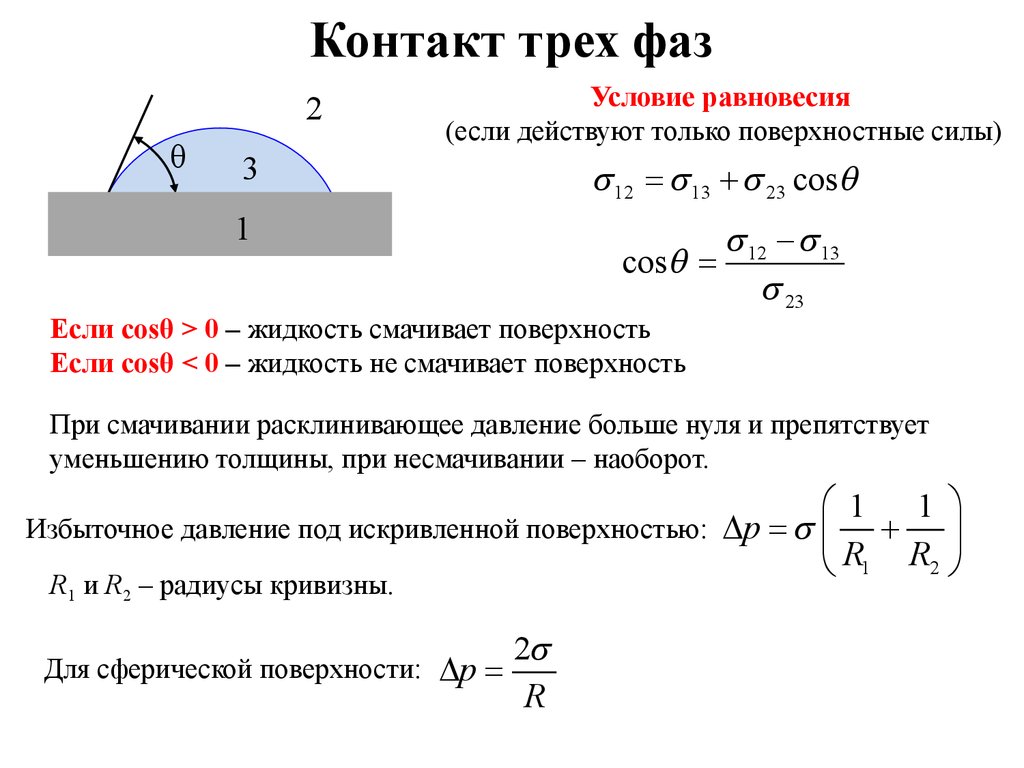
Контакт трех фаз2
θ
Условие равновесия
(если действуют только поверхностные силы)
3
1
s 12 = s 13 + s 23 cosq
cos q =
s 12 - s 13
s 23
Если cosθ > 0 – жидкость смачивает поверхность
Если cosθ < 0 – жидкость не смачивает поверхность
При смачивании расклинивающее давление больше нуля и препятствует
уменьшению толщины, при несмачивании – наоборот.
æ 1
1 ö
Избыточное давление под искривленной поверхностью: Dp = s ç
+ ÷
è R1 R2 ø
R1 и R2 – радиусы кривизны.
2s
Для сферической поверхности: Dp =
R
5.
Часть I.Теплообмен при конденсации
6.
Классификация процессов конденсацииКонденсация – процесс образования
жидкой фазы из газообразной. Возможна
только в докритической области как при
понижении температуры, так и при
повышении давления.
р
тв
ж
г
Т
По месту образования жидкости а) в объеме; б) на поверхности.
В состоянии насыщения
пар и жидкость находятся
в равновесии
Процессы
переноса
невозможны
Для конденсации нужна
температура, которая ниже
температуры насыщения
Для объемной конденсации это температура самого пара, которая должна
быть существенно ниже температуры насыщения. Давление пара должно в
несколько раз превышать давление насыщения!
Для поверхностной конденсации это температура стенки, на которой
конденсируется пар. Требуемая разность температуры стенки и температуры
насыщения существенно ниже, чем при объемной конденсации.
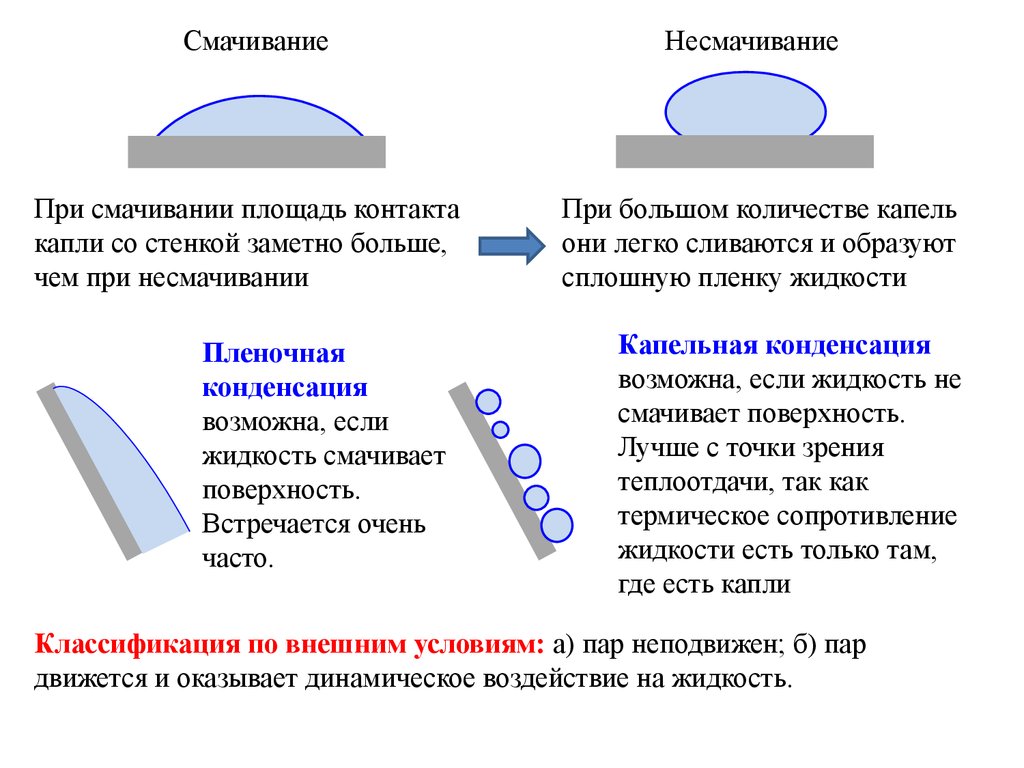
7.
СмачиваниеПри смачивании площадь контакта
капли со стенкой заметно больше,
чем при несмачивании
Пленочная
конденсация
возможна, если
жидкость смачивает
поверхность.
Встречается очень
часто.
Несмачивание
При большом количестве капель
они легко сливаются и образуют
сплошную пленку жидкости
Капельная конденсация
возможна, если жидкость не
смачивает поверхность.
Лучше с точки зрения
теплоотдачи, так как
термическое сопротивление
жидкости есть только там,
где есть капли
Классификация по внешним условиям: а) пар неподвижен; б) пар
движется и оказывает динамическое воздействие на жидкость.
8.
Термические сопротивления приконденсации
Tn - Tcm = R + R
RS =
d
ф
q
Тп
Тпов
Тст
a=
1
RS
Rδ – термическое сопротивление пленки жидкости,
обусловлено конечным значением ее теплопроводности.
Rф – термическое сопротивление фазового перехода, связано
с неравновесностью процессов на межфазной поверхности.
Вблизи поверхности существует слой Кнудсена, в котором приближение
локального термодинамического равновесия не работает!
жидкость
Тпов
слой
Кнудсена
j+
пар
(сплошная
среда)
j – Тп
j = j- - j+ = r - w- - r + w+
r = p RT
j=
pп
2p RTп
w = RT 2p
-
psпов
(T
)
2p RTпов
9.
В общем случае конденсируются не все молекулы пара, падающие намежфазную поверхность. Для учета этого фактора вводят коэффициент
конденсации:
æ
psпов
(T )
pп
j=bç
ç 2p RT
2p RTпов
п
è
b = jконд j-
ö
÷÷
ø
формула
Герца – Кнудсена
Более точные расчеты, учитывающие столкновения в слое Кнудсена (Д.А.
Лабунцов, Т.М. Муратова, 1969):
pп - ps ( Tпов )
b
j=
×
1 - 0, 4 b
2p RTпов
ΔТф
Для воды
6
0,1 атм
4
При атмосферном и более высоком
давлении термическим
сопротивлением фазового перехода
можно пренебречь.
1 атм
2
β
0,01
0,1
Tп - Tпов
<< 1
Tпов
1
Для большинства веществ
коэффициент конденсации по данным
различных экспериментов имеет
слишком большой разброс.







 physics
physics








