Similar presentations:
Биохимия крови. Биохимия печени
1. КУБАНСКИЙ ГОСУДАРСТВЕННЫЙ МЕДИЦИНСКИЙ УНИВЕРСИТЕТ КАФЕДРА ФУНДАМЕНТАЛЬНОЙ И КЛИНИЧЕСКОЙ БИОХИМИИ
Лекция по теме:Биохимия крови-2
Краснодар
2017
2. Плазменные факторы свёртывания крови
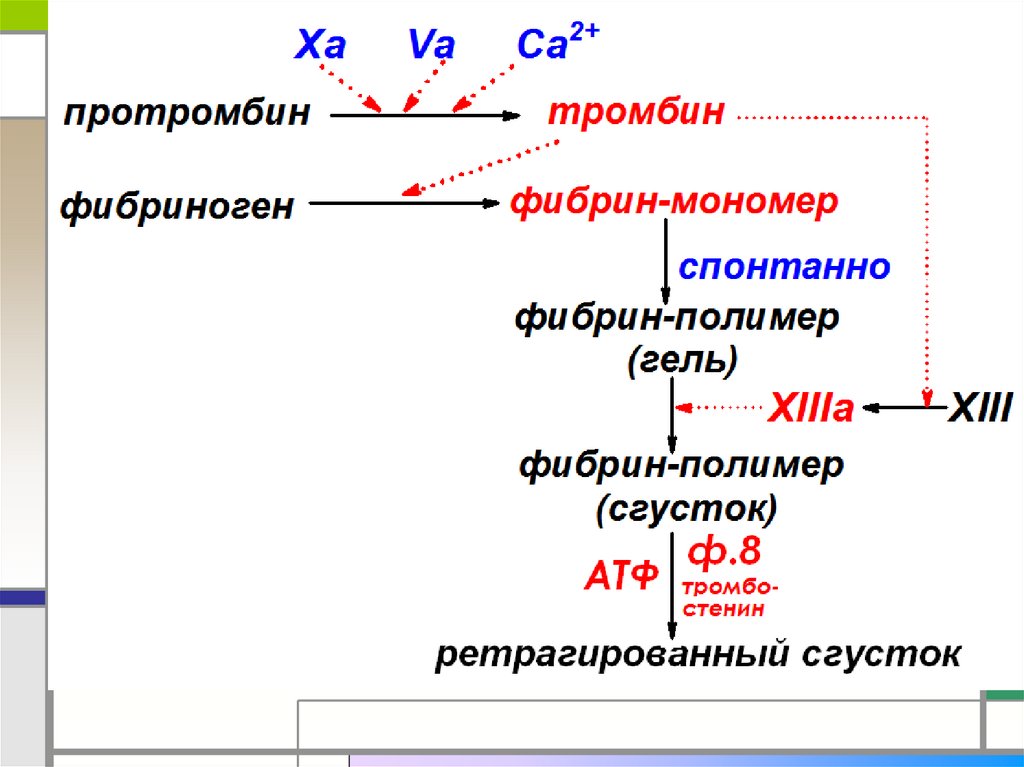
3. Общая схема каскада гемокоагуляции
4.
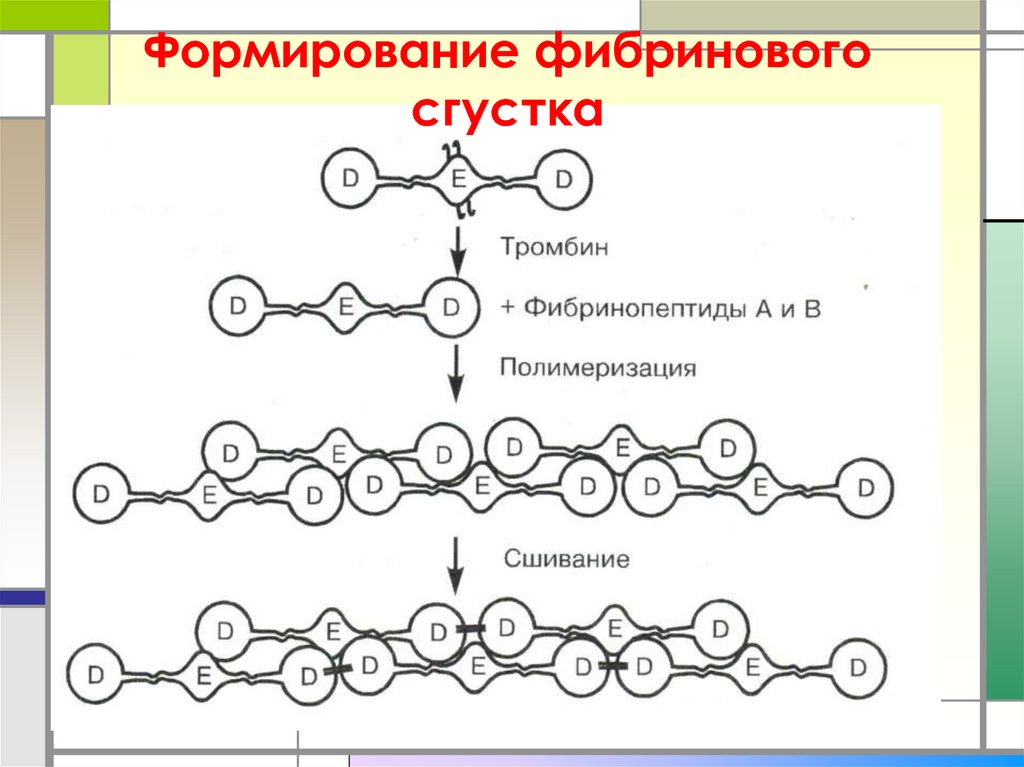
5. Формирование фибринового сгустка
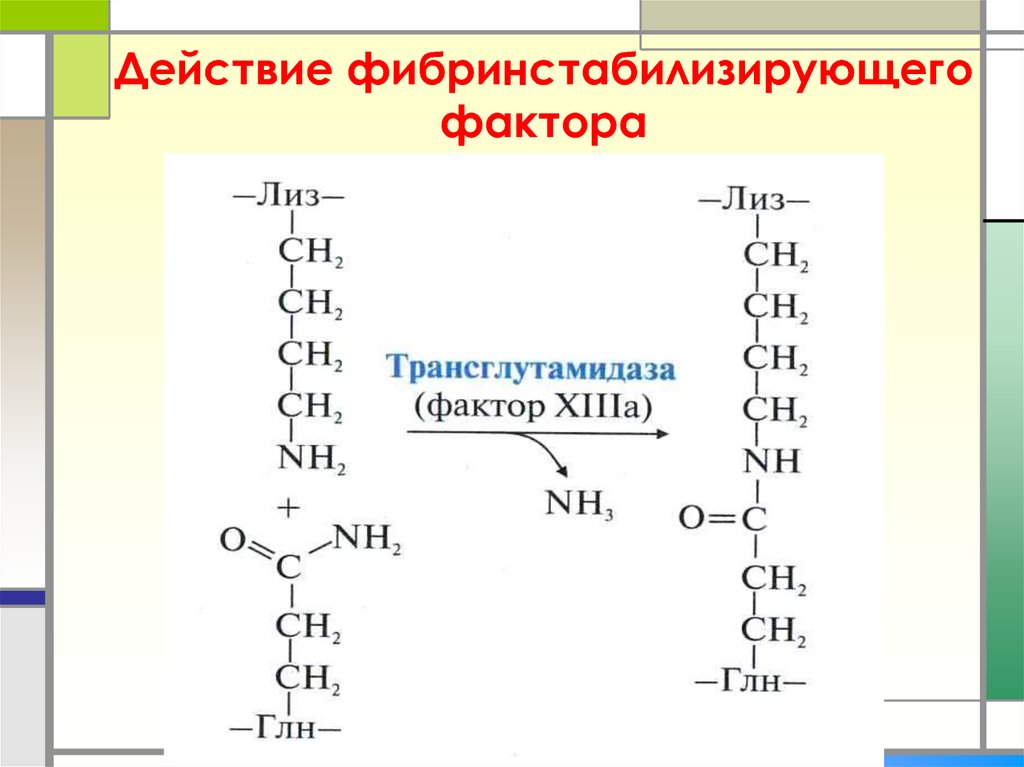
6. Действие фибринстабилизирующего фактора
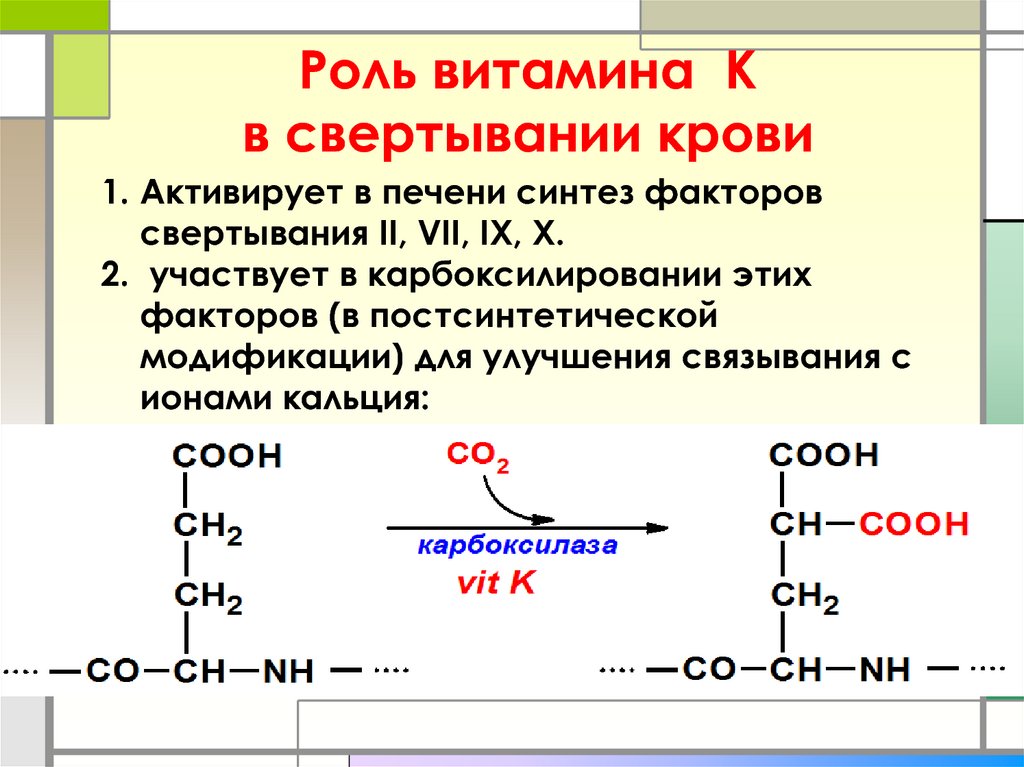
7. Роль витамина К в свертывании крови
1. Активирует в печени синтез факторовсвертывания II, VII, IX, X.
2. участвует в карбоксилировании этих
факторов (в постсинтетической
модификации) для улучшения связывания с
ионами кальция:
8. Антикоагулянтая система
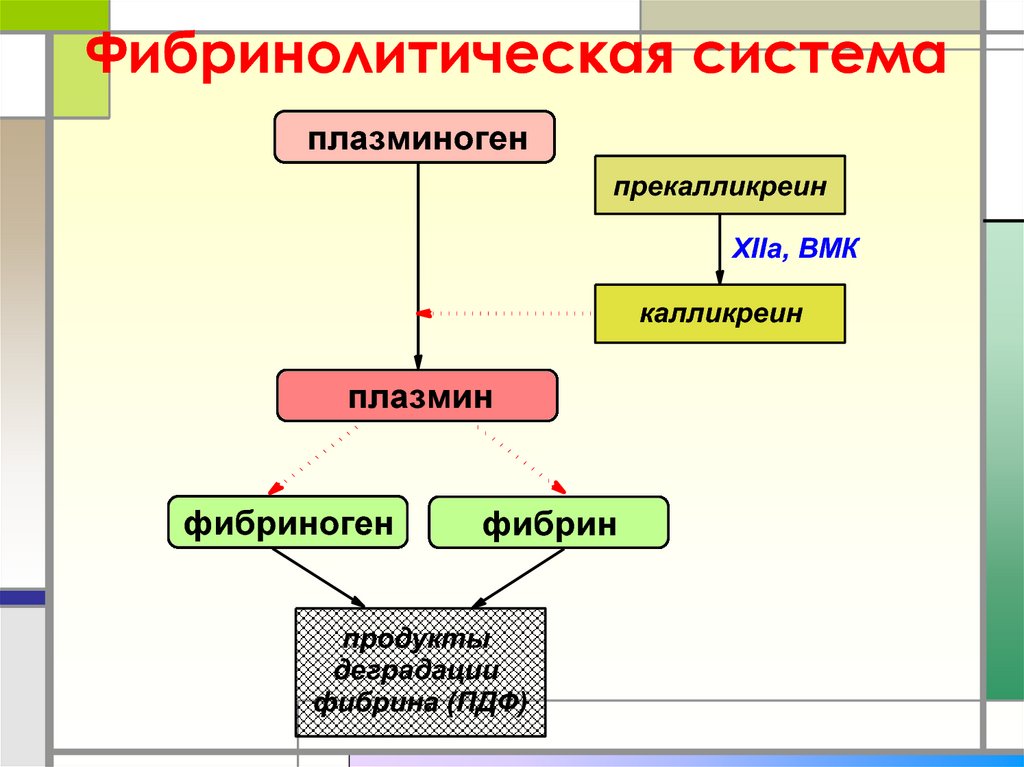
VIIIa9. Фибринолитическая система
плазминогенпрекалликреин
XIIa, ВМК
калликреин
плазмин
фибриноген
фибрин
продукты
деградации
фибрина (ПДФ)
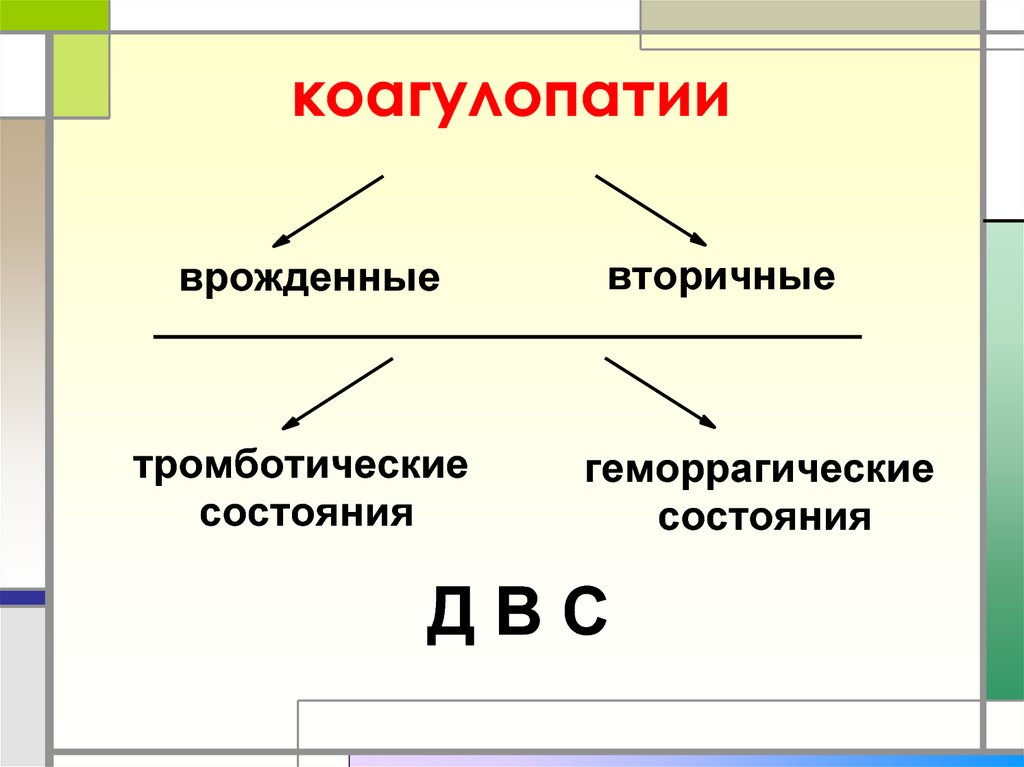
10. коагулопатии
врожденныетромботические
состояния
вторичные
геморрагические
состояния
ДВС
11.
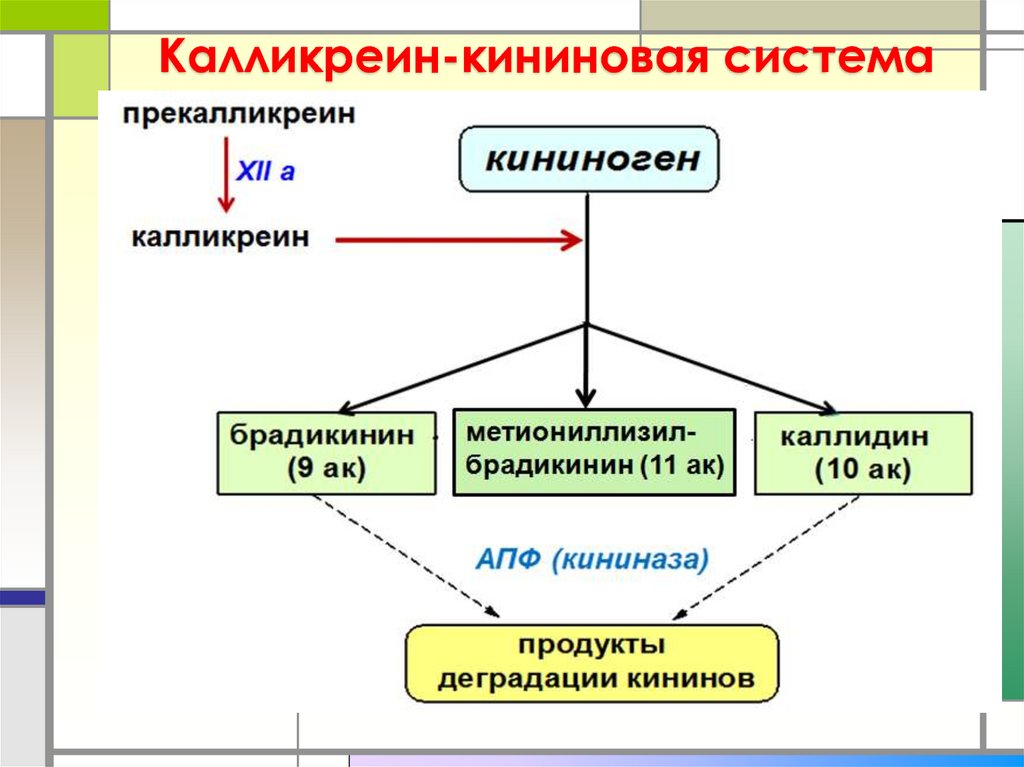
Калликреин-кининовая система12. Роль кининов
□ расширяют сосуды (гипотензивноедействие, снижают АД),
□ оказывают болевой эффект,
□ участвуют в воспалительных реакциях,
□ повышают проницаемость сосудов,
□ способствуют выходу лейкоцитов
(лейкопедез),
□ регулируют деятельность экзокринных
желез,
□ способствуют выработке простагландинов.
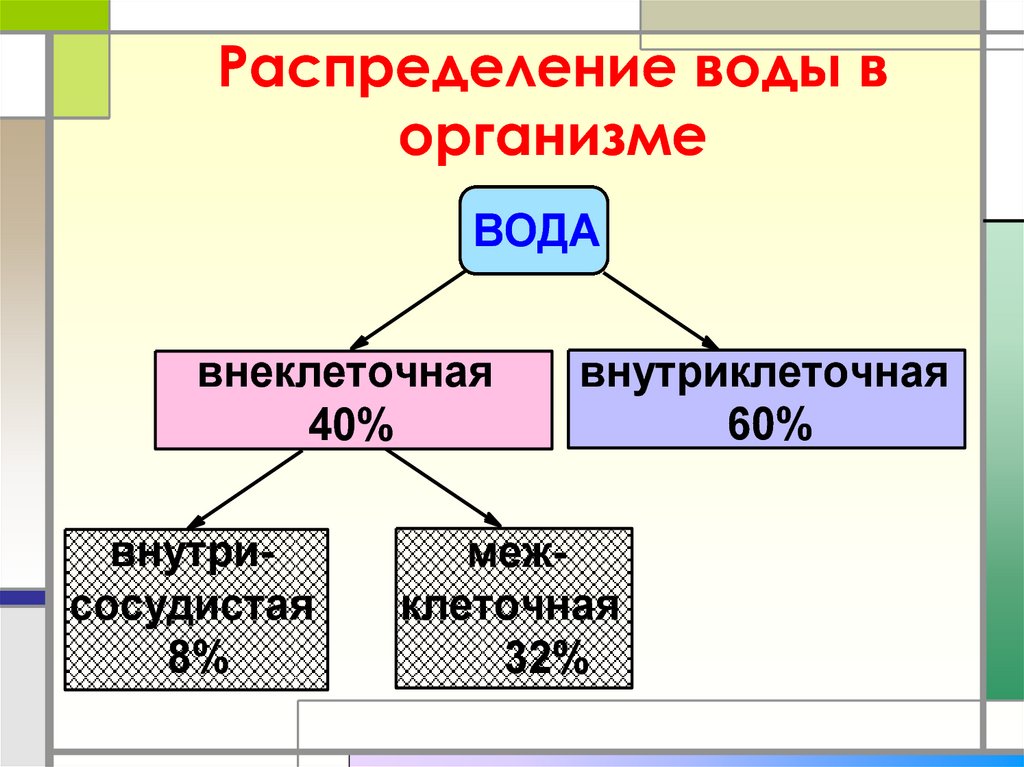
13. Распределение воды в организме
ВОДАвнеклеточная
40%
внутрисосудистая
8%
внутриклеточная
60%
межклеточная
32%
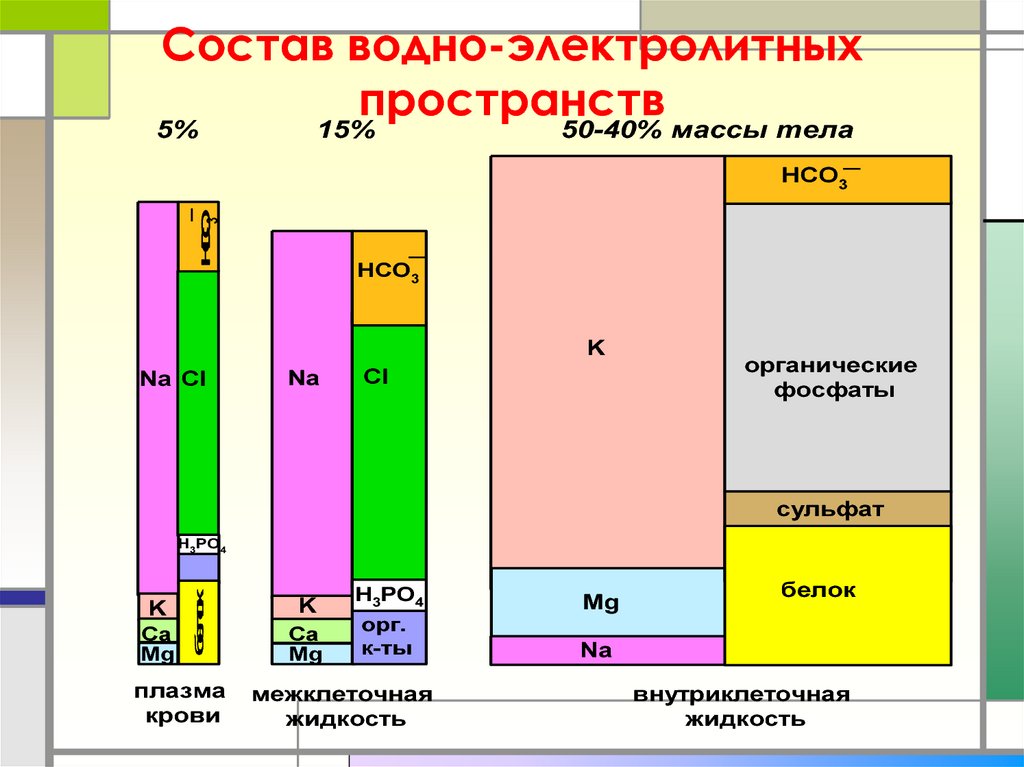
14. Состав водно-электролитных пространств
5%15%
50-40% массы тела
HCO3
HCO3
HCO3
K
Na Cl
Na
Cl
органические
фосфаты
сульфат
K
Ca
Mg
белок
Н3РО4
плазма
крови
K
Ca
Mg
Н3РО4
орг.
к-ты
межклеточная
жидкость
Mg
белок
Na
внутриклеточная
жидкость
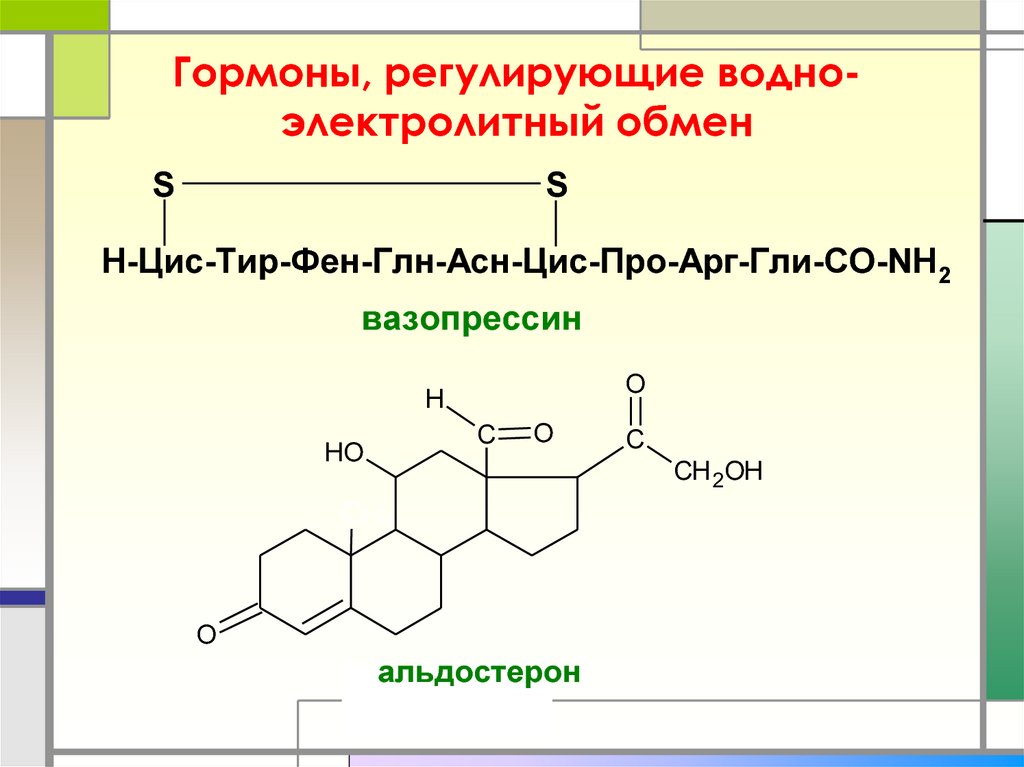
15. Гормоны, регулирующие водно-электролитный обмен
Гормоны, регулирующие водноэлектролитный обменS
S
Н-Цис-Тир-Фен-Глн-Асн-Цис-Про-Арг-Гли-СО-NH2
вазопрессин
O
H
С
HO
O
С
СН 2ОН
CH3
O
альдостерон
альдостерон
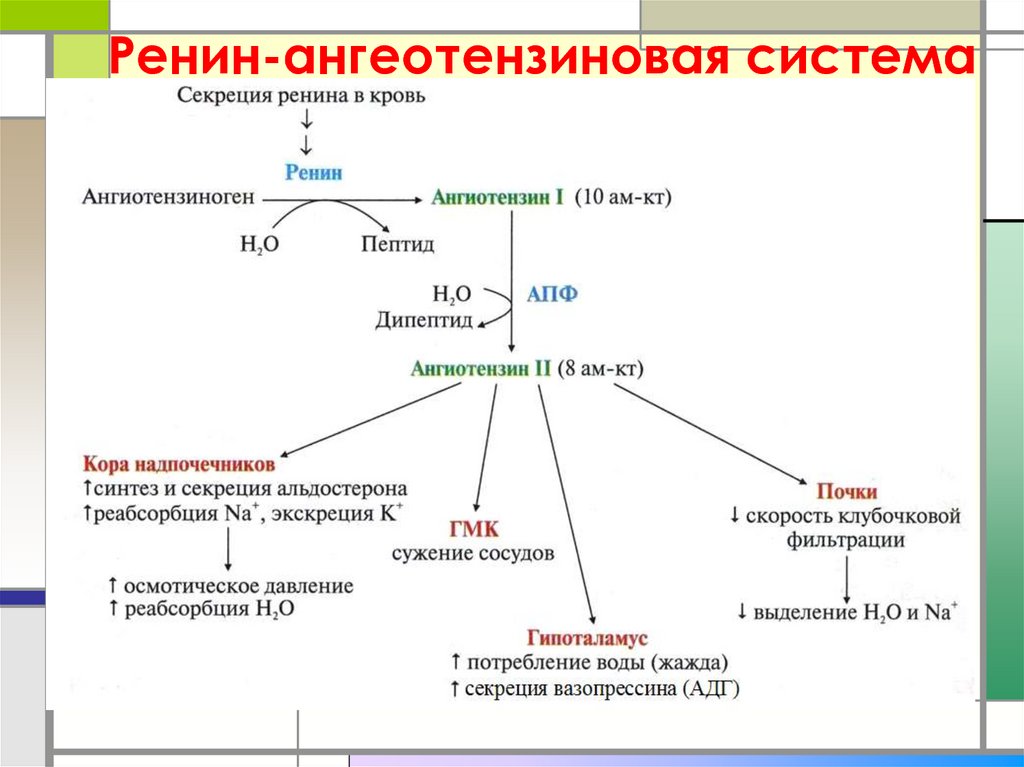
16. Ренин-ангеотензиновая система
17.
18. Основные показатели КОС крови
□ БО (буферные основания)□ СБО
(сдвиг буферных оснований)
44-54 ммоль/л
± 2,5 ммоль/л
□ СБ (стандартный бикарбонат) 21-25 ммоль/л
□ рН
7,36-7,42
19. Механизмы поддержания КОС
□ Буферные системы□ Лёгочный механизм
□ Почечный механизм
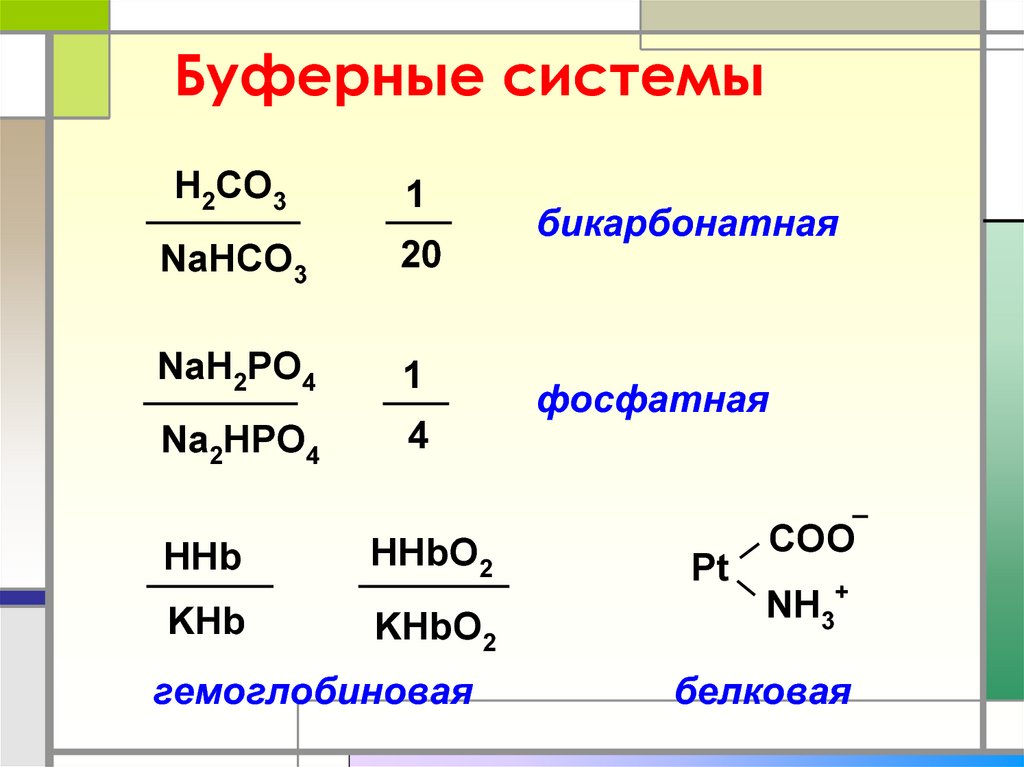
20. Буферные системы
Н2СО31
NaНСО3
20
NaН2PО4
1
Na2НPО4
4
НHb
KHb
НHbO2
KHbO2
гемоглобиновая
бикарбонатная
фосфатная
Pt
COO
NH3+
белковая
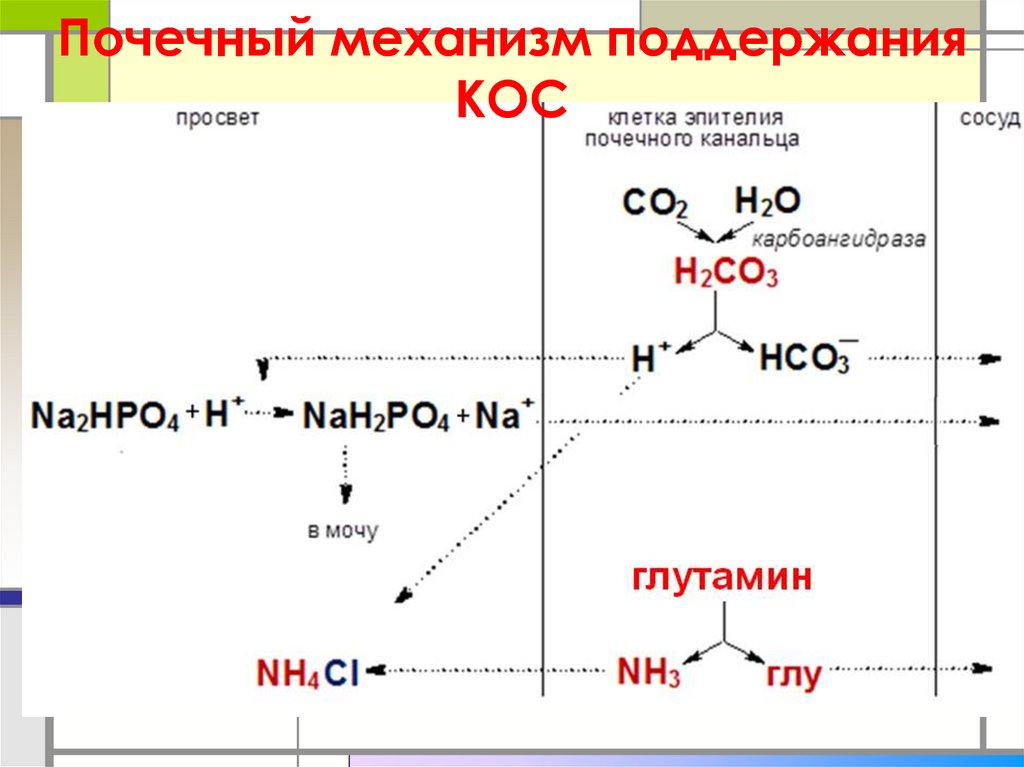
21. Почечный механизм поддержания КОС
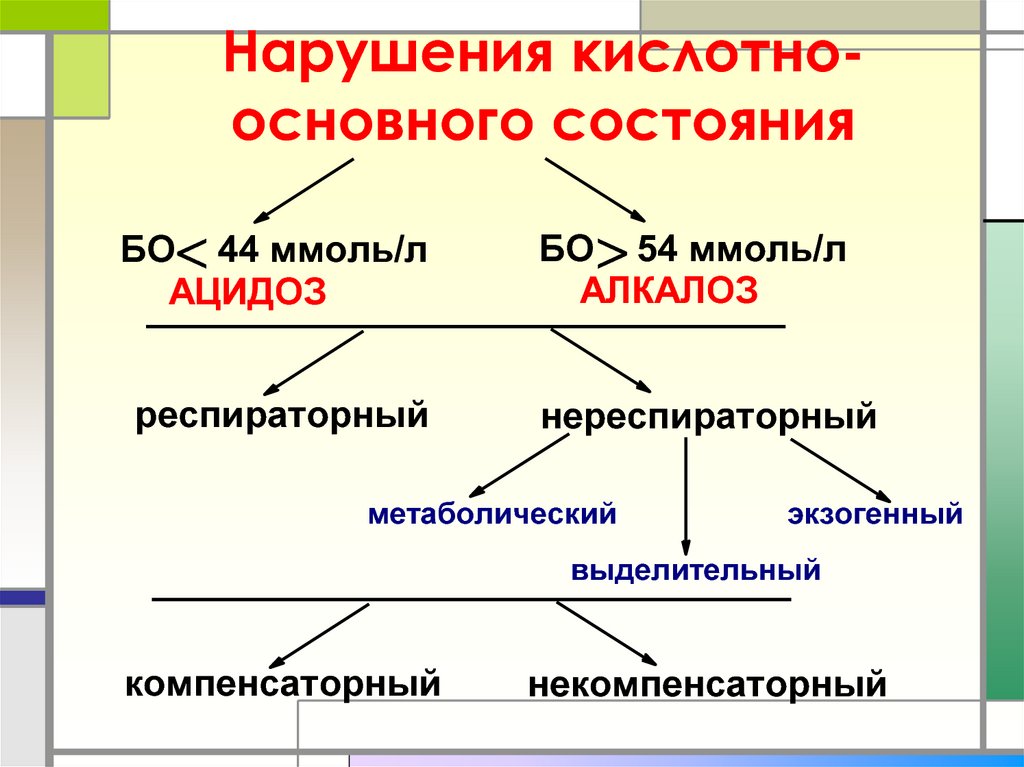
22. Нарушения кислотно-основного состояния
Нарушения кислотноосновного состоянияБО< 44 ммоль/л
АЦИДОЗ
респираторный
БО> 54 ммоль/л
АЛКАЛОЗ
нереспираторный
метаболический
экзогенный
выделительный
компенсаторный
некомпенсаторный
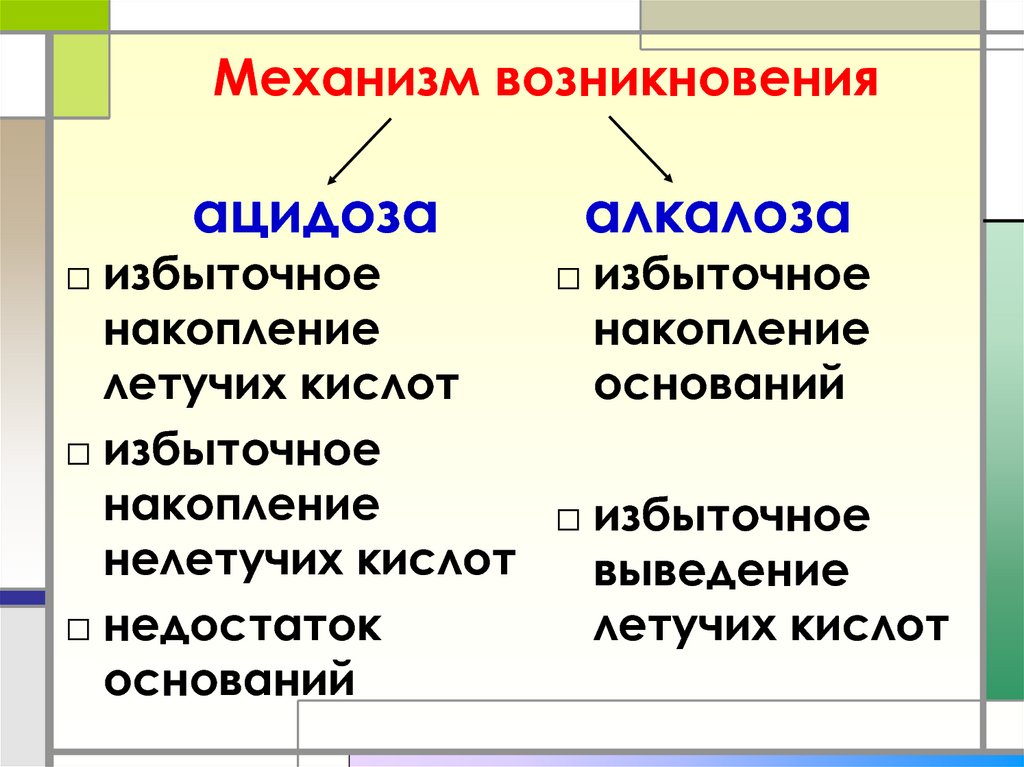
23. Механизм возникновения ацидоза алкалоза
□ избыточное□ избыточное
накопление
накопление
летучих кислот
оснований
□ избыточное
накопление
□ избыточное
нелетучих кислот
выведение
□ недостаток
летучих кислот
оснований
24. Причины нарушений КОС
□ нарушение дыхательнойфункции лёгких
□ нарушение выделительной
функции почек
□ метаболические нарушения в
тканях
□ экзогенные причины
(погрешности питания)
25. КУБАНСКИЙ ГОСУДАРСТВЕННЫЙ МЕДИЦИНСКИЙ УНИВЕРСИТЕТ КАФЕДРА ФУНДАМЕНТАЛЬНОЙ И КЛИНИЧЕСКОЙ БИОХИМИИ
Лекция по теме:Биохимия печени
Краснодар
2017
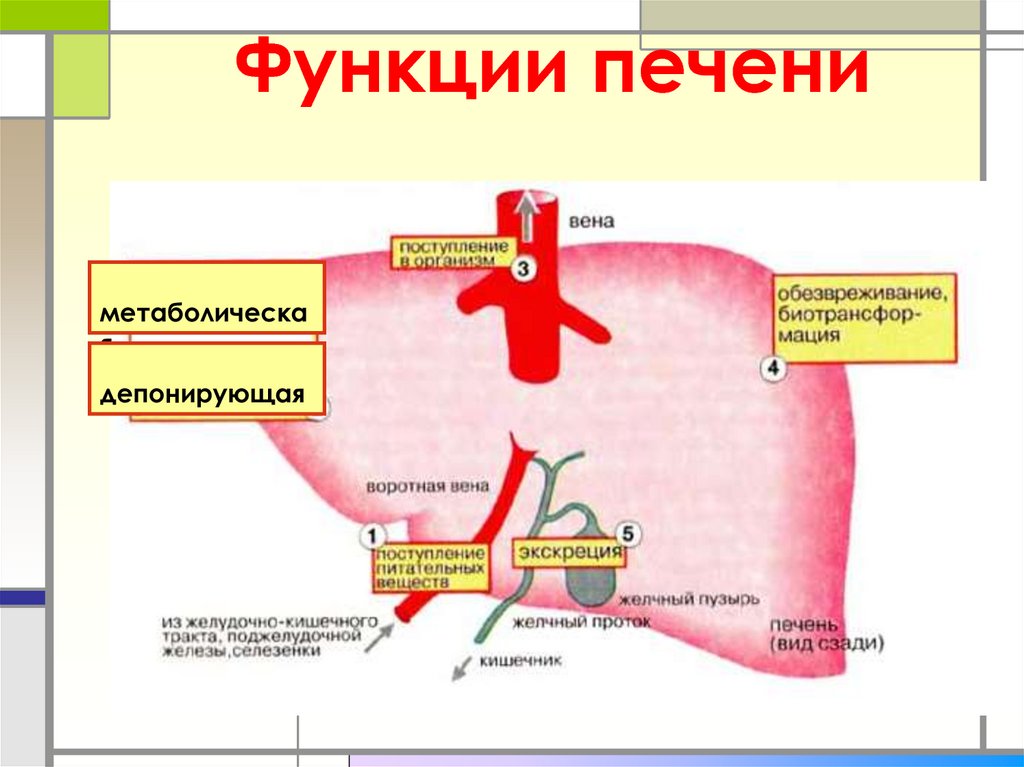
26. Функции печени
метаболическая
депонирующая
27. Роль печени в белковом обмене
□ Синтез собственных белков печени□ Синтез 100% альбуминов и до 90%
глобулинов плазмы крови (в том числе
ферментых системы гемостаза)
□ Синтез апобелков липопротеинов
□ Синтез заменимых аминокислот
□ Процессы трансаминирования,
декарбоксилирования,
трансметилирования
□ Распад и синтез пуриновых и
пиримидиновых нуклеотидов
28. Роль печени в липидном обмене
□ Превращение экзогенных липидов ссобственные (синтез собственных ТАГ и
ФЛ)
□ Синтез холестерина и его этерификация
□ Образование желчных кислот
□ β-окисление жирных кислот
□ Синтез жирных кислот
□ Образование транспортных форм
липидов – ЛПОНП и ЛПВП
□ Синтез кетоновых тел
29. Роль печени в обмене углеводов
□ Гликостатическая функция –поддержание постоянства уровня
глюкозы в крови
□ Синтез и распад гликогена
□ Взаимопревращение моносахаридов
□ Гликонеогенез
□ Окисление глюкозы дихотомическим
путём (2/3) и апотомическим путём
(1/3)
30. Обезвреживающая функция печени
Вещества, обезвреживаемые впечени:
Собственные (эндогенные):
□ конечные продукты метаболизма (NH3,
продукты гниения аминокислот),
□ промежуточные метаболиты,
□ биологически активные вещества
(гормоны, биогенные амины)
Экзогенные (ксенобиотики):
□ яды,
□ лекарства
31. Стадии обезвреживания
1. Метаболическая(окисление, восстановление, гидролиз)
2. Конъюгация (объединение с
эндогенными молекулами или
группами):
Ацетильная (с ацетил-КоА)
Метильная (с SAM)
Глутатионовая
Аминокислотная (с Гли или Глн)
Сульфатная (с ФАФС)
Глюкуронидная (с УДФГК)
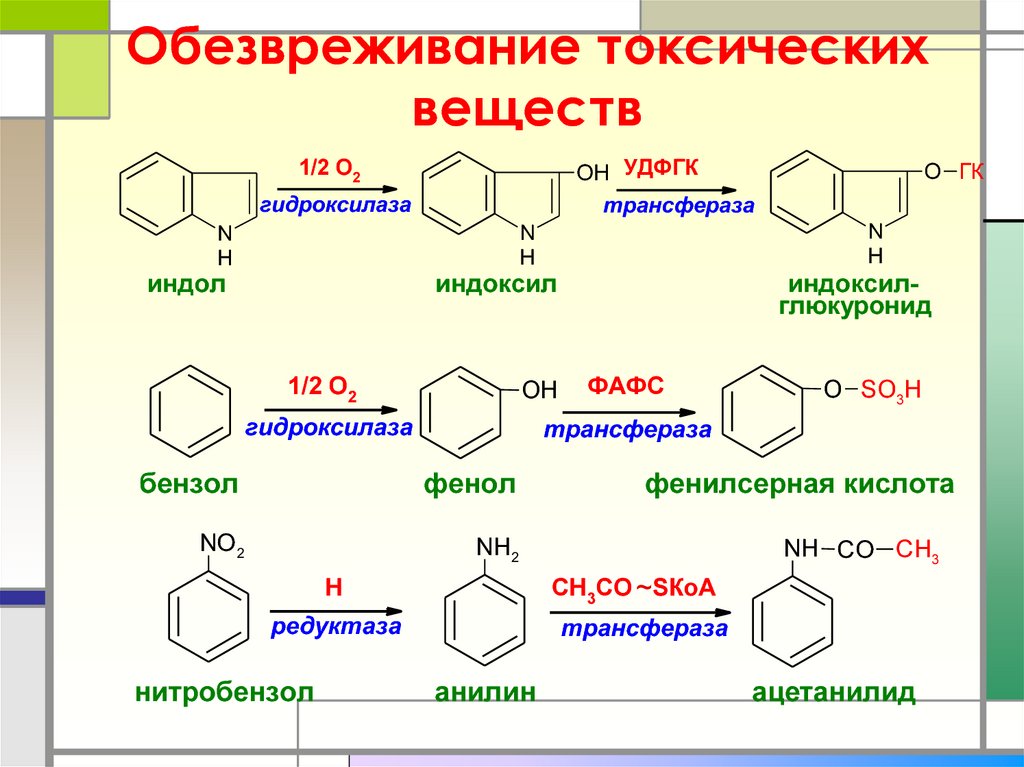
32. Обезвреживание токсических веществ
1/2 О2OH УДФГК
трансфераза
гидроксилаза
N
H
N
H
N
H
индол
индоксил
1/2 О2
OH
гидроксилаза
индоксилглюкуронид
ФАФС
O SO3H
трансфераза
бензол
фенол
NO 2
NH2
Н
фенилсерная кислота
NH СО СН3
СН3СО ~SКоА
редуктаза
нитробензол
O ГК
трансфераза
анилин
ацетанилид
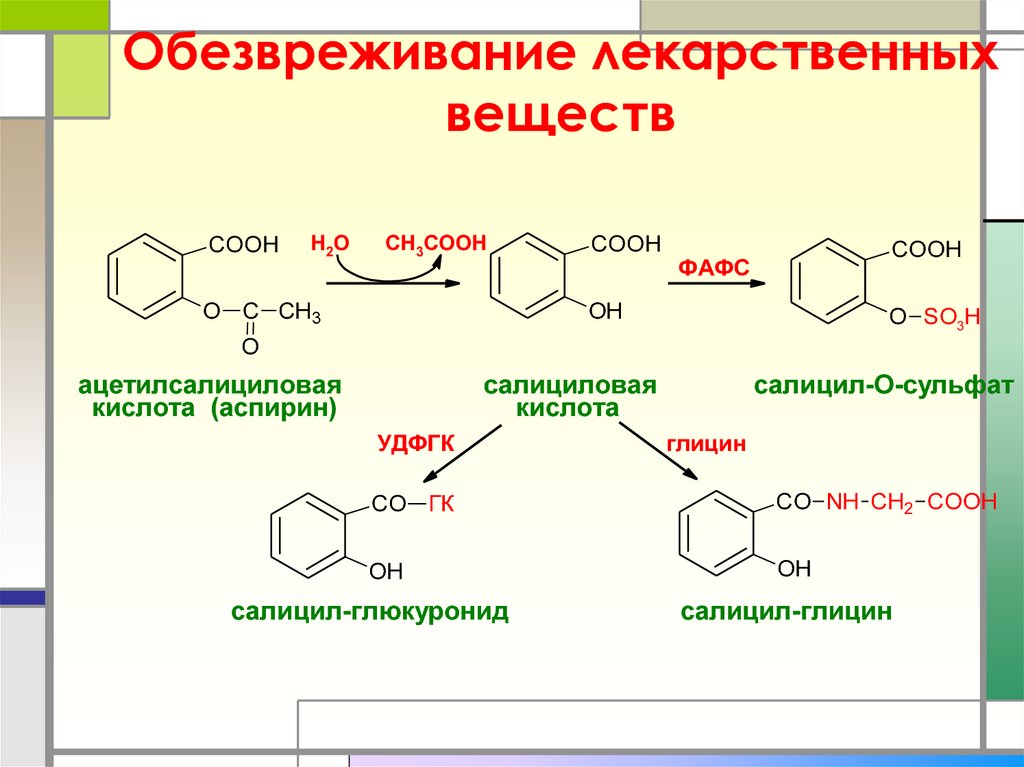
33. Обезвреживание лекарственных веществ
COOHН2О
СН3СООН
O С CH3
COOH
COOH
ФАФС
OH
O SO3H
O
ацетилсалициловая
кислота (аспирин)
салициловая
кислота
УДФГК
салицил-О-сульфат
глицин
CO ГК
CO NH СН2 COOH
OH
OH
салицил-глюкуронид
салицил-глицин
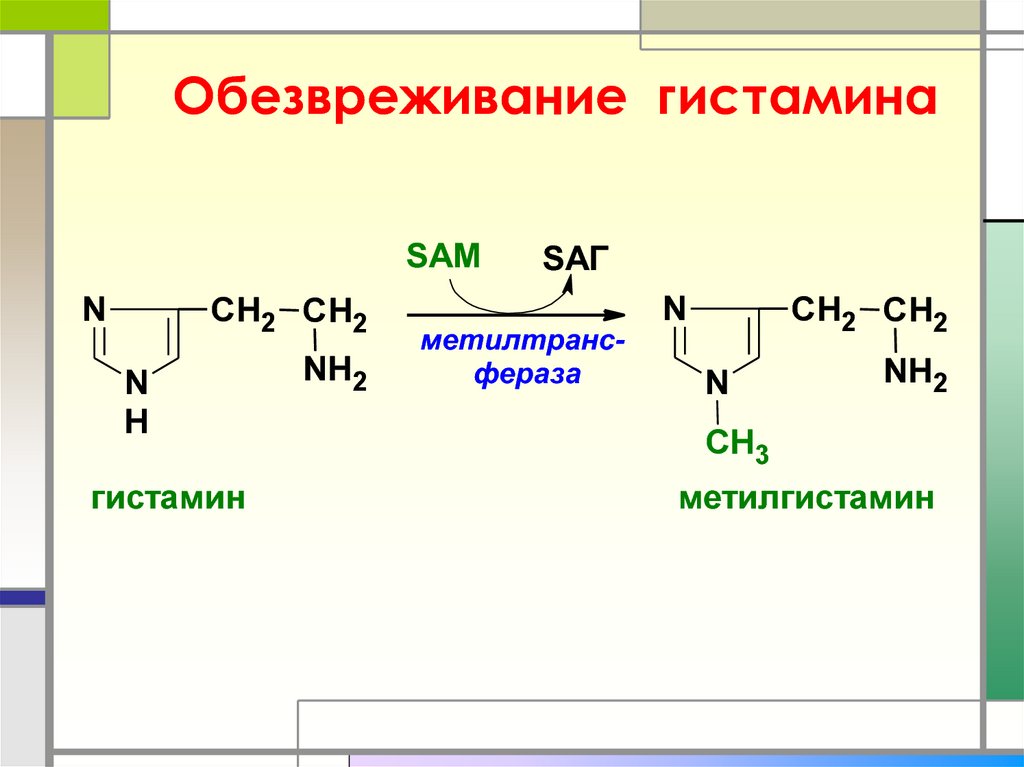
34. Обезвреживание гистамина
SAМСН2 СН2
N
N
H
гистамин
NH2
SAГ
метилтрансфераза
СН2 СН2
N
N
NH2
CH3
метилгистамин
35. Глутатион
COOH-CH-(CH2)2-CO-NH-CH-CO-NH-CH2-COOHNH2
CH2-SH
G-SН + R
2 G-SН
G-S-R
-2Н
G-S-S-G
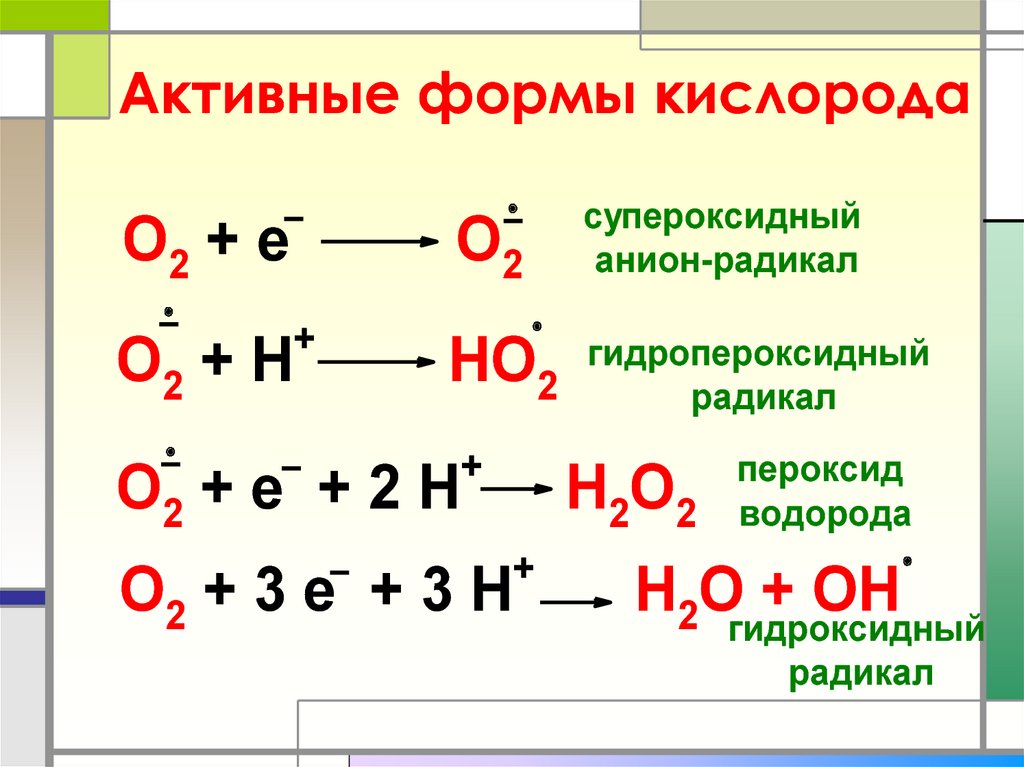
36. Активные формы кислорода
О2 + е+
О2 + Н
О2
супероксидный
анион-радикал
НО2
гидропероксидный
радикал
+
О2 + е + 2 Н
Н2О2
+
О2 + 3 е + 3 Н
пероксид
водорода
Н2Огидроксидный
+ ОН
радикал
37. Образование активных форм кислорода
Окисление железа гемагем-Fe2+ + О2
.
гемин-Fe3+ + О2
38. Окислительная способность активных форм кислорода
..
О2 < О2 < О2 < НО2
.
< Н2О2 < OН
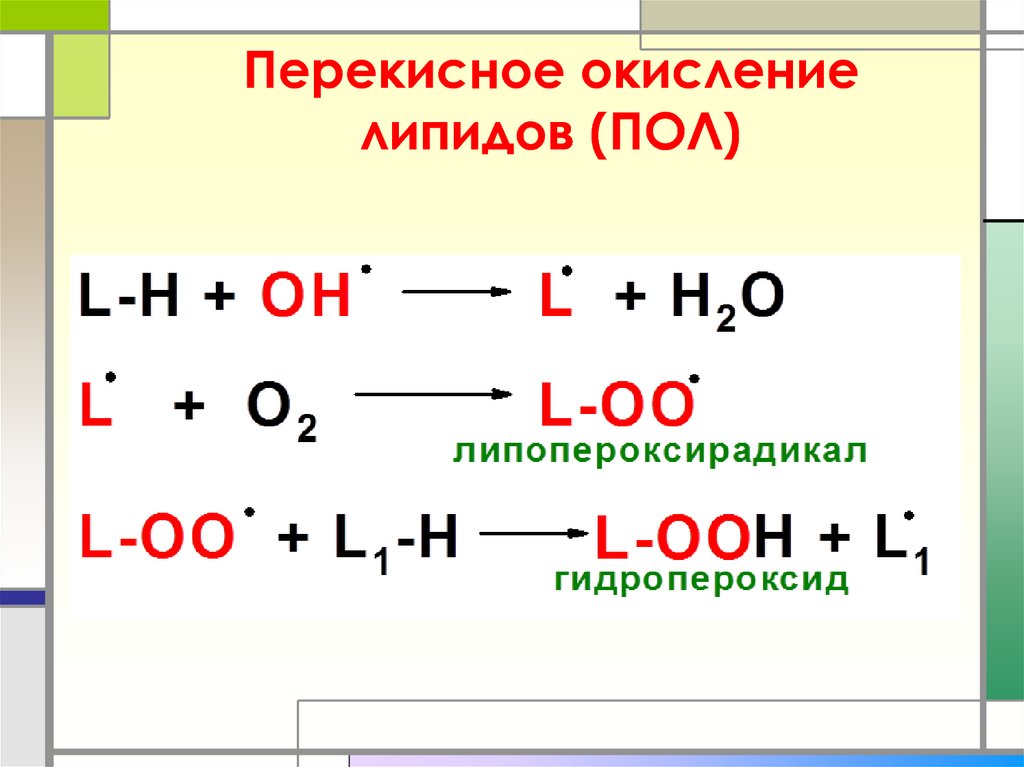
39. Перекисное окисление липидов (ПОЛ)
40. Антиоксидантная система
ферментативное звено:• супероксиддисмутаза (СОД)
• каталаза
• пероксидаза
неферментативное звено:
• витамины А, Е и С
• цинк, селен
• глутатион
41. Антиоксидантная система
СупероксиддисмутазаКаталаза
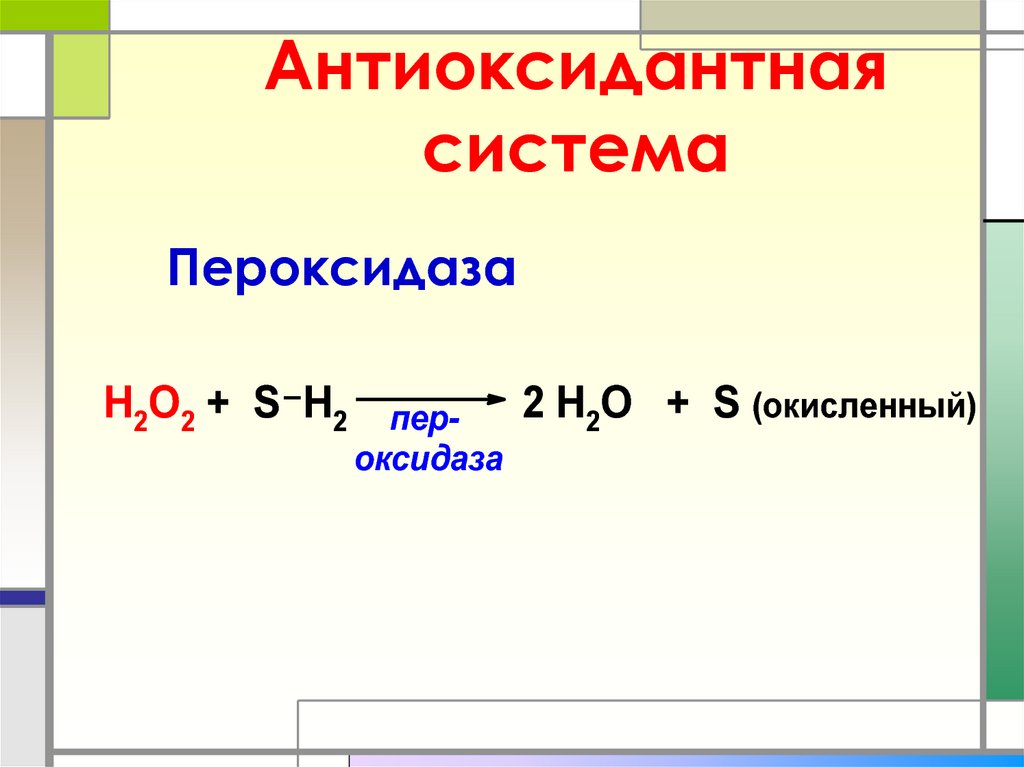
42. Антиоксидантная система
ПероксидазаН2О2 + S Н2 пероксидаза
2 Н2О + S (окисленный)
43. Химический канцерогенез
РАК – это неконтролируемаяклеточная пролиферация,
сопровождающаяся нарушением
клеточной дифференцировки.
44. Канцерогенные факторы
□ Физические: R-лучи, УФ-лучи, γ-облучение. Ониоказывают прямое воздействие на ДНК за счет
разрыва цепей ДНК, и непрямое
повреждающее действие за счет появления
свободнорадикальных форм кислорода и их
токсического действия на НК.
□ Химические: полициклические ароматические
углеводороды (бензопирен, бензантрацен),
ароматические амины, которые используются
при производстве анилиновых красителей,
нитрозамины, нитриты, вторичные амины,
афлотоксины как продукты плесеней.
Неорганические вещества такие как хлор,
свинец, кадмий, бериллий, асбест.
□ Биологические или онковирусы. Они
встраиваются в геном клетки человека и
вызывают ее трансформацию.
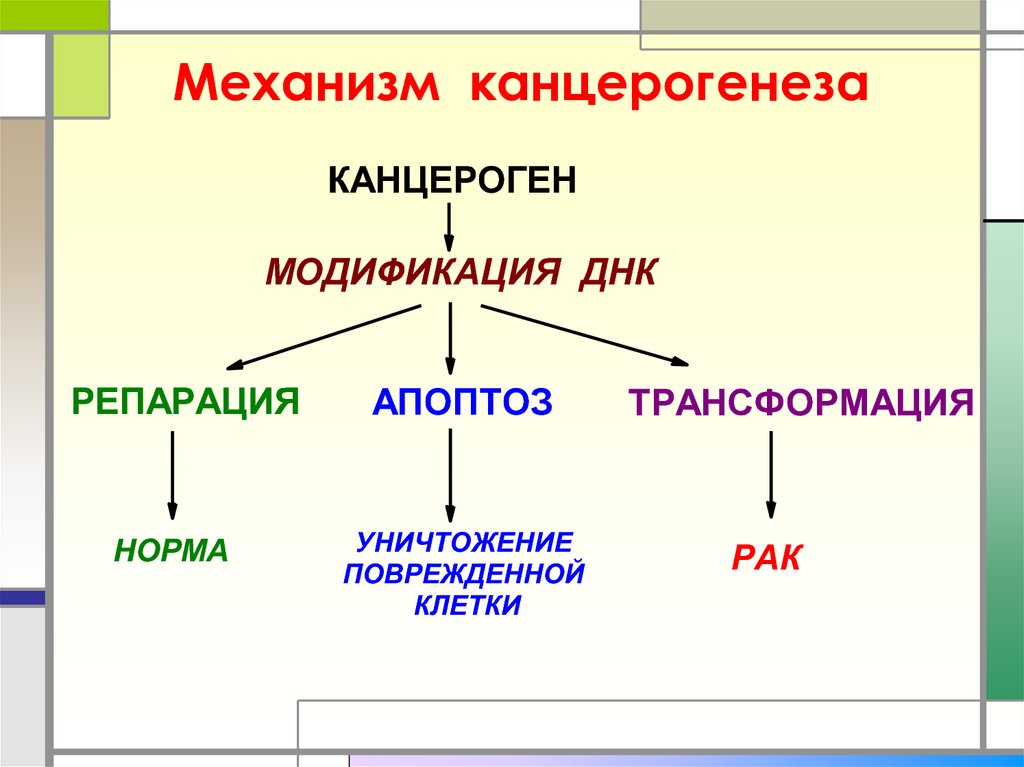
45. Механизм канцерогенеза
КАНЦЕРОГЕНМОДИФИКАЦИЯ ДНК
РЕПАРАЦИЯ
НОРМА
АПОПТОЗ
УНИЧТОЖЕНИЕ
ПОВРЕЖДЕННОЙ
КЛЕТКИ
ТРАНСФОРМАЦИЯ
РАК
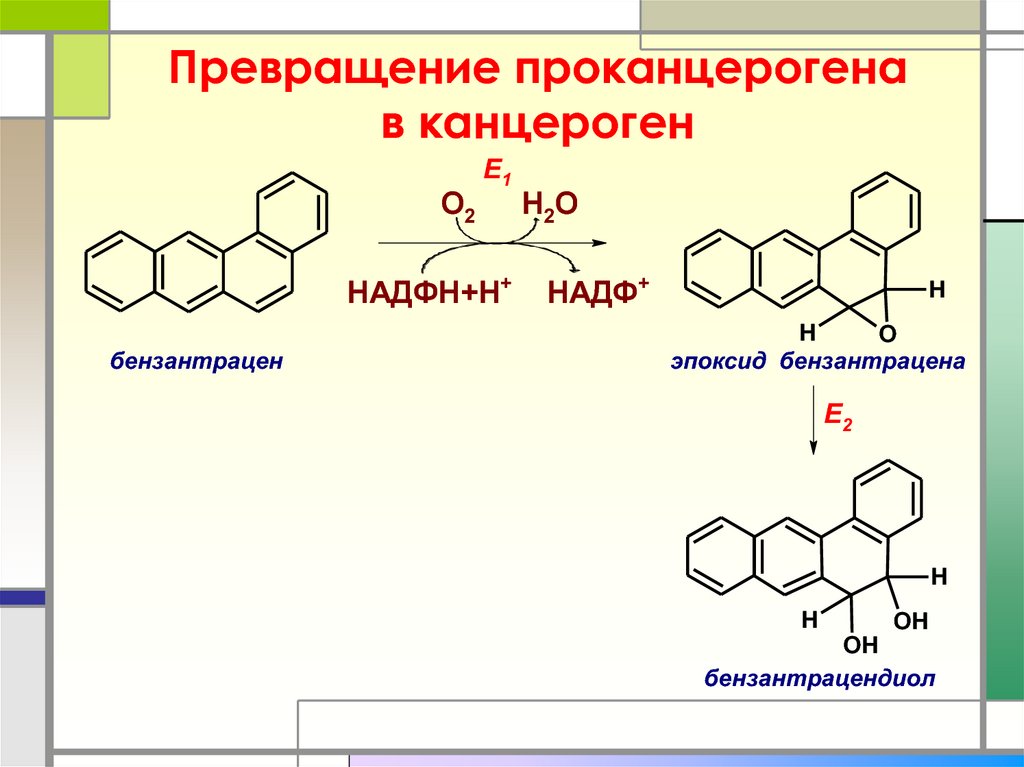
46. Превращение проканцерогена в канцероген
О2Е1
НАДФН+Н+
бензантрацен
Н2О
НАДФ+
H
H
O
эпоксид бензантрацена
Е2
H
H
OH
OH
бензантрацендиол
47. Стадии трансформации нормальной клетки в опухолевую
□ ИНИЦИАЦИЯ – повреждение ДНК имеет местов одной клетке. Возможны: репарация,
апоптоз или дальнейшая трансформация
□ ПРОМОЦИЯ ОПУХОЛИ, в этой стадии идет
преимущественное размножение опухолевых
клеток. Этот процесс может длиться годами.
□ ПРОГРЕССИЯ ОПУХОЛИ – идет процесс
размножения опухолевых клеток, идет инвазия
и метастазирование.





















 medicine
medicine biology
biology chemistry
chemistry