Similar presentations:
Общие вопросы аналитической химии. Химические методы обнаружения неорганических веществ
1. Тема лекции Общие вопросы аналитической химии. Химические методы обнаружения неорганических веществ.
12.
План лекции:1. Общие вопросы аналитической
химии.
2. Литература по аналитической химии.
3. Химические методы обнаружения
неорганических веществ.
3. Реакции обнаружения катионов I
аналитической группы.
4. Реакции обнаружения катионов I I
аналитической группы.
3. РЕКОМЕНДУЕМАЯ ЛИТЕРАТУРА
4. КОНСПЕКТ В ИНТЕРНЕТЕ
5. Определение предмета «Аналитическая химия»
6. Аналитическая химия, или аналитика – это раздел химической науки, разрабатывающий на основе фундаментальных законов химии и
физики методы и приемыкачественного и количественного
анализа атомного, молекулярного
и фазового состава вещества.
7. Определение VIII Европейской конференции по аналитической химии (Эдинбург, 1993)- Аналитическая химия – это научная дисциплина,
Определение VIII Европейскойконференции по аналитической
химии (Эдинбург, 1993)Аналитическая химия – это
научная дисциплина, которая
развивает и применяет методы,
средства и общую методологию
получения информации о
составе и природе вещества
8. Определение по Г.Кристиану со ссылкой на Чарльза Н.Рейли
•Аналитическаяхимия – это то, чем
занимаются химикианалитики
9. Аналитическая служба
• Административная система,обеспечивающая конкретный анализ
определенных объектов с
использованием методов,
рекомендуемых аналитической
химией, называется аналитической
службой. Аналитическая служба
государства представляет собой
совокупность аналитических служб
отдельных ведомств.
10. СТРУКТУРА ДИСЦИПЛИНЫ «АНАЛИТИЧЕСКАЯ ХИМИЯ»
• 1) КАЧЕСТВЕННЫЙ(QUALITY) АНАЛИЗ;
• 2) КОЛИЧЕСТВЕННЫЙ
(QUANTITY) АНАЛИЗ;
• 3) ФИЗИКО-ХИМИЧЕСКИЕ
МЕТОДЫ АНАЛИЗА
11. ОСНОВНАЯ ЦЕЛЬ КУРСА АХ
• ОБЩЕОБРАЗОВАТЕЛЬНЫЙПРЕДМЕТ, НУЖНЫЙ
ВПОСЛЕДСТВИИ ПРИ
ИЗУЧЕНИИ
ФАРМАЦЕВТИЧЕСКОЙ
ХИМИИ
12. Основные понятия аналитической химии: принцип, метод и методика анализа
13. Принцип анализа
• Явление, используемое дляполучения аналитической
информации, называется
принципом анализа. (Например,
явление - поглощение света
веществом, аналитическая
информация - природа
определяемого вещества и его
концентрация)
14. Метод анализа
• Краткое изложение принципов,лежащих в основе анализа вещества
(вне зависимости от определяемого
компонента и анализируемого
объекта), носит название метода
анализа. Например,
гравиметрический анализ основан
на определении массы веществ, или
люминесцентный метод анализа
15. Методика анализа
• Методика анализа – это подробноеописание хода выполнения
конкретного анализа данного объекта
с использованием выбранного метода,
обеспечивающее регламентированные
характеристики правильности и
воспроизводимости (раздел – методы
математической статистики в
аналитической химии) анализа.
16. В зависимости от цели различают качественный, количественный и структурный анализ.
17. Качественный анализ
• Качественный анализпредполагает
обнаружение или
идентификацию
компонентов
анализируемого образца.
18. Структурный анализ (ОДНА ИЗ РАЗНОВИДНОСТЕЙ КАЧЕСТВЕННОГО АНАЛИЗА)
• Цель структурногоанализа – установление
химического и
пространственного
строения исследуемого
соединения.
19. Количественный анализ
• В процессеколичественного анализа
происходит определение
концентраций или масс
компонентов.
20. Классификация видов анализа в зависимости от определяемого компонента
21. Классификация видов анализа в зависимости от массы или объема анализируемой пробы
22. Классификация видов анализа в зависимости от процедуры проведения анализа
• Систематический –разделение смесиионов на группы или подгруппы.
• Дробный – определение
определенного элемента, для
подтверждения его нахождения в
смеси.
• Локальный – определение элементов
на определенном участке поверхности.
23. Характеристики аналитической реакции
• Избирательность ( селективность) –возможность определения в результате
аналитической реакции определенного
вещества (одного или нескольких ) в
сложной смеси веществ;
• Предел обнаружения (определения) –
минимальное количество вещества,
которое можно определить качественно
(количественно);
24. Избирательность аналитической реакции (в зависимости от числа веществ)
• Специфические реакции – позволяютопределять только одно вещество;
• Избирательные реакции - позволяют
определять небольшое число о веществ;
• Групповые реакции – используются в
систематическом анализе для выделения
группы веществ;
25. ПРЕДЕЛ ОБНАРУЖЕНИЯ
• НАИМЕНЬШЕЕ СОДЕРЖАНИЕ АНАЛИТА(ОПРЕДЕЛЯЕМОГО ВЕЩЕСТВА) КОТОРОЕ ПО
ДАННОЙ МЕТОДИКЕ МОЖНО ОТЛИЧИТЬ ОТ
СИГНАЛА КОНТРОЛЬНОГО ОПЫТА.
СОГЛАСНО IUPAC, МИНИМАЛЬНО
ОБНАРУЖИВАЕМЫМ СИГНАЛОМ
СЧИТАЕТСЯ ТАКОЙ КОТОРЫЙ ПРЕВЫШАЕТ
СРЕДНЕЕЕ ЗНАЧЕНИЕ СИГНАЛА
КОНТРОЛЬНОГО ОПЫТА НА 3 СТАНДАРТНЫХ
ОТКЛОНЕНИЯ ( ПОНЯТИЕ
МАТЕМАТИЧЕСКОЙ СТАТИСТИКИ)
26. ПРЕДЕЛ ОПРЕДЕЛЕНИЯ
• СОДЕРЖАНИЕ АНАЛИТА(ОПРЕДЕЛЯЕМОГО ВЕЩЕСТВА)
КОТОРЫЙ ПРЕВЫШАЕТ СРЕДНЕЕ
ЗНАЧЕНИЕ СИГНАЛА
КОНТРОЛЬНОГО ОПЫТА НА
ВЕЛИЧИНУ В 10 СТАНДАРТНЫХ
ОТКЛОНЕНИЙ (ПОНЯТИЕ
МАТЕМАТИЧЕСКОЙ СТАТИСТИКИ)
27. ДИАПАЗОН ОПРЕДЕЛЯЕМЫХ СОДЕРЖАНИЙ
• РАЗНОСТЬ МЕЖДУ НИЖНЕЙ И ВЕРХНЕЙГРАНИЦАМИ ОПРЕДЕЛЯЕМЫХ
СОДЕРЖАНИЙ.
28. Методы аналитической химии
29. Методы аналитической химии при анализе образцов
• 1. Метод пробоотбора;• 2. Метод разложения проб;
• 3. Метод разделения и
концентрирования;
• 4. Метод обнаружения и
количественного определения
30. Химические методы обнаружения неорганических веществ.
31. ГЛАВНАЯ ТАБЛИЦА ПО АНАЛИТИКЕ
32. Химические методы обнаружения неорганических веществ основаны на проведении аналитических реакций. Аналитическими называются
химические реакции, результаткоторых несет определенную
аналитическую информацию.
33. Эффекты при аналитических реакциях
• 1. Образование и растворениеосадков
• 2. Образование характерных
кристаллов
• 3. Появление или изменение
окраски растворов
• 4. Выделение газов
34. Понятие аналитической группы ионов
35. Понятие аналитической группы ионов
• Аналитическая группа ионовотличается от групп Периодической
таблицы Менделеева Д.И.
• Аналитическая группа ионов
обладает общностью свойств в
реакциях осаждения или
выделения, позволяющих отделить
их от остальных ионов близкой
химической природы
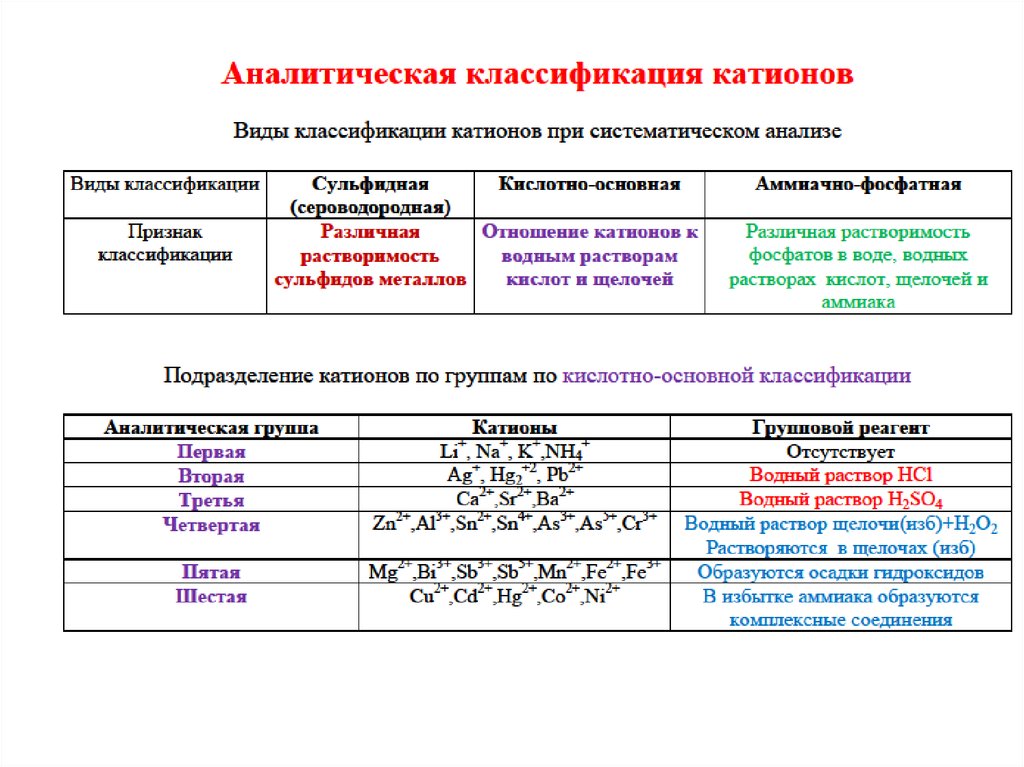
36. Аналитическая классификация катионов
37.
38. Аналитическая классификация катионов
•Сульфидная;•Кислотно-основная;
Аммиачнофосфатная;
39. АНАЛИТИЧЕСКИЕ ГРУППЫ ИОНОВ
• 6 ГРУПП• 3 ГРУППЫ
КАТИОНОВ ПО АНИОНОВ ПО
КИСЛОТНОРАСТВОРИОСНОВНОЙ
МОСТИ СОЛЕЙ
КЛАССИФИБАРИЯ И
КАЦИИ
СЕРЕБРА
40.
41. Сульфидная Аналитическая классификация катионов
• Групповые реагенты – сульфидаммония, сероводород и карбонат
аммония.
• Все катионы подразделяются на
• 5 аналитических групп. Различия в
растворимости и сульфидов и
образования осадков с карбонатом
аммония
42. Кислотно-основная аналитическая классификация катионов
• Все катионы подразделяются на 6аналитических групп. Используется
различие в растворимости
соединений по отношения к
раствором кислот и щелочей с
учетом комплексообразования в
растворах.
43. Аммиачно-фосфатная аналитическая классификация катионов
• В основу положенаразличная растворимость
фосфатов в воде, водных
растворах кислот, щелочей и
аммиака. Все катионы
делятся на 5 аналитических
групп.
44. АНАЛИЗ КАТИОНОВ (ПО Кислотно-основной классификация)
АНАЛИЗ КАТИОНОВ(ПО Кислотноосновной
классификация)
45. МЕШАЮЩЕЕ ВЛИЯНИЕ ИОНОВ
• Li+ (Na+) + Zn(UO2)3CH3COO-=46. ПО ОТНОШЕНИЮ К ГРУППОВОМУ РЕАГЕНТУ
• НЕ ИМЕЮТ •ИМЕЮТГРУППОВОГО ГРУППОВОЙ
РЕАГЕНТА
РЕАГЕНТ
47. Подразделение катионов по группам по кислотно-основной классификации
Аналитическая
группа
Катионы
Групповой реагент
Первая
Вторая
Третья
Четвертая
Li+, Na+, K+,NH4+
Ag+, Hg2+2, Pb2+
Ca2+,Sr2+,Ba2+
Zn2+,Al3+,Sn2+, Sn4+, Cr3+
Отсутствует
Водный раствор HCl
Водный раствор H2SO4
Водный раствор
щелочи(изб)+H2O2
Растворяются в щелочах (изб)
Пятая
Mg2+,Bi3+, Sb3+,Sb5+,Mn2+,
Fe2+, Fe3+
Образуются осадки гидроксидов
Шестая
Cu2+, Cd2+, Hg2+, Co2+, Ni2+
В избытке аммиака образуются
комплексные соединения
48. ИМЕЮТ ГРУППОВОЙ РЕАГЕНТ
• КИСЛОТЫ• ОСНОВАНИЯ
НЕРАСТВОРМЫЕ • Амфотерные
ХЛОРИДЫ – HCl гидроксиды:
• Ag+,, Hg22+,, Pb2+, • Al3+, Zn2+ , Cr3+
• НЕРАСТВОРИМЫЕ • Нерастворимыеги
дроксиды:
СУЛЬФАТЫ
Растворимые
• H2SO4 (NH4)2SO4аммиачные
2+,
2+,
2+,
Ca Sr Ba
комплексы:
49. ОСОБОЕ ПОВЕДЕНИЕ Pb2+,
ρ*(PbСl2)=9,8 г/л•ρ*(PbSO4)= 0,045 г/л
2+,
•Вывод Рb можно
отнести и ко II, и к III
• .
аналитической группе
50. Первая аналитическая группа катионов -Li+, Na+, K+, NH4+
Перваяаналитическая
группа катионов +
+
+
Li , Na+, K , NH4
51. Реакции ионов Li+
Реакции ионов+
Li
52. Реакция с двузамещенным гидроортофосфатом натрия Na2НРO4.
+• 3Li
2- +
ОН
+ НРО4
=Li3PО4↓ + Н2О
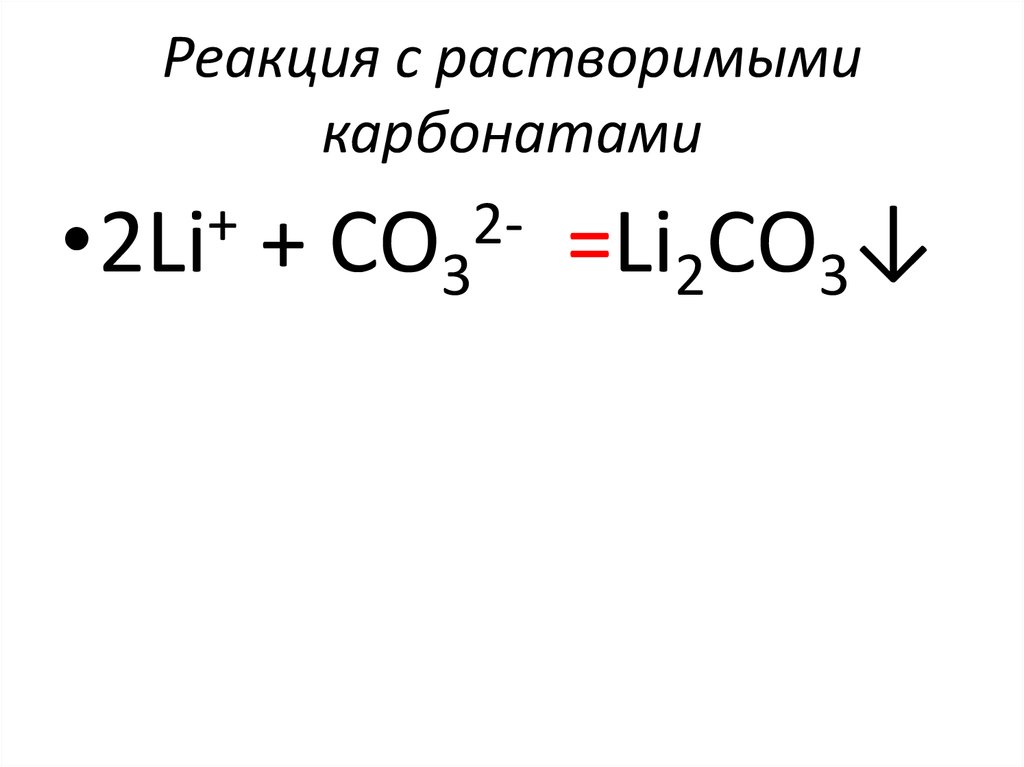
53. Реакция с растворимыми карбонатами
+2•2Li + СО3 =Li2CО3↓
54. Реакция с растворимыми фторидами
+•Li
+
F
= LiF
↓
55. Реакции ионов Na+
56. Микрокристаллоскопическая реакция с цинкуранилацетатом (уже не фармакопейная).
• Na+ + Zn[(UО2)3(CH3CОО)8] +СН3СОО- + 9Н2О
=NaZn(UО2)3(CH3CОО)9∙9Н2О
57. .Реакция с гексагидроксостибатом (V) калия
+•Na
+ [Sb(OH)6
=Na[Sb(OH)6]↓
]
58. Реакции ионов K+
Реакции ионов+
K
59. Реакция с гексанитрокобальтатом (III) натрия кобальтинитритом натрия (фармакопейная)
+•2К
+ Na3[Co(NО2)6] =
+
NaK2[Co(NО2)6↓ + 2Na .
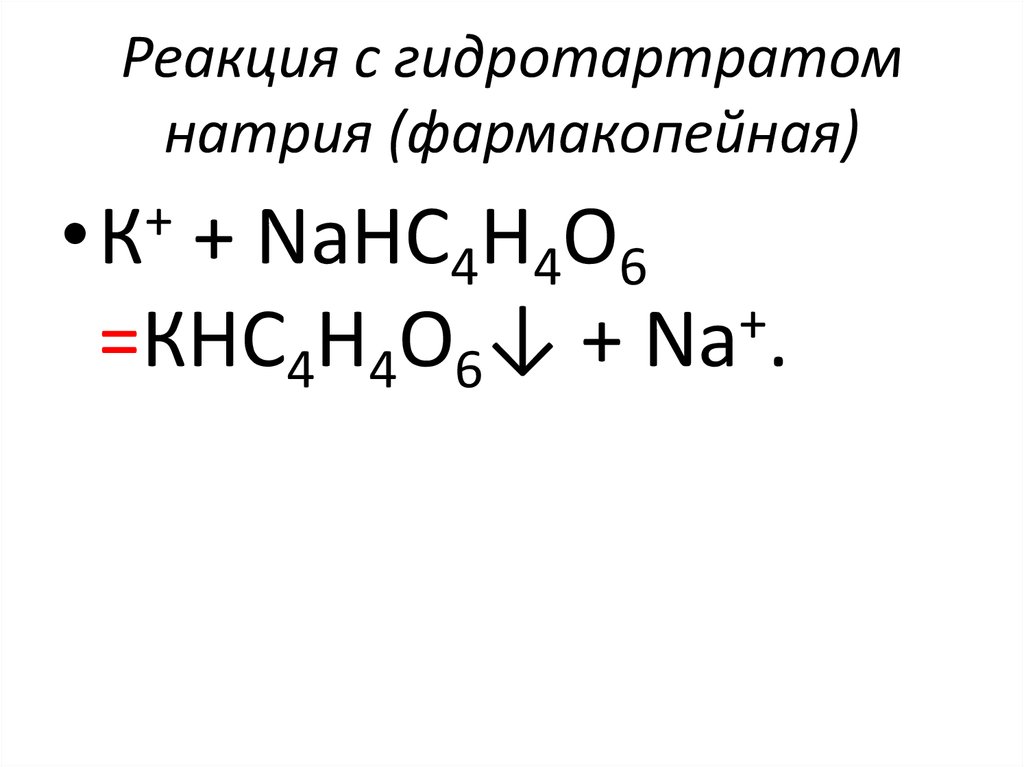
60. Реакция с гидротартратом натрия (фармакопейная)
+•К
+ NaHC4H4О6
+
=КНС4Н4О6↓ + Na .
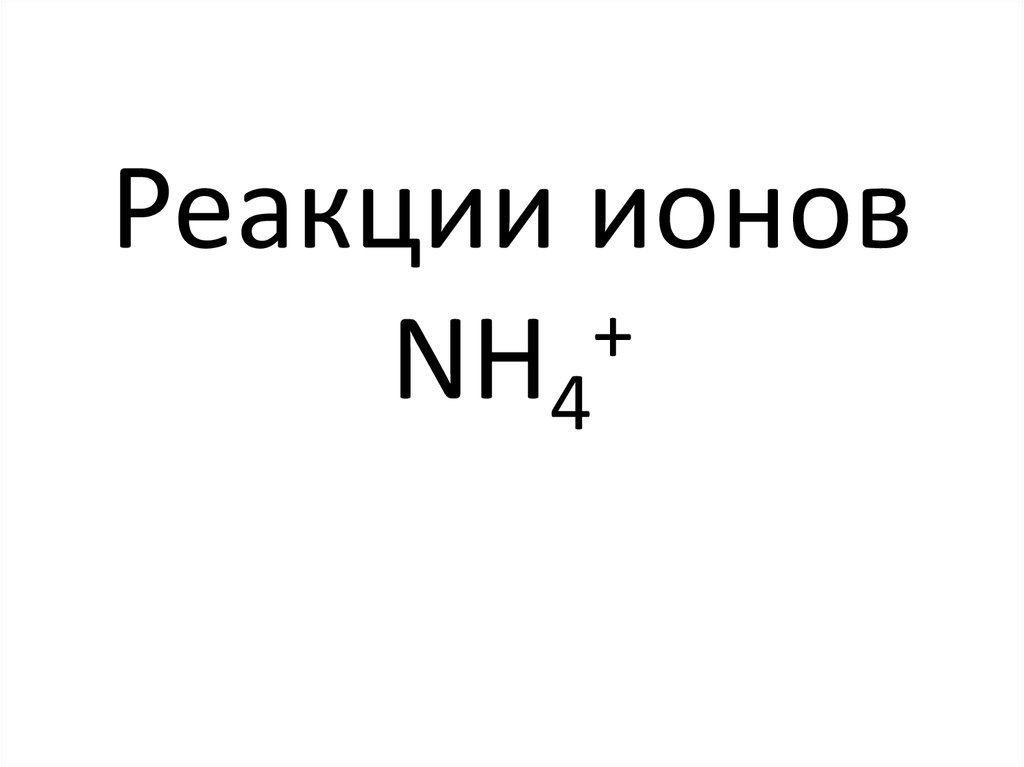
61. Реакции ионов NH4+
Реакции ионов+
NH4
62. Реакция разложения солей аммония щелочами (фармакопейная)
+• NH4
+
ОН
=NH3↑ + Н2О.
63. Реакция с реактивом Несслера — смесью раствора тетрайодомеркурama(II) калия K2[HgI4] с КОН (фармакопейная)
+• NH4
22[HgI4]
4OH
+
+
=[OHg2NH2]I + 7I + 3H2O
64. Систематический анализ смеси катионов Li+, Na+, K+, NH4+
Систематический анализ смесикатионов
+
Li ,
Na+,
+
K,
NH4
+
• Сразу удаляют аммоний
прокаливаем в щелочной среде,
затем Li+– осаждением фторидом
аммония или гидроортофосфатом
натрия.
• Ионы Na+, K+, определяют
дробными реакциями
65. Вторая аналитическая группа катионов -Ag+, Pb2+, Hg22+,
Втораяаналитическая
группа катионов +
2+
2+
Ag , Pb , Hg2 ,
66. Микрокристаллоскопическая реакция с цинкуранилацетатом (фармакопейная).
• Na+ + Zn[(UО2)3(CH3CОО)8] +СН3СОО- + 9Н2О
=NaZn(UО2)3(CH3CОО)9∙9Н2О
67. Реакции ионов Ag+
Реакции ионов+
Ag
68. Реакция со щелочами
+• 2Ag
+
2ОН
Ag2O↓ +
Н2О.
• Ag2O + 4NH3 + Н2О
+
2[Ag(NH3)2] + 2ОН
69. Растворимые галогениды
+•Ag
Сl
+ = AgCl↓;
+
•Ag + Br = AgBr↓;
+
•Ag + I = AgI↓.
70. Различие галогенидов серебра
• Осадок хлорида серебрарастворим в растворе аммиака.
Иодид серебра не растворяется в
растворе аммиака, а бромид
серебра растворяется
незначительно
71. Хромат калия - осадок кирпично-красного цвета:
+•2Ag
2-
+ CrО4 =
Ag2CrО4↓
72. Гидрофосфат натрия
• 3Ag+ + 2HPO42- = Ag3PO4↓ + H2PO4-73. Реакция восстановления Ag+ до металлического серебра
• 4[Ag(NH3)2]OH + CH2O =• 4Ag↓ + (NH4)2CO3 + 6NH3 + 2H2O
74. Реакции ионов Pb2+
Реакции ионов2+
Pb
75. Действие щелочей и аммиака
2+•Pb
+
2OH
= Pb(OH)2 ↓
76. Растворимые галогениды
• Pb2+ +2Cl - = PbCl2 ↓• Pb2+ +2Br - = PbBr2 ↓
• Pb2+ +2I - = PbI2 ↓
77. Осадки галогенидов свинца (II) растворимы в горячей воде и в присутствии избытка галогенид-ионов
Осадки галогенидов свинца (II)растворимы в горячей воде и в
присутствии избытка галогенидионов
2•PbI2↓ + 2I = [РbI4]
PbI2↓ + 2I[РbI4]2-.
78. Хромат калия образует желтый осадок
2+•Pb
2CrO4
+
PbCrO4 ↓
=
79. Реакция с сульфид-ионами
2+•Pb
2S
+
= PbS ↓
80. Реакции ионов Hg22+
Реакции ионов2+
Hg2
81. Действие щелочей
2+•Hg2
2OH
+
=
Hg2O↓ + H2O
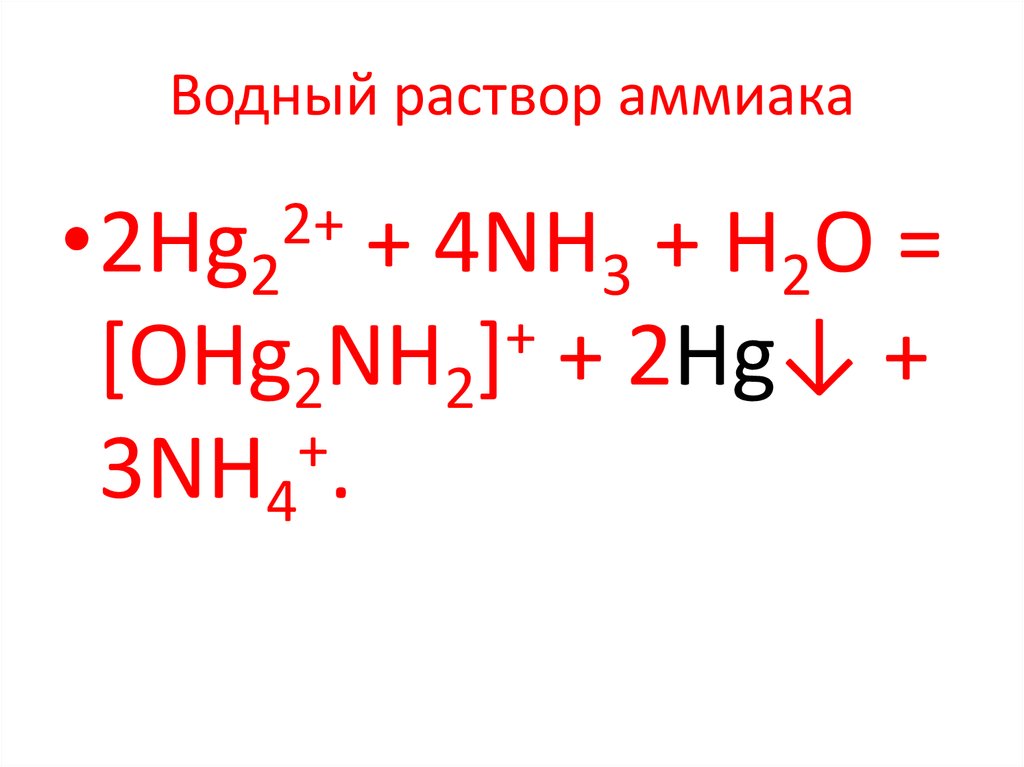
82. Водный раствор аммиака
2+•2Hg2
+ 4NH3 + Н2О =
+
[OHg2NH2] + 2Hg↓ +
+
3NH4 .
83. Растворимые хлориды
2+•Hg2
2Сl
+
=
Hg2Cl2↓
(каломель).
84. Растворимые иодиды
•Hg2 +Hg2I2↓.
2+
2I
=
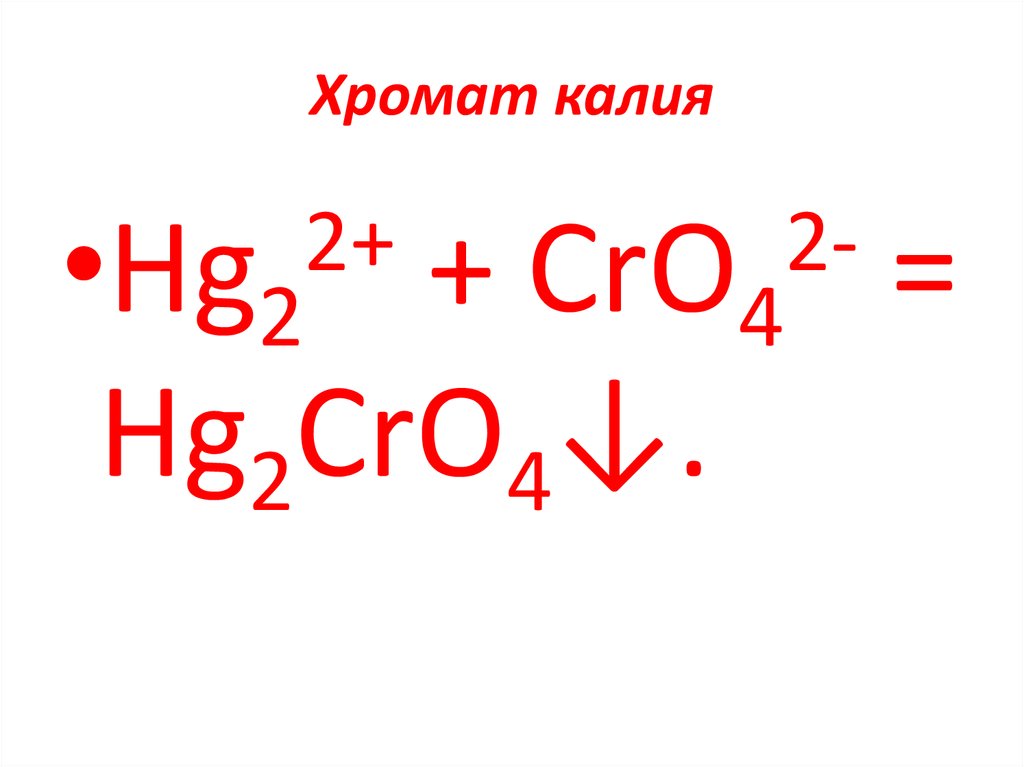
85. Хромат калия
2+•Hg2
2CrО4
+
Hg2CrО4↓.
=
86. Восстановление ртути (I) до металлической ртути.
2+•Hg2
+ Сu =
2+
2Hg↓ + Сu .
87. Третья аналитическая группа катионов -Ca2+ , Sr2+, Ba2+,
Третьяаналитическая
группа катионов 2+
2+
2+
Ca , Sr , Ba ,
88. Реакции ионов Ca2+
Реакции ионов2+
Ca
89. Серная кислота
2+• Са
2-
+ SO4 + 2Н2О =
CaSO4∙2Н2О↓.
90. Карбонат аммония
2+•Са
2СO3
+
СаСO3↓.
=
91. Оксалат аммония
2+•Са
2-
+ С2O4 =
СаС2О4↓
92. Гексацианоферрат (II) калия
• Са2+ + К+ + NH4++ [Fe(CN)6]4- =NH4KCa[Fe(CN)6]↓.
93. Реакции ионов Sr2+
Реакции ионов2+
Sr
94. Серная кислота, растворимые сульфаты и гипсовая вода (насыщенный водный раствор сульфата кальция)
2+•Sr +
2-
SO4 =
SrSO4↓.
95. Карбонат аммония
2+•Sr
2-
+ СО3 =
SrCO3↓.
96. Оксалат аммония
2+Sr
2С2O4
+
SrC2O4↓.
=
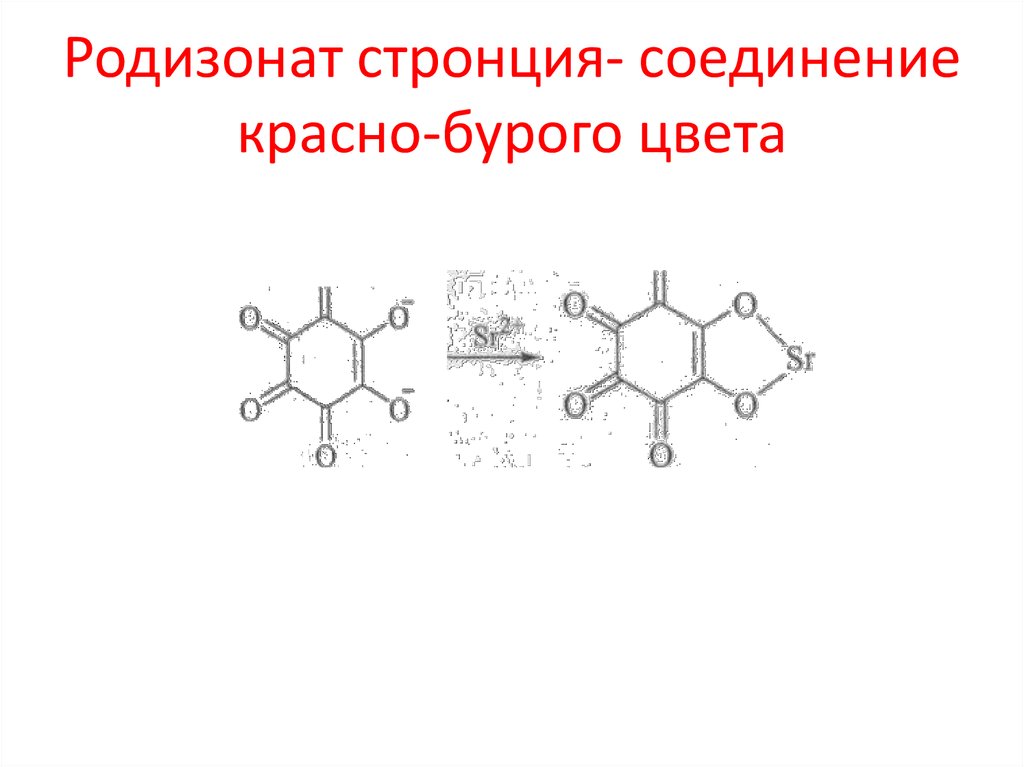
97. Родизонат стронция- соединение красно-бурого цвета
98. Реакции ионов Ba2+
Реакции ионов2+
Ba
99. Серная кислота и растворимые сульфаты
2+•Ва +
2-
SO4 =
BaSO4↓.
100. Карбонат аммония
2+•Ва +
2СO3
BaCO3↓.
=
101. Оксалат аммония
2+•Ва +
2С2O4
BaC2O4↓.
=
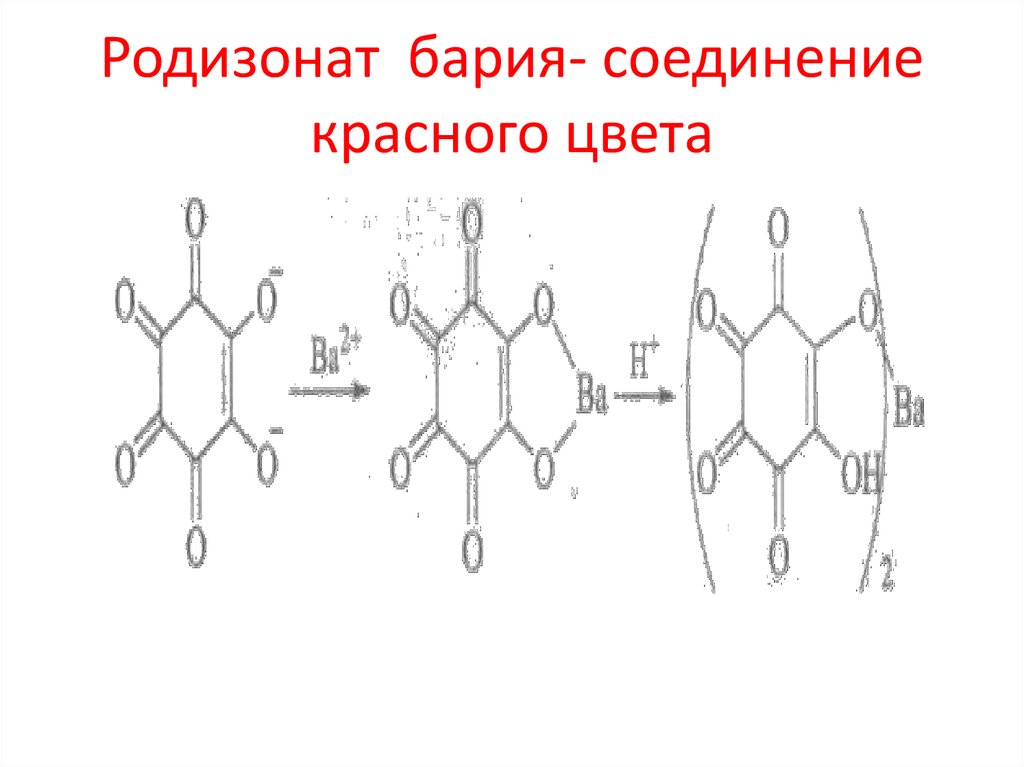
102. Родизонат бария- соединение красного цвета
103. Хромат или дихромат калия дают осадки ярко-желтого цвета
• Ва2+ + СгO42- = ВаСrO4↓;• 2Ва2+ + Сг2O72- + Н2O = 2ВаСrO4↓ +
2Н+.
104. Систематический ход анализа
Третья аналитическаягруппа катионов
СИСТЕМАТИЧЕСКИЙ
ХОД АНАЛИЗА
105. ПЕРЕВОД ОСАДКОВ В РАСТВОРИМОЕ СОСТОЯНИЕ
• СУЛЬФАТЫ КАТИНОВ III ГРУППЫ С СН3СООННЕ ВЗАИМОДЕЙСТВУЮТ, ПОЭТОМУ ИХ
ПРЕДВАРИТЕЛЬНО ПРВРАЩАЮТ В
КАРБОНАТЫ ОБРАБОТКОЙ ГОРЯЧИМ
НАСЫЩЕННЫМ РАСТВОРОМ Na2CO3,
ЗАТЕМ ОБРАБАТЫВАЮТ СН3СООН.
106. ИДЕНТИФИКАЦИЯ КАТИОНА БАРИЯ
• ОБНАРУЖИВАЮТ РЕАКЦИЙ С K2Cr2O7СН3СООNa, ОСАЖДАЮТ С K2CrO4 7 ,
СТРОНЦИЙ И КАЛЬЦИЙ ОСАЖДАЮТ В ВИДЕ
КАРБОНАТОВ, ПОСЛЕ ОТДЕЛЕНИЯ ОСАДКА
ПРОВОДЯТ ОБНАРУЖЕНИЕ ЭТИХ ИОНОВ
107. ОБНАРУЖЕНИЕ СТРОНЦИЯ И КАЛЬЦИЯ.
• РАЗДЕЛЕНИЕ ОСНОВАНИЕ НАТОМ, ЧТО В НАСЫЩЕНОЙ
2РАСТВОРЕ (NH4)2SO4 [Ca(SO4)2] ,
ОБРАЗУЕТ РАСТВОРИМЫЙ
КОМПЛЕКС, КАЛЬЦИЙ И
СТРОНЦИЙ ОБНАРУЖИВАЮТ
ДРОБНЫМИ РЕАКЦИЯМИ
108. Анализ смеси катионов IVаналитической группы
109. Общая характеристика химических свойств
110. Катионы IV группы
3+•Al ,
2+
Zn
3+
Cr
,
2+
Sn
,
Sn (IV).
,
111. Основное свойство
• Амфотерность. В данномслучае - это способность
растворяться в щелочах с
образованием
гидроксокомплексов
112. Гидроксокомплексы при избытке NaOH
•[Al(OH)4[Cr(OH)4] ,
2[Zn(OH)4]
],
113. Катионы в водных растворах
• Обладают выраженнымикислотными свойствами;
• Бесцветны, за исключением
[Cr(Н2O)6]3+ - серо-зеленого
цвета
114. Al3+
характеристикахимических свойств
3+
AL
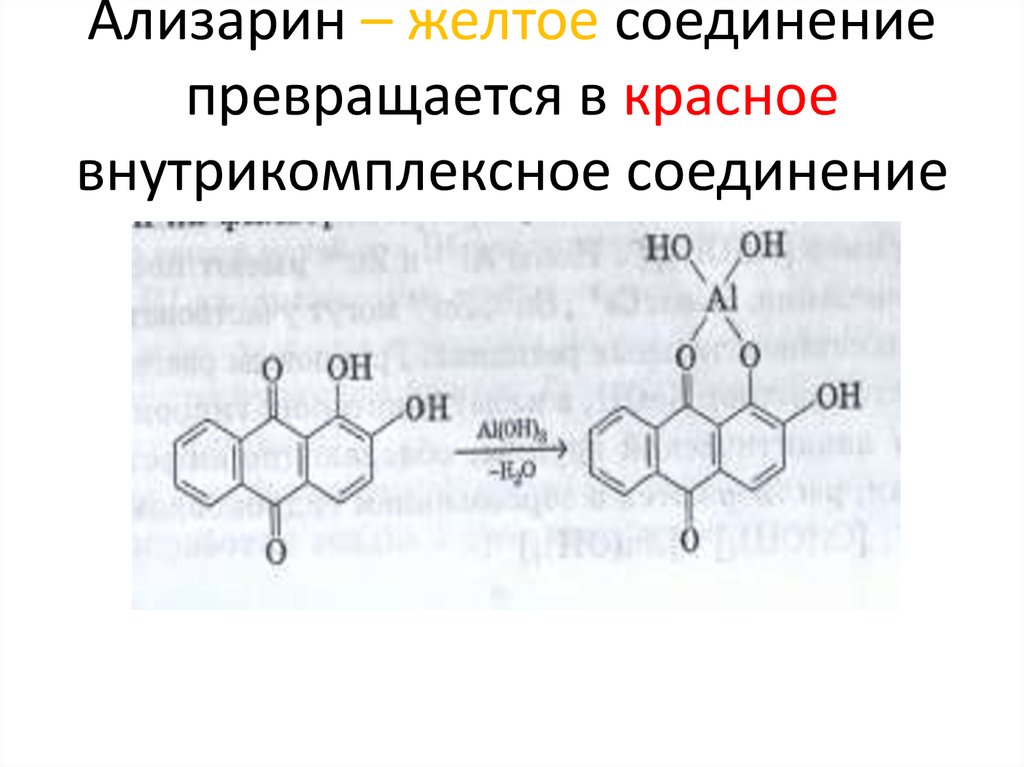
115. Ализарин – желтое соединение превращается в красное внутрикомплексное соединение
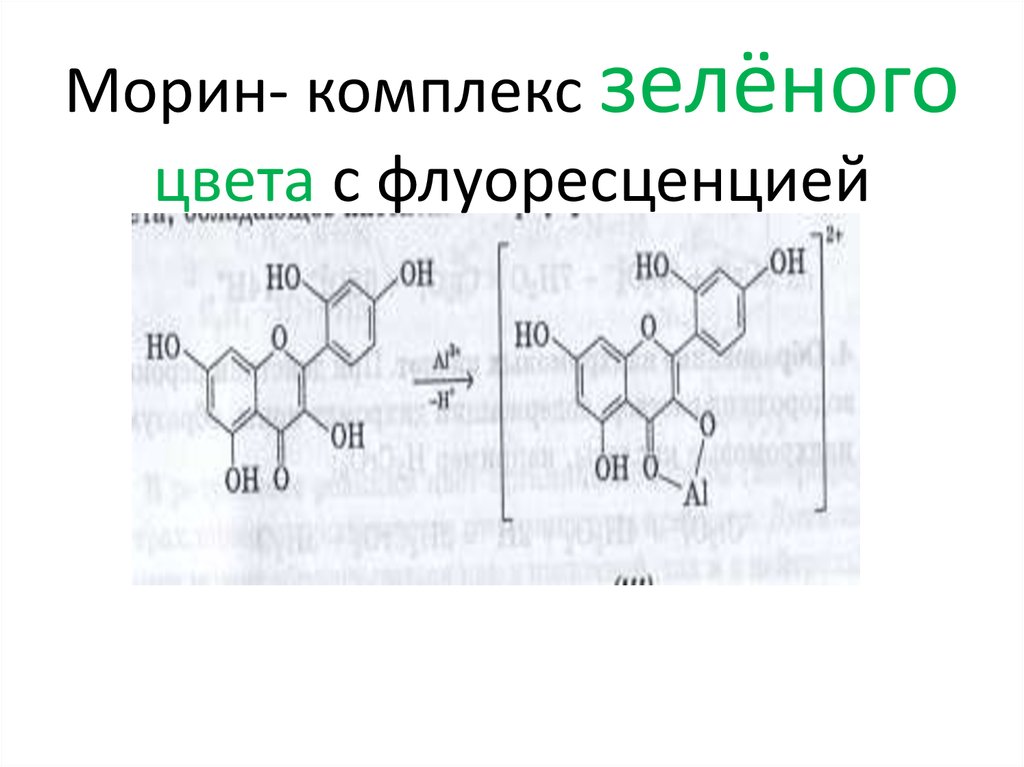
116. Морин- комплекс зелёного цвета с флуоресценцией
117. CR3+
характеристикахимических свойств
3+
CR
118. АММИАКАТЫ ХРОМА
• ОРАНЖЕВОГО ЦВЕТА,n=6 , ОДНАКО РЕАКЦИЯ
ПРОТЕКАЕТ КРАЙНЕ
3+
МЕДЛЕННО [Cr(NH3)6]
119. Окисление Cr(III) до Cr(VI)
• Щелочная среда• 2[Cr(OH)6]3- + 3H2O2 =
2• 2CrO4 + 2OH +8H2O
• Кислая среда
• 10Cr3+ + 6MnO4- + 11H2O =
2+
2+
• 5Cr2O7 + 22H + 6Mn
120. Образование надхромовых кислот
•Cr2O7 + 4H2O2 +2-
=
+6
2H2Cr O6
+
2H
+ 3H2O
121. ПОЯСНЕНИЕ
• НАДКИСЛОТЫ- КИСЛОТЫ, ВКОТОРЫХ
ОДИН
ИЛИ
НЕСКОЛЬКО
КИСЛОРОДОВ
О2ЗАМЕНЕН
НА
ПЕРОКСИДНУЮ
ГРУППИРОВКУ О22-
122. ЭКСТРАКЦИЯ надхромовых кислот
•Экстргент диэтиловый эфир ,этилацетат –
органическая фаза
синего цвета
123. Zn2+
Общая характеристикахимических свойств
2+
ZN
124. Действие щелочей и аммиака
Zn2+ + 2OH- = Zn(OH)2 ↓
Zn2+ + 2NH3 + 2H2O = Zn(OH)2 ↓ +2NH4+
Zn(OH)2 ↓ +2H+ = Zn2+ + 2H2O
Zn(OH)2 ↓ + 2OH- = [Zn(OH)4]2Zn(OH)2 ↓ + 4NH3 = [Zn(NH3)4]2+ +2OH-
125. Реакция с сульфидом натрия – белый осадок
2+•Zn
+
2S
= ZnS ↓
126. Реакция с дитизоном – цвет изменяется от зеленого до красного
127. ОСОБЕННОСТИ
•В ЩЕЛОЧНОЙСРЕДЕ В КРАСНЫЙ
ЦВЕТ ОКРАШЕНЫ
ОБЕ ФАЗЫ
128. Гекса циано феррит калия Гекса циано феррaт (II) калия - ОСАДОК БЕЛОГО ЦВЕТА
2+•3Zn
+
2K
+
+
42[Fe(CN)6] =
Zn3K2[Fe(CN)6]2↓
129. Sn2+ и Sn(IV)
характеристикахимических свойств
2+
SN И
SN(IV)
130. Реакции сульфид-ионов
2+•Sn
2S
+ = SnS ↓
(бурый)
2•[SnCl6] +H2S=
+
•6Cl +2H +
SnS2↓(желтый)
131. Реакции окисления-восстановления
132. Анализ смеси катионов IV аналитической группы по систематическому анализу
133. ОБНАРУЖЕНИЕ ХРОМА
• ЧЕРЕЗ ОКИСЛЕНИЕН2О2 В ЩЕЛОЧНОЙ
СРЕДЕ. ОБРАЗУЕТСЯ
ЖЕЛТЫЙ ХРОМАТ
134. ВЫДЕЛЕНИЕ Al+3 И Sn (IV) В ВИДЕ ГИДРОКСИДОВ
•ПЕРЕВОД В ОСАДКИГИДРОКСИДОВ ПРИ
ОБРАБОТКЕ NH4Cl
(КИСЛАЯ СРЕДА ЗА
СЧЕТ ГИДРОЛИЗА)
135. РАСТВОРЕНИЕ ОСАДКОВ И АНАЛИЗ
2 М HClИ ОБНАРУЖИВАЮТ
+3
Al И Sn (IV)
РАСТВОРЯЮТ ОСАДКИ В
ДРОБНЫМИ РЕАКЦИЯМИ
136. ПЕРЕВОД ЦИНКА В ОСАДОК – (ZnOH)2CO3
•ОБРАБОТКА Na2CO3137. ТЕМА СЛЕДУЮЩЕЙ ЛЕКЦИИ
•ХИМИЧЕСКИЕМЕТОДЫ
ОБНАРУЖЕНИЯ
НЕОРГАНИЧЕСКИХ
ВЕЩЕСТВ


















































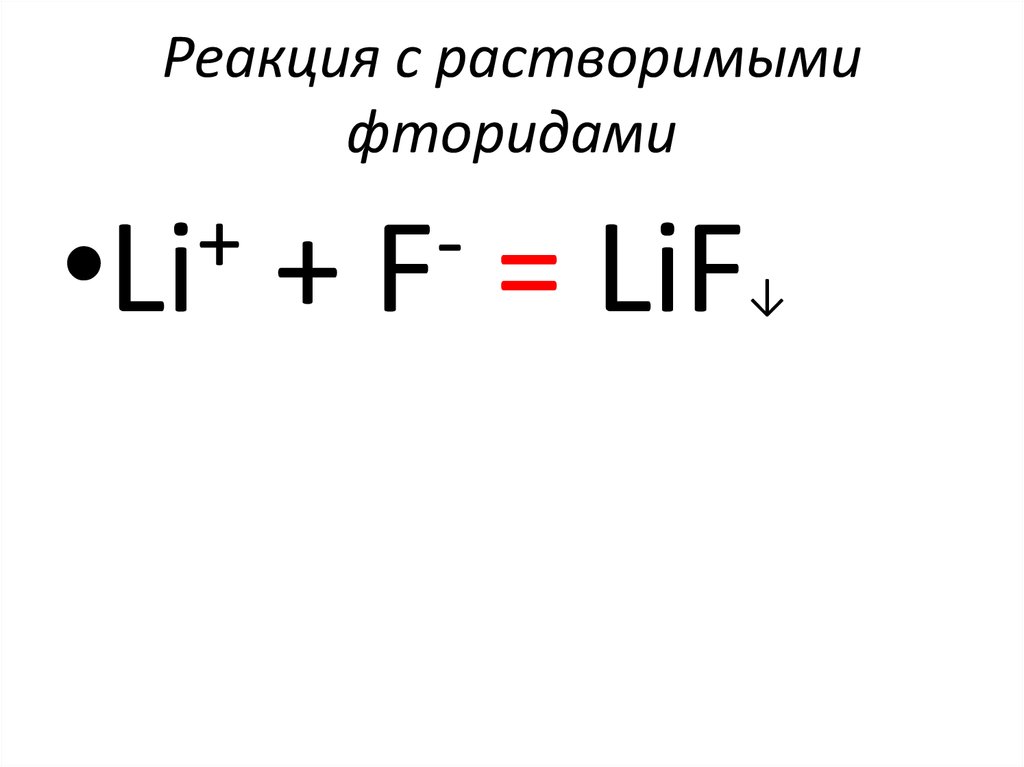






![Реакция с реактивом Несслера — смесью раствора тетрайодомеркурama(II) калия K2[HgI4] с КОН (фармакопейная) Реакция с реактивом Несслера — смесью раствора тетрайодомеркурama(II) калия K2[HgI4] с КОН (фармакопейная)](https://cf.ppt-online.org/files1/slide/p/pZJNceBG3Kkudj5If642xFbOqQrzw0gRto8LXDWH9/slide-62.jpg)

































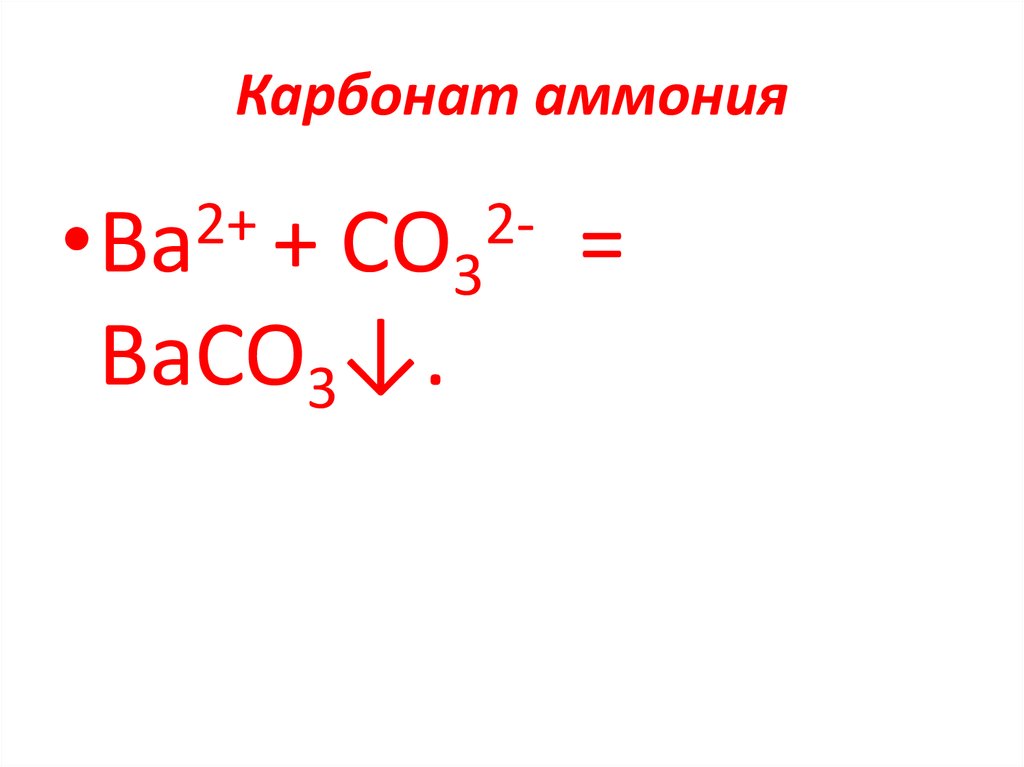


































 chemistry
chemistry








