Similar presentations:
Амфотерность
1. Амфотерность
2. СПЛАВЫ (без воды)
2KOH(тв.) + H2ZnO2(тв.) (t,сплавление)→ K2ZnO2 +2H2O
Be(OH)2(тв.) + 2NaOH(тв.) (t,сплавление)→
2H2O + Na2BeO2 (метабериллат натрия, или
бериллат)
Pb(OH)2(тв.) + 2NaOH(тв.) (t,сплавление)→
2H2O + Na2PbO2 (метаплюмбат натрия, или
плюмбат)
3.
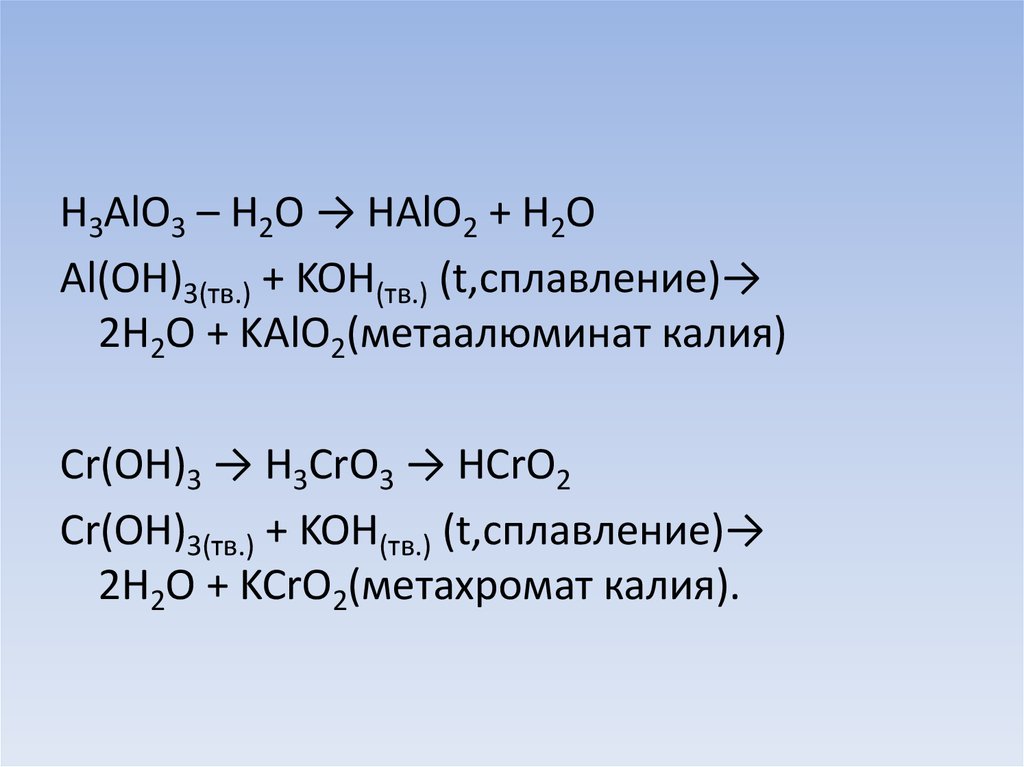
H3AlO3 – H2O → HAlO2 + H2OAl(OH)3(тв.) + KOH(тв.) (t,сплавление)→
2H2O + KAlO2(метаалюминат калия)
Cr(OH)3 → H3CrO3 → HCrO2
Cr(OH)3(тв.) + KOH(тв.) (t,сплавление)→
2H2O + KCrO2(метахромат калия).
4.
Степеньокисления
+2
+4
Формула
гидроксида
Sn(OH)2
Pb(OH)2
Sn(OH)4
Pb(OH)4
Формула
гидроксида в виде
кислоты
H2SnO2
H2PbO2
H2SnO3
H2PbO3
Соль(калиевая)
K2SnO2
K2PbO2
K2SnO3
K2PbO3
Название соли
станнИТ
блюмбИТ
метастаннА
Т
метаблюм
бАТ
5.
6. СПЛАВЛЕНИЕ!!!
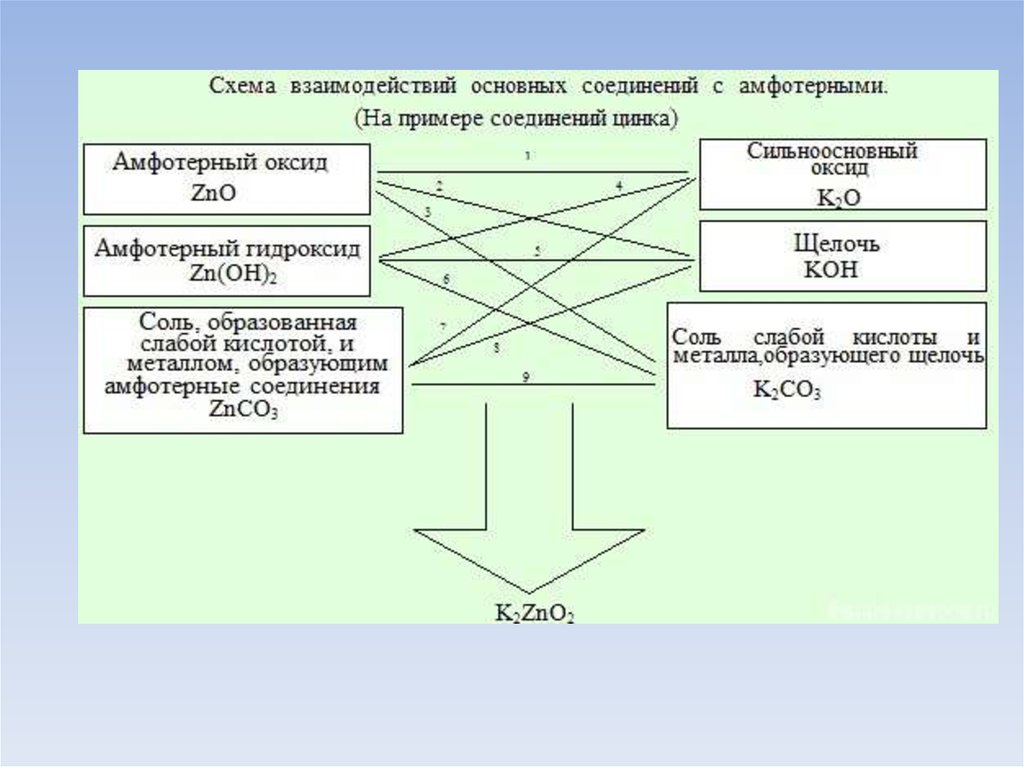
1. Амфотерного оксида с сильноосновным оксидом:ZnO(тв.) + K2O(тв.) (t,сплавление)→ K2ZnO2 (метацинкат калия/цинкат калия)
2. Амфотерного оксида со щелочью:
ZnO(тв.) + 2KOH(тв.) (t,сплавление)→ K2ZnO2 + H2O↑
3. Амфотерного оксида с солью слабой кислоты и металла, образующего щелочь:
ZnO(тв.) + K2CO3(тв.) (t,сплавление)→ K2ZnO2 + CO2↑
4. Амфотерного гидроксида с сильноосновным оксидом:
Zn(OH)2(тв.) + K2O(тв.) (t,сплавление)→ K2ZnO2 + H2O↑
5. Амфотерного гидроксида со щелочью:
Zn(OH)2(тв.) + 2KOH(тв.) (t,сплавление)→ K2ZnO2 + 2H2O↑
6. Амфотерного гидроксида с солью слабой кислоты и металла, образующего щелочь:
Zn(OH)2(тв.) + K2CO3(тв.) (t,сплавление)→ K2ZnO2 + CO2↑ + H2O↑
7. Соли слабой кислоты и металла, образующего амфотерные соединение с
сильноосновным оксидом:
ZnCO3(тв.) + K2O(тв.) (t,сплавление)→ K2ZnO2 + CO2↑
8. Соли слабой кислоты и металла, образующего амфотерные соединение со щелочью:
ZnCO3(тв.) + 2KOH(тв.) (t,сплавление)→ K2ZnO2 + CO2↑ + H2O↑
9. Соли слабой кислоты и металла, образующего амфотерные соединение с солью слабой
кислоты и металла, образующего щелочь:
ZnCO3(тв.) + K2CO3(тв.) (t,сплавление)→ K2ZnO2 + 2CO2↑
7. РАСТВОРЫ!!
Al2O3 + 2NaOH + 3H2O → 2Na[Al(OH)4]Al2O3 + 6NaOH + 3H2O → 2Na3[Al(OH)6]
2Al + 2NaOH + 6H2O → 2Na[Al(OH)4] + 3H2↑
2Al + 6NaOH + 6H2O → 2Na3[Al(OH)6] + 3H2↑
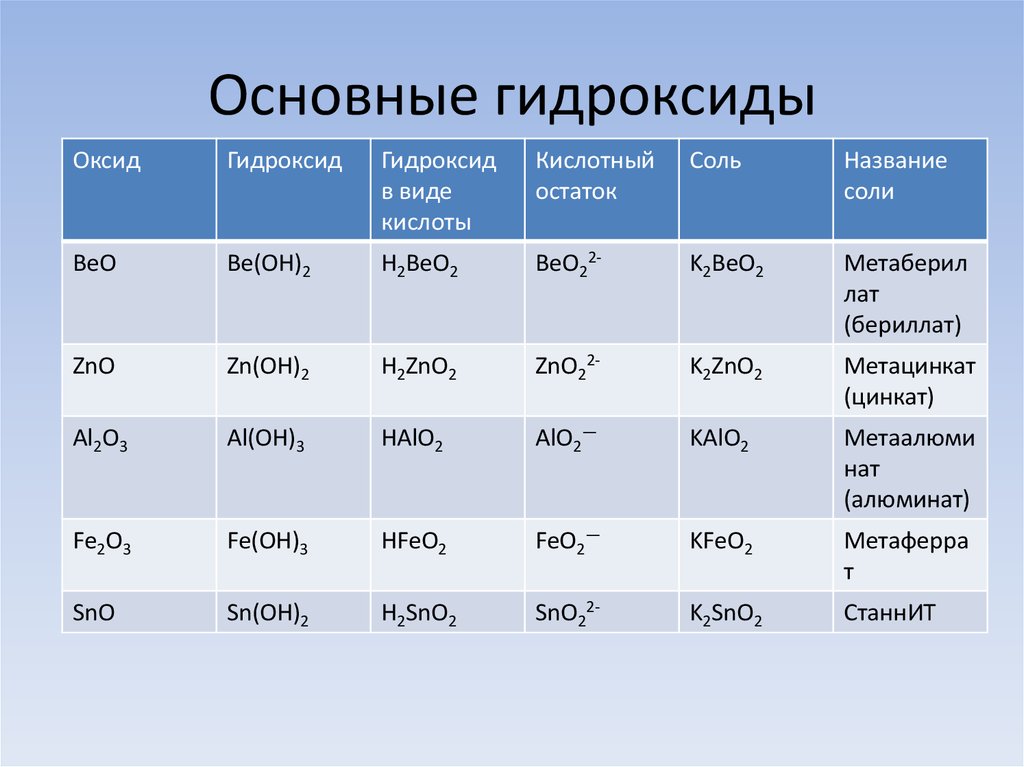
8. Основные гидроксиды
ОксидГидроксид
Гидроксид
в виде
кислоты
Кислотный
остаток
Соль
Название
соли
BeO
Be(OH)2
H2BeO2
BeO22-
K2BeO2
Метаберил
лат
(бериллат)
ZnO
Zn(OH)2
H2ZnO2
ZnO22-
K2ZnO2
Метацинкат
(цинкат)
Al2O3
Al(OH)3
HAlO2
AlO2—
KAlO2
Метаалюми
нат
(алюминат)
Fe2O3
Fe(OH)3
HFeO2
FeO2—
KFeO2
Метаферра
т
SnO
Sn(OH)2
H2SnO2
SnO22-
K2SnO2
СтаннИТ
9. Основные гидроксиды
ОксидГидроксид
Гидроксид
в виде
кислоты
Кислотный
остаток
Соль
Название
соли
PbO
Pb(OH)2
H2PbO2
PbO22-
K2PbO2
БлюмбИТ
SnO2
Sn(OH)4
H2SnO3
SnO32-
K2SnO3
МетастаннА
Т (станнат)
PbO2
Pb(OH)4
H2PbO3
PbO32-
K2PbO3
Метаблюмб
АТ
(плюмбат)
Cr2O3
Cr(OH)3
HCrO2
CrO2—
KCrO2
Метахрома
т
10.
1. Na[Al(OH)4] - Тетрагидроксоалюминатнатрия
Al(OH)3 + NaOH → Na[Al(OH)4]
Al2O3 + 2NaOH + 3H2O → 2Na[Al(OH)4]
2Al + 2NaOH + 6H2O → 2Na[Al(OH)4] + 3H2↑
2. Na3[Al(OH)6] -Гексагидроксоалюминат
натрия
Al(OH)3 + 3NaOH → Na3[Al(OH)6]
Al2O3 + 6NaOH + 3H2O → 2Na3[Al(OH)6]
2Al + 6NaOH + 6H2O → 2Na3[Al(OH)6] + 3H2↑
11.
3. K2[Zn(OH)4] -тетрагидроксоцинкат натрияZn(OH)2 + 2NaOH → Na2[Zn(OH)4]
ZnO + 2NaOH + H2O → Na2[Zn(OH)4]
Zn + 2NaOH + 2H2O → Na2[Zn(OH)4]+ H2↑
4. K4[Zn(OH)6] -гексагидроксоцинкат натрия
Zn(OH)2 + 4NaOH → Na4[Zn(OH)6]
ZnO + 4NaOH + H2O → Na4[Zn(OH)6]
Zn + 4NaOH + 2H2O → Na4[Zn(OH)6]+ H2↑
12.
5. Li2[Be(OH)4] -тетрагидроксобериллат литияBe(OH)2 + 2LiOH → Li2[Be(OH)4]
BeO + 2LiOH + H2O → Li2[Be(OH)4]
Be + 2LiOH + 2H2O → Li2[Be(OH)4]+ H2↑
6. Li4[Be(OH)6] -гексагидроксобериллат лития
Be(OH)2 + 4LiOH → Li4[Be(OH)6]
BeO + 4LiOH + H2O → Li4[Be(OH)6]
Be + 4LiOH + 2H2O → Li4[Be(OH)6]+ H2↑
13.
7. Na[Cr(OH)4] -тетрагидроксохромат натрияCr(OH)3 + NaOH → Na[Cr(OH)4]
Cr2O3 + 2NaOH + 3H2O → 2Na[Cr(OH)4]
8. Na3[Cr(OH)6] - гексагидроксохромат натрия
Cr(OH)3 + 3NaOH → Na3[Cr(OH)6]
Cr2O3 + 6NaOH + 3H2O → 2Na3[Cr(OH)6]
9. Na[Fe(OH)4] - тетрагидроксоферрат натрия
Fe(OH)3 + NaOH → Na[Fe(OH)4]
Fe2O3 + 2NaOH + 3H2O → 2Na[Fe(OH)4]
10. Na3[Fe(OH)6] -гексагидроксоферрат натрия
Fe(OH)3 + 3NaOH → Na3[Fe(OH)6]
Fe2O3 + 6NaOH + 3H2O → 2Na3[Fe(OH)6]
14.
Полученные в этих взаимодействиях солиреагируют с кислотами, образуя две
другие соли (соли данной кислоты и двух
металлов):
2Na3[Al(OH)6] + 6H2SO4 → 3Na2SO4 + Al2(SO4)3 +
12H2O











 chemistry
chemistry








