Similar presentations:
Рекомбинантные белки, современные способы получения и свойства
1. Рекомбинантные белки, современные способы получения и свойства
каф. мол. биологии, МГУ16.10.08
2. Общий метод получения рекомбинантного белка
1. Молекулярное клонирование гена или егофрагмента
2. Трансформация клеток, отбор клонов
3. Выращивание культуры или организма
4. Выделение и очистка белка
3. Молекулярное клонирование
4. Электропорация
25 мкФ = 2500 Впри 200 Ω за 5 мс
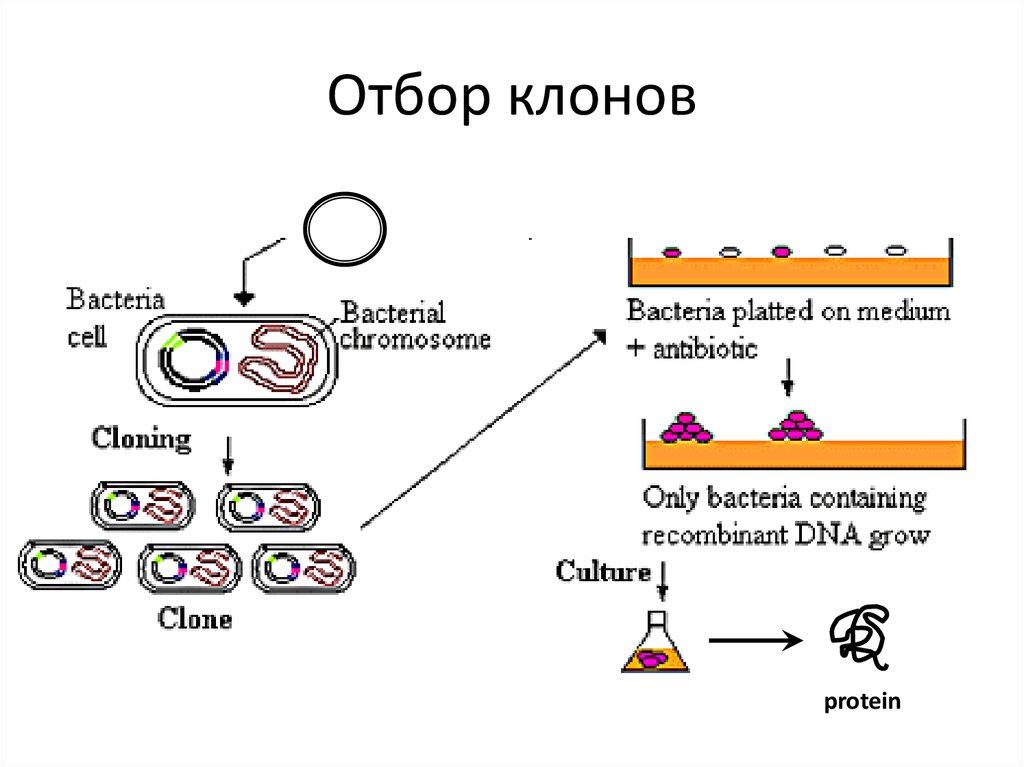
5. Отбор клонов
protein6. Использование рекомбинантных белков
•Научные исследования – внесение мутаций, гомогенныеферменты, структурные исследования, слитые белки,
антигены и т.д.
•Все остальное – биотехнологическое применение
7.
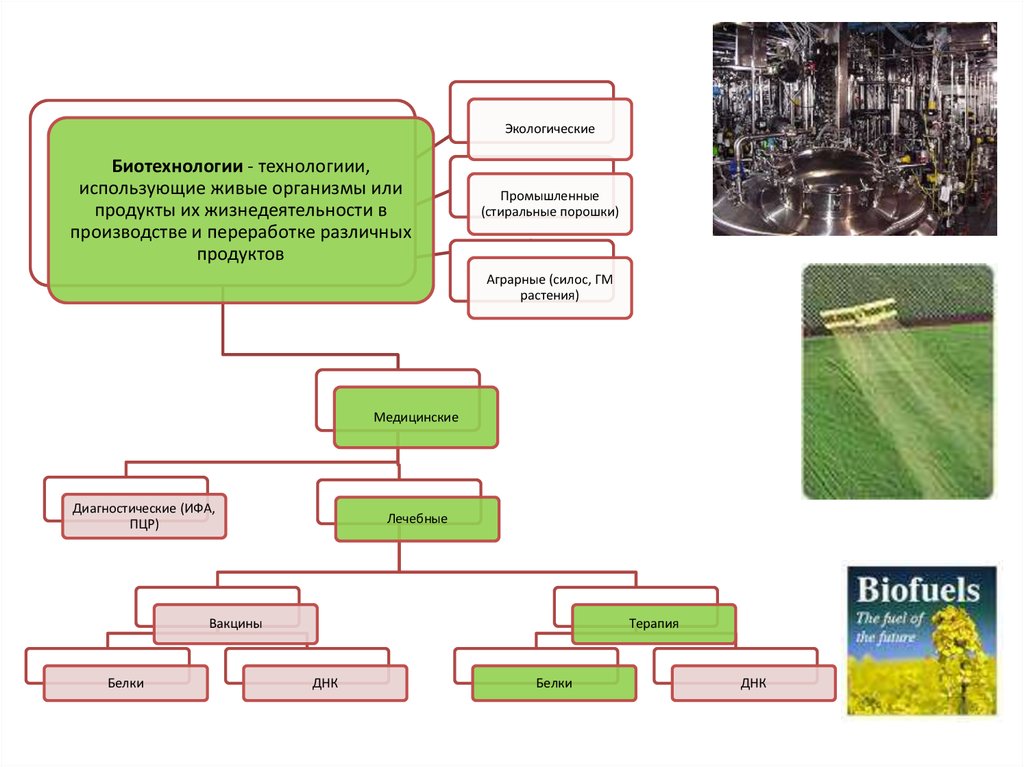
ЭкологическиеБиотехнологии - технологиии,
использующие живые организмы или
продукты их жизнедеятельности в
производстве и переработке различных
продуктов
Промышленные
(стиральные порошки)
Аграрные (силос, ГМ
растения)
Медицинские
Диагностические (ИФА,
ПЦР)
Лечебные
Вакцины
Белки
Терапия
ДНК
Белки
ДНК
8.
МедицинскиеЛечебные
Терапия
Вакцины
ДНК генотерапия,
антисенстехнология, siRNA.
аптамеры,
рибозимы
Белки
Белки
ДНК-вакцины
Из прирдных
источников
Синтетические
Рекомбинантные
Культивируемые
клетки
Трансгенные
животные
9. Рекомбинантные белки для лечения заболеваний: особые требования
• Высокая степень очистки• Точная копия природного белка или научные
доказательства безопасности мутаций для пациентов
• Проверенный, стабильный и безопасный продуцент
• Как можно более полное удаление ВСЕХ биополимеров
и пирогенов продуцента (ДНК <10 пг/мг)
• Раствор или порошок, в котором белок полностью
сохраняет свои свойства не менее 1 года
• Полная демонстрация стабильности, качества и
обоснованности процесса получения – GMP (Good
Manufacturing Process)
10. Используемые системы экспресии
• Бактерии Esherichia coli и Bacillus subtilis• Дрожжи Saccharomyces cerevisae и Pichia
pastoris
• Линии клеток млекопитающих CHO, BHK, A293
• Трансгенные животные
11. Экспрессионный вектор
• Точка инициациирепликации - ORI
• Селекционные
маркеры
• Промотор целевого
гена
• Терминатор
транскрипции
• Полилинкер - MCS
12. Бактерия Esherichia coli
Преимущества• Быстрый рост (6-12 часов от
посева до окончания
индукции)
• Относительно высокий
выход целевого белка (1002000 мг/л)
• Низкая цена ростовой среды
(натуральные простые
компоненты)
• Низкая стоимость
ферментации
• Возможность получать
микрокристаллы целевого
белка (тельца включения)
Недостатки
• Затруднен биосинтез крупных
полипептидов (>50 кДа)
• Нет системы гликозилирования
• Ограниченные возможности
секреции белков
• Многие гетерологичные белки
токсичны для клеток
• Затруднено образование
дисульфидных связей
• Многие гетерологичные белки
образуют только тельца
включения
13. E.coli – пример системы экспресии
• Внехромосомнаярепликация вектора
• Индуцибельный
промотор
• Специальный штамм
• Дополнительный остаток
Met[-1] или лидерный
пептид
• Блок стоп-кодонов
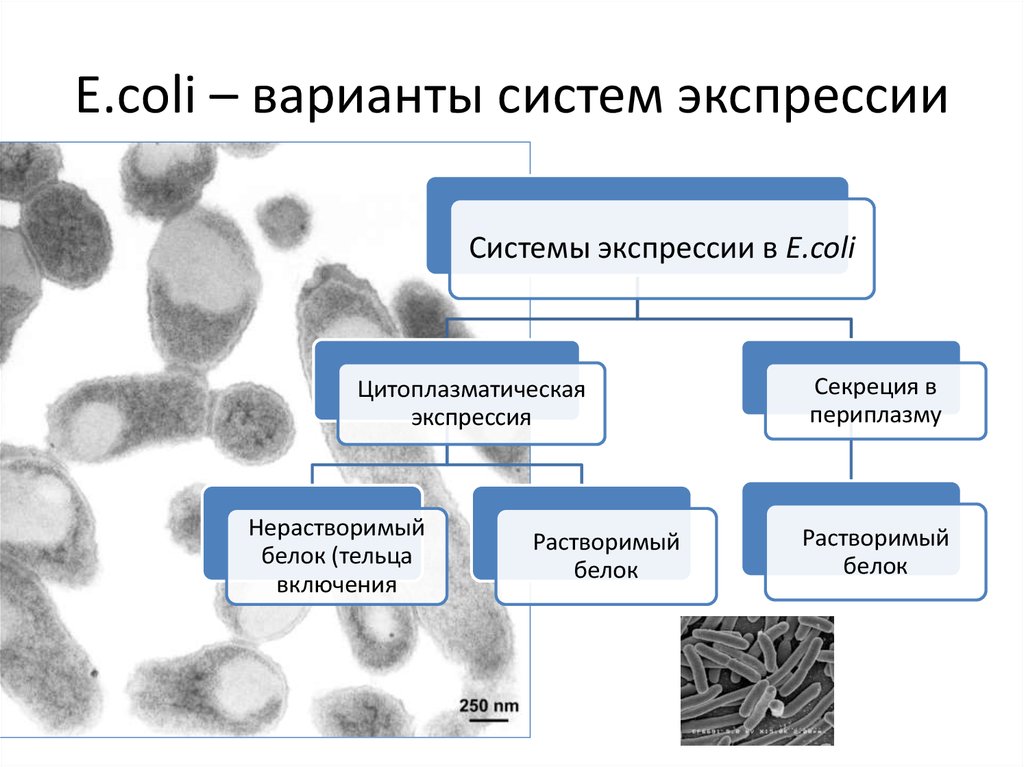
14. E.сoli – варианты систем экспрессии
Системы экспрессии в E.coliЦитоплазматическая
экспрессия
Нерастворимый
белок (тельца
включения
Растворимый
белок
Секреция в
периплазму
Растворимый
белок
15. E.coli – примеры использования
БелкиBactericidal/permeability-increasing Protein,
rDNA
Carboxypeptidase, rDNA
G-CSF, rDNA/Amgen
GM-CSF, rDNA/Schering-Plough
Hyaluronidase, rDNA
Insulin-like Growth Factor-1, rDNA/Tercica
Interferon alfa-2a, rDNA
Interferon alfa-2b, rDNA
Interferon alfacon-1, rDNA
Interferon betaser, rDNA/Berlex
Interferon gamma, rDNA
Interleukin-1ra, rDNA
Interleukin-11, rDNA
Interleukin-2, rDNA/Chiron
Keratinocyte growth factor, rDNA
Somatropin, rDNA/
Somatropin antagonist, rDNA, PEGT4 Endonuclease, rDNA, Liposomal
TNF, rDNA
tPA, rDNA/PDL
Urokinase Plasminogen Activator, rDNA
Слитые белки
Interleukin-13–Pseudomonas toxin, rDNA
Interleukin-2/diphtheria toxin, rDNA
Вакцины
Cholera Vaccine (rDNA)/SBL
Staphylococcus vaccine (rDNA)
Anthrax Vaccine, rDNA/VaxGen
Lyme Vaccine, rDNA/Aventis
Pertussis Toxoid, rDNA
Пептиды
Calcitonin, rDNA
Glucagon, rDNA/Lilly
Insulin, rDNA/Lilly
Insulin glargine, rDNA
Natriuretic peptide, rDNA
Parathyroid hormone (1-34), rDNA
Parathyroid hormone (1-84), rDNA
Антитела и фрагменты
антител
Complement C5 Mab, rDNA
Heat shock protein Mab Mab, rDNA
TNF Mab Fab', rDNA, PEGVEGF Mab Fab, rDNA
16. Дрожжи Pichia pastoris
ПреимуществаОтносительно быстрый рост (3-5
дней от посева до окончания
индукции)
Высокий выход целевого белка (до
40 г/л)
Очень низкая цена ростовой среды
(глицерин, метанол, аммиак)
Умеренная стоимость
ферментации
Возможна экспрессия крупных
полипептидов (>50 кДа)
Возможно гликозилирование
Секреция белка в ростовую среду,
низкий уровень секреции протеаз
Недостатки
N-гликозилирование дает
иммуногенные олигосахариды
Не все белки эффективно
секретируются
Патентные ограничения на
промышленное использование
17. P.pastoris – получение продуцента
18. P.pastoris – схема ферментации
19. P.pastoris – примеры использования
• Alfimeprase - Accfib; 3203-fibrolase (3-serine)(Agkistrodon contortrix
recombinant)
• DX-88; ecallantide;
kallikrein inhibitor
protein, recombinant
20. Линия клеток CHO
Преимущества• Пригодна для белков любого
размера
• Любые пост-трансляционные
модификации
• Не содержит трансмиссивных
вирусов
• Существует сублиния DG44,
дефектная по гену DHFR (легкая
амплификация кассет)
Недостатки
• Большое время создания
продуцента (до 1 года)
• Медленный рост ( промышленное
культивирование до 200 дней)
• Требует соблюдения полной
стерильности и защиты от
заражения вирусами
• Некоторые ферментные системы
пост-трансляционных модификаций
имеют ограниченные возможности
и требуют оверэкспрессии генов
• Ограниченный пролиферативный
потенциал (до 25 пассажей)
• Дорогая культуральная среда
21. CHO – вариант системы экспресии
• Внехромосомнаярепликация вектора
• Индуцибельный
промотор
• Специальный штамм
• Дополнительный остаток
Met[-1] или лидерный
пептид
• Блок стоп-кодонов
22. Methotrexate (MTX) Selection
Gene of interestDHFR
Transfect
dfhr- cells
Grow in
Nucleoside
Free medium
Culture a
Colony of
cells
Grow in
0.05 uM Mtx
Culture a
Colony of
cells
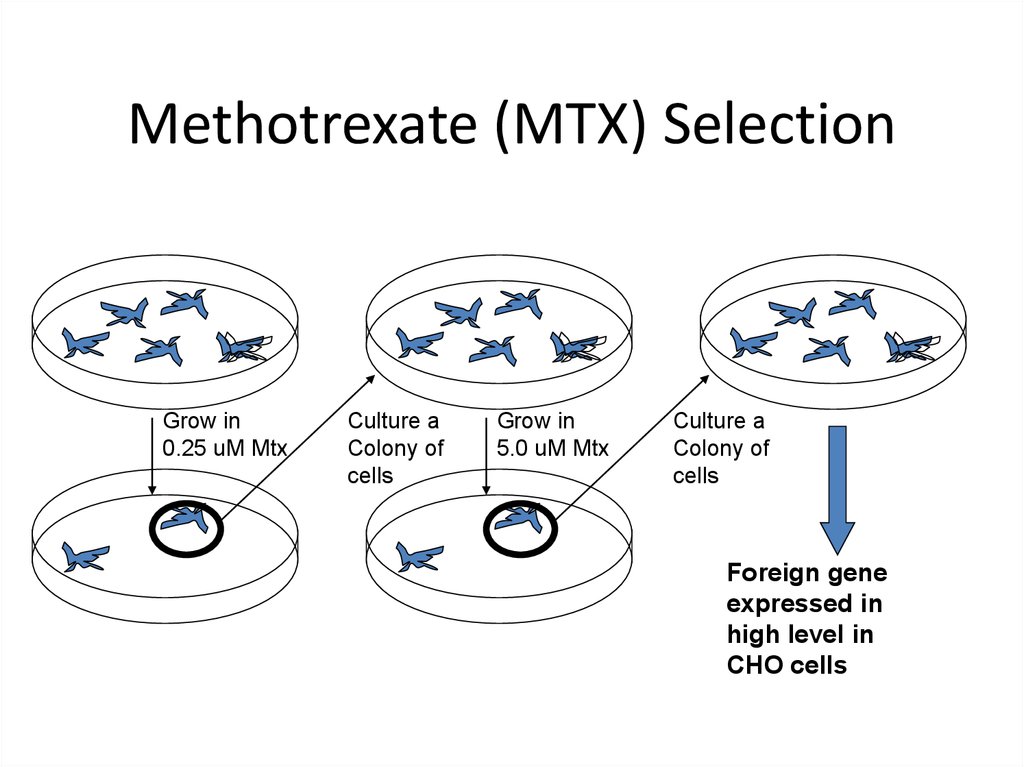
23. Methotrexate (MTX) Selection
Grow in0.25 uM Mtx
Culture a
Colony of
cells
Grow in
5.0 uM Mtx
Culture a
Colony of
cells
Foreign gene
expressed in
high level in
CHO cells
24. CHO – примеры использования
Гормоны и цитокиныАнтитела
•Bone Morphogenic Protein-2, rDNA
•Bone Morphogenic Protein-7, rDNA
•EPO, rDNA/Amgen
•EPO, darb-, rDNA
•Corifollitropin alfa, rDNA
•FSH rDNA/Schering-Plough
•G-CSF, rDNA/Sanofi
•Luteinizing hormone, rDNA
•Interferon beta-1a, rDNA/Biogen
•Insulin-like Growth Factor-1/IGFBP-3, rDNA
•Thyroid stimulating hormone, rDNA
•hCG, rDNA
•CD11a Mab, rDNA
•CD20 Mab, rDNA
•CD20 Mab, rDNA conc.
•CD20 Mab, rDNA/Y-90 & In-111 radioconj.
•CD52 Mab, rDNA
•EGF receptor Mab, human, rDNA/Amgen
•HER2 receptor Mab, rDNA
•Immunoglobulin E Mab, rDNA
•RANKL Mab, rDNA
•TNF Receptor-IgG Fc, rDNA
•VEGF Mab, rDNA
•CTLA4-Ig, rDNA
•LFA-3/IgG1, rDNA
Ферменты
Система свертываемости крови
•Arylsulfatase B, rDNA
•DNase, rDNA
•Galactosidase, beta rDNA
•Glucocerebrosidase, rDNA
•Glucosidase, rDNA
•Iduronidase, rDNA
•Factor IX, rDNA/Wyeth
•Factor VIII, rDNA/Baxter
•Factor VIII BDD, rDNA, PFM
•tPA, rDNA/Genentech
•tPA, TNK-, rDNA
•Thrombin, rDNA
25.
Иван И. Воробьев,лаборатория медицинской биотехнологии
Гематологического научного центра РАМН,
лаборатория биокатализа Института
биоорганической химии РАН,
ptichman@gmail.com
Слайды можно скачать:
lmbt.ru/lectures/kmb08.ppt





















 biology
biology