Similar presentations:
:Химиялық реакциялардың кинетикалық жіктелуі.Ферментті катализ.Ферменттердің әсер ету ерекшеліктері
1. Қарағанды Мемлекеттік Медицина Университеті Химия курсы мен фармацевтикалық пәндер кафедрасы СӨЖ Тақырыбы:Химиялық
реакциялардың кинетикалықжіктелуі.Ферментті катализ.Ферменттердің әсер ету
ерекшеліктері.
Орындаған:Абулов Ш.Р.
117 топ
Тексерген:Сәрсенбекова А.Ж
Қарағанды 2011ж
2. Жоспар
• Кіріспе• Негізгі бөлім
1. Химиялық реакциялардың кинетикалық
жіктелуі.
2. Катализ.
3. Ферментті катализ
4. Ферменттердің әсер ету механизмдері.
• Қорытынды
• Пайдаланылган әдебиеттер.
3. 1)Химиялық реакциялардың кинетикалық жіктелуі.
1)Химиялық
реакциялардың
кинетикалық жіктелуі.
Химиялық кинет ика-химиялық реакцияның жылдамдығын
және oғaнәрт урлi факт орлардың әcepiн, реакцияның журу
механизмiн зерттейдi
.
Химиялық реакцияның жылдамдығы дегенiмiз белгiлi бiр
уақытта әрекеттесет iн заттар мелшерiнiң згеруiн айт ады.
Мыс: белгiлi бiр уақыт аралығында
болғанда, әрекеттесушi заттардың концент рациясы да
өзгередi, яғни кемидi:
Сонда химиялық
реакцияның орт аша жьшдамдығы
уақыт аралығында
тең болады.
Теңдеудiң сол жағындағы (-) белгi, химияльық реакция
барысында әрекеттесушi заттардың концент рациясының
кемит iндiгiн,cоғaн орай реакция жылдамдығының
баяулайт ындығын керсет едi.
4. Химиялық реакциялардың кинетикалық жіктелуі.
Химиялық реакциялардың кинет икалық жікт елуі.Әрекеттесушi заттардьң концент рациясын, әдeттe ерiт iндiнiң белгiлi бiр
келемiнде epiген заттың моль санымен керсет едi (моль/л), ал уақытты сек.
не мин. керсет едi. Химиялық реакция жылдамдығынмреакцияға қат ысушы
заттардыц бiрiнiң концент рациясының азаюы аркылыда керсет уге болады
Реакцияның орт аша жышдамдығын әрекеттесушi заттың концент рациясының
шексiз езгеруiнiн ең шексiз кiшкене yaқыт аралығына қат ынасы өлшемiмен
керсет едi:
Химиялық реакция жылдамдығын реакцияға қат ысқан заттардың
табиғат ына, (ерiт кiшт iң т абиғат ына) реагенттердiң концент рациясына,
температ ураға және кат ализат ордың қат ысу қат ыспауына т iкелей т әуелдi
болады. Реакцияға қат ысат ын заттардың агрегаттық куйiне байланыст ы
химиялық реакция гомогендiк және гет ерогендiк болып екі т опқа бөлiнедi.
Әрекеттесет iн және т үзiлет iн заттар бiрдей агрегаттьқ күйде болат ын
химиялық реакцияны гомогендiк деп, ал қат ысат ын не т үзiлет iн заттардың
агрегаттық куйi әр т үрлi болат ын реакцияны гет ерогендiк деп ат айды.
5. Химиялық реакциялардың кинетикалық жіктелуі.
Химиялық реакциялардың кинет икалық жікт елуі.Гомогендiк реакция, гет ерогендiк реакцияға қарағанда
жылдамырақ журедi. Гет ерогендiк реакцияныц жылдамдығы
әрекеттесушi заттардыңжанасу бет кейiнiң көлемiне,
дисперсиялық дәрежесiне т iкелей байланыст ы. Егер
әрекеттесушi заттар газ куйiнде болса, химиялық реакцияның
жылдамдығы қысымға т iкелей байланыст ы болады, себебi
қысымның езгеруiне байланыст ы әрекеттесушi заттардыц
концент рациясы да езгередi. Әрекеттесушi заттардың
концент рациясы химиялық реакция жылдамдығына қалай
әcep ет едi?
Химиялық реакция журу ушiн әрекеттесушi заттардың
молекулаларыбiрiмен-бiрi соқт ығысулары қажет . Бiрақ әрбiр
соқт ығысқан сайын бөлшект ер әрекеттece бермейдi.
6. Химиялық реакциялардың кинетикалық жіктелуі.
Химиялық реакциялардың кинет икалық жікт елуі.• Белгiлi бiр келемде белшект ердiң, молекулаларының саны
неғұрлым көп болса, соғұрлым әpeкeттecy нәт ижелi болады.
Коновалов және 1864 жылы норвег ғалымдары К. Гулъберг
пен П. Baaгeннің; ашқанан әрекеттесушi массалар заңы
бойынша «Тұрақт ы т емперат урадағы химиялык реакцияның
жылдамдығы,ст ехиомет риялық коэффиценттерi дәреже
керсет кiш т урiнде әрекеттесушi заттардың
концент рацияларының кебейт iндiсiне т ура пропорционалдық
тәуелдiлiкт е болады». Мыс: мына схема бойынша журет iн
яғни А-В т ипт i мономолекулалық реакциялардың
жълдамдығы т өмендегiдей кинет икалық т ендеумен
керсет iледi:V=K [А]=К.[А] немесе V=кСл=КСл[А] не СА - А
зат ының сол кезендегi концент рациясы; К жылдамдықконст ант асы, егер А зат ының концент рациясы [А]
= lмолъ·л болса, V = К болады. К-А зат ының т абиғат ына,
температ ураға, кат ализат ордың қат ысуына т әуелдi болады
да, концент рациясына т әуелсiз болады. Жылдамдық
конст ант асы неғұрлым көп болса, реакция жът лдамдығы
соғұрлым т езiрек болады.
7. 2)Катализ
Химиялық езгерiст ердiң маңызды реттегiшi кат ализат орлар
болып т абылады. Кат ализат орлар реакция компоненттерiмен
аралық химиялық әрекеттесуге бiрнеше рет кат ысып,
құрамын сол күйiнде сақт ап қалуы нәт ижесінде химиялық
реакция жылдамдығын езгерт ет ін заттар.
Кат ализат ор кызмет i берiлген реакцияның акт ивт ендiру
энергиясынт емендет iп, оның жаңа т иiмдi жолмен жүруiн
қамт амасыз ет едi.
Егер А + В → АВ реакциясы Еа акт ивт ендiру энергиясын
иемденсе (сурет 1), онда кат ализат ор (к) аралық өнім А + К
→ AК т үзуi арқылы Еа шамасын т емендет едi. Онда АК
комплекс В компонент пен әрекеттеседi. Бұл реакция Еа
салыст ырғанда акт ивт ендiру энергиясы т өмен жағдайда
журедi. Сонымен, әрекеттесудiң қосындысы нәт ижесiнде АВ
өнімі т үзiлдi, ал кат ализат ор реакциядан езгерiссiз қалады.
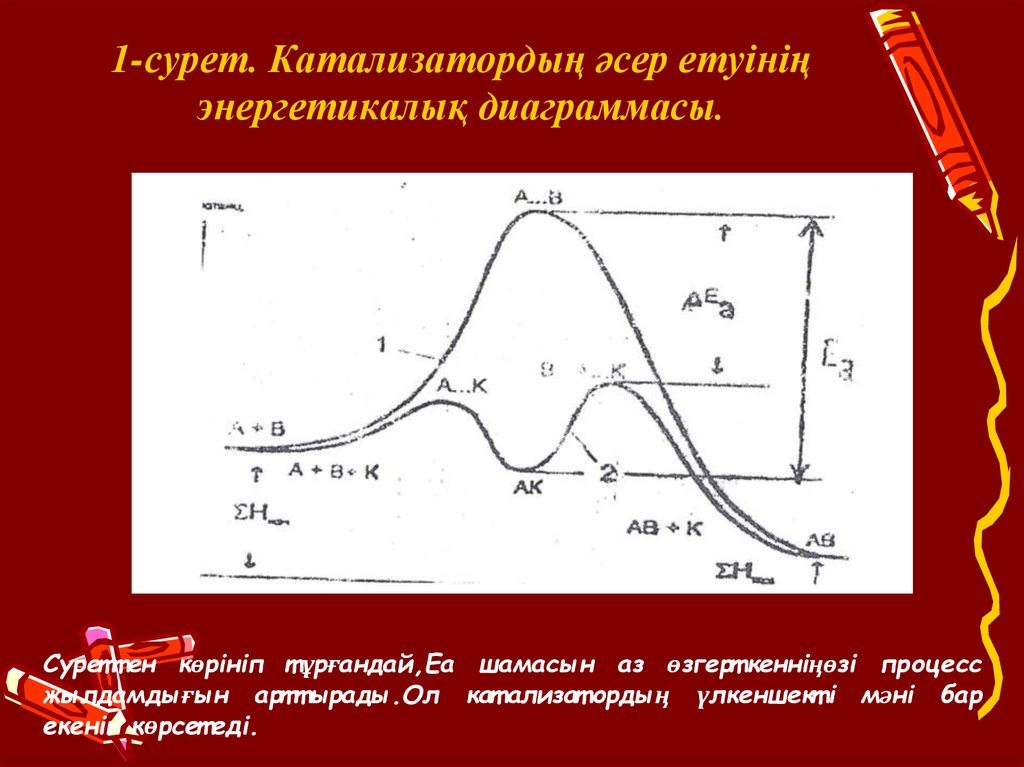
8. 1-сурет. Катализатордың әcep eтyiнің энергетикалық диаграммасы.
Суретт ен көрiнiп т ұрғандай,Еа шамасын аз өзгерт кеннiңөзi процессжылдамдығын артт ырады.Ол кат ализат ордың үлкеншект i мәні бар
eкенін көрсет едi.
9. Катализ eкiгe бөлiнедi 1) оң (реакция жылдамдығы артады) және 2)теріс(реакция аз жылдамдықпен өтедi).
Соңғы кат ализдiң т ypін ингибирлеу деп ат айды. Ингибит орлер
практ икада консерванттар,ант иоксиданттар және т .б. рет iнде
қолданылады. Ингбирлеу оң кат ализ сияқт ы биопроцест ердiң
жылдамдықт арын реттеу ушiн қажет .
Егер реакция нәт ижесiнде т үзiлген өнім жылдамдыққа әcep ет се,
оны авт окат ализ деп ат айды. Авт окат ализ мысалына КМn04
тот ығyын келт iредi, оның жылдамдығының арт уы реакциялық
орт ада жүрген кат ионының әсерінен жүзеге асады
.
10. Катализ бөлінеді: 1)Гомогенді 2)Гетерогенді
Гомогендi кат ализде кат ализат ормен реакцияға қат ысат ын
заттар бiрт ект i жүйе т үзедi (әдeттe сұйық немесе газды).
Мысалы, СО-ның СО2 дейiн т от ыry су буының әcepiнен
жүредi.
Гет ерогендi кат ализде кат ализат ор реакцияға т үceт iн
заттардан бөлек фаза кұрайды да, кат алит икалық процесс
жүйенiң бөлiну шекарасында өт едi. Гет ерогендi
кат ализат орлар рет iнде мет алдар және олардың оксидт ерi
және т .б. пайдаланылады. Гет ерогендi кат ализдiц т еориясы
ет е күрделi .
Кат ализде микрогет ерогендi кат ализ ерекше орын алады,
онда кат ализат ор коллоидт ы немесе жоғары молекулалық
күйде болады. Мысалы рет iнде биокат ализат орферменттердiң әcepiнeн жүрет iн барлық биопроцест ердi
келт iруге болады .
11. 3)Ферментті катализ
Ферменттер ағзада журет iн химиялық реакциялардың
кат ализат орлары болып т абылады. қазiргi кезде 10000 жуық
биохимиялық реакция белгiлi, олардың әрқайсысы
ферменттердiң қат ысуында жузеге асырылады.
Ферменттердiң ерекше қасиет i – жоғарғы т иiмдiлiriнде.
Мысалы, сут ект iң aсқын т от ығyының ыдырауы
кат ализат орсыз акт ивт ендiру энергиясы 75 кДж/моль,
гет ерогендi кат ализде плат инаның әcepiненакт ивт ендiру
энергиясы 48 кДж/мольге дейiн т өмендейдi,ал фермент кат алазаның қат ысуында акт ивт ендiру энергиясының шамасы
небарi 23 кДж/мольге ие болады. Мұндай акт ивт ендiру
энергиясының езгерiсi реакция жылдамдығын 20 000 және
3-1011 есе арттыруға әкелiп соқт ыpaды.
Aқсыл заттардың НСl әcepiнeн гидролизге ұшыpayы ушiн
акт ивт ендiру энергиясы 80 кДж/моль болу кажет , ал ақазан
сөлiнде кездесет iн фермент т рипсиннiң қат ысуында оның
шамасы 50 кДж/моль болады, сөйт iп асқазанның ақсыл
затты, т ағамды сіңіруі іске асырылады.
12. Ферментті катализ
Бiр моль фермент 1000-100000 моль затты бiр секунд iшiнде
тасымалдап фермент i жоқ реакцияның жылдамдығын 1010_101 есе
арттырады. Ферменттiң мыдадай әcep кepceт yi, бiрiншiденферменттiң концент рациясына т әуелдi, яғни ферменттiң
концент рациясы apт қaн сайын оның субст ратты өзiне сорбциясы өсiп
реакция жыдамдығын мың есе арттырады.
Екiншiден-ферменттер кеңiст iкт iк бағдарлану құбылысын т аныт ады,
ол реакция жылдамдығын шамамен мың есе арттырады. Осы
құбылыс негiзiнде фермент пен субст рат кеңiст iкт е оңт айлы
туйiседi.
Үшiншiден-ферменттер полифункциялық эффект ке ие,ол олардың
шешiмдi мацызын көрсет едi. Бұл эффект iң негiзiнде субст раттың
молекуласына бiр уақытта бiрнеше шабуылдайт ын ферменттер
тобының әсерінде жат ыр.
13.
Ферменттердiң акт иват орлары рет iнде мет алл иондары немесе
органикалық молекулалар болып т абылады, оларға нуклеот идт ер
немесе вит аминдер (дәpyмeндep) жат ады. Оларды коферменттер деп
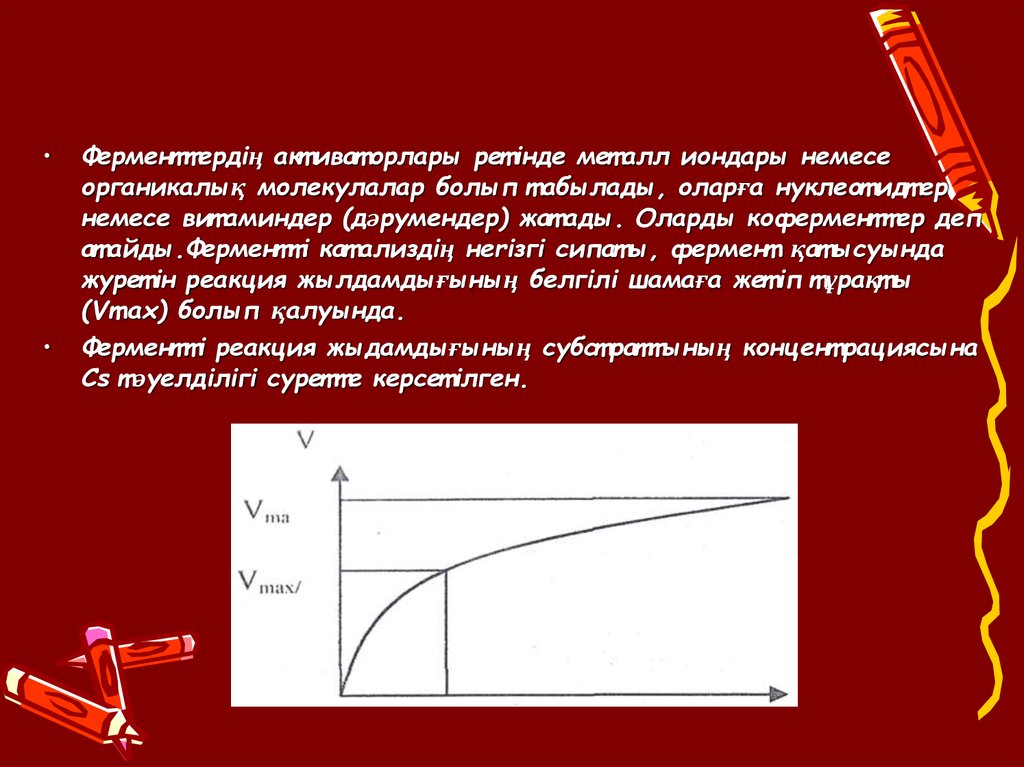
ат айды.Ферменттi кат ализдiң неriзгi сипат ы, фермент қат ысуында
журет iн реакция жылдамдығының белгiлi шамaға жет iп т ұрақт ы
(Vmах) болып қалуында.
Ферменттi реакция жыдамдығының субст раттының концент рациясына
Cs т әуелдiлiгi суретте керсет iлген.
14. Ферментті катализ
Ферментті кат ализФерменттi реакция жылдамдығының субст рат
концент рациясына т әуелдiлiгi 1913 жылы Михаэлис пен
Мент ен осы т әуелдiлiкт iң т еориясын ұсынaды. Ферменттi
процест iң схемасын былай ұсынуға болады:
Концентрациясына турапропорционал
Ондағы Е және S фермент және субст рат , ЕS-аралық фермент субст ратт ы комплекс, Р-реакция өнімі, ал К1-з реакцияларға сәйкес
жылдамдық т ұрақт ылығы.
Реакция өнімі Р т узiлуiнiң баст апқы
жылдамдығы
аралық
комплекст iң
Концент рациясына
турапропорционал .
15. Ферментті катализ
Ферментті кат ализБасқа жағынан, реакция жылдамдығы барлық үшреакциялардың
жылдамдықт арымен анықт алынады.
Ферменттің концентрациясы бiрнеше уақыт аралығынан кейiн
былай көpiнic бередi
Қайтымды процесте тепе-тецдiк куйiнде ES комплекстiц
тузiлу жылдамдығы V,оның ыдырау жылдамдыңына V2+ Vз
тең
16. Ферментті катализ
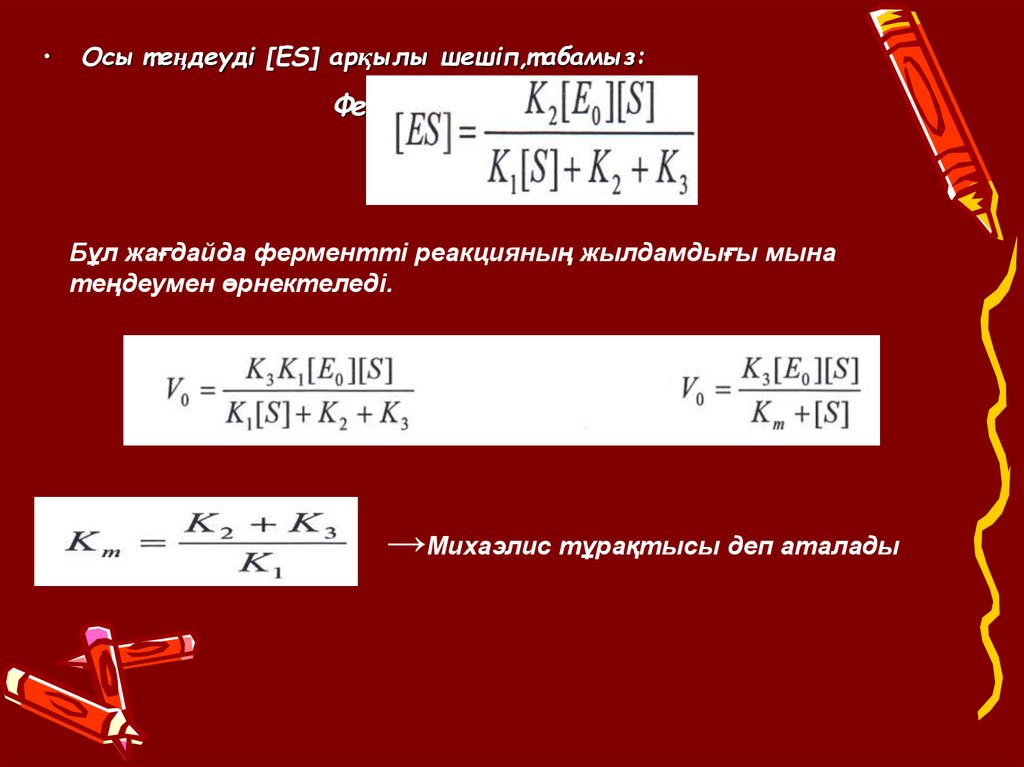
Осы т еңдеуді [ES] арқылы шешiп,т абамыз:
Ферментті кат ализ
Бұл жағдайда ферменттi реакцияның жылдамдығы мына
теңдеумен өрнектеледі.
→Михаэлис тұрақтысы деп аталады
17. Ферментті катализ
Ферментті кат ализКинет икалық зерттеуде максималды жылдамдық V mах шамасы
пайдаланылады, яғни ферменттің комплекс т үрiнде ES
жылдамдығы. Онда [Eo]=[ES], Vmах Кз[ЕS]-Кз[Ео]Осы мәндердi
алдындағы т еңдеуге қойып мына т еңдеудi аламыз:
Егер
болса, онда Кт = [S]
Михаэлис тұрақтысы рН, температураға, субстрат табиғатына және
басқа факторларға тәуелдi.
18. Ферментті катализ
Ферментті кат ализФерменттер адам өмiрiнде ерт е кезден қолданылады. Ашыт у,
қышқылдау құбылыст ары, жемiс-жидект ердi өңдеу
процест ерiнiң негiзiнде фермент гiк кат ализ процест ерi жат ыр.
• Кейiнгi кездерi медициналық энзимология қарқынды
түрде дамып келе жат ыр, ол ферменттi дәрiлiк заттар
рет iнде пайдаланумен шұғылданады, сонымен қaт ap
ферменттер көмeгiмeн диагност ика әдiсiн ойлап т абуда
кең көлемдi жұмыст ар жүргiзiлiп жат ыр.
• ХИМИЯЛЬIҚ кинет ика заңдылықт арының медицина
ғылымына колдану т абуы - фармокинет ика және
токсикинет ика, оның мақсат ы дәрiлiк зат rардың және
улы зат гардың әcep ет у жылдамдығы мен ағзадан
шығарумен шұғылдану болып т абылады.
19. 4)Ферменттердің әсер ету ерекшеліктері
• Сур. 8.Сур. 9.
Ферменттік реакция жүруі үшін фермент субст рат қа әсер ет уі
қажет . Бұл т ек фермент молекуласындағы акт ивт і
орт алықт ың құрылымына жанасу, кат алиттік орт алықт ың,
ғана емес сонымен бірге субст раттың да химиялық
құрылысының ерекшелікт еріне байланыст ы болады. Фермент
пен субст рат бір біріне сәйкес келуі қажет , немесе фермент
өзі әсер ет ет ін субст ратты т анып біледі. Бұл үшін фермент
құрылымындағы жанаст ырушы орт алықт ың қызмет і ерекше.
Жанаст ырушы орт алықт ың көмегімен реакцияласушы зат фермент -субст рат комплексі т үзіледі.
20.
Субстраттық әсерлесу ерекшеліктері.Субстраттық (талғамдылық) әсерлесу ерекшелігі —
бұл фермент молекуласының бір субстратқа немесе
химиялық байланыстары мен топтары ұқсас
бірнеше субстраттар топтарына әсері етуі қабілеті.
Ферменттердің субстраттық әсерлесу ерекшелігі
(талғамдылығы) оның активті орталығының
субстратпен комплементарлы болып келуіне тәуелді
болады. Субстраттық талғамдылықты шартты түрде
үш түрге бөледі:
21. Ферменттердің әсер ету ерекшеліктері
:
1. Абсолюттік субстраттық әсерлесу ерекшелігі (талғамдылық) -бұл
ферметтің тек белгілі бір ғана субстратқа әсер ету қабілеті. Мысалы,
уреаза ферменті тек мочевинаның гидролиттік ыдырау реакциясын
катализдейді, ал ұқсас құрылыстағы метилмочевинаға әсер етпейді:
Глюкокиназа ферменті гликолиттік ыдырау реакциясында тек глюкозаға әсер етеді.
22. Ферменттердің әсер ету ерекшеліктері
Субст раттық әсерлесу ерекшелікт ері. Субст раттық
(т алғамдылық) әсерлесу ерекшелігі — бұл фермент
молекуласының бір субст рат қа немесе химиялық
байланыст ары мен т опт ары ұқсас бірнеше субст раттар
топт арына әсері ет уі қабілет і. Ферменттердің субст раттық
әсерлесу ерекшелігі (т алғамдылығы) оның акт ивт і
орт алығының субст рат пен комплемент арлы болып келуіне
тәуелді болады. Субст раттық т алғамдылықт ы шартты т үрде
үш т үрге бөледі:
1. Абсолюттік субст раттық әсерлесу ерекшелігі
(т алғамдылық) -бұл ферметтің т ек белгілі бір ғана
субст рат қа әсер ет у қабілет і. Мысалы, уреаза фермент і т ек
мочевинаның гидролиттік ыдырау реакциясын кат ализдейді,
ал ұқсас құрылыст ағы мет илмочевинаға әсер ет пейді:
Глюкокиназа фермент і гликолиттік ыдырау реакциясында т ек
23. 4)Ферменттердің әсер ету ерекшеліктері
2. Субстраттық стереохимиялық әсерлесу ерекшелігі (талғамдылық)— бұл ферменттің тек бір ғана оптикалық (D немесе L), немесе,
геометриялық (цис-, немесе тране-) изомерге әсер ету қабілеті.
Мысалы, протеолиттік ферменттердің тек L-аминқышқылдардан
түзілген пептидтерге әсер етуі немесе L-аминооксидаза мен Dаминооксидазаның әсер етуі, лактатдегидрогеназаның тек L-сүт
қышқылына әсер етіп, D-сүт қышқылына әсер етпеуі жатқызылады.
24. 4)Ферменттердің әсер ету ерекшеліктері
Ферменттік әсерлесу ерекшелігі. Ферменттердің әсеріндегі
талғамдылығы — бұл бір субст рат қа әрт үрлі ферменттердің
әсер ет іп әрт үрлі т ек өзіне ғана т ән реакцияларды
кат ализдеуге қабілеттілігі.
E1, E2, E3 — ферменттерP1, P2, P3 — өнімдерS — субст рат
Ферменттер (Е1, Е2, Е3) т ек өздеріне ғана т ән әсерлесу
талғамдылығына қабілетті және олар бір ғана субст рат қа (S)
әсер ет еді. Бірақ әрбір фермент т ек бір ғана т ипт егі
реакцияны жүрт ізеді. Бұл т алғамдылықт ың ерекшелігі
фермент молекуласының кат алиттік орт алығындағы
реакцияласушы т опт ардың қасиет іне (жай ферменттерде)
және кофакт орлардың химиялық қасиеттеріне (күрделі
ферменттер) т ығыз байланыст ылығында.
25. 5)Пайдаланылган әдебиеттер.
• 1)Ә.К.Пат саев,С.А.Шит ыбаев,Қ.Н.Дәуренбеков,
• «Бейорганакалық және физколлойдт ық
химия» Шымкент 2004ж.
• 2)Ә.К.Пат саев,С.А.Шит ыбаев,
«Бейорганакалық және физколлойдт ық
химияның т әжірибелік зерт ханалық
сабақт арына қолданба» Шымкент 2004ж.
• Ферменттердің әсер ет у механизмдері.






















 chemistry
chemistry








